Калориметр - Calorimeter
эта статья нужны дополнительные цитаты для проверка. (Ноябрь 2017 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
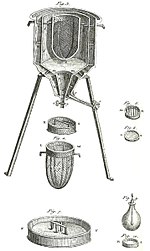
А калориметр это объект, используемый для калориметрия, или процесс измерения тепла химические реакции или физические изменения а также теплоемкость. Дифференциальные сканирующие калориметры, изотермические микрокалориметры, титрование калориметры и калориметры с ускоренной скоростью являются одними из наиболее распространенных типов. Простой калориметр состоит из термометра, прикрепленного к металлическому контейнеру с водой, подвешенному над камерой сгорания. Это один из измерительных приборов, используемых при изучении термодинамики, химии и биохимии.
Чтобы найти энтальпия изменение за моль вещества A в реакции между двумя веществами A и B, вещества отдельно добавляются в калориметр, а начальный и конечный температуры (до начала реакции и после ее завершения). Умножая изменение температуры на массу и удельная теплоемкость веществ дает значение для энергия выделяется или поглощается во время реакции. Разделение изменения энергии на количество присутствующих молей A дает изменение энтальпии реакции.
куда q количество тепла в соответствии с изменением температуры, измеренное в джоулях, и Cv - теплоемкость калориметра, представляющая собой значение, связанное с каждым отдельным устройством, в единицах энергии на температуру (Джоуль / Кельвин).
История
В 1761 году Джозеф Блэк представил идею скрытого тепла, что привело к созданию первых ледяных калориметров.[1] В 1780 году Антуан Лавуазье использовал тепло от дыхания морской свинки, чтобы растопить снег, окружающий его аппарат, показывая, что дыхательный газообмен - это горение, подобное горению свечи.[2] Лавуазье назвал этот прибор калориметром, основываясь на греческих и латинских корнях. Один из первых ледяных калориметров был использован зимой 1782 года Лавуазье и Пьером-Симоном Лапласом, который полагался на тепло, необходимое для плавления льда в воду, для измерения тепла, выделяемого в результате химических реакций.[3]
Адиабатические калориметры

An адиабатический калориметр - это калориметр, используемый для исследования реакции неуправляемого типа. Поскольку калориметр работает в адиабатической среде, любое тепло, выделяемое исследуемым образцом материала, вызывает повышение температуры образца, тем самым подпитывая реакцию.
Ни один адиабатический калориметр не является полностью адиабатическим - некоторое количество тепла будет передаваться образцом держателю образца. Математический поправочный коэффициент, известный как phi-фактор, может использоваться для корректировки калориметрического результата с учетом этих тепловых потерь. Фи-фактор - это соотношение термическая масса образца и держателя образца только к тепловой массе образца.
Калориметры реакции
Реакционный калориметр - это калориметр, в котором химическая реакция инициируется в закрытом изолированном контейнере. Теплота реакции измеряется, и общая теплота получается путем интегрирования теплового потока в зависимости от времени. Это стандарт, используемый в промышленности для измерения тепла, поскольку промышленные процессы спроектированы для работы при постоянной температуре.[нужна цитата ] Калориметрия реакций также может использоваться для определения максимальной скорости тепловыделения для химической технологии процессов и для отслеживания общей кинетики реакций. Существует четыре основных метода измерения тепла в реакционном калориметре:
Калориметр теплового потока
Рубашка охлаждения / нагрева контролирует либо температуру процесса, либо температуру рубашки. Тепло измеряется путем отслеживания разницы температур между теплоносителем и технологической жидкостью. Кроме того, для получения правильного значения необходимо определить объемы заполнения (т.е. смачиваемую площадь), удельную теплоемкость и коэффициент теплопередачи. Этот тип калориметра позволяет проводить реакции при кипячении с обратным холодильником, хотя он очень менее точен.
Калориметр теплового баланса
Рубашка охлаждения / нагрева контролирует температуру процесса. Тепло измеряется путем отслеживания тепла, полученного или потерянного теплоносителем.
Компенсация мощности
Компенсация мощности использует нагреватель, расположенный внутри емкости для поддержания постоянной температуры. Энергия, подводимая к этому нагревателю, может изменяться по мере необходимости, и калориметрический сигнал выводится исключительно из этой электроэнергии.
Постоянный поток
Калориметрия постоянного потока (или COFLUX, как ее часто называют) выводится из калориметрии теплового баланса и использует специальные механизмы управления для поддержания постоянного теплового потока (или потока) через стенку сосуда.
Калориметры бомбы


Бомбовый калориметр - это тип калориметра постоянного объема, который используется для измерения теплоты сгорания конкретной реакции. Калориметры бомбы должны выдерживать большое давление внутри калориметра во время измерения реакции. Электрическая энергия используется для зажигания топлива; когда топливо горит, оно нагревает окружающий воздух, который расширяется и выходит через трубку, которая выводит воздух из калориметра. Когда воздух выходит через медную трубку, он также нагревает воду за ее пределами. Изменение температуры воды позволяет рассчитать калорийность топлива.
В более поздних конструкциях калориметров вся бомба, находящаяся под давлением избыточного чистого кислорода (обычно при 30 атм) и содержащая взвешенную массу образца (обычно 1–1,5 г) и небольшое фиксированное количество воды (для насыщения внутренней атмосферы, Таким образом гарантируется, что вся произведенная вода является жидкой, и устраняется необходимость включать энтальпию испарения в расчеты), она погружается в известный объем воды (около 2000 мл) до электрического воспламенения заряда. Бомба с известной массой образца и кислорода образует замкнутую систему - во время реакции газы не выходят. Взвешенный реагент, помещенный в стальной контейнер, воспламеняется. При сгорании выделяется энергия, и тепловой поток проходит через стенку из нержавеющей стали, повышая тем самым температуру стальной бомбы, ее содержимого и окружающей водяной рубашки. Затем изменение температуры воды точно измеряется термометром. Это показание, вместе с коэффициентом бомбы (который зависит от теплоемкости металлических частей бомбы), используется для расчета энергии, выделяемой при горении образца. Небольшая поправка сделана для учета подводимой электроэнергии, горящего предохранителя и образования кислоты (титрованием остаточной жидкости). После измерения повышения температуры в бомбе сбрасывается избыточное давление.
По сути, бомбовый калориметр состоит из небольшой чашки, в которой находится образец, кислорода, бомбы из нержавеющей стали, воды, мешалки, термометра, емкости Дьюара или изоляционного контейнера (для предотвращения теплового потока от калориметра в окружающую среду) и цепи зажигания. подключен к бомбе. При использовании в бомбе нержавеющей стали реакция будет происходить без изменения объема.
Поскольку теплообмен между калориметром и окружающей средой отсутствует (Q = 0) (адиабатический), работа не выполняется (W = 0).
Таким образом, полное изменение внутренней энергии
Кроме того, общее изменение внутренней энергии
- (постоянный объем )
где теплоемкость бомбы
Прежде чем бомбу можно будет использовать для определения теплоты сгорания какого-либо соединения, ее необходимо откалибровать. можно оценить по
- и можно измерить;
В лаборатории определяется путем использования смеси с известной теплотой сгорания:
Общие соединения бензойная кислота () или п-метилбензойной кислоты ().
Температура (Т) записывается каждую минуту и
Небольшой фактор, способствующий корректировке общей теплоты сгорания, - это плавкая проволока. Никелевая плавкая проволока часто используется и имеет теплоту сгорания = 981,2 кал / г.
Для калибровки бомбы взвешивается небольшое количество (~ 1 г) бензойной кислоты или п-метилбензойной кислоты. Длина никелевой плавкой проволоки (~ 10 см) взвешивается как до, так и после процесса горения. Масса сгоревшего провода предохранителя
Сжигание образца (бензойной кислоты) внутри бомбы
однажды стоимость бомбы определена, бомба готова к использованию для расчета теплоты сгорания любых соединений по
Сжигание негорючих веществ
Более высокое давление и концентрация O2 в системе бомбы может сделать горючие некоторые соединения, которые обычно не воспламеняются. Некоторые вещества не сгорают полностью, что затрудняет расчеты, поскольку необходимо учитывать оставшуюся массу, что значительно увеличивает возможную ошибку и ставит под угрозу данные.
При работе с негорючими компаундами (которые могут не сгорать полностью) одним из решений может быть смешивание компаунда с некоторыми легковоспламеняющимися составами с известной теплотой сгорания и изготовление поддона из смеси. Однажды бомбы известна теплота сгорания горючего соединения (CFC), проволоки (CW) и массы (мFC и мW), а изменение температуры (ΔТ) теплота сгорания менее горючего соединения (CLFC) можно рассчитать с помощью:
- CLFC = Cv · ΔТ − CFC·мFC − CW·мW[6][неудачная проверка ]
Калориметры типа Кальве
Обнаружение основано на трехмерном датчике флюксметра. Элемент флюксметра состоит из кольца, состоящего из нескольких последовательно соединенных термопар. Соответствующая термобатарея с высокой теплопроводностью окружает экспериментальное пространство внутри калориметрического блока. Радиальное расположение термобатареи гарантирует почти полную интеграцию тепла. Это подтверждается расчетом коэффициента эффективности, который показывает, что среднее значение 94% +/- 1% тепла передается через датчик во всем диапазоне температур калориметра типа Кальве. В этой установке чувствительность калориметра не зависит от тигля, типа продувочного газа или скорости потока. Основным преимуществом установки является увеличение размера экспериментального сосуда и, следовательно, размера образца, не влияя на точность калориметрических измерений.
Калибровка калориметрических детекторов является ключевым параметром и требует очень тщательного выполнения. Для калориметров типа Кальве требуется специальная калибровка, так называемая Эффект Джоуля или электрическая калибровка, была разработана для решения всех проблем, возникающих при калибровке с использованием стандартных материалов. Основные преимущества этого типа калибровки заключаются в следующем:
- Это абсолютная калибровка.
- Использование стандартных материалов для калибровки не требуется. Калибровку можно проводить при постоянной температуре, в режиме нагрева и в режиме охлаждения.
- Его можно применить к экспериментальному сосуду любого объема.
- Это очень точная калибровка.
Примером калориметра типа Кальве является калориметр C80 (реакционный, изотермический и сканирующий калориметр).[7]
Адиабатические и изопериболические калориметры
Иногда упоминается как калориметры постоянного давления, адиабатические калориметры измеряют изменение энтальпия реакции, происходящей в решение во время которого не допускается теплообмен с окружающей средой (адиабатический ) и атмосферное давление остается постоянным.
Примером может служить калориметр кофейной чашки, который состоит из двух вложенных Пенополистирол чашки, обеспечивающие изоляцию от окружающей среды, и крышка с двумя отверстиями, позволяющая вставить термометр и стержень для перемешивания. Внутренняя чашка содержит известное количество растворителя, обычно воды, которая поглощает тепло от реакции. Когда происходит реакция, внешняя чашка обеспечивает изоляция. потом
где
- = Удельная теплоемкость при постоянном давлении
- = Энтальпия раствора
- = Изменение температуры
- = масса растворителя
- = молекулярная масса растворителя
Измерение тепла с помощью простого калориметра, такого как калориметр для кофейной чашки, является примером калориметрии постоянного давления, поскольку давление (атмосферное давление) остается постоянным во время процесса. Калориметрия постоянного давления используется для определения изменений энтальпии, происходящих в растворе. В этих условиях изменение энтальпии равняется теплоте.
Аналогичным образом работают коммерческие калориметры. Полуадиабатические (изопериболические) калориметры измеряют изменения температуры до 10-6 ° C и учитывают потери тепла через стенки реакционного сосуда в окружающую среду, следовательно, полуадиабатические. Реакционный сосуд представляет собой колбу Дьюара, погруженную в баню с постоянной температурой. Это обеспечивает постоянную скорость утечки тепла, которую можно скорректировать с помощью программного обеспечения. Теплоемкость реагентов (и емкости) измеряется путем введения известного количества тепла с помощью нагревательного элемента (напряжение и ток) и измерения изменения температуры.
Дифференциальный сканирующий калориметр
В дифференциальный сканирующий калориметр (DSC), тепловой поток в образец - обычно содержится в небольшом алюминий капсула или «чаша» - измеряется дифференциально, т. е. путем сравнения ее с потоком в пустую эталонную чашу.
В Тепловой поток DSC, обе сковороды находятся на небольшой пластине материала с известным (откалиброванным) тепловым сопротивлением K. Температура калориметра линейно повышается со временем (сканируется), т. е. скорость нагрева
- dT / dt = β
остается постоянным. На этот раз линейность требует хорошей конструкции и хорошего (компьютеризированного) контроля температуры. Конечно, также возможны контролируемое охлаждение и изотермические эксперименты.
Тепло течет в две кастрюли за счет теплопроводности. Поток тепла в образец больше из-за его теплоемкость Cп. Разница в потоке dq/dt вызывает небольшую разницу температур ΔТ поперек плиты. Эта разница температур измеряется с помощью термопара. По этому сигналу в принципе можно определить теплоемкость:
Обратите внимание, что эта формула (эквивалентная Закон теплового потока Ньютона ) аналогичен и намного старше, Закон Ома электрического потока:
- ΔV = рdQ/dt = RI.
Когда образец внезапно поглощает тепло (например, когда образец плавится), сигнал отреагирует и покажет пик.
От интеграл по этому пику можно определить энтальпию плавления, а по его началу - температуру плавления.
Дифференциальная сканирующая калориметрия - это рабочая лошадка во многих областях, особенно в полимер характеристика.
А дифференциальный сканирующий калориметр с модулированной температурой (MTDSC) - это тип DSC, в котором небольшие колебания накладываются на линейную скорость нагрева.
Это дает ряд преимуществ. Он облегчает прямое измерение теплоемкости за одно измерение даже в (квази) изотермических условиях. Он позволяет одновременно измерять тепловые эффекты, которые реагируют на изменение скорости нагрева (реверсивное) и не реагируют на изменение скорости нагрева (нереверсивное). Это позволяет оптимизировать как чувствительность, так и разрешение в одном тесте, обеспечивая медленную среднюю скорость нагрева (оптимизация разрешения) и быстро меняющуюся скорость нагрева (оптимизация чувствительности).[8]
Проверка безопасности: - DSC также может использоваться в качестве начального инструмента проверки безопасности. В этом режиме образец будет помещен в нереактивный тигель (часто Золото, или позолоченная сталь), и которая сможет выдержать давление (обычно до 100 бар ). Наличие экзотермический событие затем можно использовать для оценки стабильность вещества для нагрева. Однако из-за комбинации относительно низкой чувствительности, более медленных, чем обычно, скоростей сканирования (обычно 2–3 ° / мин - из-за гораздо более тяжелого тигля) и неизвестных энергия активации, необходимо вычесть около 75–100 ° C от начального начала наблюдаемого экзотерма до предложить максимальная температура материала. Гораздо более точный набор данных можно получить с помощью адиабатического калориметра, но такой тест может занять 2–3 дня от окружающий с шагом 3 ° C за полчаса.
Калориметр изотермического титрования
В изотермическом титрование калориметр, теплота реакции используется для отслеживания эксперимента по титрованию. Это позволяет определить среднюю точку (стехиометрия ) (N) реакции, а также ее энтальпия (дельта H), энтропия (дельта S) и первостепенное значение имеет аффинность связывания (Ka)
Этот метод приобретает все большее значение, особенно в области биохимия, поскольку облегчает определение связывания субстрата с ферменты. Этот метод обычно используется в фармацевтической промышленности для характеристики потенциальных лекарств-кандидатов.
Смотрите также
- Энтальпия
- Высокая температура
- Калорийность
- Теплота сгорания
- Постоянная калориметра
- Калориметр реакции
- Калориметр (физика элементарных частиц)
использованная литература
- ^ Чисхолм, Хью, изд. (1911). «Блэк, Джозеф». Encyclopdia Britannica. 4 (11-е изд.). Издательство Кембриджского университета.
- ^ Антуан Лоран Лавуазье, Элементы химии: в новом систематическом порядке; Содержит все современные открытия, 1789 г .: «Я признаю, что название Калориметр, которое я дал ему, как производное частично от греческого, а частично от латинского, в некоторой степени открыто для критики; но в вопросах науки есть небольшое отклонение от строгая этимология ради придания ясности идее простительна, и я не мог получить название полностью из греческого языка, не прибегая слишком близко к названиям известных инструментов, используемых для других целей ».
- ^ Бухгольц, Андреа С; Шоллер, Дейл А. (2004). «Калория - это калория?». Американский журнал клинического питания. 79 (5): 899S – 906S. Дои:10.1093 / ajcn / 79.5.899S. PMID 15113737. Получено 2007-03-12.
- ^ Полик, В. (1997). Калориметрия бомбы. Полученное из http://www.chem.hope.edu/~polik/Chem345-2000/bombcalorimetry.htm В архиве 2015-10-06 на Wayback Machine
- ^ Боццелли, Дж. (2010). Теплота сгорания с помощью калориметрии: подробные процедуры. Chem 339-Лаборатория физической химии для инженеров-химиков - Руководство лаборатории.
- ^ Беч Н., Дженсен П. А. и Дам-Йохансен К. (2009). Определение элементного состава топлива с помощью калориметрии бомбы и обратной корреляции HHV с элементным составом. Биомасса и биоэнергетика, 33 (3), 534-537. 10.1016 / j.biombioe.2008.08.015
- ^ «Калориметр C80 от Setaram Instrumentation». Архивировано из оригинал на 2010-05-31. Получено 2010-07-12.
- ^ «Архивная копия» (PDF). Архивировано из оригинал (PDF) в 2014-07-29. Получено 2014-07-25.CS1 maint: заархивированная копия как заголовок (ссылка на сайт)



























