Перитонеальный диализ - Peritoneal dialysis
| Перитонеальный диализ | |
|---|---|
 Схема перитонеального диализа | |
| Специальность | нефрология |
| МКБ-9-СМ | 54.98 |
| MeSH | D010530 |
Перитонеальный диализ (PD) является разновидностью диализ который использует брюшина в человеке брюшная полость как мембрана, через которую жидкость и растворенные вещества обмениваются с кровь.[1] Применяется для удаления лишней жидкости, коррекции проблемы с электролитом, и удалить токсины у людей с почечная недостаточность.[2] Результаты перитонеального диализа лучше, чем у гемодиализ в течение первых двух лет.[3] Другие преимущества включают большую гибкость и лучшую переносимость у пациентов со значительными сердечное заболевание.[3]
Осложнения могут включать: инфекции в брюшной полости, грыжи, высокое содержание сахара в крови, кровотечение в брюшной полости и закупорка катетера.[2] Использование невозможно в тех случаях, когда абдоминальная хирургия или же воспалительное заболевание кишечника.[2] Чтобы сделать это правильно, требуется определенная степень технических навыков.[3]
При перитонеальном диализе специальный раствор вводится через постоянную трубку в нижней части живота, а затем удаляется.[2] Это может происходить через равные промежутки времени в течение дня, известное как непрерывный амбулаторный диализ (CAPD), или ночью с помощью аппарата, известного как автоматический перитонеальный диализ (APD).[2] Решение обычно состоит из хлорид натрия, гидрокарбонат, и осмотический агент Такие как глюкоза.[2]
Перитонеальный диализ впервые был проведен в 1920-х годах; однако долгосрочное использование не вошло в медицинскую практику до 1960-х годов.[4] Раствор, используемый для перитонеального диализа, находится на Список основных лекарственных средств Всемирной организации здравоохранения, самые безопасные и эффективные лекарства, необходимые в система здоровья.[5] Стоимость диализного лечения зависит от богатства страны.[6] В Соединенных Штатах перитонеальный диализ обходится государству примерно в 53 400 долларов на человека в год.[3] По состоянию на 2009 г. перитонеальный диализ был доступен в 12 из 53 африканских стран.[6]
Влияние на здоровье
ПД менее эффективен при удалении шлаков из организма, чем гемодиализ, и наличие трубки представляет риск перитонит из-за возможности занести бактерии в брюшную полость.[7] Недостаточно доказательств, чтобы однозначно определить наилучшее лечение перитонита, связанного с БП, хотя прямая инфузия антибиотики в брюшину дает небольшое преимущество перед внутривенным путем введения; нет явных преимуществ для других часто используемых методов лечения, таких как рутинный перитонеальный лаваж или использование урокиназа.[8] Использование профилактического назального мупироцин имеет неясное действие в отношении перитонита.[9] Инфекции могут происходить не реже одного раза в 15 месяцев (0,8 эпизода на пациента в год). По сравнению с гемодиализом, ПД обеспечивает большую мобильность пациента, вызывает меньше колебаний в симптомах из-за его непрерывного характера и фосфат соединения лучше удаляются, но большое количество альбумин удаляются, что требует постоянного контроля статуса питания. Стоимость PD обычно ниже, чем стоимость HD в большинстве частей мира, это ценовое преимущество наиболее очевидно в развитых странах.[10] Недостаточно исследований, чтобы адекватно сравнить риски и преимущества между CAPD и APD; а Кокрановский обзор из трех маленьких клинические испытания не обнаружили разницы в клинически значимых исходах (т.е. болезненность или же смертность ) для пациентов с терминальная стадия почечной недостаточности, и не было никакого преимущества в сохранении функциональности почек. Результаты показали, что APD может иметь психосоциальные преимущества для молодых пациентов и тех, кто работает или получает образование.[11]
Другие осложнения включают: гипотония (из-за избыточного обмена жидкости и удаление натрия ), люмбаго и грыжа или утечка жидкости из-за высокого давления в брюшной полости. PD также может использоваться для пациентов с сердечная нестабильность поскольку это не приводит к быстрым и значительным изменениям жидкостей организма, а у пациентов с инсулин -зависимый сахарный диабет из-за невозможности контролировать содержание сахара в крови уровни через катетер. Гипертриглицеридемия и ожирение также вызывают беспокойство из-за большого объема глюкозы в жидкости, который может добавить 500-1200 калории к диете в день.[12] Из трех типов систем соединения и обмена жидкости (стандартный, двойной мешок и Y-образный комплект; последние два включают два мешка и только одно соединение с катетером, Y-комплект использует одно Y-образное соединение между мешками, включая опорожнение, промывание и заполнение брюшины через одно и то же соединение) системы двойного мешка и Y-образной формы превосходят обычные системы в предотвращении перитонита.[13]
Метод
Передовой опыт перитонеального диализа гласит, что перед внедрением перитонеального диализа необходимо оценить понимание человеком процесса и систем поддержки, а также обучить уходу за катетером и устранить любые пробелы в понимании, которые могут существовать. Человек должен находиться под постоянным наблюдением для обеспечения адекватного диализа и регулярно обследоваться на предмет наличия осложнений. Наконец, они должны быть осведомлены о важности инфекционного контроля и установления соответствующего режима лечения при их сотрудничестве.[14]
- Процесс диализа
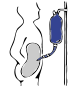
Монтировать
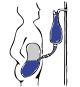
Настой

Распространение (свежий)
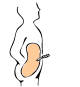
Распространение (отходы)

Дренаж

Живот очищается перед операцией и катетер хирургическим путем вводится одним концом в брюшную полость, а другой выступает из кожи.[15] Перед каждой инфузией катетер необходимо очищать и проверять, как он течет в брюшную полость и выходит из нее. В течение следующих десяти-пятнадцати минут в брюшную полость вводят 2-3 литра диализирующего раствора.[16] Общий объем обозначается как жить[7] в то время как сама жидкость называется диализатом. Выдержка может достигать 3 литров, также можно добавлять лекарства в жидкость непосредственно перед инфузией.[16] Жилище остается в брюшной полости, а продукты жизнедеятельности распространяются через брюшину из нижележащих кровеносных сосудов. Через переменный период времени в зависимости от лечения (обычно 4–6 часов[16] ) жидкость удаляется и заменяется свежей. Это может происходить автоматически, пока пациент спит (автоматический перитонеальный диализ, APD), или в течение дня, если постоянно держать два литра жидкости в брюшной полости, обменивая жидкости четыре-шесть раз в день (непрерывный амбулаторный перитонеальный диализ, CAPD ).[7][17]
Используемая жидкость обычно содержит хлорид натрия, лактат или же бикарбонат и высокий процент глюкоза для обеспечения гиперосмолярность. Количество проводимого диализа зависит от объема тела, регулярности обмена и концентрации жидкости. APD циклически составляет от 3 до 10 жилищ за ночь, в то время как CAPD включает четыре жилища в день по 2–3 литра на каждое проживание, каждое из которых остается в брюшной полости в течение 4–8 часов. Внутренние органы составляют примерно четыре пятых общей площади поверхности мембраны, но париетальная брюшина является наиболее важной из двух частей для БП. Две взаимодополняющие модели объясняют диализ через мембрану - модель трех пор (в которой молекулы обмениваются через мембраны, которые просеивают молекулы, либо белки, электролиты или вода, в зависимости от размера пор) и распределенная модель (которая подчеркивает роль капилляры и способность раствора увеличивать количество активных капилляров, участвующих в БП). Высокая концентрация глюкозы стимулирует фильтрацию жидкости путем осмоса (осмотического УФ) из перитонеальных капилляров в брюшную полость. Глюкоза довольно быстро диффундирует из диализата в кровь (капилляры). После 4-6 часов выдержки осмотический градиент глюкозы обычно становится слишком низким, чтобы обеспечить дальнейшее осмотическое УФ. Следовательно, диализат теперь будет реабсорбироваться из брюшной полости в капилляры за счет осмотического давления коллоидов плазмы, которое превышает осмотическое давление коллоидов в брюшине примерно на 18-20 мм рт.ст. (см. Механизм Старлинга).[18] Лимфатическая абсорбция также будет в некоторой степени способствовать реабсорбции жидкости из брюшной полости в плазму. Пациенты с высокой водопроницаемостью (УФ-коэффициент) перитонеальной мембраны могут иметь повышенную скорость реабсорбции жидкости из брюшины к концу пребывания. Способность обменивать мелкие растворенные вещества и жидкость между брюшиной и плазмой может быть классифицирована как высокая (быстрая), низкая (медленная) или промежуточная. Высокие переносчики имеют тенденцию хорошо рассеивать вещества (легко обмениваются небольшими молекулами между кровью и диализирующей жидкостью, с несколько улучшенными результатами при частых кратковременных пребываниях, таких как APD), в то время как низкие переносчики имеют более высокий UF (из-за более медленной реабсорбции глюкозы из брюшной полости, что приводит к несколько лучшим результатам при длительном пребывании в большом объеме), хотя на практике любой тип транспортера обычно можно контролировать с помощью соответствующего использования APD или CAPD.[19]
Хотя существует несколько различных форм и размеров катетеров, которые можно использовать, разные места введения, количество манжет в катетере и иммобилизация, нет никаких доказательств, демонстрирующих какие-либо преимущества с точки зрения заболеваемости, смертности или количества инфекций, хотя качество информации пока недостаточно, чтобы сделать твердые выводы.[20]
А тест на уравновешивание брюшины может быть сделано для оценки пациента, проходящего перитонеальный диализ, путем определения характеристик массопереноса через перитонеальную мембрану.
Осложнения
Контролируют объем удаленного диализата, а также вес пациента. Если в течение трех последовательных сеансов лечения остается более 500 мл жидкости или теряется литр жидкости, обычно уведомляется врач пациента. Чрезмерная потеря жидкости может привести к гиповолемический шок или же гипотония в то время как чрезмерная задержка жидкости может привести к гипертония и отек. Также контролируется цвет удаляемой жидкости: обычно она имеет розовый оттенок в течение первых четырех циклов и затем становится прозрачным или бледно-желтым. Наличие розовых или кровянистых выделений указывает на кровотечение в брюшной полости, а кал указывает на перфорированный кишечник а мутная жидкость указывает на инфекцию. Пациент также может испытывать боль или дискомфорт, если диализат слишком кислый, слишком холодный или вводится слишком быстро, в то время как диффузная боль с мутными выделениями может указывать на инфекцию. Сильная боль в прямая кишка или же промежность может быть результатом неправильно установленного катетера. Остановка также может увеличить давление на диафрагма вызывая нарушение дыхания, и запор может препятствовать прохождению жидкости через катетер.[16]
Потенциально смертельным осложнением, которое, по оценкам, возникает примерно у 2,5% пациентов, является инкапсуляция перитонеального склероза, при котором кишечник становится непроходимым из-за роста толстого слоя фибрин внутри брюшины.[21]
Жидкость, используемая для диализа, использует глюкоза в качестве основного осмотического агента, но это может привести к перитонит, упадок почка и функция перитонеальных мембран и другие негативные последствия для здоровья. В кислотность, высокая концентрация и присутствие лактат и продукты разложения глюкозы в растворе (особенно последний) могут способствовать этим проблемам со здоровьем. Решения, которые нейтральный, использовать бикарбонат вместо лактата и наличие небольшого количества продуктов разложения глюкозы может принести больше пользы для здоровья, хотя это еще не изучено.[22]
использование
Во всемирном опросе 2004 г. пациентов в терминальная стадия почечной недостаточности, примерно 11% получали PD, по сравнению с гораздо более распространенными гемодиализ. В Гонконге и Мексика, PD встречается чаще, чем в среднем в мире, при этом Мексика проводит большую часть диализа (75%) через PD, в то время как Япония и Германия имеют ставки ниже, чем в среднем в мире.[23]
Импровизированный диализ
Перитонеальный диализ может быть импровизирован в таких условиях, как боевая хирургия или помощь при стихийных бедствиях с использованием хирургических катетеров и диализата, приготовленного из обычных медицинских растворов, для обеспечения временной замены почек людям, у которых нет других вариантов.[24]
Смотрите также
Рекомендации
- ^ Биллингс, Дайан М. (1 ноября 2008 г.). Обзор содержания Липпинкотта для NCLEX-RN. Липпинкотт Уильямс и Уилкинс. п. 575. ISBN 9781582555157. В архиве из оригинала от 13.01.2017.
- ^ а б c d е ж Всемирная организация здоровья (2009). Стюарт М.С., Куимци М., Хилл С.Р. (ред.). Типовой формуляр ВОЗ 2008 г.. Всемирная организация здоровья. п. 453. HDL:10665/44053. ISBN 9789241547659.
- ^ а б c d Баркуда, Эбрахим (2016). «Начало диализа во время пребывания в больнице». Том 5, Выпуск 4, Выпуск клиник госпитальной медицины. Elsevier Health Sciences. ISBN 9780323463164. В архиве из оригинала от 08.04.2017.
- ^ Нольф, К. Д. (09.03.2013). «История перитонеального диализа». Перитонеальный диализ. Springer Science & Business Media. п. 1.0 и 2.0. ISBN 9789401725606. В архиве из оригинала от 13.01.2017.
- ^ Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ а б Ронко, Клаудио; Крепальди, Карло; Круз, Динна Н. (2009). Перитонеальный диализ: от базовых концепций к клиническому совершенству. Медицинские и научные издательства Karger. п. 244. ISBN 9783805592024. В архиве из оригинала от 13.01.2017.
- ^ а б c Кроули, Л.В. (2009). Введение в болезни человека: взаимосвязь патологии и патофизиологии. Jones & Bartlett Publishers. С. 507–509. ISBN 978-0-7637-6591-0. В архиве из оригинала 18.06.2013.
- ^ Баллинджер, AE; Палмер, Южная Каролина; Виггинс, К.Дж.; Крейг, JC; Джонсон, DW; Крест, NB; Стрипполи, Г. Ф. (26 апреля 2014 г.). «Лечение перитонита, связанного с перитонеальным диализом» (PDF). Кокрановская база данных систематических обзоров (4): CD005284. Дои:10.1002 / 14651858.CD005284.pub3. PMID 24771351.
- ^ Кэмпбелл, Д.; Mudge, DW; Крейг, JC; Джонсон, DW; Тонг, А; Стрипполи, Г. Ф. (8 апреля 2017 г.). «Противомикробные средства для профилактики перитонита у пациентов на перитонеальном диализе». Кокрановская база данных систематических обзоров. 4: CD004679. Дои:10.1002 / 14651858.CD004679.pub3. ЧВК 6478113. PMID 28390069.
- ^ Karopadi, AN; Mason G; Rettore E; Ронко С (2013). Зоккали, Кармин (ред.). «Стоимость перитонеального диализа и гемодиализа в мире». Пересадка нефрола Dial. 28 (10): 2553–69. Дои:10.1093 / ndt / gft214. PMID 23737482.
- ^ Рабиндранат, Канзас; и другие. (2007). Рабиндранат, Каннайян С (ред.). «Непрерывный амбулаторный перитонеальный диализ по сравнению с автоматическим перитонеальным диализом при терминальной стадии почечной недостаточности». Кокрановская база данных систематических обзоров. 2 (2): CD006515. Дои:10.1002 / 14651858.CD006515. ЧВК 6669246. PMID 17443624. В архиве из оригинала от 08.10.2009.
- ^ Эрман, JK; Гордон П. Visich PS; Кетейян SJ (2008). Клиническая физиология упражнений. Кинетика человека. С. 268–269. ISBN 978-0-7360-6565-8. В архиве из оригинала 18.06.2013.
- ^ Дэли, Конал; Коди, июнь Д.; Хан, Ижар; Rabindranath, Kannaiyan S .; Вейл, Люк; Уоллес, Шейла А. (13 августа 2014 г.). «Двойной мешок или Y-образная система по сравнению со стандартными системами переноса для непрерывного амбулаторного перитонеального диализа при терминальной стадии болезни почек». Кокрановская база данных систематических обзоров (8): CD003078. Дои:10.1002 / 14651858.CD003078.pub2. ISSN 1469-493X. ЧВК 6457793. PMID 25117423.
- ^ Дерево, М; и другие. (2008-08-01). «Стандарты и практические рекомендации нефрологической медсестры» (PDF). Канадская ассоциация медсестер и технологов нефрологии. Архивировано из оригинал (PDF) 31 марта 2010 г.. Получено 2010-09-08.
- ^ Harissis HV, Katsios CS, Koliousi EL, Ikonomou MG, Siamopoulos KC, Fatouros M, Kappas AM (июль 2006 г.). «Новая упрощенная однопортовая лапароскопическая техника установки катетера перитонеального диализа с интраабдоминальной фиксацией». Являюсь. J. Surg. 192 (1): 125–9. Дои:10.1016 / j.amjsurg.2006.01.033. PMID 16769289.
- ^ а б c d Уилкинс, Липпинкотт Уильямс (2007). Лучшие практики: процедуры сестринского ухода, основанные на доказательствах. ISBN 978-1-58255-532-4.
- ^ Макфи, SJ; Тирни Л.М.; Пападакис М.А. (2007). Текущий медицинский диагноз и лечение. Макгроу-Хилл. С. 934–935. ISBN 978-0-07-147247-0.
- ^ Риппе Б., Вентуроли Д., Симонсен О, де Артеага Дж. (2004). «Транспорт жидкости и электролитов через перитонеальную мембрану во время CAPD в соответствии с трехпоровой моделью». Perit Dial Int. 24 (1): 10–27. Дои:10.1177/089686080402400102. PMID 15104333. S2CID 25034246.
- ^ Даугирдас, JT; Блейк П.Г.; Ing TS (2006). «Физиология перитонеального диализа». Справочник по диализу. Липпинкотт Уильямс и Уилкинс. п. 323. ISBN 9780781752534. В архиве из оригинала 18.06.2013.
- ^ Хтай, Хтай; Джонсон, Дэвид В .; Крейг, Джонатан С .; Шена, Франческо Паоло; Стрипполи, Джованни FM; Тонг, Эллисон; Чо, Ёнджи (31 мая 2019 г.). «Тип катетера, методы размещения и введения для предотвращения инфекций, связанных с катетером, у пациентов с хроническим перитонеальным диализом». Кокрановская база данных систематических обзоров. 5: CD004680. Дои:10.1002 / 14651858.CD004680.pub3. ISSN 1469-493X. ЧВК 6543877. PMID 31149735.
- ^ Kawanishi, H .; Морииши, М. (2007). «Инкапсулирующий склероз брюшины: профилактика и лечение». Международный перитонеальный диализ: журнал Международного общества перитонеального диализа. 27 Приложение 2: S289 – S292. PMID 17556321.
- ^ Perl, J .; Nessim, S.J .; Баргман, Дж. М. (2011). «Биосовместимость растворов для перитонеального диализа с нейтральным pH и низким ВВП: польза в лабораторных условиях, у постели больного или в обоих случаях?». Kidney International. 79 (8): 814–824. Дои:10.1038 / ки.2010.515. PMID 21248712.
- ^ Грассманн, А; Gioberge S; Moeller S; Браун G (2005). «Пациенты с ХПН в 2004 году: глобальный обзор количества пациентов, методов лечения и связанных тенденций». Нефрологическая диализная трансплантация. 20 (12): 2587–2593. Дои:10.1093 / ndt / gfi159. PMID 16204281.
- ^ Pina, J. S .; Moghadam, S .; Cushner, H.M .; Бейлман, Г. Дж .; Макалистер, В. К. (2010). «Перитонеальный диализ в театре при почечной недостаточности, связанной с боевыми действиями». Журнал травм: травмы, инфекции и неотложная помощь. 68 (5): 1253–1256. Дои:10.1097 / TA.0b013e3181d99089. PMID 20453775. S2CID 24251777.





