Ununennium - Ununennium
| Ununennium | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Произношение | /ˌuп.uпˈɛпяəм/ ( | ||||||||||||||||||||
| Альтернативные названия | элемент 119, эка-франций | ||||||||||||||||||||
| Массовое число | [315] (предсказано) | ||||||||||||||||||||
| Унунениум в периодическая таблица | |||||||||||||||||||||
| |||||||||||||||||||||
| Атомный номер (Z) | 119 | ||||||||||||||||||||
| Группа | группа 1: H и щелочные металлы | ||||||||||||||||||||
| Период | период 8 | ||||||||||||||||||||
| Блокировать | s-блок | ||||||||||||||||||||
| Категория элемента | Неизвестные химические свойства, но предположительно щелочной металл | ||||||||||||||||||||
| Электронная конфигурация | [Og ] 8s1 (предсказано)[1] | ||||||||||||||||||||
| Электронов на оболочку | 2, 8, 18, 32, 32, 18, 8, 1 (предсказано) | ||||||||||||||||||||
| Физические свойства | |||||||||||||||||||||
| Фаза вSTP | неизвестно (может быть твердым или жидким)[1] | ||||||||||||||||||||
| Температура плавления | 273–303 K (0–30 ° C, 32–86 ° F) (предсказано)[1] | ||||||||||||||||||||
| Точка кипения | 903 К (630 ° С, 1166 ° F) (предсказано)[2] | ||||||||||||||||||||
| Плотность (околоr.t.) | 3 г / см3 (предсказано)[1] | ||||||||||||||||||||
| Теплота плавления | 2.01–2.05 кДж / моль (экстраполировано)[3] | ||||||||||||||||||||
| Атомные свойства | |||||||||||||||||||||
| Состояния окисления | (+1), (+3) (предсказано)[1] | ||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 0,86 (предсказано)[4] | ||||||||||||||||||||
| Энергии ионизации |
| ||||||||||||||||||||
| Радиус атома | эмпирические: 240вечера (предсказано)[1] | ||||||||||||||||||||
| Ковалентный радиус | 263–281 ч. (экстраполировано)[3] | ||||||||||||||||||||
| Другие свойства | |||||||||||||||||||||
| Кристальная структура | объемно-центрированный кубический (скрытая копия) (экстраполировано)[6] | ||||||||||||||||||||
| Количество CAS | 54846-86-5 | ||||||||||||||||||||
| История | |||||||||||||||||||||
| Именование | ИЮПАК систематическое имя элемента | ||||||||||||||||||||
| Основные изотопы унунения | |||||||||||||||||||||
| |||||||||||||||||||||
Ununennium, также известен как эка-франций или элемент 119, является гипотетическим химический элемент с символом Uue и атомный номер 119. Ununennium и Uue временные систематическое название и символ ИЮПАК соответственно, которые используются до тех пор, пока элемент не будет обнаружен, подтвержден и не будет принято решение о постоянном названии. в периодическая таблица элементов, ожидается, что это будет s-блок элемент, щелочной металл, а первый элемент в восьмом период. Это самый легкий элемент, который еще не синтезирован.
Эксперименты по синтезу унунниума начались в июне 2018 г. RIKEN в Японии; очередная попытка команды на Объединенный институт ядерных исследований в Дубна, Россия планируется начать в конце 2020 года. До этого были предприняты две безуспешные попытки синтезировать унунениум: одна американская команда, а другая немецкая. Теоретические и экспериментальные данные показали, что синтез унунениума, вероятно, будет намного сложнее, чем синтез предыдущих элементов, и что это может быть даже предпоследний элемент, который можно синтезировать с помощью современных технологий.
Положение унунениума как седьмого щелочного металла предполагает, что он будет иметь свойства, аналогичные его более легким сородичи: литий, натрий, калий, рубидий, цезий, и франций. Однако, релятивистские эффекты может привести к тому, что некоторые из его свойств будут отличаться от ожидаемых от прямого применения периодические тенденции. Например, ожидается, что унунений будет менее реактивным, чем цезий и франций, и по поведению будет ближе к калию или рубидию, и хотя он должен иметь характеристику +1 степень окисления Для щелочных металлов прогнозируется также степень окисления +3, которая неизвестна ни в одном другом щелочном металле.
История
Сверхтяжелые элементы производятся термоядерная реакция. Эти реакции синтеза можно разделить на «горячий» и «холодный» синтез.[а] в зависимости от энергии возбуждения образовавшегося составного ядра. В реакциях горячего синтеза очень легкие высокоэнергетические снаряды разгоняются по очень тяжелым целям (актиниды ), с образованием составных ядер при высоких энергиях возбуждения (~ 40–50МэВ ), которые могут делиться или испарять несколько (от 3 до 5) нейтронов.[9] В реакциях холодного синтеза (при которых используются более тяжелые снаряды, обычно Четвертый период, и более легкие цели, обычно вести и висмут ) образовавшиеся конденсированные ядра имеют относительно низкую энергию возбуждения (~ 10–20 МэВ), что снижает вероятность того, что эти продукты будут подвергаться реакциям деления. Когда слитые ядра охлаждаются до основное состояние, они требуют испускания всего одного или двух нейтронов. Однако в реакциях горячего синтеза обычно образуются продукты, богатые нейтронами, потому что актиниды имеют самое высокое отношение нейтронов к протонам среди любых элементов, которые в настоящее время могут быть получены в макроскопических количествах.[10]
Ununennium и unbinilium (элементы 119 и 120) - это элементы с наименьшими атомными номерами, которые еще не были синтезированы. Попытки их синтезировать раздвинули бы пределы нынешней технологии из-за уменьшения поперечные сечения производственных реакций и их, вероятно, коротких период полураспада,[11] Ожидается, что это будет порядка микросекунд.[1][7] Элементы за пределами unbiunium (элемент 121), вероятно, будет слишком недолговечным, чтобы его можно было обнаружить с помощью современных технологий: они будут распадаться за микросекунду, прежде чем достигнут детекторов. Возможность обнаружения элементов 121 через 124 сильно зависит от используемой теоретической модели, так как их период полураспада, по прогнозам, очень близок к границе в одну микросекунду.[11] Раньше важную помощь (характеризуемую как «серебряные пули») в синтезе сверхтяжелых элементов оказывали деформированные ядерные снаряды около хасиум -270, что повысило стабильность окружающих ядер и существование квазистабильного нейтронно-богатого изотопа кальций-48 который можно было бы использовать в качестве снаряда для производства большего количества нейтронно-богатых изотопов сверхтяжелых элементов.[12] Чем больше нейтронов, тем тяжелее нуклид есть, тем ближе он будет к востребованному остров стабильности.[b] Даже в этом случае синтезированные изотопы по-прежнему имеют меньше нейтронов, чем ожидается на острове стабильности.[15] Кроме того, использование кальция-48 для синтеза унунения потребует целевого эйнштейний -253 или -254, которые очень трудно производить в достаточно больших количествах (в настоящее время доступны только микрограммы; для сравнения доступны миллиграммы берклия и калифорния). Более практичное производство дополнительных сверхтяжелых элементов потребует снарядов тяжелее 48Ca.[12]
Попытки синтеза
прошлое
Впервые попытка синтеза унунения была предпринята в 1985 году путем бомбардировки мишени эйнштейния-254 с помощью кальций-48 ионы на ускорителе superHILAC в Беркли, Калифорния:
- 254
99Es
+ 48
20Ca
→ 302
119Uue
* → без атомов
Атомы не были идентифицированы, что привело к ограничению поперечное сечение из 300 nb.[16] Более поздние расчеты показывают, что сечение 3n-реакции (которая приведет к 299Uue и три нейтрона в качестве продуктов) фактически будет в шестьсот тысяч раз ниже этого верхнего предела, равного 0,5 pb.[17]
Поскольку унунний является самым легким неоткрытым элементом, в последние годы он был целью экспериментов по синтезу, проводимых группами из Германии, России и Японии. Сборная России на Объединенный институт ядерных исследований в Дубне, Россия, планировала провести эксперимент до 2012 года, но никаких результатов не было, что явно означало, что либо эксперимент не проводился, либо не были идентифицированы атомы унунения.[нужна цитата ] С апреля по сентябрь 2012 г. предпринята попытка синтеза изотопов. 295Ууэ и 296Ууэ было сделано путем бомбардировки цели берклий -249 с титан -50 на GSI Центр исследования тяжелых ионов имени Гельмгольца в Дармштадт, Германия.[18][19] На основании теоретически предсказанного сечения ожидалось, что атом унунения будет синтезирован в течение пяти месяцев после начала эксперимента.[11]
- 249
97Bk
+ 50
22Ti
→ 299
119Uue
* → 296
119Uue
+ 3 1
0
п - 249
97Bk
+ 50
22Ti
→ 299
119Uue
* → 295
119Uue
+ 4 1
0
п
Изначально планировалось продолжить эксперимент до ноября 2012 г.[20] но был остановлен раньше, чтобы воспользоваться 249Мишень Bk для подтверждения синтеза Tennessine (таким образом меняя снаряды на 48Са).[21] Эта реакция между 249Bk и 50Было предсказано, что Ti будет наиболее благоприятной практической реакцией для образования унунения,[19] так как он довольно асимметричный,[11] хотя тоже несколько холодно.[21] (Реакция между 254Es и 48Са будет лучше, но приготовление миллиграммов 254Ес для мишени сложно.)[11] Тем не менее, необходимое изменение от «серебряной пули» 48Ca к 50Ti делит ожидаемый выход унунения примерно на двадцать, так как выход сильно зависит от асимметрии реакции слияния.[11]
Из-за прогнозируемых коротких периодов полураспада команда GSI использовала новую «быструю» электронику, способную регистрировать события распада за микросекунды.[19] Атомы унунния не идентифицированы, что предполагает предельное сечение 70 фбн.[21] Прогнозируемое фактическое поперечное сечение составляет около 40 фб, что находится в пределах существующих технологий.[11] (Рекордно низкое сечение экспериментально успешной реакции составляет 30 фб для реакции между 209Би и 70Zn производство нихоний.)[11]
настоящее время
Команда на RIKEN в Вако, Япония начала бомбардировки кюрий -248 мишеней с ванадий -51 балка в июне 2018 г.[22] для поиска элемента 119. В качестве цели был выбран кюрий, а не более тяжелый берклий или калифорний, так как эти более тяжелые мишени сложно подготовить.[23] В 248Мишени см предоставлены Национальная лаборатория Окриджа, который предоставил необходимые 249Bk мишень от синтеза Tennessine (элемент 117) в Дубне. Эксперимент RIKEN начался с того, что он проводился на циклотроне во время модернизации его линейных ускорителей, которые возобновят работу в 2020 году. Бомбардировка может продолжаться с обеих машин до тех пор, пока не будет обнаружено первое событие; В настоящее время эксперимент проводится с перерывами не менее 100 дней в году.[23][24] Hideto En'yo, директор центра RIKEN Nishina, предсказал, что элементы 119 и 120, вероятно, будут обнаружены к 2022 году.[25] Усилия команды RIKEN финансируются Императором Японии.[26]
- 248
96См
+ 51
23V
→ 299
119Uue
* → 296
119Uue
+ 3 1
0
п - 248
96См
+ 51
23V
→ 299
119Uue
* → 295
119Uue
+ 4 1
0
п
Предполагается, что произведенные изотопы унунения претерпят два альфа-распада до известных изотопов москва (288Мак и 287Mc соответственно), что позволило бы привязать их к известной последовательности из пяти дальнейших альфа-распадов и подтвердить их образование. Прогнозируемое сечение этих реакций составляет около 10 фб.[23]
Планируется
После заявленного синтеза 293Ог в 1999 г. Национальная лаборатория Лоуренса Беркли от 208Pb и 86Kr, аналогичные реакции 209Би + 86Kr и 208Pb + 87Rb были предложены для синтеза элемента 119 и его неизвестного тогда альфа-распада. дочери, элементы 117, 115, и 113.[27] Отзыв этих результатов в 2001 г.[28] и более поздние расчеты сечений реакций «холодного» синтеза ставят под сомнение эту возможность; например, максимальная доходность 2 fb прогнозируется производство 294Uue в бывшей реакции.[29] Пучки радиоактивных ионов могут предоставить альтернативный метод с использованием вести или висмут мишенью, и может позволить производить больше нейтронно-богатых изотопов, если они станут доступны при требуемой интенсивности.[29]
Команда на Объединенный институт ядерных исследований в Дубна Россия планировала начать новые эксперименты по синтезу унунения с использованием 249Bk + 50Реакция Ti в 2019 году с использованием нового экспериментального комплекса.[30][31][32][33][34][35] По состоянию на ноябрь 2019 года планировалось, что эксперимент начнется в конце 2020 года и продлится примерно 150 дней, а результаты будут получены не раньше середины 2021 года.[36]
Лаборатории RIKEN в Японии и ОИЯИ в России лучше всего подходят для этих экспериментов, поскольку они единственные в мире, где для реакций с такими низкими предсказанными сечениями доступны большие времена пучка.[37]
Именование
С помощью Номенклатура Менделеева для безымянных и неоткрытых элементов, ununennium следует называть эка-франций. Используя 1979 ИЮПАК рекомендации, элемент должен быть временно называется унунениум (символ Uue) до тех пор, пока оно не будет обнаружено, открытие будет подтверждено и выбрано постоянное имя.[38] Хотя эти рекомендации широко используются в химическом сообществе на всех уровнях, от кабинетов химии до сложных учебников, они по большей части игнорируются учеными, которые работают теоретически или экспериментально над сверхтяжелыми элементами, которые называют его «элементом 119» с обозначением E119, (119) или 119.[1]
Прогнозируемые свойства
Ядерная стабильность и изотопы


Стабильность ядер сильно падает с увеличением атомного номера после кюрий, элемент 96, период полураспада которого на четыре порядка больше, чем у любого известного в настоящее время элемента с более высоким номером. Все изотопы с атомным номером выше 101 пройти радиоактивный распад с периодом полураспада менее 30 часов. Нет элементов с атомными номерами выше 82 (после вести ) имеют стабильные изотопы.[40] Тем не менее, по причинам, еще не совсем понятным, наблюдается небольшое повышение ядерной стабильности вокруг атомных номеров. 110 –114, что приводит к появлению того, что в ядерной физике называется "остров стабильности ". Эта концепция, предложенная Калифорнийский университет профессор Гленн Сиборг, объясняет, почему сверхтяжелые элементы служат дольше, чем предполагалось.[41]
Период полураспада альфа-распада, предсказанный для 291–307Uue порядка микросекунд. Максимальный предсказанный период полураспада альфа-распада составляет ~ 485 микросекунд для изотопа. 294Uue.[42][43][44] Если учесть все режимы распада, прогнозируемые периоды полураспада уменьшаются до десятков микросекунд.[1][7] Некоторые более тяжелые изотопы могут быть более стабильными; Фрике и Вабер предсказали 315Uue был самым стабильным изотопом унунения в 1971 году.[2] Это имеет последствия для синтеза унунения, так как изотопы с периодом полураспада менее одной микросекунды будут распадаться до того, как достигнут детектора, а более тяжелые изотопы не могут быть синтезированы при столкновении каких-либо известных пригодных для использования ядер мишени и снаряда.[1][7] Тем не менее, новые теоретические модели показывают, что ожидаемый разрыв в энергии между протонные орбитали 2f7/2 (заполнено в элементе 114) и 2f5/2 (заполненный на элементе 120) меньше, чем ожидалось, так что элемент 114 больше не выглядит стабильной сферической замкнутой ядерной оболочкой, и этот энергетический зазор может повысить стабильность элементов 119 и 120. Следующий вдвойне магия теперь ожидается, что ядро будет около сферической 306Ubb (элемент 122 ), но ожидаемый низкий период полураспада и низкое производство поперечное сечение этого нуклида затрудняет его синтез.[39]
Атомный и физический
Быть первым период 8 элемент, унунений, по прогнозам, является щелочным металлом, занимающим свое место в периодической таблице ниже. литий, натрий, калий, рубидий, цезий, и франций. Каждый из этих элементов имеет один валентный электрон на самой внешней s-орбитали (валентная электронная конфигурация пs1), который легко теряется в химических реакциях с образованием +1 степень окисления: таким образом, щелочные металлы очень реактивный элементы. Прогнозируется, что унунениум продолжит тенденцию и будет иметь конфигурацию валентных электронов 8s1. Поэтому ожидается, что он будет вести себя так же, как и его зажигалка. сородичи; однако предполагается, что он будет отличаться от более легких щелочных металлов по некоторым свойствам.[1]
Основная причина предсказанных различий между унунением и другими щелочными металлами - это спин-орбитальное (СО) взаимодействие - взаимное взаимодействие движения электронов и вращение. Взаимодействие SO особенно сильно для сверхтяжелых элементов, потому что их электроны движутся быстрее - со скоростями, сравнимыми с скорость света - чем в более легких атомах.[45] В атомах унунения он понижает уровни энергии электронов 7p и 8s, стабилизируя соответствующие электроны, но два из уровней энергии электронов 7p более стабилизированы, чем четыре других.[46] Эффект называется расщеплением подоболочки, поскольку он разбивает подоболочку 7p на более стабилизированные и менее стабилизированные части. Вычислительные химики понимают расщепление как смену второго (азимутальный ) квантовое число л от 1 до 1/2 и 3/2 для более стабилизированной и менее стабилизированной частей подоболочки 7p соответственно.[45][c] Таким образом, внешний 8s-электрон унунения стабилизируется, и его становится труднее удалить, чем ожидалось, в то время как 7p3/2 электроны соответственно дестабилизируются, что, возможно, позволяет им участвовать в химических реакциях.[1] Эта стабилизация внешней s-орбитали (уже значимая для франция) является ключевым фактором, влияющим на химию ununennium, и заставляет все тенденции атомных и молекулярных свойств щелочных металлов менять направление после цезия.[4]
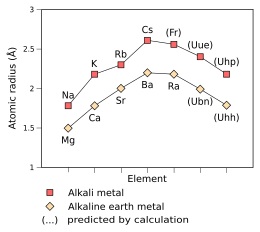 Эмпирический (Na – Cs, Mg – Ra) и прогнозируемые (Fr – Uhp, Ubn – Uhh) атомные радиусы щелочных и щелочноземельных металлов из в третьих к девятый период, измеряется в ангстремы[1][47] |  Эмпирическое (Na – Cs), полуэмпирическое (Fr) и предсказанное (Uue) сродство к электрону щелочных металлов от третьего до восьмой период, измеряется в электрон-вольт.[1][47] Они уменьшаются от Li до Cs, но значение Fr 492±10 мэВ, на 20 мэВ выше, чем у Cs, а у Uue еще выше, и составляет 662 мэВ.[48] |
Из-за стабилизации его внешнего 8s-электрона первый унунениум энергия ионизации - энергия, необходимая для удаления электрона из нейтрального атома, - по прогнозам, составит 4,53 эВ, что выше, чем у известных щелочных металлов, начиная с калия. Этот эффект настолько велик, что, по прогнозам, унбиуний (элемент 121) будет иметь более низкую энергию ионизации 4,45 эВ, так что щелочной металл в периоде 8 не будет иметь самую низкую энергию ионизации в периоде, как это верно для всех предыдущих периодов.[1] Унунениума электронное сродство ожидается, будет намного больше, чем у цезия и франция; действительно, ожидается, что унунений будет иметь сродство к электрону выше, чем у всех щелочных металлов, легче, чем он, примерно на 0,662 эВ, что близко к таковому у кобальт (0,662 эВ) и хром (0,676 эВ).[48] Релятивистские эффекты также вызывают очень большое падение поляризуемость унунениума[1] до 169,7а.е.[49] Действительно, статическая дипольная поляризуемость (αD) унунения, количество, для которого влияние теории относительности пропорционально квадрату атомного номера элемента, было вычислено как небольшое и аналогичное количеству натрия.[50]
Электрон водородоподобный атом унунения - окисленный, поэтому он имеет только один электрон, Uue118+- предсказывается, что он движется так быстро, что его масса в 1,99 раза больше массы неподвижного электрона, что связано с релятивистские эффекты. Для сравнения: водородоподобный франций - 1,29, водородоподобный цезий - 1,091.[45] Согласно простым экстраполяциям законов относительности, это косвенно указывает на сжатие радиус атома[45] примерно до 240вечера,[1] очень близок к рубидию (247 пм); то металлический радиус также соответственно снижается до 260 пм.[1] В ионный радиус Ууэ+ ожидается 180 часов.[1]
Предполагается, что температура плавления унунения составляет от 0 ° C до 30 ° C: таким образом, это может быть жидкость при комнатной температуре.[5] Неизвестно, продолжает ли это тенденция к снижению точек плавления в группе, поскольку точка плавления цезия составляет 28,5 ° C, а температура франция оценивается примерно в 8,0 ° C.[51] Температура кипения унунения ожидается около 630 ° C, что аналогично температуре кипения франция, которая, по оценкам, составляет около 620 ° C; это ниже точки кипения цезия 671 ° C.[2][51] Плотность унунения по разным прогнозам составляет от 3 до 4 г / см3.3, продолжая тенденцию к увеличению плотности по группе: плотность франция оценивается примерно в 2,48 г / см3, а цезия, как известно, составляет 1,93 г / см3.[2][3][51]
Химическая
Длины связей и энергии диссоциации связей димеров щелочных металлов. Данные для Fr2 и Ууэ2 предсказано.[52] Соединение Длина связи (Å) Энергия диссоциации связи (кДж / моль) Ли2 2.673 101.9 Na2 3.079 72.04 K2 3.924 53.25 Руб.2 4.210 47.77 CS2 4.648 43.66 Пт2 ~ 4.61 ~ 42.1 Uue2 ~ 4.27 ~ 53.4
Согласно прогнозам, химический состав унунения аналогичен химическому составу щелочных металлов,[1] но он, вероятно, будет вести себя больше как калий[53] или рубидий[1] чем цезий или франций. Это связано с релятивистскими эффектами, так как при их отсутствии периодические тенденции предсказывает, что унунениум будет даже более реактивным, чем цезий и франций. Это понижено реактивность происходит из-за релятивистской стабилизации валентного электрона унунения, увеличивая первую энергию ионизации унунения и уменьшая металлический и ионные радиусы;[53] этот эффект уже наблюдается для франция.[1]
Химический состав унунения в степени окисления +1 должен быть больше похож на химию рубидия, чем на химию франция. С другой стороны, ионный радиус Uue+ прогнозируется, что он больше, чем у Rb+, потому что 7p-орбитали дестабилизированы и, таким образом, больше, чем p-орбитали нижних оболочек. Ununennium может также показать +3 степень окисления,[1] чего нет ни в одном другом щелочном металле,[54] в дополнение к степени окисления +1, которая характерна для других щелочных металлов, а также является основной степенью окисления всех известных щелочных металлов: это происходит из-за дестабилизации и расширения 7p3/2 спинор, в результате чего его внешние электроны имеют более низкую энергию ионизации, чем можно было бы ожидать.[1][54] Ожидается, что многие соединения унунения будут иметь большую ковалентный характер, в связи с участием 7p3/2 электронов в связи: этот эффект также в меньшей степени проявляется во франции, который показывает около 6p3/2 вклад в облигации во франции супероксид (Пт.2).[45] Таким образом, вместо того, чтобы унунениум был самым электроположительный элемент, как могло бы показаться простой экстраполяцией, цезий вместо этого сохраняет это положение, с унунениумом электроотрицательность скорее всего, быть рядом с натрий (0,93 по шкале Полинга).[4] В стандартный восстановительный потенциал Ууэ+Для пары / Uue прогнозируется значение −2,9 В, такое же, как у пары Fr+/ Fr пара и чуть больше K+/ K пара при −2,931 В.[5]
Длины связей и энергии диссоциации связей MAu (M = щелочной металл). Все данные предсказаны, за исключением энергий диссоциации связей KAu, RbAu и CsAu.[4] Соединение Длина связи (Å) Энергия диссоциации связи (кДж / моль) KAu 2.856 2.75 RbAu 2.967 2.48 CsAu 3.050 2.53 Фрау 3.097 2.75 UueAu 3.074 2.44
В газовой фазе и при очень низких температурах в конденсированной фазе щелочные металлы образуют ковалентно связанные двухатомные молекулы. Металл – металл длина облигаций в этих M2 молекулы увеличиваются вниз по группе от Ли2 в Cs2, но затем уменьшаются после этого до Uue2, из-за вышеупомянутых релятивистских эффектов, которые стабилизируют орбиталь 8s. Противоположная тенденция наблюдается для металла – металла. энергии диссоциации связи. Связь Uue – Uue должна быть немного прочнее, чем связь K – K.[4][52] Из этих M2 энергии диссоциации, энтальпия сублимации (ΔЧАСсуб) унунения прогнозируется на уровне 94 кДж / моль (значение для франция должно быть около 77 кДж / моль).[4]
Ожидается, что молекула UueF будет иметь значительный ковалентный характер из-за высокого сродства к электрону унунения. Связь в UueF преимущественно находится между 7p-орбиталью на унунениуме и 2p-орбиталью на фторе, с меньшим вкладом от 2s-орбитали фтора и 8s, 6d.z2, и две другие 7p-орбитали унунениума. Это сильно отличается от поведения элементов s-блока, а также золото и Меркурий, в котором s-орбитали (иногда смешанные с d-орбиталями) участвуют в связывании. Связь Uue – F релятивистски расширяется за счет расщепления 7p-орбитали на 7p1/2 и 7п3/2 спиноры, вынуждающие связывающие электроны перейти на самую большую орбиталь, измеряемую по радиусу: аналогичное расширение длины связи обнаруживается в гидридах В Х и ЦХ.[55] Связь Uue – Au должна быть самой слабой из всех связей между золотом и щелочным металлом, но при этом должна быть стабильной. Это дает экстраполированные энтальпии адсорбции среднего размера (−ΔЧАСОбъявления) 106 кДж / моль на золото (значение франция должно быть 136 кДж / моль), 76 кДж / моль на платина, и 63 кДж / моль на Серебряный, наименьший из всех щелочных металлов, который демонстрирует возможность изучения хроматографический адсорбция унунениума на поверхности из благородные металлы.[4] В энтальпия из адсорбция унунениума на Тефлон прогнозируется, что поверхность будет составлять 17,6 кДж / моль, что будет самым низким среди щелочных металлов: эта информация будет очень полезна для будущих химических экспериментов с унунением.[49] ΔЧАСсуб и −ΔЧАСОбъявления значения не связаны пропорционально для щелочных металлов, поскольку они меняются в противоположных направлениях с увеличением атомного номера.[4]
Смотрите также
Заметки
- ^ Несмотря на название, «холодный синтез» в контексте синтеза сверхтяжелых элементов представляет собой концепцию, отличную от идеи о том, что ядерный синтез может быть осуществлен в условиях комнатной температуры (см. холодный синтез ).[8]
- ^ Стабильные изотопы самых легких элементов обычно имеют нейтронно-протонное отношение, близкое или равное единице (например, единственный стабильный изотоп алюминий имеет 13 протонов и 14 нейтронов,[13] что делает нейтронно-протонное отношение равным 1,077). Однако изотопы более тяжелых элементов имеют более высокое нейтронно-протонное отношение, увеличивающееся с увеличением числа протонов (йод единственный стабильный изотоп России имеет 53 протона и 74 нейтрона, нейтронно-протонное отношение 1,396; золото единственный стабильный изотоп России имеет 79 протонов и 118 нейтронов, нейтрон-протонное отношение 1,494; плутоний Самый стабильный изотоп России имеет 94 протона и 150 нейтронов, нейтронно-протонное отношение 1,596).[13] Ожидается, что тенденция продолжится к сверхтяжелым элементам,[14] что затрудняет синтез их наиболее стабильных изотопов, поскольку нейтронно-протонные отношения элементов, из которых они синтезируются, ниже, чем ожидаемые отношения наиболее стабильных изотопов сверхтяжелых элементов.
- ^ Квантовое число соответствует букве в названии электронной орбиты: от 0 до s, от 1 до p, 2 до d и т. Д. азимутальное квантовое число за дополнительной информацией.
использованная литература
- ^ а б c d е ж г час я j k л м п о п q р s т ты v ш Икс у z Hoffman, Darleane C .; Ли, Диана М .; Першина, Валерия (2006). «Трансактиниды и элементы будущего». In Morss; Эдельштейн, Норман М .; Фугер, Жан (ред.). Химия актинидных и трансактинидных элементов (3-е изд.). Дордрехт, Нидерланды: Springer Science + Business Media. ISBN 978-1-4020-3555-5.
- ^ а б c d е Fricke, B .; Вабер, Дж. Т. (1971). «Теоретические предсказания химии сверхтяжелых элементов» (PDF). Отзывы об актинидах. 1: 433–485. Получено 7 августа 2013.
- ^ а б c Бончев, Данаил; Каменская, Вергиния (1981). «Прогнозирование свойств 113–120 трансактинидных элементов». Журнал физической химии. Американское химическое общество. 85 (9): 1177–1186. Дои:10.1021 / j150609a021.
- ^ а б c d е ж г час Першина, В .; Борщевский, А .; Антон, Дж. (20 февраля 2012 г.). «Полностью релятивистское исследование интерметаллических димеров элементов группы 1 K через элемент 119 и прогноз их адсорбции на поверхностях благородных металлов». Химическая физика. Эльзевир. 395: 87–94. Bibcode:2012CP .... 395 ... 87P. Дои:10.1016 / j.chemphys.2011.04.017. В этой статье электроотрицательность Малликена равна 2,862, которая была преобразована в шкалу Полинга с помощью χп = 1,35хM1/2 − 1.37.
- ^ а б c Фрике, Буркхард (1975). «Сверхтяжелые элементы: прогноз их химических и физических свойств». Недавнее влияние физики на неорганическую химию. 21: 89–144. Дои:10.1007 / BFb0116498. Получено 4 октября 2013.
- ^ Сиборг, Гленн Т. (1969). «Перспективы дальнейшего значительного расширения таблицы Менделеева» (PDF). Журнал химического образования. 46 (10): 626–634. Bibcode:1969JChEd..46..626S. Дои:10.1021 / ed046p626. Получено 22 февраля 2018.
- ^ а б c d е Хофманн, Сигурд (2013). Обзор и перспективы исследований SHE в GSI SHIP. п. 23–32. Дои:10.1007/978-3-319-00047-3.
- ^ Флейшманн, Мартин; Понс, Стэнли (1989). «Электрохимически индуцированный ядерный синтез дейтерия». Журнал электроаналитической химии и межфазной электрохимии. 261 (2): 301–308. Дои:10.1016/0022-0728(89)80006-3.
- ^ Барбер, Роберт С .; Gäggeler, Heinz W .; Кароль, Пол Дж .; Накахара, Хиромити; Вардачи, Эмануэле; Фогт, Эрих (2009). «Открытие элемента с атомным номером 112 (Технический отчет IUPAC)». Чистая и прикладная химия. 81 (7): 1331. Дои:10.1351 / PAC-REP-08-03-05.
- ^ Армбрустер, Питер и Мюнзенберг, Готфрид (1989). «Создание сверхтяжелых элементов». Scientific American. 34: 36–42.
- ^ а б c d е ж г час я Загребаев Валерий; Карпов, Александр; Грейнер, Уолтер (2013). «Будущее исследований сверхтяжелых элементов: какие ядра могут быть синтезированы в ближайшие несколько лет?» (PDF). Журнал физики. 420 (1): 012001. arXiv:1207.5700. Bibcode:2013JPhCS.420a2001Z. Дои:10.1088/1742-6596/420/1/012001. S2CID 55434734.
- ^ а б Folden III, C.M .; Майоров, Д. А .; Werke, T. A .; Alfonso, M.C .; Bennett, M.E .; ДеВанцо, М. Дж. (2013). «Перспективы открытия следующего нового элемента: Влияние снарядов с Z > 20". Journal of Physics: Серия конференций. 420 (1): 012007. arXiv:1209.0498. Bibcode:2013JPhCS.420a2007F. Дои:10.1088/1742-6596/420/1/012007. S2CID 119275964.
- ^ а б Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; и другие. (2003). «Оценка ядерных и распадных свойств NUBASE» (PDF). Ядерная физика A. 729 (1): 3–128. Bibcode:2003НуФА.729 .... 3А. CiteSeerX 10.1.1.692.8504. Дои:10.1016 / j.nuclphysa.2003.11.001. Архивировано из оригинал (PDF) на 2011-07-20. Получено 2010-07-05.
- ^ Карпов, А. В .; Загребаев, В. И .; Паленсуэла, Ю. Мартинес; Грейнер, Уолтер (2013). «Сверхтяжелые ядра: распад и стабильность». Увлекательная междисциплинарная физика. п. 69. Дои:10.1007/978-3-319-00047-3_6. ISBN 978-3-319-00046-6. S2CID 55180285.
- ^ «Универсальная карта нуклидов». Nucleonica. Институт трансурановых элементов. 2007–2012. Получено 2012-07-03. (требуется регистрация)
- ^ Lougheed, R .; Landrum, J .; Hulet, E .; Wild, J .; Dougan, R .; Дуган, А .; Gäggeler, H .; Schädel, M .; Муди, К. (1985). "Поиск сверхтяжелых элементов с помощью 48Ca + 254Esг реакция ». Физический обзор C. 32 (5): 1760–1763. Bibcode:1985PhRvC..32.1760L. Дои:10.1103 / PhysRevC.32.1760. PMID 9953034.
- ^ Feng, Z; Jin, G .; Li, J .; Шайд, В. (2009). «Производство тяжелых и сверхтяжелых ядер в реакциях массивного синтеза». Ядерная физика A. 816 (1): 33. arXiv:0803.1117. Bibcode:2009НуФА.816 ... 33Ф. Дои:10.1016 / j.nuclphysa.2008.11.003. S2CID 18647291.
- ^ Современная алхимия: сворачивая черту, Экономист, 12 мая 2012 г.
- ^ а б c Кампания по поиску сверхтяжелых элементов на TASCA. Дж. Хуягбаатар
- ^ "Поиск элемента 119: Кристоф Э. Дюльманн для TASCA E119 сотрудничество » (PDF). Архивировано из оригинал (PDF) на 2016-03-04. Получено 2015-09-15.
- ^ а б c Исследование сверхтяжелых элементов в TASCA. Александр Якушев
- ^ Болл, П. (2019). «Экстремальная химия: эксперименты на краю периодической таблицы». Природа. 565 (7741): 552–555. Bibcode:2019Натура.565..552B. Дои:10.1038 / d41586-019-00285-9. ISSN 1476-4687. PMID 30700884.
- ^ а б c Сакаи, Хидеюки (27 февраля 2019 г.). «Поиск нового элемента в центре RIKEN Nishina» (PDF). infn.it. Получено 17 декабря 2019.
- ^ Болл, П. (2019). «Экстремальная химия: эксперименты на краю периодической таблицы» (PDF). Природа. 565 (7741): 552–555. Bibcode:2019Натура.565..552B. Дои:10.1038 / d41586-019-00285-9. PMID 30700884. S2CID 59524524.
- ^ «Охота за набором 119-го элемента начинается». Мир химии. 12 сентября 2017 г.. Получено 9 января 2018.
- ^ Чепмен, Кит; Тернер, Кристи (13 февраля 2018 г.). "Охота началась". Образование в области химии. Королевское химическое общество. Получено 28 июн 2019.
Охота за 113 элементом была почти прекращена из-за нехватки ресурсов, но на этот раз император Японии финансирует усилия Рикена по расширению таблицы Менделеева до восьмой строки.
- ^ Хоффман, округ Колумбия; Ghiorso, A .; Сиборг, Г. (2000). Трансурановые люди: внутренняя история. Imperial College Press. ISBN 978-1-86094-087-3.
- ^ Департамент по связям с общественностью (21 июля 2001 г.). «Результаты эксперимента по элементу 118 отозваны». Лаборатория Беркли. Архивировано из оригинал 29 января 2008 г.. Получено 18 января 2008.
- ^ а б Лавленд, В. (2007). «Синтез ядер трансактинидов с использованием радиоактивных пучков» (PDF). Физический обзор C. 76 (1): 014612. Bibcode:2007PhRvC..76a4612L. Дои:10.1103 / PhysRevC.76.014612.
- ^ «В 2019 году ученые начнут эксперименты по синтезу 119-го элемента». www.jinr.ru. ОИЯИ. 28 сентября 2016 г.. Получено 31 марта 2017.
«Открытие элементов 115, 117 и 118 - свершившийся факт; они были внесены в периодическую таблицу Менделеева, хотя до сих пор не названы и будут подтверждены только в конце года. Периодическая таблица Д. И. Менделеева не бесконечна. В 2019 году ученые приступят к синтезу элементов 119 и 120, которые являются первыми в 8 периоде », - сказал С.Н. Дмитриев.
- ^ Дмитриев, Сергей; Иткис, Михаил; Оганесян, Юрий (2016). Состояние и перспективы Дубненского завода сверхтяжелых элементов (PDF). Нобелевский симпозиум NS160 - Химия и физика тяжелых и сверхтяжелых элементов. Дои:10.1051 / epjconf / 201613108001.
- ^ «Что нужно для создания нового элемента». Мир химии. Получено 2016-12-03.
- ^ Роберто, Дж. Б. (31 марта 2015 г.). «Актинидные мишени для исследования сверхтяжелых элементов» (PDF). cyclotron.tamu.edu. Техасский университет A&M. Получено 28 апреля 2017.
- ^ Морита, Косуке (5 февраля 2016 г.). «Открытие элемента 113». YouTube. Получено 28 апреля 2017.
- ^ Моримото, Кодзи (2016). «Открытие 113-го элемента в RIKEN» (PDF). www.physics.adelaide.edu.au. 26-я Международная конференция по ядерной физике. Получено 14 мая 2017.
- ^ «Ю. Оганесян прокомментировал синтез новых элементов». ОИЯИ. 18 ноября 2019 г.. Получено 16 июн 2020.
Академик отмечает, что задание будет выполнено до конца 2020 года, а еще 150 дней уйдет на эксперименты с заданием по синтезу элемента 119. Таким образом, результатов следует ждать не ранее середины 2021 года.
- ^ Хагино, Коити; Хофманн, Сигурд; Миятаке, Хироари; Накахара, Хиромичи (2012). "平 成 23 年度 研究 業績 レ ビ ュ ー (中間 レ ビ ュ ー) の 実 施 に つ い て" (PDF). www.riken.jp. РИКЕН. Архивировано из оригинал (PDF) 4 ноября 2018 г.. Получено 5 мая 2017.
- ^ Чатт, Дж. (1979). «Рекомендации по присвоению имен элементам с атомными номерами больше 100». Чистая и прикладная химия. 51 (2): 381–384. Дои:10.1351 / pac197951020381.
- ^ а б Кратц, Дж. В. (5 сентября 2011 г.). Влияние сверхтяжелых элементов на химические и физические науки (PDF). 4-я Международная конференция по химии и физике трансактинидных элементов. Получено 27 августа 2013.
- ^ де Марсильяк, Пьер; Корон, Ноэль; Дамбье, Жерар; и другие. (2003). «Экспериментальное обнаружение α-частиц от радиоактивного распада природного висмута». Природа. 422 (6934): 876–878. Bibcode:2003Натура.422..876D. Дои:10.1038 / природа01541. PMID 12712201. S2CID 4415582.
- ^ Considine, Glenn D .; Кулик, Питер Х. (2002). Научная энциклопедия Ван Ностранда (9-е изд.). Wiley-Interscience. ISBN 978-0-471-33230-5. OCLC 223349096.
- ^ Чоудхури, П. Рой; Саманта, К. и Басу, Д. Н. (2007). «Прогнозы периодов полураспада тяжелых и сверхтяжелых элементов при альфа-распаде». Nucl. Phys. А. 789 (1–4): 142–154. arXiv:nucl-th / 0703086. Bibcode:2007НуФА.789..142С. CiteSeerX 10.1.1.264.8177. Дои:10.1016 / j.nuclphysa.2007.04.001. S2CID 7496348.
- ^ Чоудхури, П. Рой; Саманта, К. и Басу, Д. Н. (2008). «Поиски долгоживущих тяжелейших ядер за пределами долины стабильности». Phys. Ред. C. 77 (4): 044603. arXiv:0802.3837. Bibcode:2008PhRvC..77d4603C. Дои:10.1103 / PhysRevC.77.044603. S2CID 119207807.
- ^ Чоудхури, П. Рой; Саманта, К. и Басу, Д. Н. (2008). «Ядерные периоды полураспада для α -радиоактивности элементов с 100 ≤ Z ≤ 130». Атомные данные и таблицы ядерных данных. 94 (6): 781–806. arXiv:0802.4161. Bibcode:2008ADNDT..94..781C. Дои:10.1016 / j.adt.2008.01.003.
- ^ а б c d е Тайер, Джон С. (2010). «Релятивистские эффекты и химия более тяжелых элементов основной группы». В Марии, Барыше; Исикава, Ясуюки (ред.). Релятивистские методы для химиков. Проблемы и достижения вычислительной химии и физики. 10. Springer Нидерланды. С. 63–7, 81, 84. Дои:10.1007/978-1-4020-9975-5_2. ISBN 978-1-4020-9974-8.
- ^ Фэгри младший, Кнут; Сауэ, Тронд (2001). «Двухатомные молекулы между очень тяжелыми элементами группы 13 и группы 17: исследование релятивистских эффектов на связывание». Журнал химической физики. 115 (6): 2456. Bibcode:2001ЖЧФ.115.2456Ф. Дои:10.1063/1.1385366.
- ^ а б c Pyykkö, Пекка (2011). «Предлагаемая таблица Менделеева до Z ≤ 172, основанная на расчетах Дирака – Фока для атомов и ионов». Физическая химия Химическая физика. 13 (1): 161–8. Bibcode:2011PCCP ... 13..161P. Дои:10.1039 / c0cp01575j. PMID 20967377. S2CID 31590563.
- ^ а б Ландау, Арье; Элиав, Ефрем; Исикава, Ясуюки; Кадор, Узи (25 мая 2001 г.). «Контрольные расчеты электронного сродства щелочных атомов натрия к эка-францию (элемент 119)». Журнал химической физики. 115 (6): 2389–92. Bibcode:2001ЖЧФ.115.2389Л. Дои:10.1063/1.1386413. Получено 15 сентября 2015.
- ^ а б Борщевский, А .; Першина, В .; Eliav, E .; Калдор, У. (22 марта 2013 г.). "Ab initio исследования атомных свойств и экспериментального поведения элемента 119 и его более легких гомологов » (PDF). Журнал химической физики. 138 (12): 124302. Bibcode:2013ЖЧФ.138л4302Б. Дои:10.1063/1.4795433. PMID 23556718.
- ^ Лим, Иван С .; Пернпойнтнер, Маркус; Сет, Майкл; Laerdahl, Jon K .; Швердтфегер, Питер; Неограды, Павел; Урбан, Мирослав (1 октября 1999 г.). "Статические дипольные поляризуемости релятивистских связанных кластеров щелочных металлов от Li до элемента 119". Физический обзор A. 60 (4): 2822. Bibcode:1999ПхРвА..60.2822Л. Дои:10.1103 / PhysRevA.60.2822.
- ^ а б c Лаврухина Августа Константиновна; Поздняков, Александр Александрович (1970). Аналитическая химия технеция, прометия, астатина и франция. Перевод Р. Кондора. Издательство Ann Arbor – Humphrey Science Publishers. п. 269. ISBN 978-0-250-39923-9.
- ^ а б Джонс, Кэмерон; Маунтфорд, Филип; Сташ, Андреас; Блейк, Мэтью П. (22 июня 2015 г.). «Металл-металл облигаций s-block». В Liddle, Стивен Т. (ред.). Молекулярные связи металл-металл: соединения, синтез, свойства. Джон Уайли и сыновья. С. 23–24. ISBN 9783527335411.
- ^ а б Сиборг (ок. 2006 г.). «трансурановый элемент (химический элемент)». Британская энциклопедия. Получено 2010-03-16.
- ^ а б Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. п. 28. ISBN 978-0-08-037941-8.
- ^ Miranda, Patrícia S .; Мендес, Анна Паула S .; Gomes, Jose S .; Алвес, Клаудио Н .; de Souza, Aguinaldo R .; Sambrano, Julio R .; Гаргано, Рикардо; де Маседо, Луис Гильерме М. (2012). "Ab Initio коррелированные все электронные расчеты Дирака-Фока для фторида Eka-Francium (E119F)". Журнал Бразильского химического общества. 23 (6): 1104–1113. Дои:10.1590 / S0103-50532012000600015. Получено 14 января 2018.
внешние ссылки
 Словарное определение унунениум в Викисловарь
Словарное определение унунениум в Викисловарь

