Питательные вещества для растений в почве - Plant nutrients in soil - Wikipedia
Семнадцать элементов или питательные вещества необходимы для роста и размножения растений. Они есть углерод (С), водород (ЧАС), кислород (O), азот (N), фосфор (П), калий (К), сера (S), кальций (Ca), магний (Mg), утюг (Fe), бор (B), марганец (Mn), медь (Cu), цинк (Zn), молибден (Пн), никель (Ni) и хлор (Cl).[1][2][3] Учитываются питательные вещества, необходимые растениям для завершения их жизненного цикла. основные питательные вещества. Питательные вещества, которые усиливают рост растений, но не являются необходимыми для завершения жизненного цикла растения, считаются несущественными. За исключением углерода, водорода и кислорода, которые поставляются углекислым газом и водой, и азота, поставляемого через азотфиксация,[3] питательные вещества исходят из минерального компонента почвы. В Закон минимума выражает, что когда доступная форма питательного вещества не находится в достаточной пропорции в почвенном растворе, тогда другие питательные вещества не могут быть поглощены растением с оптимальной скоростью.[4] Таким образом, для оптимизации роста растений обязательно определенное соотношение питательных веществ в почвенном растворе, значение, которое может отличаться от соотношений питательных веществ, рассчитанных на основе состава растений.[5]
Поглощение растениями питательных веществ может происходить только тогда, когда они присутствуют в доступной для растений форме. В большинстве случаев питательные вещества абсорбируются в ионной форме из почвенной воды (или вместе с ней). Хотя минералы являются источником большинства питательных веществ, и большая часть большинства питательных элементов в почве содержится в кристаллической форме в составе первичных и вторичных минералов, они Погода слишком медленно, чтобы поддерживать быстрый рост растений. Например, применение тонкоизмельченных минералов, полевой шпат и апатит, в почву редко поступает необходимое количество калия и фосфора со скоростью, достаточной для хорошего роста растений, поскольку большинство питательных веществ остается связанными в кристаллах этих минералов.[6]
Питательные вещества адсорбируются на поверхности коллоидов глины и органическое вещество почвы обеспечивают более доступный резервуар для многих питательных веществ для растений (например, K, Ca, Mg, P, Zn). По мере того, как растения поглощают питательные вещества из почвенной воды, запас растворимых веществ пополняется из поверхностного бассейна. Разложение органическое вещество почвы с помощью микроорганизмов - это еще один механизм, посредством которого пополняется пул растворимых питательных веществ - это важно для поступления доступных для растений азота, серы, фосфора и витамина B из почвы.[7]
Грамм на грамм, вместимость перегной удерживать питательные вещества и воду намного больше, чем у глинистых минералов, большая часть почвы катионообменная емкость возникающий из обвинения карбоновый группы по органическому веществу.[8] Однако, несмотря на высокую способность гумуса удерживать воду после замачивания, его высокая гидрофобность снижает ее смачиваемость.[9] В общем, небольшое количество гумуса может значительно увеличить способность почвы способствовать росту растений.[10][7]
| Элемент | Символ | Ион или молекула |
|---|---|---|
| Углерод | C | CO2 (в основном через листья) |
| Водород | ЧАС | ЧАС+, HOH (вода) |
| Кислород | О | О2−, ОЙ −, CO32−, ТАК42−, CO2 |
| Фосфор | п | ЧАС2PO4 −, HPO42− (фосфаты) |
| Калий | K | K+ |
| Азот | N | NH4+, НЕТ3 − (нитрат аммония) |
| Сера | S | ТАК42− |
| Кальций | Ca | Ca2+ |
| Утюг | Fe | Fe2+, Fe3+ (железо, железо) |
| Магний | Mg | Mg2+ |
| Бор | B | ЧАС3BO3, H2BO3 −, В (ОН)4 − |
| Марганец | Mn | Mn2+ |
| Медь | Cu | Cu2+ |
| Цинк | Zn | Zn2+ |
| Молибден | Пн | МоО42− (молибдат) |
| Хлор | Cl | Cl − (хлористый) |
Процессы поглощения
Питательные вещества, содержащиеся в почве, попадают в растение через его корни, и в частности корневые волоски. Чтобы растение усвоило питательный элемент, он должен находиться у поверхности корня; однако запас питательных веществ в контакте с корнем быстро истощается на расстоянии прибл. 2 мм.[12] Существует три основных механизма, посредством которых ионы питательных веществ, растворенные в почвенном растворе, контактируют с корнями растений:
- Массовый поток воды
- Распространение в воде
- Перехват корневым ростом
Все три механизма работают одновременно, но тот или иной механизм может быть наиболее важным для конкретного питательного вещества.[13] Например, в случае кальция, которого обычно много в почвенном растворе, за исключением случаев, когда алюминий чрезмерно конкурирует с кальцием на катионный обмен участки в очень кислых почвах (pH менее 4),[14] Один только массовый поток обычно может доставить достаточное количество к поверхности корня. Однако в случае фосфора диффузия необходима для пополнения массового расхода. По большей части ионы питательных веществ должны пройти некоторое расстояние в почвенном растворе, чтобы достичь поверхности корней. Это движение может происходить за счет массового потока, например, когда растворенные питательные вещества уносятся вместе с почвенной водой, текущей к корню, который активно забирает воду из почвы. В этом типе движения ионы питательных веществ в чем-то похожи на листья, плывущие по течению. Кроме того, ионы питательных веществ непрерывно перемещаются путем диффузии из областей с большей концентрацией к обедненным питательными веществами участкам с более низкой концентрацией вокруг поверхности корня. Этот процесс происходит из-за случайного движения, также называемого Броуновское движение молекул в градиенте убывающей концентрации.[15] Таким образом, растения могут продолжать поглощать питательные вещества даже ночью, когда вода лишь медленно всасывается в корни. испарение почти перестал следовать устьичный закрытие. Наконец, в игру вступает перехват корней, так как корни постоянно прорастают в новую, необработанную почву. Таким образом, корни также могут поглощать наноматериалы Такие как наночастицы органическая материя.[16]
| Питательный | Примерный процент предоставлен: | ||
|---|---|---|---|
| Массовый поток | Корневой перехват | Распространение | |
| Азот | 98.8 | 1.2 | 0 |
| Фосфор | 6.3 | 2.8 | 90.9 |
| Калий | 20.0 | 2.3 | 77.7 |
| Кальций | 71.4 | 28.6 | 0 |
| Сера | 95.0 | 5.0 | 0 |
| Молибден | 95.2 | 4.8 | 0 |
В приведенной выше таблице питательные вещества, содержащие фосфор и калий, перемещаются больше за счет диффузии, чем за счет массового потока в водном растворе почвы, поскольку они быстро поглощаются корнями, создавая почти нулевую концентрацию около корней (растения не могут пропускать достаточно воды. чтобы привлечь больше этих питательных веществ к корням). Очень крутой градиент концентрации имеет большее влияние на движение этих ионов, чем движение их массовым потоком.[18] Движение массовым потоком требует транспирации воды из растения, в результате чего ионы воды и раствора также перемещаются к корням.[19] Движение путем перехвата корней является самым медленным, поскольку растения должны расширять свои корни.[20]
Растения выводят ионы из своих корней, чтобы перенести питательные вещества из почвы, и этот процесс обмена происходит в корне. апопласт.[21] Водород H+ обменивается на другие катионы, а карбонат (HCO3−) и гидроксид (OH−) анионы обмениваются на анионы питательных веществ.[22] Когда корни растений удаляют питательные вещества из водного раствора почвы, они пополняются, поскольку другие ионы удаляются из глины и гумуса (за счет ионный обмен или же десорбция ), добавляются из выветривание минералов почвы, и высвобождаются разложение органического вещества почвы. Однако скорость, с которой корни растений удаляют питательные вещества, может не соответствовать скорости, с которой они пополняются в почвенном растворе, что приводит к ограничению питательных веществ для роста растений.[23] Растения получают большую часть своих анионных питательных веществ из разлагающихся органических веществ, которые обычно содержат около 95 процентов почвенного азота, от 5 до 60 процентов почвенного фосфора и около 80 процентов почвенной серы. При выращивании сельскохозяйственных культур восполнение запасов питательных веществ в почве обычно должно быть увеличено за счет добавления удобрений или органических веществ.[17]
Поскольку поглощение питательных веществ является активным метаболическим процессом, условия, которые препятствуют метаболизму корней, также могут препятствовать поглощению питательных веществ.[24] Примеры таких условий включают: заболачивание или же уплотнение почвы приводит к бедным аэрация почвы, чрезмерно высокие или низкие температуры почвы и наземные условия, которые приводят к низкому перемещению сахаров к корням растений.[25]
Углерод

Растения получают углерод из атмосферного углекислого газа через фотосинтетический карбоксилирование, к которому необходимо добавить поглощение растворенного углерода из почвенного раствора[26] и перенос углерода через микоризные сети.[27] Около 45% сухой массы растения составляет углерод; растительные остатки обычно имеют отношение углерода к азоту (C / N) от 13: 1 до 100: 1. Поскольку органический материал почвы переваривается микроорганизмы и сапрофаг почвенная фауна, отношение C / N уменьшается по мере метаболизма углеродистого материала и двуокиси углерода (CO2) выбрасывается в качестве побочного продукта, который затем попадает из почвы в атмосферу. Оборот азота (в основном участвует в белковый оборот ) меньше, чем углерода (в основном участвует в дыхание ) в живом, затем в мертвом веществе разлагатели, которые всегда богаче азотом, чем подстилка, и поэтому он накапливается в почве.[28] Нормальный CO2 концентрация в атмосфере 0,03%, это может быть фактором, ограничивающим рост растений. На поле кукурузы в тихий день в условиях высокой освещенности в период вегетации CO2 концентрация падает очень низко, но в таких условиях культура может использовать концентрацию, в 20 раз превышающую нормальную. Дыхание CO2 почвенными микроорганизмами, разлагающими органическое вещество почвы и CO2 вдыхаемые корнями вносят большое количество CO2 к фотосинтез растения, к которым необходимо добавить СО2 дышит надземными тканями растений.[29] СО с корневым дыханием2 могут накапливаться в течение ночи в полых стеблях растений, чтобы в дальнейшем использовать их для фотосинтеза в течение дня.[30] В почве CO2 концентрация в 10–100 раз выше атмосферных уровней, но может возрасти до токсичных уровней, если пористость почвы низкая или если диффузия затруднена из-за наводнения.[31][1][32]
Азот
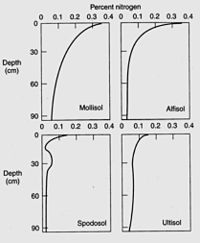
Азот является наиболее важным элементом, получаемым растениями из почвы, за исключением влажных тропических лесов, где фосфор является основным элементом. ограничение питательных веществ в почве,[33] и дефицит азота часто ограничивает рост растений.[34] Растения могут использовать азот в качестве аммоний катион (NH4+) или анион нитрат (НЕТ3−). Растения обычно классифицируются как аммиачные или нитратные в соответствии с их предпочтительным азотным питанием.[35] Обычно большая часть азота в почве связана с органическими соединениями, составляющими органическое вещество почвы, и должна быть минерализованный в аммонийную или нитратную форму, прежде чем она сможет усвоиться большинством растений. Однако симбиоз с микоризные грибы позволяют растениям получить доступ к бассейну органического азота там, где и когда минеральные формы азота недоступны.[36] Общее содержание азота в значительной степени зависит от содержания органического вещества почвы, которое, в свою очередь, зависит от текстуры, климата, растительности, топографии, возраста и управление почвой.[37] Азот в почве обычно уменьшается на 0,2–0,3% при каждом повышении температуры на 10 ° C. Обычно почвы пастбищ содержат больше почвенного азота, чем лесные почвы, из-за более высокой скорости оборота органического вещества пастбищ.[38] Культивирование снижает почвенный азот, подвергая органическое вещество почвы разложению микроорганизмами.[39] большинство потерь вызвано денитрификация,[40] а почвы без обработки почвы содержат больше азота в почве, чем пахотные почвы.[41]
Немного микроорганизмы способны метаболизировать органические вещества и выделять аммоний в процессе, называемом минерализация. Другие, называемые нитрификаторы возьми бесплатно аммоний или же нитрит как промежуточный шаг в процессе нитрификация, и окислить до нитрат. Азотфиксирующие бактерии способны метаболизировать N2 в виде аммиак или родственные азотистые соединения в процессе, называемом азотфиксация. И аммоний, и нитрат могут быть обездвижен путем их включения в живые клетки микробов, где он временно изолируется в виде аминокислоты и белки. Нитраты могут быть потеряны из почвы в атмосферу, когда бактерии метаболизируют его до газов NH.3, N2 и н2О, процесс называется денитрификация. Азот также может быть выщелоченный от вадозная зона если в форме нитрата, действующего как загрязнитель если он достигнет уровень грунтовых вод или же течет по земле, особенно в сельскохозяйственных почвах с высоким использованием питательных удобрений.[42] Аммоний также может быть изолирован в соотношении 2: 1. глинистые минералы.[43] Небольшое количество азота добавляется в почву осадки, за исключением обширных территорий Северной Америки и Западной Европы, где чрезмерное использование азотные удобрения и навоз вызвало загрязнение атмосферы выбросами аммиака, попадающими в закисление почвы и эвтрофикация почв и водные экосистемы.[44][45][7][46][47][48]
Прибыль
В процессе минерализация, микробы питаются органическими веществами, выделяя аммиак (NH3), аммоний (NH4+), нитрат (NO3−) и другие питательные вещества. Пока отношение углерода к азоту (C / N) свежих остатков в почве превышает 30: 1, азот будет в дефиците для богатой азотом микробной биомассы (дефицит азота ), а другие бактерии будут поглощать аммоний и, в меньшей степени, нитраты, и включать их в свои клетки в иммобилизация процесс.[49] В такой форме азот считается обездвижен. Позже, когда такие бактерии умирают, они тоже минерализованный и часть азота выделяется в виде аммония и нитрата. Хищничество бактерий почвенной фауной, в частности простейшие и нематоды, играют решающую роль в возвращении иммобилизованного азота в минеральные формы.[50] Если C / N свежих остатков меньше 15, минеральный азот попадает в почву и напрямую становится доступным для растений.[51] Бактерии могут в среднем добавлять 25 фунтов (11 кг) азота на акр, а на неоплодотворенных полях это самый важный источник пригодного для использования азота. В почве с 5% органического вещества, возможно, от 2 до 5% этого разложения попадает в почву. Быстрее всего возникает в теплой, влажной, хорошо аэрированной почве.[52] Минерализация 3% органического материала почвы, которая состоит из 4% органических веществ в целом, приведет к высвобождению 120 фунтов (54 кг) азота в виде аммония на акр.[53]
| Органический материал | Соотношение C: N |
|---|---|
| Люцерна | 13 |
| Бактерии | 4 |
| Клевер, сладкий зеленый | 16 |
| Клевер зрелый сладкий | 23 |
| Грибы | 9 |
| Лесная подстилка | 30 |
| Гумус в теплых окультуренных почвах | 11 |
| Бобово-злаковое сено | 25 |
| Бобовые (люцерна или клевер), зрелые | 20 |
| Навоз, коровий | 18 |
| Навоз, лошадь | 16–45 |
| Навоз человеческий | 10 |
| Овсяная солома | 80 |
| Солома, стебли кукурузы | 90 |
| Опилки | 250 |
В азотфиксация, ризобий бактерии конвертируют N2 в аммиак (NH3), который быстро преобразуется в аминокислоты, части которых используются ризобиями для синтеза белков собственной биомассы, а другие части транспортируются в ксилема растения-хозяина.[55] Ризобия поделиться симбиотические отношения с растениями-хозяевами, поскольку ризобии снабжают хозяина азотом, а хозяин обеспечивает ризобии другими питательными веществами и безопасную среду. Считается, что такие симбиотические бактерии в корневые узелки из бобовые добавьте от 45 до 250 фунтов азота на акр в год, что может быть достаточно для урожая. Другой, свободноживущий азотфиксатор диазотроф бактерии и археи живут независимо в почве и выделяют минеральные формы азота, когда их мертвые тела преобразуются посредством минерализация.[56]
Некоторое количество используемого азота фиксируется молния в виде оксида азота (NO) и диоксида азота (NO2−).[57] Двуокись азота растворяется в воде с образованием азотная кислота (HNO3) диссоциирует в H+ и нет3−. Аммиак, NH3, ранее выбрасываемые из почвы, могут выпадать с осадками в виде азотной кислоты из расчета около пяти фунтов азота на акр в год.[58]
Секвестр
Когда бактерии питаются растворимыми формами азота (аммоний и нитрат), они временно улавливают этот азот в своих телах в процессе, называемом иммобилизация. Позже, когда эти бактерии умирают, их азот может выделяться в виде аммония в процессе минерализации, ускоряемого хищной фауной.[59]
Белковый материал легко расщепляется, но скорость его разложения замедляется из-за его прикрепления к кристаллической структуре глины и захвата между слоями глины.[60] или прикреплены к грубым глиняным поверхностям.[61] Слои достаточно малы, чтобы бактерии не могли проникнуть внутрь.[62] Некоторые организмы могут выделять внеклеточные ферменты, которые действуют на секвестрированные белки. Однако эти ферменты также могут задерживаться на кристаллах глины, что приводит к сложному взаимодействию между белками, микробными ферментами и минеральными поверхностями.[63]
Фиксация аммония происходит в основном между слоями глинистых минералов типа 2: 1, таких как иллит, вермикулит или же монтмориллонит, вместе с ионами аналогичных ионный радиус и низкий энергия гидратации Такие как калий, но небольшая часть аммония также фиксируется в ил дробная часть.[64] Таким образом удерживается лишь небольшая часть почвенного азота.[65]
Убытки
Полезный азот может теряться из почвы, когда он находится в форме нитрат, так как это легко выщелоченный, вопреки аммоний что легко исправить.[66] Дальнейшие потери азота происходят из-за денитрификация, процесс, при котором почвенные бактерии превращают нитраты (NO3−) к газообразному азоту, N2 или N2О. Это происходит при плохой аэрация почвы ограничивает свободный кислород, заставляя бактерии использовать кислород, содержащийся в нитратах, для дыхательных процессов. Денитрификация увеличивается, когда доступен окисляемый органический материал, как в органическое земледелие[66] и когда почвы теплые и слегка кислые, как в настоящее время происходит в тропических регионах.[67] Денитрификация может варьироваться в зависимости от почвы, поскольку аэрация варьируется от места к месту.[68] Денитрификация может вызвать потерю от 10 до 20 процентов доступных нитратов в течение дня, а когда условия благоприятны для этого процесса, могут произойти потери до 60 процентов нитратов, применяемых в качестве удобрения.[69]
Улетучивание аммиака происходит, когда аммоний химически реагирует с щелочная почва, конвертируя NH4+ в NH3.[70] Внесение аммиачных удобрений на такое поле может привести к потерям от испарения до 30 процентов.[71]
Все виды потерь азота, будь то выщелачивание или испарение, ответственны за большую часть водоносный горизонт загрязнение[72] и загрязнение воздуха, с сопутствующим действием на закисление почвы и эвтрофикация,[73] новое сочетание экологических угроз (кислотность и избыток азота), к которым существующие организмы плохо приспособлены, что приводит к серьезным потерям биоразнообразия в естественных экосистемах.[74]
Фосфор
После азота фосфор, вероятно, является элементом, наиболее вероятно дефицитным в почвах, хотя он часто оказывается наиболее дефицитным в тропических почвах, где минеральные запасы истощаются в условиях интенсивного воздействия. выщелачивание и минеральное выветривание при этом, в отличие от азота, запасы фосфора не могут быть восполнены из других источников.[75] Минерал почвы апатит является наиболее распространенным минеральным источником фосфора, из которого он может быть извлечен микробными и корневыми экссудатами,[76][77] с важным вкладом арбускулярный микоризный грибы.[78] Наиболее распространенная форма органического фосфата - это фитат, основная форма хранения фосфора во многих тканях растений. Хотя в почве содержится в среднем 1000 фунтов на акр (1120 кг на гектар) фосфора, он обычно находится в форме ортофосфат с низкой растворимостью, за исключением случаев, когда они связаны с аммонием или кальцием, поэтому использование диаммонийфосфат или же монокальций фосфат как удобрения.[79] Общий фосфор составляет около 0,1 процента от веса почвы, но только один процент от этого количества напрямую доступен для растений. Из доступной части более половины приходится на минерализацию органических веществ. Возможно, потребуется удобрение сельскохозяйственных полей, чтобы восполнить фосфор, который был удален из урожая.[80]
Когда фосфор действительно образует солюбилизированные ионы H2PO4−, если они не попадают в корни растений, они быстро образуют нерастворимые фосфаты кальция или водные оксиды железа и алюминия. Фосфор в основном неподвижен в почве и не выщелачивается, но фактически накапливается в поверхностном слое, если его не обрабатывать. Внесение растворимых удобрений в почву может привести к цинк недостатки как фосфаты цинка формы, но уровни pH почвы, частично зависящие от формы фосфора в удобрении, сильно влияют на этот эффект, в некоторых случаях приводя к увеличению доступности цинка.[81] Недостаток фосфора может помешать нормальному открытию листьев растения. устьица, уменьшилось устьичная проводимость что привело к уменьшению фотосинтез и частота дыхания[82] пока уменьшился испарение повышает температуру растений.[83] Фосфор наиболее доступен, когда pH почвы составляет 6,5 в минеральных почвах и 5,5 в органических почвах.[71]
Калий
Количество калия в почве может достигать 80000 фунтов на акро-фут, из которых только 150 фунтов доступны для роста растений. Общие минеральные источники калия - слюда. биотит и калиевый полевой шпат, КАЛСИ3О8. Ризосфера бактерии, также называемые ризобактерии, внести свой вклад в производство органические кислоты к его солюбилизации.[84] При растворении половина будет удерживаться в виде обменных катионов на глине, а другая половина - в водном растворе почвы. Фиксация калия часто происходит, когда почва высыхает и калий связывается между слоями 2: 1. экспансивная глина минералы, такие как иллит, вермикулит или же монтмориллонит.[85] При определенных условиях, в зависимости от текстуры почвы, интенсивности высыхания и начального количества обменного калия, фиксированный процент может достигать 90 процентов в течение десяти минут. Калий может выщелачиваться из почв с низким содержанием глины.[86][87]
Кальций
Кальций составляет один процент от веса почвы и обычно доступен, но может быть низким, поскольку он растворим и может выщелачиваться. Таким образом, он низкий в песчаных и сильно выщелоченных почвах или сильнокислых минеральных почвах, что приводит к чрезмерной концентрации свободных ионов водорода в почвенном растворе, и, следовательно, эти почвы требуют известкования.[88] Кальций поступает в растения в виде обменных ионов и умеренно растворимых минералов. В почве есть четыре формы кальция. Почвенный кальций может находиться в нерастворимых формах, таких как кальцит или же доломит, в почвенном растворе в виде двухвалентный катион или сохраняется в обменная форма на поверхности минеральных частиц. Другая форма - это когда кальций соединяется с органическими веществами, образуя ковалентные связи между органические соединения которые способствуют структурная устойчивость.[89] Кальций более доступен в коллоидах почвы, чем калий, потому что общий минерал кальцит, CaCO3, более растворим, чем минералы, содержащие калий, такие как полевой шпат.[90]
Поглощение кальция корнями необходимо для питание растений, вопреки старому утверждению, что это было потребление роскоши.[91] Кальций считается важным компонентом растений. клеточные мембраны, а противоион для неорганических и органических анионы в вакуоль, и внутриклеточный мессенджер в цитозоль играет роль в сотовой учусь и объем памяти.[92]
Магний
Магний является одним из основных обменных катионов в большинстве почв (после кальция и калия). Магний является важным элементом для растений, микробов и животных, участвуя во многих каталитические реакции и в синтезе хлорофилл. Основные минералы, которые способствуют выделению магния, включают: роговая обманка, биотит и вермикулит. Концентрации магния в почве обычно достаточно для оптимального роста растений, но сильно выветрившиеся и песчаные почвы могут испытывать дефицит магния из-за вымывания сильными осадками.[7][93]
Сера
Большая часть серы, как и фосфор, становится доступной для растений, высвобождаясь при разложении органических веществ.[93] В некоторых почвах (особенно песчаных) может существовать дефицит, и при возделывании необходимо добавить серу. Внесение большого количества азота на поля с незначительным содержанием серы может вызвать дефицит серы из-за эффект разбавления когда стимуляция роста растений азотом увеличивает потребность растений в сере.[94] 15-тонный урожай лука использует до 19 фунтов серы, а 4 тонны люцерны - 15 фунтов на акр. Содержание серы зависит от глубины. В образце почв в Огайо, США, содержание серы варьировалось в зависимости от глубины: 0–6 дюймов, 6–12 дюймов, 12–18 дюймов, 18–24 дюймов в количествах: 1056, 830, 686, 528 фунтов на акр соответственно.[95]
Микроэлементы
В микроэлементы необходимые для жизни растений, в порядке важности, включают утюг,[96] марганец,[97] цинк,[98] медь,[99] бор,[100] хлор[101] и молибден.[102] Этот термин относится к потребностям растений, а не к их изобилию в почве. Они требуются в очень небольших количествах, но необходимы для здоровье растений в том, что большинство необходимых частей фермент системы, которые задействованы в заводе метаболизм.[103] Обычно они присутствуют в минеральном компоненте почвы, но сильное внесение фосфатов может вызвать дефицит цинка и железа из-за образования нерастворимых фосфатов цинка и железа.[104] Недостаток железа в растении хлороз и ризосфера подкисление также может быть результатом чрезмерного содержания в почве тяжелых металлов или минералов кальция (извести).[105][106] Избыточные количества растворимого бора, молибдена и хлорида токсичны.[107][108]
Несущественные питательные вещества
Питательные вещества, укрепляющие здоровье, но дефицит которых не останавливает жизненный цикл растений, включают: кобальт, стронций, ванадий, кремний и никель.[109] По мере оценки их важности они могут быть добавлены к списку основных питательных веществ для растений, как в случае кремния.[110]
Смотрите также
- Щелочная почва
- Натриевые почвы
- Катионообменная емкость
- Загрязнение почвы
- Плодородие почвы
- Указатель статей о почве
Рекомендации
- ^ а б Дин 1957, п. 80.
- ^ Рассел 1957 С. 123–25.
- ^ а б Брэди, Найл С.; Вейл, Рэй Р. (2008). Природа и свойства почв (14-е изд.). Река Аппер Сэдл: Пирсон.
- ^ Van der Ploeg, Rienk R .; Бём, Вольфганг и Киркхэм, Мэри Бет (1999). «О происхождении теории минерального питания растений и закона минимума». Журнал Американского общества почвоведов. 63 (5): 1055–62. Bibcode:1999SSASJ..63.1055V. CiteSeerX 10.1.1.475.7392. Дои:10.2136 / sssaj1999.6351055x.
- ^ Кнехт, Магнус Ф. и Йоранссон, Андерс (2004). «Наземным растениям требуются питательные вещества в аналогичных пропорциях». Физиология деревьев. 24 (4): 447–60. Дои:10.1093 / treephys / 24.4.447. PMID 14757584.
- ^ Дин 1957 С. 80–81.
- ^ а б c d Рой, Р. Н .; Финк, Арнольд; Блэр, Грэм Дж .; Тандон, Хари Лал Сингх (2006). «Глава 4: Плодородие почвы и растениеводство» (PDF). Питание растений для обеспечения продовольственной безопасности: руководство по комплексному управлению питательными веществами. Рим, Италия: Продовольственная и сельскохозяйственная организация Объединенных Наций. С. 43–90. ISBN 978-92-5-105490-1. Получено 21 июля 2019.
- ^ Parfitt, Roger L .; Гилтрап, Донна Дж. И Уиттон, Джо С. (1995). «Вклад органического вещества и глинистых минералов в катионообменную способность почвы» (PDF ). Коммуникации в области почвоведения и анализа растений. 26 (9–10): 1343–55. Дои:10.1080/00103629509369376. Получено 28 июля 2019.
- ^ Хайнос, Мечислав; Йозефачук, Гжегож; Соколовская, Зофия; Грайффенхаген, Андреас и Вессолек, Герд (2003). «Водоемкость, поверхность и структурные свойства песчаных лесогумусовых горизонтов» (PDF ). Журнал питания растений и почвоведения. 166 (5): 625–34. Дои:10.1002 / jpln.200321161. Получено 28 июля 2019.
- ^ Донахью, Миллер и Шиклуна 1977 С. 123–31.
- ^ Донахью, Миллер и Шиклуна 1977, п. 125.
- ^ Фёзе, Дорис; Клаассен, Норберт и Юнгк, Альбрехт (1991). «Эффективность растений по фосфору. II. Значение радиуса корня, корневых волосков и катионно-анионного баланса для притока фосфора у семи видов растений» (PDF). Растение и почва. 132 (2): 261–72. Дои:10.1007 / BF00010407. S2CID 28489187. Получено 4 августа 2019.
- ^ Барбер, Стэнли А .; Уокер, Дж. М. и Васи, Эдфред Х. (1963). «Механизмы перемещения питательных веществ для растений от почвы и удобрений к корням растений». Журнал сельскохозяйственной и пищевой химии. 11 (3): 204–07. Дои:10.1021 / jf60127a017.
- ^ Лоуренс, Грегори Б.; Дэвид, Марк Б. и Шортл, Уолтер С. (1995). «Новый механизм потери кальция в лесных почвах» (PDF ). Природа. 378 (6553): 162–65. Bibcode:1995Натура 378..162л. Дои:10.1038 / 378162a0. S2CID 4365594. Получено 11 августа 2019.
- ^ Крамерс, Хендрик Энтони (1940). «Броуновское движение в силовом поле и диффузионная модель химических реакций» (PDF). Physica. 7 (4): 284–304. Bibcode:1940Phy ..... 7..284K. Дои:10.1016 / S0031-8914 (40) 90098-2. Получено 11 августа 2019.
- ^ Лин, Сиджи; Репперт, Джейсон; Ху Цянь; Хадсон, Джоан С .; Reid, Michelle L .; Ратникова, Татьяна А .; Rao, Apparao M .; Ло, Хун и Кэ, Пу Чун (2009). «Поглощение, перемещение и передача углеродных наноматериалов в рисовых растениях» (PDF ). Маленький. 5 (10): 1128–32. Дои:10.1002 / smll.200801556. PMID 19235197. Получено 11 августа 2019.
- ^ а б Донахью, Миллер и Шиклуна 1977, п. 126.
- ^ «Питание растений». Университет Северной Аризоны. В архиве из оригинала 14 мая 2013 г.. Получено 18 апреля 2019.
- ^ Матимати, Великолепный; Вербум, Г. Энтони и Крамер, Майкл Д. (2014). «Азотная регуляция транспирации контролирует массовый расход питательных веществ». Журнал экспериментальной ботаники. 65 (1): 159–68. Дои:10.1093 / jxb / ert367. ЧВК 3883293. PMID 24231035.
- ^ Менгель, Дэйв. «Корни, рост и потребление питательных веществ» (PDF). Университет Пердью, факультет агрономии. Получено 18 апреля 2019.
- ^ Саттельмахер, Буркхард (2001). «Апопласт и его значение для минерального питания растений». Новый Фитолог. 149 (2): 167–92. Дои:10.1046 / j.1469-8137.2001.00034.x.
- ^ Хинзингер, Филипп; Плассар, Клод; Тан, Caixian и Jaillard, Бенуа (2003). "Истоки опосредованных корнями изменений pH в ризосфере и их реакция на ограничения окружающей среды: обзор" (PDF ). Растение и почва. 248 (1): 43–59. Дои:10.1023 / А: 1022371130939. S2CID 23929321. Получено 18 августа 2019.
- ^ Чапин, Ф. Стюарт III; Витоусек, Питер М. и Ван Клив, Кейт (1986). «Природа ограничения питательных веществ в растительных сообществах». Американский натуралист. 127 (1): 48–58. Дои:10.1086/284466. JSTOR 2461646.
- ^ Алам, Сайед Манзур (1999). «Поглощение питательных веществ растениями в стрессовых условиях». В Пессаракли, Мохаммад (ред.). Справочник по стрессу растений и сельскохозяйственных культур (2-е изд.). Нью Йорк, Нью Йорк: Марсель Деккер. С. 285–313. ISBN 978-0824719487.
- ^ Донахью, Миллер и Шиклуна 1977 С. 123–28.
- ^ Расмуссен, Джим и Кузяков, Яков (2009). «Изотопы углерода как доказательство поглощения растениями органического азота: актуальность поглощения неорганического углерода» (PDF ). Биология и биохимия почвы. 41 (7): 1586–87. Дои:10.1016 / j.soilbio.2009.03.006. Получено 8 сентября 2019.
- ^ Слесарь, Аластер Х .; Грейвс, Джонатан Д.; Watkins, N.K .; Робинсон, Дэвид и Скримджер, Чарли (1998). «Перенос углерода между растениями и его контроль в сетях арбускулярной микоризы». Функциональная экология. 12 (3): 406–12. Дои:10.1046 / j.1365-2435.1998.00206.x.
- ^ Манцони, Стефано; Трофимоу, Джон А .; Джексон, Роберт Б. и Порпорато, Амилкар (2010). «Стехиометрический контроль динамики углерода, азота и фосфора при разложении подстилки» (PDF). Экологические монографии. 80 (1): 89–106. Дои:10.1890/09-0179.1. Получено 15 сентября 2019.
- ^ Тески, Роберт О .; Савейн, Ан; Степь, Кэти и Макгуайр, Мэри Энн (2007). «Происхождение, судьба и значение СО2 в стволах деревьев». Новый Фитолог. 177 (1): 17–32. Дои:10.1111 / j.1469-8137.2007.02286.x. PMID 18028298.
- ^ Биллингс, Уильям Дуайт и Годфри, Пол Джозеф (1967). «Фотосинтетическое использование внутреннего углекислого газа полостебельными растениями». Наука. 158 (3797): 121–23. Bibcode:1967Sci ... 158..121B. Дои:10.1126 / science.158.3797.121. JSTOR 1722393. PMID 6054809. S2CID 13237417.
- ^ Уодли 1957, п. 41.
- ^ Бродбент 1957, п. 153.
- ^ Витаусек, Питер М. (1984). «Опад, круговорот питательных веществ и ограничение питательных веществ в тропических лесах» (PDF ). Экология. 65 (1): 285–98. Дои:10.2307/1939481. JSTOR 1939481. Получено 29 сентября 2019.
- ^ Донахью, Миллер и Шиклуна 1977, п. 128.
- ^ Форд, Брайан Г. и Кларксон, Дэвид Т. (1999). «Нитратное и аммонийное питание растений: физиологические и молекулярные перспективы» (PDF ). Достижения в ботанических исследованиях. 30 (C): 1–90. Дои:10.1016 / S0065-2296 (08) 60226-8. Получено 29 сентября 2019.
- ^ Ходж, Анджела; Кэмпбелл, Колин Д. и Установщик, Аластер Х. (2001). «Арбускулярный микоризный гриб ускоряет разложение и получает азот непосредственно из органического материала» (PDF). Природа. 413 (6853): 297–99. Bibcode:2001Натура.413..297H. Дои:10.1038/35095041. PMID 11565029. S2CID 4423745. Получено 29 сентября 2019.
- ^ Берк, Ингрид С .; Йонкер, Кэролайн М .; Партон, Уильям Дж .; Коул, К. Вернон; Флах, Клаус и Шимель, Дэвид С. (1989). «Влияние текстуры, климата и выращивания на содержание органических веществ в почвах пастбищ США» (PDF ). Журнал Американского общества почвоведов. 53 (3): 800–05. Bibcode:1989SSASJ..53..800B. Дои:10.2136 / sssaj1989.03615995005300030029x. Получено 6 октября 2019.
- ^ Энрикес, Сусана; Дуарте, Карлос М. и Санд-Йенсен, Кай (1993). «Модели скорости разложения среди фотосинтезирующих организмов: важность содержания C: N: P в детрите» (PDF ). Oecologia. 94 (4): 457–71. Bibcode:1993Oecol..94..457E. Дои:10.1007 / BF00566960. PMID 28313985. S2CID 22732277. Получено 6 октября 2019.
- ^ Тиссен, Холм; Стюарт, Джон В. Б. и Беттани, Джефф Р. (1982). «Воздействие культивирования на количество и концентрацию углерода, азота и фосфора в лугопастбищных почвах» (PDF). Агрономический журнал. 74 (5): 831–35. Дои:10.2134 / agronj1982.00021962007400050015x. Получено 13 октября 2019.
- ^ Филиппот, Лоран; Холлин, Сара и Шлотер, Майкл (2007). «Экология денитрифицирующих прокариот в сельскохозяйственных почвах». В Sparks, Дональд Л. (ред.). Успехи агрономии, Том 96. Амстердам, Нидерланды: Эльзевир. С. 249–305. CiteSeerX 10.1.1.663.4557. ISBN 978-0-12-374206-3.
- ^ Доран, Джон В. (1987). «Микробная биомасса и распределение минерализируемого азота в беспахотных и вспаханных почвах» (PDF ). Биология и плодородие почв. 5 (1): 68–75. Дои:10.1007 / BF00264349. S2CID 44201431. Получено 13 октября 2019.
- ^ Махви, Амир Х .; Нури, Джафар; Бабаи, Али А. и Набизаде, Рамин (2005). «Влияние сельскохозяйственной деятельности на нитратное загрязнение подземных вод» (PDF ). Международный журнал экологических наук и технологий. 2 (1): 41–47. Дои:10.1007 / BF03325856. S2CID 94640003. Получено 20 октября 2019.
- ^ Scherer, Heinrich W .; Фейлс, Э. и Бойтерс, Патрик (2014). «Фиксация и выделение аммония глинистыми минералами под влиянием калия» (PDF). Растения, почва и окружающая среда. 60 (7): 325–31. Дои:10.17221 / 202/2014-PSE. S2CID 55200516. Получено 20 октября 2019.
- ^ Барак, Филипп; Jobe, Babou O .; Krueger, Armand R .; Петерсон, Ллойд А. и Лэрд, Дэвид А. (1997). «Влияние длительного закисления почвы из-за внесения азотных удобрений в Висконсине» (PDF ). Растение и почва. 197 (1): 61–69. Дои:10.1023 / А: 1004297607070. S2CID 2410167. Получено 27 октября 2019.
- ^ Ван Эгмонд, Клаас; Брессер, Тон и Боуман, Лекс (2002). «Европейский азотный случай» (PDF). Ambio. 31 (2): 72–78. Дои:10.1579/0044-7447-31.2.72. PMID 12078012. S2CID 1114679. Получено 27 октября 2019.
- ^ Эллисон 1957 С. 85–94.
- ^ Бродбент 1957 С. 152–55.
- ^ Донахью, Миллер и Шиклуна 1977 С. 128–31.
- ^ Рекус, Сильви и Мэри, Бруно (1990). «Микробная иммобилизация аммония и нитрата в культурных почвах» (PDF ). Биология и биохимия почвы. 22 (7): 913–22. Дои:10.1016 / 0038-0717 (90) 90129-Н. Получено 3 ноября 2019.
- ^ Верхоф, Герман А. и Брюссард, Лейберт (1990). «Разложение и минерализация азота в природных и агроэкосистемах: вклад почвенных животных» (PDF ). Биогеохимия. 11 (3): 175–211. Дои:10.1007 / BF00004496. S2CID 96922131. Получено 3 ноября 2019.
- ^ Чен, Баоцин; Лю, ЭнКе; Тиан, Цичжуо; Ян, Чанжун и Чжан, Яньцин (2014). «Динамика почвенного азота и пожнивные остатки: обзор» (PDF ). Агрономия в интересах устойчивого развития. 34 (2): 429–42. Дои:10.1007 / s13593-014-0207-8. S2CID 18024074. Получено 3 ноября 2019.
- ^ Гриффин, Тимоти С .; Ханикатт, Чарльз В. и Он, Чжицзюнь (2002). «Влияние температуры, водного статуса почвы и типа почвы на трансформацию азота свиного навоза» (PDF ). Биология и плодородие почв. 36 (6): 442–46. Дои:10.1007 / s00374-002-0557-2. S2CID 19377528. Получено 24 ноября 2019.
- ^ Донахью, Миллер и Шиклуна 1977 С. 129–30.
- ^ Донахью, Миллер и Шиклуна 1977, п. 145.
- ^ Лодвиг, Эмма; Хози, Артур Х. Ф .; Бурдес, Александр; Финдли, Ким; Аллауэй, Дэвид; Карунакаран, Рамакришнан; Дауни, Дж. Аллан и Пул, Филип С. (2003). «Аминокислотный цикл стимулирует азотфиксацию в симбиозе бобовых и ризобий» (PDF ). Природа. 422 (6933): 722–26. Bibcode:2003Натура.422..722Л. Дои:10.1038 / природа01527. PMID 12700763. S2CID 4429613. Получено 10 ноября 2019.
- ^ Донахью, Миллер и Шиклуна 1977 С. 128–29.
- ^ Hill, R.D .; Ринкер, Роберт Г. и Уилсон, Х. Дейл (1980). «Фиксация атмосферного азота молниями». Журнал атмосферных наук. 37 (1): 179–92. Bibcode:1980JAtS ... 37..179H. Дои:10.1175 / 1520-0469 (1980) 037 <0179: ANFBL> 2.0.CO; 2.
- ^ Эллисон 1957, п. 87.
- ^ Феррис, Ховард; Венетт, Роберт С .; Ван дер Меулен, Ханс Р. и Лау, Серрин С. (1998). «Минерализация азота нематодами, питающимися бактериями: проверка и измерение» (PDF ). Растение и почва. 203 (2): 159–71. Дои:10.1023 / А: 1004318318307. S2CID 20632698. Получено 17 ноября 2019.
- ^ Виоланте, Антонио; де Кристофаро, Аннунциата; Рао, Мария А. и Джанфреда, Лилиана (1995). «Физико-химические свойства комплексов белок-смектит и белок-Al (OH) x-смектит» (PDF ). Глина Минералы. 30 (4): 325–36. Bibcode:1995ClMin..30..325V. Дои:10.1180 / Клинамин.1995.030.4.06. S2CID 94630893. Получено 24 ноября 2019.
- ^ Фогель, Кордула; Мюллер, Карстен В .; Хёшен, Кармен; Буггер, Франц; Хайстер, Катя; Шульц, Стефани; Шлотер, Михаэль и Кегель-Кнабнер, Ингрид (2014). «Субмикронные структуры обеспечивают предпочтительные места для связывания углерода и азота в почвах». Nature Communications. 5 (2947): 1–7. Bibcode:2014 НатКо ... 5.2947 В. Дои:10.1038 / ncomms3947. ЧВК 3896754. PMID 24399306.
- ^ Руампс, Лео Симон; Нунан, Наойс и Чену, Клэр (2011). «Микробная биогеография в масштабе пор почвы» (PDF ). Биология и биохимия почвы. 43 (2): 280–86. Дои:10.1016 / j.soilbio.2010.10.010. Получено 1 декабря 2019.
- ^ Quiquampoix, Эрве и Бернс, Ричард Г. (2007). «Взаимодействие между белками и минеральными поверхностями почвы: последствия для окружающей среды и здоровья» (PDF ). Элементы. 3 (6): 401–06. Дои:10.2113 / GSELEMENTS.3.6.401. Получено 24 ноября 2019.
- ^ Нидер, Рольф; Бенби, Динеш К. и Шерер, Генрих В. (2011). «Фиксация и дефиксация аммония в почвах: обзор» (PDF). Биология и плодородие почв. 47 (1): 1–14. Дои:10.1007 / s00374-010-0506-4. S2CID 7284269. Получено 8 декабря 2019.
- ^ Эллисон 1957, п. 90.
- ^ а б Крамер, Саша Б .; Реганольд, Джон П .; Гловер, Джерри Д.; Боханнан, Брендан Дж. М. И Муни, Гарольд А. (2006). «Снижение выщелачивания нитратов и повышение активности и эффективности денитрификаторов в почвах, удобренных органическими веществами» (PDF). Труды Национальной академии наук Соединенных Штатов Америки. 103 (12): 4522–27. Bibcode:2006ПНАС..103.4522К. Дои:10.1073 / pnas.0600359103. ЧВК 1450204. PMID 16537377. Получено 8 декабря 2019.
- ^ Робертсон, Дж. Филип (1989). «Нитрификация и денитрификация во влажных тропических экосистемах: потенциальный контроль удержания азота» (PDF ). В Проктор, Джон (ред.). Минеральные питательные вещества в экосистемах тропических лесов и саванн. Кембридж, Массачусетс: Blackwell Scientific. стр.55–69. ISBN 978-0632025596. Получено 15 декабря 2019.
- ^ Parkin, Timothy B. & Robinson, Joseph A. (1989). "Stochastic models of soil denitrification" (PDF). Прикладная и экологическая микробиология. 55 (1): 72–77. Дои:10.1128/AEM.55.1.72-77.1989. ЧВК 184056. PMID 16347838. Получено 15 декабря 2019.
- ^ Donahue, Miller & Shickluna 1977, п. 130.
- ^ Rao, Desiraju L.N. & Batra, Lalit (1983). "Ammonia volatilization from applied nitrogen in alkali soils" (PDF ). Растение и почва. 70 (2): 219–28. Дои:10.1007/BF02374782. S2CID 24724207. Получено 15 декабря 2019.
- ^ а б Donahue, Miller & Shickluna 1977, п. 131.
- ^ Lallouette, Vincent; Magnier, Julie; Petit, Katell & Michon, Janik (2014). "Agricultural practices and nitrates in aquatic environments" (PDF). Краткое. 11 (December): 1–16. Получено 15 декабря 2019.
- ^ Choudhury, Abu T.M.A. & Kennedy, Ivan R. (2005). "Nitrogen fertilizer losses from rice soils and control of environmental pollution problems" (PDF ). Коммуникации в области почвоведения и анализа растений. 36 (11–12): 1625–39. Дои:10.1081/css-200059104. S2CID 44014545. Получено 15 декабря 2019.
- ^ Roth, Tobias; Kohli, Lukas; Rihm, Beat & Achermann, Beat (2013). "Nitrogen deposition is negatively related to species richness and species composition of vascular plants and bryophytes in Swiss mountain grassland" (PDF ). Сельское хозяйство, экосистемы и окружающая среда. 178: 121–26. Дои:10.1016/j.agee.2013.07.002. Получено 15 декабря 2019.
- ^ Vitousek, Peter M. (1984). "Litterfall, nutrient cycling, and nutrient limitation in tropical forests" (PDF ). Экология. 65 (1): 285–98. Дои:10.2307/1939481. JSTOR 1939481. Получено 22 декабря 2019.
- ^ Kucey, Reg M.N. (1983). "Phosphate-solubilizing bacteria and fungi in various cultivated and virgin Alberta soils". Канадский журнал почвоведения. 63 (4): 671–78. Дои:10.4141/cjss83-068.
- ^ Khorassani, Reza; Hettwer, Ursula; Ratzinger, Astrid; Steingrobe, Bernd; Karlovsky, Petr & Claassen, Norbert (2011). "Citramalic acid and salicylic acid in sugar beet root exudates solubilize soil phosphorus". BMC Биология растений. 11 (121): 1–8. Дои:10.1186/1471-2229-11-121. ЧВК 3176199. PMID 21871058.
- ^ Duponnois, Robin; Colombet, Aline; Hien, Victor & Thioulouse, Jean (2005). "The mycorrhizal fungus Glomus intraradices and rock phosphate amendment influence plant growth and microbial activity in the rhizosphere of Acacia holosericea" (PDF). Биология и биохимия почвы. 37 (8): 1460–68. Дои:10.1016/j.soilbio.2004.09.016. Получено 22 декабря 2019.
- ^ Syers, John Keith; Johnston, A. Edward & Curtin, Denis (2008). Efficiency of soil and fertilizer phosphorus use: reconciling changing concepts of soil phosphorus behaviour with agronomic information (PDF). Рим, Италия: Продовольственная и сельскохозяйственная организация Объединенных Наций. ISBN 978-92-5-105929-6. Получено 29 декабря 2019.
- ^ Olsen & Fried 1957, п. 96.
- ^ Lambert, Raphaël; Grant, Cynthia & Sauvé, Sébastien (2007). "Cadmium and zinc in soil solution extracts following the application of phosphate fertilizers" (PDF ). Наука об окружающей среде в целом. 378 (3): 293–305. Bibcode:2007ScTEn.378..293L. Дои:10.1016/j.scitotenv.2007.02.008. PMID 17400282. Получено 5 января 2020.
- ^ Terry, Norman & Ulrich, Albert (1973). "Effects of phosphorus deficiency on the photosynthesis and respiration of leaves of sugar beet" (PDF). Физиология растений. 51 (1): 43–47. Дои:10.1104/pp.51.1.43. ЧВК 367354. PMID 16658294. Получено 5 января 2020.
- ^ Pallas, James E. Jr; Michel, B.E. & Harris, D.G. (1967). "Photosynthesis, transpiration, leaf temperature, and stomatal activity of cotton plants under varying water potentials" (PDF). Физиология растений. 42 (1): 76–88. Дои:10.1104/pp.42.1.76. ЧВК 1086491. PMID 16656488. Получено 12 января 2020.
- ^ Meena, Vijay Singh; Maurya, Bihari Ram; Verma, Jai Prakash; Aeron, Abhinav; Кумар, Ашок; Kim, Kangmin & Bajpai, Vivek K. (2015). "Potassium solubilizing rhizobacteria (KSR): isolation, identification, and K-release dynamics from waste mica" (PDF ). Экологическая инженерия. 81: 340–47. Дои:10.1016/j.ecoleng.2015.04.065. Получено 12 января 2020.
- ^ Sawhney, Brij L. (1972). "Selective sorption and fixation of cations by clay minerals: a review". Глины и глинистые минералы. 20 (2): 93–100. Bibcode:1972CCM....20...93S. Дои:10.1346/CCMN.1972.0200208.
- ^ Donahue, Miller & Shickluna 1977 С. 134–35.
- ^ Reitemeier 1957, стр. 101–04.
- ^ Loide, Valli (2004). "About the effect of the contents and ratios of soil's available calcium, potassium and magnesium in liming of acid soils" (PDF). Agronomy Research. 2 (1): 71–82. S2CID 28238101. Получено 19 января 2020.
- ^ Wuddivira, Mark N.; Camps-Roach, Geremy (2007). "Effects of organic matter and calcium on soil structural stability" (PDF ). Европейский журнал почвоведения. 58 (3): 722–27. Дои:10.1111/j.1365-2389.2006.00861.x. Получено 19 января 2020.
- ^ Donahue, Miller & Shickluna 1977 С. 135–36.
- ^ Smith, Garth S.; Cornforth, Ian S. (1982). "Concentrations of nitrogen, phosphorus, sulphur, magnesium, and calcium in North Island pastures in relation to plant and animal nutrition". Новозеландский журнал сельскохозяйственных исследований. 25 (3): 373–87. Дои:10.1080/00288233.1982.10417901.
- ^ White, Philip J.; Broadley, Martin R. (2003). "Calcium in plants". Annals of Botany. 92 (4): 487–511. Дои:10.1093/aob/mcg164. ЧВК 4243668. PMID 12933363.
- ^ а б Donahue, Miller & Shickluna 1977, п. 136.
- ^ Jarrell, Wesley M.; Beverly, Reuben B. (1981). "The dilution effect in plant nutrition studies". Достижения в агрономии. 34: 197–224. Дои:10.1016/S0065-2113(08)60887-1. ISBN 9780120007349.
- ^ Jordan & Reisenauer 1957, п. 107.
- ^ Holmes & Brown 1957 С. 111.
- ^ Sherman 1957, п. 135.
- ^ Seatz & Jurinak 1957, п. 115.
- ^ Reuther 1957, п. 128.
- ^ Russel 1957, п. 121.
- ^ Stout & Johnson 1957, п. 146.
- ^ Stout & Johnson 1957, п. 141.
- ^ Welsh, Ross M. (1995). "Micronutrient nutrition of plants" (PDF ). Критические обзоры в науках о растениях. 14 (1): 49–82. Дои:10.1080/713608066. Получено 9 февраля 2020.
- ^ Summer, Malcolm E.; Farina, Mart P. W. (1986). "Phosphorus interactions with other nutrients and lime in field cropping systems" (PDF ). In Stewart, Bobby A. (ed.). Advances in soil science. 5. Нью-Йорк, Нью-Йорк: Springer. pp. 201–36. Дои:10.1007/978-1-4613-8660-5_5. ISBN 978-1-4613-8660-5. Получено 9 февраля 2020.
- ^ Lešková, Alexandra; Giehl, Ricardo F.H.; Hartmann, Anja; Fargašová, Agáta & von Wirén, Nicolaus (2017). "Heavy metals induce iron deficiency responses at different hierarchic and regulatory levels". Физиология растений. 174 (3): 1648–68. Дои:10.1104/pp.16.01916. ЧВК 5490887. PMID 28500270.
- ^ M’Sehli, Wissal; Youssfi, Sabah; Donnini, Silvia; Dell’Orto, Marta; De Nisi, Patricia; Zocchi, Graziano; Abdelly, Chedly & Gharsalli, Mohamed (2008). "Root exudation and rhizosphere acidification by two lines of Medicago ciliaris in response to lime-induced iron deficiency" (PDF ). Растение и почва. 312 (151): 151–62. Дои:10.1007/s11104-008-9638-9. S2CID 12585193. Получено 9 февраля 2020.
- ^ Donahue, Miller & Shickluna 1977 С. 136–37.
- ^ Stout & Johnson 1957, п. 107.
- ^ Pereira, B.F. Faria; He, Zhenli; Stoffella, Peter J.; Montes, Celia R.; Melfi, Adolpho J. & Baligar, Virupax C. (2012). "Nutrients and nonessential elements in soil after 11 Years of wastewater irrigation" (PDF ). Журнал качества окружающей среды. 41 (3): 920–27. Дои:10.2134/jeq2011.0047. PMID 22565273. Получено 16 февраля 2020.
- ^ Richmond, Kathryn E. & Sussman, Michael (2003). "Got silicon? The non-essential beneficial plant nutrient" (PDF). Текущее мнение в области биологии растений. 6 (3): 268–72. Дои:10.1016/S1369-5266(03)00041-4. PMID 12753977. Получено 16 февраля 2020.
Библиография
- Donahue, Roy Luther; Miller, Raymond W.; Shickluna, John C. (1977). Soils: An Introduction to Soils and Plant Growth. Прентис-Холл. ISBN 978-0-13-821918-5.
- "Arizona Master Gardener". Cooperative Extension, College of Agriculture, University of Arizona. Получено 27 мая 2013.
- Stefferud, Alfred, ed. (1957). Soil: The Yearbook of Agriculture 1957. Министерство сельского хозяйства США. OCLC 704186906.
- Келлогг. "We Seek; We Learn ". В Stefferud (1957).
- Simonson. "What Soils Are ". В Stefferud (1957).
- Russell. "Физические свойства ". В Stefferud (1957).
- Richards & Richards. "Soil Moisture ". В Stefferud (1957).
- Wadleigh. "Growth of Plants ". В Stefferud (1957).
- Allaway. "pH, Soil Acidity, and Plant Growth ". В Stefferud (1957).
- Coleman & Mehlich. "The Chemistry of Soil pH ". В Stefferud (1957).
- Dean. "Plant Nutrition and Soil Fertility ". В Stefferud (1957).
- Allison. "Nitrogen and Soil Fertility ". В Stefferud (1957).
- Olsen & Fried. "Soil Phosphorus and Fertility ". В Stefferud (1957).
- Reitemeier. "Soil Potassium and Fertility ". В Stefferud (1957).
- Jordan & Reisenauer. "Sulfur and Soil Fertility ". В Stefferud (1957).
- Holmes & Brown. "Iron and Soil Fertility ". В Stefferud (1957).
- Seatz & Jurinak. "Zinc and Soil Fertility ". В Stefferud (1957).
- Рассел. "Boron and Soil Fertility ". В Stefferud (1957).
- Reuther. "Copper and Soil Fertility ". В Stefferud (1957).
- Шерман. "Manganese and Soil Fertility ". В Stefferud (1957).
- Stout & Johnson. "Микроэлементы ". В Stefferud (1957).
- Бродбент. "Organic Matter ". В Stefferud (1957).
- Кларк. "Living Organisms in the Soil ". В Stefferud (1957).
- Флемминг. "Soil Management and Insect Control ". В Stefferud (1957).
