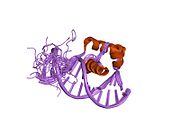
TERF2 - TERF2
Фактор связывания теломерного повтора 2 это белок что присутствует в теломеры на протяжении клеточный цикл. Он также известен как TERF2, TRF2 и TRBF2 и у человека кодируется TERF2 ген.[5] Это компонент укрытие нуклеопротеидный комплекс и второй негативный регулятор длины теломер, играющий ключевую роль в защитной активности теломер. Впервые об этом сообщили в 1997 году в лаборатории Тития де Ланге,[6] где Последовательность ДНК похож, но не идентичен TERF1 был обнаружен в отношении Myb-домен. Де Ланж выделил новую последовательность белка, содержащую Myb, и назвал ее TERF2.
Структура и домены
TERF2 имеет структуру, аналогичную структуре TERF1. Оба белка несут C-конец Myb мотив и большие, связанные с TERF1 димеризация доменов рядом с их N-конец.[6] Однако оба белка существуют исключительно в виде гомодимеры и не гетеродимеризуются друг с другом, что доказано анализ коиммунопреципитации.[6] Также в TERF2 есть базовый N-конец, отличный от TERF1 кислый N-конец, и оказалось, что он намного больше консервированный, предполагая, что два белка имеют разные функции.[7]
Есть 4 домен категории белка TERF2, которые позволяют ему связываться с обоими другими белками в укрытие белковый комплекс и определенные типы ДНК.
Область гомологии TERF
Область гомологии TERF (TRFH; ИнтерПро: IPR013867 ) представляет собой область, которая способствует гомодимеризации TERF2 с самим собой. Это приводит к образованию четвертичная структура что характерно для этого белка. Этот домен TRFH также позволяет TERF2 связываться со многими другими типами белков и действовать как док-станция для них. Аполлон нуклеаза, вспомогательный фактор shelterin, использует домен TRFH в качестве док-станции. Вербовка Аполлона TERF2 позволяет теломерные концы, образованные Синтез ДНК для обработки. Поступая так, концы теломер могут избежать Активация киназы ATM через создание терминальной структуры.[8] SLX4, что важно в Ремонт ДНК действуя как строительные леса для структур-специфичных нуклеаз репарации ДНК также связывается с доменом TRFH TERF2.[9] Домен TRFH отвечает за другие события связывания, включая RTEL1 и белки, которые содержат сайт TBD.
Myb Домен
В Myb домен (ИнтерПро: IPR017930 ) действует путем привязки к двухцепочечный теломерная ДНК. Этот регион получил свое название от вирусный белок называется Myb, производным от вирус птичьего миелобластоза. В частности, последовательность, на которую нацелен этот домен Myb на ДНК, является (GGTTAG / CCAATC) n.
Базовый и шарнирный домены
Два других домена также работают, чтобы связывать и влиять на активность белков, связанных с белком TERF2. Оба уникальны для TERF2. Базовый домен находится на N-конце и выполняет две основные функции: предотвращение иссечения t-петли посредством XRCC3, и ингибирование SLX4. Последний домен TERF2 называется шарнирным доменом (ИнтерПро: IPR031902 ). Этот домен содержит мотив связывания белка шелтерина. TIN2, который действует как стабилизирующий белок, соединяющий единицы, которые прикреплены к двухцепочечной и одноцепочечной ДНК.[10] Этот домен также отвечает за привязку к RAP1, и помогает ингибировать рекрутирование RNF168 на теломерах.
Функция
Этот белок присутствует на теломерах в метафаза из клеточный цикл, является вторым негативным регулятором длины теломер и играет ключевую роль в защитной активности теломер. Обладая сходной активностью связывания теломер и организацией домена, TERF2 отличается от TERF1 тем, что его N-конец является основным, а не кислотным.[7]
Образование Т-образной петли

Концы теломеров структурно похожи на двухцепочечные разрывы на хромосома. Чтобы предотвратить оборудование для восстановления клеточной ДНК из-за ошибочной идентификации теломер как разрывов хромосом образуются t-петли, в которых выступ 3 ’TTAGGG петель теломер возвращается обратно в дуплекс ДНК. TERF2 способствует образованию t-петли, предпочтительно связываясь с теломерным двухцепочечным дуплексом ДНК, содержащим одноцепочечный выступ 3 ’TTAGGG. Если выступ 3 ’TTAGGG отсутствует, TERF2 не связывается. После связывания он мигрирует в соединение t-петли, где одноцепочечный выступ вторгается в двухцепочечную область. вверх по течению. Никакой другой белок шелтерин не способствует этому процессу, но показано, что взаимодействие TERF2 с TERF2IP способствует более высокому образованию t-петли. in vitro.[12] Исследования показали, что делеция TERF2 предотвращает образование t-петли, что приводит к чрезмерной потере теломерной ДНК и раннему смерть клетки.[13]
Профилактика киназ в банкоматах
TERF2 играет центральную роль в предотвращении киназы ATM Ответ на повреждение ДНК. Он связывает теломерные дцДНК и предотвращает активацию теломерами киназы ATM. Это взаимодействие TERF2 с ATM считается релевантным для механизма, с помощью которого TERF2 блокирует передачу сигналов ATM. Из-за его олигомерный природа, TERF2 потенциально может перекрестная ссылка Мономеры ATM и удерживают киназу в неактивном димерном состоянии, тем самым блокируя усиление сигнала банкомата на раннем этапе его активации. Однако, поскольку мутации в домене димеризации TERF2 дестабилизируют белок, невозможно напрямую проверить вклад олигомеризации TERF2 на репрессию ATM. Удаление TERF2 вызывает ATM-зависимую апоптоз путем локализации активных, фосфорилированный форма АТМ к незащищенным концам хромосом. Поскольку TERF2 специфически связывается на теломерах и остается там, когда индуцируется повреждение ДНК, маловероятно, что он будет мешать активации киназы ATM на разных участках повреждения ДНК. Следовательно, TERF2 может действовать как теломер-специфичный ингибитор киназы ATM.[14]
Эффекты нокаута TERF2
Условное удаление TERF2 в клетках мышей эффективно удаляет комплекс нуклеопротеидов шелтерина. В результате удаления этого комплекса активируются несколько путей нежелательной реакции на повреждение ДНК, включая передачу сигналов киназы ATM, передачу сигналов киназы ATR, негомологичное соединение концов (NHEJ), alt-NHEJ, C-NHEJ, 5 'резекция и гомологически направленный ремонт (HDR).[15] Эти пути восстановления (при наличии P53 нокаут и Cre ) часто вносят свой вклад в фенотип где концы хромосом соединены друг с другом в очень длинную цепочку, что можно визуализировать с помощью комбинации DAPI пятно и флуоресценция in situ гибридизация (РЫБА) техника.
Взаимодействия

Известно также, что TERF2 рекрутирует определенные клиентские белки, также известные как дополнительные факторы. Эти клиентские белки часто привлекаются к TERF2 для выполнения определенной функции в определенное время, часто временно. Домен TRFH содержит остаток F120, который является сайтом связывания TERF2, где он рекрутирует клиентские белки. Эти клиентские белки также содержат TRFH-связывающий мотив, который состоит из консервативного 6-аминокислота последовательность следующей формулы: YИксLИксп, где «x» может быть любой замещенной аминокислотой.[16] Вышеупомянутая нуклеаза Apollo (один из многих белков-клиентов TERF2) также содержит формульный мотив; его специфическая последовательность мотива YLLТп.
TERF1 также демонстрирует аналогичный механизм рекрутирования клиентского белка, что и TERF2, за исключением того, что он расходится в двух концепциях: 1) TRFH TERF1 содержит остаток F142, 2) клиентские белки, специфичные для TERF1, содержат последовательность связывающего мотива TRFH FИксLИксп, где аминокислота Y (тирозин ) заменяется на F (фенилаланин ).
TERF2 также был показан взаимодействовать с:
Актуальность TERF2 для болезни
Рак
Теломераза представляет собой фермент, который создает концы теломеров для ДНК, и считается, что он играет важную роль в развитии рак. В частности, известно, что стабильность теломеров является обычным явлением в раковых клетках.[23] Наряду с теломеразой, комплекс шелтерина и, в частности, TERF2 и TERF1, также, как было отмечено, контролируют длину теломер, образованных этими теломеразами. Шелтерин защищает теломеры от неподходящей активации пути ответа на повреждение ДНК, как указано в разделе функций выше. Известно, что TERF2 как часть комплекса shelterin блокирует сигнальные пути ATM и предотвращает слияние концов хромосом. В раковых клетках TERF2 фосфорилирование к киназа, регулируемая внеклеточными сигналами (ERK1 /2 ) является контролирующим фактором в основных проонкогенных сигнальных путях (РАН / РАФ / МЭК / ЭРК ), которые влияют на стабильность теломеров.[23] Кроме того, когда TERF2 не был фосфорилирован в клетки меланомы, имел место индуцированный клеткой ответ на повреждение ДНК, остановивший рост и вызвавший реверсия опухоли.[23] Исследования показали, что в опухолевые клетки, Уровни TERF2 высокие, и этот повышенный уровень TERF2 способствует онкогенез разными способами.[24][25][26] Этот высокий уровень TERF2 снижает способность вербовать и активировать естественные клетки-киллеры в опухолевых клетках человека.[24] В одном исследовании использовался доминирующая отрицательная форма ТЕРФ2ΔBΔC, чтобы ингибировать TERF2, и обнаружили, что он может вызывать реверсию злокачественного фенотипа в клетках меланомы человека.[25] Следовательно, чрезмерное выражение ТЕРФ2ΔBΔC, вызывая блокировку TERF2, индуцировал апоптоз и уменьшал онкогенность в определенных клеточных линиях.[25] Кроме того, усиление регулирования TERF2 может быть причиной образования и поддержания коротких теломер.[26] Эти короткие теломеры увеличиваются хромосомная нестабильность, и увеличивают шансы на прогрессирование определенных видов рака в организме, например, при лейкемия.[26] В ткани слизистой оболочки желудка, экспрессия белков TERF2 была значительно выше, чем обычно, и эта сверхэкспрессия TERF2, наряду со сверхэкспрессией TERF1, TIN2, TERT, и BRCA1 транспозиция белка, может вызывать уменьшение длины теломер, что в дальнейшем способствует многоступенчатому канцерогенезу рак желудка.[27]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000132604 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000031921 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ссылка на Mouse PubMed:». Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Сакагути А.Ю., Падалеки С.С., Маттерн В., Родригес А., Лич Р.Дж., МакГилл Дж. Р., Чавес М., Джамбернарди Т.А. (май 1998 г.). «Хромосомная сублокализация транскрибируемого гена фактора 2 связывания теломерных повторов человека и сравнительное картирование у мышей». Сомат. Cell Mol. Genet. 24 (3): 157–63. Дои:10.1023 / b: scam.0000007118.47691.d7. PMID 10226653. S2CID 26610531.
- ^ а б c Broccoli D, Smogorzewska A, Chong L, de Lange T (октябрь 1997 г.). «Человеческие теломеры содержат два различных Myb-родственных белка, TRF1 и TRF2». Природа Генетика. 17 (2): 231–5. Дои:10.1038 / ng1097-231. PMID 9326950. S2CID 41204064.
- ^ а б «Ген Entrez: фактор 2 связывания теломерных повторов TERF2».
- ^ Ву П., ван Овербек М., Руни С., де Ланге Т. (август 2010 г.). «Apollo способствует поддержанию G-выступа и защищает теломеры ведущего конца». Молекулярная клетка. 39 (4): 606–17. Дои:10.1016 / j.molcel.2010.06.031. ЧВК 2929323. PMID 20619712.
- ^ Уилсон Дж. С., Техера А. М., Кастор Д., Тот Р., Бласко М. А., Роуз Дж. (Сентябрь 2013 г.). «Зависимые от локализации и независимые роли SLX4 в регуляции теломер». Отчеты по ячейкам. 4 (5): 853–60. Дои:10.1016 / j.celrep.2013.07.033. ЧВК 3969258. PMID 23994477.
- ^ Пальма В, де Ланге Т. (2008-11-04). «Как шелтерин защищает теломеры млекопитающих». Ежегодный обзор генетики. 42 (1): 301–34. Дои:10.1146 / annurev.genet.41.110306.130350. PMID 18680434.
- ^ Арно Н, Карлседер Дж. (Ноябрь 2015 г.). «Сложные взаимодействия между ответом на повреждение ДНК и теломерами млекопитающих». Структурная и молекулярная биология природы. 22 (11): 859–66. Дои:10.1038 / nsmb.3092. ЧВК 4739752. PMID 26581520.
- ^ Arat NÖ, Griffith JD (декабрь 2012 г.). «Человеческий Rap1 напрямую взаимодействует с теломерной ДНК и регулирует локализацию TRF2 на теломере». Журнал биологической химии. 287 (50): 41583–94. Дои:10.1074 / jbc.M112.415984. ЧВК 3516710. PMID 23086976.
- ^ Стансель Р.М., де Ланге Т., Гриффит Д.Д. (октябрь 2001 г.). «Сборка Т-петли in vitro включает связывание TRF2 около 3'-выступающей части теломера». Журнал EMBO. 20 (19): 5532–40. Дои:10.1093 / emboj / 20.19.5532. ЧВК 125642. PMID 11574485.
- ^ Карлседер Дж., Хок К., Мирзоева ОК, Баккенист К., Кастан М.Б., Петрини Дж. Х., де Ланге Т. (август 2004 г.). «Теломерный белок TRF2 связывает киназу ATM и может ингибировать ATM-зависимый ответ на повреждение ДНК». PLOS Биология. 2 (8): E240. Дои:10.1371 / journal.pbio.0020240. ЧВК 509302. PMID 15314656.
- ^ Sfeir A, de Lange T (май 2012 г.). «Удаление укрытия обнаруживает проблему защиты концов теломер». Наука. 336 (6081): 593–7. Bibcode:2012Sci ... 336..593S. Дои:10.1126 / наука.1218498. ЧВК 3477646. PMID 22556254.
- ^ а б Чен Й, Ян Й, ван Овербек М., Донигиан Дж. Р., Басиу П., де Ланге Т., Лей М. (февраль 2008 г.). «Общий стыковочный мотив в TRF1 и TRF2, используемый для дифференциального набора теломерных белков». Наука. 319 (5866): 1092–6. Bibcode:2008Sci ... 319.1092C. Дои:10.1126 / science.1151804. PMID 18202258. S2CID 54523266.
- ^ Song K, Jung D, Jung Y, Lee SG, Lee I (сентябрь 2000 г.). «Взаимодействие Ku70 человека с TRF2». Письма FEBS. 481 (1): 81–5. Дои:10.1016 / s0014-5793 (00) 01958-x. PMID 10984620. S2CID 22753893.
- ^ а б c d Чжу XD, Кюстер Б., Манн М., Петрини Дж. Х., де Ланге Т. (июль 2000 г.). «Регулируемая клеточным циклом ассоциация RAD50 / MRE11 / NBS1 с TRF2 и теломерами человека». Природа Генетика. 25 (3): 347–52. Дои:10.1038/77139. PMID 10888888.
- ^ а б О'Коннор М.С., Safari A, Лю Д., Цинь Дж., Сунъян З. (июль 2004 г.). «Белковый комплекс человека Rap1 и модуляция длины теломер». Журнал биологической химии. 279 (27): 28585–91. Дои:10.1074 / jbc.M312913200. PMID 15100233.
- ^ Чжан П., Касадай-Поттс Р., Прехт П., Цзян Х., Лю И, Пазин М.Дж., Мэттсон депутат (сентябрь 2011 г.). «Нетеломерный вариант сплайсинга фактора 2, связывающего теломерные повторы, сохраняет нейрональные свойства за счет секвестрации репрессорного элемента 1, подавляющего фактор транскрипции». Труды Национальной академии наук Соединенных Штатов Америки. 108 (39): 16434–9. Дои:10.1073 / pnas.1106906108. ЧВК 3182730. PMID 21903926.
- ^ Ли Б., Эстрайх С., де Ланге Т. (май 2000 г.). «Идентификация человеческого Rap1: значение для эволюции теломер». Клетка. 101 (5): 471–83. Дои:10.1016 / S0092-8674 (00) 80858-2. PMID 10850490. S2CID 7956545.
- ^ Опреско П.Л., фон Коббе С., Лайне Дж. П., Харриган Дж., Хиксон И. Д., Бор В. А. (октябрь 2002 г.). «Теломер-связывающий белок TRF2 связывает и стимулирует геликазы синдрома Вернера и Блума». Журнал биологической химии. 277 (43): 41110–9. Дои:10.1074 / jbc.M205396200. PMID 12181313.
- ^ а б c Пикко В., Кост I, Жиро-Пани MJ, Ренно Т., Жильсон Е., Паж Г. (июль 2016 г.). "ERK1 / 2 / MAPK-зависимая регуляция теломерного фактора TRF2". Oncotarget. 7 (29): 46615–46627. Дои:10.18632 / oncotarget.10316. ЧВК 5216822. PMID 27366950.
- ^ а б Бирокчо А., Черфилс-Вичини Дж., Ожеро А., Пинте С., Баувенс С., Йе Дж., Симонет Т., Хорард Б., Джамет К., Сервера Л., Мендес-Бермудес А., Понсе Д., Гратароли Р., де Роденбике К. Т., Сальвати Э, Rizzo A, Zizza P, Ricoul M, Cognet C, Kuilman T, Duret H, Lépinasse F, Marvel J, Verhoeyen E, Cosset FL, Peeper D, Smyth MJ, Londoño-Vallejo A, Sabatier L, Picco V, Pages G, Scoazec JY, Stoppacciaro A, Leonetti C, Vivier E, Gilson E (июль 2013 г.). «TRF2 ингибирует клеточно-внешний путь, посредством которого естественные клетки-киллеры уничтожают раковые клетки». Природа клеточной биологии. 15 (7): 818–28. Дои:10.1038 / ncb2774. PMID 23792691. S2CID 205287459.
- ^ а б c Бироччио А., Риццо А., Элли Р., Керинг С. Е., Бельвиль А., Бенасси Б., Леонетти С., Стивенс М. Ф., Д'Инкальчи М., Зупи Г., Гилсон Е. (август 2006 г.). «Ингибирование TRF2 запускает апоптоз и снижает онкогенность клеток меланомы человека». Европейский журнал рака. 42 (12): 1881–8. Дои:10.1016 / j.ejca.2006.03.010. PMID 16750909.
- ^ а б c Беллон М., Датта А., Браун М., Пуликен Дж. Ф., Куппи П., Казанджи М., Никот С. (ноябрь 2006 г.). «Повышенная экспрессия регулирующих длину теломер факторов TRF1, TRF2 и TIN2 у пациентов с Т-клеточным лейкозом взрослых». Международный журнал рака. 119 (9): 2090–7. Дои:10.1002 / ijc.22026. PMID 16786598. S2CID 37883075.
- ^ Ху Х, Чжан И, Цзоу М., Ян С., Лян XQ (сентябрь 2010 г.). «Экспрессия белков TRF1, TRF2, TIN2, TERT, KU70 и BRCA1 связана с укорочением теломер и может способствовать многоступенчатому канцерогенезу рака желудка». Журнал исследований рака и клинической онкологии. 136 (9): 1407–14. Дои:10.1007 / s00432-010-0795-х. PMID 20127252. S2CID 19253770.
дальнейшее чтение
- Bilaud T., Koering CE, Binet-Brasselet E, Ancelin K, Pollice A, Gasser SM, Gilson E (апрель 1996). «Телобокс, связанный с Myb мотив связывания теломерной ДНК, обнаруженный в белках дрожжей, растений и человека». Исследования нуклеиновых кислот. 24 (7): 1294–303. Дои:10.1093 / nar / 24.7.1294. ЧВК 145771. PMID 8614633.
- Било Т., Брун С., Анселин К., Керинг К.Э., Ларош Т., Гилсон Э. (октябрь 1997 г.). «Теломерная локализация TRF2, нового белка телобокса человека». Природа Генетика. 17 (2): 236–9. Дои:10.1038 / ng1097-236. PMID 9326951. S2CID 26959918.
- ван Стенсель Б., Смогожевская А., де Ланге Т. (февраль 1998 г.). «TRF2 защищает теломеры человека от слияния конца в конец». Клетка. 92 (3): 401–13. Дои:10.1016 / S0092-8674 (00) 80932-0. PMID 9476899. S2CID 15976686.
- Гриффит Дж. Д., Комо Л., Розенфилд С., Стансель Р. М., Бьянки А., Мосс Х., де Ланге Т. (май 1999 г.). «Теломеры млекопитающих заканчиваются большой дуплексной петлей». Клетка. 97 (4): 503–14. Дои:10.1016 / S0092-8674 (00) 80760-6. PMID 10338214. S2CID 721901.
- Тейхманн М., Ван З., Мартинес Э., Тьернберг А., Чжан Д., Фоллмер Ф., Чайт Б. Т., Рёдер Р. Г. (ноябрь 1999 г.). «Человеческий фактор-2, связанный с ТАТА-связывающим белком (hTRF2), стабильно связывается с hTFIIA в клетках HeLa». Труды Национальной академии наук Соединенных Штатов Америки. 96 (24): 13720–5. Bibcode:1999PNAS ... 9613720T. Дои:10.1073 / пнас.96.24.13720. ЧВК 24131. PMID 10570139.
- Smogorzewska A, van Steensel B, Bianchi A, Oelmann S, Schaefer MR, Schnapp G, de Lange T (март 2000 г.). «Контроль длины теломер человека с помощью TRF1 и TRF2». Молекулярная и клеточная биология. 20 (5): 1659–68. Дои:10.1128 / MCB.20.5.1659-1668.2000. ЧВК 85349. PMID 10669743.
- Ли Б., Эстрайх С., де Ланге Т. (май 2000 г.). «Идентификация человеческого Rap1: значение для эволюции теломер». Клетка. 101 (5): 471–83. Дои:10.1016 / S0092-8674 (00) 80858-2. PMID 10850490. S2CID 7956545.
- Чжу XD, Кюстер Б., Манн М., Петрини Дж. Х., де Ланге Т. (июль 2000 г.). «Регулируемая клеточным циклом ассоциация RAD50 / MRE11 / NBS1 с TRF2 и теломерами человека». Природа Генетика. 25 (3): 347–52. Дои:10.1038/77139. PMID 10888888.
- Song K, Jung D, Jung Y, Lee SG, Lee I (сентябрь 2000 г.). «Взаимодействие Ku70 человека с TRF2». Письма FEBS. 481 (1): 81–5. Дои:10.1016 / S0014-5793 (00) 01958-X. PMID 10984620. S2CID 22753893.
- Song K, Jung Y, Jung D, Lee I (март 2001). «Ku70 человека взаимодействует с гетерохроматиновым белком 1альфа». Журнал биологической химии. 276 (11): 8321–7. Дои:10.1074 / jbc.M008779200. PMID 11112778.
- Fairall L, Chapman L, Moss H, de Lange T, Rhodes D (август 2001 г.). «Структура домена димеризации TRFH теломерных белков человека TRF1 и TRF2». Молекулярная клетка. 8 (2): 351–61. Дои:10.1016 / S1097-2765 (01) 00321-5. PMID 11545737.
- Бейли С. М., Корнфорт М. Н., Куримаса А., Чен Д. Д., Гудвин Е. Н. (сентябрь 2001 г.). «Нитьспецифический пострепликативный процессинг теломер млекопитающих». Наука. 293 (5539): 2462–5. Bibcode:2001Научный ... 293.2462B. Дои:10.1126 / science.1062560. PMID 11577237. S2CID 26358800.
- Карлседер Дж., Смогожевская А., де Ланге Т. (март 2002 г.). «Старение вызвано изменением состояния теломер, а не потерей теломер». Наука. 295 (5564): 2446–9. Bibcode:2002Наука ... 295.2446K. Дои:10.1126 / science.1069523. PMID 11923537. S2CID 21567827.
- Миньон-Равикс С., Депетрис Д., Делобель Б., Крокетт М.Ф., Маттей М.Г. (февраль 2002 г.). «Интерстициальные теломеры человека связываются in vivo со специфическими белками TRF2 и TIN2». Европейский журнал генетики человека. 10 (2): 107–12. Дои:10.1038 / sj.ejhg.5200775. PMID 11938440.
- Анселин К., Брунори М., Баувенс С., Керинг С.Э., Брун С., Рикуль М., Поммье Дж. П., Сабатье Л., Гилсон Э. (май 2002 г.). «Целевой анализ для изучения цис-функций теломерных белков человека: доказательства ингибирования теломеразы TRF1 и активации деградации теломер TRF2». Молекулярная и клеточная биология. 22 (10): 3474–87. Дои:10.1128 / MCB.22.10.3474-3487.2002. ЧВК 133804. PMID 11971978.
- Опреско П.Л., фон Коббе С., Лайне Дж. П., Харриган Дж., Хиксон И. Д., Бор В. А. (октябрь 2002 г.). «Теломер-связывающий белок TRF2 связывает и стимулирует геликазы синдрома Вернера и Блума». Журнал биологической химии. 277 (43): 41110–9. Дои:10.1074 / jbc.M205396200. PMID 12181313.
- Chagnon P, Michaud J, Mitchell G, Mercier J, Marion JF, Drouin E, Rasquin-Weber A, Hudson TJ, Richter A (декабрь 2002 г.). «Миссенс-мутация (R565W) цирроза печени (FLJ14728) при циррозе у детей в Северной Америке». Американский журнал генетики человека. 71 (6): 1443–9. Дои:10.1086/344580. ЧВК 378590. PMID 12417987.
внешняя ссылка
- PDBe-KB предоставляет обзор всей структурной информации, доступной в PDB для человеческого фактора связывания теломерных повторов 2 (TERF2)