Открытие и разработка бета2-агонистов - Discovery and development of beta2 agonists - Wikipedia
β2агонисты адренорецепторов группа препаратов, которые избирательно действуют на β2-рецепторы в легких, вызывающие бронходилатация. β2-агонисты используются для лечения астма и ХОБЛ, заболевания, вызывающие обструкцию дыхательных путей. До их открытия неселективный бета-агонист изопреналин использовался. Целью разработки лекарств на протяжении многих лет было минимизировать побочные эффекты, добиться селективности и большей продолжительности действия. Механизм действия хорошо изучен и облегчил разработку. Структура сайта связывания и природа связывания также хорошо известны, как и структура деятельности отношения.
История
Β2-селективные агонисты были разработаны в 20 веке и представляют собой очень ценный класс лекарств. В 1901 г. Дзёкичи Такамине выделил гормон адреналин, также известный как адреналин.[1] В 1890 году адреналин впервые стали вводить больным астмой перорально. Он имел незначительный эффект или не имел никакого эффекта, потому что он метаболизируется в пищеварительном тракте и дезактивируется. В 1930 году был впервые введен адреналин. подкожно и было обнаружено, что он оказывает положительное влияние на астму.[1] При подкожном введении адреналин влияет на все тело, вызывая различные побочные эффекты и тем самым снижая ценность этого лечения. Позднее был опробован ингаляционный путь, и он дал гораздо меньше побочных эффектов, но все же имел неудобные побочные эффекты, такие как страх, беспокойство, беспокойство, головная боль, головокружение и сердцебиение.[1]
В 1940 г. изопротеренол (изопреналин ) был открыт. Это соединение имело такое же действие, как и адреналин, но было обнаружено меньше побочных эффектов. В 1949 г. изопротеренол в основном использовался для лечения больных астмой, учитывая сублингвально или вдыхал.[1] Первый дозирующий ингалятор под давлением был представлен в 1956 году. Он был намного удобнее для пациентов, чем ранее использовавшиеся ингаляторы с выдавливаемой грушей. Напорный дозированный ингалятор техника быстро развивалась в 1970-х годах.
В 1967 году было показано, что β2-рецептор отвечает за расширение бронхов, что привело к разработке более селективных препаратов.[1] В 1961 г. орципреналин β2-агонист был найден, но он не был таким сильным, как изопротеренол. Орципреналин не имеет катехол структура, что послужило причиной более длительного времени действия. В середине 1960-х годов был открыт альбутерол или сальбутамол, а несколько лет спустя последовали трибуталин и фенотерол. Альбутерол и тербуталин вызывали меньше побочных эффектов, таких как учащение пульса, чем изопротеренол. Фармацевтическая компания Glaxo открыла сальметерол, β-препарат длительного действия.2-агонист, обладающий бронходилатационной активностью до 12 часов. Он поступил в продажу в 1990 году. Формотерол, еще один β-препарат длительного действия.2-агонист, был продан вскоре после этого. Такая длительная продолжительность действия сделала лечение тяжелой астмы и ХОБЛ более удобным для пациентов, так как его вдыхают дважды в день.[1]В 2013 году сверхдлительно действующий β2-агонист, вилантерол, был продан. Его продолжительность действия составляет 24 часа, что должно улучшить комплаентность пациентов и сделать лечение более удобным.[2]
Клиническое использование
Астма
β2-агонисты используются для лечения астма воспалительное заболевание дыхательных путей. Воспаление делает бронхи чувствительными к некоторым факторам окружающей среды, что вызывает сужение бронхов. Когда это сужение происходит, дыхательные пути сужаются, что вызывает такие симптомы, как хрипы, стеснение в груди, одышка и кашель. Мышцы в дыхательных путях сжимаются, и клетки в дыхательных путях начинают производить больше слизи, чем обычно, что еще больше сужает дыхательные пути. Симптомы часто начинаются в детстве, но могут появиться в любом возрасте.[3]
Хроническая обструктивная болезнь легких
Как короткого, так и длительного действия β2-агонисты используются для лечения хроническая обструктивная болезнь легких. ХОБЛ вызывает ограничение воздушного потока в легких из-за воспаления. Курение является основным фактором риска, но вдыхание токсичных и вредных частиц и газов также может вызвать заболевание. Симптомами являются аномальное выделение слизи, вздутие легких, вызывающее ограничение воздушного потока, аномальный газообмен и легочная гипертензия. ХОБЛ чаще всего встречается у людей старше пятидесяти лет, давно курящих. Сначала симптомы легкие, но со временем ухудшаются.[4]
Использовать
Есть два типа β2-агонисты, длительного и короткого действия. Их как вдыхают, так и вводят с помощью устройств для доставки аэрозолей.[5][6]Длительный β2-агонистов часто дают в сочетании с кортикостероиды для лечения астмы. Короткого действия β2-агонисты используются для лечения астмы, вызванной физической нагрузкой,[7] и для пациентов, страдающих астмой, для быстрого облегчения симптомов. Их принимают за 10–15 минут до тренировки. Бронходилатация начинается через несколько минут после вдыхания β-β короткого действия.2-агонистов и длится от 4 до 8 часов.[8][9]Длительный β2- героям не рекомендуется лечить острые астма, вызванная физической нагрузкой потому что их хроническое употребление может маскировать плохо контролируемую астму.[10]
Механизм действия
Фармакокинетический
Кинетика релаксации гладкой мускулатуры дыхательных путей с учетом начала и продолжительности бронходилатация у больных астмой, отражаются в различии механизма взаимодействия короткая- (SABA) и долго действующий β2-агонисты (LABA) и β2-рецептор.[11]Существует множество составов селективного β2-агонисты; Ингаляция - это предпочтительный путь, потому что он наиболее быстро эффективен и связан с минимальными побочными эффектами.[12]Сульфатные конъюгаты основные метаболиты; связывание с белками довольно слабое и незначительное взаимодействия были обнаружены с другими препаратами.[13]Основные ферменты, регулирующие метаболизм катехоламинов: COMT и МАО. Коммерческие SABA, сальбутамол и тербуталин устойчивы к COMT, но медленно метаболизируются MAO, в то время как LABA устойчивы как к COMT, так и к MAO. Кроме того, большая продолжительность действия салметерола связана с повышенной липофильностью молекул, что позволяет ему дольше оставаться в легких.[14] β2- герои в основном устранен через почечный процесс после парентерального введения, в то время как после перорального приема более выраженный метаболический клиренс (высокий эффект первого прохождения) отвечает за низкую биодоступность. Выведение после ингаляции не изучалось, но профиль, вероятно, находится где-то между тем, что мы наблюдаем после парентерального и перорального введения.[13]
Связывание с β-адренорецепторами
β-рецепторы представляют собой мембранные рецепторы, связанные с G-белки. Три типа β-рецепторы были идентифицированы молекулярной фармакологией. β1 рецепторы составляют до 75% всех бета-рецепторов и преимущественно расположены в сердце. β2 рецепторы находятся в гладких мышцах сосудов и бронхов. β3 рецепторы, которые, как предполагается, участвуют в метаболизме жирных кислот, расположены в адипоциты.[15]

Рецепторы, сопряженные с G-белком, состоят из одиночных полипептид цепи из 300-600 аминокислот и семь раз покрывают плазматическую мембрану.[16] Существует три внеклеточных петли, одна из которых амино-конец, и три внутриклеточные петли с карбокси-конец.[11] Гидрофильный карман образован внутри мембраны семью альфа-спиралями. трансмембранные домены. В лиганд связывается с гидрофильным карманом в рецепторном белке и активирует рецептор, вызывая клеточный эффект.[16]
Когда β2-агонист связывает и активирует β2-адренорецепторная внутриклеточная передача сигналов в значительной степени зависит от циклического аденозинмонофосфата (лагерь ) и протеинкиназа А (PKA ). Связь β2-рецептор к аденилатциклаза на него воздействует тримерный белок Gs, как показано на рисунке 2, состоящий из α-субъединица (который стимулирует аденилатциклазу) и βγ-субъединицы (которые передают другие сигналы). Аденилатциклаза катализирует превращение аденозинтрифосфат в цАМФ, который является второй посланник, тем самым увеличивая внутриклеточные уровни цАМФ, что приводит к расслаблению гладких мышц. Уровни цАМФ регулируются за счет активности фосфодиэстераза изоферменты / изоформы, которые разлагают его до 5'-АМП.[11][16]Механизм, с помощью которого цАМФ вызывает расслабление гладкомышечных клеток дыхательных путей, полностью не изучен. Считается, что цАМФ катализирует активацию PKA, которая, в свою очередь, фосфорилирует ключевые регуляторные белки, участвующие в контроле мышечного тонуса. цАМФ также играет роль в ингибировании ион кальция (Ca2+) высвобождение из внутриклеточных хранилищ, секвестрация внутриклеточного Ca2+, и восстановление мембранного Ca2+ вход, приводящий к расслаблению гладких мышц дыхательных путей.[11]

Связывание норэфинефрина с сайтом связывания состоит из одного ионная связь, три водородные связи и ван дер Ваальс взаимодействие в двух местах. Ионная связь образуется между протонированным амином и Asp-113 в спирали 3. Водородные связи образуются из гидроксильных групп, связанных с катехольным кольцом, с Ser-204 и Ser-207 в спирали 5. Это связывание ограничивает конфигурацию и свободу вращения. Силы Ван-дер-Ваальса между ароматическим катехиновым кольцом и Phe-290 в остатке спирали 6 и Val-114 в остатке спирали 3 усиливают связывание. Считается, что N-алкильные заместители помещаются в гидрофобный карман, образованный между остатками спирали 6 и 7. Бета-углерод хиральный и должен иметь R-конфигурацию, чтобы бета-гидроксильная группа была ориентирована в сторону остатка Asn-293 в спирали 6 для образования водородной связи, необходимой для связывания с рецептором бета-2.[14]
Механизм длительного действия β2- герои
Две теории объясняют длительное время действия LABA. Первый объяснил длительные действия с точки зрения предполагаемого «экзозит »Или« экзоцептор », отличный от β2-адренорецептор, с которым длинный алифатический хвост салметерола связывается с высоким сродством. Это позволяет активной салигениновой головке поворачиваться и отклоняться от рецептора, чтобы активировать его многократно.[17] Формотерол не имеет длинной боковой цепи, как у салметерола, для связывания с «экзосайтом», поэтому эта теория подвергается сомнению. В 1994 году Андерсон. и другие. представил теорию микрокинетической диффузии плазмалеммы, объясняя, что происходит с β2- агонист в липидном бислое клеточной мембраны и в водной биофазе, ближайшей к сайту связывания β2-адренорецептор. Постулируется, что плазмалемма липидный бислой гладких мышц дыхательных путей действует как депо для β2-агонисты адренорецепторов. β2агонисты -адренорецепторы остаются доступными для взаимодействия с β2-адренорецепторный активный центр после разделения на липидный бислой.[17]
Взаимосвязи структуры деятельности (SAR)
Базовый состав агонистов
Фундаментальный фармакофор для всех адренергических агонистов является замещенным фенэтиламин что увеличивает продолжительность действия.[14]
Активность β2агонисты адренорецепторов
Адренергические агонисты, селективные в отношении β2 подтип вызывает расширение бронхов и может облегчить бронхоспазм при приступе астмы. Неселективные β-агонисты обладают стимулирующим действием на сердце и поэтому имеют ограниченное применение у кардиологических пациентов с астмой.[14]
Введение более высоких доз β-β короткого действия2-агонистов увеличивает продолжительность действия, но также увеличивает побочные эффекты такие как сердечные эффекты. Один из подходов к предотвращению этих побочных эффектов - использование структурно различных функций, которые могут минимизировать поглощение в Систематическая циркуляция. Например, можно использовать лекарства, которые при попадании в системный кровоток превращаются в неактивные метаболиты.[18]
Заместители на фармакофор влияет, будет ли аналог иметь прямое или непрямое действие или их смесь. Это также влияет на специфичность подтипов β-рецепторов. Аналог прямого действия связывает β-адренорецепторы напрямую и генерирует сочувствующий ответ. Аналог непрямого действия вызывает агонистический эффект, но без прямого связывания с β-адренорецептором, например, за счет стимуляции высвобождения норэпинефрин (NE) от пресинаптического терминала или путем ингибирования обратный захват выпущенных NE.[14]
Базовая структура для каждого β2- герои

На рис.4 показаны фенильные кольца, которые используются для β2- герои. Их называют резорциновым кольцом, салициловым спиртом или м-формамидной группой.[14] На рис. 5 показано, где разные заместители в фенилэтиламине занимают места, отмеченные разными R-группами.
Активность перечисленных R-групп
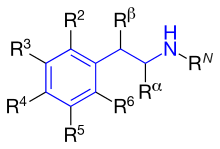
Разница между заместителями R1-R5 описана ниже. Все продаваемые β2- у героев есть гидроксильная группа в позиции R3 и чаще всего в позиции R5.[14]
рN: Эта группа определяет селективность α- или β-рецепторов. Чем больше заместитель, тем выше селективность в отношении β-рецептора. Если трет-бутил расположен в RN он показывает высокое сродство к β2-рецептор. Длинный фенилбутоксигексильный заместитель в этом положении дает высокий β2-селективность, а также высокая липофильность и, следовательно, более длительная продолжительность действия.[14]
рα: Заместители, отличные от водорода, увеличивают продолжительность действия. An этил группа увеличила бы селективность для β2-рецептор. Однако этильная группа, по-видимому, вызывает усиление побочных эффектов и низкий уровень β.2-рецепторная активность по сравнению с другими β2-селективные агонисты.[14]
рβ: Гидроксильная группа оказывает прямое действие на β-рецептор. Как отмечалось ранее, все продаваемые β2-агонисты имеют гидроксильную группу в этом положении, что делает соединение хиральный, и активен, если он имеет (R) -конфигурацию.[14]
р5 или R3: Гидроксильная группа размещена на углеродном номере 5 или 3 (мета-позиция ) оказывает прямое действие на β-адренорецепторы.[14]
р4: Либо гидроксильная группа, либо водородная группа в этом положении оказывает прямое действие на β-рецептор.[14]
Обобщая несколько β2Агонисты -адренорецепторы и их структурная активность показывает, как они действуют по-разному в отношении эффективности, селективности, аффинности и продолжительности действия (см. Таблица 1):
| Химическая структура | Имя | Описание |
|---|---|---|
 | Адреналин (адреналин) | Комбинация ядра катехина, β-гидроксильной группы и N-метильной группы. Эти качества обеспечивают прямое действие и сильное сродство ко всем адренергическим рецепторам.[14] |
 | Тербуталин | Комбинация N-трет-бутила и фенильного кольца резорцина, придающая активность β2-рецептору.[14] |
 | Альбутерол (сальбутамол) | Имеет фенильное кольцо N-трет-бутила и салицилового спирта, что придает ему оптимальную β2-селективность.[14] Сальбутамол является β2-агонистом короткого действия, но имеет быстрое начало действия.[18] Начало его при вдыхании - в течение 5 минут. Гидроксильная группа на β-углероде представляет собой смесь S- и R-изомеров, где R-изомер является активным. Другой препарат, Левальбутерол, имеет точно такую же структуру. он содержит только R-изомер альбутарола и, следовательно, гораздо более активен, и доза для левалбутерола будет в четыре раза меньше, чем для альбутарола.[14] |
 | Сальметерол | Имеет N-фенилбутоксигексильный заместитель, β-гидроксильную группу и салицилфенильное кольцо, которое дает эффективность и прямую селективность в отношении β2-рецептора.[14] Оптимальное положение эфирного кислорода в цепи салметерола как по активности, так и по продолжительности составляет шесть атомов углерода от основного азота.[18] |
 | Формотерол | Имеет N-изопропил-п-метоксифенильную группу, которая оказывает прямое действие на β-рецепторы. Форметерол также имеет м-формамидное и п-гидроксифенильное кольцо, которое придает селективность β2-рецепторам. Начало действия форметерола составляет около 20 минут, а продолжительность действия - 12 часов. Если сравнивать форметерол с салметеролом, то он обладает большей растворимостью в воде, что позволяет ему быстрее добраться до рецепторов, а липофильность дольше удерживает его в легких. Форметерол имеет два асимметричных центра. Сообщается, что R, R-энантиомер в 1000 раз более активен, чем S, S-энантиомер.[14] |
 | Вилантерол | Последний препарат на рынке. Он имеет структуру, аналогичную салметеролу, но также имеет 2,6-дихлорбензил и два алкокси группы на N-цепи. Он продемонстрировал селективность, аналогичную сальметеролу, в отношении β2-рецептора, но более высокую селективность по сравнению со всеми другими протестированными агонистами. Было показано, что собственная активность выше, чем у салметерола.[19] Вилантерол очень эффективен и обладает высокой эффективностью. Обладает быстрым началом действия и длительным действием. Включение дополнительной алкоксигруппы в боковую цепь дает мощный β2-агонист, который быстро метаболизируется в печени человека. 2,6-дихлорбензил, кажется, дает большую эффективность, селективность, быстрое начало действия, большую продолжительность действия и быструю смену.[18] |
Синтез β2агонисты адренорецепторов
Β2-агонистами, которые используются в клинической практике, являются все замещенные β-фенэтиламин (см. рис. 5), и они имеют три типа фенильных колец, показанных на рис. 4. Они называются кольцом резорцина, кольцом салицилового спирта или кольцом N-формамида. Спиртовые заместители в фенильном кольце реакционноспособны и усложняют синтез β2- герои. При добавлении N-остатка в положение R1 требуется ступень защиты (рисунок 5). Еще одна вещь, усложняющая синтез, - это получение оптически чистого R (-) энантиомера соединения. Стереохимия очень важна для активности, поскольку только R (-) энантиомер способен образовывать водородные связи, необходимые для того, чтобы соответствовать сайту связывания и активировать β2-рецептор.[14]
Сальбутамол обычно вдыхают в виде рацемических смесей (например, вентолина). Путем лечения астмы оптически чистым (R) -сальбутамолом можно минимизировать риск побочных эффектов, таких как эффекты стимуляции нервной системы и сердечная аритмия.[20] Вот почему описано несколько способов получения оптически чистого сальбутамола, но они недостаточно эффективны для использования в фармацевтической промышленности. Наиболее эффективный способ получения чистого (R) -сальбутамола - это получение рацемической смеси с последующим разделением изомеров.[21]
Стереоселективный синтез трибуталина и сальбутамола ацеталя может быть осуществлен из O-защищенных- (R) -циангидринов. F. Effenberg и др. описать способ синтеза. Основные сложности заключаются в том, чтобы выполнить этап снятия защиты без рацемизация и образовать чистую соль. А Реакция Риттера может быть использован для N-третичного бутилирования. В этом эксперименте деацетилирование (R) -сальбутамола ацеталя было безуспешным, поэтому его нельзя использовать для получения чистого (R) -сальбутамола. На рис. 6 показаны основные этапы синтеза салметерола и трибуталина.[22]
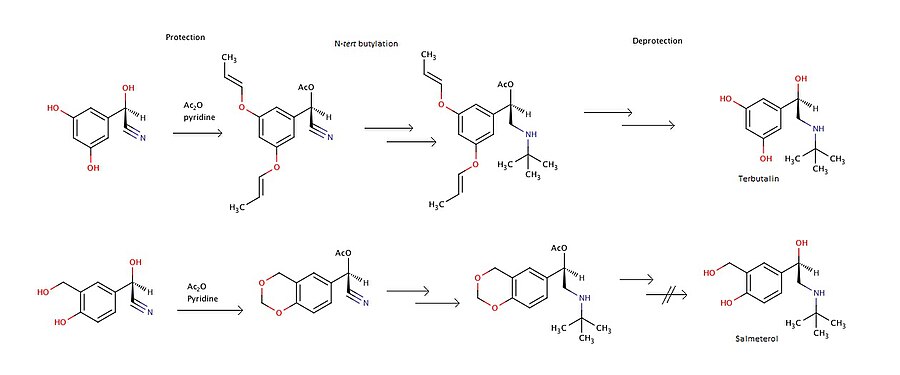
Β2-агонист салметерол может быть синтезирован из фенэтиловый спирт. Дибромгексан используется для связывания фенэтилового спирта с этиламином салицилового спирта. На рисунке 7 показаны основные этапы синтеза.[23]

Смотрите также
- Бета2-адренергический агонист
- Альфа-адренергический агонист
- Астма
- Бета-блокатор
- Бета-1 адренергический рецептор
- Бета-2-адренорецептор
- Бета-3-адренорецептор
- ХОБЛ
- Ингаляционная терапия
- GPCR
- Катехоламин
Рекомендации
- ^ а б c d е ж Таттерсфилд, A.E. (2006). «Текущие проблемы с агонистами бета2-адренорецепторов: историческая справка». Am J Med. 68 (4): 471–472. Дои:10.1385 / CRIAI: 31: 2: 107. PMID 17085787.
- ^ Донохью, Дж. Ф .; Niewoehner, D .; Brooks, J .; О'Делл, Д .; Чёрч, А. (2014). «Безопасность и переносимость умеклидиния / вилантерола 125/25 мкг и умеклидиния 125 мкг один раз в день у пациентов с хронической обструктивной болезнью легких: результаты 52-недельного рандомизированного двойного слепого плацебо-контролируемого исследования». Respir Res. 15: 78. Дои:10.1186/1465-9921-15-78. ЧВК 4113670. PMID 25015176.
- ^ "Что такое астма?". nhlbi.nih.gov. Получено 22 октября 2014.
- ^ Celli, B.R .; Макни, В. (2006). «Стандарты диагностики и лечения пациентов с ХОБЛ: краткое изложение позиции ATS / ERS». Европейский респираторный журнал. 27 (1): 242. Дои:10.1183/09031936.06.00129305.
- ^ Барнер, П.Дж. (2002). «Научное обоснование ингаляционной комбинированной терапии с бета2-агонистами длительного действия и кортикостероидами». Eur Respir J. 19 (1): 182–191. Дои:10.1183/09031936.02.00283202.
- ^ Гомер, Си-Джей (1997). «Лечение астмы». N Engl J Med. 337 (20): 1461–1463. Дои:10.1056 / nejm199711133372010. PMID 9358146.
- ^ Lazarinis, N; Йоргенсен, L; Экстром, Т; Bjermer, L; Dahlen, B; Пуллерит, Т; Ларссон, К. (2014). ". Комбинация будесонида / формотерола по требованию улучшает контроль астмы за счет уменьшения вызванного физической нагрузкой бронхоспазма". Грудная клетка. 69 (2): 130–136. Дои:10.1136 / thoraxjnl-2013-203557. ЧВК 3913208. PMID 24092567.
- ^ Макфадден, Э. Р. младший (1980). «Астма, вызванная физической нагрузкой». Am J Med. 68 (4): 471–472. Дои:10.1016 / 0002-9343 (80) 90282-х.
- ^ Буле, Л.П (1994). «Β2-агонисты длительного действия и короткого действия». Наркотики. 47 (2): 207–222. Дои:10.2165/00003495-199447020-00001. PMID 7512898.
- ^ «Краткий справочник по лечению астмы, диагностика и лечение астмы» (PDF). nhlbi.nih.gov. Национальный институт сердца, легких и крови. п. 4. Получено 24 октября 2014.
- ^ а б c d Джонсон, М. (2006). «Молекулярные механизмы функции, ответа и регуляции бета (2) -адренергических рецепторов». J Allergy Clin Immunol. 117 (1): 18–24. Дои:10.1016 / j.jaci.2005.11.012. PMID 16387578.
- ^ Армстронг, Д. Дж .; Моттрам, Д. Р. (2010). «Бета-2 агонисты». Наркотики в спорте. 98.
- ^ а б Hochhaus, G; Моллманн, H (1992). «Фармакокинетические фармакодинамические характеристики бета-2-агонистов тербуталина, сальбутамола и фенотерола». Международный журнал клинической фармакологии и терапии. 30 (9): 342–362.
- ^ а б c d е ж грамм час я j k л м п о п q р s Lemke, T.L .; Уильямс, D.A .; Roche, V.F .; Зито, С. (2013). Принципы медицинской химии Фуа. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс. С. 1314–1320.
- ^ Ladage, R.HG; Schwinger, D; Бриксиус, К. (2013). «Кардио-селективный бета-блокатор: фармакологические доказательства и их влияние на способность к физической нагрузке». Сердечно-сосудистая терапия. 31 (2): 76–83. Дои:10.1111 / J.1755-5922.2011.00306.X. PMID 22279967.
- ^ а б c Кинг, Ф. Д. (2002). Принципы и практика медицинской химии (2-е изд.). Кембридж, Великобритания: Королевское химическое общество. С. 1ö24.
- ^ а б Андерсон, Г. П .; Linden, A .; Рабе, К. Ф. (1994). «Почему агонисты бета-адренорецепторов длительного действия обладают длительным действием?». Eur Respir J. 7 (3): 569–578. Дои:10.1183/09031936.94.07030569. PMID 7912202.
- ^ а б c d Procopiou, Panayiotis A .; Барретт, Виктория Дж .; Беван, Никола Дж .; Биггэдайк, Кейт; Box, Philip C .; Мясники, Питер Р .; Коу, Дайан М .; Конрой, Ричард; Эммонс, Аманда; Форд, Элисон Дж .; Холмс, Дункан С .; Хорсли, Хелен; Керр, Ферн; Ли-Квай-Чунг, Анн-Мари; Looker, Брайан Э .; Mann, Inderjit S .; Маклей, Иэн М .; Моррисон, Валери С .; Матч, Питер Дж .; Смит, Клэр Э .; Томлин, Паула (2010). «Синтез и взаимосвязь структура-активность агонистов β-адренергических рецепторов длительного действия, включая метаболическую инактивацию: подход к лечению». Журнал медицинской химии. 53 (11): 4522–4530. Дои:10.1021 / jm100326d. PMID 20462258.
- ^ Slack, R.J .; Barret, V.J .; Моррисон, В.С.; Sturton, R.G .; Emmons, A.J .; Ford, A.J .; Ноулз, Р. (2013). «Фармакологическая характеристика in vitro вилантерола, нового агониста β2-адренорецепторов длительного действия с 24-часовой продолжительностью действия». Журнал фармакологии и экспериментальной терапии. 344 (1): 218–230. Дои:10.1124 / jpet.112.198481. PMID 23131596.
- ^ Барберих, Т. «Способ лечения астмы с использованием оптически чистого (R) -альбутерола». Патенты Google. Получено 27 октября 2014.
- ^ Hettich, Джером. «Химия, биохимия и применение сальбутамола». Имперский колледж - Химический факультет. Получено 27 октября 2014.
- ^ Эффенбергер, Франц; Jäger, Юрген (1997). «Синтез адренергических бронходилататоров (R) -тербуталин и (R) -сальбутамол из (R) -циангидринов». J. Org. Chem. 62 (12): 3867–3873. Дои:10.1021 / jo970032d.
- ^ Скидмор, И. Ф .; Lunts, L.H.C .; Finch, H .; Naylor, A .; German Offen., 1984, 3414752; Chem. Абстракция, 1986, 102, 95383.

