Олигосахарилтрансфераза - Oligosaccharyltransferase
| STT3 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
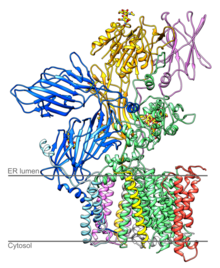 Состав дрожжевого ОСТ [1] | |||||||||
| Идентификаторы | |||||||||
| Символ | STT3 | ||||||||
| Pfam | PF02516 | ||||||||
| Pfam клан | CL0111 | ||||||||
| ИнтерПро | IPR003674 | ||||||||
| OPM суперсемейство | 242 | ||||||||
| Белок OPM | 3rce | ||||||||
| CAZy | GT66 | ||||||||
| Мембранома | 275 | ||||||||
| |||||||||
Олигосахарилтрансфераза или же OST (EC 2.4.1.119 ) это мембранный белок сложный который передает 14-сахар олигосахарид из долихол к зарождению белок. Это тип гликозилтрансфераза. Сахар Glc3мужчина9GlcNAc2 (где Glc =Глюкоза, Мужчина =Манноза, а GlcNAc =N-ацетилглюкозамин ) прикреплен к аспарагин (Asn) остаток в последовательности Asn-X-Сер или Asn-X-Thr где X - любая аминокислота, кроме пролин. Эта последовательность называется гликозилированием. секвон. Реакция, катализируемая OST, является центральным этапом в N-связанное гликозилирование путь.
Место расположения

OST является составной частью Translocon в эндоплазматический ретикулум (ER) мембрана. Связанный с липидом сердцевинный олигосахарид собирается на мембране эндоплазматического ретикулума и переносится на выбранный аспарагин остатки зарождающегося полипептид цепи олигосахарилтрансферазы сложный.[3] Активный центр OST расположен примерно в 4 нм от просвета мембраны ER.[4]
Обычно действует во время перевод по мере того, как зарождающийся белок входит в ЭПР, но это котрансляционное гликозилирование, тем не менее, называется посттрансляционная модификация. Было обнаружено несколько примеров использования OST после завершения перевода.[5][6] Текущее мнение таково, что посттрансляционная активность может возникать, если белок плохо сложенный или складывается медленно.[6]
Структура и функции
OST дрожжей состоит из восьми различных мембранных белков в трех субкомплексах (один из них OST4 ).[7][8] Эти октомеры не образуют более высокого порядка. олигомеры, и три из восьми белков сами гликозилируются.[7] Известно, что ОЗТ у млекопитающих имеет аналогичный состав.[9][10]
Считается, что для OST требуется много подразделов, потому что он должен:[11]
- Расположитесь рядом с порой транслокона.
- Узнавайте и связывайте олигосахарилдолихол.
- Сканируйте зарождающийся белок, чтобы распознать и связать секвоны.
- Переместите эти две большие подложки на их правильные места и формы.
- Активируйте Asn амид азот атом для фактического переноса олигосахарида.
- Освободите его подложки.
Каталитически активная субъединица OST называется STT3. У эукариот существуют два паралога, называемые STT3A и STT3B. STT3A в первую очередь отвечает за котрансляционное гликозилирование растущего полипептида, поскольку он входит в просвет эндоплазматического ретикулума, тогда как STT3B может также опосредовать посттрансляционное гликозилирование.[12] Структура PglB, прокариотический гомолог STT3 был решен.[13] Высокое сходство последовательностей между прокариотическим и эукариотическим STT3 предполагает, что их структуры похожи.
Клиническое значение
Синдромы CDG находятся генетические нарушения пути гликозилирования. Они помечаются как «Тип I», если неисправный ген для фермент участвует в сборке или передаче Glc3мужчина9GlcNAc2-предшественник долихола. Они помечаются как «Тип II», если дефектная ступень возникает после действия ОЗТ в N-связанное гликозилирование путь или вовлекает О-связанное гликозилирование.[14]
Смотрите также
Рекомендации
- ^ Уайлд Р., Коваль Дж., Айринг Дж., Нгва Э.М., Эби М., Лочер К.П. (2018). «Структура дрожжевого олигосахарилтрансферазного комплекса дает представление о N-гликозилировании эукариот». Наука. 359 (6375): 545–550. Bibcode:2018Sci ... 359..545W. Дои:10.1126 / science.aar5140. PMID 29301962.
- ^ Пфеффер С., Дудек Дж., Гогала М., Шорр С., Линксвайлер Дж., Ланг С., Беккер Т., Бекманн Р., Циммерманн Р., Фёрстер Ф. (2014). «Структура комплекса олигосахарилтрансферазы млекопитающих в транслоконе нативного белка ER». Nat. Сообщество. 5 (5): 3072. Bibcode:2014 НатКо ... 5.3072P. Дои:10.1038 / ncomms4072. PMID 24407213.
- ^ Zufferey R, Knauer R, Burda P, Stagljar I, te Heesen S, Lehle L, Aebi M (октябрь 1995 г.). «STT3, высококонсервативный белок, необходимый для активности дрожжевой олигосахарилтрансферазы in vivo». EMBO J. 14 (20): 4949–60. Дои:10.1002 / j.1460-2075.1995.tb00178.x. ЧВК 394598. PMID 7588624.
- ^ Нильссон И.М., von Heijne G (Март 1993 г.). «Определение расстояния между активным центром олигосахарилтрансферазы и мембраной эндоплазматического ретикулума». J. Biol. Chem. 268 (8): 5798–801. PMID 8449946.
- ^ Плесс Д.Д., Леннарц В.Дж.; Леннарз (январь 1977 г.). «Ферментативное превращение белков в гликопротеины». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 74 (1): 134–8. Bibcode:1977ПНАС ... 74..134П. Дои:10.1073 / пнас.74.1.134. ЧВК 393212. PMID 264667.
- ^ а б Duvet S, Op De Beeck A, Cocquerel L, Wychowski C, Cacan R, Dubuisson J (февраль 2002 г.). «Гликозилирование белка оболочки E1 вируса гепатита С происходит посттрансляционно в мутантной линии клеток CHO с дефицитом маннозилфосфорилдолихола». Гликобиология. 12 (2): 95–101. Дои:10,1093 / гликоб / 12.2.95. PMID 11886842.
- ^ а б Knauer R, Lehle L (январь 1999 г.). «Комплекс олигосахарилтрансферазы дрожжей». Биохим. Биофиз. Acta. 1426 (2): 259–73. Дои:10.1016 / S0304-4165 (98) 00128-7. PMID 9878773.
- ^ Демпски Р. Э., Империали Б (декабрь 2002 г.). «Олигосахарилтрансфераза: привратник секреторного пути». Curr Opin Chem Biol. 6 (6): 844–50. Дои:10.1016 / S1367-5931 (02) 00390-3. PMID 12470740.
- ^ Nilsson I, Kelleher DJ, Miao Y, Shao Y, Kreibich G, Gilmore R, von Heijne G, Johnson AE (май 2003 г.). «Фотоперекрестное связывание растущих цепей с субъединицей STT3 олигосахарилтрансферазного комплекса». J. Cell Biol. 161 (4): 715–25. Дои:10.1083 / jcb.200301043. ЧВК 2199356. PMID 12756234.
- ^ Караоглу Д., Келлехер Д. Д., Гилмор Р. (октябрь 2001 г.). «Аллостерическая регуляция обеспечивает молекулярный механизм для предпочтительного использования полностью собранного олигосахарида, связанного с долихолом, олигосахарилтрансферазой дрожжей». Биохимия. 40 (40): 12193–206. Дои:10.1021 / bi0111911. PMID 11580295.
- ^ Imperiali B (ноябрь 1997 г.). «Гликозилирование белков: Битва титанов». Отчеты о химических исследованиях. 30 (11): 452–459. Дои:10.1021 / ar950226k.
- ^ Руис-Канада C, Келлехер DJ, Гилмор Р. (январь 2009 г.). «Котрансляционное и посттрансляционное N-гликозилирование полипептидов с помощью различных изоформ OST млекопитающих». Клетка. 136 (2): 272–83. Дои:10.1016 / j.cell.2008.11.047. ЧВК 2859625. PMID 19167329.
- ^ Лизак С., Гербер С., Нумао С., Эби М., Лочер К.П. (июнь 2011 г.). «Рентгеноструктура бактериальной олигосахарилтрансферазы». Природа. 474 (7351): 350–5. Дои:10.1038 / природа10151. PMID 21677752.
- ^ Марквардт Т., Денеке Дж. (Июнь 2003 г.). «Врожденные нарушения гликозилирования: обзор их молекулярных основ, клинических проявлений и специфических методов лечения». Евро. J. Pediatr. 162 (6): 359–79. Дои:10.1007 / s00431-002-1136-0. PMID 12756558.
внешняя ссылка
- олигосахарилтрансфераза в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
