Путь передачи сигналов бета TGF - TGF beta signaling pathway
В сигнальный путь трансформирующего фактора роста бета (TGFB) участвует во многих клеточных процессах как во взрослом организме, так и в развивающемся эмбрион включая рост клеток, дифференциация клеток, апоптоз, клеточный гомеостаз и другие клеточные функции. Несмотря на широкий спектр клеточных процессов, которые регулирует сигнальный путь TGFβ, этот процесс относительно прост. Суперсемейство TGFβ лиганды связываются с рецептором типа II, который привлекает и фосфорилаты рецептор типа I. Рецептор типа I затем фосфорилирует SMAD, регулируемые рецептором (R-SMAD ), который теперь может связывать coSMAD SMAD4. Комплексы R-SMAD / coSMAD накапливаются в ядре, где они действуют как факторы транскрипции и участвовать в регуляции экспрессии целевого гена.
Механизм
Связывание лиганда
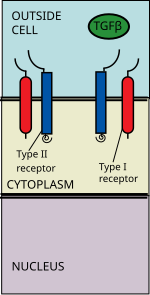
Суперсемейство лигандов TGF beta включает: Костные морфогенетические белки (BMP), Факторы роста и дифференциации (GDF), Антимюллеров гормон (АМГ), Активин, Узловой и TGFβ с.[1] Передача сигналов начинается со связывания лиганда суперсемейства TGF бета с рецептором TGF бета типа II. Рецептор типа II представляет собой киназу серин / треонинового рецептора, которая катализирует то фосфорилирование рецептора типа I. Каждый класс лигандов связывается со специфическим рецептором типа II.[2] У млекопитающих известно семь рецепторов типа I и пять рецепторов типа II.[3]
Есть три вида деятельности: Активин А, Активин B и Activin AB. Активины участвуют в эмбриогенезе и остеогенезе. Они также регулируют многие гормоны включая гипофиз, гонадные и гипоталамический гормоны, а также инсулин. Они также нервная клетка факторы выживания.
BMP привязаны к рецептор костного морфогенетического белка типа 2 (БМПР2). Они участвуют во множестве клеточных функций, включая остеогенез, дифференциация клеток, спецификация передней / задней оси, рост и гомеостаз.
Семейство бета-версий TGF включает: TGFβ1, TGFβ2, TGFβ3. Подобно BMP, бета TGF участвуют в эмбриогенезе и дифференцировке клеток, но они также участвуют в апоптозе, а также в других функциях. Они привязаны к TGF-бета-рецептор типа 2 (TGFBR2).
Узловой связывается с рецептором активина A типа IIB ACVR2B. Затем он может образовывать рецепторный комплекс с рецептором активина А типа IB (ACVR1B ) или с рецептором активина А типа IC (ACVR1C ).[3]
Когда связывание рецептор-лиганд происходит посредством местного действия, это классифицируется как паракринная передача сигналов.
Набор рецепторов и фосфорилирование

Бета-лиганд TGF связывается с димером рецептора типа II, который рекрутирует димер рецептора типа I, образуя гетеротетрамерный комплекс с лигандом.[4] Эти рецепторы рецепторы серин / треонинкиназы. У них есть цистеин богатые внеклеточный домен, а трансмембранный домен и цитоплазматический богатый серином / треонином домен. В GS домен рецептора типа I состоит из примерно тридцати серин -глицин повторяется.[5] Связывание лиганда семейства TGF бета вызывает вращение рецепторов, так что их цитоплазматические киназные домены располагаются в каталитически благоприятной ориентации. Рецептор типа II фосфорилаты серин остатки рецептора типа I, активирующего белок.
SMAD фосфорилирование

Существует пять SMAD, регулируемых рецепторами: SMAD1, SMAD2, SMAD3, SMAD5, и SMAD9 (иногда обозначается как SMAD8). По сути, существует два внутриклеточных пути, в которых участвуют R-SMAD. TGF бета, активины, узлы и некоторые GDF опосредуются SMAD2 и SMAD3, тогда как BMP, AMH и некоторые GDF опосредуются SMAD1, SMAD5 и SMAD9. Связывание R-SMAD с рецептором типа I опосредуется белком, содержащим домен FYVE с цинковым двойным пальцем. Два таких белка, которые опосредуют бета-путь TGF, включают SARA (якорь SMAD для активации рецептора) и HGS (субстрат тирозинкиназы, регулируемый фактором роста гепатоцитов).
SARA присутствует в раннем эндосома который, по клатрин-опосредованный эндоцитоз, интернализует рецепторный комплекс.[6] САРА набирает R-SMAD. SARA позволяет связывать R-SMAD с областью L45 рецептора типа I.[7] SARA ориентирует R-SMAD таким образом, чтобы остатки серина на его C-конец сталкивается с каталитической областью рецептора типа I. Рецептор I типа фосфорилаты остаток серина R-SMAD. Фосфорилирование вызывает конформационные изменения в MH2 домен R-SMAD и его последующая диссоциация от рецепторного комплекса и SARA.[8]
CoSMAD привязка

Фосфорилированный RSMAD имеет высокое сродство к coSMAD (например, SMAD4 ) и образует комплекс с единицей. Фосфатная группа не действует как стыковочный сайт для coSMAD, скорее, фосфорилирование открывает аминокислотный участок, позволяющий взаимодействие.
Транскрипция

Фосфорилированный комплекс RSMAD / coSMAD входит в ядро, где он связывает промоторы / кофакторы транскрипции и вызывает транскрипцию ДНК.
Костные морфогенетические белки вызывают транскрипцию мРНК участвует в остеогенез, нейрогенез, и вентральная мезодерма Технические характеристики.
TGF-бета вызывают транскрипцию мРНК, участвующих в апоптоз, внеклеточный матрикс регенерация и иммуносупрессия. Он также участвует в G1 арест в клеточный цикл.
Активин вызывает транскрипцию мРНК, участвующих в гонадный рост, дифференцировка эмбриона и формирование плаценты.
Nodal вызывает транскрипцию мРНК, участвующих в спецификации левой и правой оси, мезодерма и энтодерма индукция.
Регуляция пути
Путь передачи сигналов TGF beta участвует в широком спектре клеточных процессов и, следовательно, очень сильно регулируется. Существует множество механизмов, при которых этот путь модулируется положительно или отрицательно: существуют агонисты лигандов и R-SMAD; есть рецепторы-ловушки; и R-SMAD и рецепторы убиквитинированный.
Агонисты / антагонисты лигандов
Обе хордин и голова находятся антагонисты БМП. Они связывают BMP, предотвращая связывание лиганда с рецептором.[9] Было продемонстрировано, что Чордин и Ноггин дорсализируют мезодерма. Оба они находятся в спинной губе Xenopus и конвертировать иначе эпидермис указанной ткани в нервную ткань (см. нейруляция ). Noggin играет ключевую роль в формировании хрящевой и костной ткани. У мышей Noggin - / - избыток хрящевой ткани и отсутствие образования суставов.[9]
Члены семейства белков DAN также противодействуют членам семейства бета-TGF. Они включают Цербер, ДАН, и Гремлин. Эти белки содержат девять консервативных цистеины которые могут образовывать дисульфидные мостики. Считается, что ДАН противодействует GDF5, GDF6 и GDF7.
Фоллистатин ингибирует активин, который связывает. Это напрямую влияет фолликулостимулирующего гормона (ФСГ) секреция. Фоллистатин также участвует в развитии рака простаты, когда мутации в его гене могут препятствовать его действию на активин, который обладает антипролиферативными свойствами.[9]
Левша является регулятором TGFβ и участвует в формировании осевого паттерна во время эмбриогенеза. Он также является членом суперсемейства белков TGF. Он асимметрично экспрессируется в левой части мышиных эмбрионов и впоследствии играет роль в спецификации слева-справа. Левти действует, предотвращая фосфорилирование R-SMAD. Это происходит через конститутивно активный рецептор TGFβ типа I и через процесс, следующий за его активацией.[10]
Также были идентифицированы антагонисты на основе лекарственных препаратов, такие как SB431542,[11] который избирательно ингибирует ALK4, ALK5 и ALK7.
Рецепторная регуляция
В трансформирующий рецептор фактора роста 3 (TGFBR3) - самый распространенный из рецепторов TGF-β,[12] у него нет известного сигнального домена.[13] Однако это может служить для усиления связывания бета-лигандов TGF с рецепторами TGF бета типа II за счет связывания TGFβ и представления его TGFBR2. Одна из нижестоящих мишеней передачи сигналов TGF β, GIPC, связывается со своим PDZ-доменом, что предотвращает его протеосомную деградацию, что впоследствии увеличивает активность TGFβ. Он также может служить ингибин корецептор к ActivinRII.[9]
BMP и активин, связывающийся с мембраной ингибитор (BAMBI), имеет такой же внеклеточный домен, что и рецепторы типа I. Он лишен внутриклеточного домена серин / треониновой протеинкиназы и, следовательно, является псевдорецептором. Он связывается с рецептором типа I, предотвращая его активацию. Он служит негативным регулятором передачи сигналов TGF-бета и может ограничивать экспрессию tgf-бета во время эмбриогенеза. Для его экспрессии требуется передача сигналов BMP.
FKBP12 связывает GS-область рецептора типа I, предотвращая фосфорилирование рецептора рецепторами типа II. Считается, что FKBP12 и его гомологи помогают предотвратить активацию рецептора типа I в отсутствие лигандов, поскольку связывание лиганда вызывает его диссоциацию.
R-SMAD регулирование
Роль тормозных SMAD
Есть еще два SMAD, которые дополняют семейство SMAD: тормозящие SMAD (I-SMADS), SMAD6 и SMAD7. Они играют ключевую роль в регуляции передачи сигналов TGF beta и участвуют в отрицательной обратной связи. Как и другие SMAD, у них есть домен MH1 и MH2. SMAD7 конкурирует с другими R-SMAD с рецептором типа I и предотвращает их фосфорилирование.[9][14] Он находится в ядре и после активации бета-рецептора TGF перемещается в цитоплазму, где связывается с рецептором типа I. SMAD6 связывает SMAD4, предотвращая связывание других R-SMAD с coSMAD. Уровни I-SMAD увеличиваются с передачей сигналов TGF-бета, что позволяет предположить, что они являются нижележащими мишенями передачи сигналов TGF-бета.
Убиквитинирование R-SMAD
Убиквитин-белок E3 лигазы SMURF1 и SMURF2 регулируют уровни SMAD. Они принимают убиквитин от фермента, конъюгированного с E2, где они переносят убиквитин в RSMAD, что вызывает их убиквитинирование и последующее протеосомный деградация. SMURF1 связывается с SMAD1 и SMAD5 пока SMURF2 связывает SMAD1, SMAD2, SMAD3, SMAD6 и SMAD7. Это[требуется разъяснение ] усиливает ингибирующее действие SMAD7 при одновременном снижении транскрипционной активности SMAD2.
Таблица результатов
TGF-β лиганды Х. сапиенс выделено серым цветом, из D.melanogaster лиганды в розовом, из C.elegans желтым.
внешняя ссылка
- Киотская энциклопедия генов и геномов -Путь передачи сигналов бета TGF карта
- Netpath - Кураторский ресурс путей передачи сигналов у людей
Рекомендации
- ^ "Проспект Документация PDOC00223". Архивировано из оригинал на 2011-05-25. Получено 2006-07-01.
- ^ Альбертс Б., Джонсон А., Льюис Дж., Рафф М., Робертс К., Уолтер П. (2002). Молекулярная биология клетки. Нью-Йорк, Нью-Йорк: Наука о гирляндах. ISBN 978-0-8153-3218-3.
- ^ а б Мунир С., Сюй Г, Ву И, Ян Б., Лала П. К., Пэн С. (июль 2004 г.). «Nodal и ALK7 ингибируют пролиферацию и вызывают апоптоз в клетках трофобласта человека». Журнал биологической химии. 279 (30): 31277–86. Дои:10.1074 / jbc.M400641200. PMID 15150278.
- ^ Врана Дж. Л., Аттисано Л., Каркамо Дж., Зентелла А., Дуди Дж., Лайхо М. и др. (Декабрь 1992 г.). «TGF бета передает сигналы через комплекс рецепторов гетеромерной протеинкиназы». Клетка. 71 (6): 1003–14. Дои:10.1016 / 0092-8674 (92) 90395-С. PMID 1333888.
- ^ "Запись Pfam TGF_beta_GS". Получено 2006-07-01.
- ^ Рунян К.Э., Шнапер Х.В., Понселе А.С. (март 2005 г.). «Роль интернализации в трансформирующей индуцированной фактором роста бета1 ассоциации Smad2 с якорем Smad для активации рецептора (SARA) и Smad2-зависимой передачи сигналов в мезангиальных клетках человека». Журнал биологической химии. 280 (9): 8300–8. Дои:10.1074 / jbc.M407939200. PMID 15613484.
- ^ Мустакас А. (сентябрь 2002 г.). «Сеть сигнализации Smad». Журнал клеточной науки. 115 (Пт 17): 3355–6. PMID 12154066.
- ^ Souchelnytskyi S, Rönnstrand L, Heldin CH, ten Dijke P (2001). «Фосфорилирование сигнальных белков Smad рецепторными серин / треонинкиназами». Протоколы протеинкиназы. Методы молекулярной биологии. 124. С. 107–20. Дои:10.1385/1-59259-059-4:107. ISBN 1-59259-059-4. PMID 11100470.
- ^ а б c d е Massagué J, Chen YG (март 2000 г.). «Контроль передачи сигналов TGF-бета». Гены и развитие. 14 (6): 627–44. PMID 10733523.
- ^ Уллоа Л., Табибзаде С. (июнь 2001 г.). «Левша ингибирует регулируемое рецептором фосфорилирование Smad, индуцированное активированным рецептором трансформирующего фактора роста-бета». Журнал биологической химии. 276 (24): 21397–404. Дои:10.1074 / jbc.M010783200. PMID 11278746.
- ^ Laping NJ, Grygielko E, Mathur A, Butter S, Bomberger J, Tweed C и др. (Июль 2002 г.). «Ингибирование индуцированного трансформирующим фактором роста (TGF) -бета1 внеклеточного матрикса с новым ингибитором киназной активности рецептора TGF-бета типа I: SB-431542». Молекулярная фармакология. 62 (1): 58–64. Дои:10,1124 / моль 62,1,58. PMID 12065755.
- ^ Blobe GC, Лю X, Fang SJ, How T, Lodish HF (октябрь 2001 г.). «Новый механизм регуляции передачи сигналов трансформирующего фактора роста бета (TGF-бета). Функциональная модуляция экспрессии рецептора TGF-бета типа III посредством взаимодействия с белком домена PDZ, GIPC». Журнал биологической химии. 276 (43): 39608–17. Дои:10.1074 / jbc.M106831200. PMID 11546783.
- ^ Онлайн-менделевское наследование в человеке (OMIM): ТРАНСФОРМИРУЮЩИЙ ФАКТОР РОСТА-БЕТА-РЕЦЕПТОР, ТИП III; TGFBR3 - 600742
- ^ Ито Ф, Асао Х, Сугамура К., Хелдин Ч., тен Диджке П., Ито С. (август 2001 г.). «Содействие передаче сигналов костного морфогенетического белка посредством отрицательной регуляции ингибирующих Smads». Журнал EMBO. 20 (15): 4132–42. Дои:10.1093 / emboj / 20.15.4132. ЧВК 149146. PMID 11483516.
