Треонин-аммиак-лиаза - Threonine ammonia-lyase
| L-треонин-аммиак-лиаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 Трехмерное мультяшное изображение тетрамера треониндезаминазы | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 4.3.1.19 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Треонин-аммиак-лиаза, также обычно называемый треониндезаминаза или же треониндегидратаза, является фермент ответственный за катализирующий преобразование L-треонин в альфа-кетобутират и аммиак. Альфа-кетобутират может быть преобразован в L-изолейцин, поэтому треонинаммиаклиаза функционирует как ключевой фермент в BCAA синтез.[1] В нем работает пиридоксаль-5'-фосфат кофактор, подобно многим ферментам, участвующим в аминокислота метаболизм. Он находится в бактерии, дрожжи, и растения, хотя большинство исследований на сегодняшний день сосредоточено на формах фермента в бактериях. Этот фермент был одним из первых, в котором негативный отзыв торможение конечным продуктом метаболический путь непосредственно наблюдались и изучались.[2] Фермент служит отличным примером регуляторных стратегий, используемых в аминокислотах. гомеостаз.
Структура
Треонин-аммиак-лиаза представляет собой тетрамер идентичных подразделения, и оформлен как димер димеров. Каждая подблок имеет два домены: домен, содержащий каталитический активный сайт и домен с аллостерический нормативные сайты. Было показано, что эти два региона являются разными,[3] но регуляторный сайт одной субъединицы фактически взаимодействует с каталитическим сайтом другой субъединицы.[4] Оба домена содержат повторяющийся структурный мотив бета-листы окружен альфа спирали.[5] Хотя сайт связывания треонина до конца не изучен, структурные исследования действительно показывают, как связывается пиридоксальфосфатный кофактор.[4] Кофактор PLP связан с лизин остаток с помощью База Шиффа, а фосфат группа PLP удерживается амин группы, полученные из повторяющейся последовательности глицин остатки. В ароматный кольцо связано с фенилаланин, а азот на кольце водородная связь к гидроксил группы, содержащие остатки.[6]

Механизм
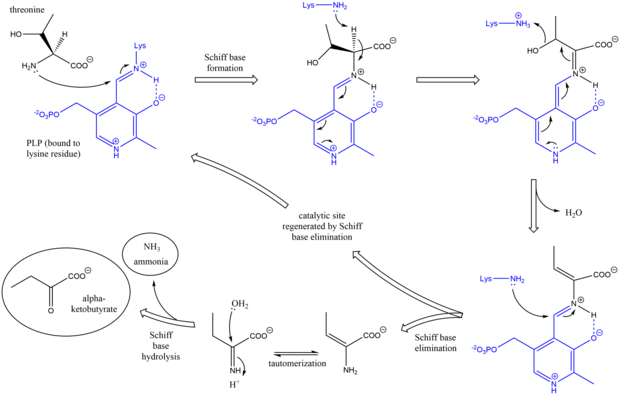
Механизм треонинаммиаклиазы аналогичен другим дезаминирующим ферментам PLP при использовании основания Шиффа. промежуточные звенья.[7] Первоначально аминогруппа треонина атакует основание Шиффа лизин / PLP, вытесняя лизин. После депротонирование аминокислоты альфа-углерод и последующие обезвоживание (отсюда и общее название треонин дегидратаза) формируется новая база Шиффа. Это основание Шиффа заменяется атакой лизина, реформируя каталитически активный PLP и высвобождая начальный алкен -содержащий продукт. Этот продукт таутомеризуется, и после гидролиз базы Шиффа генерируются конечные продукты.[8][9] После образования конечного продукта альфа-кетобутирата изолейцин синтезируется путем прохождения через промежуточные продукты альфа-ацетогидроксибутирата до альфа-бета-дигидрокси-бета-метилвалерата, а затем до альфа-кето-бета-метилвалерата.[10]
Регулирование
Было показано, что треонинаммиаклиаза не влияет на Кинетика Михаэлиса-Ментен скорее, он подлежит сложному аллостерическому контролю.[11] Фермент подавленный изолейцином, продуктом пути, в котором он участвует, и активируется валин, продукт параллельного пути.[1] Таким образом, увеличение концентрации изолейцина останавливает его производство, а увеличение концентрации валина отвлекает исходный материал (гидроксиэтил-ТЭС ) вдали от производства валина. Фермент имеет два сайта связывания изолейцина; у одного высокий близость для изолейцина, а другой имеет низкое сродство.[12] Связывание изолейцина с сайтом с высоким сродством увеличивает сродство связывания с сайтом с низким сродством, и дезактивация фермента происходит, когда изолейцин связывается с сайтом с низким сродством. Валин усиливает активность фермента за счет конкурентного связывания с сайтом с высоким сродством, предотвращая ингибирующий эффект изолейцина.[12] Комбинация этих двух методов обратной связи уравновешивает концентрацию BCAA.

Изоформы и другие функции
Несколько формы треонин-аммиак-лиазы наблюдались в различных разновидность организма. В кишечная палочка, система, в которой фермент был широко изучен, были обнаружены две различные формы фермента. Один биосинтетический и напоминает характеристики фермента, представленные здесь, в то время как другой деградирующий и функции для генерации углеродных фрагментов для производство энергии.[2] Пара изоформ также наблюдалась у других бактерий. У многих бактерий биоразлагаемая изоформа фермента выражается в анаэробный условия и продвигаются лагерь и треонин, в то время как биосинтетическая изоформа экспрессируется в аэробный условия.[13] Это позволяет бактерии сбалансировать запасы энергии и препятствовать энергоемким синтетическим путям, когда энергии не хватает.
У растений треонинаммиаклиаза играет важную роль в защитных механизмах против травоядные животные и активируется в ответ на абиотический стресс.[14] Адаптированная изоформа фермента с уникальными свойствами, отпугивающими травоядных, экспрессируется в листьях растений. Каталитический домен этой изоформы чрезвычайно устойчив к протеолиз, в то время как регуляторный домен легко разрушается, поэтому при попадании в организм другого организма способность фермента дезаминировать треонин не контролируется. Это разрушает треонин до того, как травоядное животное сможет его поглотить, в результате чего травоядное животное незаменимая аминокислота.[15] Исследования треонинаммиаклиазы в растениях также предложили новые стратегии в развитии ГМО с повышенной пищевой ценностью за счет увеличения содержания незаменимых аминокислот.[14]
Были обнаружены другие, более экзотические формы фермента, которые чрезвычайно малы по размеру, но все же сохраняют все каталитические и регуляторные функции.[4]
Эволюция
Существует пять основных типов складок для PLP-зависимых ферментов. Треонинаммиаклиаза является членом семейства складчатых типов II, также известных как триптофансинтаза семья.[7] Хотя треонин-аммиак-лиаза не обладает туннелирование субстрата как и триптофансинтаза, он содержит много консервированных гомология. Треонинаммиаклиаза наиболее близка к сериндегидратаза, и оба обладают одним и тем же общим каталитическим механизмом.[9] Фактически было показано, что треонин-аммиаклиаза проявляет некоторую специфичность в отношении серин и может превращать серин в пируват.[2] Регуляторный домен треонинаммиаклиазы очень похож на регуляторный домен фосфоглицератдегидрогеназа.[4] Все эти отношения демонстрируют, что треонинаммиаклиаза имеет близкие эволюционный связи с этими ферментами. Благодаря степени сохранности структура и последовательность в ферментах, распознающих аминокислоты, вполне вероятно, что эволюционное разнообразие этих ферментов возникло в результате совмещения отдельных регуляторных и каталитических доменов различными способами.[1]
Актуальность для человека
Треонин-аммиак-лиаза не обнаруживается у человека. Таким образом, это один из примеров того, почему люди не могут синтезировать все 20 протеиногенные аминокислоты; в этом конкретном случае люди не могут преобразовать треонин в изолейцин и должны потреблять изолейцин с пищей.[1] Фермент также изучался в прошлом как возможный агент, подавляющий опухоль по ранее описанным причинам, поскольку он лишает опухолевые клетки незаменимой аминокислоты и убивает их,[16] но это лечение не использовалось.
Рекомендации
- ^ а б c d е Берг Дж. М., Тимочко Дж. Л., Страйер Л. (2012). Биохимия (7-е изд.). Нью-Йорк: W.H. Фримен и компания. ISBN 978-1-4292-7635-1.
- ^ а б c Umbarger HE, Brown B (январь 1957 г.). «Дезаминирование треонина в Escherichia coli. II. Доказательства наличия двух L-треониновых дезаминаз». Журнал бактериологии. 73 (1): 105–12. Дои:10.1128 / jb.73.1.105-112.1957. ЧВК 289754. PMID 13405870.
- ^ Changeux J (1963). «Аллостерические взаимодействия на биосинтетической L-треониндезаминазе из E. coli K12». Симпозиумы Колд-Спринг-Харбор по количественной биологии. 28: 497–504. Дои:10.1101 / SQB.1963.028.01.066.
- ^ а б c d Галлахер Д.Т., Гиллиланд Г.Л., Сяо Дж., Зондло Дж., Фишер К.Э., Шиншилла Д., Эйзенштейн Э. (апрель 1998 г.). «Структура и контроль пиридоксальфосфат-зависимой аллостерической треониндезаминазы». Структура. 6 (4): 465–75. Дои:10.1016 / s0969-2126 (98) 00048-3. PMID 9562556.
- ^ Шнайдер Г., Кек Х., Линдквист Ю. (январь 2000 г.). «Многообразие витамин В6-зависимых ферментов». Структура. 8 (1): R1-6. Дои:10.1016 / S0969-2126 (00) 00085-X. PMID 10673430.
- ^ а б Гото М (2005). «Кристаллическая структура T.th. HB8 треониндезаминазы». Дои:10.2210 / pdb1ve5 / pdb. Цитировать журнал требует
| журнал =(помощь) - ^ а б Элиот AC, Кирш JF (2004). «Пиридоксальфосфатные ферменты: механистические, структурные и эволюционные соображения». Ежегодный обзор биохимии. 73 (1): 383–415. Дои:10.1146 / annurev.biochem.73.011303.074021. PMID 15189147.
- ^ а б Umbarger HE (2009). «Треонин дезаминазы». В Meister A (ред.). Достижения в энзимологии и смежных областях молекулярной биологии. Достижения в энзимологии и смежных областях молекулярной биологии. 37. Джон Вили и сыновья. С. 349–95. Дои:10.1002 / 9780470122822.ch6. ISBN 978-0-471-59172-6. PMID 4570068.
- ^ а б c Джин Дж, Ханефельд У (март 2011 г.). «Селективное добавление воды к связям C = C; ферменты - лучшие химики». Химические коммуникации. 47 (9): 2502–10. Дои:10.1039 / c0cc04153j. PMID 21243161.
- ^ Сквайрс С.Х., Левинталь М., Де Феличе М. (ноябрь 1981 г.). «Роль треониндезаминазы в регуляции биосинтеза альфа-ацетолактата в Escherichia coli K12». Журнал общей микробиологии. 127 (1): 19–25. Дои:10.1099/00221287-127-1-19. PMID 7040602.
- ^ Changeux JP (1961). «Механизмы контроля обратной связи биосинтетической L-треониндезаминазы с помощью L-изолейцина». Симпозиумы Колд-Спринг-Харбор по количественной биологии. 26: 313–8. Дои:10.1101 / SQB.1961.026.01.037. PMID 13878122.
- ^ а б Wessel PM, Graciet E, Douce R, Dumas R (декабрь 2000 г.). «Доказательства двух различных сайтов связывания эффекторов в треониндезаминазе с помощью сайт-направленного мутагенеза, кинетических и связывающих экспериментов» (PDF). Биохимия. 39 (49): 15136–43. Дои:10.1021 / bi001625c. PMID 11106492.
- ^ Luginbuhl GH, Hofler JG, Decedue CJ, Burns RO (октябрь 1974 г.). «Биоразлагаемая L-треониндезаминаза Salmonella typhimurium». Журнал бактериологии. 120 (1): 559–61. Дои:10.1128 / jb.120.1.559-561.1974. ЧВК 245803. PMID 4370904.
- ^ а б Джоши В., Джунг Дж., Фей З, Джандер Дж. (Октябрь 2010 г.). «Взаимозависимость метаболизма треонина, метионина и изолейцина в растениях: накопление и регуляция транскрипции в условиях абиотического стресса». Аминокислоты. 39 (4): 933–47. Дои:10.1007 / s00726-010-0505-7. PMID 20186554.
- ^ Гонсалес-Виджил Э., Бьянкетти С.М., Филлипс Г.Н., Хау Г.А. (апрель 2011 г.). «Адаптивная эволюция треониндезаминазы в защите растений от насекомых-травоядных». Труды Национальной академии наук Соединенных Штатов Америки. 108 (14): 5897–902. Дои:10.1073 / pnas.1016157108. ЧВК 3078374. PMID 21436043.
- ^ Гринфилд Р.С., Велнер Д. (август 1977 г.). «Влияние треониндезаминазы на рост и жизнеспособность клеток млекопитающих в культуре ткани и ее избирательная цитотоксичность по отношению к клеткам лейкемии». Исследования рака. 37 (8, п. 1): 2523–9. PMID 559542.