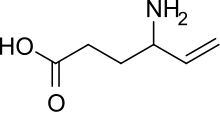
Вигабатрин - Vigabatrin
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Сабрил, Вигадрон |
| Другие имена | γ-винил-ГАМК |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a610016 |
| Беременность категория |
|
| Маршруты администрация | Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 80–90% |
| Связывание с белками | 0% |
| Метаболизм | не метаболизируется |
| Устранение период полураспада | 5-8 часов у молодых людей, 12-13 часов у пожилых людей. |
| Экскреция | Почечный |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.165.122 |
| Химические и физические данные | |
| Формула | C6ЧАС11NО2 |
| Молярная масса | 129.159 г · моль−1 |
| 3D модель (JSmol ) | |
| Температура плавления | От 171 до 177 ° C (от 340 до 351 ° F) |
| |
| |
| (проверять) | |
Вигабатрин, имя бренда Сабрил, это лекарство, используемое для лечения эпилепсия. Он стал доступен как дженерик в 2019 году.[1]
Он работает, подавляя авария из γ-аминомасляная кислота (ГАМК). Он также известен как γ-винил-ГАМК, и является структурный аналог ГАМК, но не связывается с Рецепторы ГАМК.[2]
Медицинское использование
Эпилепсия
В Канаде вигабатрин одобрен для использования в качестве дополнительного лечения (с другими препаратами) при лечении резистентных эпилепсия, сложные парциальные припадки, вторичные генерализованные приступы, а также для использования в монотерапии в инфантильные спазмы в Синдром Веста.[2]
С 2003 г. вигабатрин одобрен в Мексике для лечения эпилепсии, которая не контролируется в достаточной степени традиционной терапией (дополнительная или монотерапия), или у недавно диагностированных пациентов, которые не пробовали другие препараты (монотерапия).[3]
Вигабатрин также показан для монотерапии при вторично генерализованном тонико-клонические припадки, парциальные припадки и при инфантильных спазмах, вызванных синдромом Веста.[3]
21 августа 2009 г. компания Lundbeck объявила, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США выдало два разрешения на применение вигабатрина на новые лекарства. Препарат показан в качестве монотерапии для пациентов детского возраста от одного месяца до двух лет с инфантильные спазмы для которых потенциальные преимущества перевешивают потенциальный риск потери зрения, и в качестве дополнительной (дополнительной) терапии для взрослых пациентов с рефрактерными сложными парциальными припадками (CPS), которые неадекватно ответили на несколько альтернативных методов лечения и для которых потенциальные преимущества перевешивают риск потери зрения.
В 1994 году Feucht и Brantner-Inthaler сообщили, что вигабатрин снижает судороги на 50-100% у 85% детей с Синдром Леннокса-Гасто у кого были плохие результаты с вальпроат натрия.[4]
Другие
Вигабатрин сниженный холецистокинин тетрапептид -индуцированные симптомы паническое расстройство, помимо повышенных кортизол и АКТГ уровни у здоровых добровольцев.[5]
Вигабатрин также используется для лечения судорог при дефицит янтарной полуальдегиддегидрогеназы (SSADHD), который является врожденным дефектом метаболизма ГАМК, вызывающим Интеллектуальная недееспособность, гипотония, припадки, нарушение речи, и атаксия за счет накопления γ-оксимасляной кислоты (GHB ). Вигабатрин помогает снизить уровень ГОМК за счет ингибирования трансаминазы ГАМК. Однако это только в мозгу; он не влияет на периферическую трансаминазу ГАМК, поэтому GHB продолжает накапливаться и в конечном итоге достигает мозга.[6]
Побочные эффекты
Центральная нервная система
Сонливость (12.5%), Головная боль (3,8%), головокружение (3,8%), нервозность (2,7%), депрессия (2,5%), нарушения памяти (2,3%), диплопия (2,2%), агрессия (2,0%), атаксия (1.9%), головокружение (1.9%), гиперактивность (1,8%), потеря зрения (1,6%) (см. Ниже), путаница (1.4%), бессонница (1,3%), нарушение концентрации внимания (1,2%), проблемы с личностью (1.1%).[2] Из 299 детей 33 (11%) стали гиперактивными.[2]
У некоторых пациентов развивается психоз во время курса терапии вигабатрином,[7] что чаще встречается у взрослых, чем у детей.[8] Это может случиться даже с пациентами, у которых в анамнезе не было психоза.[9] Другие редкие побочные эффекты со стороны ЦНС включают беспокойство, эмоциональная лабильность, раздражительность, тремор, ненормальное походка, и нарушение речи.[2]
Желудочно-кишечный тракт
Боль в животе (1,6%), запор (1,4%), рвота (1,4%) и тошнота (1,4%). Диспепсия и повышенный аппетит наблюдался менее чем у 1% субъектов клинических испытаний.[2]
Тело в целом
Усталость (9,2%), увеличение веса (5,0%), астения (1.1%).[2]
Тератогенность
А тератология исследование, проведенное на кроликах, показало, что доза 150 мг / кг / день вызвала волчья пасть у 2% детенышей и в дозе 200 мг / кг / сут вызывало его у 9%.[2] Это может быть связано с уменьшением метионин уровней, согласно исследованию, опубликованному в марте 2001 г.[10] В 2005 г. было опубликовано исследование, проведенное в Университете Катании, в котором говорилось, что крысы, чьи матери потребляли 250–1000 мг / кг / день, имели более низкие показатели в водный лабиринт и задачи открытого типа крысы в группе 750 мг имели недостаточный вес при рождении и не догнали контрольную группу, а крысы в группе 1000 мг не пережили беременность.[11]
На сегодняшний день нет данных о контролируемой тератологии у людей.
Сенсорный
В 2003 году Фрисен и Мальмгрен показали, что вигабатрин вызывает необратимую диффузную атрофия из сетчатка нервное волокно слой в ретроспектива исследование 25 пациентов.[12] Это больше всего влияет на внешнюю область (в отличие от макулярный, или центральная область) сетчатки.[13]О дефектах поля зрения сообщили еще в 1997 году Том Эке и другие в Великобритании. Некоторые авторы, включая Comaish et al. считают, что потеря поля зрения и электрофизиологические изменения могут быть продемонстрированы почти у 50% пользователей Вигабатрина.
Токсичность вигабатрина для сетчатки глаза можно отнести к таурин истощение.[14]
Из соображений безопасности Вигабатрин REMS Программа требуется FDA для принятия обоснованных решений до начала и обеспечения надлежащего использования этого препарата.[15]
Взаимодействия
Исследование, опубликованное в 2002 году, показало, что вигабатрин вызывает статистически значимый увеличить в плазма оформление карбамазепин.[16]
В 1984 году доктора Риммер и Риченс из Университета Уэльса сообщили, что введение вигабатрина с фенитоин снизил концентрацию фенитоина в сыворотке крови у пациентов с резистентной к лечению эпилепсией.[17] Пять лет спустя те же два ученых сообщили о падении концентрации фенитоина на 23% в течение пяти недель в статье, описывающей их неудачную попытку выяснить механизм этого взаимодействия.[18]
Фармакология
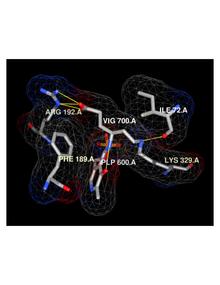
Вигабатрин - необратимый механический ингибитор из аминотрансфераза гамма-аминомасляной кислоты (ГАБА-АТ), фермент ответственный за катаболизм из ГАМК. Ингибирование ГАМК-АТ приводит к повышению уровня ГАМК в мозгу.[2][19] Вигабатрин - это рацемический соединение, и его [S] -энантиомер фармакологически активен.[20],[21]
Фармакокинетика
Для большинства лекарств период полувыведения является полезным предиктором графика дозирования и времени, необходимого для достижения стационарные концентрации. Однако в случае вигабатрина было обнаружено, что период полураспада биологической активности намного больше, чем период полувыведения.[23]
Для вигабатрина не существует диапазона целевых концентраций, потому что исследователи не обнаружили разницы между уровнями концентрации в сыворотке респондеров и тех, кто не отвечает.[24] Вместо этого считается, что продолжительность действия в большей степени зависит от скорости ресинтеза ГАМК-Т; Уровни ГАМК-Т обычно не возвращаются к своему нормальному состоянию в течение шести дней после прекращения приема лекарства.[21]
История
Вигабатрин был разработан в 1980-х годах с конкретной целью повышения концентрации ГАМК в головном мозге, чтобы остановить эпилептический припадок. Для этого был разработан препарат для необратимого ингибирования ГАМК-трансаминазы, разрушающей субстрат ГАМК. Хотя препарат был одобрен для лечения в Великобритании в 1989 г., санкционированное использование вигабатрина Управлением по контролю за продуктами и лекарствами США дважды откладывалось в США до 2009 г. Это было отложено в 1983 г., поскольку испытания на животных вызвали внутримиелиновый отек, однако Эффекты не были очевидны в испытаниях на людях, поэтому разработка препарата продолжалась. В 1997 году испытания были временно приостановлены, поскольку они были связаны с дефектами периферического поля зрения у людей.[25]
Общество и культура
Фирменные наименования
Вигабатрин продается в Канаде как Сабрил,[26] Мексика,[3]и Соединенное Королевство.[27] Торговая марка в Дании - Sabrilex. Sabril был одобрен в США 21 августа 2009 года и продается в США компанией Lundbeck Inc., которая приобрела Ovation Pharmaceuticals, спонсора США в марте 2009 года.
Общие эквиваленты
16 января 2019 г. Управление по контролю за продуктами и лекарствами (FDA) одобрило первую генерическую версию Сабрила (вигабатрина) в США.[28]
Рекомендации
- ^ «Объявления для прессы - FDA одобряет первую генерическую версию Sabril для лечения припадков у взрослых и детей, страдающих эпилепсией». www.fda.gov. Получено 21 января 2019.
- ^ а б c d е ж грамм час я Лонг, Филип У. «Вигабатрин». В архиве 23 апреля 2006 г. Wayback Machine Интернет Психическое здоровье. 1995–2003 гг.
- ^ а б c DEF Мексика: Сабрил В архиве 14 сентября 2005 г. Wayback Machine Diccionario de Especialdades Farmaceuticas. Издание 49, 2003 г.
- ^ Feucht M, Brantner-Inthaler S (1994). «Гамма-винил-ГАМК (вигабатрин) в терапии синдрома Леннокса-Гасто: открытое исследование». Эпилепсия. 35 (5): 993–8. Дои:10.1111 / j.1528-1157.1994.tb02544.x. PMID 7925171. S2CID 24204172.
- ^ Zwanzger P, Baghai TC, Schuele C, Strohle A, Padberg F, Kathmann N, Schwarz M, Moller HJ, Rupprecht R (2001). «Вигабатрин снижает панику, вызванную холецистокинин-тетрапептидом (CCK-4), у здоровых добровольцев». Нейропсихофармакология. 25 (5): 699–703. Дои:10.1016 / S0893-133X (01) 00266-4. PMID 11682253.
- ^ Перл, Филип Л; Роббинс, Эмили; Капп, Филип К; Гасиор, Мацей; Гибсон, К. Майкл (5 мая 2004 г.). «Дефицит янтарной полуальдегиддегидрогеназы». GeneReviews. Сиэтл, Вашингтон: Вашингтонский университет. Получено 6 сентября, 2010.
- ^ Сандер Дж. У., Харт Ю. М. (1990). «Вигабатрин и нарушение поведения». Ланцет. 335 (8680): 57. Дои:10.1016 / 0140-6736 (90) 90190-Г. PMID 1967367. S2CID 34456538.
- ^ Кьяретти А., Касторина М., Тортороло Л., Пиастра М., Полидори Г. (1994). «[Острый психоз и вигабатрин в детстве]». La Pediatria Medica e Chirurgica: Медицинская и хирургическая педиатрия (на итальянском). 16 (5): 489–90. PMID 7885961.
- ^ Сандер Дж. У., Харт Ю. М., Trimble MR, Шорвон С. Д. (1991). «Вигабатрин и психоз». Журнал неврологии, нейрохирургии и психиатрии. 54 (5): 435–9. Дои:10.1136 / jnnp.54.5.435. ЧВК 488544. PMID 1865207.
- ^ Абдулраззак Ю.М., Падманабхан Р., Бастаки С.М., Ибрагим А., Бенер А. (2001). «Плацентарный перенос вигабатрина (гамма-винил-ГАМК) и его влияние на концентрацию аминокислот в эмбрионе мышей TO». Тератология. 63 (3): 127–33. Дои:10.1002 / tera.1023. PMID 11283969.
- ^ Lombardo SA, Leanza G, Meli C, Lombardo ME, Mazzone L, Vincenti I, Cioni M (2005). «Воздействие на мать противоэпилептического препарата вигабатрина влияет на постнатальное развитие крыс» (PDF). Неврологические науки. 26 (2): 89–94. Дои:10.1007 / s10072-005-0441-6. HDL:2108/194069. PMID 15995825. S2CID 25257244.
- ^ Фризен Л., Мальмгрен К. (2003). «Характеристика атрофии зрительного нерва, связанной с вигабатрином». Acta Ophthalmologica Scandinavica. 81 (5): 466–73. Дои:10.1034 / j.1600-0420.2003.00125.x. PMID 14510793.
- ^ Buncic JR, Westall CA, Panton CM, Munn JR, MacKeen LD, Logan WJ (2004). «Характерная атрофия сетчатки со вторичной« обратной »атрофией зрительного нерва указывает на токсичность вигабатрина у детей». Офтальмология. 111 (10): 1935–42. Дои:10.1016 / j.ophtha.2004.03.036. ЧВК 3880364. PMID 15465561.
- ^ Гоше Д; Арно Э; Husson Z; и другие. (Ноябрь 2012 г.). «Дефицит таурина повреждает нейроны сетчатки: фоторецепторы колбочек и ганглиозные клетки сетчатки». Аминокислоты. 43 (5): 1979–1993. Дои:10.1007 / s00726-012-1273-3. ЧВК 3472058. PMID 22476345.
- ^ «САБРИЛ® (вигабатрин) таблетки для перорального применения САБРИЛ® (вигабатрин) порошок для перорального ...» Sabril.net. Получено 2019-05-31.
- ^ Санчес-Алькарас, Агустин; Quintana MB; Лопес Э; Родригес I; Ллопис П. (2002). «Влияние вигабатрина на фармакокинетику карбамазепина». Журнал клинической фармации и терапии. 27 (6): 427–30. Дои:10.1046 / j.1365-2710.2002.00441.x. PMID 12472982. S2CID 29986581.
- ^ Риммер Э.М., Риченс А. (1984). «Двойное слепое исследование гамма-винил-ГАМК у пациентов с рефрактерной эпилепсией». Ланцет. 1 (8370): 189–90. Дои:10.1016 / S0140-6736 (84) 92112-3. PMID 6141335. S2CID 54336689.
- ^ Риммер Э.М., Риченс А. (1989). «Взаимодействие между вигабатрином и фенитоином». Британский журнал клинической фармакологии. 27 (Приложение 1): 27С – 33С. Дои:10.1111 / j.1365-2125.1989.tb03458.x. ЧВК 1379676. PMID 2757906.
- ^ Rogawski MA, Löscher W (2004). «Нейробиология противоэпилептических препаратов». Nat Rev Neurosci. 5 (7): 553–564. Дои:10.1038 / номер 1430. PMID 15208697. S2CID 2201038.
- ^ Sheean, G .; Schramm T; Андерсон Д.С.; Иди MJ. (1992). «Вигабатрин - концентрации энантиомеров в плазме и клинические эффекты». Клиническая и экспериментальная неврология. 29: 107–16. PMID 1343855.
- ^ а б Грамм Л., Ларссон О.М., Йонсен А., Шоусбо А. (1989). «Экспериментальные исследования влияния вигабатрина на систему ГАМК». Британский журнал клинической фармакологии. 27 (Прил. 1): 13С – 17С. Дои:10.1111 / j.1365-2125.1989.tb03455.x. ЧВК 1379673. PMID 2757904.
- ^ Сторичи Паола; De Biase D; Bossa F; Bruno S; Моцарелли А; Пенефф С; Silverman R; Ширмер Т. (2003). «Структуры гамма-аминомасляной кислоты (ГАМК) аминотрансферазы, пиридоксаль-5'-фосфата и [2Fe-2S] кластерного фермента, в комплексе с гамма-этинил-ГАМК и противоэпилептическим препаратом вигабатрином». Журнал биологической химии. 279 (1): 363–73. Дои:10.1074 / jbc.M305884200. PMID 14534310.
- ^ Браун TR (1998). «Фармакокинетика противоэпилептических препаратов». Неврология. 51 (5 доп. 4): S2–7. Дои:10.1212 / wnl.51.5_suppl_4.s2. PMID 9818917. S2CID 39231047.
- ^ Линдбергер М., Лур О., Йоханнесен С.И., Ларссон С., Томсон Т. (2003). «Концентрации в сыворотке и эффекты габапентина и вигабатрина: наблюдения из исследования титрования дозы». Терапевтический мониторинг лекарственных средств. 25 (4): 457–62. Дои:10.1097/00007691-200308000-00007. PMID 12883229. S2CID 35834401.
- ^ Бен-Менахем Э. (2011). «Механизм действия вигабатрина: исправление неправильных представлений». Acta Neurologica Scandinavica. 124 (192): 5–15. Дои:10.1111 / j.1600-0404.2011.01596.x. PMID 22061176. S2CID 25347559.
- ^ Drugs.com Информация о препарате Вигабатрин
- ^ Лечение эпилепсии - Вигабатрин Партнерство Норфолка и Уэйвни в области психического здоровья NHS Trust
- ^ «FDA одобряет первую генерическую версию Sabril для лечения припадков у взрослых и детей с эпилепсией». НАС. Управление по контролю за продуктами и лекарствами (FDA) (Пресс-релиз). 2019-09-11.
внешняя ссылка
- «Вигабатрин». Портал информации о наркотиках. Национальная медицинская библиотека США.
