Синтез эфира Вильямсона - Williamson ether synthesis
| Синтез эфира Вильямсона | |
|---|---|
| Названный в честь | Александр Уильям Уильямсон |
| Тип реакции | Реакция сцепления |
| Идентификаторы | |
| Портал органической химии | синтез Уильямсона |
| RSC ID онтологии | RXNO: 0000090 |

В Синтез эфира Вильямсона является органическая реакция, формируя эфир из органо-галогенид и депротонированный спирт (алкоксид ). Эта реакция была разработана Александр Вильямсон в 1850 г.[2] Обычно это реакция алкоксид-ион с первичным алкилом галогенид через SN2 реакция. Эта реакция важна в истории органической химии, потому что она помогла доказать структуру эфиры.
Общий механизм реакции следующий:[3]
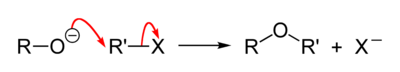
Примером может служить реакция этоксид натрия с хлорэтаном с образованием диэтиловый эфир и хлорид натрия:
- [Na]+[C2ЧАС5O]− + C2ЧАС5Cl → C2ЧАС5OC2ЧАС5 + [Na]+[Cl]−
Механизм
Реакция эфира Вильямсона следует SN2 бимолекулярный механизм нуклеофильного замещения. В SN2 механизм реакции: обратная атака электрофила нуклеофилом происходит по согласованному механизму (происходит сразу). Для того, чтобы SN2 должна иметь место хорошая уходящая группа, которая является сильно электроотрицательной, обычно галогенид.[4]
В реакции эфира Вильямсона присутствует алкоксид-ион (RO−), который действует как нуклеофил, атакуя электрофильный углерод с уходящей группой, которая в большинстве случаев представляет собой алкилтозилат или алкилгалогенид. Уходящий сайт должен быть первичным углеродом, потому что вторичные и третичные уходящие сайты обычно предпочитают действовать как реакция элиминации. Кроме того, эта реакция не способствует образованию объемных простых эфиров, таких как ди-трет-бутиловый эфир, из-за стерических затруднений и преимущественного образования алкенов.[5]

Объем
Реакция Вильямсона имеет широкий спектр применения, широко используется как в лабораторном, так и в промышленном синтезе и остается самым простым и популярным методом получения простых эфиров. Легко готовятся как симметричные, так и асимметричные эфиры. Внутримолекулярная реакция галогидрины в частности, дает эпоксиды.
В случае асимметричных эфиров есть две возможности для выбора реагентов, и одна обычно предпочтительна либо на основе доступности, либо на основе реакционной способности. Реакция Вильямсона также часто используется для получения эфира косвенно из двух спиртов. Один из спиртов сначала превращается в уходящую группу (обычно тозилат ), затем оба реагируют вместе.
Алкоксид (или арилоксид ) может быть первичным, вторичным или третичным. С другой стороны, наиболее предпочтительно, чтобы алкилирующий агент был первичным. Вторичные алкилирующие агенты также вступают в реакцию, но третичные, как правило, слишком склонны к побочным реакциям, чтобы иметь практическое применение. Уходящая группа чаще всего представляет собой галогенид или сложный эфир сульфоновой кислоты, синтезируемый с целью реакции. Поскольку условия реакции достаточно жесткие, защитные группы часто используются для успокоения других частей реагирующих молекул (например, других спирты, амины, так далее.)
Синтез эфира Вильямсона - обычная реакция в области органической химии при промышленном синтезе и в учебных лабораториях бакалавриата. При сокращении времени реакции выходы для этих синтезов простых эфиров традиционно низкие, что может иметь место во время лабораторных занятий в бакалавриате. Не позволяя реакциям кипеть с обратным холодильником в течение правильного промежутка времени (где-то от 1-8 часов от 50 до 100 ° C), реакция может не продолжиться до завершения, что приведет к низкому общему выходу продукта. Чтобы помочь смягчить эту проблему, в настоящее время используется микроволновая технология для ускорения времени реакции для таких реакций, как синтез эфира Вильямсона. Эта технология изменила время реакции, требующее кипячения с обратным холодильником не менее 1,5 часов, до быстрой 10-минутной работы в микроволновой печи при 130 ° C, и это увеличило выход синтезированного эфира с 6-29% до 20-55% (данные был составлен из нескольких различных лабораторных разделов, в которых использовалась технология в своих синтезах).[6]
Также были достигнуты значительные успехи в синтезе простых эфиров при использовании температур 300 ° C и выше и использовании более слабых алкилирующих агентов для облегчения более эффективного синтеза. Эта методология помогает оптимизировать процесс синтеза и делает синтез в промышленных масштабах более осуществимым. Более высокая температура делает слабый алкилирующий агент более реактивным и с меньшей вероятностью будет производить соли в качестве побочного продукта. Этот метод оказался высокоселективным и особенно полезным при производстве ароматических простых эфиров, таких как анизол, которые находят все более широкое применение в промышленности.[7]
Условия
Поскольку ионы алкоксида обладают высокой реакционной способностью, их обычно получают непосредственно перед реакцией или образуются на месте. В лабораторной химии, на месте генерация чаще всего достигается за счет использования карбонат база или гидроксид калия, а в промышленных синтезах фазовый катализ очень часто. Можно использовать широкий спектр растворителей, но протонные растворители и неполярные растворители имеют тенденцию сильно замедлять скорость реакции в результате снижения доступности свободного нуклеофила. По этой причине, ацетонитрил и N,N-диметилформамид особенно часто используются.
Типичная реакция Вильямсона проводится при температуре от 50 до 100 ° C и завершается за 1-8 часов. Часто бывает трудно добиться полного исчезновения исходного материала, и часто возникают побочные реакции. Выход 50–95% обычно достигается при лабораторном синтезе, в то время как почти количественное преобразование может быть достигнуто в промышленных процессах.
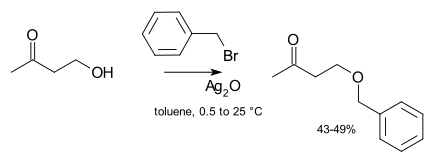
Катализ обычно не требуется при лабораторном синтезе. Однако если неактивный алкилирующий агент (например, алкилхлорид), то скорость реакции может быть значительно улучшена путем добавления каталитического количества растворимой йодидной соли (которая претерпевает галогенидный обмен с хлоридом с образованием гораздо более реакционноспособного йодида, варианта Реакция Финкельштейна ). В крайних случаях соединения серебра, такие как оксид серебра могут быть добавлены:[8]
Ион серебра координируется с уходящей группой галогенида, чтобы сделать его уход более легким. Наконец, иногда используются катализаторы межфазного переноса (например, бромид тетрабутиламмония или же 18-крон-6 ), чтобы увеличить растворимость алкоксида, предлагая более мягкий противоион Еще одним примером реакции этерификации в трехфазной системе в каталитических условиях фазового переноса является реакция бензилхлорида и фурфурилового спирта.[9]
Побочные реакции
Реакция Вильямсона часто конкурирует с катализируемым основанием удалением алкилирующего агента,[3] и природа уходящей группы, а также условия реакции (в частности, температура и растворитель) могут иметь сильное влияние, на которые отдается предпочтение. В частности, некоторые структуры алкилирующего агента могут быть особенно подвержены удалению.
Когда нуклеофил представляет собой арилоксид-ион, реакция Вильямсона также может конкурировать с алкилированием по кольцу, поскольку арилоксид является амбидентный нуклеофил.
Смотрите также
- Конденсация Ульмана для образования бис-ариловых эфиров
- Диметилсульфат и Диэтилсульфат, относительно недорогой органосульфаты используется в альтернативных методах синтеза эфира
Рекомендации
- ^ Burgstahler, Альберт В .; Уорден, Леонард Р. (1966). «Кумарон». Органический синтез. 46: 28. Дои:10.15227 / orgsyn.046.0028.; Коллективный объем, 5, п. 251
- ^ Уильямсон, Александр (1850). «Теория террификации». Философский журнал. 37 (251): 350–356. Дои:10.1080/14786445008646627. (Ссылка на отрывок. )
- ^ а б Бойд, Роберт Нейлсон; Моррисон, Роберт Торнтон (1992). Органическая химия (6-е изд.). Энглвуд Клиффс, Нью-Джерси: Prentice Hall. С. 241–242. ISBN 9780136436690.
- ^ Уэйд, Лерой (2017). Органическая химия. Пирсон. С. 261–274. ISBN 9780321971371.
- ^ Уэйд, Лерой (2017). Органическая химия. Пирсон. С. 682–683. ISBN 9780321971371.
- ^ Baar, Marsha R .; Фальконе, Даниэль; Гордон, Кристофер (2010). "Микроволновые улучшенные органические синтезы для студенческой лаборатории: циклоприсоединение Дильса-Альдера, реакция Виттига и синтез эфира Вильямсона". Журнал химического образования. 87 (1): 84–86. Bibcode:2010JChEd..87 ... 84B. Дои:10.1021 / ed800001x.
- ^ Фурманн, Эдгар; Талберский, Йорг (2005). «Синтез алкилариловых эфиров каталитическим синтезом эфира Вильямсона со слабыми агентами алкилирования». Исследования и разработки в области органических процессов. 9 (2): 206–211. Дои:10.1021 / op050001h.
- ^ Танабэ, Масато; Питерс, Ричард Х. (1981). "(р,S) -Мевалонолактон-2-13С (2ЧАС-Пиран-2-он-13С, тетрагидро-4-гидрокси-4-метил-) ». Органический синтез. 60: 92. Дои:10.15227 / orgsyn.060.0092.; Коллективный объем, 7, п. 386
- ^ Католь Д.О., Ядав Г.Д. Интенсификация процесса и минимизация отходов с использованием катализатора с трехфазным переносом жидкость-жидкость-жидкость для синтеза 2 - ((бензилокси) метил) фурана. Молекулярный катализ 2019; 466: 112–21. https://doi.org/10.1016/j.mcat.2019.01.004