Хлорид цезия - Caesium chloride
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК Хлорид цезия | |
| Другие имена Хлорид цезия | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.728 |
| Номер ЕС |
|
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| CsCl | |
| Молярная масса | 168,36 г / моль |
| Внешность | белое твердое вещество гигроскопичный |
| Плотность | 3,988 г / см3[1] |
| Температура плавления | 646 ° С (1195 ° F, 919 К)[1] |
| Точка кипения | 1297 ° С (2367 ° F, 1570 К)[1] |
| 1910 г / л (25 ° С)[1] | |
| Растворимость | растворим в этиловый спирт[1] |
| Ширина запрещенной зоны | 8,35 эВ (80 К)[2] |
| -56.7·10−6 см3/ моль[3] | |
| 1,712 (0,3 мкм) 1,640 (0,59 мкм) 1,631 (0,75 мкм) 1,626 (1 мкм) 1,616 (5 мкм) 1,563 (20 мкм)[4] | |
| Структура | |
| CsCl, cP2 | |
| Вечера3м, №221[5] | |
а = 0,4119 нм | |
Объем решетки (V) | 0,0699 нм3 |
Формула единиц (Z) | 1 |
| Кубический (Cs+) Кубический (Cl−) | |
| Опасности | |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Предупреждение |
| H302, H341, H361, H373 | |
| P201, P202, P260, P264, P270, P281, P301 + 312, P308 + 313, P314, P330, P405, P501 | |
| Смертельная доза или концентрация (LD, LC): | |
LD50 (средняя доза ) | 2600 мг / кг (перорально, крыса)[6] |
| Родственные соединения | |
Другой анионы | Фторид цезия Бромид цезия Йодид цезия Цезий астатид |
Другой катионы | Лития хлорид Натрия хлорид Хлорид калия Рубидий хлорид Хлорид франция |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Хлорид цезия или хлорид цезия это неорганическое соединение с формулой CSCl. Эта бесцветная соль - важный источник цезий ионы во множестве нишевых приложений. Его кристаллическая структура образует основной структурный тип, в котором каждый ион цезия координируется 8 ионами хлора. Хлорид цезия растворяется в воде. CsCl при нагревании переходит в структуру NaCl. Хлорид цезия встречается в природе в виде примесей в карналлит (до 0,002%), сильвит и каинит. Менее 20 тонны CsCl производится ежегодно во всем мире, в основном из цезийсодержащих минералов. поллюцит.[7]
Хлорид цезия является широко используемым лекарственным составом в изопикническое центрифугирование для разделения различных типов ДНК. Это реагент в аналитическая химия, где он используется для идентификации ионов по цвету и морфологии осадка. При обогащении радиоизотопы, такие как 137CsCl или 131CsCl, хлорид цезия используется в ядерная медицина такие приложения, как лечение рак и диагностика инфаркт миокарда. Другая форма лечения рака была изучена с использованием обычного нерадиоактивного CsCl. В то время как обычный хлорид цезия имеет довольно низкую токсичность для людей и животных, радиоактивная форма легко загрязняет окружающую среду из-за высокой растворимости CsCl в воде. Распространение 137Порошок CsCl из 93-граммового контейнера в 1987 г. в г. Гояния, Бразилия, привела к одной из самых страшных аварий с разливом радиации, в результате чего погибли четыре человека и напрямую пострадали более 100 000 человек.
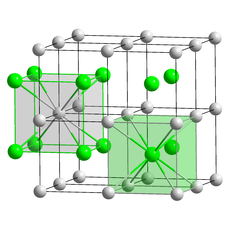
Кристальная структура
Структура хлорида цезия имеет примитивную кубическую решетку с двухатомной основой, где оба атома имеют восьмикратную координацию. Атомы хлора лежат в узлах решетки на краях куба, а атомы цезия - в отверстиях в центре куба. Эта структура используется совместно с CsBr и CsI и многие бинарные металлические сплавы. Напротив, другие щелочные галогениды имеют хлорид натрия (каменная) структура.[8] Когда оба иона близки по размеру (Cs+ ионный радиус 174 пм для этого координационного числа, Cl− 181 пм) принята структура CsCl, когда они разные (Na+ ионный радиус 102 вечера, Cl− 181 вечера) хлорид натрия структура принята. При нагревании до температуры выше 445 ° C нормальная структура хлорида цезия (α-CsCl) преобразуется в форму β-CsCl со структурой каменной соли (космическая группа FM3м).[5] Структура каменной соли также наблюдается в обычных условиях в пленках CsCl нанометровой толщины, выращенных на слюда, Подложки LiF, KBr и NaCl.[9]
Физические свойства
Хлорид цезия бесцветен в виде крупных кристаллов и белого цвета при измельчении. Он легко растворяется в воде, максимальная растворимость увеличивается с 1865 г / л при 20 ° C до 2705 г / л при 100 ° C.[10] Кристаллы очень гигроскопичный и постепенно распадаются в условиях окружающей среды.[11] Хлорид цезия не образует гидраты.[12]
| Т (° С) | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| S (мас.%) | 61.83 | 63.48 | 64.96 | 65.64 | 66.29 | 67.50 | 68.60 | 69.61 | 70.54 | 71.40 | 72.21 | 72.96 |
В отличие от хлорид натрия и хлористый калий, хлорид цезия легко растворяется в концентрированной соляной кислоте.[14][15] Хлорид цезия также имеет относительно высокую растворимость в Муравьиная кислота (1077 г / л при 18 ° C) и гидразин; средняя растворимость в метанол (31,7 г / л при 25 ° C) и низкая растворимость в этиловый спирт (7,6 г / л при 25 ° C),[12][15][16] диоксид серы (2,95 г / л при 25 ° C), аммиак (3,8 г / л при 0 ° C), ацетон (0,004% при 18 ° C), ацетонитрил (0,083 г / л при 18 ° C),[15] этилацетаты и другие сложные эфиры, бутанон, ацетофенон, пиридин и хлорбензол.[17]
Несмотря на широкую запрещенная зона около 8,35 эВ при 80 К,[2] хлорид цезия слабо проводит электричество, и проводимость не электронная, а ионный. Электропроводность имеет величину порядка 10−7 См / см при 300 ° C. Это происходит за счет скачков вакансий в решетке ближайших соседей, а подвижность Cl− чем Cs+ свободные места. Электропроводность увеличивается с температурой примерно до 450 ° C, а энергия активации изменяется от 0,6 до 1,3 эВ при примерно 260 ° C. Затем она резко падает на два порядка из-за фазового перехода от фазы α-CsCl к фазе β-CsCl. Проводимость также подавляется приложением давления (уменьшение примерно в 10 раз при 0,4 ГПа), что снижает подвижность вакансий решетки.[18]
| Концентрация, вес% | Плотность, кг / л | Концентрация, Молл | показатель преломления (при 589 нм) | Понижение точки замерзания, ° С относительно воды | Вязкость, 10−3 Па · с |
|---|---|---|---|---|---|
| 0.5 | – | 0.030 | 1.3334 | 0.10 | 1.000 |
| 1.0 | 1.0059 | 0.060 | 1.3337 | 0.20 | 0.997 |
| 2.0 | 1.0137 | 0.120 | 1.3345 | 0.40 | 0.992 |
| 3.0 | 0.182 | 1.3353 | 0.61 | 0.988 | |
| 4.0 | 1.0296 | 0.245 | 1.3361 | 0.81 | 0.984 |
| 5.0 | 0.308 | 1.3369 | 1.02 | 0.980 | |
| 6.0 | 1.0461 | 0.373 | 1.3377 | 1.22 | 0.977 |
| 7.0 | 0.438 | 1.3386 | 1.43 | 0.974 | |
| 8.0 | 1.0629 | 0.505 | 1.3394 | 1.64 | 0.971 |
| 9.0 | 0.573 | 1.3403 | 1.85 | 0.969 | |
| 10.0 | 1.0804 | 0.641 | 1.3412 | 2.06 | 0.966 |
| 12.0 | 1.0983 | 0.782 | 1.3430 | 2.51 | 0.961 |
| 14.0 | 1.1168 | 0.928 | 1.3448 | 2.97 | 0.955 |
| 16.0 | 1.1358 | 1.079 | 1.3468 | 3.46 | 0.950 |
| 18.0 | 1.1555 | 1.235 | 1.3487 | 3.96 | 0.945 |
| 20.0 | 1.1758 | 1.397 | 1.3507 | 4.49 | 0.939 |
| 22.0 | 1.1968 | 1.564 | 1.3528 | – | 0.934 |
| 24.0 | 1.2185 | 1.737 | 1.3550 | – | 0.930 |
| 26.0 | 1.917 | 1.3572 | – | 0.926 | |
| 28.0 | 2.103 | 1.3594 | – | 0.924 | |
| 30.0 | 1.2882 | 2.296 | 1.3617 | – | 0.922 |
| 32.0 | 2.497 | 1.3641 | – | 0.922 | |
| 34.0 | 2.705 | 1.3666 | – | 0.924 | |
| 36.0 | 2.921 | 1.3691 | – | 0.926 | |
| 38.0 | 3.146 | 1.3717 | – | 0.930 | |
| 40.0 | 1.4225 | 3.380 | 1.3744 | – | 0.934 |
| 42.0 | 3.624 | 1.3771 | – | 0.940 | |
| 44.0 | 3.877 | 1.3800 | – | 0.947 | |
| 46.0 | 4.142 | 1.3829 | – | 0.956 | |
| 48.0 | 4.418 | 1.3860 | – | 0.967 | |
| 50.0 | 1.5858 | 4.706 | 1.3892 | – | 0.981 |
| 60.0 | 1.7886 | 6.368 | 1.4076 | – | 1.120 |
| 64.0 | 7.163 | 1.4167 | – | 1.238 |
Реакции
Хлорид цезия полностью диссоциирует при растворении в воде, и Cs+ катионы находятся растворенный в разбавленном растворе. CsCl преобразуется в сульфат цезия при нагревании в концентрированной серной кислоте или нагревании с гидросульфат цезия при 550–700 ° C:[21]
- 2 CsCl + H2ТАК4 → Cs2ТАК4 + 2 HCl
- CsCl + CsHSO4 → Cs2ТАК4 + HCl
Хлорид цезия образует множество двойных солей с другими хлоридами. Примеры включают 2CsCl · BaCl2,[22] 2CsCl · CuCl2, CsCl · 2CuCl и CsCl·LiCl,[23] и с межгалогенный соединения:[24]
Возникновение и производство
Хлорид цезия встречается в природе как примесь в галогенидных минералах. карналлит (KMgCl3· 6H2O с содержанием CsCl до 0,002%),[26] сильвит (KCl) и каинит (MgSO4· KCl · 3H2O),[27] и в минеральных водах. Например, вода Бад-Дюркхайм spa, который использовался для выделения цезия, содержал около 0,17 мг / л CsCl.[28] Ни один из этих минералов не имеет коммерческого значения.
В промышленных масштабах CsCl производится из минерального сырья. поллюцит, который измельчают и обрабатывают соляной кислотой при повышенной температуре. Экстракт обрабатывают хлорид сурьмы, монохлорид йода или хлорид церия (IV) с получением малорастворимой двойной соли, например:[29]
- CsCl + SbCl3 → CsSbCl4
Лечение двойной солью сероводород дает CsCl:[29]
- 2 CsSbCl4 + 3 часа2S → 2 CsCl + Sb2S3 + 8 HCl
CsCl высокой чистоты также получают из перекристаллизованного (и ) термическим разложением:[30]
Всего около 20 тонны соединений цезия, с основным вкладом из CsCl, производились ежегодно примерно в 1970-х годах.[31] и 2000-е годы по всему миру.[32] Хлорид цезия, обогащенный цезием-137 для радиационная терапия заявки производятся на едином предприятии Маяк в Уральский регион России[33] и продается на международном уровне через дилера в Великобритании. Соль синтезируется при 200 ° C из-за ее гигроскопичности и герметизируется в стальном контейнере в форме гильзы, который затем помещается в другой стальной корпус. Уплотнение требуется для защиты соли от влаги.[34]
Лабораторные методы
В лаборатории CsCl можно получить путем обработки гидроксид цезия, карбонат, бикарбонат цезия или сульфид цезия с соляной кислотой:
- CsOH + HCl → CsCl + H2О
- CS2CO3 + 2 HCl → 2 CsCl + 2 H2O + CO2
Использует
Предшественник металла Cs
Хлорид цезия является основным прекурсором металлического цезия путем высокотемпературного восстановления:[31]
- 2 CsCl (л) + Mg (л) → MgCl2 (s) + 2 Cs (г)
Похожая реакция - нагрев CsCl с кальцием в вакууме в присутствии фосфор - впервые сообщил в 1905 году французский химик М. Л. Хакспилл.[35] и до сих пор используется в промышленности.[31]
Гидроксид цезия получается электролиз водного раствора хлорида цезия:[36]
- 2 CsCl + 2 Н2О → 2 CsOH + Cl2 + H2
Раствор для ультрацентрифугирования
Хлорид цезия широко используется в центрифугирование в технике, известной как изопикническое центрифугирование. Центростремительные и диффузионные силы создают градиент плотности, который позволяет разделить смеси на основе их молекулярной плотности. Этот метод позволяет разделить ДНК разной плотности (например, фрагменты ДНК с различным содержанием A-T или G-C).[31] Для этого применения требуется раствор с высокой плотностью и при этом относительно низкой вязкостью, и CsCl подходит для этого из-за его высокой растворимости в воде, высокой плотности из-за большой массы Cs, а также низкой вязкости и высокой стабильности растворов CsCl.[29]
Органическая химия
Хлорид цезия редко используется в органической химии. Он может действовать как катализатор межфазного переноса реагент в выбранных реакциях. Одна из таких реакций - синтез глютаминовая кислота производные
где TBAB представляет собой бромид тетрабутиламмония (межфазный катализатор), а CPME представляет собой циклопентилметиловый эфир (растворитель).[37]
Другая реакция - замена тетранитрометан[38]
где ДМФ диметилформамид (растворитель).
Аналитическая химия
Хлорид цезия - это реагент в традиционных аналитическая химия используется для обнаружения неорганических ионов по цвету и морфологии осадков. Количественное измерение концентрации некоторых из этих ионов, например Mg2+, с участием масс-спектрометрия с индуктивно связанной плазмой, используется для оценки жесткости воды.[39]
| Ион | Сопутствующие реагенты | Остаток | Морфология | Предел обнаружения (мкг) |
|---|---|---|---|---|
| AsO33− | KI | CS2[Как и я5] или Cs3[Как и я6] | Красные шестиугольники | 0.01 |
| Au3+ | AgCl, HCl | CS2Ag [AuCl6] | Серо-черные кресты, четырех- и шестилучевые звезды | 0.01 |
| Au3+ | NH4SCN | Cs [Au (SCN)4] | Оранжево-желтые иглы | 0.4 |
| Би3+ | KI, HCl | CS2[BiI5] или 2,5H2О | Красные шестиугольники | 0.13 |
| Cu2+ | (CH3COO)2Pb, CH3COOH, KNO2 | CS2Pb [Cu (NO2)6] | Маленькие черные кубики | 0.01 |
| В3+ | — | CS3[InCl6] | Малые октаэдры | 0.02 |
| [IrCl6]3− | — | CS2[IrCl6] | Маленькие темно-красные октаэдры | – |
| Mg2+ | Na2HPO4 | CsMgPO4 или 6H2О | Маленькие тетраэдры | – |
| Pb2+ | KI | Cs [PbI3] | Желто-зеленая хвоя | 0.01 |
| Pd2+ | NaBr | CS2[PdBr4] | Темно-красные иглы и призмы | – |
| [ReCl4]− | — | Cs [ReCl4] | Темно-красные ромбы, бипирамиды | 0.2 |
| [ReCl6]2− | — | CS2[ReCl6] | Маленькие желто-зеленые октаэдры | 0.5 |
| ReO4− | — | CsReO4 | Тетрагональные бипирамиды | 0.13 |
| Rh3+ | KNO2 | CS3[Rh (НЕТ2)6] | Желтые кубики | 0.1 |
| RU3+ | — | CS3[RuCl6] | Розовые иглы | – |
| [RuCl6]2− | — | CS2[RuCl6] | Мелкие темно-красные кристаллы | 0.8 |
| Sb3+ | — | CS2[SbCl5]·пЧАС2О | Шестиугольники | 0.16 |
| Sb3+ | NaI | или | Красные шестиугольники | 0.1 |
| Sn4+ | — | CS2[SnCl6] | Малые октаэдры | 0.2 |
| TeO33− | HCl | CS2[TeCl6] | Светло-желтые октаэдры | 0.3 |
| Tl3+ | NaI | Оранжево-красные шестиугольники или прямоугольники | 0.06 |
Он также используется для обнаружения следующих ионов:
| Ион | Сопутствующие реагенты | Обнаружение | Предел обнаружения (мкг / мл) |
|---|---|---|---|
| Al3+ | K2ТАК4 | В нейтральной среде после испарения образуются бесцветные кристаллы. | 0.01 |
| Ga3+ | ХСО4 | Бесцветные кристаллы образуются при нагревании | 0.5 |
| Cr3+ | ХСО4 | Бледно-фиолетовые кристаллы выпадают в осадок в слабокислой среде. | 0.06 |
Лекарство
В Американское онкологическое общество заявляет, что «имеющиеся научные данные не подтверждают утверждения о том, что добавки с нерадиоактивным хлоридом цезия имеют какое-либо влияние на опухоли».[40] В Управление по контролю за продуктами и лекарствами предупредил о рисках безопасности, включая значительную сердечную токсичность и смерть, связанные с использованием хлорида цезия в натуропатической медицине.[41][42]
Ядерная медицина и радиография
Хлорид цезия, состоящий из радиоизотопы такие как 137CsCl и 131CsCl,[43] используется в ядерная медицина, включая лечение рак (брахитерапия ) и диагностика инфаркт миокарда.[44][45] В производстве радиоактивный источников, обычно выбирают химическую форму радиоизотопа, которая не будет легко рассеиваться в окружающей среде в случае аварии. Например, радиотермические генераторы (РИТЭГ) часто используют титанат стронция, который не растворяется в воде. За телетерапия источников, однако радиоактивная плотность (Ci в данном объеме) должно быть очень высоким, что невозможно с известными нерастворимыми соединениями цезия. Контейнер радиоактивного хлорида цезия в форме наперстка является активным источником.
Разные приложения
Хлорид цезия используется при приготовлении электропроводящих материалов. очки[43][46] и экраны электронно-лучевых трубок.[31] Вместе с инертными газами CsCl используется в эксимерные лампы[47][48] и эксимерные лазеры. Другие применения включают активацию электродов при сварке;[49] производство минеральной воды, пива[50] и буровые растворы;[51] и жаропрочные припои.[52] Высококачественные монокристаллы CsCl имеют широкий диапазон прозрачности от УФ до инфракрасного излучения и поэтому использовались для изготовления кювет, призм и окон в оптических спектрометрах;[31] это использование было прекращено с разработкой менее гигроскопичных материалов.
CsCl является мощным ингибитором каналов HCN, которые переносят h-ток в возбудимых клетках, таких как нейроны.[53] Следовательно, он может быть полезен в экспериментах по электрофизиологии в нейробиологии.
Токсичность
Хлорид цезия малотоксичен для человека и животных.[54] это средняя смертельная доза (LD50) у мышей составляет 2300 мг на килограмм массы тела для перорального введения и 910 мг / кг для внутривенной инъекции.[55] Легкая токсичность CsCl связана с его способностью снижать концентрацию калия в организме и частично замещать его в биохимических процессах.[56] Однако при приеме в больших количествах может вызвать значительный дисбаланс калия и привести к гипокалиемия, аритмия, и острый остановка сердца.[57] Однако порошок хлорида цезия может раздражать слизистые оболочки и причина астма.[51]
Из-за своей высокой растворимости в воде хлорид цезия очень подвижен и может даже диффундировать через бетон. Это недостаток его радиоактивной формы, который требует поиска более стабильных радиоизотопных материалов. Коммерческие источники радиоактивного хлорида цезия надежно закрыты двойным стальным корпусом.[34] Однако в Гоянская авария в Бразилия, такой источник, содержащий около 93 граммов 137CsCl был украден из заброшенной больницы и взломан двумя мусорщиками. Голубое свечение, излучаемое радиоактивным хлоридом цезия в темноте, привлекло воров и их родственников, которые не подозревали о связанных с этим опасностях, и рассыпали порошок. Это привело к одной из самых серьезных аварий с разливом радиации, в которой 4 человека погибли в течение месяца после облучения, 20 проявили признаки заражения. лучевая болезнь, 249 человек были заражены радиоактивным хлоридом цезия, а около тысячи получили дозу, превышающую годовой уровень радиационного фона. Более 110 000 человек переполнили местные больницы, и несколько городских кварталов пришлось снести в ходе уборочных работ. В первые дни заражения несколько человек испытали расстройства желудка и тошноту из-за лучевой болезни, но только через несколько дней один человек связал симптомы с порошком и принес властям образец.[58][59]
Смотрите также
Рекомендации
- ^ а б c d е Хейнс, стр. 4,57
- ^ а б Лущик, А; Feldbach, E; Фрорип, А; Ибрагимов К; Куусманн, I; Лущик, Ц (1994). «Релаксация экситонов в широкозонных кристаллах CsCl». Журнал физики: конденсированное вещество. 6 (12): 2357–2366. Bibcode:1994JPCM .... 6.2357L. Дои:10.1088/0953-8984/6/12/009.
- ^ Хейнс, стр. 4,132
- ^ Хейнс, стр. 10,240
- ^ а б Watanabe, M .; Токонами, М .; Моримото, Н. (1977). «Механизм перехода между структурами типа CsCl и NaCl в CsCl». Acta Crystallographica Раздел A. 33 (2): 294. Bibcode:1977AcCrA..33..294W. Дои:10.1107 / S0567739477000722.
- ^ Хлорид цезия. nlm.nih.gov
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.
- ^ Уэллс А.Ф. (1984) Структурная неорганическая химия 5-е издание Oxford Science Publications ISBN 0-19-855370-6
- ^ Шульц, Л. Г. (1951). «Полиморфизм галогенидов цезия и таллия». Acta Crystallographica. 4 (6): 487–489. Дои:10.1107 / S0365110X51001641.
- ^ Лидин, п. 620
- ^ "ЭСБЕ / Цезий". Энциклопедический словарь Брокгауза и Ефрона. 1890–1907. Получено 2011-04-15.
- ^ а б Кнунянц, И.Л., изд. (1998). «Цезия галогениды». Химическая энциклопедия (Химическая энциклопедия). 5. Москва: Советская энциклопедия. п. 657. ISBN 978-5-85270-310-1.
- ^ Хейнс, стр. 5,191
- ^ Турова, Н.Я. (1997). Неорганическая химия в таблицах. Москва. п. 85.
- ^ а б c Плюшев, В.Е .; Степин, Б. Д (1975). Аналитическая химия рубидия и цезия. Москва: Наука. С. 22–26.
- ^ Плюшев, п. 97
- ^ Плюшев, В.Е .; и другие. (1976). Большаков К.А. (ред.). Химия и технология редких и рассеянных элементов. 1 (2-е изд.). Москва: Высшая школа. С. 101–103.
- ^ Эренрайх, Генри (1984). Физика твердого тела: достижения в исследованиях и приложениях. Академическая пресса. С. 29–31. ISBN 978-0-12-607738-4.
- ^ Хейнс, стр. 5,126
- ^ Лидин, п. 645
- ^ Лидин, Р. А; Молочко В .; Андреева, Л. Л. А. (2000). Химические свойства неорганических веществ (3-е изд.). Москва: Химия. п. 49. ISBN 978-5-7245-1163-6.
- ^ Кнунянц, И.Л., изд. (1988). «Бария хлорид». Химическая энциклопедия. 1. Москва: Советская энциклопедия. п. 463.
- ^ Национальный исследовательский совет (США). Управление критических таблиц, изд. (1962). Сводный указатель отдельных значений свойств: физическая химия и термодинамика (Издание 976-е изд.). Вашингтон, округ Колумбия: Национальная академия наук. п. 271.
- ^ Кнунянц, И.Л., изд. (1992). «Полигалогениды». Химическая энциклопедия. 3. Москва: Советская энциклопедия. С. 1237–1238. ISBN 978-5-85270-039-1.
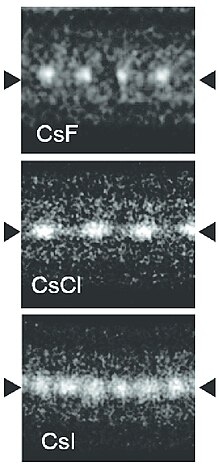
- ^ Сенга, Рёске; Комса, Ханну-Пекка; Лю, Чжэн; Хиросе-Такай, Каори; Крашенинников, Аркадий В .; Суэнага, Кадзу (2014). «Атомная структура и динамическое поведение по-настоящему одномерных ионных цепочек внутри углеродных нанотрубок». Материалы Природы. 13 (11): 1050–4. Bibcode:2014НатМа..13.1050С. Дои:10.1038 / nmat4069. PMID 25218060.
- ^ Кнунянц, И.Л., изд. (1998). «Цезий». Химическая энциклопедия (Химическая энциклопедия). 5. Москва: Советская энциклопедия. С. 654–656. ISBN 978-5-85270-310-1.
- ^ Плюшев, с. 210–211.
- ^ Плюшев, п. 206
- ^ а б c «Цезий и соединения цезия». Энциклопедия химической технологии Кирка-Отмера. 5 (4-е изд.). Нью-Йорк: Джон Вили и сыновья. 1994. С. 375–376.
- ^ Плсюшев, с. 357–358.
- ^ а б c d е ж Бик, Манфред и Принц, Хорст (2002) «Цезий и соединения цезия» в Энциклопедия промышленной химии Ульмана, Wiley-VCH, Weinheim. Vol. A6, стр. 153–156. Дои:10.1002 / 14356007.a06_153
- ^ Халка М .; Нордстром Б. (2010). Щелочные и щелочноземельные металлы. Публикация информационной базы. п. 52. ISBN 978-0-8160-7369-6.
- ^ Энрике Лима «Цезий: радионуклид» в Энциклопедии неорганической химии, 2006, Wiley-VCH, Weinheim. Дои:10.1002 / 0470862106.ia712
- ^ а б Национальный исследовательский совет (США). Комитет по использованию и замене источников излучения; Совет по ядерным и радиационным исследованиям (январь 2008 г.). Использование и замена источников излучения: сокращенная версия. Национальная академия прессы. С. 28–. ISBN 978-0-309-11014-3.CS1 maint: несколько имен: список авторов (ссылка на сайт)
- ^ Хакспилл, М. Л. (1905). "Sur une nouvelle preapratíon du rubidium et du cæsium". Comptes Rendus Hebdomadaires des Séances de l'Académie des Sciences (На французском). 141: 106.
- ^ Плюшев, п. 90
- ^ Kano T .; Кумано Т .; Маруока К. (2009). «Повышение скорости добавления конъюгатов, катализируемых фазовым переносом, с помощью CsCl». Органические буквы. 11 (9): 2023–2025. Дои:10.1021 / ol900476e. PMID 19348469.
- ^ Катрицкий А. Р.; Meth-Cohn O .; Rees Ch. W. (1995). Гилкрист, Т. Л. (ред.). Синтез: углерод с тремя или четырьмя присоединенными гетероатомами. Комплексные органические трансформации функциональных групп. 6 (Первое изд.). Нью-Йорк: Эльзевир. п.283. ISBN 978-0-08-040604-6.
- ^ ГОСТ 52407-2005. Вода питьевая. Методы определения жесткости. Москва: Стандартинформ. 2006 г.
- ^ «Хлорид цезия». Дополнительная и альтернативная медицина: травы, витамины и минералы. Американское онкологическое общество. 30 ноября 2008 г.. Получено 2011-05-13.
- ^ «FDA предупреждает медицинских работников о значительных рисках безопасности, связанных с хлоридом цезия». Управление по контролю за продуктами и лекарствами. 23 июля 2018.
- ^ «FDA занесло в черный список хлорид цезия, неэффективное и опасное лечение натуропатического рака». Научная медицина. 2 августа 2018 г.
- ^ а б Цезий. Сводные данные о минеральном сырье, январь 2010 г. Геологическая служба США.
- ^ Карреа-младший; Глисон, G; Шоу, Дж; Кронц, В (1964). «Прямая диагностика инфаркта миокарда с помощью фотосканирования после введения цезия-131» (PDF). Американский журнал сердца. 68 (5): 627–36. Дои:10.1016/0002-8703(64)90271-6. HDL:2027.42/32170. PMID 14222401.
- ^ МакГихан, Джон Т. (1968). «Фотосканирование с цезием 131: помощь в диагностике инфаркта миокарда». JAMA: Журнал Американской медицинской ассоциации. 204 (7): 585. Дои:10.1001 / jama.1968.03140200025006. PMID 5694480.
- ^ Тверьянович, Ю. С .; и другие. (1998). «Оптическое поглощение и состав ближайшего окружения неодима в стеклах на основе системы галлий-германий-халькоген». Glass Phys. Chem. 24: 446.
- ^ Кленовский, М.С .; Кельман, В.А .; Жменяк, Ю.В .; Шпеник, Ю.О. (2010). «Электроразрядный источник УФ-излучения на основе парогазовой смеси Xe-CsCl». Техническая физика. 55 (5): 709–714. Bibcode:2010JTePh..55..709K. Дои:10.1134 / S1063784210050178. S2CID 120781022.
- ^ Кленовский, М.С .; Кельман, В.А .; Жменяк, Ю.В .; Шпеник, Ю.О. (2013). «Люминесценция эксиплексных молекул XeCl * и XeBr *, инициированная продольным импульсным разрядом в трехкомпонентной смеси Xe с парами CsCl и CsBr». Оптика и спектроскопия. 114 (2): 197–204. Bibcode:2013OptSp.114..197K. Дои:10.1134 / S0030400X13010141. S2CID 123684289.
- ^ "Тугоплавкие и химически активные металлы". Мигатроник. Получено 2011-02-24.
- ^ Моррис, гл. Г., изд. (1992). «Хлорид цезия». Словарь академической прессы по науке и технологиям. Сан-Диего: Academic Press. п.395. ISBN 978-0-12-200400-1.
- ^ а б «Паспорт безопасности хлорида цезия» (PDF). Цезиевые чистые химикаты. Cabot Corporation. Получено 2011-04-11.
- ^ Kogel, J. E .; Триведи, Н. С .; Баркер, Дж. М., ред. (2006). Промышленные полезные ископаемые и горные породы: сырьевые товары, рынки и использование (7-е изд.). Литтлтон: Общество горного дела, металлургии и разведки. п. 1430. ISBN 978-0-87335-233-8.
- ^ Биль, Мартин; Кристиан Валь-Шотт; Стилианос Михалакис; Сянган Цзун (2009). «Катионные каналы, активируемые гиперполяризацией: от генов к функциям». Физиологические обзоры. 89 (3): 847–85. Дои:10.1152 / Physrev.00029.2008. PMID 19584315. S2CID 8090694.
- ^ «Данные химической безопасности: хлорид цезия». Практический научный (H-Sci) проект: База данных по химической безопасности. Лаборатория физической и теоретической химии Оксфордского университета. Получено 2011-04-08.
- ^ «Данные по безопасности хлорида цезия». Информация о химической и другой безопасности. Лаборатория физической и теоретической химии Оксфордского университета. Получено 2011-04-08.
- ^ Лазарев Н.В., Гадаскина И.Д. / Под ред. (1977). Вредные вещества в промышленности. Справочник для химиков, инженеров и врачей (на русском). 3 (7-е изд.). Санкт-Петербург: Химия. С. 328–329.
- ^ Мельников, П; Занони, Л.З. (июнь 2010 г.). «Клинические эффекты от приема цезия». Биологические исследования микроэлементов. 135 (1–3): 1–9. Дои:10.1007 / s12011-009-8486-7. PMID 19655100. S2CID 19186683.
- ^ Радиологическая авария в Гоянии. Вена: МАГАТЭ. 1988. ISBN 978-92-0-129088-5.. Резюме см. На стр. 1–6 и на стр. 22 для описания источника
- ^ Худшие ядерные катастрофы, Журнал Тайм
Библиография
- Хейнс, Уильям М., изд. (2011). CRC Справочник по химии и физике (92-е изд.). Бока-Ратон, Флорида: CRC Press. ISBN 1439855110.
- Лидин, Р. А; Андреева, Л.Л .; Молочко В. А. (2006). Константы неорганических веществ: справочник (Неорганические соединения: справочник). Москва. ISBN 978-5-7107-8085-5.
- Плюшев, В. Э .; Степин Б. Д. (1970). Химия и техтестнология соединений лития, рубидия и цезия (на русском). Москва: Химия.

![{ Displaystyle { ce {CsCl + ICl3 -> Cs [ICl4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6b106856bd4fcba7764e52dc61de8ec0049b4a3e)
![{ displaystyle { ce {Cs [ICl2]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/179cfcb1c479f90128c3ac48e2906b3f844d8781)
![{ displaystyle { ce {Cs [ICl4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7ae265895d0004997e064fbc7fa581ef0db7a2c4)
![{ displaystyle { ce {Cs [ICl2] -> {CsCl} + ICl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7824fed40e3efe7816a0e91633974ab54eb1aa87)
![{ displaystyle overbrace { ce {CH2 = CHCOOCH3}} ^ { text {Метилакрилат}} + { ce {ArCH = N-CH (CH3) -COOC (CH3) 3 -> [{ ce {TBAB , CsCl, K2CO3}}] [{ ce {CPME, 0 ^ { circ} C}}] {ArCH = NC (C2H4COOCH3) (CH3) -COOC (CH3) 3}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5f20c83eb7669c6266c0cc534608d0b13cef0f5a)
![{ displaystyle overbrace {{ ce {C (NO2) 4}}} ^ { text {тетранитрометан}} + { ce {CsCl -> [{ ce {DMF}}] {C (NO2) 3Cl} + CsNO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ddc9c983cd359a8ffceb4f8aeb9a0aa392b3f0da)
![{ Displaystyle { ce {Cs [SbI4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/78c190f0fcfde2966d052ab2d73b0e938953df43)
![{ Displaystyle { ce {Cs2 [SbI5]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1eb7ac284505510c341e93e2c1743311fb4e25b6)
![{ displaystyle { ce {Cs [TlI4]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/d3c1830f454449a2bcdcf18f352984bf51997de0)