Нуклеосома - Nucleosome

А нуклеосома является основной структурной единицей ДНК упаковка в эукариоты. Структура нуклеосомы состоит из сегмента ДНК, намотанного на восемь частей. гистоновые белки[1] и напоминает нить, намотанную на катушку. Нуклеосома является основной субъединицей хроматин. Каждая нуклеосома состоит из немногим менее двух витков ДНК, обернутых вокруг набора из восьми белков, называемых гистонами, которые известны как октамер гистонов. Каждый октамер гистонов состоит из двух копий каждого гистонового белка. H2A, H2B, H3, и H4.
ДНК должна быть уплотнена в нуклеосомы, чтобы соответствовать ядро клетки.[2] Помимо обертывания нуклеосом, эукариотические хроматин далее уплотняется, складываясь в ряд более сложных структур, в конечном итоге формируя хромосома. Каждая клетка человека содержит около 30 миллионов нуклеосом.[3]
Считается, что нуклеосомы несут эпигенетически унаследованная информация в виде ковалентные модификации их ядра гистоны. Положения нуклеосом в геноме не случайны, и важно знать, где находится каждая нуклеосома, потому что это определяет доступность ДНК для регуляторные белки.[4]
Впервые нуклеосомы были обнаружены как частицы в электронном микроскопе Доном и Адой Олинс в 1974 году.[5] и их существование и структура (в виде октамеров гистонов, окруженных приблизительно 200 парами оснований ДНК) были предложены Роджер Корнберг.[6][7] Роль нуклеосомы как общего репрессора генов была продемонстрирована Lorch et al. in vitro,[8] и Хан и Грюнштейн in vivo в 1987 и 1988 годах соответственно.[9]
Частица ядра нуклеосомы состоит примерно из 146 пар оснований (бп) из ДНК[10] завернутый в 1,67 левый сверхспиральные повороты вокруг гистон октамер, состоящий из 2 копий каждого из ядерных гистонов H2A, H2B, H3, и H4.[11] Частицы ядра связаны отрезками линкер ДНК, который может составлять до 80 п.н. Технически нуклеосома определяется как коровая частица плюс одна из этих линкерных областей; однако это слово часто является синонимом основной частицы.[12] Карты позиционирования нуклеосом по всему геному теперь доступны для многих модельных организмов, включая печень и мозг мышей.[13]
Гистоны-линкеры, такие как H1 и его изоформы участвуют в уплотнении хроматина и сидят в основании нуклеосомы рядом с входом и выходом ДНК, связываясь с линкерной областью ДНК.[14] Неконденсированные нуклеосомы без линкерного гистона напоминают «бусинки на нити ДНК» под электронный микроскоп.[15]
В отличие от большинства эукариотических клеток, зрелые сперматозоиды в основном используют протамины чтобы упаковать свою геномную ДНК, скорее всего, для достижения еще более высокого коэффициента упаковки.[16] Эквиваленты гистонов и упрощенная структура хроматина также были обнаружены в Археи,[17] предполагая, что эукариоты - не единственные организмы, использующие нуклеосомы.
Структура
Структура ядерной частицы

Обзор
Пионерские структурные исследования в 1980-х годах, проведенные группой Аарона Клуга, предоставили первые доказательства того, что октамер гистоновых белков оборачивает ДНК вокруг себя примерно на 1,7 витка левой суперспирали.[18] В 1997 г. был выпущен первый аппарат с разрешением около атома Кристальная структура нуклеосомы была решена группой Ричмонда, показав наиболее важные детали частицы. Человек альфа-спутник палиндромная ДНК критически важный для достижения кристаллической структуры нуклеосом 1997 года был разработан группой Буника в Национальной лаборатории Ок-Ридж в Теннесси.[19][20][21][22][23] На сегодняшний день решены структуры более 20 различных ядер нуклеосомных частиц,[24] включая те, которые содержат варианты гистонов и гистоны разных видов. Структура ядерной частицы нуклеосомы заметно сохраняется, и даже замена более чем на 100 остатков между гистонами лягушки и дрожжей приводит к картам электронной плотности с общим среднеквадратичное отклонение всего 1,6Å.[25]
Частица ядра нуклеосомы (NCP)
Частица ядра нуклеосомы (показанная на рисунке) состоит примерно из 146 базовая пара ДНК[10] завернутый в 1,67 левый сверхспиральные повороты вокруг октамер гистонов, состоящий из 2 копий каждого из ядерных гистонов H2A, H2B, H3, и H4. Соседние нуклеосомы соединены отрезком свободной ДНК, называемым линкер ДНК (длина которого варьируется от 10 до 80 п.н. в зависимости от вида и типа ткани[17]Вся структура образует цилиндр диаметром 11 нм и высотой 5,5 нм.
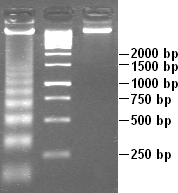

Частицы ядра нуклеосомы наблюдаются, когда хроматин в интерфазе обрабатывают, чтобы заставить хроматин частично разворачиваться. Полученное изображение, полученное с помощью электронного микроскопа, представляет собой «бусинки на нитке». Нить - это ДНК, а каждая бусинка в нуклеосоме - это центральная частица. Частица ядра нуклеосомы состоит из ДНК и гистоновых белков.[29]
Частичное ДНКаза переваривание хроматин раскрывает его нуклеосомную структуру. Поскольку участки ДНК ядер нуклеосомных частиц менее доступны для ДНКазы, чем связывающие участки, ДНК расщепляется на фрагменты, длина которых равна кратности расстояния между нуклеосомами (180, 360, 540 пар оснований и т. Д.). Отсюда очень характерный узор похож на лестницу виден во время гель-электрофорез этой ДНК.[26] Такое пищеварение может происходить и в естественных условиях во время апоптоз («клеточное самоубийство» или запрограммированная смерть клетки), потому что автодеструкция ДНК обычно это его роль.
Белковые взаимодействия внутри нуклеосомы
Основные гистоновые белки содержат характерный структурный мотив, называемый «гистоновая складка», который состоит из трех альфа-спиралей (α1-3), разделенных двумя петлями (L1-2). В растворе гистоны образуют гетеродимеры H2A-H2B и гетеротетрамеры H3-H4. Гистоны димеризуются вокруг своих длинных α2-спиралей в антипараллельной ориентации, и в случае H3 и H4 два таких димера образуют 4-спиральный пучок, стабилизированный обширным взаимодействием H3-H3 '. Димер H2A / H2B связывается с тетрамером H3 / H4 за счет взаимодействий между H4 и H2B, которые включают образование гидрофобного кластера.[11] Октамер гистонов образован центральным тетрамером H3 / H4, зажатым между двумя димерами H2A / H2B. Из-за высокого основного заряда всех четырех ядер гистонов октамер гистонов стабилен только в присутствии ДНК или очень высоких концентраций соли.
Гистон - взаимодействия ДНК
Нуклеосома содержит более 120 прямых взаимодействий белок-ДНК и несколько сотен опосредованных водой.[30] Прямые взаимодействия белок-ДНК не распределяются равномерно по поверхности октамера, а скорее расположены в дискретных участках. Это связано с образованием двух типов сайтов связывания ДНК внутри октамера; сайт α1α1, который использует спираль α1 из двух соседних гистонов, и сайт L1L2, образованный петлями L1 и L2. Соль ссылки и водородная связь между основными и гидроксильными группами боковых цепей и амидами основной цепи с фосфатами основной цепи ДНК образуют основную часть взаимодействий с ДНК. Это важно, учитывая, что повсеместное распределение нуклеосом по геномам требует, чтобы он был неспецифическим для последовательности ДНК-связывающим фактором. Хотя нуклеосомы, как правило, предпочитают одни последовательности ДНК другим,[31] они способны связываться практически с любой последовательностью, что, как полагают, связано с гибкостью в образовании этих опосредованных водой взаимодействий. Кроме того, между боковыми цепями белка и дезоксирибозными группами осуществляются неполярные взаимодействия, и боковая цепь аргинина внедряется в малую бороздку ДНК во всех 14 участках, где она обращена к поверхности октамера. Распределение и сила связывания ДНК. участки на поверхности октамера искажают ДНК в ядре нуклеосомы. ДНК неравномерно изогнута и также содержит дефекты скручивания. Скручивание свободной B-формы ДНК в растворе составляет 10,5 п.н. за оборот. Однако общий поворот нуклеосомной ДНК составляет всего 10,2 п.н. на оборот, варьируя от 9,4 до 10,9 п.н. на оборот.
Гистоновые хвостовые домены
Удлинения гистоновых хвостов составляют до 30% по массе гистонов, но не видны в кристаллических структурах нуклеосом из-за их высокой внутренней гибкости и, как полагают, в значительной степени неструктурированы.[32] N-концевые хвосты гистонов H3 и H2B проходят через канал, образованный малыми бороздками двух нитей ДНК, выступающими из ДНК каждые 20 п.н. В N-концевой хвост гистона H4, с другой стороны, имеет область высокоосновных аминокислот (16-25), которая в кристаллической структуре образует взаимодействие с высококислотной областью поверхности димера H2A-H2B другой нуклеосомы, потенциально значимы для структуры нуклеосом более высокого порядка. Считается, что это взаимодействие происходит и в физиологических условиях, и это предполагает, что ацетилирование хвоста H4 искажает структуру хроматина высшего порядка.
Структура высшего порядка

Организация ДНК, которая достигается нуклеосомой, не может полностью объяснить упаковку ДНК, наблюдаемую в ядре клетки. Дальнейшее уплотнение хроматин в ядро клетки необходимо, но еще недостаточно изучено. Текущее понимание[24] заключается в том, что повторяющиеся нуклеосомы с промежуточной «линкерной» ДНК образуют 10-нм волокно, описываются как «бусинки на нитке» и имеют коэффициент упаковки примерно от пяти до десяти.[17] Цепочка нуклеосом может быть расположена в виде 30 нм волокно, уплотненная конструкция с коэффициентом упаковки ~ 50[17] и чье образование зависит от наличия Гистон H1.
Кристаллическая структура тетрануклеосомы была представлена и использована для создания предложенной структуры 30-нм волокна в виде двухзаходной спирали.[33]В отношении этой модели все еще существуют определенные споры, поскольку она несовместима с недавними электронная микроскопия данные.[34] Помимо этого, структура хроматина плохо изучена, но классически предполагается, что 30-нм волокно расположено в виде петель вдоль центрального белкового каркаса с образованием транскрипционно активных эухроматин. Дальнейшее уплотнение приводит к транскрипционно неактивному гетерохроматин.
Динамика
Хотя нуклеосома представляет собой очень стабильный комплекс белок-ДНК, он не статичен и, как было показано, претерпевает ряд различных структурных перестроек, включая скольжение нуклеосом и экспонирование участков ДНК. В зависимости от контекста нуклеосомы могут ингибировать или облегчать связывание фактора транскрипции. Положения нуклеосом контролируются тремя основными факторами: во-первых, внутреннее сродство связывания гистонового октамера зависит от последовательности ДНК. Во-вторых, нуклеосома может вытесняться или рекрутироваться за счет конкурентного или кооперативного связывания других белковых факторов. В-третьих, нуклеосома может активно перемещаться с помощью АТФ-зависимых ремоделирующих комплексов.[35]
Скольжение нуклеосом
Работа, выполненная в лаборатории Брэдбери, показала, что нуклеосомы, воссозданные на позиционной последовательности 5S ДНК, способны репозиционировать себя трансляционно на соседние последовательности при термической инкубации.[36] Более поздняя работа показала, что это изменение положения не требует разрушения октамера гистонов, но согласуется с тем, что нуклеосомы могут «скользить» по ДНК. в снг. В 2008 году выяснилось, что CTCF сайты связывания действуют как якоря позиционирования нуклеосом, так что при использовании для выравнивания различных геномных сигналов можно легко идентифицировать множественные фланкирующие нуклеосомы.[37] Хотя нуклеосомы по своей природе подвижны, эукариоты развили большое семейство АТФ-зависимых ферментов ремоделирования хроматина для изменения структуры хроматина, многие из которых делают это посредством скольжения нуклеосом. В 2012 году лаборатория Бины Пиллаи продемонстрировала, что скольжение нуклеосом является одним из возможных механизмов крупномасштабной тканеспецифичной экспрессии генов. Работа показывает, что сайт начала транскрипции для генов, экспрессируемых в конкретной ткани, истощены, в то время как тот же набор генов в другой ткани, где они не экспрессируются, связаны с нуклеосомами.[13]
Обнаружение участка ДНК
Работа лаборатории Widom показала, что нуклеосомная ДНК находится в равновесии между завернутым и развернутым состояниями. Измерения этих скоростей с использованием разрешенных по времени FRET показали, что ДНК внутри нуклеосомы остается полностью обернутой всего лишь 250 мс, после чего она разворачивается на 10-50 мс и затем быстро перематывается.[38] Это означает, что ДНК не нужно активно диссоциировать от нуклеосомы, но есть значительная часть времени, в течение которой она полностью доступна. В самом деле, это можно распространить на наблюдение, что введение ДНК-связывающей последовательности в нуклеосому увеличивает доступность соседних участков ДНК при связывании.[39] Эта склонность ДНК в нуклеосоме «дышать» имеет важные функциональные последствия для всех ДНК-связывающих белков, которые действуют в среде хроматина.[38] В частности, динамическое дыхание нуклеосом играет важную роль в ограничении продвижения РНК-полимераза II во время удлинения транскрипции.[40]
Свободная от нуклеосом область
Промоторы активных генов имеют участки, свободные от нуклеосом (NFR). Это обеспечивает доступность промоторной ДНК для различных белков, таких как факторы транскрипции. Свободная от нуклеосом область обычно охватывает 200 нуклеотидов в S. cerevisae[41] Правильно расположенные нуклеосомы образуют границы NFR. Эти нуклеосомы называются + 1-нуклеосомой и -1-нуклеосомой и расположены на канонических расстояниях ниже и выше, соответственно, от сайта начала транскрипции.[42] + 1-нуклеосома и несколько нижестоящих нуклеосом также имеют тенденцию включать вариант гистона H2A.Z.[42]
Модуляция структуры нуклеосом
Геномы эукариот повсеместно связаны с хроматином; однако клетки д. пространственно и временно регулировать специфические локусы независимо от основной массы хроматина. Для достижения высокого уровня контроля, необходимого для координации ядерных процессов, таких как репликация, репарация и транскрипция ДНК, клетки разработали множество средств для локальной и специфической модуляции структуры и функции хроматина. Это может включать ковалентную модификацию гистонов, включение вариантов гистонов и нековалентное ремоделирование с помощью АТФ-зависимых ферментов ремоделирования.
Посттрансляционные модификации гистонов
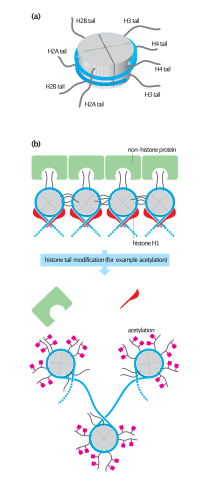
С тех пор как они были открыты в середине 1960-х, было предсказано, что модификации гистонов влияют на транскрипцию.[43] Тот факт, что большинство обнаруженных ранних посттрансляционных модификаций было сосредоточено внутри удлинений хвостов, которые выступают из ядра нуклеосомы, приводит к двум основным теориям относительно механизма модификации гистонов. Первая из теорий предполагала, что они могут влиять на электростатические взаимодействия между хвостами гистонов и ДНК, чтобы «ослабить» структуру хроматина. Позже было высказано предположение, что комбинации этих модификаций могут создавать связывающие эпитопы, с помощью которых можно привлекать другие белки.[44] Недавно, учитывая, что в структурированных областях гистонов было обнаружено больше модификаций, было выдвинуто предположение, что эти модификации могут влиять на гистоновую ДНК.[45] и гистон-гистон[46] взаимодействия внутри ядра нуклеосомы. Предполагается, что модификации (такие как ацетилирование или фосфорилирование), которые понижают заряд ядра глобулярного гистона, «ослабят» ассоциацию ядра-ДНК; сила эффекта зависит от расположения модификации в ядре.[47]Было показано, что некоторые модификации коррелируют с подавлением генов; другие, кажется, коррелируют с активацией генов. Общие модификации включают ацетилирование, метилирование, или же убиквитинирование из лизин; метилирование из аргинин; и фосфорилирование из серин. Информация, хранящаяся таким образом, считается эпигенетический, поскольку он не закодирован в ДНК, но по-прежнему передается дочерним клеткам. Поддержание репрессированного или активированного статуса гена часто необходимо для клеточная дифференциация.[17]
Варианты гистонов
Хотя гистоны в значительной степени консервативны на протяжении всей эволюции, было идентифицировано несколько вариантных форм. Эта диверсификация функции гистонов ограничена H2A и H3, причем H2B и H4 в основном инвариантны. H2A можно заменить на H2AZ (что приводит к снижению стабильности нуклеосом) или H2AX (что связано с репарацией ДНК и Т-клетка дифференциация), тогда как неактивные Х-хромосомы у млекопитающих обогащены macroH2A. H3 может быть заменен на H3.3 (который коррелирует с активирующими генами и регуляторными элементами), а в центромеры H3 заменяется на CENPA.[17]
АТФ-зависимое ремоделирование нуклеосом
С этим термином связан ряд различных реакций АТФ-зависимое ремоделирование хроматина. Было показано, что ферменты ремоделирования скользят по нуклеосомам по ДНК,[48] нарушают контакты гистонов с ДНК до степени дестабилизации димера H2A / H2B[49][50] и для создания отрицательного суперспирального кручения в ДНК и хроматине.[51] Недавно было показано, что фермент ремоделирования Swr1 вводит вариантный гистон H2A.Z в нуклеосомы.[52] В настоящее время неясно, представляют ли все они отдельные реакции или просто альтернативные результаты общего механизма. Что общего у всех, и это действительно отличительный признак АТФ-зависимого ремоделирования хроматина, так это то, что все они приводят к изменению доступности ДНК.
Исследования по активации генов in vivo[53] и, что еще более удивительно, реконструкция in vitro[54] показали, что события ремоделирования хроматина и связывания транскрипционных факторов имеют циклический и периодический характер. Хотя последствия этого для механизма реакции ремоделирования хроматина неизвестны, динамический характер системы может позволить ей быстрее реагировать на внешние стимулы. Недавнее исследование показывает, что положения нуклеосом значительно меняются во время развития эмбриональных стволовых клеток мыши, и эти изменения связаны со связыванием онтогенетических факторов транскрипции.[55]
Динамическое ремоделирование нуклеосом в геноме дрожжей
Исследования 2007 года каталогизировали положения нуклеосом в дрожжах и показали, что нуклеосомы обеднены промоутер регионы и истоки репликации.[56][57][58]Около 80% генома дрожжей покрыто нуклеосомами.[59] и паттерн расположения нуклеосом явно относится к участкам ДНК, которые регулируют транскрипция, области, которые транскрибируются, и области, которые инициируют репликацию ДНК.[60] Совсем недавно новое исследование изучило динамические изменения в репозиционировании нуклеосом во время глобального события репрограммирования транскрипции, чтобы выяснить влияние на смещение нуклеосом во время полногеномных изменений транскрипции у дрожжей (Saccharomyces cerevisiae ).[61] Результаты показали, что нуклеосомы, локализованные в промоторных областях, смещаются в ответ на стресс (например, тепловой удар ). Кроме того, удаление нуклеосом обычно соответствует активации транскрипции, а замена нуклеосом обычно соответствует репрессии транскрипции, предположительно потому, что фактор транскрипции сайты связывания стали более-менее доступны соответственно. В общем, только одна или две нуклеосомы были репозиционированы на промоторе, чтобы вызвать эти транскрипционные изменения. Однако даже в хромосомных областях, которые не были связаны с изменениями транскрипции, наблюдали репозиционирование нуклеосом, предполагая, что покрытие и раскрытие транскрипционной ДНК не обязательно вызывает событие транскрипции. После транскрипции область рДНК должна быть защищена от любого повреждения, это предполагает, что белки HMGB играют важную роль в защите области, свободной от нуклеосом.[62][63]
Сборка нуклеосом in vitro
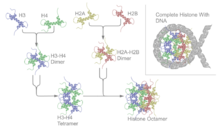
Нуклеосомы можно собирать in vitro либо с использованием очищенных нативных, либо рекомбинантных гистонов.[64][65] Один из стандартных методов загрузки ДНК вокруг гистонов включает использование соли. диализ. Реакция, состоящая из октамеров гистонов и голой матрицы ДНК, может быть инкубирована вместе при концентрации соли 2 М. Постепенно уменьшая концентрацию соли, ДНК уравновесится до положения, в котором она оборачивается вокруг октамеров гистонов, образуя нуклеосомы. В соответствующих условиях этот процесс восстановления позволяет экспериментально картировать сродство нуклеосомного позиционирования данной последовательности.[66]
Дисульфидно-сшитые ядерные частицы нуклеосом
Недавний прогресс в производстве ядер нуклеосомных частиц с повышенной стабильностью включает сайт-специфичные дисульфид сшивки.[67] В ядерную частицу нуклеосомы можно ввести две разные поперечные связи. Первый сшивает две копии H2A через введенный цистеин (N38C), что приводит к октамер гистонов который устойчив к потере димера H2A / H2B во время восстановления нуклеосом. Вторая перекрестная связь может быть введена между N-концевым гистоновым хвостом H3 и концами нуклеосомной ДНК через встроенный конвертируемый нуклеотид.[68] Сшивка октамера ДНК-гистона стабилизирует ядерную частицу нуклеосомы против диссоциации ДНК при очень низких концентрациях частиц и при повышенных концентрациях соли.
Сборка нуклеосом in vivo

Нуклеосомы - это основная единица упаковки ДНК, построенная из гистоновых белков, вокруг которых спиралью ДНК. Они служат каркасом для формирования структуры хроматина более высокого порядка, а также для уровня регуляторного контроля экспрессии генов. Нуклеосомы быстро собираются на вновь синтезированной ДНК позади репликационной вилки.
H3 и H4
Гистоны H3 и H4 из разобранных старых нуклеосом хранятся поблизости и случайным образом распределяются по вновь синтезированной ДНК.[69] Они собираются комплексом фактора сборки хроматина-1 (CAF-1), который состоит из трех субъединиц (p150, p60 и p48).[70] Недавно синтезированные H3 и H4 собираются с помощью фактора сборки сцепления репликации (RCAF). RCAF содержит субъединицу Asf1, которая связывается с вновь синтезированными белками H3 и H4.[71] Старые белки H3 и H4 сохраняют свои химические модификации, что способствует передаче эпигенетической сигнатуры. Вновь синтезированные белки H3 и H4 постепенно ацетилируются по различным остаткам лизина как часть процесса созревания хроматина.[72] Также считается, что старые белки H3 и H4 в новых нуклеосомах привлекают модифицирующие гистоны ферменты, которые маркируют новые гистоны, способствуя эпигенетической памяти.
H2A и H2B
В отличие от старых H3 и H4, старые H2A и H2B гистоновые белки высвобождаются и разрушаются; следовательно, недавно собранные белки H2A и H2B включаются в новые нуклеосомы.[73] H2A и H2B собираются в димеры, которые затем загружаются в нуклеосомы с помощью белка сборки нуклеосом-1 (NAP-1), который также способствует скольжению нуклеосом.[74] Нуклеосомы также разделены АТФ-зависимыми нуклеосомными ремоделирующими комплексами, содержащими ферменты, такие как Isw1 Ino80 и Chd1, и впоследствии собираются в структуру более высокого порядка.[75][76]
Галерея
Кристаллическая структура ядерной частицы нуклеосомы (PDB: 1EQZ[27][28]) - различные виды, показывающие детали складывания и организации гистонов. Гистоны H2A, H2B, H3, H4 и ДНК окрашены.
Смотрите также
Рекомендации
- ^ Рис Дж, Кэмпбелл Н. (2006). Биология. Сан-Франциско: Бенджамин Каммингс. ISBN 978-0-8053-6624-2.
- ^ Альбертс Б. (2002). Молекулярная биология клетки (4-е изд.). Нью-Йорк: Наука Гарланд. п. 207. ISBN 978-0-8153-4072-0.
- ^ Хромосомная ДНК и ее упаковка в хроматиновом волокне.
- ^ Тейф В.Б., Кларксон СТ (2019). «Нуклеосомное позиционирование». Энциклопедия биоинформатики и вычислительной биологии. 2: 308–317. Дои:10.1016 / B978-0-12-809633-8.20242-2. ISBN 9780128114322.
- ^ Олинс А.Л., Олинс Д.Е. (январь 1974 г.). «Сфероидные хроматиновые единицы (v-тельца)». Наука. 183 (4122): 330–2. Bibcode:1974Научный ... 183..330O. Дои:10.1126 / science.183.4122.330. PMID 4128918. S2CID 83480762.
- ^ Макдональд Д (декабрь 2005 г.). "Этап 9, (1973-1974) Гипотеза нуклеосом: альтернативная теория струн". Вехи природы: экспрессия генов. Дои:10.1038 / nrm1798.
- ^ Корнберг Р.Д. (май 1974 г.). «Структура хроматина: повторяющаяся единица гистонов и ДНК». Наука. 184 (4139): 868–71. Bibcode:1974Наука ... 184..868K. Дои:10.1126 / science.184.4139.868. PMID 4825889.
- ^ Lorch Y, LaPointe JW, Kornberg RD (апрель 1987 г.). «Нуклеосомы подавляют начало транскрипции, но допускают удлинение цепи со смещением гистонов». Клетка. 49 (2): 203–10. Дои:10.1016/0092-8674(87)90561-7. PMID 3568125. S2CID 21270171.
- ^ Хан М, Грюнштейн М (1988). «Потеря нуклеосом активирует последующие промоторы дрожжей in vivo». Клетка. 55 (6): 1137–45. Дои:10.1016/0092-8674(88)90258-9. PMID 2849508. S2CID 41520634.
- ^ а б В разных кристаллах наблюдались значения 146 и 147 пар оснований.
- ^ а б Люгер К., Мэдер А.В., Ричмонд Р.К., Сарджент Д.Ф., Ричмонд Т.Дж. (сентябрь 1997 г.). «Кристаллическая структура ядерной частицы нуклеосомы при разрешении 2,8 A». Природа. 389 (6648): 251–60. Bibcode:1997Натура.389..251Л. Дои:10.1038/38444. PMID 9305837. S2CID 4328827.
- ^ Альбертс Б. (2007). Молекулярная биология клетки (5-е изд.). Нью-Йорк: Наука Гарланд. п. 211. ISBN 978-0-8153-4106-2.
- ^ а б Баргадже Р., Алам М.П., Патовари А., Саркар М., Али Т., Гупта С., Гарг М., Сингх М., Пурканти Р., Скария В., Сивасуббу С., Брахмачари В., Пиллай Б. (октябрь 2012 г.). «Близость нуклеосомы, содержащей H2A.Z, к сайту начала транскрипции влияет на уровни экспрессии генов в печени и мозге млекопитающих». Исследования нуклеиновых кислот. 40 (18): 8965–78. Дои:10.1093 / нар / гкс665. ЧВК 3467062. PMID 22821566.
- ^ Чжоу Ю.Б., Герхман С.Е., Рамакришнан В., Траверс А., Мюлдерманс С. (сентябрь 1998 г.). «Положение и ориентация глобулярного домена линкерного гистона H5 на нуклеосоме». Природа. 395 (6700): 402–5. Bibcode:1998Натура.395..402Z. Дои:10.1038/26521. PMID 9759733. S2CID 204997317.
- ^ Тома Ф., Коллер Т., Клуг А. (ноябрь 1979 г.). «Участие гистона H1 в организации нуклеосомы и солевой надстройки хроматина». Журнал клеточной биологии. 83 (2, ч. 1): 403–27. Дои:10.1083 / jcb.83.2.403. ЧВК 2111545. PMID 387806.
- ^ Кларк HJ (1992). «Ядерный и хроматиновый состав гамет и ранних эмбрионов млекопитающих». Биохимия и клеточная биология. 70 (10–11): 856–66. Дои:10.1139 / o92-134. PMID 1297351.
- ^ а б c d е ж Felsenfeld G, Groudine M (январь 2003 г.). «Управление двойной спиралью». Природа. 421 (6921): 448–53. Bibcode:2003Натура.421..448F. Дои:10.1038 / природа01411. PMID 12540921.
- ^ Структура ядерной частицы нуклеосомы при разрешении 7Å, Ричмонд, Т., Финч, Дж. Т., Раштон, Б., Родс, Д. и Клуг, А. (1984) Nature 311, 532-37
- ^ Харп Дж. М., Палмер Е. Л., Йорк М. Х., Гевис А., Дэвис М., Буник Дж. Дж. (Октябрь 1995 г.). «Препаративное разделение ядер нуклеосомных частиц, содержащих ДНК с определенной последовательностью, в нескольких фазах трансляции». Электрофорез. 16 (10): 1861–4. Дои:10.1002 / elps.11501601305. PMID 8586054.
- ^ Палмер Е.Л., Гевис А., Харп Дж. М., Йорк М. Х., Буник Г. Дж. (1995). «Масштабное производство фрагментов палиндромной ДНК». Аналитическая биохимия. 231 (1): 109–14. Дои:10.1006 / abio.1995.1509. PMID 8678288.
- ^ Харп Дж. М., Убербахер Э. К., Роберсон А. Э., Палмер Е. Л., Гевис А., Буник Г. Дж. (1996). «Рентгеноструктурный анализ кристаллов, содержащих двуосимметричные ядерные частицы нуклеосом». Acta Crystallographica Раздел D. 52 (Pt 2): 283–8. Дои:10.1107 / S0907444995009139. PMID 15299701.
- ^ Харп Дж. М., Хэнсон Б. Л., Тимм Д. Е., Буник Дж. Дж. (2000). «Асимметрии в ядерной частице нуклеосомы при разрешении 2,5 А». Acta Crystallographica Раздел D. 56 (Пт 12): 1513–34. Дои:10.1107 / s0907444900011847. PMID 11092917.
- ^ Хэнсон Б.Л., Александр С., Харп Дж. М., Буник Дж. Дж. (2004). «Приготовление и кристаллизация ядер нуклеосомной частицы». Методы в энзимологии. 375: 44–62. Дои:10.1016 / с0076-6879 (03) 75003-4. ISBN 9780121827793. PMID 14870658.
- ^ а б Chakravarthy S, Park YJ, Chodaparambil J, Edayathumangalam RS, Luger K (февраль 2005 г.). «Структура и динамические свойства ядер нуклеосомных частиц». Письма FEBS. 579 (4): 895–8. Дои:10.1016 / j.febslet.2004.11.030. PMID 15680970.
- ^ Белый CL, Суто РК, Люгер К. (сентябрь 2001 г.). «Структура ядра нуклеосомной частицы дрожжей показывает фундаментальные изменения межнуклеосомных взаимодействий». Журнал EMBO. 20 (18): 5207–18. Дои:10.1093 / emboj / 20.18.5207. ЧВК 125637. PMID 11566884.
- ^ а б Страйер Л. (1995). Биохимия (четвертое изд.). Нью-Йорк - Бейзингсток: В. Х. Фриман и компания. ISBN 978-0716720096.
- ^ а б Harp JM, Hanson BL, Timm DE, Bunick GJ (6 апреля 2000 г.). «Рентгеновская структура ядерной частицы нуклеосомы с разрешением 2,5 A». Банк данных белков RCSB (PDB). Дои:10.2210 / pdb1eqz / pdb. Идентификатор PDB: 1EQZ. Получено 8 октября 2012. Цитировать журнал требует
| журнал =(помощь) - ^ а б Harp JM, Hanson BL, Timm DE, Bunick GJ (декабрь 2000 г.). «Асимметрии в ядерной частице нуклеосомы при разрешении 2,5 А». Acta Crystallographica Раздел D. 56 (Пт 12): 1513–34. Дои:10.1107 / S0907444900011847. PMID 11092917. Идентификатор PDB: 1EQZ.
- ^ Альбертс, Брюс. Эссенциальная клеточная биология. 2-е изд. Нью-Йорк: Garland Science, 2009. Печать.
- ^ Дэйви К.А., Сарджент Д.Ф., Люгер К., Мейдер А.В., Ричмонд Т.Дж. (июнь 2002 г.). «Опосредованные растворителем взаимодействия в структуре ядерной частицы нуклеосомы с разрешением 1,9». Журнал молекулярной биологии. 319 (5): 1097–113. Дои:10.1016 / S0022-2836 (02) 00386-8. PMID 12079350.
- ^ Сегал Э., Фондуфе-Миттендорф Ю., Чен Л., Тострем А., Филд Y, Мур И.К., Ван Дж. П., Видом Дж. (Август 2006 г.). «Геномный код для позиционирования нуклеосом». Природа. 442 (7104): 772–8. Bibcode:2006Натура.442..772S. Дои:10.1038 / природа04979. ЧВК 2623244. PMID 16862119.
- ^ Чжэн С., Хейс Дж. Дж. (Апрель 2003 г.). «Структуры и взаимодействия основных гистоновых хвостовых доменов». Биополимеры. 68 (4): 539–46. Дои:10.1002 / bip.10303. PMID 12666178.
- ^ Шальч Т., Дуда С., Сарджент Д.Ф., Ричмонд Т.Дж. (июль 2005 г.). «Рентгеновская структура тетрануклеосомы и ее значение для волокна хроматина». Природа. 436 (7047): 138–41. Bibcode:2005Натура.436..138С. Дои:10.1038 / природа03686. PMID 16001076. S2CID 4387396.
- ^ Робинсон П.Дж., Файролл Л., Хюин В.А., Родс Д. (апрель 2006 г.). «ЭМ-измерения определяют размеры« 30-нм »хроматинового волокна: свидетельство компактной встречно-гребенчатой структуры». Труды Национальной академии наук Соединенных Штатов Америки. 103 (17): 6506–11. Bibcode:2006ПНАС..103.6506Р. Дои:10.1073 / pnas.0601212103. ЧВК 1436021. PMID 16617109.
- ^ Тейф В.Б., Риппе К. (сентябрь 2009 г.). «Прогнозирование положения нуклеосом на ДНК: сочетание предпочтений внутренней последовательности и активности ремоделиров». Исследования нуклеиновых кислот. 37 (17): 5641–55. Дои:10.1093 / нар / gkp610. ЧВК 2761276. PMID 19625488.
- ^ Пеннингс С., Мюлдерманс С., Мерсеман Г., Винс Л. (май 1989 г.). «Формирование, стабильность и позиционирование гистонов ядра нуклеосом, собранных на изогнутых и других нуклеосомных ДНК». Журнал молекулярной биологии. 207 (1): 183–92. Дои:10.1016 / 0022-2836 (89) 90449-Х. PMID 2738923.
- ^ Fu Y, Sinha M, Peterson CL, Weng Z (июль 2008 г.). Ван Стинсель Б. (ред.). «Белок, связывающий инсулятор, CTCF позиционирует 20 нуклеосом вокруг своих сайтов связывания в геноме человека». PLOS Genetics. 4 (7): e1000138. Дои:10.1371 / journal.pgen.1000138. ЧВК 2453330. PMID 18654629.
- ^ а б Ли Дж., Левитус М., Бустаманте С., Видом Дж. (Январь 2005 г.). «Быстрая спонтанная доступность нуклеосомной ДНК». Структурная и молекулярная биология природы. 12 (1): 46–53. Дои:10.1038 / nsmb869. PMID 15580276. S2CID 14540078.
- ^ Ли Дж., Уидом Дж. (Август 2004 г.). «Нуклеосомы облегчают собственное вторжение». Структурная и молекулярная биология природы. 11 (8): 763–9. Дои:10.1038 / nsmb801. PMID 15258568. S2CID 11299024.
- ^ Ходжес С., Бинту Л., Любковска Л., Кашлев М., Бустаманте С. (июль 2009 г.). «Нуклеосомные колебания определяют динамику транскрипции РНК-полимеразы II». Наука. 325 (5940): 626–8. Bibcode:2009Sci ... 325..626H. Дои:10.1126 / science.1172926. ЧВК 2775800. PMID 19644123.
- ^ Юань Г.К., Лю Ю.Дж., Дион М.Ф., Slack MD, Ву Л.Ф., Альтшулер С.Дж., Рандо О.Дж. (июль 2005 г.). "Геномная идентификация положений нуклеосом в S. cerevisiae". Наука. 309 (5734): 626–30. Bibcode:2005Наука ... 309..626л. Дои:10.1126 / наука.1112178. PMID 15961632. S2CID 43625066.
- ^ а б Лай В.К., Пью Б.Ф. (сентябрь 2017 г.). «Понимание динамики нуклеосом и их связи с экспрессией генов и репликацией ДНК». Обзоры природы Молекулярная клеточная биология. 18 (9): 548–562. Дои:10.1038 / nrm.2017.47. ЧВК 5831138. PMID 28537572.
- ^ Олфри В.Г., Фолкнер Р., Мирский А.Е. (май 1964 г.). «ацетилирование и метилирование гистонов и их возможная роль в регуляции синтеза РНК». Труды Национальной академии наук Соединенных Штатов Америки. 51 (5): 786–94. Bibcode:1964ПНАС ... 51..786А. Дои:10.1073 / пнас.51.5.786. ЧВК 300163. PMID 14172992.
- ^ Strahl BD, Allis CD (январь 2000 г.). «Язык ковалентных модификаций гистонов». Природа. 403 (6765): 41–5. Bibcode:2000Натура 403 ... 41С. Дои:10.1038/47412. PMID 10638745. S2CID 4418993.
- ^ Cosgrove MS, Boeke JD, Wolberger C (ноябрь 2004 г.). «Регулируемая подвижность нуклеосом и гистоновый код». Структурная и молекулярная биология природы. 11 (11): 1037–43. Дои:10.1038 / nsmb851. PMID 15523479. S2CID 34704745.
- ^ Йе Дж, Ай Х, Евгени Э., Чжан Л., Карпентер Л. Р., Елинек М. А., Фрейтас М. А., Партхун М. Р. (апрель 2005 г.). «Ацетилирование лизина 91 гистона H4, модификация основного домена, связанная со сборкой хроматина». Молекулярная клетка. 18 (1): 123–30. Дои:10.1016 / j.molcel.2005.02.031. ЧВК 2855496. PMID 15808514.
- ^ Фенли А.Т., Адамс Д.А., Онуфриев А.В. (сентябрь 2010 г.). «Зарядное состояние ядра глобулярного гистона контролирует стабильность нуклеосомы». Биофизический журнал. 99 (5): 1577–85. Bibcode:2010BpJ .... 99.1577F. Дои:10.1016 / j.bpj.2010.06.046. ЧВК 2931741. PMID 20816070.
- ^ Whitehouse I, Flaus A, Cairns BR, White MF, Workman JL, Owen-Hughes T (август 1999). «Мобилизация нуклеосом, катализируемая дрожжевым комплексом SWI / SNF». Природа. 400 (6746): 784–7. Bibcode:1999Натура 400..784Вт. Дои:10.1038/23506. PMID 10466730. S2CID 2841873.
- ^ Кассабов С.Р., Чжан Б., Персингер Дж., Варфоломей Б. (февраль 2003 г.). «SWI / SNF разворачивает, скользит и перематывает нуклеосомы». Молекулярная клетка. 11 (2): 391–403. Дои:10.1016 / S1097-2765 (03) 00039-X. PMID 12620227.
- ^ Бруно М., Флаус А., Стокдейл С., Ренкурель С., Феррейра Н., Оуэн-Хьюз Т. (декабрь 2003 г.). «Обмен димера гистона H2A / H2B с помощью АТФ-зависимой активности ремоделирования хроматина». Молекулярная клетка. 12 (6): 1599–606. Дои:10.1016 / S1097-2765 (03) 00499-4. ЧВК 3428624. PMID 14690611.
- ^ Хавас К., Флаус А., Фелан М., Кингстон Р., Уэйд П.А., Лилли Д.М., Оуэн-Хьюз Т. (декабрь 2000 г.). «Генерация суперспирального кручения с помощью АТФ-зависимой активности ремоделирования хроматина». Клетка. 103 (7): 1133–42. Дои:10.1016 / S0092-8674 (00) 00215-4. PMID 11163188. S2CID 7911590.
- ^ Мидзугути Дж., Шен Х, Ландри Дж., Ву У.Х., Сен С., Ву С. (январь 2004 г.). «АТФ-управляемый обмен варианта гистона H2AZ, катализируемый комплексом ремоделирования хроматина SWR1». Наука. 303 (5656): 343–8. Bibcode:2004Наука ... 303..343М. Дои:10.1126 / science.1090701. PMID 14645854. S2CID 9881829.
- ^ Métivier R, Penot G, Hübner MR, Reid G, Brand H, Kos M, Gannon F (декабрь 2003 г.). «Рецептор эстрогена-альфа управляет упорядоченным, циклическим и комбинаторным набором кофакторов на природном промоторе-мишени». Клетка. 115 (6): 751–63. Дои:10.1016 / S0092-8674 (03) 00934-6. PMID 14675539. S2CID 145525.
- ^ Нагайч А.К., Уокер Д.А., Вольффорд Р., Хагер Г.Л. (апрель 2004 г.). «Быстрое периодическое связывание и смещение рецептора глюкокортикоидов во время ремоделирования хроматина». Молекулярная клетка. 14 (2): 163–74. Дои:10.1016 / S1097-2765 (04) 00178-9. PMID 15099516.
- ^ Тейф В.Б., Вайнштейн Ю., Кодрон-Хергер М., Маллм Дж. П., Март С., Хёфер Т., Риппе К. (ноябрь 2012 г.). «Позиционирование нуклеосом по всему геному во время развития эмбриональных стволовых клеток». Структурная и молекулярная биология природы. 19 (11): 1185–92. Дои:10.1038 / nsmb.2419. PMID 23085715. S2CID 34509771.
- ^ Альберт I, Маврич Т.Н., Томшо Л.П., Ци Дж., Зантон С.Дж., Шустер С.К., Пью Б.Ф. (март 2007 г.). «Настройки трансляции и вращения нуклеосом H2A.Z в геноме Saccharomyces cerevisiae». Природа. 446 (7135): 572–6. Bibcode:2007Натура.446..572А. Дои:10.1038 / природа05632. PMID 17392789. S2CID 4416890.
- ^ Ли Б., Кэри М., Уоркман Дж. Л. (февраль 2007 г.). «Роль хроматина при транскрипции». Клетка. 128 (4): 707–19. Дои:10.1016 / j.cell.2007.01.015. PMID 17320508. S2CID 1773333.
- ^ Белый дом I, Рандо О.Дж., Делроу Дж., Цукияма Т. (декабрь 2007 г.). «Ремоделирование хроматина на промоторах подавляет антисмысловую транскрипцию». Природа. 450 (7172): 1031–5. Bibcode:2007 Натур.450.1031W. Дои:10.1038 / природа06391. PMID 18075583. S2CID 4305576.
- ^ Ли В., Тилло Д., Брей Н., Морс Р. Х., Дэвис Р. В., Хьюз Т. Р., Нислоу С. (октябрь 2007 г.). «Атлас занятости нуклеосом в дрожжах с высоким разрешением». Природа Генетика. 39 (10): 1235–44. Дои:10,1038 / ng2117. PMID 17873876. S2CID 12816925.
- ^ Eaton ML, Galani K, Kang S, Bell SP, MacAlpine DM (апрель 2010 г.). «Консервативное положение нуклеосом определяет начало репликации». Гены и развитие. 24 (8): 748–53. Дои:10.1101 / gad.1913210. ЧВК 2854390. PMID 20351051.
- ^ Шивасвами С., Бхинге А., Чжао Ю., Джонс С., Херст М., Айер В.Р. (март 2008 г.). «Динамическое ремоделирование отдельных нуклеосом в эукариотическом геноме в ответ на нарушение транскрипции». PLOS Биология. 6 (3): e65. Дои:10.1371 / journal.pbio.0060065. ЧВК 2267817. PMID 18351804.
- ^ Муругесапиллай Д., МакКоли М.Дж., Хо Р., Нельсон Холте М.Х., Степанянц А., Махер Л.Дж., Исраэлофф Н.Э., Уильямс М.С. (август 2014 г.). «Соединение ДНК и образование петель посредством HMO1 обеспечивает механизм стабилизации хроматина, свободного от нуклеосом». Исследования нуклеиновых кислот. 42 (14): 8996–9004. Дои:10.1093 / нар / gku635. ЧВК 4132745. PMID 25063301.
- ^ Murugesapillai D, McCauley MJ, Maher LJ, Williams MC (февраль 2017 г.). «Одномолекулярные исследования белков, изгибающих архитектурную ДНК группы B с высокой подвижностью». Биофизические обзоры. 9 (1): 17–40. Дои:10.1007 / s12551-016-0236-4. ЧВК 5331113. PMID 28303166.
- ^ Хейс Дж. Дж., Ли К. М. (май 1997 г.). «Восстановление in vitro и анализ мононуклеосом, содержащих определенные ДНК и белки». Методы. 12 (1): 2–9. Дои:10.1006 / мет.1997.0441. PMID 9169189.
- ^ Dyer PN, Edayathumangalam RS, White CL, Bao Y, Chakravarthy S, Muthurajan UM, Luger K (2004). «Восстановление ядер нуклеосомных частиц из рекомбинантных гистонов и ДНК». Методы в энзимологии. 375: 23–44. Дои:10.1016 / с0076-6879 (03) 75002-2. ISBN 9780121827793. PMID 14870657.
- ^ Енидуня А., Дэйви С., Кларк Д., Фельсенфельд Г., Аллан Дж. (Апрель 1994 г.). «Позиционирование нуклеосом на промоторах гена глобина курицы и человека in vitro. Новые методы картирования». Журнал молекулярной биологии. 237 (4): 401–14. Дои:10.1006 / jmbi.1994.1243. PMID 8151701.
- ^ Frouws TD, Barth PD, Richmond TJ (январь 2018 г.). «Сайт-специфичные сшитые дисульфидом нуклеосомы с повышенной стабильностью». Журнал молекулярной биологии. 430 (1): 45–57. Дои:10.1016 / j.jmb.2017.10.029. ЧВК 5757783. PMID 29113904.
- ^ Ферент А.Е., Вердин Г.Л. (1994). «Конвертируемый нуклеозидный подход: структурная инженерия нуклеиновых кислот с помощью дисульфидных перекрестных связей». В Eckstein F, Lilley DM (ред.). Нуклеиновые кислоты и молекулярная биология. Нуклеиновые кислоты и молекулярная биология. 8. С. 14–40. Дои:10.1007/978-3-642-78666-2_2. ISBN 978-3-642-78668-6.
- ^ Ямасу К., Сэншу Т. (1990). «Консервативная сегрегация тетраметрических единиц гистонов H3 и H4 во время репликации нуклеосом». Журнал биохимии. 170 (1): 15–20. Дои:10.1093 / oxfordjournals.jbchem.a122999. PMID 2332416.
- ^ Кауфман П.Д., Кобаяши Р., Кесслер Н., Стиллман Б. (июнь 1995 г.). «Субъединицы p150 и p60 фактора сборки хроматина I: молекулярная связь между вновь синтезированными гистонами и репликацией ДНК». Клетка. 81 (7): 1105–14. Дои:10.1016 / S0092-8674 (05) 80015-7. PMID 7600578. S2CID 13502921.
- ^ Тайлер Дж. К., Адамс С. Р., Чен С. Р., Кобаяши Р., Камакака Р. Т., Кадонага Д. Т. (декабрь 1999 г.). «Комплекс RCAF опосредует сборку хроматина во время репликации и репарации ДНК». Природа. 402 (6761): 555–60. Bibcode:1999Натура 402..555Т. Дои:10.1038/990147. PMID 10591219. S2CID 205097512.
- ^ Benson LJ, Gu Y, Yakovleva T., Tong K, Barrows C, Strack CL, Cook RG, Mizzen CA, Annunziato AT (апрель 2006 г.). «Модификации H3 и H4 во время репликации хроматина, сборки нуклеосом и обмена гистонов». Журнал биологической химии. 281 (14): 9287–96. Дои:10.1074 / jbc.M512956200. PMID 16464854.
- ^ Лаутерс Л., Чолкли Р. (июнь 1985 г.). «Обмен гистонов H1, H2A и H2B in vivo». Биохимия. 24 (13): 3080–5. Дои:10.1021 / bi00334a002. PMID 4027229.
- ^ Пак Й.Дж., Чодапарамбил СП, Бао Ю., Макбрайант С.Дж., Люгер К. (январь 2005 г.). «Белок сборки нуклеосом 1 обменивает димеры гистонов H2A-H2B и способствует скольжению нуклеосом». Журнал биологической химии. 280 (3): 1817–25. Дои:10.1074 / jbc.M411347200. PMID 15516689.
- ^ Винсент Дж. А., Квонг Т. Дж., Цукияма Т. (май 2008 г.). «АТФ-зависимое ремоделирование хроматина формирует ландшафт репликации ДНК». Структурная и молекулярная биология природы. 15 (5): 477–84. Дои:10.1038 / nsmb.1419. ЧВК 2678716. PMID 18408730.
- ^ Ядав Т., Белый дом I (апрель 2016 г.). «Сборка и позиционирование связанных с репликацией нуклеосом с помощью АТФ-зависимых ферментов ремоделирования хроматина». Отчеты по ячейкам. 15 (4): 715–723. Дои:10.1016 / J.CELREP.2016.03.059. ЧВК 5063657. PMID 27149855.
внешняя ссылка
- MBInfo - Что такое нуклеосомы
- Нуклеосомы на сайте Richmond Lab
- Протеопедия Нуклеосомы
- Нуклеосома в PDB
- Динамическое ремоделирование отдельных нуклеосом в геноме эукариот в ответ на нарушение транскрипции
- Данные и инструменты для позиционирования нуклеосом онлайн (аннотированный список, постоянно обновляемый)
- Структура гистонового белка
- HistoneDB 2.0 - База данных гистонов и вариантов в NCBI




