RAB11B - RAB11B
Ras-родственный белок Rab-11B это белок что у людей кодируется RAB11B ген.[5][6] Rab11b считается наиболее распространенным выразил в головном мозге, сердце и яичках.
Раб (Ras-связанные в головном мозге) белки составляют самую большую часть Рас надсемейство малых GTPases. Белки семейства Rab регулируют процессы внутриклеточного переноса мембран, включая везикул почкование, привязка и слияние. Изоформы Rab11a, Rab11b и Rab11c /Rab25 составляют подсемейство Rab11 на основе конкретных последовательность мотивов.[7] Пока RAB11A находится на хромосома 15[8] и RAB11C на хромосома 1, RAB11B размещен на хромосома 19. Белки Rab11 участвуют в эндоцитоз и экзоцитоз.[9] Rab11b наиболее широко экспрессируется в головном мозге, сердце и яичках.[10] Ранние исследования с делециями гомологов RAB11 в Saccharomyces cerevisiae доказали свою важность для выживания клеток.[11][12]Несмотря на высокий уровень гомология последовательностей, Rab11a и Rab11b, по-видимому, располагаются в разных компартментах пузырьков.[13] Большинство Rab11b не сотрудничают с рецептор трансферрина ни с полимерный рецептор IgA. Этот белок также имеет зависимость от микротрубочек. цитоскелет это отличается от Rab11a.[13] Высокое разнообразие последовательностей в С-концевой гипервариабельной области отвечает за нацеливание на различные мембраны между этими белками.
Функция
Члены подсемейства Rab11 участвуют в рециркуляции белков из эндосомы к плазматическая мембрана, при переносе молекул из сеть транс-Гольджи к плазматической мембране и в фагоцитоз. Это подсемейство также участвует в поляризованном переносе в эпителиальные клетки.[14][15][16][17][18] В то время как большинство исследований относится к изоформе Rab11a, о Rab11b пока известно немного. Rab11b локализуется преимущественно в компартменте рециркуляции перицентриолярных клеток и служит важным компонентом везикулярного аппарата.[19] Это необходимо для передачи интернализованных трансферрин из камеры рециркуляции в плазматическую мембрану, для которой активен Rab11b, а также GTP гидролиз необходим.[19]
Структура
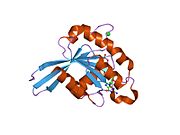
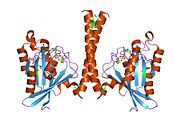
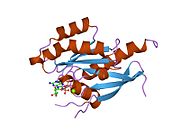
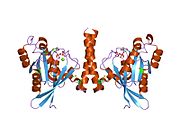
Все Ras GTPases состоят из аналогичной основной структуры и высококонсервативны. P-петля, переключите 1 и переключите регионы 2. Мономер Rab11b обнаруживает типичную Ras-подобную небольшую складку GTPase с шестицепочечным β-лист ядро (β1-β6) окружено пятью основными α-спирали (α1-α5)[16] и одна малая α-спираль (α6). По сходству последовательностей с другими Rab GTPases можно предположить, что они показывают очень похожие характеристики в связывании нуклеотидов и гидролиз. Однако изоформы Rab11 могут различаться по кинетике гидролиза из-за различий в конформация, поскольку Rab11a и Rab11b не обнаруживают области α-спирального переключателя 2, как другие Rab GTPases. Rab11b имеет 90% аминокислотную идентичность с Rab11a.[16] Кинетические эксперименты с Rab11a / b и Rab11-взаимодействующими белками (FIP) показывают, что FIP не могут различать GTP-связанные Rab11a и Rab11b in vitro.[20] Основное расхождение проявляется в неактивном состоянии. Хотя Паскуалато и др. кристаллизовал неактивный Rab11a в виде димера в асимметричном звене, Scapin et al. наблюдали монокристаллографически независимые мономеры как GDP-, так и GppNHp-связанных структур Rab11b.[16][21]


Клиническое значение
Благодаря своей решающей роли в транспорте и рециклинге везикул, белки Rab11 связаны с различными непатогенами или болезнями, вызванными патогенами. В большинстве опубликованных данных не указывается, является ли это a- или b-изоформой. Белки Rab11 участвуют в Болезнь Альцгеймера,[22][23] Артрогрипоз-почечная дисфункция-холестаз (ARC),[24] Болезнь Баттена,[25] и Невропатия Шарко-Мари-Зуба, тип 4С (CMT4C).[26]Внутриклеточные бактерии Chlamydia pneumoniae и Хламидия трахоматис которые реплицируются в мембраносвязанных компартментах, захватывают механизм трафика, рекрутируя Rab GTPases, чтобы способствовать их репликации в клетка-хозяин. Нокдаун Rab11 уменьшал образование инфекционных частиц.[27][28][29]Недавние исследования сообщают об аналогичном использовании внутриклеточного трафика Хантавирус и Вирус гриппа А. Реплицированные вирусы получают выгоду от рециркуляции, опосредованной Rab11 эндосома путь выхода из клетки и заражения окружающей ткани.[30][31][32][33]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000185236 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000077450 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Zhu AX, Zhao Y, Flier JS (декабрь 1994 г.). «Молекулярное клонирование двух небольших GTP-связывающих белков из скелетных мышц человека». Сообщения о биохимических и биофизических исследованиях. 205 (3): 1875–82. Дои:10.1006 / bbrc.1994.2889. PMID 7811277.
- ^ «Ген Entrez: RAB11B RAB11B, член семейства онкогенов RAS».
- ^ Бхартур С.Г., Калхун BC, Вудрам Дж., Куркджиан Дж., Айер С., Лай Ф., Голденринг Дж. Р. (март 2000 г.). «Геномная структура мышиных членов семьи Rab11». Сообщения о биохимических и биофизических исследованиях. 269 (2): 611–7. Дои:10.1006 / bbrc.2000.2334. PMID 10708602.
- ^ Громов П.С., Селис Дж. Э., Хансен С., Томмеруп Н., Громова И., Мадсен П. (июнь 1998 г.). «Rab11a человека: транскрипция, картирование хромосом и влияние на уровни экспрессии GTP-связывающих белков хозяина». Письма FEBS. 429 (3): 359–64. Дои:10.1016 / s0014-5793 (98) 00607-3. PMID 9662449. S2CID 22139183.
- ^ Вилке М., Йоханнес Л., Галли Т., Маяу В., Гоуд Б., Саламеро Дж. (Декабрь 2000 г.). «Rab11 регулирует компартментализацию ранних эндосом, необходимых для эффективного транспорта от ранних эндосом к сети транс-Гольджи». Журнал клеточной биологии. 151 (6): 1207–20. Дои:10.1083 / jcb.151.6.1207. ЧВК 2190589. PMID 11121436.
- ^ Лай Ф., Стаббс Л., Артц К. (август 1994 г.). «Молекулярный анализ мыши Rab11b: новый тип белка YPT / Rab млекопитающих». Геномика. 22 (3): 610–6. Дои:10.1006 / geno.1994.1434. PMID 8001972.
- ^ Бенли М., Деринг Ф., Робинсон Д.Г., Ян Х, Галлвиц Д. (декабрь 1996 г.). «Две изоформы GTPase, Ypt31p и Ypt32p, необходимы для функции Гольджи у дрожжей». Журнал EMBO. 15 (23): 6460–75. Дои:10.1002 / j.1460-2075.1996.tb01037.x. ЧВК 452471. PMID 8978673.
- ^ Джедд Дж., Малхолланд Дж., Сегев Н. (май 1997 г.). «Две новые ГТФазы Ypt необходимы для выхода из дрожжевого транс-Гольджи-компартмента». Журнал клеточной биологии. 137 (3): 563–80. Дои:10.1083 / jcb.137.3.563. ЧВК 2139891. PMID 9151665.
- ^ Чен В., Фенг Й., Чен Д., Вандингер-Несс А. (ноябрь 1998 г.). «Rab11 необходим для транспорта от сети Гольджи к плазматической мембране и является предпочтительной мишенью для ингибитора диссоциации GDP». Молекулярная биология клетки. 9 (11): 3241–57. Дои:10.1091 / mbc.9.11.3241. ЧВК 25617. PMID 9802909.
- ^ Кокс Д., Ли Д. Д., Дейл Б. М., Калафат Дж., Гринберг С. (январь 2000 г.). «Компартмент, содержащий Rab11, быстро рециркулирующий в макрофагах, который способствует фагоцитозу». Труды Национальной академии наук Соединенных Штатов Америки. 97 (2): 680–5. Bibcode:2000PNAS ... 97..680C. Дои:10.1073 / пнас.97.2.680. ЧВК 15390. PMID 10639139.
- ^ а б c d е ж Скапин С.М., Карнейро Ф.Р., Алвес А.С., Медрано Ф.Дж., Гимарайнш Б.Г., Занчин Н.И. (июнь 2006 г.). «Кристаллическая структура малой GTPase Rab11b обнаруживает критические отличия от изоформы Rab11a». Журнал структурной биологии. 154 (3): 260–8. Дои:10.1016 / j.jsb.2006.01.007. PMID 16545962.
- ^ Ullrich O, Reinsch S, Urbé S, Zerial M, Parton RG (ноябрь 1996 г.). «Rab11 регулирует рециркуляцию через эндосомы перицентриолярного рециклинга». Журнал клеточной биологии. 135 (4): 913–24. Дои:10.1083 / jcb.135.4.913. ЧВК 2133374. PMID 8922376.
- ^ Ван Х, Кумар Р., Наварра Дж., Казанова Дж. Э., Голденринг Дж. Р. (сентябрь 2000 г.). «Регулирование везикул в клетках почек собак Madin-Darby с помощью Rab11a и Rab25». Журнал биологической химии. 275 (37): 29138–46. Дои:10.1074 / jbc.M004410200. PMID 10869360.
- ^ а б Шлирф Б., Фей Г. Х., Хаубер Дж., Хокке Г. М., Розориус О. (август 2000 г.). «Rab11b необходим для возврата трансферрина к плазматической мембране». Экспериментальные исследования клеток. 259 (1): 257–65. Дои:10.1006 / excr.2000.4947. PMID 10942597.
- ^ Шиба Т., Кога Х., Шин Х.В., Кавасаки М., Като Р., Накаяма К., Вакацуки С. (октябрь 2006 г.). «Структурная основа Rab11-зависимого мембранного рекрутирования семейства Rab11-взаимодействующего белка 3 (FIP3) / арфофилин-1». Труды Национальной академии наук Соединенных Штатов Америки. 103 (42): 15416–21. Bibcode:2006ПНАС..10315416С. Дои:10.1073 / pnas.0605357103. ЧВК 1622838. PMID 17030804.
- ^ Pasqualato S, Senic-Matuglia F, Renault L, Goud B, Salamero J, Cherfils J (март 2004 г.). «Структурный цикл GDP / GTP Rab11 обнаруживает новый интерфейс, участвующий в динамике рециклирования эндосом». Журнал биологической химии. 279 (12): 11480–8. Дои:10.1074 / jbc.M310558200. PMID 14699104.
- ^ Гринфилд Дж. П., Люнг Л. В., Кай Д., Каасик К., Гросс Р. С., Родригес-Булан Е., Грингард П., Сюй Х. (апрель 2002 г.). «Эстроген снижает образование бета-амилоида при болезни Альцгеймера за счет стимуляции биогенеза везикул транс-сети Гольджи». Журнал биологической химии. 277 (14): 12128–36. Дои:10.1074 / jbc.M110009200. PMID 11823458.
- ^ Dumanchin C, Czech C, Campion D, Cuif MH, Poyot T, Martin C, Charbonnier F, Goud B, Pradier L, Frebourg T (июль 1999 г.). «Пресенилины взаимодействуют с Rab11, небольшой GTPase, участвующей в регуляции везикулярного транспорта». Молекулярная генетика человека. 8 (7): 1263–9. Дои:10.1093 / hmg / 8.7.1263. PMID 10369872.
- ^ Cullinane AR, Straatman-Iwanowska A, Zaucker A, Wakabayashi Y, Брюс CK, Luo G, Rahman F, Gürakan F, Utine E, Ozkan TB, Denecke J, Vukovic J, Di Rocco M, Mandel H, Cangul H, Matthews RP , Томас С.Г., Раппопорт Дж.З., Ариас И.М., Вольбург Х., Книзели А.С., Келли Д.А., Мюллер Ф., Махер Э.Р., Гиссен П. (апрель 2010 г.). «Мутации в VIPAR вызывают артрогрипоз, почечную дисфункцию и фенотип синдрома холестаза с дефектами поляризации эпителия». Природа Генетика. 42 (4): 303–12. Дои:10,1038 / нг.538. ЧВК 5308204. PMID 20190753.
- ^ Луиро К., Юлианнала К., Ахтиайнен Л., Мауну Х., Ярвеля И., Кюттяля А., Яланко А. (декабрь 2004 г.). «Взаимосвязи белков CLN3, Hook1 и Rab связывают болезнь Баттена с дефектами эндоцитарного пути». Молекулярная генетика человека. 13 (23): 3017–27. Дои:10,1093 / hmg / ddh321. PMID 15471887.
- ^ Стендель С., Роос А., Кляйне Х., Арно Э., Озчелик М., Сидиропулос П.Н., Зенкер Дж., Шюпфер Ф., Леманн Ю., Собота Р.М., Литчфилд Д.В., Люшер Б., Краст Р., Сутер Ю., Сендерек Дж. (Август 2010 г.). «SH3TC2, белок мутант при нейропатии Шарко-Мари-Тута, связывает миелинизацию периферических нервов с рециркуляцией эндосом». Мозг. 133 (Pt 8): 2462–74. Дои:10.1093 / мозг / awq168. PMID 20826437.
- ^ Cortes C, Rzomp KA, Tvinnereim A, Scidmore MA, Wizel B (декабрь 2007 г.). «Белок включения мембраны включения Chlamydia pneumoniae Cpn0585 взаимодействует с множеством Rab GTPases». Инфекция и иммунитет. 75 (12): 5586–96. Дои:10.1128 / IAI.01020-07. ЧВК 2168330. PMID 17908815.
- ^ Рейман Липински А., Хейманн Дж., Мейснер С., Карлас А., Бринкманн В., Мейер Т.Ф., Хойер Д. (октябрь 2009 г.). «Rab6 и Rab11 регулируют развитие Chlamydia trachomatis и golgin-84-зависимую фрагментацию Гольджи». Патогены PLOS. 5 (10): e1000615. Дои:10.1371 / journal.ppat.1000615. ЧВК 2752117. PMID 19816566.
- ^ Рзомп К.А., Шольтес Л.Д., Бриггс Б.Дж., Уиттакер Г.Р., Скадмор М.А. (октябрь 2003 г.). «Rab GTPases задействованы во включениях хламидий как в зависимости от вида, так и независимо от вида». Инфекция и иммунитет. 71 (10): 5855–70. Дои:10.1128 / IAI.71.10.5855-5870.2003. ЧВК 201052. PMID 14500507.
- ^ Аморим MJ, Брюс EA, Рид EK, Foeglein A, Mahen R, Стюарт AD, Digard P (май 2011 г.). «Rab11- и микротрубочко-зависимый механизм цитоплазматического транспорта вирусной РНК вируса гриппа А.». Журнал вирусологии. 85 (9): 4143–56. Дои:10.1128 / JVI.02606-10. ЧВК 3126276. PMID 21307188.
- ^ Брюс Е.А., Дигард П., Стюарт А.Д. (июнь 2010 г.). «Путь Rab11 необходим для почкования вируса гриппа A и образования филаментов». Журнал вирусологии. 84 (12): 5848–59. Дои:10.1128 / JVI.00307-10. ЧВК 2876627. PMID 20357086.
- ^ Момосе Ф, Сэкимото Т., Окура Т., Джо С., Кавагути А., Нагата К., Морикава Y (2011-06-22). «Апикальный транспорт рибонуклеопротеина вируса гриппа A требует Rab11-позитивной рециклирующей эндосомы». PLOS ONE. 6 (6): e21123. Bibcode:2011PLoSO ... 621123M. Дои:10.1371 / journal.pone.0021123. ЧВК 3120830. PMID 21731653.
- ^ Роу, Регина К .; Джейсон В. Сушко; Эндрю Пекош (2008-12-20). «Роли рециклирующих эндосом Rab8 и Rab11 в высвобождении хантавируса из эпителиальных клеток». Вирусология. 382 (2): 239–249. Дои:10.1016 / j.virol.2008.09.021. ISSN 0042-6822. ЧВК 2648827. PMID 18951604.
дальнейшее чтение
- Маруяма К., Сугано С. (январь 1994 г.). «Олиго-кэппинг: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Ген. 138 (1–2): 171–4. Дои:10.1016/0378-1119(94)90802-8. PMID 8125298.
- Судзуки Ю., Ёситомо-Накагава К., Маруяма К., Суяма А., Сугано С. (октябрь 1997 г.). «Конструирование и характеристика полноразмерной библиотеки кДНК с обогащением по 5'-концу». Ген. 200 (1–2): 149–56. Дои:10.1016 / S0378-1119 (97) 00411-3. PMID 9373149.
- Шлирф Б., Фей Г. Х., Хаубер Дж., Хокке Г. М., Розориус О. (август 2000 г.). «Rab11b необходим для возврата трансферрина к плазматической мембране». Экспериментальные исследования клеток. 259 (1): 257–65. Дои:10.1006 / excr.2000.4947. PMID 10942597.
- Лапьер Л.А., Кумар Р., Хейлз К.М., Наварра Дж., Бхартур С.Г., Бернетт Дж. О., Прованс Д.В., Мерсер Дж. А., Белер М., Голденринг-младший (июнь 2001 г.). «Миозин vb связан с системами рециркуляции плазматической мембраны». Молекулярная биология клетки. 12 (6): 1843–57. Дои:10.1091 / mbc.12.6.1843. ЧВК 37346. PMID 11408590.
- Прекерис Р., Дэвис Дж. М., Шеллер Р. Х. (октябрь 2001 г.). «Идентификация нового связывающего домена Rab11 / 25, присутствующего в белках Eferin и Rip». Журнал биологической химии. 276 (42): 38966–70. Дои:10.1074 / jbc.M106133200. PMID 11481332.
- Хейлз С.М., Гринер Р., Хобди-Хендерсон К.С., Дорн М.С., Харди Д., Кумар Р., Наварра Дж., Чан Е.К., Лапьер Л.А., Голденринг-младший (октябрь 2001 г.). «Идентификация и характеристика семейства Rab11-взаимодействующих белков». Журнал биологической химии. 276 (42): 39067–75. Дои:10.1074 / jbc.M104831200. PMID 11495908.
- Хвотчев М.В., Рен М., Такамори С., Ян Р., Зюдхоф ТЦ (ноябрь 2003 г.). «Дивергентные функции нейронов Rab11b в Ca2 + -регулируемом по сравнению с конститутивным экзоцитозом». Журнал неврологии. 23 (33): 10531–9. Дои:10.1523 / JNEUROSCI.23-33-10531.2003. ЧВК 6740915. PMID 14627637.
- Скапин С.М., Карнейро Ф.Р., Алвес А.С., Медрано Ф.Дж., Гимарайнш Б.Г., Занчин Н.И. (июнь 2006 г.). «Кристаллическая структура малой GTPase Rab11b обнаруживает критические отличия от изоформы Rab11a». Журнал структурной биологии. 154 (3): 260–8. Дои:10.1016 / j.jsb.2006.01.007. PMID 16545962.