Вирус гриппа А - Influenza A virus - Wikipedia
| Вирус гриппа А | |
|---|---|
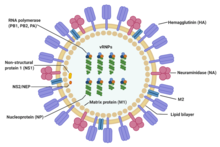 | |
| Структура вируса гриппа А. | |
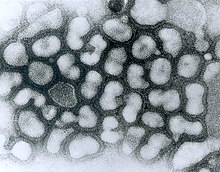 | |
| ТЕМ микрофотография вирусов гриппа А | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область: | Рибовирия |
| Королевство: | Орторнавиры |
| Тип: | Негарнавирикота |
| Учебный класс: | Insthoviricetes |
| Заказ: | Articulavirales |
| Семья: | Ортомиксовирусы |
| Род: | Альфа-гриппозавирус |
| Разновидность: | Вирус гриппа А |
| Подтипы | |
Грипп Вирус причины грипп в птицах и некоторых млекопитающие, и это единственный разновидность из род Альфа-гриппозавирус семейства вирусов Ортомиксовирусы.[1] Штаммы всех подтипов вируса гриппа А были изолированы от диких птиц, хотя заболевание встречается редко. Немного изолирует вируса гриппа А вызывают тяжелые заболевания как у домашней птицы, так и, реже, у человека.[2] Иногда вирусы передаются от диких водных птиц домашним птицам, и это может вызвать вспышку или вызвать грипп человека. пандемии.[3][4]
Вирусы гриппа A: отрицательный смысл, одноцепочечный, сегментированный РНК-вирусы. Несколько подтипов помечены в соответствии с номером H (для типа гемагглютинин ) и номер N (для типа нейраминидаза ). Есть 18 различных известных H антигены (От H1 до H18) и 11 различных известных антигенов N (от N1 до N11).[5][6] H17N10 был выделен из фруктовые летучие мыши в 2012.[7][8] H18N11 был обнаружен у перуанской летучей мыши в 2013 году.[6]
Каждый подтип вируса имеет мутировавший на множество штаммов с разными патогенный профили; некоторые из них являются патогенными для одного вида, но не являются патогенными для других, некоторые - для нескольких видов.
Отфильтрованная и очищенная вакцина против гриппа А для людей была разработана, и многие страны накопили ее для быстрого введения населению в случае заражения. птичий грипп пандемия. Птичий грипп иногда называют птичьим гриппом, а в просторечии - птичьим гриппом. В 2011 году исследователи сообщили об открытии антитело эффективен против всех типов вируса гриппа А.[9]
Варианты и подтипы

Вирусы гриппа типа А: РНК-вирусы делятся на подтипы по типу два белки на поверхности вирусной оболочки:
- H = гемагглютинин, белок, который вызывает красные кровяные тельца к агглютинировать.
- N = нейраминидаза, фермент, который расщепляет гликозидные связи из моносахарид сиаловая кислота (ранее назывался нейраминовая кислота ).
Гемагглютинин играет центральную роль в распознавании вируса и его связывании с клетками-мишенями, а также в его последующем заражении клетки своим РНК. С другой стороны, нейраминидаза имеет решающее значение для последующего высвобождения дочерних вирусных частиц, созданных внутри инфицированной клетки, чтобы они могли распространяться на другие клетки.
Различные вирусы гриппа кодируют разные белки гемагглютинина и нейраминидазы. Например, Вирус H5N1 обозначает подтип гриппа A, который имеет белок гемагглютинин (H) типа 5 и белок нейраминидазы (N) типа 1. Существует 18 известных типов гемагглютинина и 11 известных типов нейраминидазы, поэтому теоретически возможно 198 различных комбинаций этих белков.[5][6]
Некоторые варианты идентифицированы и названы в соответствии с изолятом, на который они похожи, поэтому предполагается, что они имеют общее происхождение (пример Фуцзянский грипп вирусоподобный); в соответствии с их типичным хозяином (пример человеческий грипп вирус); по подтипу (пример H3N2); и по их смертоносности (например, LP, низкопатогенный). Так грипп от вируса, подобного изоляту A / Fujian / 411/2002 (H3N2), называется Фуцзянь грипп, человеческий грипп и грипп H3N2.
Иногда варианты называют в зависимости от вида (хозяина), для которого штамм является эндемиком или к которому он адаптирован. Основными вариантами, названными с использованием этого соглашения, являются:
Варианты также иногда называли в соответствии с их смертоносностью для домашней птицы, особенно для кур:
- Низкопатогенный птичий грипп (LPAI)
- Высокопатогенный птичий грипп (HPAI), также называемый смертельным гриппом или смертельным гриппом.
Большинство известных штаммов - это вымершие штаммы. Например, ежегодный подтип гриппа H3N2 больше не содержит штамм, вызвавший Гонконгский грипп.
Ежегодный грипп
Ежегодный грипп (также называемый «сезонным гриппом» или «человеческим гриппом») в США. «ежегодно приводит к примерно 36 000 смертей и более 200 000 госпитализаций. В дополнение к человеческим жертвам, грипп ежегодно вызывает в США более 10 миллиардов долларов».[10] В глобальном масштабе число жертв вируса гриппа оценивается в 290 000–645 000 смертей ежегодно, что превышает предыдущие оценки.[11]
Ежегодно обновляемый, трехвалентный вакцина против гриппа состоит из гемагглютинин (НА) компоненты поверхностных гликопротеинов от гриппа H3N2, H1N1, и Грипп B вирусы.[12]
Измеряли устойчивость к стандартным противовирусным препаратам. амантадин и римантадин в H3N2 увеличилась с 1% в 1994 году до 12% в 2003 году до 91% в 2005 году.
"Современные вирусы гриппа человека H3N2 сейчас эндемичный у свиней на юге Китая и может пересортировать с птичьим H5N1 вирусов в этом промежуточном хосте ".[13]
FI6 антитело
FI6, антитело которое нацелено на белок гемагглютинин, было обнаружено в 2011 году. FI6 - единственное известное антитело, эффективное против всех 16 подтипов вируса гриппа А.[14][15][16]
Строение и генетика

Вирусы гриппа типа A очень похожи по структуре на вирусы гриппа типов B, C и D.[19] Вирусная частица (также называемая вирионом) имеет диаметр 80–120 нанометров, так что самые маленькие вирионы принимают эллиптическую форму.[20][18] Длина каждой частицы значительно различается из-за того, что грипп является плеоморфным и может превышать многие десятки микрометров, образуя нитчатые вирионы.[21] Заблуждение о природе плеоморфии вируса гриппа связано с наблюдением, что лабораторно адаптированные штаммы обычно теряют способность образовывать нити.[22] и что эти адаптированные в лаборатории штаммы были первыми, которые были визуализированы с помощью электронной микроскопии.[23] Несмотря на эти различные формы, вирионы всех вирусов гриппа типа А похожи по составу. Все они состоят из вирусной оболочки, содержащей два основных типа белков, обернутой вокруг центрального ядра.[24]
Два больших белка, обнаруженных снаружи вирусных частиц, - это гемагглютинин (HA) и нейраминидаза (NA). НА - это белок, который опосредует связывание вириона с клетками-мишенями и проникновение вирусного генома в клетку-мишень. NA участвует в высвобождении из множества непродуктивных участков прикрепления, присутствующих в слизи.[25] а также высвобождение потомства вирионов из инфицированных клеток.[26] Эти белки обычно являются мишенями для противовирусных препаратов.[27] Кроме того, они также являются белками-антигенами, с которыми могут связываться антитела хозяина и запускать иммунный ответ. Вирусы гриппа типа A подразделяются на подтипы в зависимости от типа этих двух белков на поверхности вирусной оболочки. Известно 16 подтипов HA и 9 подтипов NA, но у людей обычно встречаются только H 1, 2 и 3, а также N 1 и 2.[28]
Центральное ядро вириона содержит вирусный геном и другие вирусные белки, которые упаковывают и защищают генетический материал. В отличие от геномов большинства организмов (включая людей, животных, растения и бактерии), которые состоят из двухцепочечной ДНК, многие вирусные геномы состоят из другой одноцепочечной нуклеиновой кислоты, называемой РНК. Однако, что необычно для вируса, геном вируса гриппа типа А не представляет собой единого фрагмента РНК; вместо этого он состоит из сегментированных фрагментов РНК с отрицательным смыслом, каждый фрагмент содержит один или два гена, которые кодируют продукт гена (белок).[24] Термин РНК с отрицательным смыслом просто означает, что геном РНК не может быть транслирован в белок напрямую; он должен быть сначала транскрибирован в РНК с положительным смыслом, прежде чем он может быть переведен в белковые продукты. Сегментированный характер генома позволяет обмениваться целыми генами между различными вирусными штаммами.[24]

Полный геном вируса гриппа A составляет 13 588 оснований и состоит из восьми сегментов РНК, кодирующих от 10 до 14 белков, в зависимости от штамма. Актуальность или наличие альтернативных генных продуктов может варьироваться:[29]
- Сегмент 1 кодирует субъединицу РНК-полимеразы (PB2).
- Сегмент 2 кодирует субъединицу РНК-полимеразы (PB1) и белок PB1-F2, который индуцирует гибель клеток, за счет использования разных рамок считывания из одного и того же сегмента РНК.
- Сегмент 3 кодирует субъединицу РНК-полимеразы (PA) и белок PA-X, который играет роль в отключении транскрипции хозяина.[30]
- Сегмент 4 кодирует HA (гемагглютинин). Для образования одного вириона необходимо около 500 молекул гемагглютинина. HA определяет степень и серьезность вирусной инфекции в организме хозяина.
- Сегмент 5 кодирует NP, который является нуклеопротеином.
- Сегмент 6 кодирует NA (нейраминидазу). Для образования одного вириона необходимо около 100 молекул нейраминидазы.
- Сегмент 7 кодирует два матричных белка (M1 и M2) за счет использования разных рамок считывания из одного и того же сегмента РНК. Для создания одного вириона необходимо около 3000 молекул матричного белка.
- Сегмент 8 кодирует два разных неструктурных белка (NS1 и NEP) за счет использования разных рамок считывания из одного и того же сегмента РНК.

Сегменты РНК вирусного генома имеют комплементарные последовательности оснований на концевых концах, что позволяет им связываться друг с другом водородными связями.[26] Транскрипция вирусного (-) смыслового генома (вРНК) может продолжаться только после связывания белка PB2 с РНК, кэпированной хозяином, что позволяет субъединице PA расщеплять несколько нуклеотидов после кэпа. Этот полученный от хозяина кэп и сопровождающие его нуклеотиды служат праймером для инициации вирусной транскрипции. Транскрипция продолжается вдоль вРНК до тех пор, пока не будет достигнут участок из нескольких оснований урацила, инициируя «заикание», в результате чего возникающая вирусная мРНК полиаденилируется, производя зрелый транскрипт для ядерного экспорта и трансляции с помощью механизма хозяина.[31]
Синтез РНК происходит в ядре клетки, а синтез белков - в цитоплазме. После того, как вирусные белки собраны в вирионы, собранные вирионы покидают ядро и мигрируют к клеточной мембране.[32] Мембрана клетки-хозяина имеет участки вирусных трансмембранных белков (HA, NA и M2) и нижележащий слой белка M1, который помогает собранным вирионам проходить через мембрану, высвобождая готовые вирусы в оболочке во внеклеточную жидкость.[32]
Повторная активация множественности
Вирус гриппа способен подвергаться многократной реактивации после инактивации УФ-излучением,[33][34] или ионизирующим излучением.[35] Если какая-либо из восьми цепей РНК, составляющих геном, содержит повреждение, препятствующее репликации или экспрессии важного гена, вирус становится нежизнеспособным, когда он один заражает клетку (единичная инфекция). Однако, когда два или более поврежденных вируса заражают одну и ту же клетку (множественная инфекция), могут быть получены жизнеспособные потомки вирусов при условии, что каждый из восьми геномных сегментов присутствует по крайней мере в одной неповрежденной копии. То есть может произойти повторная активация множественности.
При заражении вирус гриппа вызывает ответную реакцию хозяина, включающую повышенное производство активных форм кислорода, и это может повредить геном вируса.[36] Если в естественных условиях выживаемость вируса обычно уязвима для проблемы окислительного повреждения, то реактивация множественности, вероятно, является селективно выгодной как своего рода процесс репарации генома. Было высказано предположение, что реактивация множественности с участием сегментированных геномов РНК может быть похожей на самую раннюю развитую форму сексуального взаимодействия в мире РНК, которая, вероятно, предшествовала миру ДНК.[37] (Также см Гипотеза мира РНК.)
Вирус гриппа человека

«Вирус гриппа человека» обычно относится к тем подтипам, которые широко распространены среди людей. H1N1, H1N2 и H3N2 - единственные известные подтипы вируса гриппа А, циркулирующие в настоящее время среди людей.[38]
Генетические факторы, позволяющие провести различие между «вирусами человеческого гриппа» и «вирусами птичьего гриппа», включают:
- PB2: (РНК-полимераза): Аминокислота (или же остаток ) положение 627 в белке PB2, кодируемом геном РНК PB2. До H5N1 все известные вирусы птичьего гриппа имели Glu в положении 627, в то время как все вирусы гриппа человека имели лизин.
- HA: (гемагглютинин): HA птичьего гриппа связывает альфа-2–3 сиаловая кислота рецепторы, тогда как HA гриппа человека связывает альфа 2-6 рецепторы сиаловой кислоты. Вирусы свиного гриппа обладают способностью связывать оба типа рецепторов сиаловой кислоты.
Симптомы человеческого гриппа обычно включают жар, кашель, больное горло, мышечные боли, конъюнктивит и, в тяжелых случаях, проблемы с дыханием и пневмония это может быть фатальным. Тяжесть инфекции во многом зависит от состояния инфицированного человека. иммунная система и если жертва ранее подвергалась воздействию штамма и, следовательно, имеет частичный иммунитет. Последующие исследования влияния статинов на репликацию вируса гриппа показывают, что предварительная обработка клеток аторвастатином подавляет рост вируса в культуре.[39]
Высокопатогенный птичий грипп H5N1 для человека протекает гораздо хуже, убивая 50% людей, которые им заражаются. В одном случае мальчик с H5N1 испытал понос быстро наступает кома без развития респираторных или гриппоподобных симптомов.[40]
Подтипы вируса гриппа A, которые были подтверждены у людей, отсортированные по количеству известных случаев пандемической смерти людей:
- H1N1 вызванный "Испанский грипп "в 1918 г. и Пандемия свиного гриппа 2009 г.
- H2N2 вызванный "Азиатский грипп "в конце 1950-х гг.
- H3N2 вызванный "Гонконгский грипп "в конце 1960-х
- H5N1 считается глобальным пандемия гриппа угроза через его распространение в середине 2000-х
- H7N9 ответственен за эпидемию 2013 года в Китае[41] и рассмотрен доктором Майкл Грегер, автор Как не умереть, чтобы иметь самую большую пандемическую угрозу вирусов гриппа А.[42]
- H7N7 есть некоторые зоонозный потенциал: редко вызывает заболевание у людей[43][44]
- H1N2 в настоящее время эндемичен для свиней, но не для человека.[45]
- H9N2, H7N2, H7N3, H5N2, и H10N7.
- H1N1
- H1N1 был ответственен за пандемию 2009 года как среди людей, так и среди свиней. Вариант H1N1 стал причиной пандемии испанского гриппа, унесшей жизни от 50 до 100 миллионов человек во всем мире примерно за год в 1918 и 1919 годах.[46] Другой вариант был назван угрозой пандемии в Пандемия гриппа 2009 г.. Споры возникли в октябре 2005 г., после того, как H1N1 геном было опубликовано в журнале, Наука, из-за опасений, что эта информация может быть использована для биотерроризм.[47]
 Случаи заболевания людей и летальные исходы, вызванные различными подтипами вируса гриппа А.
Случаи заболевания людей и летальные исходы, вызванные различными подтипами вируса гриппа А.
- H1N2
- H1N2 в настоящее время[когда? ] эндемичен как для человека[нужна цитата ] и популяции свиней. Новый штамм H1N2, по-видимому, возник в результате реассортации генов нынешнего[когда? ] циркулирующие подтипы гриппа H1N1 и H3N2. Белок гемагглютинина вируса H1N2 аналогичен белку современных[когда? ] циркулирующих вирусов H1N1, а белок нейраминидазы аналогичен белку современных[когда? ] Вирусы H3N2.[требуется медицинская цитата ]
- H2N2
- Азиатский грипп, пандемическая вспышка птичьего гриппа H2N2, возникшая в Китае в 1957 году, распространилась по всему миру в том же году, в течение которого была разработана вакцина против гриппа, продолжалась до 1958 года и унесла жизни от одного до четырех миллионов человек.[нужна цитата ]
- H3N2
- H3N2 в настоящее время[когда? ] эндемичен как для людей, так и для свиней. Он образовался из H2N2 путем антигенный сдвиг и вызвала пандемию гонконгского гриппа в 1968 и 1969 годах, унесшую жизни 750 000 человек.[48] В конце 2003 года тяжелая форма вируса H3N2 убила несколько детей в Соединенных Штатах.[49]
- Доминирующим штаммом ежегодного гриппа в январе 2006 г. был H3N2. Измеренная устойчивость к стандартным противовирусным препаратам амантадин и римантадин у H3N2 увеличилась с 1% в 1994 году до 12% в 2003 году до 91% в 2005 году.[50] Вирусы гриппа человека H3N2 теперь[когда? ] эндемичен для свиней на юге Китая, где они циркулируют вместе с птичьим вирусом H5N1.[13]
- H5N1
 |
H5N1 представляет собой главную угрозу пандемии гриппа в мире.[требуется разъяснение ][нужна цитата ]
- H5N2
- В январе 2006 года министерство здравоохранения Японии заявило, что рабочие птицефабрики в префектуре Ибараки могли подвергнуться воздействию H5N2 в 2005 году.[51] Титры антител к H5N2 парных сывороток 13 субъектов увеличились в четыре и более раз.[52]
- H5N9
- Высокопатогенный штамм H5N9 вызвал незначительную грипп вспышка в 1966 г. в Онтарио и Манитоба, Канада в индейки.[53]
- H7N2
- Один человек в Нью-Йорке в 2003 году и один человек в Вирджиния в 2002 г. были обнаружены серологические свидетельства инфекции H7N2.[нужна цитата ] Оба полностью выздоровели.[54][неудачная проверка ]
- H7N3
- В Северной Америке присутствие штамма птичьего гриппа H7N3 было подтверждено на нескольких птицефабриках в Британской Колумбии в феврале 2004 г. По состоянию на апрель 2004 г. 18 ферм были помещены в карантин, чтобы остановить распространение вируса. В этом регионе подтверждены два случая заболевания людей птичьим гриппом. «Симптомы включали конъюнктивит и легкое гриппоподобное заболевание».[55] Оба полностью выздоровели.
- H7N7
- H7N7 обладает необычным зоонозным потенциалом. В 2003 году в Нидерландах было подтверждено, что 89 человек инфицированы вирусом гриппа H7N7 после вспышки среди домашних птиц на нескольких фермах. Зарегистрирована одна смерть.
- H7N9
- 2 апреля 2013 г. Центр охраны здоровья (CHP) Министерства здравоохранения Гонконга подтвердили еще четыре случая в Цзянсу провинции в дополнение к трем случаям, первоначально зарегистрированным 31 марта 2013 года.[56] Этот вирус также обладает наибольшим потенциалом пандемии гриппа среди всех подтипов гриппа А.[57]
- H9N2
- Низкопатогенная инфекция птичьего гриппа A (H9N2) была подтверждена в 1999 году в Китае и Гонконге у двух детей и в 2003 году в Гонконге у одного ребенка. Все трое полностью выздоровели.[54][неудачная проверка ]
- H10N7
- В 2004 г. Египет, H10N7 был впервые обнаружен у людей. В Египте он вызвал болезнь у двух младенцев. Отец одного ребенка был торговцем домашней птицей.[58]
Эволюция

В соответствии с Джеффри Таубенбергер:
- «Все пандемии гриппа A после [пандемии испанского гриппа], и фактически почти все случаи гриппа A во всем мире (за исключением случаев инфицирования людей птичьими вирусами, такими как H5N1 и H7N7), были вызваны потомками вируса 1918 года, включая« дрейфующий » Вирусы H1N1 и повторно сортированные вирусы H2N2 и H3N2. Последние состоят из ключевых генов вируса 1918 года, обновленных за счет впоследствии включенных генов птичьего гриппа, кодирующих новые поверхностные белки, что делает вирус 1918 года действительно «матерью» всех пандемий ».[59]
Исследователи из Национальные институты здоровья использовали данные из Проект секвенирования генома гриппа и пришел к выводу, что в течение исследуемого десятилетнего периода большую часть времени ген гемагглютинина в H3N2 не обнаруживал значительного избытка мутаций в антигенных областях, в то время как накапливалось все большее количество штаммов. Это привело к тому, что один из вариантов, в конечном итоге, достиг более высокой физической формы, стал доминирующим и в короткий промежуток времени эволюция, быстро охватывая популяцию и устраняя большинство других вариантов.[60]
Исследование 2006 г. показало, что в краткосрочной эволюции вируса гриппа А ключевыми факторами являются стохастические или случайные процессы.[61] Эволюция антигена НА вируса гриппа А, по-видимому, характеризуется скорее прерывистыми, спорадическими скачками, чем постоянной скоростью изменения антигена.[62] Используя филогенетический анализ 413 полных геномов вирусов гриппа А человека, собранных по всему штату Нью-Йорк, авторы Nelson et al. В 2006 году удалось показать, что генетическое разнообразие, а не дрейф антигенов, сформировало краткосрочную эволюцию гриппа А посредством случайной миграции и реассортировки. В эволюции этих вирусов преобладает случайный импорт генетически различных вирусных штаммов из других географических регионов, а не естественный отбор. В течение данного сезона адаптивная эволюция происходит нечасто и оказывает в целом слабый эффект, о чем свидетельствуют данные, собранные для 413 геномов. Филогенетический анализ показал, что различные штаммы были получены из недавно импортированного генетического материала, в отличие от изолятов, которые циркулировали в Нью-Йорке в предыдущие сезоны. Следовательно, поток генов в эту популяцию и из нее, а не естественный отбор, был более важен в краткосрочной перспективе.
Другие животные
- Видеть H5N1 для текущего[когда? ] эпизоотический (эпидемия среди животных) и панзоотический (болезнь, поражающая животных многих видов, особенно на обширных территориях) гриппа H5N1
- Птичий грипп
Курица действовать как естественный бессимптомные носители вирусов гриппа А. До нынешнего[когда? ] Эпизоотия H5N1, штаммы вируса гриппа А передаются от диких птиц только птицам, свиньям, лошадям и т. Д. уплотнения, киты и люди; и только между людьми и свиньями и между людьми и домашней птицей; а не другие пути, такие как домашняя птица к лошади.[63]
Дикие водные птицы являются естественными хозяевами большого разнообразия вирусов гриппа А. Иногда вирусы передаются от этих птиц другим видам и могут затем вызывать опустошительные вспышки среди домашних птиц или вызывать пандемии гриппа человека.[3][4]
Было показано, что H5N1 передается тиграм, леопардам и домашним кошкам, которых кормили этим вирусом сырые домашние птицы (куры). H3N8 вирусы от лошадей пересеклись и вызвали вспышки среди собак. Лабораторные мыши были успешно инфицированы различными генотипами птичьего гриппа.[64]
Вирусы гриппа А распространяются в воздухе и в навоз, и дольше выживает в холодную погоду. Они также могут передаваться через зараженный корм, воду, оборудование и одежду; однако нет никаких доказательств того, что вирус может выжить в хорошо приготовленном мясе. Симптомы у животных различны, но вирулентные штаммы могут вызвать смерть в течение нескольких дней. Вирусы птичьего гриппа, которые Всемирная организация здоровья животных и другие тесты для борьбы с болезнями птицы включают H5N1, H7N2, H1N7, H7N3, H13N6, H5N9, H11N6, H3N8, H9N2, H5N2, H4N8, H10N7, H2N2, H8N4, H14N5, H6N5 и H12N5.
- Известные вспышки высокопатогенного гриппа среди домашних птиц в 1959–2003 гг.[65]
| Год | Площадь | Затронутый | Подтип |
|---|---|---|---|
| 1959 | Шотландия | Курица | H5N1 |
| 1963 | Англия | индюк | H7N3 |
| 1966 | Онтарио (Канада) | индюк | H5N9 |
| 1976 | Виктория (Австралия) | Курица | H7N7 |
| 1979 | Германия | Курица | H7N7 |
| 1979 | Англия | индюк | H7N7 |
| 1983 | Пенсильвания (США) * | Курица, индейка | H5N2 |
| 1983 | Ирландия | индюк | H5N8 |
| 1985 | Виктория (Австралия) | Курица | H7N7 |
| 1991 | Англия | индюк | H5N1 |
| 1992 | Виктория (Австралия) | Курица | H7N3 |
| 1994 | Квинсленд (Австралия) | Курица | H7N3 |
| 1994 | Мексика* | Курица | H5N2 |
| 1994 | Пакистан* | Курица | H7N3 |
| 1997 | Новый Южный Уэльс (Австралия) | Курица | H7N4 |
| 1997 | Гонконг (Китай) * | Курица | H5N1 |
| 1997 | Италия | Курица | H5N2 |
| 1999 | Италия* | индюк | H7N1 |
| 2002 | Гонконг (Китай) | Курица | H5N1 |
| 2002 | Чили | Курица | H7N3 |
| 2003 | Нидерланды* | Курица | H7N7 |
* Вспышки со значительным распространением на многочисленные фермы, приводящие к большим экономическим потерям. Большинство других вспышек были связаны с незначительным распространением или отсутствием распространения от первоначально зараженных ферм.
Зарегистрировано более 400 смертей морских тюленей в Новая Англия в период с декабря 1979 г. по октябрь 1980 г. от острой пневмонии, вызванной вирусом гриппа A / Seal / Mass / 1/180 (H7N7).[66]
- Свиной грипп
- Грипп свиней (или «грипп свиней») относится к подгруппе Orthomyxoviridae, вызывающих грипп и являющихся эндемичными для свиней. Виды Orthomyxoviridae, которые могут вызывать грипп у свиней, - это вирус гриппа A и вирус гриппа С, но не все генотипы этих двух видов заражают свиней. Известными подтипами вируса гриппа A, вызывающими грипп и эндемичными для свиней, являются H1N1, H1N2, H3N1 и H3N2. В 1997 году вирусы H3N2 от человека проникли в популяцию свиней, вызвав широкое распространение болезни среди свиней.[67]
- Конский грипп
- Конский грипп (или «конский грипп») относится к разновидностям вируса гриппа А, поражающим лошадей. Вирусы конского гриппа были выделены только в 1956 году. Два основных типа вируса называются конский-1 (H7N7), который обычно поражает сердечную мышцу лошади, и конский-2 (H3N8), который обычно более серьезен. Вирусы H3N8 от лошадей заразили собак.[67]
- Собачий грипп
- Собачий грипп (или «собачий грипп») относится к разновидностям вируса гриппа А, поражающим собак. Было обнаружено, что вирус гриппа лошадей H3N8 заражает и убивает - с респираторным заболеванием - собак породы борзых на ипподроме во Флориде в январе 2004 года.
- Летучий грипп
- Летучий грипп (или «Летучий грипп») относится к штаммам вируса гриппа A H17N10 и H18N11, которые были обнаружены у плодовых летучих мышей Центральной и Южной Америки, а также к вирусу H9N2, выделенному из египетских плодовых летучих мышей.[68] До сих пор неясно, циркулируют ли эти вирусы, полученные от летучих мышей, у каких-либо видов, кроме летучих мышей, и представляют ли они зоонозную угрозу. Однако первоначальная характеристика подтипа H18N11 позволяет предположить, что этот вирус гриппа летучих мышей плохо адаптирован ни к каким другим видам, кроме летучих мышей.[69]
- H3N8
- H3N8 в настоящее время является эндемичным для птиц, лошадей и собак.
Список подтипов
Вирус гриппа А имеет следующие подтипы:
- Вирус гриппа A подтипа H1N1
- Вирус гриппа A подтипа H1N2
- Вирус гриппа A подтипа H2N2
- Вирус гриппа A подтипа H2N3
- Вирус гриппа A подтипа H3N1
- Вирус гриппа A подтипа H3N2
- Вирус гриппа A подтипа H3N8
- Вирус гриппа A подтипа H5N1
- Вирус гриппа A подтипа H5N2
- Вирус гриппа A подтипа H5N3
- Вирус гриппа A подтипа H5N6
- Вирус гриппа A подтипа H5N8
- Вирус гриппа A подтипа H5N9
- Вирус гриппа A подтипа H6N1
- Вирус гриппа A подтипа H6N2
- Вирус гриппа A подтипа H7N1
- Вирус гриппа A подтипа H7N2
- Вирус гриппа A подтипа H7N3
- Вирус гриппа A подтипа H7N4
- Вирус гриппа A подтипа H7N7
- Вирус гриппа A подтипа H7N9
- Вирус гриппа A подтипа H9N2
- Вирус гриппа A подтипа H10N7
- Вирус гриппа A подтипа H10N8
- Вирус гриппа A подтипа H11N2
- Вирус гриппа A подтипа H11N9
- Вирус гриппа A подтипа H17N10
- Вирус гриппа A подтипа H18N11
Смотрите также
Примечания
- ^ «Таксономия». Международный комитет по таксономии вирусов (ICTV). Получено 19 июля 2018.
- ^ «Птичий грипп (« птичий грипп ») - Информационный бюллетень». ВОЗ.
- ^ а б Кленк Х, Матросович М, Стеч Дж (2008). «Птичий грипп: молекулярные механизмы патогенеза и круг хозяев». В Mettenleiter TC, Sobrino F (ред.). Вирусы животных: молекулярная биология. Caister Academic Press. ISBN 978-1-904455-22-6.
- ^ а б Каваока Y, изд. (2006). Вирусология гриппа: актуальные темы. Caister Academic Press. ISBN 978-1-904455-06-6.
- ^ а б «Вирусы и подтипы гриппа типа А». Центры по контролю и профилактике заболеваний. 2 апреля 2013 г.. Получено 13 июн 2013.
- ^ а б c Тонг С., Чжу Х, Ли И, Ши М, Чжан Дж., Буржуа М, Ян Х, Чен Х, Рекуэнко С., Гомес Дж., Чен Л. М., Джонсон А., Тао Й, Дрейфус К., Ю В, Макбрайд Р., Карни П. Дж. , Gilbert AT, Chang J, Guo Z, Davis CT, Paulson JC, Stevens J, Rupprecht CE, Holmes EC, Wilson IA, Donis RO (октябрь 2013 г.). «Летучие мыши Нового Света являются носителями различных вирусов гриппа А». Патогены PLOS. 9 (10): e1003657. Дои:10.1371 / journal.ppat.1003657. ЧВК 3794996. PMID 24130481.
- ^ «Уникальный новый вирус гриппа обнаружен у летучих мышей». NHS Choices. 1 марта 2012 г.. Получено 16 мая 2012.
- ^ Тонг С., Ли И, Ривайллер П., Конрарди К., Кастильо Д. А., Чен Л. М., Рекуэнко С., Эллисон Дж. А., Дэвис К. Т., Йорк И. А., Турмел А. С., Моран Д., Роджерс С., Ши М., Тао Ю., Вейл М. Р., Тан К. , Rowe LA, Sammons S, Xu X, Frace M, Lindblade KA, Cox NJ, Anderson LJ, Rupprecht CE, Donis RO (март 2012 г.). «Отдельная линия вируса гриппа А от летучих мышей». Труды Национальной академии наук Соединенных Штатов Америки. 109 (11): 4269–74. Bibcode:2012ПНАС..109.4269Т. Дои:10.1073 / pnas.1116200109. ЧВК 3306675. PMID 22371588.
- ^ Gallagher J (29 июля 2011 г.). "'Суперантитела борются с гриппом ». Новости BBC. Получено 29 июля 2011.
- ^ whitehouse.gov В архиве 9 января 2009 г. Wayback Machine Национальная стратегия борьбы с пандемическим гриппом - Введение - «Хотя за последнее столетие в науке и медицине были достигнуты значительные успехи, нам постоянно напоминают, что мы живем во вселенной микробов - вирусов, бактерий, простейших и грибов, которые постоянно меняются и адаптируются. к человеческому хозяину и защите, которую создают люди. Вирусы гриппа отличаются своей устойчивостью и адаптируемостью. Хотя науке удалось разработать высокоэффективные вакцины и средства лечения многих инфекционных заболеваний, угрожающих общественному здоровью, получение этих средств является постоянной проблемой с вирусом гриппа. Изменения в генетическом составе вируса требуют от нас разрабатывать новые вакцины на ежегодной основе и прогнозировать, какие штаммы могут преобладать. В результате, несмотря на ежегодные вакцинации, США сталкиваются с бременем гриппа, которое приводит к примерно 36 000 смертей и более 200 000 госпитализаций каждый год. Помимо этого количества человеческих жертв, Общая стоимость гриппа в США превышает 10 миллиардов долларов в год. Пандемия или всемирная вспышка нового вируса гриппа может затмить это воздействие, подавив наше здоровье и медицинские возможности, что может привести к сотням тысяч смертей, миллионам госпитализаций и сотням миллиардов долларов прямых и косвенных затрат. Эта Стратегия будет определять нашу готовность и меры реагирования для смягчения этого воздействия ».
- ^ Iuliano AD, Roguski KM, Chang HH, Muscatello DJ, Palekar R, Tempia S, Cohen C, Gran JM, Schanzer D, Cowling BJ, Wu P, Kyncl J, Ang LW, Park M, Redlberger-Fritz M, Yu H, Эспенхайн Л., Кришнан А., Эмукуле Г., ван Астен Л., Перейра да Силва С., Аунгкуланон С., Буххольц Ю., Виддоусон М. А., Брези Дж. С. (март 2018 г.). «Оценки глобальной респираторной смертности, связанной с сезонным гриппом: модельное исследование». Ланцет. 391 (10127): 1285–1300. Дои:10.1016 / с0140-6736 (17) 33293-2. ЧВК 5935243. PMID 29248255.
- ^ Даум Л.Т., Шоу М.В., Климов А.И., Канас Л.С., Масиас Е.А., Нимейер Д., Чемберс Дж. П., Рентал Р., Шреста С.К., Ачарья Р.П., Хуздар С.П., Римал Н., Мьинт К.С., Гулд П. (август 2005 г.). «Вспышка гриппа A (H3N2), Непал». Возникающие инфекционные заболевания. 11 (8): 1186–91. Дои:10.3201 / eid1108.050302. ЧВК 3320503. PMID 16102305.
«Сезон гриппа 2003–2004 гг. Был тяжелым с точки зрения воздействия на болезнь из-за широкого распространения антигенно отличных от вирусов гриппа A (H3N2) фуцзянь-подобных вирусов. Эти вирусы впервые появились поздно в течение сезона гриппа 2002–2003 гг. И продолжали сохраняться в течение доминирующий циркулирующий штамм в течение последующего сезона гриппа 2003–2004 гг., заменивший A / Panama / 2007/99-подобные вирусы H3N2 (1). Из 172 вирусов H3N2, генетически охарактеризованных Министерством обороны в 2003–2004 гг., только один изолят (из Таиланда) принадлежали к линии A / Panama. В феврале 2003 г. Всемирная организация здравоохранения (ВОЗ) изменила компонент H3N2 в вакцине против гриппа 2004–2005 гг., чтобы обеспечить защиту от широко распространенного появления вирусов, подобных Фуцзяню (2 Ежегодно обновляемая трехвалентная вакцина состоит из компонентов поверхностного гликопротеина гемагглютинина (НА) вирусов гриппа H3N2, H1N1 и B. " - ^ а б Махмуд 2005, п.126
«Вирус H5N1 в настоящее время эндемичен для домашней птицы в Азии (таблица 2-1) и занял прочную экологическую нишу, из которой представляет собой долговременную пандемическую угрозу для человека. В настоящее время эти вирусы плохо передаются от домашней птицы к человеку, и нет убедительных доказательств передачи от человека к человеку. Однако продолжающееся обширное воздействие вирусов H5N1 на человеческую популяцию увеличивает вероятность того, что вирусы приобретут необходимые характеристики для эффективной передачи от человека к человеку в результате генетической мутации или повторной сортировки с преобладающим вирусом гриппа человека А. Кроме того, современные вирусы гриппа человека H3N2 в настоящее время являются эндемичными для свиней в южном Китае (Peiris et al., 2001) и могут реассортироваться с вирусами птичьего H5N1 в этом «промежуточном хозяине». Поэтому крайне важно, чтобы вспышки болезни H5N1 среди домашней птицы в Азии быстро и устойчиво контролировались. Сезонность болезни домашней птицы вместе с уже принятыми мерами борьбы, вероятно, временно снизит частоту вспышек гриппа H5N1 и вероятность заражения человека ". - ^ Gallagher J (29 июля 2011 г.). "'Суперантитела борются с гриппом ». Новости BBC.
- ^ «Ученые приветствуют перспективу создания универсальной вакцины от гриппа». 29 июля 2011 г.
- ^ Чан А.Л. (28 июля 2011 г.). «Универсальная вакцина против гриппа на горизонте: исследователи обнаружили« суперантитела »'". HuffPost.
- ^ "Подробности - Библиотека изображений общественного здравоохранения (PHIL)". phil.cdc.gov. Получено 24 апреля 2018.
- ^ а б Сугита Ю., Нода Т., Сагара Х., Каваока Ю. (ноябрь 2011 г.). «Ультрацентрифугирование деформирует нефиксированные вирионы гриппа А». Журнал общей вирусологии. 92 (Pt 11): 2485–93. Дои:10.1099 / vir.0.036715-0. ЧВК 3352361. PMID 21795472.
- ^ Накацу С., Мураками С., Синдо К., Хоримото Т., Сагара Н., Нода Т., Каваока И. (март 2018 г.). "Восемь организованных рибонуклеопротеиновых комплексов, содержащих вирусы гриппа C и D". Журнал вирусологии. 92 (6): e02084–17. Дои:10.1128 / jvi.02084-17. ЧВК 5827381. PMID 29321324.
- ^ Нода Т (2011). «Нативная морфология вирионов гриппа». Границы микробиологии. 2: 269. Дои:10.3389 / fmicb.2011.00269. ЧВК 3249889. PMID 22291683.
- ^ Дадонайте Б., Виджаякришнан С., Фодор Е., Бхелла Д., Хатчинсон ЕС (август 2016 г.). «Вирусы нитчатого гриппа». Журнал общей вирусологии. 97 (8): 1755–64. Дои:10.1099 / jgv.0.000535. ЧВК 5935222. PMID 27365089.
- ^ Селади-Шульман Дж., Сталь Дж., Лоуэн А.С. (декабрь 2013 г.). «Сферические вирусы гриппа имеют преимущество в пригодности для яиц с эмбрионами, в то время как штаммы, продуцирующие нити, отбираются in vivo». Журнал вирусологии. 87 (24): 13343–53. Дои:10.1128 / JVI.02004-13. ЧВК 3838284. PMID 24089563.
- ^ Мосли В.М., Вайкофф Р.В. (март 1946 г.). «Электронная микрография вируса гриппа». Природа. 157 (3983): 263. Bibcode:1946Натура.157..263М. Дои:10.1038 / 157263a0. PMID 21016866. S2CID 6478026.
- ^ а б c Бувье Н.М., Палезе П. (сентябрь 2008 г.). «Биология вирусов гриппа». Вакцина. 26 (Дополнение 4): D49–53. Дои:10.1016 / j.vaccine.2008.07.039. ЧВК 3074182. PMID 19230160.
- ^ Коэн М., Чжан XQ, Сенаати HP, Чен Х.В., Варки Н.М., Schooley RT, Gagneux P (ноябрь 2013 г.). «Грипп A проникает в слизь хозяина, расщепляя сиаловые кислоты нейраминидазой». Журнал вирусологии. 10: 321. Дои:10.1186 / 1743-422x-10-321. ЧВК 3842836. PMID 24261589.
- ^ а б Suzuki Y (март 2005 г.). «Сиалобиология гриппа: молекулярный механизм вариации круга хозяев вирусов гриппа». Биологический и фармацевтический бюллетень. 28 (3): 399–408. Дои:10.1248 / bpb.28.399. PMID 15744059.
- ^ Wilson JC, von Itzstein M (июль 2003 г.). «Последние стратегии в поисках новых методов лечения гриппа». Текущие цели в отношении лекарств. 4 (5): 389–408. Дои:10.2174/1389450033491019. PMID 12816348.
- ^ Линч Дж. П., Уолш Э. Э. (апрель 2007 г.). «Грипп: развивающиеся стратегии лечения и профилактики». Семинары по респираторной медицине и реанимации. 28 (2): 144–58. Дои:10.1055 / с-2007-976487. PMID 17458769.
- ^ Эйсфельд AJ, Neumann G, Kawaoka Y (январь 2015 г.). «В центре: рибонуклеопротеины вируса гриппа А». Обзоры природы. Микробиология. 13 (1): 28–41. Дои:10.1038 / nrmicro3367. ЧВК 5619696. PMID 25417656.
- ^ Хаперский Д.А., Шмалинг С., Ларкинс-Форд Дж., Маккормик С., Гаглия М.М. (февраль 2016 г.). «Селективная деградация транскриптов РНК-полимеразы II хозяина под действием белка выключения хозяина PA-X вируса гриппа A». Патогены PLOS. 12 (2): e1005427. Дои:10.1371 / journal.ppat.1005427. ЧВК 4744033. PMID 26849127.
- ^ Те Велтуис А.Дж., Фодор Э. (август 2016 г.). «РНК-полимераза вируса гриппа: понимание механизмов синтеза вирусной РНК». Обзоры природы. Микробиология. 14 (8): 479–93. Дои:10.1038 / nrmicro.2016.87. ЧВК 4966622. PMID 27396566.
- ^ а б Смит А.Е., Хелениус А. (апрель 2004 г.). «Как вирусы попадают в клетки животных». Наука. 304 (5668): 237–42. Bibcode:2004Наука ... 304..237S. Дои:10.1126 / science.1094823. PMID 15073366. S2CID 43062708.
- ^ Барри Р.Д. (август 1961 г.). «Размножение вируса гриппа. II. Множественная реактивация вируса, облученного ультрафиолетом». Вирусология. 14 (4): 398–405. Дои:10.1016/0042-6822(61)90330-0. HDL:1885/109240. PMID 13687359.
- ^ Хенле В., Лю О.К. (октябрь 1951 г.). «Исследования взаимодействий вирус-хозяин в системе вируса гриппа цыпленка. VI. Доказательства реактивации множественности инактивированного вируса». Журнал экспериментальной медицины. 94 (4): 305–22. Дои:10.1084 / jem.94.4.305. ЧВК 2136114. PMID 14888814.
- ^ Гилкер Дж. К., Павиланис В., Гис Р. (июнь 1967 г.). «Реактивация множественности в гамма-облученных вирусах гриппа». Природа. 214 (5094): 1235–7. Bibcode:1967Натура.214.1235G. Дои:10.1038 / 2141235a0. PMID 6066111. S2CID 4200194.
- ^ Петерханс Э (май 1997 г.). «Окислители и антиоксиданты при вирусных заболеваниях: механизмы болезни и регуляция метаболизма». Журнал питания. 127 (5 Прил.): 962S – 965S. Дои:10.1093 / jn / 127.5.962S. PMID 9164274.
- ^ Бернштейн Х., Байерли Х.С., Хопф Ф.А., Мичод Р. Э. (октябрь 1984 г.). «Происхождение пола». Журнал теоретической биологии. 110 (3): 323–51. Дои:10.1016 / S0022-5193 (84) 80178-2. PMID 6209512.
- ^ CDC Основные факты о птичьем гриппе (птичьем гриппе) и вирусе птичьего гриппа A (H5N1)
- ^ Episcopio D, Aminov S, Benjamin S, Germain G, Datan E, Landazuri J, Lockshin RA, Zakeri Z (апрель 2019). «Аторвастатин ограничивает способность вируса гриппа генерировать липидные капли и сильно подавляет репликацию вируса». Журнал FASEB. 33 (8): 9516–9525. Дои:10.1096 / fj.201900428RR. ЧВК 6662987. PMID 31125254.
- ^ de Jong MD, Bach VC, Phan TQ, Vo MH, Tran TT, Nguyen BH, Beld M, Le TP, Truong HK, Nguyen VV, Tran TH, Do QH, Farrar J (февраль 2005 г.). «Смертельный птичий грипп A (H5N1) у ребенка с диареей с последующей комой». Медицинский журнал Новой Англии. 352 (7): 686–91. Дои:10.1056 / NEJMoa044307. PMID 15716562. S2CID 17703507.
- ^ ВОЗ: «Новый штамм птичьего гриппа в Китае» - один из самых смертоносных.. МеркоПресс. Получено 6 декабря 2020.
- ^ «Следующая пандемия и как ее предотвратить: придерживайтесь растительной диеты». Южно-Китайская утренняя почта. 19 Октябрь 2020. Получено 6 декабря 2020.
- ^ Бостон, 677 Хантингтон-авеню; Ma 02115 + 1495-1000 (24 октября 2013 г.). "Совершая прыжок". Новости. Получено 6 декабря 2020.
- ^ Унгчусак, Кумнуан; Ауеваракул, Прасерт; Доуэлл, Скотт Ф .; Китфати, Рунгруенг; Ауванит, Ваттана; Путхаватана, Пилайпан; Уипрасерткуль, Монгкол; Бооннак, Кобпорн; Питтаявонганон, Чакрарат; Кокс, Нэнси Дж .; Заки, Шериф Р. (27 января 2005 г.). «Вероятная передача птичьего гриппа A (H5N1) от человека к человеку». Медицинский журнал Новой Англии. 352 (4): 333–340. Дои:10.1056 / NEJMoa044021. ISSN 0028-4793. PMID 15668219.
- ^ «Первый случай заболевания человека редким вариантом гриппа H1N2 зарегистрирован в Канаде». IFLScience. Получено 6 декабря 2020.
- ^ Махмуд 2005, п.7
- ^ "NOVA | scienceNOW | Reviving the Virus (non-Flash) | PBS". www.pbs.org. Получено 6 декабря 2020.
- ^ Подробная диаграмма его эволюции Вот В архиве 9 мая 2009 г. Wayback Machine в PDF называется Экология и эволюция гриппа
- ^ Махмуд 2005, п.115
«Существует особое давление, чтобы признать и принять во внимание уроки прошлых пандемий гриппа в тени тревожного сезона гриппа 2003–2004 годов. Тяжелая форма гриппа с ранним началом A H3N2 попала в заголовки газет, когда она унесла жизни нескольких детей в Соединенные Штаты в конце 2003 года. В результате более высокий, чем обычно, спрос на ежегодную вакцину, инактивированную против гриппа, превысил предложение вакцины, от 10 до 20 процентов которой обычно остаются неиспользованными. Поскольку статистические данные о смертях от гриппа у детей ранее не собирались, неизвестно, были ли Сезон 2003–2004 гг. стал свидетелем значительных изменений в структуре смертности ». - ^ Причина В архиве 26 октября 2006 г. Wayback Machine Альтман Л.К. (15 января 2006 г.). «Вирус гриппа этого сезона устойчив к 2 стандартным лекарствам». Нью-Йорк Таймс.
- ^ CBS Новости статья Десятки людей в Японии могут заболеть легким птичьим гриппом Январь 2006 г.
- ^ Огата Т., Ямадзаки Ю., Окабе Н., Накамура Ю., Таширо М., Нагата Н., Итамура С., Ясуи Ю., Накашима К., Дои М., Изуми Ю., Фудзида Т., Ямато С., Кавада Ю. (июль 2008 г.). «Инфекция птичьего гриппа человека H5N2 в Японии и факторы, связанные с высоким титром нейтрализующих H5N2 антител». Журнал эпидемиологии. 18 (4): 160–6. Дои:10.2188 / jea.JE2007446. ЧВК 4771585. PMID 18603824.
- ^ ВОЗ
- ^ а б CDC Инфекция птичьего гриппа у людей
- ^ Твид С.А., Сковронски Д.М., Дэвид С.Т., Лардер А., Петрик М., Лис В., Ли Й., Кац Дж., Крайден М., Телье Р., Хальперт С., Херст М., Астелл С., Лоуренс Д., Мак А. (декабрь 2004 г.). «Болезнь человека от птичьего гриппа H7N3, Британская Колумбия». Возникающие инфекционные заболевания. 10 (12): 2196–9. Дои:10.3201 / eid1012.040961. ЧВК 3323407. PMID 15663860.
- ^ Шнирринг Л. (2 апреля 2013 г.). «Китай сообщает о еще 4 случаях инфицирования H7N9». Новости CIDRAP.
- ^ "Вирус птичьего гриппа A (H7N9) | Птичий грипп (грипп)". www.cdc.gov. Получено 24 февраля 2017.
- ^ niaid.nih.gov В архиве 26 декабря 2005 г. Wayback Machine Хронология пандемий человеческого гриппа
- ^ Таубенбергер Дж. К., Моренс Д. М. (январь 2006 г.). «Грипп 1918 года: мать всех пандемий». Возникающие инфекционные заболевания. 12 (1): 15–22. Дои:10.3201 / eid1201.050979. ЧВК 3291398. PMID 16494711.
- ^ Science Daily статья Новое исследование имеет важное значение для эпиднадзора за гриппом опубликовано 27 октября 2006 г.
- ^ Nelson MI, Simonsen L, Viboud C, Miller MA, Taylor J, George KS, Griesemer SB, Ghedin E, Ghedi E, Sengamalay NA, Spiro DJ, Volkov I, Grenfell BT, Lipman DJ, Taubenberger JK, Holmes EC (декабрь 2006 г.) ). «Стохастические процессы - ключевые детерминанты краткосрочной эволюции вируса гриппа A». Патогены PLOS. 2 (12): e125. Дои:10.1371 / journal.ppat.0020125. ЧВК 1665651. PMID 17140286.
- ^ Smith DJ, Lapedes AS, de Jong JC, Bestebroer TM, Rimmelzwaan GF, Osterhaus AD, Fouchier RA (июль 2004 г.). «Картирование антигенной и генетической эволюции вируса гриппа». Наука. 305 (5682): 371–6. Bibcode:2004Наука ... 305..371С. Дои:10.1126 / science.1097211. PMID 15218094. S2CID 1258353.
- ^ Махмуд 2005, п.30
- ^ Махмуд 2005, п.82
«Интересно, что рекомбинантные вирусы гриппа, содержащие HA и NA 1918 года, и до трех дополнительных генов, происходящих от вируса 1918 года (другие гены происходят от вируса A / WSN / 33), все были очень вирулентными у мышей (Tumpey et al., 2004) .Кроме того, экспрессионный микроматричный анализ, проведенный на цельной легочной ткани мышей, инфицированных рекомбинантом 1918 HA / NA, показал повышенную регуляцию генов, участвующих в апоптозе, повреждении ткани и окислительном повреждении (Kash et al., 2004). необычно, потому что вирусы с генами 1918 года не были адаптированы для мышей. Завершение последовательности всего генома вируса 1918 года, а также реконструкция и характеристика вирусов с генами 1918 года при соответствующих условиях биобезопасности прольют больше света на эти выводы и должен позволить окончательно изучить это объяснение.Антигенный анализ рекомбинантных вирусов, обладающих 1918 HA и NA, с помощью тестов ингибирования гемагглютинации с использованием хорька и c hicken антисыворотка предположила тесную связь с вирусом A / swine / Iowa / 30 и вирусами H1N1, выделенными в 1930-х годах (Tumpey et al., 2004), что дополнительно подтверждает данные Shope из 1930-х годов (Shope, 1936). Интересно, что когда мышей иммунизировали различными штаммами вируса H1N1, исследования контрольного заражения с использованием вирусов, подобных 1918, выявили частичную защиту от этого лечения, что позволяет предположить[когда? ] стратегии вакцинации адекватны против вируса, подобного 1918 г. (Tumpey et al., 2004) ». - ^ «Птичий грипп A (H5N1) - обновленная информация 31: Ситуация (домашняя птица) в Азии: необходимость долгосрочных ответных мер, сравнение с предыдущими вспышками». Предупреждение об эпидемиях и пандемиях и ответные меры (EPR). ВОЗ. 2004 г.
Известные вспышки высокопатогенного гриппа среди птиц в 1959–2003 гг. - ^ Джерачи Дж. Р., Сент-Обен Д. Д., Баркер И. К., Вебстер Р. Г., Хиншоу В. С., Бин В. Дж., Рунке Г. Л., Прескотт Д. Н., Ранний Г., Бейкер А. С., Мэдофф С., Скули Р. Т. (февраль 1982 г.). «Массовая гибель морских тюленей: пневмония, связанная с вирусом гриппа А». Наука. 215 (4536): 1129–31. Bibcode:1982Научный ... 215.1129G. Дои:10.1126 / science.7063847. PMID 7063847.
Более 400 морских тюленей, большинство из которых были неполовозрелыми, умерли вдоль побережья Новой Англии в период с декабря 1979 по октябрь 1980 года от острой пневмонии, связанной с вирусом гриппа A / Seal / Mass / 1/180 (H7N7). Вирус имеет птичьи характеристики, воспроизводится преимущественно у млекопитающих и вызывает легкое респираторное заболевание у экспериментально зараженных тюленей. Сопутствующая инфекция с ранее не описанной микоплазмой или неблагоприятные условия окружающей среды могли вызвать эпизоотию. Сходство между этой эпизоотической смертностью и смертностью других тюленей в прошлом предполагает, что эти события могут быть связаны общими биологическими и экологическими факторами.
- ^ а б CDC Центры по контролю и профилактике заболеваний - Передача вирусов гриппа А между животными и людьми
- ^ Кандейл А., Гомаа М.Р., Шехата М.М., Эль-Тавил А.Н., Махмуд С.Х., Багато О. (январь 2019 г.). «Выделение и характеристика отличного вируса гриппа А от египетских летучих мышей». Журнал вирусологии. 93 (2): e01059-18. Дои:10.1128 / JVI.01059-18. ЧВК 6321940. PMID 30381492.
- ^ Ciminski K, Ran W., Gorka M, Lee J, Schinköthe J, Eckley M, Murrieta MA, Aboellail TA, Campbell CL, Ebel GD, Ma J, Pohlmann A, Franzke K, Ulrich R, Hoffmann D, Garcia-Sastre A, Ма В., Шунтц Т., Бир М., Швеммле М. (2019). «Вирусы гриппа летучих мышей передаются среди летучих мышей, но плохо адаптированы к другим видам, кроме летучих мышей». Природная микробиология. 4 (12): 2298–2309. Дои:10.1038 / s41564-019-0556-9. PMID 31527796. S2CID 202580293.
дальнейшее чтение
- Официальные источники
- Птичий грипп и Пандемии гриппа от Центры по контролю и профилактике заболеваний
- Птичий грипп Часто задаваемые вопросы от Всемирная организация здоровья
- Информация о птичьем гриппе от Продовольственная и сельскохозяйственная организация
- Информационный веб-сайт правительства США о птичьем гриппе
- Европейский центр профилактики и контроля заболеваний (ECDC ) Стокгольм, Швеция
- Общая информация
- "Птичий грипп и ты" Полноцветный плакат предоставлен Центром технологий и политики национальной безопасности Национальный университет обороны, в сотрудничестве с Центром политики здравоохранения национальной безопасности
- Отчет о гриппе 2006 г. Электронная книга. Информация о качестве исследования. Настоятельно рекомендуется.
- Спецвыпуск о птичьем гриппе из Природа
- Отчеты о природе: Домашняя страница: Птичий грипп
- Бейгель Дж. Х., Фаррар Дж., Хан А. М., Хайден Ф. Г., Хайер Р., де Йонг, доктор медицины, Лочиндарат С., Нгуен Т. К., Нгуен Т. Х., Тран Т.Х., Николл А., Тач С., Юен К.Ю. (сентябрь 2005 г.). «Инфекция птичьего гриппа A (H5N1) у людей». Медицинский журнал Новой Англии. 353 (13): 1374–85. CiteSeerX 10.1.1.730.7890. Дои:10.1056 / NEJMra052211. PMID 16192482.
- Пандемический грипп: меры внутренней готовности Отчет Исследовательской службы Конгресса о готовности к пандемии.
- Справочник по птичьему гриппу и его симптомам из BBC Здоровье
- Разнообразие изображений и изображений птичьего гриппа
- Махмуд (2005). Стейси Л. Ноблер; Элисон Мак; Махмуд, Адель; Стэнли М. Лемон (ред.). Угроза пандемического гриппа: готовы ли мы? : резюме семинара / подготовлено для Форума по микробным угрозам Совета по глобальному здоровью. Издательство национальных академий. п. 285. ISBN 0-309-09504-2.
Высокопатогенный вирус птичьего гриппа входит в каждую десятку списка потенциальных агентов сельскохозяйственного биологического оружия.
- Махмуд А.А., Институт медицины, Ноблер С., Мак А. (2005). Угроза пандемического гриппа: готовы ли мы ?: Резюме семинара. Вашингтон, округ Колумбия: National Academies Press. ISBN 978-0-309-09504-4.
- 'Угроза птичьего гриппа': HealthPolitics.com
- Неизбежна ли глобальная пандемия гриппа? из Инфекционный контроль сегодня.
- Птичий грипп - реальная угроза пандемии для людей Леонарда Крейна, автора Девятый день творения.
- Ссылки на фотографии птичьего гриппа (Hardin MD / Univ of Iowa)
- Каваока Y (2006). Вирусология гриппа: актуальные темы. Caister Academic Pr. ISBN 978-1-904455-06-6.
- Собрино Ф, Меттенлейтер Т (2008). Вирусы животных: молекулярная биология. Caister Academic Pr. ISBN 978-1-904455-22-6.
внешняя ссылка
- База данных исследований гриппа - База данных геномных последовательностей гриппа и сопутствующей информации.
- Портал Здоровье-ЕС Евросоюз ответ на грипп

