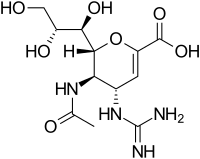
Занамивир - Zanamivir
 | |
| Клинические данные | |
|---|---|
| Произношение | /zəˈпæмɪvɪər/ |
| Торговые наименования | Реленца |
| Другие имена | 5-ацетамидо-4-гуанидино-6- (1,2,3-тригидроксипропил) - 5,6-дигидро-4ЧАС-пиран-2-карбоновая кислота |
| AHFS /Drugs.com | Монография |
| Беременность категория |
|
| Маршруты администрация | Вдыхание, в / в |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 2% (устно) |
| Связывание с белками | <10% |
| Метаболизм | Незначительный |
| Устранение период полураспада | 2,5–5,1 часов |
| Экскреция | Почечный |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Лиганд PDB | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.218.632 |
| Химические и физические данные | |
| Формула | C12ЧАС20N4О7 |
| Молярная масса | 332.313 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| (проверять) | |
Занамивир это лекарство, используемое для лечения и профилактики грипп вызванный грипп А и B-вирусы. Это ингибитор нейраминидазы и был разработан австралийской биотехнологической фирмой Biota Holdings. Он был лицензирован Glaxo в 1990 году и одобрен в США в 1999 году только для использования в качестве лекарства от гриппа. В 2006 году он был одобрен для профилактики гриппа A и B.[1] Занамивир был первым коммерчески разработанным ингибитором нейраминидазы. В настоящее время он продается GlaxoSmithKline под торговое наименование Реленца в виде порошка для пероральных ингаляций.
Медицинское использование
Занамивир используется для лечения инфекций, вызванных вирусами гриппа A и B, но для здоровых людей его польза в целом невелика. Это снижает риск развития симптоматического, но не бессимптомного гриппа. Сочетание диагностической неопределенности, риска устойчивости к вирусным штаммам, возможных побочных эффектов и финансовых затрат перевешивает небольшие преимущества занамивира для профилактики и лечения здоровых людей.[2]По состоянию на 2009 год ни один грипп в США не проявил никаких признаков устойчивости.[3] С тех пор гены, экспрессирующие устойчивость к занамивиру, были обнаружены у китайцев, инфицированных птичьим гриппом A H7N9 во время лечения занамивиром.[4]
Уход
У здоровых в остальном людей польза в целом невелика.[2] Занамивир сокращает продолжительность симптомов гриппоподобного заболевания (неподтвержденный грипп или «грипп») менее чем на сутки. У детей с астмой не было явного влияния на время до первого облегчения симптомов.[5] Неясно, влияет ли это на риск необходимости госпитализации или на риск смерти.[2] Нет доказательств того, что занамивир уменьшал количество госпитализаций, пневмонии и других осложнений гриппа, таких как бронхит, инфекция среднего уха, и синусит.[5][6] Занамивир не снизил риск опосредованного исследователем самооценки. пневмония или рентгенологически подтвержденная пневмония у взрослых. Влияние на пневмонию у детей также было незначительным.[7]
Профилактика
Доказательства от слабых до умеренных указывают на то, что это снижает риск заражения гриппом на 1–12% у тех, кто подвергается воздействию.[2] Профилактические испытания показали, что занамивир снижает риск симптоматического гриппа у отдельных лиц и домашних хозяйств, но не было доказательств его воздействия на бессимптомный грипп или другие гриппоподобные заболевания. Также не было доказательств снижения риска передачи вируса гриппа от человека к человеку.[5]Доказательства пользы в профилактике гриппа у детей слабы, и есть опасения по поводу предвзятость публикации в литературе.[8]
Сопротивление
По состоянию на 2009 год ни один грипп в США не проявил никаких признаков устойчивости.[3] А метаанализ с 2011 г. обнаружено, что о резистентности к занамивиру сообщалось редко.[9] У некоторых людей устойчивость к противовирусным препаратам может возникать во время или после лечения противовирусными препаратами (например, иммуносупрессивный ).[10] В 2013 г. гены, экспрессирующие устойчивость к занамивиру (и осельтамивир ) были обнаружены у китайских пациентов, инфицированных птичьим гриппом A H7N9.[4]
Побочные эффекты
Дозирование ограничено путем ингаляции. Это ограничивает его использование, так как лечение астматиков может вызвать бронхоспазмы.[11] В 2006 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) обнаружили, что проблемы с дыханием (бронхоспазм), включая летальные исходы, были зарегистрированы у некоторых пациентов после первоначального одобрения препарата Реленза. Большинство этих пациентов страдали астмой или хронической обструктивной болезнью легких. Таким образом, Relenza не рекомендуется для лечения или профилактики сезонного гриппа у лиц с астмой или хронической обструктивной болезнью легких.[12] В 2009 году вкладыш в упаковке занамивира содержит предупредительную информацию о риске бронхоспазма у пациентов с респираторными заболеваниями.[13]GlaxoSmithKline (GSK) и FDA уведомили медицинских работников об отчете о смерти пациента с гриппом, получившего ингаляционный порошок занамивира, который растворяли и вводили с помощью искусственной вентиляции легких.[14]
У взрослых в исследованиях не было повышенного риска нежелательных явлений, о которых сообщалось. Доказательств возможного вреда, связанного с лечением детей занамивиром, было мало.[5] Не известно, что занамивир вызывает токсические эффекты и имеет низкое системное воздействие на организм человека.[15]
Механизм действия
Занамивир работает путем привязки к активный сайт из нейраминидаза белок, из-за чего вирус гриппа не может покинуть свою хозяйскую клетку и заразить других.[16] Он также является ингибитором репликации вируса гриппа. in vitro и in vivo. В клинических испытаниях было обнаружено, что занамивир снижает время исчезновения симптомов на 1,5 дня, если лечение было начато в течение 48 часов с момента появления симптомов.
В биодоступность занамивира составляет 2%. После ингаляции занамивир концентрируется в легких и ротоглотка, где до 15% дозы абсорбируется и выводится с мочой.[17]
История
Занамивир был впервые произведен в 1989 году учеными под руководством Питер Колман[18][19] и Джозеф Варгезе[20] на австралийском CSIRO, в сотрудничестве с Викторианский фармацевтический колледж, а Университет Монаша. Занамивир был первым из ингибиторы нейраминидазы. Открытие было первоначально профинансировано австралийской биотехнологической компанией Biota и являлось частью продолжающейся программы Biota по разработке противовирусных агентов с помощью рациональный дизайн лекарств. Его стратегия основывалась на доступности структуры нейраминидазы гриппа посредством Рентгеновская кристаллография. Еще в 1974 г. было известно, что 2-дезокси-2,3-дидегидро-N-ацетилнейраминовая кислота (ДАНА), а сиаловая кислота аналог, является ингибитором нейраминидазы.[21]
Вычислительная химия методы были использованы для исследования активного центра фермента в попытке создать производные DANA, которые будут прочно связываться с аминокислотными остатками каталитического сайта, поэтому будут мощными и специфическими ингибиторами фермента. Программное обеспечение GRID от Молекулярное открытие был использован для определения энергетически выгодных взаимодействий между различными функциональными группами и остатками в каньоне каталитического сайта. Это исследование показало, что в активном центре нейраминидазы возникает отрицательно заряженная зона, которая совпадает с C4 гидроксильная группа ДАНА. Таким образом, этот гидроксил заменяется положительно заряженной аминогруппой; Было показано, что 4-амино DANA в 100 раз лучше в качестве ингибитора, чем DANA, благодаря образованию солевого мостика с консервативной глутаминовой кислотой (119) в активном центре. Также было замечено, что Glu 119 находится на дне консервативного кармана в активном сайте, который достаточно велик, чтобы вместить более крупный, но более простой гуанидин функциональная группа.[22] Результатом стал занамивир, аналог нейраминидазы в переходном состоянии.[23]
Поскольку Biota была небольшой компанией, у нее не было ресурсов, чтобы самостоятельно вывести занамивир на рынок. В 1990 году патентные права на занамивир были переданы Glaxo, сейчас GlaxoSmithKline (ГСК). Лицензионное соглашение давало Biota право на получение роялти в размере 7% от продаж занамивира Glaxo.
В 1999 году продукт был одобрен для продажи в США и Европе для лечения гриппа A и B. Консультативный комитет FDA 13 голосами против 4 рекомендовал не одобрять его, поскольку он неэффективен и не более эффективен. чем плацебо, когда пациенты принимали другие препараты, такие как парацетамол. Но руководство FDA отклонило комитет и раскритиковало его рецензента, биостатиста Майкла Элашова. Обзор осельтамивира, который также находился в процессе утверждения в то время, был отозван у него и передан другому лицу.[24] В 2006 году занамивир был одобрен в США и Европе для профилактики гриппа A и B.[1]
Хотя занамивир был первым ингибитором нейраминидазы, появившимся на рынке, он всего на несколько месяцев опередил второго участника. осельтамивир (Тамифлю) в форме капсул для перорального применения.
Когда занамивир впервые поступил в продажу в США в 1999/2000 году, он занял лишь 25% рынка противовирусных препаратов от гриппа, несмотря на масштабную рекламную кампанию. К концу этого сезона Тамифлю был лучше занамивира 3: 1. В течение этого сезона занамивир получил всемирные предупреждения о безопасности, связанные с риском бронхоспазма и смерти. Затем Glaxo сократила продажи занамивира, и доминирование Тамифлю увеличилось. Больше, чем АМЕРИКАНСКИЙ ДОЛЛАР$ Занамивир на сумму 20 миллионов, проданный Glaxo в первом сезоне в США, был возвращен компании в следующие два сезона, поскольку его продажи пациентам были намного меньше, чем ожидалось.
Компания Biota возбудила судебное дело в 2004 году, утверждая, что сокращение продаж занамивира компанией Glaxo является нарушением контракта. Биота заявила о Австралийский доллар 700 миллионов от Glaxo. После того, как Biota потратила четыре года, пытаясь продвинуть свое дело, и понесла судебные издержки в размере 50 миллионов австралийских долларов, в июле 2008 года компания отказалась от иска, взыскав лишь 20 миллионов австралийских долларов, включая судебные издержки после урегулирования при посредничестве. Биота отказалась от ранее сделанного Glaxo тактического предложения в размере 75 миллионов австралийских долларов плюс судебные издержки.
В августе 2006 года Германия объявила, что купит 1,7 миллиона доз занамивира в рамках своей стратегии подготовки против птичьего гриппа. «Покупка Германии показывает, что страны начинают сбалансированно относиться к готовности к гриппу», - сказал Саймон Такер, руководитель исследований в Мельбурнской компании Biota, где изначально был разработан занамивир.[16]
В апреле 2009 г. многие случаи свиной грипп (Вирус типа H1N1) были зарегистрированы в США и Мексике. Занамивир - один из двух препаратов, назначаемых для его лечения. В исследовании, опубликованном в июне 2009 г., подчеркивалась срочная необходимость увеличения запасов осельтамивира дополнительными противовирусными препаратами, включая занамивир, на основе оценки эффективности этих препаратов в сценарии, согласно которому нейраминидаза свиного гриппа (NA) H1N1 2009 г. должна была приобрести Мутация устойчивости к тамифлю (His274Tyr), которая в настоящее время широко распространена в 99,6% всех протестированных сезонных штаммов H1N1.[25]
В январе 2011 года GSK объявила, что начнет фазу III испытаний занамивира для внутривенного введения в исследовании, которое будет охватывать 20 стран Северного и Южного полушарий.[26]
Рекомендации
- ^ а б «FDA утверждает второй препарат для профилактики гриппа A и B у взрослых и детей. Пресс-релиз FDA от 29 марта 2006 г.». FDA.
- ^ а б c d Michiels, B .; Van Puyenbroeck, K .; Verhoeven, V .; Vermeire, E .; Коенен, С. (2013). «Значение ингибиторов нейраминидазы для профилактики и лечения сезонного гриппа: систематический обзор систематических обзоров». PLOS One. 8 (4): e60348. Bibcode:2013PLoSO ... 860348M. Дои:10.1371 / journal.pone.0060348. ЧВК 3614893. PMID 23565231.
- ^ а б «Сезон гриппа 2008-2009 гг., 32 неделя, завершившаяся 15 августа 2009 г.». Активность гриппа и эпиднадзор. Центры по контролю и профилактике заболеваний (CDC). 21 августа 2009 г.
- ^ а б Hu, Y .; Lu, S .; Песня, З .; Wang, W .; Hao, P .; Li, J .; Чжан, X .; Yen, H.L .; Ши, Б .; Li, T .; Guan, W .; Xu, L .; Liu, Y .; Wang, S .; Чжан, X .; Tian, D .; Zhu, Z .; He, J .; Хуанг, К .; Chen, H .; Zheng, L .; Li, X .; Ping, J .; Канг, Б .; Xi, X .; Жа, Л .; Li, Y .; Zhang, Z .; Peiris, M .; Юань, З. (2013). «Связь между неблагоприятным клиническим исходом заболевания человека, вызванным новым вирусом гриппа H7N9, и устойчивым выделением вируса и возникновением устойчивости к противовирусным препаратам». Ланцет. 381 (9885): 2273–2279. Дои:10.1016 / S0140-6736 (13) 61125-3. PMID 23726392.
- ^ а б c d Джефферсон, Т; Джонс, Массачусетс; Доши, П; Дель Мар, CB; Hama, R; Томпсон, MJ; Спенсер, EA; Онакпоя, я; Махтани, КР; Nunan, D; Ховик, Дж; Хенеган, CJ (10 апреля 2014 г.). «Ингибиторы нейраминидазы для профилактики и лечения гриппа у здоровых взрослых и детей» (PDF). Кокрановская база данных систематических обзоров. 4 (4): CD008965. Дои:10.1002 / 14651858.CD008965.pub4. ЧВК 6464969. PMID 24718923.
- ^ Хенеган, CJ; Онакпоя, я; Томпсон, М; Спенсер, EA; Джонс, М; Джефферсон, Т. (9 апреля 2014 г.). «Занамивир от гриппа у взрослых и детей: систематический обзор отчетов о клинических исследованиях и резюме комментариев регулирующих органов». BMJ (под ред. Клинических исследований). 348: g2547. Дои:10.1136 / bmj.g2547. ЧВК 3981976. PMID 24811412.
- ^ Heneghan, C.J .; Onakpoya, I .; Томпсон, М .; Спенсер, Э. А .; Jones, M .; Джефферсон, Т. (9 апреля 2014 г.). «Занамивир от гриппа у взрослых и детей: систематический обзор отчетов о клинических исследованиях и резюме комментариев регулирующих органов». BMJ. 348 (апрель 09): g2547. Дои:10.1136 / bmj.g2547. ЧВК 3981976. PMID 24811412.
- ^ Ван, К; Шун-Шин, М; Gill, P; Perera, R; Харден, А (18 апреля 2012 г.). «Ингибиторы нейраминидазы для профилактики и лечения гриппа у детей (только опубликованные испытания)». Кокрановская база данных систематических обзоров. 4 (4): CD002744. Дои:10.1002 / 14651858.CD002744.pub4. ЧВК 6599832. PMID 22513907.
- ^ Торлунд, Кристиан; Авад, Тахани; Бойвин, Гай; Табане, Лехана (2011). «Систематический обзор устойчивости гриппа к ингибиторам нейраминидазы». BMC Инфекционные болезни. 11 (1): 134. Дои:10.1186/1471-2334-11-134. ЧВК 3123567. PMID 21592407.
- ^ «Противовирусные препараты от гриппа: резюме для врачей». CDC. 2018-05-11. Получено 21 апреля 2014.
- ^ Хайден Ф.Г. (декабрь 2001 г.). «Перспективы использования противовирусных препаратов во время пандемического гриппа». Философские труды Лондонского королевского общества. Серия B, Биологические науки. 356 (1416): 1877–84. Дои:10.1098 / rstb.2001.1007. ЧВК 1088564. PMID 11779387.
- ^ «FDA одобряет второй препарат для профилактики гриппа A и B у взрослых и детей». Пресс-релиз FDA.
- ^ «Безопасное и надлежащее использование препаратов от гриппа». Консультации по общественному здравоохранению (лекарственные препараты). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA). 30 апреля 2009 г. Архивировано с оригинал на 2009-11-04. Получено 2009-11-11.
- ^ https://www.fda.gov/Safety/MedWatch/SafetyInformation/SafetyAlertsforHumanMedicalProducts/ucm186081.htm
- ^ Freund, B; Гравенштейн, S; Эллиотт, М; Миллер, I (октябрь 1999 г.). «Занамивир: обзор клинической безопасности». Безопасность лекарств. 21 (4): 267–81. Дои:10.2165/00002018-199921040-00003. PMID 10514019.
- ^ а б Сираноски Д. (сентябрь 2005 г.). «Угроза пандемии возвращает к жизни лекарство от гриппа». Природа Медицина. 11 (9): 909. Дои:10,1038 / нм0905-909. PMID 16145557.
- ^ Москона А (сентябрь 2005 г.). «Ингибиторы нейраминидазы при гриппе». Медицинский журнал Новой Англии. 353 (13): 1363–73. Дои:10.1056 / NEJMra050740. PMID 16192481.
- ^ Varghese, J. N .; Laver, W. G .; Колман, П. М. (1983). «Структура нейраминидазы гликопротеинового антигена вируса гриппа при разрешении 2,9». Природа. 303 (5912): 35–40. Дои:10.1038 / 303035a0. PMID 6843658.
- ^ «Архивная копия». Архивировано из оригинал 4 октября 2013 г.. Получено Второе октября, 2013.CS1 maint: заархивированная копия как заголовок (связь)
- ^ «Архивная копия». Архивировано из оригинал 5 октября 2013 г.. Получено Второе октября, 2013.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Майндл П., Бодо Дж., Палезе П., Шульман Дж., Таппи Х. (апрель 1974 г.). «Ингибирование активности нейраминидазы производными 2-дезокси-2,3-дегидро-N-ацетилнейраминовой кислоты». Вирусология. 58 (2): 457–63. Дои:10.1016/0042-6822(74)90080-4. PMID 4362431.
- ^ Лейвер, Грэм (1 марта 2007 г.). «Лекарства от гриппа - путь к открытиям». Образование в области химии. Vol. 44 нет. 2. Королевское химическое общество. С. 48–52. ISSN 0013-1350. Получено 19 июн 2018.
- ^ фон Ицштейн, М; Ву, Вайоминг; Кок, Великобритания; Пегг, MS; Дьясон, JC; Джин, Б; Ван Фан, Т; Смайт, ML; Белый, ВЧ; Оливер, SW (3 июня 1993 г.). «Рациональный дизайн мощных ингибиторов репликации вируса гриппа на основе сиалидазы». Природа. 363 (6428): 418–23. Bibcode:1993Натура.363..418В. Дои:10.1038 / 363418a0. PMID 8502295.
- ^ Cohen, D .; Картер, П. (3 июня 2010 г.). Заговоры "ВОЗ и пандемический грипп""". BMJ. 340 (июн03 4): c2912. Дои:10.1136 / bmj.c2912. PMID 20525679.
- ^ Саундарараджан В., Таракараман К., Раман Р., Рагурам С., Сасисекхаран В., Сасисекхаран Р. (июнь 2009 г.). «Экстраполяция из последовательности - вирус гриппа свиней H1N1 2009». Природа Биотехнологии. 27 (6): 510–3. Дои:10.1038 / nbt0609-510. PMID 19513050.
- ^ Хиршлер, Бен (19 января 2011 г.). «GSK тестирует внутривенное лекарство от гриппа по сравнению с Тамифлю Рош». Рейтер.
