Газообразные сигнальные молекулы - Gaseous signaling molecules
Газообразные сигнальные молекулы находятся газообразный молекулы которые либо синтезированный внутренне (эндогенно ) в организм, ткань или ячейка или поступают в организм, ткань или клетку извне (например, из атмосферы или гидросфера, как и в случае кислород ) и которые используются для передачи химических сигналов, которые вызывают определенные физиологические или биохимические изменения в организме, ткани или клетке. Этот термин применяется, например, к кислород, углекислый газ, оксид азота, монооксид углерода, сероводород, диоксид серы, оксид азота, цианистый водород, аммиак, метан, водород, этилен, так далее.
Многие, но не все, газообразные сигнальные молекулы называются газопередатчики.
Биологические роли каждой из газообразных сигнальных молекул кратко описаны ниже.
Газообразные сигнальные молекулы как передатчики газа
Газотрансмиттеры - это подсемейство эндогенных молекул газов или газообразных сигнальных молекул, включая NO, CO, ЧАС
2S.[1] Эти конкретные газы имеют много общих черт в их производстве и функциях, но выполняют свои задачи уникальным образом, который отличается от классических сигнальных молекул в человеческом теле. В 1981 году в клинической работе с закисью азота впервые было высказано предположение, что газ оказывает прямое действие на фармакологические рецепторы и тем самым действует как нейротрансмиттер.[2][3][4] Эти наблюдения подтвердили эксперименты in vitro.[5] которые позже были воспроизведены в NIDA.[6]
Терминология и критерии характеристики термина «газопередатчик» были впервые введены в 2002 году.[7] Чтобы одна молекула газа была отнесена к категории передатчиков газа, должны быть выполнены все следующие критерии.[8][7]
- Это небольшая молекула газа;
- Он свободно проницаем для мембран. Таким образом, его эффекты не зависят от родственных мембранных рецепторов. Он может иметь эндокринные, паракринные и аутокринные эффекты. Например, по своему эндокринному способу действия газотрансмиттеры могут попадать в кровоток; доставляться к удаленным целям мусорщиками и выпускаться там, а также модулировать функции удаленных целевых клеток;
- Он вырабатывается эндогенно и ферментативно, и его производство регулируется;
- Он имеет четко определенные и специфические функции при физиологически значимых концентрациях. Таким образом, манипулирование эндогенными уровнями этого газа вызывает определенные физиологические изменения;
- Функции этого эндогенного газа могут быть имитированы его экзогенно применяемым аналогом;
- Его клеточные эффекты могут быть опосредованы или не опосредованы вторичными посредниками, но должны иметь определенные клеточные и молекулярные мишени.
В 2011 г. Европейская сеть газопередатчиков (ENOG) был сформирован. Цель сети - продвигать исследования NO, CO и ЧАС
2S чтобы лучше понять биологию газотрансмиттеров и разгадать роль каждого посредника в здоровье и болезнях. Более того, сеть стремится внести свой вклад в перевод фундаментальных научных знаний в этой области исследований в терапевтические или диагностические инструменты.
Кислород
Эта секция нуждается в расширении. Вы можете помочь добавляя к этому. (Март 2016 г.) |
Углекислый газ
Углекислый газ - один из медиаторов местного саморегуляция кровоснабжения. Если его уровни высоки, капилляры расширяться, чтобы обеспечить больший приток крови к этой ткани.
Ионы бикарбоната имеют решающее значение для регулирования pH крови. Частота дыхания человека влияет на уровень CO.2 в их крови. Причины слишком медленного или поверхностного дыхания респираторный ацидоз, при слишком частом дыхании гипервентиляция, что может вызвать респираторный алкалоз.
Хотя организму необходим кислород для обмена веществ, низкий уровень кислорода обычно не стимулирует дыхание. Скорее, дыхание стимулируется повышенным уровнем углекислого газа.[9]
Дыхательные центры стараются поддерживать артериальный СО.2 давление 40 мм рт. При преднамеренной гипервентиляции СО2 содержание артериальной крови может быть снижено до 10–20 мм рт. ст. (содержание кислорода в крови мало затронуто), а дыхательная активность снижена. Вот почему после гипервентиляции можно задерживать дыхание дольше, чем без гипервентиляции. Это сопряжено с риском потери сознания до того, как потребность дышать станет непреодолимой, поэтому гипервентиляция особенно опасна перед фридайвингом.
Оксид азота
NO - одна из немногих известных газообразных сигнальных молекул, которая, кроме того, является исключительной из-за того, что представляет собой радикальный газ. Это ключ позвоночное животное биологический посланник, играя роль во множестве биологических процессов.[10] Это известный биопродукт практически всех типов организмов, от бактерий до растений, грибов и клеток животных.[11]
Оксид азота, известный как 'релаксирующий фактор эндотелия ', или' EDRF ', эндогенно биосинтезируется из L-аргинин, кислород, и НАДФН различными синтаза оксида азота (NOS) ферменты. Восстановление неорганического нитрата также может служить для образования оксида азота. В эндотелий (внутренняя подкладка) из кровеносный сосуд использует оксид азота, чтобы подать сигнал окружающим гладкая мышца расслабиться, в результате чего расширение сосудов и увеличение кровотока. Оксид азота обладает высокой реакционной способностью (срок службы составляет несколько секунд), но при этом свободно диффундирует через мембраны. Эти свойства делают оксид азота идеальным для кратковременных паракринный (между соседними ячейками) и автокринный (внутри одной клетки) сигнальная молекула.[12]
Независим от синтаза оксида азота, альтернативный путь, названный путем нитрат-нитрит-оксид азота, повышает уровень оксида азота за счет последовательного снижения количества нитратов, получаемых из продуктов растительного происхождения.[13] Богатые нитратами овощи, в частности листовая зелень, например шпинат и руккола, и свекла, было показано, что они увеличивают кардиозащитные уровни оксида азота с соответствующим снижением артериального давления в пре-гипертонический человек.[14][15] Чтобы организм вырабатывал оксид азота по пути нитрат-нитрит-оксид азота, восстановление нитрата до нитрита происходит во рту под действием комменсальных бактерий, что является обязательным и необходимым этапом.[16] Мониторинг статуса оксида азота анализ слюны обнаруживает биоконверсию нитрата растительного происхождения в оксид азота. Повышение уровня слюны свидетельствует о диетах, богатых листовыми овощами, которые часто встречаются в антигипертензивных диетах, таких как DASH диета.[17]
Производство оксида азота повышено в группах населения, живущих на больших высотах, что помогает этим людям избегать гипоксия за счет помощи в легочной сосудистой сети расширение сосудов. Эффекты включают вазодилатацию, нейротрансмиссия, модуляция цикл волос,[18] производство реактивных промежуточных соединений азота и эрекция полового члена (благодаря его способности вазодилат ). Нитроглицерин и амилнитрит служат вазодилататорами, потому что в организме они превращаются в оксид азота. Сосудорасширяющий антигипертензивный препарат миноксидил содержит фрагмент NO и может действовать как агонист NO. Точно так же Силденафила цитрат, широко известная под торговым названием Виагра, стимулирует эрекцию в первую очередь за счет усиления передачи сигналов через путь оксида азота в половом члене.
Оксид азота (NO) способствует гомеостазу сосудов, подавляя сокращение и рост гладких мышц сосудов, агрегацию тромбоцитов и адгезию лейкоцитов к эндотелию. Люди с атеросклероз, сахарный диабет, или гипертония часто показывают нарушение NO проводящих путей.[19] Было продемонстрировано, что высокое потребление соли снижает выработку NO у пациентов с гипертонической болезнью, хотя биодоступность остается нерегулируемой.[20]
Оксид азота также вырабатывается фагоцитами (моноциты, макрофаги, и нейтрофилы ) как часть человеческого иммунная реакция.[21] Фагоциты вооружены индуцибельной синтазой оксида азота (iNOS), которая активируется посредством интерферон-гамма (IFN-γ) как одиночный сигнал или фактор некроза опухоли (TNF) вместе со вторым сигналом.[22][23][24] С другой стороны, трансформирующий фактор роста-бета (TGF-β) обеспечивает сильный ингибирующий сигнал для iNOS, тогда как интерлейкин -4 (ИЛ-4) и ИЛ-10 дают слабые тормозящие сигналы. Таким образом, иммунная система может регулировать ресурсы фагоцитов, которые играют роль в воспалении и иммунных ответах.[25] Оксид азота секретируется в виде свободных радикалов при иммунном ответе и токсичен для бактерий и внутриклеточных паразитов, в том числе Лейшмания[26] и малярия;[27][28][29] механизм этого включает повреждение ДНК[30][31][32] и разложение центров железа и серы на ионы железа и железо-нитрозил соединения.[33]
В ответ многие бактериальные патогены выработали механизмы устойчивости к оксиду азота.[34] Поскольку оксид азота может оказывать провоспалительное действие при таких состояниях, как астма, растет интерес к использованию выдыхаемый оксид азота как дыхательный тест при заболеваниях с дыхательные пути воспаление. Снижение уровней выдыхаемого NO связано с воздействием загрязнения воздуха на велосипедистов и курильщиков, но в целом повышенные уровни выдыхаемого NO связаны с воздействием загрязнения воздуха.[35]
Оксид азота может способствовать реперфузионная травма когда чрезмерное количество вырабатывается во время реперфузии (после периода ишемия ) реагирует с супероксид производить разрушающий окислитель пероксинитрит. Напротив, было показано, что вдыхаемый оксид азота помогает выживанию и восстановлению после паракват отравление, при котором образуется супероксид, повреждающий ткань легких, и нарушается метаболизм NOS.
В растениях оксид азота может продуцироваться любым из четырех способов: (i) L-аргинин-зависимая синтаза оксида азота,[36][37][38] (хотя существование гомологов NOS животных у растений обсуждается),[39] (ii) связанный с плазматической мембраной нитратредуктаза, (iii) митохондриальная цепь переноса электронов или (iv) неферментативные реакции. Это сигнальная молекула, действует в основном против окислительный стресс а также играет роль во взаимодействии с патогенами растений. Лечение срезанные цветы и другие растения с оксидом азота увеличивают время до увядания.[40]
Двумя важными механизмами биологических реакций оксида азота являются S-нитрозирование тиолов и нитрозилирование ионов переходных металлов. S-нитрозирование включает (обратимое) превращение тиол группы, в том числе цистеин остатков в белках с образованием S-нитрозотиолов (RSNO). S-Нитрозирование представляет собой механизм динамической посттрансляционной регуляции большинства или всех основных классов белков.[41] Второй механизм, нитрозилирование, включает связывание NO с ионом переходного металла, такого как железо или медь. В этой функции NO упоминается как нитрозильный лиганд. Типичные случаи связаны с нитрозилированием гемовых белков, таких как цитохромы, тем самым нарушая нормальную ферментативную активность фермента. Нитрозилированное двухвалентное железо особенно стабильно, так как нитрозильный лиганд связывается с двухвалентным железом (Fe (II)) очень прочно. Гемоглобин является ярким примером гемового белка, который может быть модифицирован NO обоими путями: NO может присоединяться непосредственно к гему в реакции нитрозилирования и независимо образовывать S-нитрозотиолы путем S-нитрозирования тиоловых фрагментов.[42]
Существует несколько механизмов, с помощью которых NO влияет на биологию живых клеток. К ним относятся окисление железосодержащих белков, таких как рибонуклеотидредуктаза и аконитаза, активация растворимого гуанилатциклаза, АДФ рибозилирование белков, сульфгидрильная группа белков нитрозилирование и активация регуляторного фактора железа.[43] Было продемонстрировано, что НЕТ активирует NF-κB в мононуклеарных клетках периферической крови - важный фактор транскрипции в экспрессии гена iNOS в ответ на воспаление.[44]
Было обнаружено, что NO действует через стимуляцию растворимой гуанилатциклазы, которая является гетеродимерным ферментом, с последующим образованием циклического GMP. Cyclic-GMP активирует протеинкиназа G, что вызывает обратный захват Ca2+ и открытие кальциевых калиевых каналов. Падение концентрации Ca2+ гарантирует, что киназа легкой цепи миозина (КЛЦМ) больше не может фосфорилировать молекулу миозина, тем самым останавливая цикл перекрестных мостиков и приводя к расслаблению гладкомышечных клеток.[45]
Оксид азота
Закись азота в биологических системах может образовываться в результате ферментативного или неферментативного восстановления оксид азота.[46] Исследования in vitro показали, что эндогенная закись азота может образовываться в результате реакции между оксидом азота и тиол.[47] Некоторые авторы показали, что этот процесс восстановления NO до N2O имеет место в гепатоциты особенно в их цитоплазма и митохондрии, и предположил, что N2О может, возможно, продуцироваться в клетках млекопитающих.[48] Хорошо известно, что N2O вырабатывается некоторыми бактериями в процессе денитрификации.
Помимо прямого[5][6] и непрямое действие на опиоидные рецепторы,[49] также было показано, что N2О подавляет Рецептор NMDA -опосредованная активность и ионные токи и уменьшает опосредованную рецептором NMDA эксайтотоксичность и нейродегенерацию.[50] Закись азота также ингибирует метионинсинтазу и замедляет превращение гомоцистеин к метионин, увеличивает концентрацию гомоцистеина и снижает концентрацию метионина. Этот эффект был показан в лимфоцит клеточные культуры[51] и в образцах биопсии печени человека.[52]
Закись азота не связывается в качестве лиганда с гем и не реагирует с тиолсодержащими белки. Тем не менее, исследования показали, что закись азота может обратимо и нековалентно «вставлять» себя во внутренние структуры некоторых гемсодержащих белков, таких как гемоглобин, миоглобин, цитохромоксидаза и изменить их структуру и функцию.[53] Способность закиси азота изменять структуру и функцию этих белков была продемонстрирована сдвигами в инфракрасных спектрах цистеин тиолы гемоглобина[54] и частичным и обратимым ингибированием цитохромоксидазы.[55]
Эндогенная закись азота может играть роль в модуляции эндогенных опиоид[56][2] и системы NMDA.[50]
Монооксид углерода
Окись углерода вырабатывается естественным путем в организме человека как сигнальная молекула. Таким образом, окись углерода может иметь физиологическую роль в организме, например нейротрансмиттер или релаксант кровеносных сосудов.[57] Из-за роли окиси углерода в организме нарушения его метаболизма связаны с различными заболеваниями, включая нейродегенерации, гипертонию, сердечную недостаточность и воспаление.[57]
Краткое описание функции:[58]
- СО функционирует как эндогенная сигнальная молекула.
- CO модулирует функции сердечно-сосудистой системы.
- СО подавляет агрегацию и адгезию тромбоцитов.
- СО может играть роль потенциального терапевтического агента.
У млекопитающих окись углерода вырабатывается естественным образом под действием гемоксигеназа 1 и 2 на гем от гемоглобин сломать. Этот процесс производит определенное количество карбоксигемоглобина у нормальных людей, даже если они не дышат угарным газом.
После первого сообщения о том, что окись углерода является нормальным нейромедиатором в 1993 году,[59][60] а также один из трех газов, которые естественным образом модулируют воспалительные реакции в организме (два других - оксид азота и сероводород ), монооксид углерода получил большое клиническое внимание как биологический регулятор. Известно, что во многих тканях все три газа действуют как противовоспалительные, вазодилататоры, и вдохновители неоваскулярный рост.[61] Однако проблемы являются сложными, поскольку неоваскулярный рост не всегда полезен, поскольку он играет роль в росте опухоли, а также в ущербе от мокрый дегенерация желтого пятна, заболевание, при котором курение (основной источник окиси углерода в крови, в несколько раз превышающий естественный уровень производства) увеличивает риск от 4 до 6 раз.
Есть теория, что в какой-то нервной клетке синапсы, когда долгосрочные воспоминания При укладке, принимающая ячейка вырабатывает окись углерода, которая возвращается обратно в передающую ячейку, заставляя ее передавать более легко в будущем. Было показано, что некоторые такие нервные клетки содержат гуанилатциклаза, фермент который активируется оксидом углерода.[60]
Исследования с участием окиси углерода были проведены во многих лабораториях по всему миру на предмет его противовоспалительных и цитопротекторных свойств. Эти свойства могут быть использованы для предотвращения развития ряда патологических состояний, включая ишемическое реперфузионное повреждение, отторжение трансплантата, атеросклероз, тяжелый сепсис, тяжелую малярию или аутоиммунитет. Были проведены клинические испытания с участием людей, однако результаты еще не опубликованы.[62]
Недокись углерода

Недокись углерода, С3О2, может производиться в небольших количествах в любом биохимическом процессе, который обычно производит монооксид углерода, CO, например, при окислении гема гемоксигеназой-1. Он также может быть образован из малоновой кислоты. Было показано, что субоксид углерода в организме может быстро полимеризоваться в макроциклические поликарбонатные структуры с общей формулой (C3О2)п (в основном (C3О2)6 и (C3О2)8), и что эти макроциклические соединения являются мощными ингибиторами Na+/ К+-АТФ-аза и Са-зависимая АТФ-аза и имеют дигоксин -подобные физиологические свойства и натрийуретическое и гипотензивное действие. Эти макроциклические полимерные соединения субоксида углерода считаются эндогенными дигоксин-подобными регуляторами Na+/ К+-АТФ-азы и Са-зависимые АТФ-азы, а также эндогенные натрийуретики и гипотензивные средства.[63][64][65] Помимо этого, некоторые авторы также считают, что эти макроциклические соединения субоксида углерода, возможно, могут уменьшать образование свободных радикалов и окислительный стресс и играть роль в эндогенных противораковых защитных механизмах, например, в сетчатка.[66]
Сероводород
Сероводород в небольших количествах вырабатывается некоторыми клетками млекопитающее тела и имеет ряд биологических сигнальных функций. (В настоящее время известны только два других таких газа: оксид азота (НЕТ) и монооксид углерода (CO).)
Газ добывается из цистеин посредством ферменты цистатионин бета-синтаза и цистатионин гамма-лиаза. Он действует как релаксант гладкая мышца и как сосудорасширяющее средство[67] а также активно участвует в мозг, где он увеличивает отклик Рецептор NMDA и способствует долгосрочное потенцирование,[68] который участвует в формировании памяти.
В конечном итоге газ превращается в сульфит в митохондрии тиосульфатредуктазой, и сульфит далее окисляется до тиосульфат и сульфат от сульфитоксидаза. Сульфаты выводятся с мочой.[69]
Благодаря своим эффектам, подобным оксид азота (без возможности формирования перекиси взаимодействуя с супероксид ), сероводород в настоящее время признан потенциально защищающим от сердечно-сосудистых заболеваний.[67] Кардиозащитный эффект чеснок вызвано катаболизм из полисульфидная группа в аллицин к ЧАС
2S, реакция, которая может зависеть от восстановления, опосредованного глутатион.[70]
Хотя оба оксид азота (NO) и сероводород расслабляют кровеносные сосуды, но механизмы их действия различны: NO активирует фермент. гуанилилциклаза, ЧАС
2S активирует АТФ-чувствительные калиевые каналы в гладкомышечных клетках. Исследователи не понимают, как ответственность за расслабление сосудов распределяется между оксидом азота и сероводородом. Однако есть некоторые свидетельства того, что оксид азота выполняет большую часть расслабляющей работы в крупных сосудах, а сероводород отвечает за аналогичное действие в более мелких кровеносных сосудах.[71]
Недавние данные свидетельствуют о сильном перекрестном взаимодействии NO и ЧАС
2S,[72] демонстрируя, что сосудорасширяющие эффекты этих двух газов взаимозависимы. Дополнительно, ЧАС
2S реагирует с внутриклеточными S-нитрозотиолы для образования мельчайшего S-нитрозотиола (HSNO), и предполагается, что сероводород играет роль в контроле внутриклеточного пула S-нитрозотиола.[73]
Как и оксид азота, сероводород участвует в расслаблении гладкой мускулатуры, что вызывает эрекция полового члена, представляя возможные новые терапевтические возможности для Эректильная дисфункция.[74][75]
Сероводород (ЧАС
2S) дефицит может быть вредным для функции сосудов после острый инфаркт миокарда (AMI).[76] ОИМ может привести к сердечной дисфункции в результате двух различных изменений; усиление окислительного стресса из-за накопления свободных радикалов и снижение биодоступности NO.[77] Накопление свободных радикалов происходит из-за увеличения разобщения транспорта электронов в активном центре эндотелиальной синтазы оксида азота (eNOS), фермента, участвующего в превращении L-аргинина в NO.[76][77] Во время AMI окислительная деградация тетрагидробиоптерина (BH4), кофактора продукции NO, ограничивает доступность BH4 и ограничивает продукцию NO eNOS.[77] Вместо этого eNOS вступает в реакцию с кислородом, другим косубстратом, участвующим в производстве NO. Продукты eNOS восстанавливаются до супероксидов, увеличивая выработку свободных радикалов и окислительный стресс в клетках.[76] А ЧАС
2S его дефицит снижает активность eNOS, ограничивая активацию Akt и ингибируя фосфорилирование Akt сайта активации eNOSS1177.[76][72] Вместо этого активность Akt увеличивается, чтобы фосфорилировать сайт ингибирования eNOST495, подавляя продукцию NO eNOS.[76][72]
ЧАС
2S терапия использует ЧАС
2S донор, такой как диаллилтрисульфид (DATS), для увеличения поступления ЧАС
2S пациенту с ОИМ. ЧАС
2S доноры снижают риск повреждения миокарда и реперфузионных осложнений.[76] Вырос ЧАС
2S уровни в организме будут реагировать с кислородом с образованием сульфановой серы, промежуточного продукта для хранения ЧАС
2S.[76] ЧАС
2S бассейны в теле притягивают кислород, чтобы реагировать с избытком ЧАС
2S и eNOS для увеличения производства NO.[76] При увеличении использования кислорода для производства большего количества NO, меньше кислорода доступно для реакции с eNOS с образованием супероксидов во время AMI, что в конечном итоге снижает накопление активных форм кислорода (ROS).[76] Кроме того, снижение накопления ROS снижает окислительный стресс в гладкомышечных клетках сосудов, уменьшая окислительную дегенерацию BH4.[77] Повышенный кофактор BH4 способствует увеличению производства NO в организме.[77] Более высокие концентрации ЧАС
2S напрямую увеличивают активность eNOS через активацию Akt для увеличения фосфорилирования сайта активации eNOSS1177 и уменьшения фосфорилирования сайта ингибирования eNOST495.[76][72] Этот процесс фосфорилирования усиливает активность eNOS, катализируя большее превращение L-аргинина в NO.[76][72] Повышенное производство NO способствует активности растворимой гуанилилциклазы (sGC), что приводит к увеличению конверсии гуанозинтрифосфата (GTP) в 3 ’, 5’-циклический гуанозинмонофосфат (cGMP).[78] В ЧАС
2S При терапии сразу же после ОИМ увеличение цГМФ вызывает повышение активности протеинкиназы G (PKG).[79] PKG снижает внутриклеточный Ca2 + в гладких мышцах сосудов, чтобы увеличить расслабление гладких мышц и способствовать кровотоку.[79] PKG также ограничивает пролиферацию гладкомышечных клеток, уменьшая утолщение интимы после повреждения ОИМ, в конечном итоге уменьшая размер инфаркта миокарда.[76][78]
В Болезнь Альцгеймера концентрация сероводорода в мозге сильно снижена.[80] В определенной модели крысы болезнь Паркинсона было обнаружено, что концентрация сероводорода в мозге снижается, и введение сероводорода облегчило состояние.[81] В трисомия 21 (Синдром Дауна) организм вырабатывает избыток сероводорода.[69] Сероводород также участвует в болезненном процессе диабет 1 типа. В бета-клетки из поджелудочная железа при диабете 1 типа вырабатывается избыток газа, что приводит к гибели этих клеток и снижению выработки инсулина оставшимися.[71]
В 2005 году было показано, что мышей можно поставить в состояние приостановленная анимация -любить переохлаждение путем применения низкой дозировки сероводорода (81 промилле ЧАС
2S) в воздухе. Частота дыхания животных снизилась со 120 до 10 вдохов в минуту, а их температура упала с 37 ° C до всего на 2 ° C выше температуры окружающей среды (по сути, они стали хладнокровный ). Мыши выдержали эту процедуру в течение 6 часов и после этого не проявили никаких негативных последствий для здоровья.[82] В 2006 году было показано, что артериальное давление у мышей, получавших таким образом сероводород, существенно не уменьшилось.[83]
Похожий процесс, известный как спячка естественным образом встречается во многих млекопитающие а также в жабы, но не у мышей. (Мыши могут впадать в состояние, называемое клиническое оцепенение при нехватке еды). Если ЧАС
2S-индуцированная гибернация может работать у людей, она может быть полезна при оказании неотложной помощи тяжелораненым пациентам и при сохранении донорских органов. В 2008 году было показано, что гипотермия, вызванная сероводородом в течение 48 часов, снижает степень повреждения мозга, вызванного экспериментальным Инсульт у крыс.[84]
Как упоминалось выше, сероводород связывается с цитохромоксидаза и тем самым предотвращает связывание кислорода, что приводит к резкому замедлению метаболизм. Животные и люди естественным образом вырабатывают в своем организме некоторое количество сероводорода; исследователи предположили, что газ используется для регулирования метаболической активности и температуры тела, что объясняет вышеуказанные результаты.[85]
Два недавних исследования ставят под сомнение возможность достижения такого эффекта у более крупных млекопитающих. В исследовании 2008 года не удалось воспроизвести эффект у свиней, и был сделан вывод о том, что эффекты, наблюдаемые у мышей, не наблюдались у более крупных млекопитающих.[86] Аналогичным образом в статье Haouzi et al. отметил, что нет индукции гипометаболизма у овец.[87]
В феврале 2010 г. ТЕД конференция, Марк Рот объявил, что сероводород вызывает переохлаждение в людях завершил Фаза I клинические испытания.[88] Однако клинические испытания, проведенные по заказу компании Ikaria, которую он помог основать, были отозваны или прекращены к августу 2011 года.[89][90]
Диоксид серы
Роль диоксида серы в биологии млекопитающих еще недостаточно изучена.[91] Диоксид серы блокирует нервные сигналы от рецепторы растяжения легких и отменяет Инфляционный рефлекс Геринга – Брейера.
Было показано, что эндогенный диоксид серы играет роль в уменьшении экспериментального легкое ущерб, причиненный олеиновая кислота. Эндогенный диоксид серы снижает перекисное окисление липидов, образование свободных радикалов, окислительный стресс и воспаление во время экспериментального повреждения легких. И наоборот, успешное повреждение легких привело к значительному снижению выработки эндогенного диоксида серы и увеличению перекисного окисления липидов, образования свободных радикалов, окислительного стресса и воспаления. Более того, блокада фермент который производит эндогенный SO2 значительно увеличил объем повреждения легочной ткани в эксперименте.И наоборот, добавление ацетилцистеин или глутатион к рациону крыс увеличилось количество эндогенной СО2 вызывает и уменьшает повреждение легких, образование свободных радикалов, окислительный стресс, воспаление и апоптоз.[92]
Считается, что эндогенный диоксид серы играет важную физиологическую роль в регуляции сердечный и кровеносный сосуд функции, а аберрантный или недостаточный метаболизм диоксида серы может способствовать нескольким различным сердечно-сосудистым заболеваниям, таким как артериальная гипертензия, атеросклероз, легочная артериальная гипертензия, стенокардия.[93]
Было показано, что у детей с легочной артериальной гипертензией вследствие врожденных пороков сердца уровень гомоцистеин выше, а уровень эндогенного диоксида серы ниже, чем у здоровых детей контрольной группы. Более того, эти биохимические параметры сильно коррелировали с тяжестью легочной артериальной гипертензии. Авторы считали гомоцистеин одним из полезных биохимических маркеров тяжести заболевания, а метаболизм диоксида серы - одной из потенциальных терапевтических мишеней для этих пациентов.[94]
Эндогенный диоксид серы также снижает распространение скорость эндотелия гладкая мышца клеток в кровеносных сосудах, за счет снижения MAPK активность и активация аденилилциклаза и протеинкиназа А.[95] Разрастание гладкомышечных клеток - один из важных механизмов гипертонического ремоделирования кровеносных сосудов и их стеноз, поэтому это важный патогенетический механизм артериальной гипертензии и атеросклероза.
Эндогенный диоксид серы в низких концентрациях вызывает эндотелий-зависимый расширение сосудов. В более высоких концентрациях он вызывает эндотелий-независимую вазодилатацию и оказывает отрицательный инотропный эффект на функцию сердечного выброса, эффективно снижая кровяное давление и потребление кислорода миокардом. Сосудорасширяющее действие диоксида серы опосредуется через АТФ-зависимую кальциевые каналы и кальциевые каналы L-типа («дигидропиридин»). Эндогенный диоксид серы также является сильным противовоспалительным, антиоксидантным и цитопротекторным средством. Он снижает артериальное давление и замедляет гипертоническое ремоделирование кровеносных сосудов, особенно утолщение их интимы. Он также регулирует липидный обмен.[96]
Эндогенный диоксид серы также уменьшает повреждение миокарда, вызванное: изопротеренол адренергический гиперстимуляция, усиливает резерв антиоксидантной защиты миокарда.[97]
Цианистый водород
Некоторые авторы показали, что нейроны может производить цианистый водород при активации их опиоид рецепторы эндогенными или экзогенными опиоидами. Они также показали, что выработка HCN нейронами активирует Рецепторы NMDA и играет роль в преобразование сигнала между нейрональными клетками (нейротрансмиссия ). Более того, повышение эндогенной продукции нейронального HCN под действием опиоидов, по-видимому, было необходимо для адекватного опиоидного обезболивание, поскольку обезболивающее действие опиоидов ослаблялось акцепторами HCN. Они считали эндогенный HCN нейромодулятором.[98]
Также было показано, что при стимуляции мускариновый холинергический рецепторы в культуре феохромоцитома клетки увеличивается Продукция HCN в живом организме (in vivo) мускариновая холинергическая стимуляция уменьшается Производство HCN.[99]
Лейкоциты генерировать HCN во время фагоцитоз.[98]
В расширение сосудов, вызванный нитропруссид натрия, как было показано, опосредуется не только генерацией NO, но и эндогенным цианидом, который добавляет не только токсичность, но и некоторую дополнительную антигипертензивную эффективность по сравнению с нитроглицерин и другие нецианогенные нитраты, которые не вызывают повышения уровня цианида в крови.[100]
Аммиак
Аммиак также играет роль как у нормальных, так и у ненормальных животных. физиология. Он биосинтезируется посредством нормального метаболизма аминокислот и токсичен в высоких концентрациях.[101] В печень превращает аммиак в мочевину посредством ряда реакций, известных как цикл мочевины. Дисфункция печени, такая как цирроз, может привести к повышенному содержанию аммиака в крови (гипераммониемия ). Аналогичным образом, дефекты ферментов, ответственных за цикл мочевины, такие как орнитин-транскарбамилаза, приводят к гипераммониемии. Гипераммонемия способствует спутанности сознания и кома из печеночная энцефалопатия, а также неврологическое заболевание, распространенное у людей с дефектами цикла мочевины и органические ацидурии.[102]
Аммиак важен для нормального кислотно-щелочного баланса животных. После образования аммония из глутамин, α-кетоглутарат может разлагаться с образованием двух молекул бикарбонат, которые затем доступны в качестве буферов для пищевых кислот. Аммоний выводится с мочой, что приводит к чистой потере кислоты. Аммиак может сам диффундировать по почечным канальцам, соединяться с ионом водорода и, таким образом, способствовать дальнейшему выведению кислоты.[103]
Метан
Некоторые авторы показали, что эндогенные метан производится не только кишечная флора а затем впитался в кровь, но также производится - в небольших количествах - эукариотический клетки (в процессе перекисного окисления липидов). И они также показали, что производство эндогенного метана увеличивается во время экспериментального митохондриальный гипоксия, Например, азид натрия интоксикация. Они думали, что метан может быть одним из межклеточных сигналов гипоксии и стресса.[104]
Другие авторы показали, что выработка метана в клетках также увеличивается во время сепсис или бактериальный эндотоксемия, включая экспериментальную имитацию эндотоксемии путем введения липополисахаридов (ЛПС).[105]
Некоторые другие исследователи показали, что метан, вырабатываемый кишечной флорой, не является полностью «биологически нейтральным» для кишечника и участвует в нормальной физиологической регуляции кишечника. перистальтика. И его избыток вызывает не только отрыжку, метеоризм и боли в животе, но и функциональные запоры.[106]
Этилен
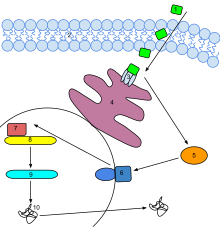
Этилен служит гормон в растения.[107] Он действует в следовых количествах на протяжении всей жизни растения, стимулируя или регулируя созревание из фрукты, открытие цветы, а опадение (или выпадение) уходит. В коммерческих камерах созревания используются «каталитические генераторы» для производства газообразного этилена из жидкого источника этанола. Обычно используется уровень газовыделения от 500 до 2000 частей на миллион в течение 24-48 часов. Необходимо соблюдать осторожность, чтобы контролировать уровень углекислого газа в камерах дозревания при газировании, так как созревание происходит при высокой температуре (20 ° C; 68 ° F).[нужна цитата ] было замечено производить CO2 уровни 10% за 24 часа.[108]
Этилен использовался со времен древних египтян, которые пилили инжир, чтобы стимулировать созревание (ранение стимулирует выработку этилена тканями растений). Древние китайцы сожгли бы ладан в закрытых помещениях для ускорения созревания груш. В 1864 году было обнаружено, что утечки газа из уличных фонарей приводят к задержке роста, скручиванию растений и аномальному утолщению стеблей.[107] В 1901 году русский ученый Димитрий Нелюбов показал, что активным компонентом является этилен.[109] Сара Сомнение обнаружила, что этилен стимулирует опадение в 1917 г.[110] Только в 1934 году Гейн сообщил, что растения синтезируют этилен.[111] В 1935 году Крокер предположил, что этилен был растительным гормоном, отвечающим за созревание плодов, а также старение вегетативных тканей.[112]

Этилен производят практически из всех частей высших растений, включая листья, стебли, корни, цветы, фрукты, клубни и семена. Производство этилена регулируется множеством факторов развития и окружающей среды. В течение жизненного цикла растения производство этилена индуцируется на определенных стадиях роста, таких как прорастание, созревание фруктов, опадение листьев и старение цветов. Производство этилена также может быть вызвано множеством внешних факторов, таких как механическое ранение, стрессы окружающей среды и некоторые химические вещества, включая ауксин и другие регуляторы.[113]
Этилен биосинтезированный из аминокислоты метионин к S-аденозил-L-метионин (SAM, также называемый адометом) ферментом Met аденозилтрансферазой. Затем SAM преобразуется в 1-аминоциклопропан-1-карбоновая кислота (АСС) ферментом АСС-синтаза (ACS). Активность ACS определяет скорость производства этилена, поэтому регулирование этого фермент является ключевым для биосинтеза этилена. Последний этап требует кислорода и включает действие фермента. АСС-оксидаза (ACO), ранее известный как фермент, образующий этилен (EFE). Биосинтез этилена может быть индуцирован эндогенным или экзогенным этиленом. Синтез АЦК увеличивается с высоким уровнем ауксины, особенно индолуксусная кислота (IAA) и цитокинины.
Этилен воспринимается семьей из пяти трансмембранных белковые димеры такие как ETR1 белок в Арабидопсис. В ген кодирование рецептор этилена[который? ] был клонирован в Arabidopsis thaliana а затем в помидор.[нужна цитата ] Рецепторы этилена кодируются множеством генов в Арабидопсис и помидор геномы. Мутации в любом из генная семья, который включает пять рецепторов в Арабидопсис и, по крайней мере, шесть в томате, могут привести к нечувствительности к этилену.[114] ДНК последовательности рецепторов этилена также были идентифицированы у многих других видов растений, и белок, связывающий этилен, был даже идентифицирован в Цианобактерии.[107]
Экологические сигналы, такие как наводнение, засуха, переохлаждение, ранение и атака патогенов, могут вызвать образование этилена в растениях. При затоплении корни страдают от недостатка кислорода, или аноксия, что приводит к синтезу 1-аминоциклопропан-1-карбоновая кислота (АКК). ACC транспортируется вверх по растению, а затем окисляется в листьях. Причины образования этилена настические движения (эпинастия) листьев, возможно, помогая растению терять воду.[115]
Этилен в растении вызывает такие реакции:
- Тройная реакция проростков, утолщение и укорочение гипокотиль с ярко выраженным апикальным крючком.
- В опыление, когда пыльца достигает рыльца, предшественника этена, АКК, секретируется на лепесток, АСС выделяет этилен с АСС-оксидазой.
- Стимулирует листья и цветы старение
- Стимулирует старение зрелых ксилема клетки в процессе подготовки к использованию в растениях
- Побуждает лист опадение
- Побуждает семена прорастание
- Вызывает корни волос рост [116]- повышение эффективности поглощения воды и минералов за счет образования ризошейки [117] [118]
- Вызывает рост придаточные корни во время наводнения [119][120]
- Стимулирует выживание в условиях низкого содержания кислорода (гипоксия ) в погруженных тканях растений [121] [122] [123]
- Стимулирует эпинастию - лист черешок вырастает, лист свисает и скручивается в себя
- Стимулирует созревание плодов [124]
- Вызывает климактерический подняться в дыхание в некоторых фруктах, что вызывает дополнительный выброс этилена.
- Влияет гравитропизм
- Стимулирует нутационное изгибание
- Подавляет рост ствола и стимулирует расширение стволовых клеток и клеток, а также рост боковых ветвей за пределами стадии проростков (см. Гипонастический ответ )
- Вмешательство в ауксин транспорт (с высоким ауксин концентрации)
- Подавляет рост побегов и устьичный закрытие, за исключением некоторых водных растений или обычно затопляемых растений, таких как некоторые сорта риса, где происходит обратное (сохранение CO
2 и О
2) - Вызывает цветение ананасы
- Подавляет индуцированное коротким днем зарождение цветков у Фарбитус ноль[125] и Хризантема морифолиум[126]
Небольшие количества эндогенного этилена также производятся в млекопитающие, в том числе люди, за счет перекисного окисления липидов. Затем часть эндогенного этилена окисляется до окись этилена, который способен алкилировать ДНК и белки, в том числе гемоглобин (образуя специфический аддукт со своим N-концом валин, N-гидроксиэтил-валин).[127] Эндогенный оксид этилена, как и экологический (экзогенный), может алкилировать гуанин в ДНК, образуя аддукт 7- (2-гидроксиэтил) -гуанин, что создает внутренний канцерогенный риск.[128] Он также обладает мутагенным действием.[129][130]
использованная литература
- ^ Мустафа А.К., Гадалла М.М., Снайдер С.Х. (2009). «Сигнализация газопередатчиками». Научный сигнал. 2 (68): re2. Дои:10.1126 / scisignal.268re2. ЧВК 2744355. PMID 19401594.
- ^ а б Гиллман М.А., Лихтигфельд Ф.Дж. (январь 1981 г.). «Сравнение эффектов обезболивания сульфатом морфина и закиси азота на состояние хронической боли у человека». J. Neurol. Наука. 49 (1): 41–45. Дои:10.1016 / 0022-510X (81) 90186-6. PMID 7205318.
- ^ Гиллман М.А., Лихтигфельд Ф.Дж. (февраль 1981 г.). «Сходство действия закиси азота и морфина». Боль. 10 (1): 110. Дои:10.1016/0304-3959(81)90054-3. PMID 7232008.
- ^ Гиллман М.А., Лихтигфельд Ф.Дж. (май 1983 г.). «Закись азота взаимодействует с опиоидными рецепторами: больше доказательств». Анестезиология. 58 (5): 483–4. Дои:10.1097/00000542-198305000-00021. PMID 6301312.
- ^ а б Дарас, К; Cantrill, R; Гиллман, Массачусетс (1983). «(3H) Замещение налоксона: данные о закиси азота как агонисте опиоидных рецепторов». Eur J Pharmacol. 89 (1–2): 177–178. Дои:10.1016 / 0014-2999 (83) 90626-х. PMID 6305684.
- ^ а б Ори, С .; Форд-Райс, Ф; Лондон, E.D. (1989). «Влияние закиси азота и галотана на мю- и каппа-опиоидные рецепторы в мозге морских свинок». Анестезиология. 70 (3): 541–544. Дои:10.1097/00000542-198903000-00027. PMID 2564264.
- ^ а б Ван, Р. (2002). «Двое в компании, три в толпе - Может ЧАС
2S быть третьим эндогенным газовым передатчиком? ». Журнал FASEB. 16 (13): 1792–1798. Дои:10.1096 / fj.02-0211hyp. PMID 12409322. S2CID 40765922. - ^ Ван Р (редактор) (2004) Преобразование сигналов и газопередатчики: NO, CO и H2S в области биологии и медицины. Humana Press, Нью-Джерси, США.
- ^ Веллер, Ричард, Может ли солнце быть полезным для вашего сердца? TedxGlasgow. Снято в марте 2012 г., опубликовано в январе 2013 г.
- ^ Росзер, Т. (2012) Биология субклеточного оксида азота. ISBN 978-94-007-2818-9
- ^ Страйер, Люберт (1995). Биохимия, 4-е издание. W.H. Фримен и компания. п. 732. ISBN 978-0-7167-2009-6.
- ^ «Растительные диеты | Растительные продукты | Свекольный сок | Овощи с оксидом азота». Тест Беркли. Архивировано из оригинал на 2013-10-04. Получено 2013-10-04.
- ^ Ghosh, S.M .; Капил, В .; Fuentes-Calvo, I .; Bubb, K.J .; Жемчуг, В .; Милсом, А. Б .; Khambata, R .; Maleki-Toyserkani, S .; Юсуф, М .; Benjamin, N .; Webb, A.J .; Колфилд, М. Дж .; Hobbs, A.J .; Ахлувалия, А. (2013). «Повышенная сосудорасширяющая активность нитрита при гипертонии: критическая роль эритроцитарной ксантиноксидоредуктазы и трансляционный потенциал». Гипертония. 61 (5): 1091–102. Дои:10.1161 / ГИПЕРТЕНЗИЯ AHA.111.00933. PMID 23589565.
- ^ Webb, A.J .; Patel, N .; Loukogeorgakis, S .; Окорие, М .; Aboud, Z .; Misra, S .; Рашид, Р .; Miall, P .; Deanfield, J .; Benjamin, N .; MacAllister, R .; Hobbs, A.J .; Ахлувалия, А. (2008). «Острое снижение артериального давления, вазопротекторные и антитромбоцитарные свойства диетических нитратов посредством биоконверсии в нитриты». Гипертония. 51 (3): 784–90. Дои:10.1161 / ГИПЕРТЕНЗИЯAHA.107.103523. ЧВК 2839282. PMID 18250365.
- ^ Хезель, депутат; Вайцберг, Э (2013). «Микробиом полости рта и гомеостаз оксида азота». Оральные заболевания. 21 (1): 7–16. Дои:10.1111 / odi.12157. PMID 23837897.
- ^ Грин, Шон Дж. (25 июля 2013 г.). «Превращение стратегии DASH в реальность для улучшения результатов кардио-здоровья: Часть II». Здравоохранение в реальном мире. Получено 2013-10-04.
- ^ Проктор, PH (август 1989 г.). «Производный эндотелием расслабляющий фактор и миноксидил: активные механизмы роста волос». Архив дерматологии. 125 (8): 1146. Дои:10.1001 / archderm.1989.01670200122026. PMID 2757417.
- ^ Dessy, C .; Феррон, О. (2004). «Патофизиологические роли оксида азота: в сердце и коронарной сосудистой сети». Современная лекарственная химия - противовоспалительные и противоаллергические средства. 3 (3): 207–216. Дои:10.2174/1568014043355348.
- ^ Осанай, Т; Fujiwara, N; Сайто, М; Сасаки, S; Tomita, H; Накамура, М; Осава, H; Ямабе, H; Окумура, К. (2002). «Взаимосвязь между потреблением соли, оксида азота и асимметричного диметиларгинина и его значение для пациентов с терминальной стадией почечной недостаточности». Очищение крови. 20 (5): 466–8. Дои:10.1159/000063555. PMID 12207094.
- ^ Грин, SJ; Меллук, S; Хоффман, С.Л .; Meltzer, MS; Нейси, Калифорния (1990). «Клеточные механизмы неспецифического иммунитета к внутриклеточной инфекции: Цитокин-индуцированный синтез токсичных оксидов азота из L-аргинина макрофагами и гепатоцитами». Письма иммунологии. 25 (1–3): 15–9. Дои:10.1016/0165-2478(90)90083-3. PMID 2126524.
- ^ Горчиниски и Станели, Клиническая иммунология. Landes Bioscience; Остин, Техас. ISBN 1-57059-625-5
- ^ Грин, SJ; Нейси, Калифорния; Schreiber, RD; Granger, DL; Кроуфорд, РМ; Meltzer, MS; Фортье, АХ (1993). «Нейтрализация гамма-интерферона и фактора некроза опухоли альфа блокирует in vivo синтез оксидов азота из L-аргинина и защиту от инфекции Francisella tularensis у мышей, получавших БЦЖ Mycobacterium bovis». Инфекция и иммунитет. 61 (2): 689–98. Дои:10.1128 / IAI.61.2.689-698.1993. ЧВК 302781. PMID 8423095.
- ^ Kamijo, R; Gerecitano, J; Шапиро, Д; Грин, SJ; Aguet, M; Ле, Дж; Вилчек, Дж (1995). «Образование оксида азота и клиренс гамма-интерферона после инфицирования БЦЖ нарушены у мышей, у которых отсутствует рецептор гамма-интерферона». Журнал воспаления. 46 (1): 23–31. PMID 8832969.
- ^ Грин, SJ; Шеллер, Л.Ф .; Марлетта, Массачусетс; Сегин, MC; Klotz, FW; Слейтер, М; Нельсон, Би Джей; Нейси, Калифорния (1994). «Оксид азота: цитокиновая регуляция оксида азота при устойчивости хозяина к внутриклеточным патогенам» (PDF). Письма иммунологии. 43 (1–2): 87–94. Дои:10.1016/0165-2478(94)00158-8. HDL:2027.42/31140. PMID 7537721.
- ^ Грин, SJ; Кроуфорд, РМ; Хокмайер, JT; Meltzer, MS; Нейси, Калифорния (1990). «Основные амастиготы Leishmania инициируют L-аргинин-зависимый механизм уничтожения в макрофагах, стимулированных IFN-гамма, путем индукции фактора некроза опухоли альфа». Журнал иммунологии. 145 (12): 4290–7. PMID 2124240.
- ^ Seguin, M. C .; Klotz, FW; Шнайдер, я; Weir, JP; Гудбэри, М; Слейтер, М; Рэйни, JJ; Aniagolu, JU; Грин, SJ (1994). «Индукция синтазы оксида азота защищает от малярии у мышей, подвергшихся воздействию облученных москитов, инфицированных Plasmodium berghei: участие интерферона гамма и CD8 + Т-клеток». Журнал экспериментальной медицины. 180 (1): 353–8. Дои:10.1084 / jem.180.1.353. ЧВК 2191552. PMID 7516412.
- ^ Меллук, S; Грин, SJ; Нейси, Калифорния; Хоффман, SL (1991). «IFN-гамма ингибирует развитие экзоэритроцитов Plasmodium berghei в гепатоцитах с помощью L-аргинин-зависимого эффекторного механизма». Журнал иммунологии. 146 (11): 3971–6. PMID 1903415.
- ^ Klotz, FW; Шеллер, Л.Ф .; Сегин, MC; Кумар, Н; Марлетта, Массачусетс; Грин, SJ; Азад, АФ (1995). «Совместная локализация индуцибельной синтазы оксида азота и Plasmodium berghei в гепатоцитах крыс, иммунизированных облученными спорозоитами». Журнал иммунологии. 154 (7): 3391–5. PMID 7534796.
- ^ Wink, D .; Kasprzak, K .; Maragos, C .; Elespuru, R .; Мисра, М; Dunams, T .; Cebula, T .; Koch, W .; Эндрюс, А .; Allen, J .; И другие. (1991). «Дезаминирующая способность ДНК и генотоксичность оксида азота и его предшественников». Наука. 254 (5034): 1001–3. Bibcode:1991Sci ... 254.1001W. Дои:10.1126 / science.1948068. PMID 1948068.
- ^ Nguyen, T .; Brunson, D .; Crespi, C.L .; Penman, B.W .; Wishnok, J. S .; Танненбаум, С. Р. (1992). «Повреждение ДНК и мутация в клетках человека, подвергшихся действию оксида азота in vitro». Труды Национальной академии наук. 89 (7): 3030–3034. Bibcode:1992ПНАС ... 89.3030Н. Дои:10.1073 / пнас.89.7.3030. ЧВК 48797. PMID 1557408. Открытый текст.
- ^ Ли, Чун-Ци; Панг, Бо; Кизилтепе, Таньел; Trudel, Laura J .; Engelward, Bevin P .; Дедон, Питер С .; Воган, Джеральд Н. (2006). «Пороговые эффекты токсичности, вызванной оксидом азота, и клеточных ответов в лимфобластоидных клетках человека дикого типа и без р53». Химические исследования в токсикологии. 19 (3): 399–406. Дои:10.1021 / tx050283e. ЧВК 2570754. PMID 16544944. открытый текст
- ^ Hibbs, John B .; Taintor, Read R .; Ваврин, Зденек; Рахлин, Эллиот М. (1988). «Оксид азота: цитотоксически активированная эффекторная молекула макрофага». Сообщения о биохимических и биофизических исследованиях. 157 (1): 87–94. Дои:10.1016 / S0006-291X (88) 80015-9. PMID 3196352.
- ^ Janeway, C.A .; и другие. (2005). Иммунобиология: иммунная система в здоровье и болезни (6-е изд.). Нью-Йорк: Наука Гарланд. ISBN 978-0-8153-4101-7.
- ^ Джейкобс, Лотте; Nawrot, Tim S; Де Геус, Бас; Мееузен, Ромен; Degraeuwe, Барт; Бернар, Альфред; Сугиш, Мухаммед; Немери, Бенуа; Панис, Люк (2010). «Субклинические реакции у здоровых велосипедистов, кратковременно подвергшихся воздействию загрязнения воздуха, связанного с дорожным движением: исследование вмешательства». Состояние окружающей среды. 9: 64. Дои:10.1186 / 1476-069X-9-64. ЧВК 2984475. PMID 20973949.
- ^ Corpas, F.J .; Barroso, JB; Каррерас, А; Quirós, M; Леон, AM; Ромеро-Пуэртас, MC; Esteban, FJ; Вальдеррама, Р. Пальма, JM; Сандалио, Л. М.; Gómez, M; Дель Рио, Лос-Анджелес (2004). «Клеточная и субклеточная локализация эндогенного оксида азота у молодых и стареющих растений гороха». Физиология растений. 136 (1): 2722–33. Дои:10.1104 / стр. 104.042812. ЧВК 523336. PMID 15347796.
- ^ Corpas, F.J .; Barroso, Juan B .; Каррерас, Альфонсо; Вальдеррама, Ракель; Пальма, Хосе М .; Леон, Ана М .; Сандалио, Луиза М .; Дель Рио, Луис А. (2006). «Конститутивная аргинин-зависимая активность синтазы оксида азота в различных органах проростков гороха во время развития растений». Planta. 224 (2): 246–54. Дои:10.1007 / s00425-005-0205-9. PMID 16397797.
- ^ Valderrama, R .; Corpas, Francisco J .; Каррерас, Альфонсо; Фернандес-Оканья, Ана; Чаки, Мунира; Луке, Франсиско; Гомес-Родригес, Мария В .; Колменеро-Вареа, Пилар; Дель Рио, Луис А .; Баррозу, Хуан Б. (2007). «Нитрозативный стресс у растений». FEBS Lett. 581 (3): 453–61. Дои:10.1016 / j.febslet.2007.01.006. PMID 17240373.
- ^ Corpas, F.J .; Barroso, Juan B .; Дель Рио, Луис А. (2004). «Ферментные источники оксида азота в растительных клетках - помимо одного белка - одна функция». Новый Фитолог. 162 (2): 246–7. Дои:10.1111 / j.1469-8137.2004.01058.x.
- ^ Зигель-Ицкович, Дж. (1999). «Виагра заставляет цветы вставать прямо». BMJ. 319 (7205): 274. Дои:10.1136 / bmj.319.7205.274a. ЧВК 1126920. PMID 10426722.
- ^ ван Фаассен, Э. и Ванин, А. (ред.) (2007) Радикалы для жизни: различные формы оксида азота.. Эльзевир, Амстердам, ISBN 978-0-444-52236-8
- ^ ван Фаассен, Э. и Ванин, А. (2004) «Оксид азота», в Энциклопедия аналитической науки, 2-е изд., Elsevier, ISBN 0127641009.
- ^ Shami, PJ; Мур, Джо; Gockerman, JP; Hathorn, JW; Misukonis, MA; Вайнберг, Дж. Б. (1995). «Модуляция оксида азота роста и дифференцировки свежевыделенных клеток острого нелимфоцитарного лейкоза». Исследование лейкемии. 19 (8): 527–33. Дои:10.1016 / 0145-2126 (95) 00013-Е. PMID 7658698.
- ^ Kaibori M .; Sakitani K .; Oda M .; Kamiyama Y .; Masu Y .; Окумура Т. (1999). «Иммунодепрессант FK506 ингибирует экспрессию индуцируемого гена синтазы оксида азота на стадии активации NF-κB в гепатоцитах крысы». J. Hepatol. 30 (6): 1138–1145. Дои:10.1016 / S0168-8278 (99) 80270-0. PMID 10406194.
- ^ Роудс, РА; Таннер, GA (2003). «Медицинская физиология 2-е издание». Сравнительная биохимия и физиология. A, Сравнительная физиология. 53 (1): 105–7. Дои:10.1016 / с0300-9629 (76) 80020-5. PMID 174.
- ^ Хогг Н., Сингх Р.Дж., Кальянараман Б. (18 марта 1996 г.). «Роль глутатиона в транспорте и катаболизме оксида азота». Письма FEBS. 382 (3): 223–228. Дои:10.1016/0014-5793(96)00086-5. PMID 8605974.
- ^ DeMaster EG, Quast BJ, Redfern B, Nagasawa HT (12 сентября 1995 г.). «Реакция оксида азота со свободной сульфгидрильной группой человеческого сывороточного альбумина дает сульфеновую кислоту и закись азота». Биохимия. 34 (36): 11494–11499. Дои:10.1021 / bi00036a023. PMID 7547878.
- ^ Хён Дж., Чаудхури Дж., Фукуто Дж. М. (1 сентября 1999 г.). «Восстановительный метаболизм оксида азота в гепатоцитах: возможное взаимодействие с тиолами». Метаболизм и утилизация лекарств. 27 (9): 1005–1009. PMID 10460799.
- ^ Finck, A.D., Samaniego, E., Ngai, S.H. [1995]. Закись азота избирательно высвобождает мет5-энкефалин и мет5-энкефалин-arg6-phe7 в спинномозговую жидкость третьего желудочка собак. Анестезия и анальгезия 80: 664-70
- ^ а б Евтович-Тодорович В., Тодорович С.М., Меннерик С., Пауэлл С., Дикраниан К., Беншофф Н., Зорумски К.Ф., Олни Дж. В. (апрель 1998 г.). «Закись азота (веселящий газ) - антагонист NMDA, нейропротектор и нейротоксин». Нат Мед. 4 (4): 460–463. Дои:10,1038 / нм0498-460. PMID 9546794.
- ^ Кристенсен Б., Рефсум Х, Гаррас А., Уиланд П.М. (июнь 1992 г.). «Реметилирование гомоцистеина во время воздействия закиси азота на клетки, культивируемые в средах, содержащих различные концентрации фолатов». J Pharmacol Exp Ther. 261 (3): 1096–1105. PMID 1602376.
- ^ Коблин Д.Д., Васкелл Л., Ватсон Дж. Э., Стокстад Е. Л., Эгер Е. И. 2-е (февраль 1982 г.). «Закись азота инактивирует метионинсинтетазу в печени человека». Анест Анальг. 61 (2): 75–78. Дои:10.1213/00000539-198202000-00001. PMID 7198880.
- ^ Сампат V, Чжао XJ, Caughey WS (27 апреля 2001 г.). «Анестезирующие взаимодействия оксида азота с альбумином и гемепротеинами. Механизм контроля функции белка». Журнал биологической химии. 276 (17): 13635–13643. Дои:10.1074 / jbc.M006588200. PMID 11278308.
- ^ Донг А., Хуан П., Чжао XJ, Сампат V, Каугей WS (30 сентября 1994 г.). «Характеристика участков, занятых анестетиком закиси азота в белках, с помощью инфракрасной спектроскопии». Журнал биологической химии. 269 (39): 23911–23917. PMID 7929038.
- ^ Эйнарсдоттир О., Каугей WS (5 июля 1988 г.). «Взаимодействие анестетика закиси азота с цитохром с оксидазой бычьего сердца. Влияние на структуру белка, активность оксидазы и другие свойства». Журнал биологической химии. 263 (19): 9199–9205. PMID 2837481.
- ^ Гиллман М.А., Лихтигфельд Ф.Дж. (март 1985 г.). «Закись азота действует непосредственно на мю-опиоидный рецептор». Анестезиология. 62 (3): 375–376. Дои:10.1097/00000542-198503000-00040. PMID 2983587.
- ^ а б Wu, L; Ван, Р. (декабрь 2005 г.). «Окись углерода: эндогенное производство, физиологические функции и фармакологические применения». Pharmacol Rev. 57 (4): 585–630. Дои:10.1124 / пр.57.4.3. PMID 16382109.
- ^ Олас, Беата (25 апреля 2014 г.). «Окись углерода не всегда является отравляющим газом для человеческого организма: физиологические и фармакологические особенности СО». Химико-биологические взаимодействия. 222 (5 октября 2014 г.): 37–43. Дои:10.1016 / j.cbi.2014.08.005. PMID 25168849.
- ^ Верма, А; Hirsch, D .; Glatt, C .; Ronnett, G .; Снайдер, С. (1993). «Окись углерода: предполагаемый нейронный мессенджер». Наука. 259 (5093): 381–4. Bibcode:1993Наука ... 259..381В. Дои:10.1126 / science.7678352. PMID 7678352.
- ^ а б Колата, Джина (26 января 1993 г.). «Угарный газ используется клетками мозга как нейротрансмиттер». Нью-Йорк Таймс. Получено 2 мая, 2010.
- ^ Ли, Л; Сюй, А; Мур, ПК (2009). «Действия и взаимодействия оксида азота, оксида углерода и сероводорода в сердечно-сосудистой системе и при воспалении - сказка о трех газах!». Фармакология и терапия. 123 (3): 386–400. Дои:10.1016 / j.pharmthera.2009.05.005. PMID 19486912.
- ^ Джонсон, Кэролайн Ю. (16 октября 2009 г.). «Ядовитый газ может принести пользу». Бостонский глобус. Получено 16 октября, 2009.
- ^ Керек Ф (сентябрь 2000 г.). «Структура дигиталисоподобных и натрийуретических факторов, идентифицированных как макроциклические производные неорганической субоксида углерода». Исследования гипертонии. 23 (Дополнение S33): S33–38. Дои:10.1291 / hypres.23.Supplement_S33. PMID 11016817.
- ^ Стимак Р., Керек Ф., Апелл Х. Дж. (Апрель 2003 г.). «Макроциклические олигомеры недооксида углерода как сильные ингибиторы Na, K-АТФазы». Летопись Нью-Йоркской академии наук. 986 (1): 327–329. Bibcode:2003НЯСА.986..327С. Дои:10.1111 / j.1749-6632.2003.tb07204.x. PMID 12763840.
- ^ Керек Ф., Стимак Р., Апелл Х. Дж., Фройденманн Ф., Мородер Л. (23 декабря 2002 г.). «Характеристика макроциклических факторов субоксида углерода как мощных ингибиторов Na, K-АТФазы и SR Са-АТФазы». Biochimica et Biophysica Acta (BBA) - Биомембраны. 1567 (1–2): 213–220. Дои:10.1016 / S0005-2736 (02) 00609-0. PMID 12488055.
- ^ Тубаро Э. (июнь 1966 г.). «Субоксид углерода, вероятный предшественник противоопухолевой клеточной устойчивости [sic]: сетчатка». Болл Чим Ферма (на итальянском). 105 (6): 415–416. PMID 6005012.
- ^ а б Лефер, Дэвид Дж. (Ноябрь 2007 г.). «Возникает новая газообразная сигнальная молекула: кардиозащитная роль сероводорода». PNAS. 104 (46): 17907–17908. Bibcode:2007ПНАС..10417907Л. Дои:10.1073 / pnas.0709010104. ЧВК 2084269. PMID 17991773.
- ^ Кимура, Хидео (2002). «Сероводород как нейромодулятор». Молекулярная нейробиология. 26 (1): 13–19. Дои:10.1385 / МН: 26: 1: 013. PMID 12392053.
- ^ а б Камун, Пьер (июль 2004 г.). "ЧАС2S, новый нейромодулятор ». Médecine / Науки. 20 (6–7): 697–700. Дои:10.1051 / medsci / 2004206-7697. PMID 15329822.
- ^ Бенавидес, Глория А; Squadrito, Джузеппе Л; Миллс, Роберт В. Патель, Хетал Д; Исбелл, Т. Скотт; Патель, Ракеш П.; Дарли-Усмар, Виктор М; Doeller, Jeannette E; Краус, Дэвид В. (13 ноября 2007 г.). «Сероводород опосредует вазоактивность чеснока». Труды Национальной академии наук Соединенных Штатов Америки. 104 (46): 17977–17982. Bibcode:2007ПНАС..10417977Б. Дои:10.1073 / pnas.0705710104. ЧВК 2084282. PMID 17951430.
- ^ а б "Токсичный газ, Спасатель ", Scientific American, Март 2010 г.
- ^ а б c d е Колетта С., Папапетропулос А., Эрдели К., Олах Г., Модис К., Панопулос П., Асимакопулу А., Геро Д., Шарина И., Мартин Е., Сабо С. (2012). «Сероводород и оксид азота взаимозависимы в регуляции ангиогенеза и эндотелий-зависимой вазорелаксации». Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 109 (23): 9161–6. Bibcode:2012PNAS..109.9161C. Дои:10.1073 / pnas.1202916109. ЧВК 3384190. PMID 22570497.
- ^ Филипович, М. Р .; Miljkovic, J. L .; Nauser, T .; Ройзен, М .; Klos, K .; Шубина, Т .; Koppenol, W.H .; Lippard, S.J .; Иванович-Бурмазович, И. (2012). «Химическая характеристика мельчайших S-нитрозотиолов, HSNO; межклеточные взаимодействия H2S и S-нитрозотиолов». Журнал Американского химического общества. 134 (29): 12016–12027. Дои:10.1021 / ja3009693. ЧВК 3408084. PMID 22741609.
- ^ Эммануэле ди Вилла Бьянка Р., Соррентино Р., Маффиа П., Мироне В., Имбимбо С., Фуско Ф., Де Пальма Р., Игнарро Л. Дж., Чирино Г. (2009). «Сероводород как медиатор расслабления гладких мышц кавернозного тела человека». PNAS. 106 (11): 4513–8. Bibcode:2009PNAS..106.4513D. Дои:10.1073 / pnas.0807974105. ЧВК 2657379. PMID 19255435.
- ^ «Сероводород: потенциальная помощь при ЭД». WebMD. 2 марта 2009 г.
- ^ а б c d е ж г час я j k л King AL, Polhemus DJ, Bhushan S, Otsuka H, Kondo K, Nicholson CK, Bradley JM, Islam KN, Calvert JW, Tao YX, Dugas TR, Kelley EE, Elrod JW, Huang PL, Wang R, Lefer DJ (январь 2014 г. ). «Цитопротекторная передача сигналов сероводорода является эндотелиальной зависимостью от синтазы оксида азота и оксида азота». PNAS. 111 (Раннее издание): 3182–3187. Bibcode:2014ПНАС..111.3182К. Дои:10.1073 / pnas.1321871111. ЧВК 3939925. PMID 24516168.
- ^ а б c d е Алп, Николай; Ченнон (2003). «Регулирование эндотелиальной синтазы оксида азота тетрагидробиоптерином при сосудистых заболеваниях». Журнал Американской кардиологической ассоциации. 24 (3): 413–420. Дои:10.1161 / 01.atv.0000110785.96039.f6. PMID 14656731.
- ^ а б Бёрт Нью-Джерси, Дей Н.Б., Корнуэлл Т.Л., Линкольн TM (1997). «Циклическая GMP-зависимая протеинкиназа регулирует фенотип клеток гладких мышц сосудов». Журнал сосудистых исследований. 34 (4): 245–259. Дои:10.1159/000159231. PMID 9256084.
- ^ а б Lincoln, T. M .; Корнуэлл, Тейлор (март 1990 г.). «ЦГМФ-зависимая протеинкиназа опосредует снижение Са2 + цАМФ в гладкомышечных клетках сосудов». Американский журнал физиологии. 258 (3): C399 – C407. Дои:10.1152 / ajpcell.1990.258.3.C399. PMID 2156436.
- ^ Это, Ко; Такаши Асада; Кунимаса Арима; Такао Макифути; Хидео Кимура (24 мая 2002). «При болезни Альцгеймера содержание сероводорода в мозге резко снижается». Сообщения о биохимических и биофизических исследованиях. 293 (5): 1485–1488. Дои:10.1016 / S0006-291X (02) 00422-9. PMID 12054683.
- ^ Ху, Л. Ф .; Лу, М .; Tiong, C. X .; Dawe, G. S .; Объятие.; Биан, Дж. С. (2010). «Нейропротекторные эффекты сероводорода на моделях крыс с болезнью Паркинсона». Ячейка старения. 9 (2): 135–146. Дои:10.1111 / j.1474-9726.2009.00543.x. PMID 20041858.
- ^ Мыши поставили "анабиоз", BBC News, 21 апреля 2005 г.
- ^ Газ вызывает анабиоз, BBC News, 9 октября 2006 г.
- ^ Флориан Б., Винтилеску Р., Бальсеану А.Т., Буга А.М., Гриск О., Уолкер Л.С., Кесслер С., Попа-Вагнер А. (2008). «Длительная гипотермия уменьшает объем инфаркта у старых крыс после очаговой ишемии». Neurosci. Латыш. 438 (2): 180–5. Дои:10.1016 / j.neulet.2008.04.020. PMID 18456407.
- ^ Марк Б. Рот и Тодд Нистул. Покупка времени в приостановленной анимации. Scientific American, 1 июня 2005 г.
- ^ Ли, Цзя; Чжан, Генчэн; Кай, Салли; Редингтон, Эндрю Н. (январь 2008 г.). «Влияние вдыхаемого сероводорода на метаболические реакции у анестезированных, парализованных и искусственно вентилируемых поросят». Педиатрическая реанимация. 9 (1): 110–112. Дои:10.1097 / 01.PCC.0000298639.08519.0C. PMID 18477923. Получено 2008-02-07.
ЧАС2S, по-видимому, не оказывает гипометаболических эффектов у крупных млекопитающих, охлаждаемых окружающей средой, и, наоборот, действует как гемодинамический и метаболический стимулятор.
- ^ Haouzi P, Notet V, Chenuel B, Chalon B, Sponne I, Ogier V и др. (2008). "ЧАС2S-индуцированный гипометаболизм у мышей отсутствует у овец, которым вводят седативные средства ". Респир Физиол Нейробиол. 160 (1): 109–15. Дои:10.1016 / j.resp.2007.09.001. PMID 17980679.
- ^ «Марк Рот: приостановленная анимация - в наших силах».
- ^ «IK-1001 (сульфид натрия (Na2S) для инъекций) у субъектов с острым инфарктом миокарда с подъемом сегмента ST». ClinicalTrials.gov. 2010-11-04.
Это исследование было отозвано до регистрации. (Решение компании. Не связано с безопасностью)
- ^ «Уменьшение сердечных травм, опосредованных ишемией-реперфузией, у субъектов, перенесших операцию по шунтированию коронарной артерии». ClinicalTrials.gov. 2011-08-03.
Это исследование было прекращено. (Исследование прекращено - решение компании)
- ^ Liu, D .; Джин, H; Тан, C; Ду, Дж (2010). «Диоксид серы: новый газовый сигнал в регуляции сердечно-сосудистых функций». Мини-обзоры по медицинской химии. 10 (11): 1039–1045. Дои:10.2174/1389557511009011039. PMID 20540708. Архивировано из оригинал на 2013-04-26. Получено 2015-03-06.
- ^ Chen S, Zheng S, Liu Z, Tang C, Zhao B, Du J, Jin H (февраль 2015 г.). «Эндогенный диоксид серы защищает от острого повреждения легких, вызванного олеиновой кислотой, в сочетании с ингибированием окислительного стресса у крыс». Лаборатория. Вкладывать деньги. 95 (2): 142–156. Дои:10.1038 / labinvest.2014.147. PMID 25581610.
- ^ Тиан Х. (ноябрь 2014 г.). «Достижения в изучении эндогенного диоксида серы в сердечно-сосудистой системе». Чин Мед Дж.. 127 (21): 3803–3807. PMID 25382339.
- ^ Ян Р, Ян И, Дон Х, Ву Х, Вэй И (август 2014 г.). «Корреляция между эндогенным диоксидом серы и гомоцистеином у детей с легочной артериальной гипертензией, связанной с врожденным пороком сердца». Чжунхуа Эр Кэ За Чжи (на китайском языке). 52 (8): 625–629. PMID 25224243.
- ^ Лю Д., Хуан И, Бу Д., Лю А. Д., Холмберг Л., Цзя И, Тан С., Ду Дж, Джин Х. (май 2014 г.). «Диоксид серы подавляет пролиферацию гладкомышечных клеток сосудов посредством подавления пути киназы Erk / MAP, опосредованного передачей сигналов цАМФ / PKA». Cell Death Dis. 5 (5): e1251. Дои:10.1038 / cddis.2014.229. ЧВК 4047873. PMID 24853429.
- ^ Ван XB, Jin HF, Tang CS, Du JB (16 ноября 2011 г.). «Биологическое действие эндогенного диоксида серы на сердечно-сосудистую систему». Eur J Pharmacol. 670 (1): 1–6. Дои:10.1016 / j.ejphar.2011.08.031. PMID 21925165.
- ^ Лян И, Лю Д., Очс Т., Тан Ч, Чен С., Чжан С., Гэн Б., Цзинь Х., Ду Дж (январь 2011 г.). «Эндогенный диоксид серы защищает от вызванного изопротеренолом повреждения миокарда и увеличивает антиоксидантную способность миокарда у крыс». Лаборатория. Вкладывать деньги. 91 (1): 12–23. Дои:10.1038 / labinvest.2010.156. PMID 20733562.
- ^ а б Боровиц Дж. Л., Гунасекар П. Г., Изом Г. Е. (12 сентября 1997 г.). «Генерация цианида водорода путем активации мю-опиатных рецепторов: возможная нейромодулирующая роль эндогенного цианида». Brain Res. 768 (1–2): 294–300. Дои:10.1016 / S0006-8993 (97) 00659-8. PMID 9369328.
- ^ Gunasekar PG, Prabhakaran K, Li L, Zhang L, Isom GE, Borowitz JL (май 2004 г.). «Рецепторные механизмы, опосредующие генерацию цианида в клетках PC12 и головном мозге крысы». Neurosci Res. 49 (1): 13–18. Дои:10.1016 / j.neures.2004.01.006. PMID 15099699.
- ^ Смит Р.П., Крушина Х. (январь 1976 г.). «Токсикология некоторых неорганических антигипертензивных анионов». Fed Proc. 35 (1): 69–72. PMID 1245233.
- ^ "Обзор субстанции PubChem". Получено 7 июля 2009.
- ^ Zschocke, Йоханнес; Георг Хоффман (2004). Vademecum Метаболизм. Фридрихсдорф, Германия: Milupa GmbH.
- ^ Роуз, Бертон; Хельмут Реннке (1994). Почечная патофизиология. Балтимор: Уильямс и Уилкинс. ISBN 978-0-683-07354-6.
- ^ Эстер Туболи; Андреа Сабо; Денес Гараб; Габор Барта; Агнес Яновски; Габор Эро; Анна Сабо; Арпад Мохачи; Габор Сабо; Йожеф Касаки; Миклош Гичи; Михай Борос (15 января 2013 г.). «Биогенез метана при индуцированной азидом натрия химической гипоксии у крыс». Американский журнал физиологии. Клеточная физиология. 304 (2): 207–214. Дои:10.1152 / ajpcell.00300.2012. PMID 23174561.
- ^ Туболи Э., Сабо А., Эрёш Г., Мохачи А., Сабо Г., Тенгёлич Р., Ракхели Г., Борос М. (декабрь 2013 г.). «Определение эндогенного образования метана с помощью фотоакустической спектроскопии» (PDF). J дыхание Res. 7 (4): 046004. Bibcode:2013JBR ..... 7d6004T. Дои:10.1088/1752-7155/7/4/046004. PMID 24185326.
- ^ Саакян А.Б., Джи С.Р., Пиментел М. (август 2010 г.). «Метан и желудочно-кишечный тракт». Dig Dis Sci. 55 (8): 2135–2143. Дои:10.1007 / s10620-009-1012-0. PMID 19830557.
- ^ а б c Lin, Z .; Чжун, S .; Грирсон, Д. (2009). «Последние достижения в исследованиях этилена». J. Exp. Бот. 60 (12): 3311–36. Дои:10.1093 / jxb / erp204. PMID 19567479.
- ^ Внешняя ссылка на дополнительную информацию о выделении этиленового газа и контроле диоксида углерода В архиве 2010-09-14 на Wayback Machine. ne-postharvest.com
- ^ Нелюбов Д. (1901). «Uber die Horizontale Nutation der Stengel von Pisum sativum und einiger anderen Pflanzen». Бей Бот Zentralbl. 10: 128–139.
- ^ Сомнение, Сара Л. (1917). «Реакция растений на световой газ». Ботанический вестник. 63 (3): 209–224. Дои:10.1086/332006. HDL:2027 / mdp.39015068299380. JSTOR 2469142.
- ^ Гейн Р. (1934). «Производство этилена некоторыми фруктами». Природа. 134 (3400): 1008. Bibcode:1934Натура.134.1008Г. Дои:10.1038 / 1341008a0.
- ^ Крокер В., Хичкок А.Е., Циммерман П.В. (1935) «Сходства в действии этлиена и ауксинов растений». Contrib. Boyce Thompson Inst. 7. 231-48. Ауксины Цитокинины ИУК Вещества для роста, Этилен
- ^ Ян, С. Ф .; Хоффман Н. Э. (1984). «Биосинтез этилена и его регуляция у высших растений». Анну. Rev. Plant Physiol. 35: 155–89. Дои:10.1146 / annurev.pp.35.060184.001103.
- ^ Bleecker, A.B .; Esch, J. J .; Холл, А. Э .; Rodríguez, F. I .; Биндер, Б. М. (1998). «Семейство рецепторов этилена из Arabidopsis: структура и функции». Философские труды Королевского общества B: биологические науки. 353 (1374): 1405–12. Дои:10.1098 / rstb.1998.0295. ЧВК 1692356. PMID 9800203.
- ^ Объяснение эпинастии. planthormones.inf
- ^ Танимото, Мими; Робертс, Кейт; Долан, Лиам (декабрь 1995 г.). «Этилен является положительным регулятором развития корневых волосков Arabidopsis thaliana». Журнал растений. 8 (6): 943–948. Дои:10.1046 / j.1365-313X.1995.8060943.x. PMID 8580964.
- ^ Чжан, Инцзяо; Ду, Хуань; Сюй, Фэйюнь; Дин, Есинь; Гуй, Яо; Чжан, Цзяньхуа; Сюй, Вэйфэн (июнь 2020 г.). «Ассоциации корневых бактерий способствуют формированию ризошита в умеренно сухой почве за счет реакции на этилен». Физиология растений. 183 (2): 780–792. Дои:10.1104 / стр.19.01020. ЧВК 7271771. PMID 32220965.
- ^ Хартман, Сьон (3 июня 2020 г.). «В ловушке ризошита: взаимодействия корень-бактерия модулируют передачу сигналов этилена». Физиология растений. 183 (2): 443–444. Дои:10.1104 / стр. 20.00379. ЧВК 7271798. PMID 32493810.
- ^ Дауд, Тикра; Ян, Синьпин; Visser, Eric J.W .; те Бик, Тим А.Х .; Kensche, Philip R .; Cristescu, Simona M .; Ли, Сангсок; Флокова, Кристина; Нгуен, Дай; Мариани, Селестина; Рье, Иво (апрель 2016 г.). «Кооперативный гормональный каскад активирует спящие придаточные корневые примордии при наводнении в Дулькамаре». Физиология растений. 170 (4): 2351–2364. Дои:10.1104 / стр.15.00773. ЧВК 4825138. PMID 26850278.
- ^ Неги, Сангита; Сукумар, Пурнима; Лю, Син; Коэн, Джерри Д.; Мудай, Глория К. (январь 2010 г.). «Генетическое изучение роли этилена в регуляции ауксин-зависимых боковых и придаточных корней в томате». Журнал растений. 61 (1): 3–15. Дои:10.1111 / j.1365-313X.2009.04027.x. HDL:10339/30054. PMID 19793078.
- ^ Хартман, S; Лю, Z; van Veen, H; Vicente, J; Reinen, E; Martopawiro, S; Чжан, Х; ван Донген, Н; Босман, Ф; Бассель, GW; Виссер, EJW; Бейли-Серрес, Дж; Теодулу, Флорида; Hebelstrup, KH; Гиббс, диджей; Холдсворт, MJ; Sasidharan, R; Voesenek, LACJ (5 сентября 2019 г.). «Этилен-опосредованное истощение оксида азота предварительно адаптирует растения к стрессу гипоксии». Nature Communications. 10 (1): 4020. Bibcode:2019НатКо..10.4020H. Дои:10.1038 / s41467-019-12045-4. ЧВК 6728379. PMID 31488841.
- ^ ван Вин и др., [1], Растительная клетка, 2013
- ^ Хартман, Сьон; Сасидхаран, Рашми; Военек, Лаврентий А.С.Дж. (18 января 2020 г.). «Роль этилена в метаболической адаптации к низкому содержанию кислорода». Новый Фитолог. Дои:10.1111 / nph.16378. PMID 31856295.
- ^ Барри, Корнелиус С .; Джованнони, Джеймс Дж. (6 июня 2007 г.). «Этилен и созревание плодов». Журнал регулирования роста растений. 26 (2): 143–159. Дои:10.1007 / s00344-007-9002-y.
- ^ Wilmowicz E, Kesy J, Kopcewicz J (декабрь 2008 г.). «Взаимодействие этилена и АБК в регуляции индукции цветков у Фарбитис ноль". J. Plant Physiol. 165 (18): 1917–28. Дои:10.1016 / j.jplph.2008.04.009. PMID 18565620.
- ^ Кокшалл К.Э., Хорридж Дж.С. (1978). "2-Хлорэтилфосфоновая кислота и инициация цветков Хризантема морифолиум Рамат. В короткие дни и в длинные дни ». Журнал садоводства и биотехнологии. 53 (2): 85–90. Дои:10.1080/00221589.1978.11514799.
- ^ Филзер Дж. Г., Денк Б., Тёрнквист М., Кесслер В., Эренберг Л. (1992). «Фармакокинетика этилена у человека; нагрузка на организм оксидом этилена и гидроксиэтилирование гемоглобина из-за эндогенного и экологического этилена». Arch. Токсикол. 66 (3): 157–163. Дои:10.1007 / bf01974008. PMID 1303633.
- ^ Bolt HM, Leutbecher M, Golka K (1997). «Заметка о физиологическом фоне аддукта этиленоксида 7- (2-гидроксиэтил) гуанина в ДНК из крови человека». Arch. Токсикол. 71 (11): 719–721. Дои:10.1007 / s002040050451. PMID 9363847.
- ^ Csanády GA, Denk B, Pütz C, Kreuzer PE, Kessler W, Baur C, Gargas ML, Filser JG (15 мая 2000 г.). «Физиологическая токсикокинетическая модель экзогенного и эндогенного этилена и оксида этилена у крыс, мышей и людей: образование 2-гидроксиэтильных аддуктов с гемоглобином и ДНК». Токсикол Аппл Фармакол. 165 (1): 1–26. Дои:10.1006 / taap.2000.8918. PMID 10814549.
- ^ Thier R, Bolt HM (сентябрь 2000 г.). «Канцерогенность и генотоксичность окиси этилена: новые аспекты и последние достижения». Крит Rev Toxicol. 30 (5): 595–608. Дои:10.1080/10408440008951121. PMID 11055837.
внешние ссылки
 СМИ, связанные с Газообразные сигнальные молекулы в Wikimedia Commons
СМИ, связанные с Газообразные сигнальные молекулы в Wikimedia Commons
