Jemmis mno правила - Jemmis mno rules
Эта статья поднимает множество проблем. Пожалуйста помоги Улучши это или обсудите эти вопросы на страница обсуждения. (Узнайте, как и когда удалить эти сообщения-шаблоны) (Узнайте, как и когда удалить этот шаблон сообщения)
|
В химия, то Джеммис mno правила представляют собой единое правило прогнозирования и систематизации структур соединения, обычно кластеры. Правила включают счет электронов. Их сформулировали Элуватингал Девасси Джеммис для объяснения структуры конденсированных полиэдрических боранов, таких как B
20ЧАС
16, которые получаются путем уплотнения многогранных боранов путем разделения треугольной грани, ребра, одной вершины или четырех вершин. Эти правила являются дополнениями и расширениями к Правила Уэйда и теория пар многогранных скелетных электронов.[1][2] Джеммис mno Правило обеспечивает связь между полиэдрическими боранами, конденсированными полиэдрическими боранами и β-ромбоэдрическим бором.[3][4] Это похоже на отношения между бензол, конденсированные бензоидные ароматические углеводороды, и графит, показано Хюккеля 4п + 2 правило, а также взаимосвязь между тетракоординированными тетраэдрическими соединениями углерода и алмаз. Джеммис mno правила сводятся к правилу Хюккеля, когда они ограничиваются двумя измерениями, и сводятся к правилам Уэйда, когда они ограничиваются одним многогранником.[5]
Правила счета электронов
Правила счета электронов используются для прогнозирования предпочтительного счета электронов для молекул. В Правило октета, то Правило 18 электронов, и Хюккеля 4п + 2 правила пи-электронов доказано, что они полезны для предсказания молекулярной стабильности. Правила Уэйда были сформулированы для объяснения электронных требований монополиэдрических борановых кластеров. Джеммис mno правила - это расширение правил Уэйда, обобщенное также на конденсированные многогранные бораны.
Первый конденсированный многогранный боран, B
20ЧАС
16, формируется разделением четырех вершин между двумя икосаэдры. По словам Уэйда п +1 правило для п-вертекс близко конструкции, B
20ЧАС
16 должен иметь заряд +2 (п + 1 = 20 + 1 = 21 требуется пара; 16 блоков BH обеспечивают 16 пар; четыре общих атома бора образуют 6 пар; Таким образом, доступно 22 пары). Чтобы учесть существование B
20ЧАС
16 как нейтральные частицы, и чтобы понять электронные потребности конденсированных полиэдрических кластеров, новой переменной, м, введено и соответствует количеству многогранников (подкластеров).[6] У Уэйда п +1 правило, 1 соответствует основной молекулярной орбитали (BMO), а п соответствует количеству вершин, которое, в свою очередь, равно количеству BMO касательной поверхности. Если м многогранники конденсируются, образуя макрополиэдр, м основные BMO будут сформированы. Таким образом, потребность в скелетных электронных парах (SEP) для плотноконденсированных полиэдрических кластеров составляет м + п.
Совместное использование одной вершины - это особый случай, когда каждый подкластер должен удовлетворять правилу Уэйда отдельно. Позволять а и б быть количеством вершин в подкластерах, включая общий атом. Первая клетка требует а +1, а для второй клетки требуется б +1 SEP. Таким образом, всего а + б + 2 или а + б + м SEPs обязательны; но а + б = п + 1, так как общий атом считается дважды. Правило можно изменить на м + п +1, или вообще м + п + о, куда о соответствует количеству одновершинных общих сгущений. Правило можно сделать более общим, введя переменную п, соответствующее количеству пропущенных вершин, и q, количество крышек. Таким образом, обобщенное правило Джеммиса можно сформулировать следующим образом:
- Требование SEP для конденсированных полиэдрических кластеров: м + п + о + п − q, куда м количество подкластеров, п - количество вершин, о - количество однократных общих сгущений, п количество пропущенных вершин и q количество крышек.[4][7]
Примеры
B20ЧАС16

м + п + о + п − q = 2 + 20 + 0 + 0 + 0 = 22 SEP необходимо; 16 блоков BH обеспечивают 16 пар; четыре общих атома бора составляют 6 пар, что объясняет, почему B
20ЧАС
16 устойчив как нейтральный вид.[7]
B21ЧАС−
18
близко-B
21ЧАС−
18 образован сгущением двух икосаэдров с разделением граней. В м + п + о + п − q правило требует 23 SEP; 18 единиц BH образуют 18 пар, а 3 общих атома бора обеспечивают4 1⁄2 пары; отрицательный заряд дает одну половину пары.[8]
B12ЧАС16
Бис-нидо-B
12ЧАС
16 формируется конденсацией с разделением ребер нидо-B
8 единица и нидо-B
6 единица. В м + п + о + п − q Число из 16 SEP удовлетворяется десятью единицами BH, которые образуют 10 пар, двумя общими атомами бора, которые образуют 3 пары, и шестью мостиковыми атомами H, которые образуют 3 пары.[7]
Cu (B11ЧАС11)3−
2
м + п + о + п − q = 26 SEP. Переходный металл с п валентные электроны обеспечивают п - 6 электронов для скелетного связывания, поскольку 6 электронов, занимающих металлоподобные орбитали, не вносят большого вклада в связывание кластеров. Поэтому Cu обеспечивает2 1⁄2 пары, 22 блока BH обеспечивают 22 пары; три отрицательных заряда обеспечивают1 1⁄2 пары.[7]
Ферроцен

Согласно м + п + о + п − q правило ферроцен требует 2 + 11 + 1 + 2-0 = 16 SEP. 10 блоков CH обеспечивают 15 пар, а Fe - одну пару. [7]
B18ЧАС2−
20
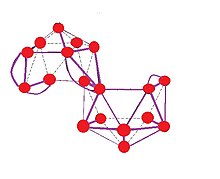
18ЧАС2−
20, удалено водород
B
18ЧАС2−
20 бис-нидо многогранник с общим ребром. Здесь, м + п + о + п − q = 2 + 18 + 0 + 2-0 = 22; 16 единиц BH образуют 16 пар, 4 мостиковых атома водорода образуют 2 пары, два общих атома бора образуют 3 пары, а два отрицательных заряда составляют 1 пару.[7]
Трехэтажные комплексы
Известно, что трехуровневые комплексы подчиняются правилу 30-валентных электронов (VE). Вычитание 6 пар несвязывающих электронов из двух атомов металла доводит количество SEP до 9 пар. Для трехэтажного комплекса с C
5ЧАС
5 как колоды, м + п + о + п − q = 3 + 17 + 2 + 2 - 0 = 24. Вычитая 15 пар, соответствующих C – C сигма-облигации, становится 9 пар. Например, рассмотрим (C
5(CH
3)
5)
3RU+
2: 15 C – CH3 группы предоставляют22 1⁄2 пары. Каждый атом рутения дает одну пару. Удаление электрона, соответствующего положительному заряду комплекса, приводит к общему количеству22 1⁄2 + 2 − 1⁄2 = 24 пары.
β-ромбоэдрический бор

105, концептуально фрагментирован на B
57 и B
48.
Структура β-ромбоэдрического бора осложняется наличием частичных заселенностей и вакансий.[9][10][11] Идеализированная элементарная ячейка, B
105 было показано, что он электронодефицитный и, следовательно, металлический согласно теоретическим исследованиям, но β-бор является полупроводником.[12] Применение правила Джеммиса показывает, что частичные заселенности и вакансии необходимы для достаточности электронов.
B
105 можно концептуально разделить на B
48 фрагмент и B
28−B − B
28 (B
57) фрагмент. Согласно правилу Уэйда, B
48 Для фрагмента требуется 8 электронов (для икосаэдра в центре (зеленый) требуется 2 электрона; каждая из шести пятиугольных пирамид (черная и красная) завершает икосаэдр в расширенной структуре; таким образом, электронное требование для каждой из них равно 1). В B
28−B − B
28 или же B
57 образован конденсацией 6 икосаэдров и двух тригональные бипирамиды. Здесь, м + п + о + п − q = 8 + 57 + 1 + 0 - 0 = 66 пар, необходимых для устойчивости, но67 1⁄2 доступны. Следовательно B
28−B − B
28 фрагмент имеет 3 лишних электрона и идеализированный B105 отсутствует 5 электронов. 3 лишних электрона в B
28−B − B
28 фрагмент можно удалить, удалив один атом B, что приводит к B
27−B − B
28 (B
56). Требование 8 электронов по B
48 фрагмент может быть удовлетворен2 2⁄3 атомов бора, а в элементарной ячейке 48 + 56 +2 2⁄3 = 106 2⁄3, что очень близко к экспериментальному результату.[3]
Рекомендации
- ^ Уэйд, К. (1971). «Структурное значение количества скелетных связывающих электронных пар в карборанах, высших боранах и анионах борана, а также различных соединениях кластера карбонила переходных металлов». J. Chem. Soc. D (15): 792. Дои:10.1039 / c29710000792.
- ^ Мингос, Д. М. П (1984). "Подход многогранных скелетных электронных пар". Соотв. Chem. Res. 17 (9): 311–319. Дои:10.1021 / ar00105a003.
- ^ а б Джеммис, Э.; Балакришнараджан, М. М. (2001). «Полиэдрические бораны и элементарный бор: прямые структурные связи и различные электронные требования». Варенье. Chem. Soc. 123 (18): 4324–4330. Дои:10.1021 / ja0026962.
- ^ а б Джеммис, Э.; Балакришнараджан, М. М .; Панчаратна, П. Д. (2001). «Объединяющее правило подсчета электронов для макрополиэдрических боранов, металлаборанов и металлоценов». Варенье. Chem. Soc. 123 (18): 4313–4323. Дои:10.1021 / ja003233z. PMID 11457198.
- ^ Джеммис, Э.; Джаясри, Э. Г. (2003). «Аналогии между бором и углеродом». Соотв. Chem. Res. 36 (11): 816–824. Дои:10.1021 / ar0300266. PMID 14622028.
- ^ Джеммис, Э.; Балакришнараджан, М. М. (2000). «Электронные требования к поликонденсированным полиэдральным боранам». Варенье. Chem. Soc. 122 (18): 4516–4517. Дои:10.1021 / ja994199v.
- ^ а б c d е ж Джеммис, Э.; Балакришнараджан, М. М .; Панчаратна, П. Д. (2002). «Электронные требования к макрополиэдральным боранам». Chem. Rev. 102 (1): 93–144. Дои:10.1021 / cr990356x. PMID 11782130.
- ^ Bernhardt, E .; Брауэр, Д. Дж .; Finze, M .; Виллнер, Х. (2007). "близко- [B21ЧАС18]−: Диикосаэдрический борат-ион с лицевым плавлением ". Энгью. Chem. Int. Эд. Англ. 46 (16): 2927–2930. Дои:10.1002 / anie.200604077. PMID 17366499.
- ^ Hughes, R.E .; Kennard, C.H.L .; Sullenger, D. B .; Weakliem, H. A .; Сэндс, Д. Э .; Клад, Дж. Л. (1963). «Строение β-ромбоэдрического бора». Варенье. Chem. Soc. 85 (3): 361–362. Дои:10.1021 / ja00886a036.
- ^ Hoard, J. L .; Sullenger, D. B .; Kennard, C.H.L .; Хьюз, Р. Э. (1970). «Структурный анализ β-ромбоэдрического бора». J. Solid State Chem.. 1 (2): 268–277. Bibcode:1970JSSCh ... 1..268H. Дои:10.1016/0022-4596(70)90022-8.
- ^ Slack, G.A .; Hejna, C. I .; Гарбаускас, М. Ф .; Каспер, Дж. С. (1988). «Кристаллическая структура и плотность β-ромбоэдрического бора». J. Solid State Chem.. 76 (1): 52–63. Bibcode:1988ЖСЩ..76 ... 52С. Дои:10.1016/0022-4596(88)90192-2.
- ^ Прасад, Д. Л. В. К; Балакришнараджан, М. М .; Джеммис, Э. (2005). «Электронная структура и связывание β-ромбоэдрического бора с использованием метода кластерных фрагментов». Phys. Ред. B. 72 (19): 195102. Bibcode:2005ПхРвБ..72с5102П. Дои:10.1103 / Physrevb.72.195102.
