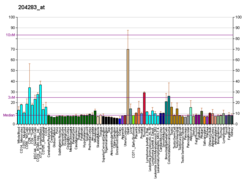
FARS2 - FARS2
Фенилаланил-тРНК синтетаза, митохондриальная (FARS2) является фермент что у людей кодируется FARS2 ген.[5] Этот белок закодировано FARS2 локализуется в митохондрия и играет роль в митохондриальной трансляция белков. Мутации в этом гене были связаны с комбинированным дефицитом окислительного фосфорилирования 14, также известным как энцефалопатия Альперса, а также спастическая параплегия 77 и младенческое начало эпилепсия и цитохром с оксидаза дефицит.[6][7]
Структура
FARS2 расположен на p рука из хромосома 6 в позиции 25.1 и имеет 15 экзоны.[6] Этот ген кодирует член аминоацил-тРНК синтетаза класса II семья.[8][9] FARS2 представляет собой фенилаланин-тРНК синтетаза (PheRS) локализован на митохондрия который состоит из одного полипептидная цепь, в отличие от (альфа-бета) 2 структуры прокариотический и эукариотический цитоплазматический формы PheRS. Структурный анализ и каталитический Свойства указывают на то, что митохондриальные PheRS могут составлять класс PheRS, отличный от ферментов, обнаруженных в прокариотах и в цитоплазме эукариот.[6]
Функция
Аминоацил-тРНК синтетазы являются классом ферменты это обвинение тРНК с их родственными аминокислоты.[6] FARS2 заряжает тРНК (Phe) с фенилаланин и катализирует прямое присоединение m-Tyr (окисленной версии Phe) к тРНК (Phe). Это делает его важным для митохондриальной перевод и для доставки мизацилированной тРНК к рибосома и включение ROS -поврежденная аминокислота в белки.[8][9][10][11] Альтернативная сварка приводит к множеству вариантов транскрипции.[6]
Каталитическая активность
АТФ + L-фенилаланин + тРНК (Phe) = AMP + дифосфат + L-фенилаланил-тРНК (Phe)[8][9][10][11]
Клиническое значение
Мутации в FARS2 были связаны с дефицитом комбинированного окислительного фосфорилирования 14, спастическая параплегия 77 и младенческое начало эпилепсия и цитохром с оксидаза дефицит. И комбинированный дефицит окислительного фосфорилирования 14, и спастическая параплегия 77 являются аутосомно-рецессивный в природе и были связаны с несколькими патогенными вариантами, включая Y144C,[12] И329Т, Д391В,[11] и D142Y.[13] Дефицит комбинированного окислительного фосфорилирования 14 характеризуется неонатальным началом глобальная задержка развития, огнеупорный припадки, лактоацидоз и дефицит множества митохондриальных дыхательных ферментов. Между тем спастическая параплегия - это нейродегенеративное расстройство характеризуется медленной, постепенной, прогрессирующей слабостью и спастичность нижних конечностей, при этом пациенты часто испытывают трудности с равновесием, слабость и скованность в ногах, мышечные спазмы и волочение пальцев ног при ходьбе.[8][9] Один случай детской эпилепсии и недостаточности цитохром с оксидазы в результате FARS2 Asp325Tyr миссенс-мутация также не поступало. Эпилепсия с ранним началом, неврологический дефицит, и комплекс IV дефицит - основные характеристики болезни, вызванной этой мутацией.[7]
Взаимодействия
Было показано, что FARS2 имеет 193 двоичных файла. белок-белковые взаимодействия включая 12 сопряженных взаимодействий. FARS2, похоже, взаимодействует с RCBTB2, КРТАП10-9, CALCOCO2, KRT40, MID2, APPL1, IKZF3, KRT13, TADA2A, STX11, TRIM27, КРТАП10-5, КРТАП10-7, TFCP2, MKRN3, KRT31, HMBOX1, AGTRAP, ADAMTSL4, NOTCH2NL, CMTM5, TRIM54, FSD2, CYSRT1, HIGD1C, homez, SPRY1, ZNF500, KRT34, YIF1A, BAG4, TPM2, SYP, КРТАП10-8, КРТАП1-1, AP1B1, TRAF2, GRB10, MESD, TRIP6, CCDC152, BEX5, FHL5, MORN3, DGAT2L6, ZNF438, KCTD17, ZNF655, БАНП, СПЕРТ, NFKBID, ZNF526, PCSK5, DVL3, АДЖУБА, PPP1R16B, MDFI, DPH2, CDCA4, KRTAP3-3, BACH2, KCNF1, MAN1C1, RIMBP3, ZRANB1, ISY1, FKBP7, и E7.[14]
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000145982 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск ансамбля 89: ENSMUSG00000021420 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Буллард Дж. М., Цай Ю. С., Демелер Б., Спремулли Л. Л. (май 1999 г.). «Экспрессия и характеристика митохондриальной фенилаланил-тРНК синтетазы». Журнал молекулярной биологии. 288 (4): 567–77. Дои:10.1006 / jmbi.1999.2708. PMID 10329163.
- ^ а б c d е «Ген Entrez: FARS2 фенилаланил-тРНК синтетаза 2, митохондриальная».
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ а б Алмалки А., Алстон К.Л., Паркер А., Симоник И., Мехта С.Г., Хе Л., Реза М., Оливейра Дж. М., Лайтаулерс Р.Н., МакФарланд Р., Тейлор Р.В., Хшановска-Лайтаулерс З.М. (январь 2014 г.). «Мутация митохондриальной фенилаланин-тРНК синтетазы человека вызывает детскую эпилепсию и дефицит цитохром с оксидазы». Biochimica et Biophysica Acta (BBA) - Молекулярная основа болезни. 1842 (1): 56–64. Дои:10.1016 / j.bbadis.2013.10.008. ЧВК 3898479. PMID 24161539.
- ^ а б c d «FARS2 - фенилаланин - тРНК-лигаза, митохондриальный предшественник - Homo sapiens (человек) - ген и белок FARS2». www.uniprot.org. Получено 2018-09-05.
 Эта статья включает текст, доступный под CC BY 4.0 лицензия.
Эта статья включает текст, доступный под CC BY 4.0 лицензия. - ^ а б c d «UniProt: универсальная база знаний о белках». Исследования нуклеиновых кислот. 45 (D1): D158 – D169. Январь 2017 г. Дои:10.1093 / нар / gkw1099. ЧВК 5210571. PMID 27899622.
- ^ а б Клипкан Л., Мур Н., Кесслер Н., Сафро М.Г. (июль 2009 г.). «Эукариотические цитозольные и митохондриальные фенилаланил-тРНК-синтетазы катализируют заряд тРНК метатирозином». Труды Национальной академии наук Соединенных Штатов Америки. 106 (27): 11045–8. Bibcode:2009ПНАС..10611045К. Дои:10.1073 / pnas.0905212106. ЧВК 2700156. PMID 19549855.
- ^ а б c Эло Дж. М., Ядавалли С. С., Евро Л., Исоханни П., Гётц А., Кэрролл С. Дж., Валан Л., Алькурая Ф. С., Уусимаа Дж., Паэтау А., Карузо Е. М., Пихко Н., Ибба М., Тюнисмаа Н., Суомалайнен А. (октябрь 2012 г.) «Мутации митохондриальной фенилаланил-тРНК-синтетазы лежат в основе фатальной детской энцефалопатии Альперса». Молекулярная генетика человека. 21 (20): 4521–9. Дои:10.1093 / hmg / dds294. PMID 22833457.
- ^ Шамселдин Х.Э., Альшаммари М., Аль-Шедди Т., Салих М.А., Алхалиди Х., Кентаб А., Репетто Г.М., Хашем М., Алькурая Ф.С. (апрель 2012 г.). «Геномный анализ митохондриальных заболеваний кровнородственной популяции обнаруживает новые гены-кандидаты болезней». Журнал медицинской генетики. 49 (4): 234–41. Дои:10.1136 / jmedgenet-2012-100836. PMID 22499341. S2CID 5856138.
- ^ Ян И, Лю В., Фанг З., Ши Дж, Че Ф, Хе Ц, Яо Л., Ван Э, Ву И (февраль 2016 г.). «Недавно идентифицированная миссенс-мутация в FARS2 вызывает аутосомно-рецессивную спастическую параплегию». Человеческая мутация. 37 (2): 165–9. Дои:10.1002 / humu.22930. PMID 26553276. S2CID 46241711.
- ^ «По запросу FARS2 найдено 193 бинарных взаимодействия». База данных по молекулярным взаимодействиям IntAct. EMBL-EBI. Получено 2018-09-05.
внешняя ссылка
- Обзор синдрома Ли, кодируемого ядерными генами
- Синдром Ли, ассоциированный с митохондриальной ДНК, и НАРП
- Обзор всей структурной информации, доступной в PDB за UniProt: O95363 (Фенилаланин - тРНК лигаза, митохондриальная) на PDBe-KB.
дальнейшее чтение
- Левин И., Кесслер Н., Мур Н., Клипкан Л., Коч Е., Темплтон П., Спремулли Л., Сафро М. (сентябрь 2007 г.). «Очистка, кристаллизация и предварительная рентгеновская характеристика митохондриальной фенилаланил-тРНК синтетазы человека». Acta Crystallographica Раздел F. 63 (Пт 9): 761–4. Дои:10.1107 / S1744309107038651. ЧВК 2376306. PMID 17768348.
- Бранденбергер Р., Вэй Х., Чжан С., Лей С., Мурадж Дж., Фиск Дж. Дж., Ли И, Сюй Ц., Фанг Р., Гуглер К., Рао М. С., Мандалам Р., Лебковски Дж., Стэнтон Л. В. (июнь 2004 г.). «Характеристика транскриптома проясняет сигнальные сети, которые контролируют рост и дифференцировку ES-клеток человека». Природа Биотехнологии. 22 (6): 707–16. Дои:10.1038 / nbt971. PMID 15146197. S2CID 27764390.
- Харрингтон Дж. Дж., Шерф Б., Рандлетт С., Джексон П. Д., Перри Р., Каин С., Левенталь К., Торнтон М., Рамачандран Р., Уиттингтон Дж., Лернер Л., Костанцо Д., Макэллиготт К., Бузер С., Мэйс Р., Смит Е., Велозо Н. , Klika A, Hess J, Cothren K, Lo K, Offenbacher J, Danzig J, Ducar M (май 2001 г.). «Создание полногеномных библиотек экспрессии белков с использованием случайной активации экспрессии генов». Природа Биотехнологии. 19 (5): 440–5. Дои:10.1038/88107. PMID 11329013. S2CID 25064683.
- Судзуки Ю., Ёситомо-Накагава К., Маруяма К., Суяма А., Сугано С. (октябрь 1997 г.). «Создание и характеристика полноразмерной библиотеки кДНК, обогащенной по 5'-концу». Ген. 200 (1–2): 149–56. Дои:10.1016 / S0378-1119 (97) 00411-3. PMID 9373149.
- Маруяма К., Сугано С. (январь 1994 г.). «Олиго-кэппинг: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Ген. 138 (1–2): 171–4. Дои:10.1016/0378-1119(94)90802-8. PMID 8125298.
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.