Морские биогеохимические циклы - Marine biogeochemical cycles

Морские биогеохимические циклы находятся биогеохимические циклы что происходит в морская среда, то есть в соленая вода морей или океанов или солоноватый вода прибрежных эстуарии. Эти биогеохимические циклы - это пути химические субстанции и элементы перемещаться в морской среде. Кроме того, вещества и элементы можно импортировать или вывозить из морской среды. Этот импорт и экспорт могут происходить в виде обмена с атмосферой наверху, дном океана внизу или в виде стока с суши.
Есть биогеохимический циклы для элементов кальций, углерод, водород, Меркурий, азот, кислород, фосфор, селен, и сера; молекулярные циклы для воды и кремнезем; макроскопические циклы, такие как рок цикл; а также вызванные человеком циклы синтетических соединений, таких как полихлорированный бифенил (Печатная плата). В некоторых циклах есть резервуары, в которых вещество может храниться длительное время. Круговорот этих элементов взаимосвязан.
Морские организмы, и особенно морские микроорганизмы имеют решающее значение для функционирования многих из этих циклов. Силы, управляющие биогеохимическими циклами, включают: метаболические процессы внутри организмов геологические процессы с участием мантии Земли, а также химические реакции между самими веществами, поэтому их называют биогеохимическими циклами. Хотя химические вещества могут быть расщеплены и рекомбинированы, сами химические элементы не могут быть ни созданы, ни разрушены этими силами, поэтому, помимо некоторых потерь и прибылей из космоса, элементы рециркулируются или хранятся (секвестрируются) где-то на планете.
Обзор
Энергия направленно течет через экосистемы, поступая в виде солнечного света (или неорганических молекул для хемоавтотрофов) и покидая тепло во время многочисленных переходов между трофическими уровнями. Однако материя, из которой состоят живые организмы, сохраняется и перерабатывается. Шесть наиболее распространенных элементов, связанных с органическими молекулами - углерод, азот, водород, кислород, фосфор и сера - принимают различные химические формы и могут длительное время существовать в атмосфере, на суше, в воде или под поверхностью Земли. . Геологические процессы, такие как выветривание, эрозия, дренаж воды и субдукция континентальных плит, - все это играет роль в повторном использовании материалов. Поскольку геология и химия играют важную роль в изучении этого процесса, рециркуляция неорганического вещества между живыми организмами и окружающей их средой называется биогеохимическим циклом.[1]
Шесть вышеупомянутых элементов используются организмами по-разному. Водород и кислород содержатся в воде и органических молекулах, которые необходимы для жизни. Углерод содержится во всех органических молекулах, тогда как азот является важным компонентом нуклеиновых кислот и белков. Фосфор используется для производства нуклеиновых кислот и фосфолипидов, составляющих биологические мембраны. Сера имеет решающее значение для трехмерной формы белков. Круговорот этих элементов взаимосвязан. Например, движение воды имеет решающее значение для вымывания серы и фосфора в реки, которые затем могут течь в океаны. Минералы циркулируют в биосфере между биотическими и абиотическими компонентами и от одного организма к другому.[2]
Круговорот воды

Вода - это среда океанов, среда, в которой переносятся все вещества и элементы, участвующие в морских биогеохимических циклах. Вода в природе почти всегда содержит растворенные вещества, поэтому воду называют «универсальным растворителем» за ее способность растворять так много веществ.[3][4] Эта способность позволяет ему быть "растворитель жизни"[5] Вода также является единственным распространенным веществом, которое существует как твердый, жидкость и газ в нормальных земных условиях.[6] Поскольку жидкая вода течет, океанские воды циркулируют и текут по всему миру. Поскольку вода легко меняет фазу, ее можно унести в атмосферу в виде водяного пара или заморозить как айсберг. Затем он может выпадать в осадок или плавиться, чтобы снова стать жидкой водой. Вся морская жизнь погружена в воду, в матрицу и утробу самой жизни.[7] Вода может быть расщеплена на составляющие водород и кислород в результате метаболических или абиотических процессов, а затем рекомбинирована, чтобы снова стать водой.
Хотя круговорот воды сам по себе биогеохимический цикл, поток воды над и под Землей является ключевым компонентом круговорота других биогеохимических веществ.[8] Сток отвечает почти за весь перенос размытый осадок и фосфор с земли на водоемы.[9] Культурный эвтрофикация озер в первую очередь из-за фосфора, внесенного в избытке сельскохозяйственные поля в удобрения, а затем транспортировали по суше и по рекам. И сток, и поток грунтовых вод играют важную роль в переносе азота с суши в водоемы.[10] В мертвая зона на выходе из Река Миссисипи является следствием нитраты от удобрений, уносимых с сельскохозяйственных полей и стекающих по речная система к Мексиканский залив. Сток также играет роль в цикл углерода, опять же за счет переноса эродированных горных пород и почвы.[11]
Соленость океана

Вертикальные перепады солености моря между поверхностью и глубиной 300 метров. Соленость увеличивается с глубиной в красных областях и уменьшается в синих областях.[12]
Соленость океана происходит в результате эрозии и переноса растворенных солей с земли.

Среднегодовая соленость поверхности моря, измеренная в 2009 г. в единицы практической солености (БП).[13]
Морской спрей

Поток переносимых по воздуху микроорганизмов кружит над планетой над погодными системами, но ниже коммерческих воздушных путей.[14] Некоторые перипатетические микроорганизмы уносятся наземными пыльными бурями, но большинство происходят от морских микроорганизмов в морские брызги. В 2018 году ученые сообщили, что на каждом квадратном метре планеты ежедневно откладываются сотни миллионов вирусов и десятки миллионов бактерий.[15][16] Это еще один пример воды, облегчающей перенос органических материалов на большие расстояния, в данном случае в виде живых микроорганизмов.
Растворенная соль не испаряется обратно в атмосферу, как вода, но образует аэрозоли морской соли в морские брызги. Много физические процессы над поверхностью океана образуются аэрозоли морской соли. Одна из частых причин - взрыв пузырьки воздуха, увлекаемые ветровым напряжением во время белая шапка формирование. Другой - срывание капель с вершин волн.[17] Общий поток морской соли из океана в атмосферу составляет около 3300 тг (3,3 миллиарда тонн) в год.[18]
Циркуляция океана




Солнечная радиация влияет на океаны: теплая вода с экватора имеет тенденцию циркулировать к полюса, а холодные полярные воды устремляются к экватору. Поверхностные течения изначально определяются условиями приземного ветра. В пассаты дуть на запад в тропиках,[20] и западные ветры дуть на восток в средних широтах.[21] Этот образец ветра применяет стресс на поверхность субтропического океана с отрицательным завиток через Северное полушарие,[22] и наоборот через Южное полушарие. Результирующий Свердруп транспорт к экватору.[23] Из-за сохранения потенциальная завихренность вызванные направленными к полюсу ветрами на субтропический хребет На западной периферии и повышенной относительной завихренности движущейся к полюсу воды перенос уравновешивается узким ускоряющимся потоком, направленным к полюсу, который течет вдоль западной границы океанского бассейна, перевешивая эффекты трения с холодным западным пограничным течением, которое возникает высокие широты.[24] Общий процесс, известный как западная интенсификация, заставляет течения на западной границе океанического бассейна быть сильнее, чем на восточной границе.[25]
По мере продвижения к полюсу теплая вода, переносимая сильным потоком теплой воды, подвергается испарительному охлаждению. Охлаждение осуществляется ветром: ветер, движущийся над водой, охлаждает воду, а также вызывает испарение, оставив более соленый рассол. В этом процессе вода становится более соленой и плотной. и понижается температура. После образования морского льда соли остаются вне льда - процесс, известный как исключение рассола.[26] Эти два процесса производят более плотную и холодную воду. Вода через северный Атлантический океан становится настолько плотным, что начинает опускаться в менее соленую и менее плотную воду. Этот нисходящий поток тяжелой, холодной и плотной воды становится частью Глубокие воды Северной Атлантики, южный ручей.[27]
Ветры вызывают океанские течения в верхних 100 метрах поверхности океана. Однако океанские течения также текут на тысячи метров под поверхностью. Эти глубоководные течения вызваны разницей в плотности воды, которая контролируется температурой (термо) и соленостью (халин). Этот процесс известен как термохалинная циркуляция. В полярных регионах Земли вода в океане очень остывает, образуя морской лед. Как следствие, окружающая морская вода становится более соленой, потому что, когда образуется морской лед, соль остается. По мере того, как морская вода становится более соленой, ее плотность увеличивается, и она начинает тонуть. Поверхностная вода втягивается, чтобы заменить тонущую воду, которая, в свою очередь, становится достаточно холодной и соленой, чтобы тонуть. Это инициирует глубоководные течения, приводящие в движение глобальную конвейерную ленту.[28]
Термохалинная циркуляция приводит в движение глобальную систему течений, называемую «глобальной конвейерной лентой». Конвейерная лента начинается на поверхности океана у полюса в Северной Атлантике. Здесь вода охлаждается арктическими температурами. Он также становится более соленым, потому что при образовании морского льда соль не замерзает и остается в окружающей воде. Холодная вода теперь более плотная из-за добавленных солей и опускается на дно океана. Поверхностная вода перемещается, чтобы заменить тонущую воду, создавая течение. Эта глубокая вода движется на юг, между континентами, мимо экватора и спускается к концам Африки и Южной Америки. Течение проходит через край Антарктиды, где вода охлаждается и снова опускается, как это происходит в Северной Атлантике. Таким образом, конвейерная лента «перезаряжается». По мере того как он движется вокруг Антарктиды, от конвейера отделяются две секции, которые поворачивают на север. Одна секция уходит в Индийский океан, другая - в Тихий океан. Эти два разделившихся участка нагреваются и становятся менее плотными по мере продвижения на север к экватору, так что они поднимаются на поверхность (апвеллинг). Затем они возвращаются на юг и запад к Южной Атлантике, в конечном итоге возвращаясь в Северную Атлантику, где цикл начинается снова. Конвейерная лента движется с гораздо меньшей скоростью (несколько сантиметров в секунду), чем ветряные или приливные течения (от десятков до сотен сантиметров в секунду). Подсчитано, что любой кубический метр воды проходит около 1000 лет, чтобы пройти по мировой конвейерной ленте. Кроме того, конвейер перемещает огромный объем воды - более чем в 100 раз больше, чем поток реки Амазонки (Росс, 1995). Конвейерная лента также является жизненно важным компонентом глобального круговорота питательных веществ и двуокиси углерода в океане. Теплые поверхностные воды обеднены питательными веществами и углекислым газом, но они снова обогащаются по мере прохождения по конвейерной ленте в виде глубоких или придонных слоев. Основа мировой пищевой цепочки зависит от прохладной, богатой питательными веществами воды, которая поддерживает рост водорослей и водорослей.[29]
| Среднее время пребывания в резервуаре [30] | |
|---|---|
| Резервуар | Среднее время пребывания |
| Антарктида | 20000 лет |
| Океаны | 3200 лет |
| Ледники | От 20 до 100 лет |
| Сезонный снежный покров | От 2 до 6 месяцев |
| Влажность почвы | 1-2 месяца |
| Подземные воды: мелкие | От 100 до 200 лет |
| Подземные воды: глубокие | 10000 лет |
| Озера (см. время удерживания в озере ) | От 50 до 100 лет |
| Реки | От 2 до 6 месяцев |
| Атмосфера | 9 дней |
Среднее время пребывания молекулы воды в океане в мире составляет около 3200 лет. Для сравнения, среднее время пребывания в атмосфере составляет около 9 дней. Если он заморожен в Антарктике или затянут в глубокие грунтовые воды, он может быть изолирован на десять тысяч лет.[30][31]
Цикл ключевых элементов
| Некоторые ключевые элементы, участвующие в морских биогеохимических циклах | ||
|---|---|---|
Элемент | Диаграмма | Описание |
Углерод |  | В морской углеродный цикл включает процессы, которые обмениваются углерод между различными бассейнами в океане, а также между атмосферой, недрами Земли и морское дно. В цикл углерода является результатом многих взаимодействующих сил в различных временных и пространственных масштабах, которые циркулируют углерод по планете, обеспечивая доступность углерода во всем мире. Морской углеродный цикл занимает центральное место в глобальном углеродном цикле и включает в себя как неорганический углерод (углерод, не связанный с живыми существами, например углекислый газ) и органический углерод (углерод, который включен или был включен в живое существо). Часть морского углеродного цикла преобразует углерод между неживым и живым веществом. Три основных процесса (или насоса), составляющие морской углеродный цикл, вызывают атмосферный углекислый газ (CO2) в глубь океана и распространит его по океанам. Этими тремя насосами являются: (1) насос растворимости, (2) карбонатный насос и (3) биологический насос. Общий активный запас углерода на поверхности Земли в течение периода менее 10 000 лет составляет примерно 40 000 гигатонн C (Гт C, гигатонна составляет один миллиард тонн или вес приблизительно 6 миллионов тонн. Голубые киты ), и около 95% (~ 38 000 Гт C) хранится в океане, в основном в виде растворенного неорганического углерода.[32][33] Состав растворенного неорганического углерода в морском углеродном цикле является основным регулятором кислотно-щелочная химия в океанах. |
Кислород |  | В кислородный цикл включает биогеохимические переходы кислород атомы между разными степени окисления в ионы, оксиды, и молекулы через окислительно-восстановительные реакции внутри и между сферы / резервуары планеты Земля.[34] Слово кислород в литературе обычно относится к молекулярный кислород (O2), поскольку это обычный товар или же реагент многих биогеохимических окислительно-восстановительных реакций в цикле.[35] Процессы в кислородном цикле считаются биологический или же геологический и оцениваются как источник (O2 производство) или раковина (O2 потребление).[34][35] |
Водород |  | В водородный цикл состоит из водород обмены между биотический (живущий) и абиотический (неживые) источники и поглотители водородсодержащих соединений. Водород (H) - самый распространенный элемент во Вселенной.[36] На Земле обычные H-содержащие неорганические молекулы включают воду (H2O), газообразный водород (H2), метан (CH4), сероводород (ЧАС2Песок аммиак (NH3). Многие органические соединения также содержат атомы H, такие как углеводороды и органическая материя. Учитывая повсеместное распространение атомов водорода в неорганических и органических химических соединениях, водородный цикл сосредоточен на молекулярном водороде (H2). |
Азот |  | В азотный цикл это процесс, посредством которого азот преобразуется во множество химических форм, поскольку циркулирует среди атмосфера, земной, и морские экосистемы. Конверсия азота может осуществляться как биологическими, так и физическими способами. Важные процессы в круговороте азота включают: фиксация, аммонификация, нитрификация, и денитрификация. 78% земная атмосфера молекулярный азот (N2),[37] что делает его крупнейшим источником азота. Однако атмосферный азот имеет ограниченную доступность для биологического использования, что приводит к дефицит пригодного для использования азота во многих типах экосистемы. Азотный цикл представляет особый интерес для экологи поскольку доступность азота может повлиять на скорость основных экосистемных процессов, в том числе основное производство и разложение. Деятельность человека, такая как сжигание ископаемого топлива, использование искусственных азотных удобрений и выброс азота в сточные воды, резко возросла. изменил глобальный цикл азота.[38][39][40] Модификация человеком глобального азотного цикла может отрицательно сказаться на системе окружающей среды, а также на здоровье человека.[41][42] |
Фосфор |  | В цикл фосфора это движение фосфор сквозь литосфера, гидросфера, и биосфера. В отличие от многих других биогеохимических циклов, атмосфера не играет значительной роли в перемещении фосфора, потому что фосфор и соединения на основе фосфора обычно являются твердыми веществами в типичных диапазонах температуры и давления, существующих на Земле. Производство фосфин газ возникает только в специализированных, местных условиях. Следовательно, цикл фосфора следует рассматривать со всей системы Земли, а затем специально сосредоточить внимание на цикле в наземных и водных системах. На местном уровне трансформации фосфора носят химический, биологический и микробиологический характер: однако основные долгосрочные перемещения в глобальном цикле обусловлены тектонический движения в геологическое время.[43] Люди вызвали серьезные изменения в глобальном круговороте фосфора благодаря доставке фосфорных минералов и использованию фосфора. удобрение, а также доставка продуктов питания с ферм в города, где они теряются в виде сточных вод. |
Сера |  | В цикл серы это набор процессов, посредством которых сера перемещается между скалами, водными путями и живыми системами. Такие биогеохимические циклы важны в геология потому что они влияют на многие минералы. Биохимические циклы также важны для жизни, потому что сера - это существенный элемент, являясь составной частью многих белки и кофакторы, и соединения серы могут использоваться в качестве окислителей или восстановителей при микробном дыхании.[44] Глобальный сера Цикл включает в себя превращения разновидностей серы через различные состояния окисления, которые играют важную роль как в геологических, так и в биологических процессах. Основной поглотитель серы на Земле - это океаны.42−, где это главное окислитель.[45] |
Утюг |  | В железный цикл (Fe) - биогеохимический цикл утюг сквозь атмосфера, гидросфера, биосфера и литосфера. Хотя Fe очень распространено в земной коре,[46] реже встречается в насыщенных кислородом поверхностных водах. Железо является ключевым микронутриентом в первичная продуктивность,[47] и ограничивающее питательное вещество в Южном океане, восточной экваториальной части Тихого океана и субарктической части Тихого океана, называемое Регионы с высоким содержанием питательных веществ и низким содержанием хлорофилла (HNLC) океана.[48] Железо существует в диапазоне степени окисления от -2 до +7; однако на Земле он преимущественно находится в окислительно-восстановительном состоянии +2 или +3 и является первичным окислительно-активным металлом на Земле.[49] Цикл железа между его состояниями окисления +2 и +3 называется циклом железа. Этот процесс можно полностью абиотический или при содействии микроорганизмы, особенно железоокисляющие бактерии. К абиотическим процессам относятся: ржавчина железосодержащих металлов, где Fe2+ абиотически окисляется до Fe3+ в присутствии кислорода, а восстановление Fe3+ к Fe2+ железо-сульфидными минералами. Биологический цикл Fe2+ осуществляется окислением железа и восстановлением микробов.[50][51] |
Кальций |  | В кальциевый цикл это перенос кальция между растворенный и твердый фазы. Есть постоянная поставка ионы кальция в водные пути из горные породы, организмы, и почвы.[52][53] Ионы кальция потребляются и удаляются из водной среды, поскольку они реагируют с образованием нерастворимых структур, таких как карбонат кальция и силикат кальция,[52][54] которые могут откладываться с образованием отложений или экзоскелеты организмов.[55] Ионы кальция также можно использовать биологически, так как кальций необходим для биологических функций, таких как производство кости и зубы или клеточная функция.[56][57] Кальциевый цикл - это связующее звено между земными, морскими, геологическими и биологическими процессами.[58] На морской кальциевый цикл влияет изменение атмосферный углекислый газ из-за закисление океана.[55] |
Кремний |  | В цикл кремнезема включает транспортировку кремнезем между системами Земли. Опал кремнезем (SiO2), также называемый диоксид кремния, представляет собой химическое соединение кремний. Кремний является жизненно важным элементом и одним из самых распространенных элементов на Земле.[59][60] Цикл кремнезема значительно перекрывается с цикл углерода (см. карбонатно-силикатный цикл ) и играет важную роль в секвестрации углерода через континентальные выветривание, биогенный вывоз и захоронение как сочится в геологических масштабах времени.[61] |
Коробочные модели
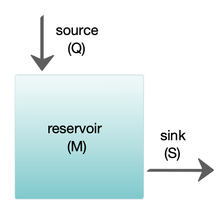
Коробчатые модели широко используются для моделирования биогеохимических систем.[63] Коробочные модели - это упрощенные версии сложных систем, сводящиеся к коробкам (или хранилищам). резервуары ) для химических материалов, связанных материалом потоки (потоки). Простые модели ящиков имеют небольшое количество ящиков со свойствами, такими как объем, которые не меняются со временем. Предполагается, что ящики ведут себя так, как если бы они были перемешаны однородно.[62] Эти модели часто используются для вывода аналитических формул, описывающих динамику и постоянную численность рассматриваемых химических веществ.
На схеме справа показана базовая модель с одним ящиком. Резервуар содержит количество материала M находится на рассмотрении в зависимости от химических, физических или биологических свойств. Источник Q приток материала в резервуар, а сток S поток материала из резервуара. Бюджет - это проверка и баланс источников и стоков, влияющих на материальный оборот в резервуаре. Резервуар находится в устойчивое состояние если Q = S, то есть, если источники уравновешивают стоки и нет никаких изменений со временем.[62]
— пластовые массы в петаграммах (Pg)
— потоки потока в петаграммах в год (Пг год−1)
На схемах в этой статье в основном используются эти устройства.
________________________________________________
один петаграмма = 1015 граммы = один гигатонна = один миллиард (109) тонны
В время оборота (также называемое временем обновления или возрастом выхода) - это среднее время, которое материал проводит в резервуаре. Если резервуар находится в устойчивом состоянии, это то же время, которое требуется для заполнения или слива резервуара. Таким образом, если τ - время оборота, то τ = M / S.[62] Уравнение, описывающее скорость изменения содержания в коллекторе:
Когда два или более резервуара соединены, материал можно рассматривать как циклическое движение между резервуарами, и могут быть предсказуемые модели циклического потока.[62] Более сложный модели multibox обычно решаются численными методами.


пример более сложной модели с множеством взаимодействующих блоков
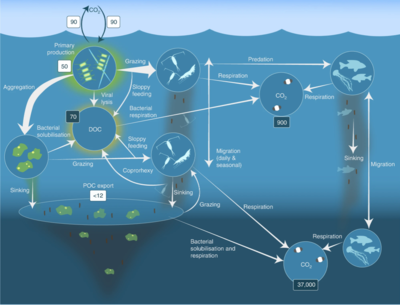
На диаграмме выше показан упрощенный бюджет океанических углеродных потоков. Он состоит из трех простых взаимосвязанных коробчатых моделей, одна для эвфотическая зона, один для интерьер океана или темный океан, и один для отложения океана. В эвфотической зоне нетто производство фитопланктона составляет около 50 Пг C каждый год. Около 10 мкг экспортируется в глубь океана, а остальные 40 мкг вдыхается. Разложение органического углерода происходит как частицы (морской снег ) расселяются по недрам океана. Только 2 Pg в конечном итоге достигают морского дна, в то время как остальные 8 Pg вдыхаются в темном океане. В отложениях временной масштаб, доступный для разложения, увеличивается на порядки, в результате чего 90% доставленного органического углерода разлагается и только 0,2 Пг C в год.−1 в конечном итоге погребается и переносится из биосферы в геосферу.[64]
Растворенные и твердые частицы


Биологические насосы
и углеродные массы (Gt C) в темных ящиках
В биологический насос в своей простейшей форме - это биологически обусловленное секвестрирование океаном углерод от атмосферы до недр океана и донных отложений.[73] Это часть океанический углеродный цикл отвечает за езду на велосипеде органическая материя сформированный в основном фитопланктон в течение фотосинтез (насос мягких тканей), а также циклическое карбонат кальция (CaCO3), образованные в оболочки некоторыми организмами, такими как планктон и моллюски (карбонатный насос).[74]
Биологический насос можно разделить на три отдельные фазы:[75] первая из которых - производство фиксированного углерода планктонными фототрофы в эвфотический (залитый солнцем) участок поверхности океана. В этих поверхностных водах фитопланктон использовать углекислый газ (CO2), азот (N), фосфор (P) и другие микроэлементы (барий, утюг, цинк и др.) во время фотосинтеза, чтобы углеводы, липиды, и белки. Некоторый планктон (например, кокколитофориды и фораминиферы ) объединяют кальций (Ca) и растворенные карбонаты (угольная кислота и бикарбонат ) с образованием карбоната кальция (CaCO3) защитное покрытие.

Как только этот углерод закрепляется в мягкой или твердой ткани, организмы либо остаются в эвфотической зоне, чтобы быть переработанными как часть регенеративного цикл питательных веществ или как только они умрут, переходят ко второй фазе биологического насоса и начинают опускаться на дно океана. Тонущие частицы часто образуют агрегаты по мере опускания, что значительно увеличивает скорость опускания. Именно эта агрегация дает частицам больше шансов избежать хищничества и разложения в толще воды и в конечном итоге добраться до морского дна.
Связанный уголь, который либо разлагается бактериями на пути вниз, либо однажды на морском дне, затем поступает в последнюю фазу насоса и реминерализуется для повторного использования в основное производство. Частицы, которые полностью ускользают от этих процессов, задерживаются в отложениях и могут оставаться там миллионы лет. Именно этот секвестрированный углерод в конечном итоге отвечает за снижение содержания CO в атмосфере.2.
| Внешнее видео | |
|---|---|
- Брам Дж. Р., Моррис Дж. Дж., Десима М. и Стукель М. Р. (2014) «Смертность в океанах: причины и последствия». Материалы симпозиума Eco-DAS IX, Глава 2, страницы 16–48. Ассоциация наук лимнологии и океанографии. ISBN 978-0-9845591-3-8.
- Матеус, доктор медицины (2017) «Преодоление разрыва между знанием и моделированием вирусов в морских системах - предстоящий рубеж». Границы морских наук, 3: 284. Дои:10.3389 / fmars.2016.00284
- Беккет, С.Дж. и Weitz, J.S. (2017) «Выявление нишевой конкуренции от пастбищной смертности в экспериментах по разбавлению фитопланктона». PLOS ONE, 12(5): e0177517. Дои:10.1371 / journal.pone.0177517.
Роль микроорганизмов
Циклы углерода, кислорода и водорода
В морской углеродный цикл состоит из процессов, которые обмениваются углерод между различными бассейнами в океане, а также между атмосферой, недрами Земли и морское дно. В цикл углерода является результатом многих взаимодействующих сил в различных временных и пространственных масштабах, которые циркулируют углерод по планете, обеспечивая доступность углерода во всем мире. Углеродный цикл океана является центральным процессом глобального углеродного цикла и включает оба неорганический углерод (углерод, не связанный с живыми существами, например углекислый газ) и органический углерод (углерод, который включен или был включен в живое существо). Часть морского углеродного цикла преобразует углерод между неживым и живым веществом.
Три основных процесса (или насоса), составляющие морской углеродный цикл, вызывают атмосферный углекислый газ (CO2) в глубь океана и распространит его по океанам. Этими тремя насосами являются: (1) насос растворимости, (2) насос для карбоната и (3) биологический насос. Общий активный запас углерода на поверхности Земли в течение периода менее 10 000 лет составляет примерно 40 000 гигатонн C (Гт C, гигатонна составляет один миллиард тонн или вес приблизительно 6 миллионов тонн. Голубые киты ), и около 95% (~ 38 000 Гт C) хранится в океане, в основном в виде растворенного неорганического углерода.[32][33] В видообразование растворенного неорганического углерода в морском углеродном цикле является основным регулятором кислотно-щелочная химия в океанах.
| Формы углерода [78] | |||
|---|---|---|---|
| Углеродная форма | Химическая формула | Состояние | Главный резервуар |
| углекислый газ | CO2 | газ | атмосфера |
| угольная кислота | ЧАС2CO3 | жидкость | океан |
| бикарбонат-ион | HCO3− | жидкость (растворенный ион ) | океан |
| органические соединения | Примеры: C6ЧАС12О6 (глюкоза) CH4 (метан) | твердый газ | морские организмы органические отложения (ископаемое топливо ) |
| другие углеродные соединения | Примеры: CaCO3 (карбонат кальция) CaMg (CO3)2 (карбонат кальция и магния) | твердый | снаряды осадочная порода |
Циклы азота и фосфора


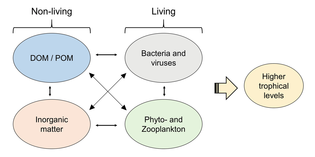
RDOC: устойчивый растворенный органический углерод
РОВ: растворенное органическое вещество
ПОМ: органический материал в виде частиц
Круговорот азота также является важным процессом в океане. Хотя общий цикл похож, есть разные игроки[79] и способы переноса азота в океане. Азот попадает в воду через осадки, сток или в виде азота.2 из атмосферы. Азот не может использоваться фитопланктон как N2 поэтому он должен подвергаться азотфиксации, которая осуществляется преимущественно цианобактерии.[80] Без поступления фиксированного азота в морской цикл фиксированный азот будет израсходован примерно за 2000 лет.[81] Фитопланктону необходим азот в биологически доступных формах для первоначального синтеза органического вещества. Аммиак и мочевина попадают в воду в результате выделения из планктона. Источники азота удалены из эвфотическая зона движением вниз органического вещества. Это может происходить в результате опускания фитопланктона, вертикального перемешивания или опускания отходов вертикальных мигрантов. The sinking results in ammonia being introduced at lower depths below the euphotic zone. Bacteria are able to convert ammonia to nitrite and nitrate but they are inhibited by light so this must occur below the euphotic zone.[80] Ammonification or Mineralization is performed by bacteria to convert organic nitrogen to ammonia. Нитрификация can then occur to convert the ammonium to nitrite and nitrate.[82] Nitrate can be returned to the euphotic zone by vertical mixing and upwelling where it can be taken up by phytoplankton to continue the cycle. N2 can be returned to the atmosphere through денитрификация.
Ammonium is thought to be the preferred source of fixed nitrogen for phytoplankton because its assimilation does not involve a редокс reaction and therefore requires little energy. Nitrate requires a redox reaction for assimilation but is more abundant so most phytoplankton have adapted to have the enzymes necessary to undertake this reduction (нитратредуктаза ). There are a few notable and well-known exceptions that include most Прохлорококк и немного Синехококк that can only take up nitrogen as ammonium.[81]
Phosphorus is an essential nutrient for plants and animals. Phosphorus is a ограничение питательных веществ for aquatic organisms. Phosphorus forms parts of important life-sustaining molecules that are very common in the biosphere. Phosphorus does enter the atmosphere in very small amounts when the dust is dissolved in rainwater and seaspray but remains mostly on land and in rock and soil minerals. Eighty percent of the mined phosphorus is used to make fertilizers. Phosphates from fertilizers, sewage and detergents can cause pollution in lakes and streams. Over-enrichment of phosphate in both fresh and inshore marine waters can lead to massive algae blooms which, when they die and decay leads to эвтрофикация of freshwaters only. Recent research suggests that the predominant pollutant responsible for algal blooms in saltwater estuaries and coastal marine habitats is nitrogen.[83]
Phosphorus occurs most abundantly in nature as part of the ортофосфат ion (PO4)3−, consisting of a P atom and 4 oxygen atoms. On land most phosphorus is found in rocks and minerals. Phosphorus-rich deposits have generally formed in the ocean or from guano, and over time, geologic processes bring ocean sediments to land. Выветривание of rocks and minerals release phosphorus in a soluble form where it is taken up by plants, and it is transformed into organic compounds. The plants may then be consumed by травоядные животные and the phosphorus is either incorporated into their tissues or excreted. After death, the animal or plant decays, and phosphorus is returned to the soil where a large part of the phosphorus is transformed into insoluble compounds. Сток may carry a small part of the phosphorus back to the океан.[84]
Nutrient cycle

А цикл питательных веществ is the movement and exchange of органический и неорганический matter back into the производство of matter. The process is regulated by the pathways available in marine food webs, which ultimately decompose organic matter back into inorganic nutrients. Nutrient cycles occur within ecosystems. Energy flow always follows a unidirectional and noncyclic path, whereas the movement of mineral nutrients is cyclic. Mineral cycles include the цикл углерода, кислородный цикл, nitrogen cycle, цикл фосфора и sulfur cycle among others that continually recycle along with other mineral nutrients into продуктивный ecological nutrition.
There is considerable overlap between the terms for the биогеохимический цикл and nutrient cycle. Some textbooks integrate the two and seem to treat them as synonymous terms.[86] However, the terms often appear independently. Nutrient cycle is more often used in direct reference to the idea of an intra-system cycle, where an ecosystem functions as a unit. From a practical point, it does not make sense to assess a terrestrial ecosystem by considering the full column of air above it as well as the great depths of Earth below it. While an ecosystem often has no clear boundary, as a working model it is practical to consider the functional community where the bulk of matter and energy transfer occurs.[87] Nutrient cycling occurs in ecosystems that participate in the "larger biogeochemical cycles of the earth through a system of inputs and outputs."[87]:425
Dissolved nutrients
Nutrients dissolved in seawater are essential for the survival of marine life. Nitrogen and phosphorus are particularly important. They are regarded as limiting nutrients in many marine environments, because primary producers, like algae and marine plants, cannot grow without them. They are critical for stimulating основное производство к фитопланктон. Other important nutrients are silicon, iron, and zinc.[88]
The process of cycling nutrients in the sea starts with biological pumping, when nutrients are extracted from surface waters by phytoplankton to become part of their organic makeup. Phytoplankton are either eaten by other organisms, or eventually die and drift down as морской снег. There they decay and return to the dissolved state, but at greater ocean depths. The fertility of the oceans depends on the abundance of the nutrients, and is measured by the основное производство, which is the rate of fixation of carbon per unit of water per unit time. "Primary production is often mapped by satellites using the distribution of chlorophyll, which is a pigment produced by plants that absorbs energy during photosynthesis. The distribution of chlorophyll is shown in the figure above. You can see the highest abundance close to the coastlines where nutrients from the land are fed in by rivers. The other location where chlorophyll levels are high is in upwelling zones where nutrients are brought to the surface ocean from depth by the upwelling process..."[88]

Океан цикл питательных веществ

Ocean nutrient flux
"Another critical element for the health of the oceans is the dissolved oxygen content. Oxygen in the surface ocean is continuously added across the air-sea interface as well as by photosynthesis; it is used up in respiration by marine organisms and during the decay or oxidation of organic material that rains down in the ocean and is deposited on the ocean bottom. Most organisms require oxygen, thus its depletion has adverse effects for marine populations. Temperature also affects oxygen levels as warm waters can hold less dissolved oxygen than cold waters. This relationship will have major implications for future oceans, as we will see... The final seawater property we will consider is the content of dissolved CO2. CO2 is nearly opposite to oxygen in many chemical and biological processes; it is used up by plankton during photosynthesis and replenished during respiration as well as during the oxidation of organic matter. As we will see later, CO2 content has importance for the study of deep-water aging."[88]


Marine sulfur cycle

Sulfate reduction in the seabed is strongly focused toward near-surface sediments with high depositional rates along the ocean margins. The benthic marine sulfur cycle is therefore sensitive to anthropogenic influence, such as ocean warming and increased nutrient loading of coastal seas. This stimulates photosynthetic productivity and results in enhanced export of organic matter to the seafloor, often combined with low oxygen concentration in the bottom water (Rabalais et al., 2014; Breitburg et al., 2018). The biogeochemical zonation is thereby compressed toward the sediment surface, and the balance of organic matter mineralization is shifted from oxic and suboxic processes toward sulfate reduction and methanogenesis (Middelburg and Levin, 2009).[89]

The sulfur cycle in marine environments has been well-studied via the tool of sulfur isotope systematics expressed as δ34S. The modern global oceans have sulfur storage of 1.3 × 1021 g,[90] mainly occurring as sulfate with the δ34S value of +21‰.[91] The overall input flux is 1.0 × 1014 g/year with the sulfur isotope composition of ~3‰.[91] Riverine sulfate derived from the terrestrial weathering of sulfide minerals (δ34S = +6‰) is the primary input of sulfur to the oceans. Other sources are metamorphic and volcanic degassing and hydrothermal activity (δ34S = 0‰), which release reduced sulfur species (e.g., H2S and S0). There are two major outputs of sulfur from the oceans. The first sink is the burial of sulfate either as marine evaporites (e.g., gypsum) or carbonate-associated sulfate (CAS), which accounts for 6 × 1013 g/year (δ34S = +21‰). The second sulfur sink is pyrite burial in shelf sediments or deep seafloor sediments (4 × 1013 g/year; δ34S = -20‰).[92] The total marine sulfur output flux is 1.0 × 1014 g/year which matches the input fluxes, implying the modern marine sulfur budget is at steady state.[91] The residence time of sulfur in modern global oceans is 13,000,000 years.[93]
In modern oceans, Hydrogenovibrio crunogenus, Halothiobacillus, и Beggiatoa are primary sulfur oxidizing bacteria,[94][95] and form chemosynthetic symbioses with animal hosts.[96] The host provides metabolic substrates (e.g., CO2, O2, H2O) to the symbiont while the symbiont generates organic carbon for sustaining the metabolic activities of the host. The produced sulfate usually combines with the leached calcium ions to form гипс, which can form widespread deposits on near mid-ocean spreading centers.[97]
Гидротермальные источники emit hydrogen sulfide that support the carbon fixation of chemolithotrophic bacteria that oxidize hydrogen sulfide with oxygen to produce elemental sulfur or sulfate.[94]
Iron cycle and dust


В железный цикл (Fe) is the biogeochemical cycle of утюг сквозь атмосфера, гидросфера, биосфера и литосфера. While Fe is highly abundant in the Earth's crust,[102] it is less common in oxygenated surface waters. Iron is a key micronutrient in первичная продуктивность,[47] и ограничение питательных веществ in the Southern ocean, eastern equatorial Pacific, and the subarctic Pacific referred to as High-Nutrient, Low-Chlorophyll (HNLC) regions океана.[48]
Iron in the ocean cycles between plankton, aggregated particulates (non-bioavailable iron), and dissolved (bioavailable iron), and becomes sediments through burial.[98][103][104] Гидротермальные источники release ferrous iron to the ocean[105] in addition to oceanic iron inputs from land sources. Iron reaches the atmosphere through volcanism,[106] эолийский wind,[107] and some via combustion by humans. в Антропоцен, iron is removed from mines in the crust and a portion re-deposited in waste repositories.[101][104]
Iron is an essential micronutrient for almost every life form. It is a key component of hemoglobin, important to nitrogen fixation as part of the Нитрогеназа enzyme family, and as part of the iron-sulfur core of ферредоксин it facilitates electron transport in chloroplasts, eukaryotic mitochondria, and bacteria. Due to the high reactivity of Fe2+ with oxygen and low solubility of Fe3+, iron is a limiting nutrient in most regions of the world.

Calcium and silica cycles


В calcium cycle is a transfer of calcium between растворенный и твердый фазы. There is a continuous supply of ионы кальция into waterways from горные породы, организмы, и почвы.[109][110] Calcium ions are consumed and removed from aqueous environments as they react to form insoluble structures such as карбонат кальция and calcium silicate,[109][111] which can deposit to form sediments or the экзоскелеты организмов.[55]Raisman, Scott; Murphy, Daniel T. (2013). Ocean acidification: Elements and Considerations. Hauppauge, New York: Nova Science Publishers, Inc. ISBN 9781629482958. Calcium ions can also be utilized биологически, as calcium is essential to biological functions such as the production of кости и зубы or cellular function.[56][112] The calcium cycle is a common thread between terrestrial, marine, geological, and biological processes.[113] Calcium moves through these different media as it cycles throughout the Earth. The marine calcium cycle is affected by changing atmospheric carbon dioxide из-за закисление океана.[55]
Biogenic calcium carbonate is formed when marine organisms, such as кокколитофориды, кораллы, pteropods, и другие моллюски transform calcium ions and бикарбонат into shells and экзоскелеты из кальцит или же арагонит, both forms of calcium carbonate.[55] This is the dominant sink for dissolved calcium in the ocean.[113] Dead organisms sink to the bottom of the ocean, depositing layers of shell which over time cement to form известняк. This is the origin of both marine and terrestrial limestone.[55]
| Часть серии о |
| Цикл углерода |
|---|
 |
With its close relation to the цикл углерода and the effects of greenhouse gasses, both calcium and carbon cycles are predicted to change in the coming years.[114] Tracking calcium isotopes enables the prediction of environmental changes, with many sources suggesting increasing temperatures in both the atmosphere and marine environment. As a result, this will drastically alter the breakdown of rock, the pH of oceans and waterways and thus calcium sedimentation, hosting an array of implications on the calcium cycle.
Due to the complex interactions of calcium with many facets of life, the effects of altered environmental conditions are unlikely to be known until they occur. Predictions can however be tentatively made, based upon evidence-based research. Increasing carbon dioxide levels and decreasing ocean pH will alter calcium solubility, preventing corals and shelled organisms from developing their calcium-based exoskeletons, thus making them vulnerable or unable to survive.[115][116]
Most biological production of биогенный кремнезем in the ocean is driven by диатомеи. These extract dissolved кремниевая кислота in surface waters during growth, with this returned by recycling throughout the столб воды after they die. Inputs of silicon to the ocean from above arrive via rivers and aeolian dust, while those from below include seafloor sediment recycling, weathering, and гидротермальная деятельность.[117]
Биоминерализация
"Biological activity is a dominant force shaping the chemical structure and evolution of the earth surface environment. The presence of an oxygenated atmosphere-hydrosphere surrounding an otherwise highly reducing solid earth is the most striking consequence of the rise of life on earth. Biological evolution and the functioning of ecosystems, in turn, are to a large degree conditioned by geophysical and geological processes. Understanding the interactions between organisms and their abiotic environment, and the resulting coupled evolution of the biosphere and geosphere is a central theme of research in biogeology. Biogeochemists contribute to this understanding by studying the transformations and transport of chemical substrates and products of biological activity in the environment."[118]
"Since the Cambrian explosion, mineralized body parts have been secreted in large quantities by biota. Because calcium carbonate, silica and calcium phosphate are the main mineral phases constituting these hard parts, biomineralization plays an important role in the global biogeochemical cycles of carbon, calcium, silicon and phosphorus"[118]
Deep cycling
Deep cycling involves the exchange of materials with the мантия.

В deep water cycle involves exchange of water with the mantle, with water carried down by подчинение oceanic plates and returning through volcanic activity, distinct from the круговорот воды process that occurs above and on the surface of Earth. Some of the water makes it all the way to the нижняя мантия and may even reach the внешнее ядро. In the conventional view of the water cycle (also known as the гидрологический цикл), water moves between reservoirs in the атмосфера and Earth's surface or near-surface (including the океан, реки и озера, ледники и полярные ледяные шапки, то биосфера и грунтовые воды ). However, in addition to the surface cycle, water also plays an important role in geological processes reaching down into the корка и мантия. Water content in магма determines how explosive a volcanic eruption is; hot water is the main conduit for economically important minerals to concentrate in hydrothermal mineral deposits; and water plays an important role in the formation and migration of нефть.[120] Petroleum is a ископаемое топливо derived from ancient окаменелый органические материалы, Такие как зоопланктон и водоросли.[121][122]
Water is not just present as a separate phase in the ground. Seawater percolates into oceanic crust and hydrates igneous rocks such as оливин и пироксен, transforming them into hydrous minerals such as serpentines, тальк и брусит.[123] In this form, water is carried down into the mantle. в верхняя мантия, heat and pressure dehydrates these minerals, releasing much of it to the overlying мантийный клин, triggering the melting of rock that rises to form вулканические дуги.[124] However, some of the "nominally anhydrous minerals" that are stable deeper in the mantle can store small concentrations of water in the form of гидроксил (ОЙ−),[125] and because they occupy large volumes of the Earth, they are capable of storing at least as much as the world's oceans.[120]
The conventional view of the ocean's origin is that it was filled by outgassing from the mantle in the early Архейский and the mantle has remained dehydrated ever since.[126] However, subduction carries water down at a rate that would empty the ocean in 1–2 billion years. Despite this, changes in the global sea level over the past 3–4 billion years have only been a few hundred metres, much smaller than the average ocean depth of 4 kilometres. Thus, the fluxes of water into and out of the mantle are expected to be roughly balanced, and the water content of the mantle steady. Water carried into the mantle eventually returns to the surface in eruptions at mid-ocean ridges и горячие точки.[127] :646 Estimates of the amount of water in the mantle range from 1⁄4 to 4 times the water in the ocean.[127]:630–634
В deep carbon cycle is the movement of углерод through the Earth's мантия и основной.It forms part of the цикл углерода and is intimately connected to the movement of carbon in the Earth's surface and atmosphere. By returning carbon to the deep Earth, it plays a critical role in maintaining the terrestrial conditions necessary for life to exist. Without it, carbon would accumulate in the atmosphere, reaching extremely high concentrations over long periods of time.[128]
Рок-цикл

Ископаемое топливо
Водный фитопланктон и зоопланктон that died and sedimented in large quantities under аноксические условия millions of years ago began forming petroleum and natural gas as a result of анаэробное разложение (by contrast, terrestrial plants tended to form каменный уголь and methane). Над геологическое время это органический иметь значение, смешанный с грязь, became buried under further heavy layers of inorganic sediment. The resulting high температура и давление caused the organic matter to chemically alter, first into a waxy material known as кероген, который находится в горючие сланцы, and then with more heat into liquid and gaseous hydrocarbons in a process known as катагенез. Despite these heat driven transformations (which increase the energy density compared to typical organic matter by removal of oxygen atoms),[129]Such organisms and their resulting fossil fuels typically have an age of millions of years, and sometimes more than 650 million years,[130] the energy released in combustion is still photosynthetic in origin.[131]
Other cycles
Such as trace minerals, micronutrients, human-induced cycles for synthetic compounds such as полихлорированный бифенил (Печатная плата).
Рекомендации
- ^ а б Biogeochemical Cycles, OpenStax, 9 May 2019.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Fisher M. R. (Ed.) (2019) Экологическая биология, 3.2 Biogeochemical Cycles, OpenStax.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. п. 620. ISBN 978-0-08-037941-8.
- ^ «Вода - универсальный растворитель». USGS. В архиве из оригинала 9 июля 2017 г.. Получено 27 июн 2017.
- ^ Reece, Jane B. (31 October 2013). Campbell Biology (10-е изд.). Пирсон. п. 48. ISBN 9780321775658.
- ^ Reece, Jane B. (31 October 2013). Campbell Biology (10-е изд.). Пирсон. п. 44. ISBN 9780321775658.
- ^ Collins J. C. (1991) The Matrix of Life: A View of Natural Molecules from the Perspective of Environmental Water Molecular Presentations. ISBN 9780962971907.
- ^ "Biogeochemical Cycles". The Environmental Literacy Council. В архиве из оригинала от 30.04.2015. Получено 2006-10-24.
- ^ "Phosphorus Cycle". The Environmental Literacy Council. В архиве из оригинала на 20.08.2016. Получено 2018-01-15.
- ^ "Nitrogen and the Hydrologic Cycle". Extension Fact Sheet. Государственный университет Огайо. Архивировано из оригинал на 2006-09-01. Получено 2006-10-24.
- ^ "The Carbon Cycle". Обсерватория Земли. НАСА. 2011-06-16. Архивировано из оригинал on 2006-09-28. Получено 2006-10-24.
- ^ Sundby, S. and Kristiansen, T. (2015) "The principles of buoyancy in marine fish eggs and their vertical distributions across the world oceans". PLOS ONE, 10(10): e0138821. Дои:10.1371/journal.pone.0138821.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ World Ocean Atlas 2009
- ^ Живые бактерии перемещаются в воздушных потоках Земли Смитсоновский журнал, 11 января 2016 г.
- ^ Роббинс, Джим (13 апреля 2018 г.). "Trillions Upon Trillions of Viruses Fall From the Sky Each Day". Нью-Йорк Таймс. Получено 14 апреля 2018.
- ^ Рече, Изабель; Д’Орта, Гаэтано; Младенов, Натали; Winget, Danielle M; Саттл, Кертис А. (29 января 2018 г.). «Скорость осаждения вирусов и бактерий над пограничным слоем атмосферы». Журнал ISME. 12 (4): 1154–1162. Дои:10.1038 / с41396-017-0042-4. ЧВК 5864199. PMID 29379178.
- ^ Levin, Zev; Cotton, William R., eds. (2009). Aerosol Pollution Impact on Precipitation. Дои:10.1007/978-1-4020-8690-8. ISBN 978-1-4020-8689-2.
- ^ IPCC Third Assessment Report: Climate Change 2001 (TAR)
- ^ Wind Driven Surface Currents: Upwelling and Downwelling НАСА. Accessed 17 June 2020.
- ^ "trade winds". Глоссарий по метеорологии. Американское метеорологическое общество. 2009. Архивировано с оригинал на 2008-12-11. Получено 2008-09-08.
- ^ Glossary of Meteorology (2009). Westerlies. В архиве 2010-06-22 at the Wayback Machine Американское метеорологическое общество. Retrieved on 2009-04-15.
- ^ Matthias Tomczak and J. Stuart Godfrey (2001). Regional Oceanography: an Introduction. В архиве 2009-09-14 на Wayback Machine Matthias Tomczak, pp. 42. ISBN 81-7035-306-8. Retrieved on 2009-05-06.
- ^ Earthguide (2007). Lesson 6: Unraveling the Gulf Stream Puzzle - On a Warm Current Running North. В архиве 2008-07-23 на Wayback Machine Калифорнийский университет в Сан-Диего. Retrieved on 2009-05-06.
- ^ Angela Colling (2001). Ocean circulation. В архиве 2018-03-02 at the Wayback Machine Butterworth-Heinemann, pp. 96. Retrieved on 2009-05-07.
- ^ National Environmental Satellite, Data, and Information Service (2009). Investigating the Gulf Stream. В архиве 2010-05-03 на Wayback Machine Университет штата Северная Каролина. Retrieved on 2009-05-06.
- ^ Russel, Randy. "Thermohaline Ocean Circulation". University Corporation for Atmospheric Research. Архивировано из оригинал на 2009-03-25. Получено 2009-01-06.
- ^ Behl, R. "Atlantic Ocean water masses". Калифорнийский государственный университет Длинный пляж. Архивировано из оригинал on May 23, 2008. Получено 2009-01-06.
- ^ Thermohaline Circulation National Ocean Service, NOAA. Retrieved: 20 May 2020.
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ The Global Conveyor Belt National Ocean Service, NOAA. Retrieved: 20 May 2020.
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ а б "Chapter 8: Introduction to the Hydrosphere". 8(b) the Hydrologic Cycle. PhysicalGeography.net. В архиве from the original on 2016-01-26. Получено 2006-10-24.
- ^ Van Der Ent, R.J. and Tuinenburg, O.A. (2017) "The residence time of water in the atmosphere revisited". Гидрология и науки о Земле, 21(2): 779–790. Дои:10.5194/hess-21-779-2017.
- ^ а б H., Schlesinger, William (2013). Biogeochemistry : an analysis of global change. Bernhardt, Emily S. (3rd ed.). Waltham, Mass.: Academic Press. ISBN 9780123858740. OCLC 827935936.
- ^ а б Falkowski, P .; Scholes, R. J.; Boyle, E.; Canadell, J.; Canfield, D.; Elser, J .; Gruber, N.; Hibbard, K.; Högberg, P. (2000-10-13). "The Global Carbon Cycle: A Test of Our Knowledge of Earth as a System". Наука. 290 (5490): 291–296. Bibcode:2000Sci...290..291F. Дои:10.1126/science.290.5490.291. ISSN 0036-8075. PMID 11030643.
- ^ а б Knoll AH, Canfield DE, Konhauser K (2012). «7». Fundamentals of geobiology. Chichester, West Sussex: John Wiley & Sons . pp. 93–104. ISBN 978-1-118-28087-4. OCLC 793103985.
- ^ а б Petsch ST (2014). "The Global Oxygen Cycle". Трактат по геохимии. Эльзевир. pp. 437–473. Дои:10.1016/b978-0-08-095975-7.00811-1. ISBN 978-0-08-098300-4.
- ^ Cameron AG (1973). "Abundances of the elements in the solar system". Обзоры космической науки. 15 (1): 121. Bibcode:1973ССРв ... 15..121С. Дои:10.1007 / BF00172440. ISSN 0038-6308.
- ^ Steven B. Carroll; Steven D. Salt (2004). Ecology for gardeners. Timber Press. п. 93. ISBN 978-0-88192-611-8. В архиве из оригинала на 2018-02-01. Получено 2016-10-23.
- ^ Кайперс, МММ; Маршан, Гонконг; Картал, Б (2011). "The Microbial Nitrogen-Cycling Network". Обзоры природы Микробиология. 1 (1): 1–14. Дои:10.1038 / nrmicro.2018.9. PMID 29398704.
- ^ Galloway, J. N.; и другие. (2004). "Nitrogen cycles: past, present, and future generations". Биогеохимия. 70 (2): 153–226. Дои:10.1007/s10533-004-0370-0.
- ^ Reis, Stefan; Bekunda, Mateete; Howard, Clare M; Karanja, Nancy; Winiwarter, Wilfried; Yan, Xiaoyuan; Bleeker, Albert; Sutton, Mark A (2016-12-01). "Synthesis and review: Tackling the nitrogen management challenge: from global to local scales". Письма об экологических исследованиях. 11 (12): 120205. Bibcode:2016ERL....11l0205R. Дои:10.1088/1748-9326/11/12/120205. ISSN 1748-9326.
- ^ Gu, Baojing; Ge, Ying; Ren, Yuan; Xu, Bin; Luo, Weidong; Цзян, Хун; Gu, Binhe; Chang, Jie (2012-08-17). "Atmospheric Reactive Nitrogen in China: Sources, Recent Trends, and Damage Costs". Экологические науки и технологии. 46 (17): 9420–9427. Bibcode:2012EnST...46.9420G. Дои:10.1021/es301446g. ISSN 0013-936X. PMID 22852755.
- ^ Kim, Haryun; Lee, Kitack; Lim, Dhong-Il; Nam, Seung-Il; Kim, Tae-Wook; Yang, Jin-Yu T.; Ko, Young Ho; Shin, Kyung-Hoon; Lee, Eunil (2017-05-11). "Widespread Anthropogenic Nitrogen in Northwestern Pacific Ocean Sediment". Экологические науки и технологии. 51 (11): 6044–6052. Bibcode:2017EnST...51.6044K. Дои:10.1021/acs.est.6b05316. ISSN 0013-936X. PMID 28462990.
- ^ Schlesinger WH (1991). Biogeochemistry: An analysis of global change.
- ^ Madigan MT, Martino JM (2006). Биология микроорганизмов Брока (11-е изд.). Пирсон. п. 136. ISBN 978-0-13-196893-6.
- ^ Bickle MJ, Alt JC, Teagle DA (1994). "Sulfur transport and sulphur isotope fractionations in ocean floor hydrothermal systems". Минералогический журнал. 58A (1): 88–89. Bibcode:1994MinM...58...88B. Дои:10.1180/minmag.1994.58A.1.49.
- ^ Taylor SR (1964). "Abundance of chemical elements in the continental crust: a new table". Geochimica et Cosmochimica Acta. 28 (8): 1273–1285. Bibcode:1964GeCoA..28.1273T. Дои:10.1016/0016-7037(64)90129-2.
- ^ а б Tagliabue A, Bowie AR, Boyd PW, Buck KN, Johnson KS, Saito MA (March 2017). "The integral role of iron in ocean biogeochemistry" (PDF). Природа. 543 (7643): 51–59. Bibcode:2017Natur.543...51T. Дои:10.1038/nature21058. PMID 28252066.
- ^ а б Martin JH, Fitzwater SE (1988). "Iron deficiency limits phytoplankton growth in the north-east Pacific subarctic". Природа. 331 (6154): 341–343. Bibcode:1988Natur.331..341M. Дои:10.1038/331341a0.
- ^ Melton ED, Swanner ED, Behrens S, Schmidt C, Kappler A (December 2014). "The interplay of microbially mediated and abiotic reactions in the biogeochemical Fe cycle". Обзоры природы. Микробиология. 12 (12): 797–808. Дои:10.1038/nrmicro3347. PMID 25329406.
- ^ Schmidt C, Behrens S, Kappler A (2010). "Ecosystem functioning from a geomicrobiological perspective – a conceptual framework for biogeochemical iron cycling". Экологическая химия. 7 (5): 399. Дои:10.1071/EN10040.
- ^ Капплер, Андреас; Straub, Kristina L. (2005-01-01). "Geomicrobiological Cycling of Iron". Обзоры по минералогии и геохимии. 59 (1): 85–108. Дои:10.2138/rmg.2005.59.5. ISSN 1529-6466.
- ^ а б Уокер, Джеймс С. Дж .; Hays, P. B .; Kasting, J. F. (1981). «Механизм отрицательной обратной связи для долговременной стабилизации температуры поверхности Земли». Журнал геофизических исследований. 86 (C10): 9776. Bibcode:1981JGR .... 86.9776W. Дои:10.1029/jc086ic10p09776. ISSN 0148-0227.
- ^ Berner, R. A. (2004-05-01). "A model for calcium, magnesium and sulfate in seawater over Phanerozoic time". Американский журнал науки. 304 (5): 438–453. Bibcode:2004AmJS..304..438B. Дои:10.2475/ajs.304.5.438. ISSN 0002-9599.
- ^ Риджвелл, Энди; Zeebe, Richard E. (2005-06-15). "The role of the global carbonate cycle in the regulation and evolution of the Earth system". Письма по науке о Земле и планетах. 234 (3–4): 299–315. Дои:10.1016/j.epsl.2005.03.006. ISSN 0012-821X.
- ^ а б c d е ж Raisman, Scott; Murphy, Daniel T. (2013). Ocean acidification: Elements and Considerations. Hauppauge, New York: Nova Science Publishers, Inc. ISBN 9781629482958.
- ^ а б Nordin, B. E. C (1988). Calcium in Human Biology. ILSI Human Nutrition Reviews. Лондон: Springer London. Дои:10.1007/978-1-4471-1437-6. ISBN 9781447114376. OCLC 853268074.
- ^ Rubin, Ronald P.; Weiss, George B.; Putney, James W. Jr (2013-11-11). Calcium in Biological Systems. Springer Science & Business Media. ISBN 9781461323778.
- ^ Fantle, Matthew S.; Tipper, Edward T. (2014). "Calcium isotopes in the global biogeochemical Ca cycle: Implications for development of a Ca isotope proxy". Обзоры наук о Земле. 131: 148–177. Дои:10.1016/j.earscirev.2014.02.002. ISSN 0012-8252 – via Elsevier ScienceDirect.
- ^ Hunt, J. W.; Dean, A. P.; Webster, R. E.; Johnson, G. N.; Ennos, A. R. (2008). "A Novel Mechanism by which Silica Defends Grasses Against Herbivory". Анналы ботаники. 102 (4): 653–656. Дои:10.1093/aob/mcn130. ISSN 1095-8290. ЧВК 2701777. PMID 18697757.
- ^ Conley, Daniel J. (December 2002). "Terrestrial ecosystems and the global biogeochemical silica cycle". Глобальные биогеохимические циклы. 16 (4): 68–1–68–8. Bibcode:2002GBioC..16.1121C. Дои:10.1029/2002gb001894. ISSN 0886-6236.
- ^ Defant, Marc J.; Drummond, Mark S. (October 1990). "Derivation of some modern arc magmas by melting of young subducted lithosphere". Природа. 347 (6294): 662–665. Bibcode:1990Natur.347..662D. Дои:10.1038/347662a0. ISSN 0028-0836.
- ^ а б c d е Bianchi, Thomas (2007) Biogeochemistry of Estuaries page 9, Oxford University Press. ISBN 9780195160826.
- ^ Sarmiento, J.L.; Toggweiler, J.R. (1984). "A new model for the role of the oceans in determining atmospheric P CO 2". Природа. 308 (5960): 621–24. Bibcode:1984Natur.308..621S. Дои:10.1038/308621a0.
- ^ а б Middelburg, J.J.(2019) Marine carbon biogeochemistry: a primer for earth system scientists, page 5, Springer Nature. ISBN 9783030108229. Дои:10.1007/978-3-030-10822-9.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Sarmiento, Jorge L.; Gruber, Nicolas (2002). "Sinks for Anthropogenic Carbon". Физика сегодня. 55 (8): 30–36. Bibcode:2002PhT....55h..30S. Дои:10.1063/1.1510279.
- ^ Chhabra, Abha (2013). "Carbon and Other Biogeochemical Cycles". Дои:10.13140/2.1.1081.8883. Цитировать журнал требует
| журнал =(помощь) - ^ Kandasamy, Selvaraj; Nagender Nath, Bejugam (2016). "Perspectives on the Terrestrial Organic Matter Transport and Burial along the Land-Deep Sea Continuum: Caveats in Our Understanding of Biogeochemical Processes and Future Needs". Границы морских наук. 3. Дои:10.3389 / fmars.2016.00259. S2CID 30408500.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Ханселл Д.А. и Крейг А.С. (2015) «Морские растворенные органические вещества и углеродный цикл». Океанография, 14(4): 41–49. Дои:10.5670 / oceanog.2001.05.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Пагано Т., Бида М. и Кенни Дж. Э. (2014) «Тенденции уровней аллохтонного растворенного органического углерода в природной воде: обзор потенциальных механизмов в условиях меняющегося климата». Вода, 6(10): 2862–2897. Дои:10.3390 / w6102862.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Монрой, П., Эрнандес-Гарсия, Э., Росси, В. и Лопес, К. (2017) "Моделирование динамического опускания биогенных частиц в океанический поток". Нелинейные процессы в геофизике, 24(2): 293–305. Дои:10.5194 / npg-24-293-2017.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 3.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 3.0. - ^ Саймон, М., Гроссарт, Х., Швейцер, Б. и Плуг, Х. (2002) "Микробная экология органических агрегатов в водных экосистемах". Водная микробная экология, 28: 175–211. Дои:10.3354 / ame028175.
- ^ Каван, Э.Л., Белчер, А., Аткинсон, А., Хилл, С.Л., Кавагути, С., МакКормак, С., Мейер, Б., Никол, С., Ратнараджа, Л., Шмидт, К. и Стейнберг, DK (2019) «Значение антарктического криля в биогеохимических циклах». Связь с природой, 10(1): 1–13. Дои:10.1038 / s41467-019-12668-7.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Sigman DM & GH Haug. 2006. Биологический насос в прошлом. В кн .: Трактат по геохимии; т. 6, (ред.). Pergamon Press, стр. 491-528.
- ^ Hain, M.P .; Sigman, D.M .; Хауг, Г. (2014). Биологический насос в прошлом (PDF). Трактат по геохимии, 2-е издание. 8. С. 485–517. Дои:10.1016 / B978-0-08-095975-7.00618-5. ISBN 9780080983004. Получено 2015-06-01.
- ^ De La Rocha CL. 2006. Биологический насос. В кн .: Трактат по геохимии; т. 6, (ред.). Pergamon Press, стр. 83-111
- ^ Heinrichs, M.E., Mori, C. и Dlugosch, L. (2020) «Сложные взаимодействия между водными организмами и их химической средой, выясненные с разных точек зрения». В: YOUMARES 9-Океаны: наши исследования, наше будущее , страницы 279–297. Springer. Дои:10.1007/978-3-030-20389-4_15.
- ^ Прентис, И. (2001). «Круговорот углерода и углекислый газ в атмосфере». Изменение климата 2001: научная основа: вклад Рабочей группы I в Третий оценочный доклад Межправительственной группы экспертов по изменению климата / Houghton, J.T. [редактировать.] Получено 31 мая 2012.
- ^ Биогеохимические циклы CK-12 Биология. Дата обращения: 2 июня 2020 г.
- ^ Moulton, Orissa M; Altabet, Mark A; Беман, Дж. Майкл; Диган, Линда А; Льорет, Хавьер; Lyons, Meaghan K; Нельсон, Джеймс А; Пфистер, Кэтрин А (май 2016 г.). «Микробные ассоциации с макробиотой в прибрежных экосистемах: закономерности и последствия для круговорота азота». Границы экологии и окружающей среды. 14 (4): 200–208. Дои:10.1002 / плата.1262. HDL:1912/8083. ISSN 1540-9295.
- ^ а б Миллер, Чарльз (2008). Биологическая океанография. 350 Main Street, Malden, MA 02148 США: Blackwell Publishing Ltd., стр. 60–62. ISBN 978-0-632-05536-4.CS1 maint: location (связь)
- ^ а б Грубер, Николас (2008). Азот в морской среде. Корпоративный Драйв 30, Люкс 400, Берлингтон, Массачусетс 01803: Эльзевир. С. 1–35. ISBN 978-0-12-372522-6.CS1 maint: location (связь)
- ^ Бойс, Эллиот, Сьюзен, Майкл. «Учебный модуль: морская среда с азотным циклом». Архивировано из оригинал 15 апреля 2012 г.. Получено 22 октября 2011.
- ^ «Эвтрофикация - Американское почвенное общество». www.soils.org. Архивировано из оригинал на 2014-04-16. Получено 2014-04-14.
- ^ Пельцер Д.А., Уордл Д.А., Эллисон В.Дж., Байсден В.Т., Барджетт Р.Д., Чедвик О.А. и др. (Ноябрь 2010 г.). «Понимание регресса экосистемы». Экологические монографии. 80 (4): 509–29. Дои:10.1890/09-1552.1.
- ^ Медведь Р. и Ринтул Д. (2018) «Биогеохимические циклы». В: Bear R, Rintoul D, Snyder B, Smith-Caldas M, Herren C и Horne E (ред.) Принципы биологии OpenStax.
- ^ Левин, Симон А; Карпентер, Стивен Р.; Годфрей, Чарльз Дж; Кинзиг, Энн П.; Лоро, Мишель; Лосос, Джонатан Б. Уокер, Брайан; Уилков, Дэвид С. (27 июля 2009 г.). Принстонское руководство по экологии. Издательство Принстонского университета. п. 330. ISBN 978-0-691-12839-9.
- ^ а б Bormann, F.H .; Ликенс, Г. Э. (1967). «Круговорот питательных веществ» (PDF). Наука. 155 (3761): 424–429. Bibcode:1967Научный ... 155..424B. Дои:10.1126 / science.155.3761.424. PMID 17737551. Архивировано из оригинал (PDF) 27 сентября 2011 г.
- ^ а б c Растворенные питательные вещества Земля в будущем, PenState / NASSA. Проверено 18 июня 2020.
- ^ а б Йоргенсен, Б. Б., Финдли, А. Дж. и Пеллерин, А. (2019) «Биогеохимический цикл серы в морских отложениях». Границы микробиологии, 10: 849. Дои:10.3389 / fmicb.2019.00849.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ Бримблкомб П (2014). «Глобальный цикл серы». Трактат по геохимии. 10. Амстердам: Эльзевир. С. 559–591. Дои:10.1016 / B978-0-08-095975-7.00814-7. ISBN 9780080983004.
- ^ а б c Фике Д.А., Брэдли А.С., Роуз CV (2015). «Переосмысление древнего цикла серы». Ежегодный обзор наук о Земле и планетах. 43 (1): 593–622. Bibcode:2015AREPS..43..593F. Дои:10.1146 / аннурьев-земля-060313-054802.
- ^ Canfield DE (2004). «Эволюция резервуара серы на поверхности Земли». Американский журнал науки. 304 (10): 839–861. Bibcode:2004AmJS..304..839C. Дои:10.2475 / ajs.304.10.839.
- ^ Kah LC, Lyons TW, Frank TD (октябрь 2004 г.). «Низкая морская сульфатность и длительное насыщение кислородом протерозойской биосферы». Природа. 431 (7010): 834–8. Bibcode:2004Натура 431..834K. Дои:10.1038 / природа02974. PMID 15483609.
- ^ а б Зиверт С.М., Хюглер М., Тейлор К.Д., Вирсен, CO (2008). Даль C, Фридрих CG (ред.). «Окисление серы в глубоководных гидротермальных источниках». Микробный метаболизм серы. Springer Berlin Heidelberg: 238–258. Дои:10.1007/978-3-540-72682-1_19. ISBN 978-3-540-72679-1.
- ^ Цзян, Л., Лю, Дж. И Шао, З. (2017) "Серный метаболизм Hydrogenovibrio thermophilus штамм s5 и его адаптации к условиям глубоководных гидротермальных источников ". Границы микробиологии, 8: 2513. Дои:10.3389 / fmicb.2017.02513.
- ^ Клотц М.Г., Брайант Д.А., Хэнсон Т.Э. (2011). «Микробный цикл серы». Границы микробиологии. 2: 241. Дои:10.3389 / fmicb.2011.00241. ЧВК 3228992. PMID 22144979.
- ^ Pedersen RB, Rapp HT, Thorseth IH, Lilley MD, Barriga FJ, Baumberger T и др. (Ноябрь 2010 г.). «Открытие жерлового поля черного курильщика и жерловой фауны на Северном Ледовитом океане». Nature Communications. 1 (8): 126. Bibcode:2010НатКо ... 1..126П. Дои:10.1038 / ncomms1124. ЧВК 3060606. PMID 21119639.
- ^ а б Никельсен Л., Келлер Д., Ошлис А. (12 мая 2015 г.). «Модуль динамического морского цикла железа в сочетании с моделью системы Земли Университета Виктории: морской биогеохимической моделью 2 в Киле для UVic 2.9». Разработка геонаучных моделей. 8 (5): 1357–1381. Bibcode:2015GMD ..... 8.1357N. Дои:10.5194 / gmd-8-1357-2015.
- ^ Джикеллс Т.Д., Ан З.С., Андерсен К.К., Бейкер А.Р., Бергаметти Дж., Брукс Н. и др. (Апрель 2005 г.). «Глобальные железные связи между пылью пустыни, биогеохимией океана и климатом». Наука. 308 (5718): 67–71. Bibcode:2005 Наука ... 308 ... 67J. Дои:10.1126 / science.1105959. PMID 15802595.
- ^ Raiswell R, Canfield DE (2012). «Прошлый и настоящий биогеохимический цикл железа» (PDF). Геохимические перспективы. 1: 1–232. Дои:10.7185 / geochempersp.1.1.
- ^ а б Ван Т., Мюллер ДБ, Граедель Т.Э. (2007-07-01). «Создание антропогенного железного цикла». Экологические науки и технологии. 41 (14): 5120–5129. Bibcode:2007EnST ... 41,5120 Вт. Дои:10.1021 / es062761t. PMID 17711233.
- ^ Тейлор С.Р. (1964). «Изобилие химических элементов в континентальной коре: новая таблица». Geochimica et Cosmochimica Acta. 28 (8): 1273–1285. Bibcode:1964GeCoA..28.1273T. Дои:10.1016/0016-7037(64)90129-2.
- ^ Völker C, Tagliabue A (июль 2015 г.). «Моделирование органических железосвязывающих лигандов в трехмерной биогеохимической модели океана» (PDF). Морская химия. 173: 67–77. Дои:10.1016 / j.marchem.2014.11.008.
- ^ а б Мацуи Х., Маховальд Н.М., Мотеки Н., Гамильтон Д.С., Охата С., Йошида А., Койке М., Сканза Р.А., Фланнер М.Г. (апрель 2018 г.). «Железо антропогенного горения как комплексный климатический фактор». Nature Communications. 9 (1): 1593. Bibcode:2018НатКо ... 9,1593 млн. Дои:10.1038 / s41467-018-03997-0. ЧВК 5913250. PMID 29686300.
- ^ Эмерсон Д. (2016). «Ирония железа - биогенные оксиды железа как источник железа в океане». Границы микробиологии. 6: 1502. Дои:10.3389 / fmicb.2015.01502. ЧВК 4701967. PMID 26779157.
- ^ Olgun N, Duggen S, Croot PL, Delmelle P, Dietze H, Schacht U, et al. (2011). «Удобрение железом на поверхности океана: роль переносимого по воздуху вулканического пепла из зоны субдукции и горячих точек вулканов и связанных с ними потоков железа в Тихий океан» (PDF). Глобальные биогеохимические циклы. 25 (4): н / д. Bibcode:2011GBioC..25.4001O. Дои:10.1029 / 2009GB003761.
- ^ Гао Ю., Кауфман Ю., Танре Д., Кольбер Д., Фальковски П. Г. (01.01.2001). «Сезонные распределения потоков эолового железа в Мировой океан». Письма о геофизических исследованиях. 28 (1): 29–32. Bibcode:2001GeoRL..28 ... 29G. Дои:10.1029 / 2000GL011926.
- ^ Басу, С., Гледхилл, М., де Бир, Д., Матондкар, С.П. и Шакед, Ю. (2019) "Колонии морских цианобактерий Триходесмий взаимодействуют с ассоциированными бактериями для получения железа из пыли ». Природа: Биология коммуникации, 2(1): 1–8. Дои:10.1038 / с42003-019-0534-з.
 Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0.
Материал был скопирован из этого источника, который доступен под Международная лицензия Creative Commons Attribution 4.0. - ^ а б Уокер, Джеймс С. Дж .; Hays, P. B .; Кастинг, Дж. Ф. (1981). «Механизм отрицательной обратной связи для долговременной стабилизации температуры поверхности Земли». Журнал геофизических исследований. 86 (C10): 9776. Bibcode:1981JGR .... 86.9776W. Дои:10.1029 / jc086ic10p09776. ISSN 0148-0227.
- ^ Бернер, Р. А. (2004-05-01). «Модель кальция, магния и сульфата в морской воде за фанерозойское время». Американский журнал науки. 304 (5): 438–453. Bibcode:2004AmJS..304..438B. Дои:10.2475 / ajs.304.5.438. ISSN 0002-9599.
- ^ Риджвелл, Энди; Зибе, Ричард Э. (2005-06-15). «Роль глобального карбонатного цикла в регулировании и эволюции системы Земли». Письма по науке о Земле и планетах. 234 (3–4): 299–315. Дои:10.1016 / j.epsl.2005.03.006. ISSN 0012-821X.
- ^ Рубин, Рональд П .; Вайс, Джордж Б .; Патни, Джеймс У. младший (11.11.2013). Кальций в биологических системах. Springer Science & Business Media. ISBN 9781461323778.
- ^ а б Фантл, Мэтью С .; Типпер, Эдвард Т. (2014). «Изотопы кальция в глобальном биогеохимическом цикле Са: последствия для разработки прокси изотопа Са». Обзоры наук о Земле. 131: 148–177. Дои:10.1016 / j.earscirev.2014.02.002. ISSN 0012-8252 - через Elsevier ScienceDirect.
- ^ Комар, Н .; Зибе, Р. Э. (январь 2016 г.). «Изотоп кальция и кальция изменяется во время нарушений углеродного цикла в конце перми». Палеоокеанография. 31 (1): 115–130. Bibcode:2016PalOc..31..115K. Дои:10.1002 / 2015pa002834. ISSN 0883-8305.
- ^ «PMEL CO2 - Программа по двуокиси углерода». www.pmel.noaa.gov. Получено 2018-10-29.
- ^ «Подкисление океана». Смитсоновский океан. Получено 2018-10-29.
- ^ Treguer, P .; Нельсон, Д. М .; Van Bennekom, A.J .; Демастер, Д. Дж .; Leynaert, A .; Кегинер, Б. (1995). «Баланс кремнезема в Мировом океане: переоценка». Наука. 268 (5209): 375–9. Bibcode:1995Научный ... 268..375T. Дои:10.1126 / science.268.5209.375. PMID 17746543.
- ^ а б Ван Каппеллен, П. (2003) "Биоминерализация и глобальные биогеохимические циклы". Обзоры по минералогии и геохимии, 54(1): 357–381. Дои:10.2113/0540357.
- ^ Дасгупта, Радждип (10 декабря 2011 г.). Влияние процессов магматического океана на современную инвентаризацию глубинного углерода Земли. Пост-AGU 2011 CIDER Workshop. Архивировано из оригинал 24 марта 2016 г.. Получено 20 марта 2019.
- ^ а б Bodnar, R.J .; Азбей, Т .; Becker, S.P .; Cannatelli, C .; Fall, A .; Северс, М.Дж. (2013). «Геогидрологический цикл всей Земли, от облаков до ядра: распределение воды в динамической системе Земли» (PDF). В М.Э., Бикфорд (ред.). Сеть геологических наук: достижения, влияние и взаимодействие: специальный доклад Геологического общества Америки 500. Геологическое общество Америки. С. 431–461. Дои:10.1130/2013.2500(13). ISBN 9780813725000. Получено 19 апреля 2019.
- ^ Квенволден, Кейт А. (2006). «Органическая геохимия - ретроспектива первых 70 лет существования». Органическая геохимия. 37: 1–11. Дои:10.1016 / j.orggeochem.2005.09.001.
- ^ Шоберт, Гарольд Х. (2013). Химия ископаемого топлива и биотоплива. Кембридж: Издательство Кембриджского университета. С. 103–130. ISBN 978-0-521-11400-4. OCLC 795763460.
- ^ Павлин, Саймон М .; Гайндман, Рой Д. (15 августа 1999 г.). «Водные минералы в мантийном клине и максимальная глубина субдукционных надвиговых землетрясений». Письма о геофизических исследованиях. 26 (16): 2517–2520. Дои:10.1029 / 1999GL900558.
- ^ Rüpke, L; Морган, Джейсон Фиппс; Хорт, Матиас; Коннолли, Джеймс А. Д. (июнь 2004 г.). «Змеевик и круговорот воды в зоне субдукции». Письма по науке о Земле и планетах. 223 (1–2): 17–34. Bibcode:2004E и PSL.223 ... 17R. Дои:10.1016 / j.epsl.2004.04.018.
- ^ Bell, D. R .; Россман, Г. Р. (13 марта 1992 г.). «Вода в мантии Земли: роль номинально безводных минералов». Наука. 255 (5050): 1391–1397. Дои:10.1126 / science.255.5050.1391. Получено 23 апреля 2019.
- ^ Кепплер, Ганс (2013). «Летучие вещества под высоким давлением». В Карато - Сюн-ичиро; Карато, Сюнъитиро (ред.). Физика и химия глубин Земли. Джон Вили и сыновья. С. 22–23. Дои:10.1002 / 9781118529492.ch1. ISBN 9780470659144.
- ^ а б Хиршманн, Марк М. (2006). "Вода, тающая, и глубокая Земля H2O цикл ". Ежегодный обзор наук о Земле и планетах. 34. Дои:10.1146 / annurev.earth.34.031405.125211.
- ^ «Глубокий углеродный цикл и наша обитаемая планета». Глубокая углеродная обсерватория. 3 декабря 2015 г.. Получено 2019-02-19.
- ^ Шмидт-Рор, К. (2015). «Почему процессы сгорания всегда экзотермичны, давая около 418 кДж на моль O2", J. Chem. Educ. 92: 2094-2099. http://dx.doi.org/10.1021/acs.jchemed.5b00333
- ^ Пол Манн, Лиза Гахаган и Марк Б. Гордон, «Тектоническая обстановка гигантских нефтяных и газовых месторождений в мире», в Мишель Т. Халбути (ред.) Гигантские месторождения нефти и газа десятилетия 1990–1999 гг., Талса, Окла: Американская ассоциация геологов-нефтяников, п. 50, по состоянию на 22 июня 2009 г.
- ^ «термохимия образования ископаемого топлива» (PDF).
Дальнейшие ссылки
- Джеймс, Рэйчел и Открытый университет (2005) Морские биогеохимические циклы Баттерворт-Хайнеманн. ISBN 9780750667937.