Причины рака - Causes of cancer
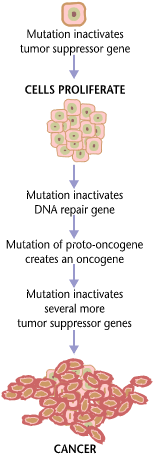
Рак это болезнь, вызванная генетический изменения, ведущие к неконтролируемому росту клеток и опухоль формирование. Основная причина спорадического (несемейного) рака - повреждение ДНК.[нужна цитата ] и геномная нестабильность.[1] Меньшая часть случаев рака вызвана наследственными генетическими мутациями.[2] Большинство видов рака связаны с воздействием окружающей среды, образом жизни или поведенческими факторами.[3] Рак - это в целом не заразный у людей, хотя это может быть вызвано онковирусы и раковые бактерии. Период, термин "относящийся к окружающей среде ", как используют исследователи рака, относится ко всему, что находится вне тела, что взаимодействует с людьми.[4] Окружающая среда не ограничивается биофизическая среда (например, воздействие таких факторов, как загрязнение воздуха или солнечный свет), но также включает факторы образа жизни и поведения.[5]
Более одной трети смертей от рака во всем мире (и около 75–80% в США) потенциально можно избежать, если снизить воздействие известных факторов.[6][7] Общие факторы окружающей среды, которые способствуют смерти от рака, включают воздействие различных химических и физических агентов (табак на потребление приходится 25–30% смертей от рака), загрязнители окружающей среды, диета и ожирение (30–35%), инфекции (15–20%), и радиация (как ионизирующие, так и неионизирующие, до 10%).[8] Эти факторы действуют, по крайней мере частично, путем изменения функции гены внутри клеток.[9] Обычно до развития рака требуется множество таких генетических изменений.[9] Старение неоднократно и последовательно рассматривалось как важный аспект, который необходимо учитывать при оценке факторов риска развития конкретных видов рака. Многие молекулярные и клеточные изменения, участвующие в развитии рака, накапливаются в процессе старения и в конечном итоге проявляются в виде рака.[10]
Генетика

Хотя существует более 50 идентифицируемых наследственных форм рака, менее 0,3% населения являются носителями генетической мутации, связанной с раком, и на них приходится менее 3–10% всех случаев рака.[2] Подавляющее большинство видов рака не являются наследственными («спорадические виды рака»). Наследственные раки в первую очередь вызваны наследственным генетическим дефектом. А онкологический синдром или синдром семейного рака представляет собой генетическое заболевание, при котором наследственные генетические мутации в одном или нескольких генах предрасполагают пораженных лиц к развитию рака, а также могут вызывать раннее начало этих видов рака. Хотя онкологические синдромы демонстрируют повышенный риск рака, риск варьируется. Для некоторых из этих заболеваний рак не является основным признаком и является редким последствием.
Многие случаи онкологического синдрома вызваны мутациями в гены-супрессоры опухолей которые регулируют рост клеток. Другие распространенные мутации изменяют функцию Гены репарации ДНК, онкогены и гены, участвующие в производстве кровеносных сосудов.[11] Определенные наследственные мутации в генах BRCA1 и BRCA2 с риском более 75% рак молочной железы и рак яичников.[2] Некоторые из наследственных генетических нарушений, которые могут вызывать колоректальный рак включают семейный аденоматозный полипоз и наследственный неполипозный рак толстой кишки; однако они составляют менее 5% случаев рака толстой кишки.[12] Во многих случаях, генетическое тестирование может использоваться для идентификации мутировавших генов или хромосом, которые передаются из поколения в поколение.
Генные мутации классифицируются как зародышевый или же соматический в зависимости от типа ячейки, в которой они появляются (клетки зародышевой линии включают яйцеклетку и сперму и соматические клетки те, что образуют тело). Мутации зародышевой линии передаются из поколения в поколение и увеличивают риск рака.[нужна цитата ]
Раковые синдромы
- Атаксия телеангиэктазия
- Синдром Блума
- BRCA1 & BRCA2
- Анемия Фанкони
- Семейный аденоматозный полипоз
- Наследственный рак груди и яичников
- Наследственный неполипозный рак толстой кишки
- Синдром Ли-Фраумени
- Синдром невоидной базальноклеточной карциномы
- Болезнь фон Гиппеля-Линдау
- Синдром Вернера
- Пигментная ксеродермия
Физические и химические агенты
Особые вещества, известные как канцерогены, были связаны с определенными типами рака. Распространенными примерами нерадиоактивных канцерогенов являются вдыхаемый асбест, некоторые диоксины и табачный дым. Хотя общественность обычно связывает канцерогенность с синтетическими химическими веществами, она с одинаковой вероятностью может возникать как в природных, так и в синтетических веществах.[13] По оценкам, около 20 000 смертей от рака и 40 000 новых случаев рака ежегодно в США связаны с оккупацией.[14] Ежегодно по крайней мере 200 000 человек во всем мире умирают от рака на рабочем месте.[15] Миллионы рабочих рискуют заболеть такими видами рака, как рак легких и мезотелиома от вдыхания асбест волокна и табачный дым, или лейкемия от воздействия на бензол на своих рабочих местах.[15] Считается, что рак, связанный с профессией, составляет от 2 до 20% всех случаев.[16] Большинство случаев смерти от рака, вызванных профессиональными факторами риска, происходит в развитых странах.[15] Стресс на работе не является значительным фактором, по крайней мере, при раке легких, толстой кишки, груди и простаты.[17]
Курение


Курение табака связан со многими формами рака,[19] и вызывает 80% рак легких.[20] Десятилетия исследований продемонстрировали связь между употреблением табака и раком легких, гортани, головы, шеи, желудка, мочевого пузыря, почек, пищевода и поджелудочной железы.[21] Есть данные, свидетельствующие о небольшом повышении риска развития миелоидного лейкоза, плоскоклеточного рака носовых пазух, рака печени, колоректального рака, рака желчного пузыря, надпочечников, тонкой кишки и различных онкологических заболеваний у детей.[21] Табачный дым содержит более пятидесяти известных канцерогенов, в том числе: нитрозамины и полициклические ароматические углеводороды.[22] Табак является причиной примерно одной из трех смертей от рака в развитом мире.[19] и примерно каждый пятый в мире.[22] Показатели смертности от рака легких в Соединенных Штатах отражают характер курения: рост курения сопровождается резким увеличением показателей смертности от рака легких, а в последнее время - снижением показателей курения с 1950-х годов с последующим снижением показателей смертности от рака легких среди мужчин с 1990 года. .[23][24] Однако количество курильщиков во всем мире продолжает расти, что приводит к тому, что некоторые организации называют табачная эпидемия.[25]
Электронные сигареты или электронные сигареты портативные электронные устройства, имитирующие чувство курения табака. Ежедневное длительное использование электронных сигарет высокого напряжения (5,0 В) может приводить к возникновению формальдегид -образующие химические вещества на более высоком уровне, чем курение, что, как было установлено, представляет собой пожизненный риск рака примерно в 5-15 раз выше, чем курение.[26] Однако общая безопасность и долгосрочное воздействие электронных сигарет на здоровье все еще остается неопределенным.[27]
Материалы
Некоторые вещества вызывают рак в первую очередь из-за своего физического, а не химического воздействия на клетки.[28] Ярким примером этого является длительное воздействие асбеста, природных минеральных волокон, которые являются основной причиной мезотелиомы, которая является раком серозный мембраны, обычно серозная оболочка, окружающая легкие.[28] Другие вещества этой категории, включая как природные, так и синтетические асбестоподобные волокна, такие как волластонит, аттапульгит, стекловата, и каменная вата, как полагают, имеют аналогичные эффекты.[28] Неволокнистые твердые частицы, вызывающие рак, включают металлический порошок. кобальт и никель, и кристаллический кремнезем (кварц, кристобалит, и тридимит ).[28] Обычно физические канцерогены должны попасть внутрь тела (например, при вдыхании крошечных кусочков), и для развития рака требуются годы воздействия.[28] Общие профессиональные канцерогены включают:[29]
Стиль жизни
Многие факторы образа жизни способствуют увеличению риска рака. Вместе диета и ожирение связаны примерно с 30–35% случаев смерти от рака.[8][30] Диетические рекомендации для профилактики рака обычно включают упор на овощи, фрукты, цельнозерновые и рыбу, а также отказ от обработанного мяса, красного мяса, животных жиров и рафинированных углеводов.[31] Доказательства в поддержку этих диетических изменений не являются окончательными.[32]
Алкоголь

Алкоголь является примером химического канцерогена. Всемирная организация здравоохранения классифицировала алкоголь как Канцероген группы 1.[33] В Западной Европе 10% случаев рака у мужчин и 3% случаев рака у женщин связаны с алкоголем.[34] Во всем мире 3,6% всех случаев рака и 3,5% смертей от рака связаны с алкоголем.[35] В частности, было показано, что употребление алкоголя увеличивает риск развития рака ротовой полости, пищевода, глотки, гортани, желудка, печени, яичников и толстой кишки.[36] Основной механизм развития рака связан с повышенным воздействием ацетальдегид, канцероген и продукт распада этанола.[37] Были предложены другие механизмы, в том числе связанные с алкоголем. дефицит питательных веществ, изменения в Метилирование ДНК, и индукция окислительный стресс в тканях.[38]
Рацион питания
Некоторые конкретные продукты связаны с определенными видами рака. Исследования показали, что люди, которые едят красное или обработанное мясо, имеют более высокий риск развития рака груди, рака простаты и рака поджелудочной железы.[39] Частично это можно объяснить наличием канцерогенов в пище, приготовленной при высоких температурах.[40] Несколько факторов риска развития колоректального рака включают высокое потребление жиров, алкоголя, красного и обработанного мяса, ожирение и отсутствие физических упражнений.[41] Высота-соль диета связана с рак желудка. Афлатоксин B1, частое загрязнение пищевых продуктов, связано с раком печени. Орех бетель Было показано, что жевание вызывает рак полости рта.[42]
Взаимосвязь между диетой и развитием конкретных видов рака может частично объяснять различия в заболеваемости раком в разных странах. Например, рак желудка чаще встречается в Японии из-за частоты высокосолевых диет, а рак толстой кишки чаще встречается в Соединенных Штатах из-за повышенного потребления переработанного и красного мяса.[43] Сообщества иммигрантов, как правило, формируют профиль риска рака в своей новой стране, часто в пределах одного-двух поколений, что предполагает существенную связь между диетой и раком.[44][45]
Ожирение
В Соединенных Штатах избыточная масса тела связана с развитием многих типов рака и является причиной 14–20% всех случаев смерти от рака.[30] Ежегодно около 85 000 новых диагнозов рака в Соединенных Штатах связаны с ожирением.[46] Лица, перенесшие бариатрической хирургии для похудания снизили заболеваемость раком и смертность.[46]
Существует связь между ожирением и раком толстой кишки, раком груди в постменопаузе, раком эндометрия, раком почек и раком пищевода.[46] Ожирение также связано с развитием рака печени.[47] Современное понимание механизма развития рака при ожирении связано с аномальными уровнями метаболических белков (включая инсулиноподобные факторы роста) и половых гормонов (эстрогены, андрогены и прогестагены ).[46] Жировая ткань также создает воспалительный окружающая среда, которая может способствовать развитию рака.[48]
Считается, что отсутствие физической активности способствует риску рака не только из-за своего воздействия на массу тела, но и из-за отрицательного воздействия на иммунная система и эндокринная система.[30] Более половины эффекта от диеты обусловлено переедание вместо того, чтобы есть слишком мало здоровой пищи.[46]
Гормоны

Немного гормоны играют роль в развитии рака, способствуя распространение клеток.[49] Инсулиноподобные факторы роста и их связывающие белки играют ключевую роль в росте, дифференцировке и дифференцировке раковых клеток. апоптоз, что предполагает возможное участие в канцерогенезе.[50]
Гормоны являются важными агентами при раковых заболеваниях, связанных с полом, таких как рак груди, эндометрия, простаты, яичников и яичек, а также рак щитовидной железы и рак кости.[49] Например, дочери женщин, больных раком груди, имеют значительно более высокий уровень эстроген и прогестерон чем дочери женщин без рака груди. Эти более высокие уровни гормонов могут объяснить, почему у этих женщин более высокий риск рака груди, даже при отсутствии гена рака груди.[49] Точно так же мужчины африканского происхождения имеют значительно более высокий уровень тестостерон чем мужчины европейского происхождения, и, соответственно, имеют гораздо более высокий уровень рак простаты.[49] Мужчины азиатского происхождения с самым низким уровнем активации тестостерона андростандиол глюкуронид, имеют самый низкий уровень рака простаты.[49]
Важны и другие факторы: у тучных людей более высокий уровень некоторых гормонов, связанных с раком, и более высокая частота этих видов рака.[49] Женщины, которые принимают заместительная гормональная терапия имеют более высокий риск развития рака, связанного с этими гормонами.[49] С другой стороны, люди, которые тренируются намного больше среднего, имеют более низкий уровень этих гормонов и более низкий риск рака.[49] Остеосаркома может продвигаться гормоны роста.[49]
Некоторые методы лечения и профилактики используют эту причину, искусственно снижая уровень гормонов и, таким образом, препятствуя развитию гормоночувствительного рака. Поскольку стероидные гормоны являются мощными двигателями экспрессии генов в определенных раковых клетках, изменение уровней или активности определенных гормонов может привести к прекращению роста определенных видов рака или даже к их гибели.[49] Пожалуй, самый известный пример гормональной терапии в онкологии - это использование селективный модулятор эстрогеновых рецепторов тамоксифен для лечения рака груди. Другой класс гормональных средств, ингибиторы ароматазы, теперь играют все более важную роль в лечении рака груди.
Инфекция и воспаление
Во всем мире около 18% случаев рака связаны с инфекционные заболевания.[8][51] Эта доля варьируется в разных регионах мира от 25% в Африке до менее 10% в развитых странах.[8] Вирусы являются обычными инфекционными агентами, вызывающими рак, но бактерии и паразиты также внести свой вклад. Инфекционные организмы, повышающие риск рака, часто являются источником повреждения ДНК или геномной нестабильности.
Вирусы

Вирусная инфекция является основным фактором риска рака шейки матки и печени.[52] Вирус, который может вызвать рак, называется онковирус. К ним относятся вирус папилломы человека (рак шейки матки ), Вирус Эпштейна-Барра (В-клеточное лимфопролиферативное заболевание и карцинома носоглотки ), Вирус герпеса саркомы Капоши (Саркома Капоши и первичные выпотные лимфомы ), гепатит Б и гепатит С вирусы (гепатоцеллюлярная карцинома ), и Вирус Т-клеточного лейкоза человека-1 (Т-клеточные лейкозы).
В западных развитых странах наиболее распространенными онковирусами являются вирус папилломы человека (ВПЧ), вирус гепатита В (ВГВ) и вирус гепатита С (ВГС).[53] В Соединенных Штатах ВПЧ вызывает большинство видов рака шейки матки, а также некоторые виды рака влагалища, вульвы, полового члена, ануса, прямой кишки, горла, языка и миндалин.[54] Среди вирусов ВПЧ высокого риска ВПЧ E6 и E7 онкопротеины инактивировать гены-супрессоры опухолей при заражении клеток. Кроме того, онкопротеины независимо друг от друга вызывают геномную нестабильность в нормальных клетках человека, что приводит к повышенному риску развития рака.[55] У людей с хронической инфекцией вируса гепатита B вероятность развития рака печени более чем в 200 раз выше, чем у неинфицированных людей.[56] Цирроз печени, независимо от того, вызван ли он хроническим вирусным гепатитом или злоупотреблением алкоголем, независимо связан с развитием рака печени, но сочетание цирроза и вирусного гепатита представляет самый высокий риск развития рака печени.[56]
Бактерии и паразиты

Некоторые бактериальные инфекции также увеличивают риск рака, как показано на Helicobacter pylori -индуцированный рак желудка.[57] Механизм, с помощью которого Хеликобактер пилори вызывает рак, может включать хроническое воспаление или прямое действие некоторых бактерий. факторы вирулентности.[58] Паразитарные инфекции, тесно связанные с раком, включают: Schistosoma haematobium (плоскоклеточный рак мочевого пузыря ) и печеночные двуустки, Описторхис виверрини и Clonorchis sinensis (холангиокарцинома ).[59] Воспаление, вызванное яйцами червя, по-видимому, вызывает рак. Некоторые паразитарные инфекции могут также увеличивать присутствие канцерогенных соединений в организме, что приводит к развитию рака.[60] Туберкулез инфекция, вызванная микобактерии М. туберкулез, также был связан с развитием рака легких.[61]
Воспаление
Есть свидетельства того, что воспаление сам по себе играет важную роль в развитии и прогрессировании рака.[62] Хроническое воспаление может со временем привести к повреждению ДНК и накоплению случайных генетических изменений в раковых клетках.[63] Воспаление может способствовать пролиферации, выживанию, ангиогенезу и миграции раковых клеток, влияя на микросреда опухоли.[64] Лица с воспалительное заболевание кишечника находятся в группе повышенного риска развития колоректального рака.[12]
Радиация
До 10% инвазивных видов рака связаны с радиационным облучением, включая оба неионизирующий радиация и ионизирующего излучения.[8] В отличие от химических или физических триггеров рака, ионизирующее излучение поражает молекулы внутри клеток случайным образом. Если случится ударить хромосома, это может сломать хромосому, что приведет к аномальное количество хромосом, инактивировать один или несколько генов в той части хромосомы, которую он поражает, удалить части последовательности ДНК, вызвать хромосомные транслокации, или вызвать другие типы хромосомные аномалии.[65] Сильное повреждение обычно приводит к гибели клетки, но меньшее повреждение может оставить стабильную, частично функциональную клетку, которая может быть способной к пролиферации и развитию рака, особенно если гены-супрессоры опухолей были повреждены радиацией.[65] Три независимых этапа, по-видимому, участвуют в создании рака под действием ионизирующего излучения: морфологические изменения клетки, приобретение клеточное бессмертие (потеря нормальных, ограничивающих жизнь клеточных регуляторных процессов) и адаптации, способствующей образованию опухоли.[65] Даже если частица радиации не попадает в ДНК напрямую, она вызывает реакции клеток, которые косвенно увеличивают вероятность мутаций.[65]
Неионизирующее излучение

Не все виды электромагнитного излучения канцерогены. Считается, что низкоэнергетические волны в электромагнитном спектре, включая радиоволны, микроволны, инфракрасное излучение и видимый свет, не относятся к ним, потому что у них недостаточно энергии для разрушения химические связи. Неионизирующий радиочастота излучение от мобильные телефоны, передача электроэнергии, и другие подобные источники были описаны как возможный канцероген Всемирная организация здоровья с Международное агентство по изучению рака.[66][67] Однако исследования не обнаружили последовательной связи между радиацией сотового телефона и риском рака.[68]
Излучение более высоких энергий, в том числе ультрафиолетовая радиация (присутствует в солнечном свете), рентгеновские лучи, и гамма-излучение, как правило, является канцерогенным при приеме в достаточных дозах. Длительное воздействие ультрафиолетовая радиация от солнце может привести к меланома и другие злокачественные новообразования кожи.[69] Подавляющее большинство неинвазивных видов рака - это немеланома. рак кожи вызвано неионизирующим ультрафиолетовым излучением. Явные доказательства устанавливают ультрафиолетовое излучение, особенно волну неионизирующей среды. UVB, как причина большинства немеланомных видов рака кожи, которые являются наиболее распространенными формами рака в мире.[69]
Ионизирующего излучения

Источники ионизирующего излучения включают: медицинская визуализация, и радон газ. Ионизирующее излучение не является особенно сильным мутагеном.[65] Использование ионизирующего излучения в медицине является растущим источником радиационно-индуцированного рака. Ионизирующее излучение можно использовать для лечения других видов рака, но в некоторых случаях это может вызвать вторую форму рака.[65] Радиация может вызвать рак в большинстве частей тела, у всех животных и в любом возрасте, хотя радиационно-индуцированные солидные опухоли обычно проявляются в течение 10–15 лет и могут занять до 40 лет, чтобы проявиться клинически. лейкемии для появления обычно требуется 2–10 лет.[65] Радиационно-индуцированный менингиомы являются нечастым осложнением краниального облучения.[70] Некоторые люди, например, с синдром невоидной базальноклеточной карциномы или же ретинобластома, более восприимчивы, чем в среднем, к развитию рака в результате радиационного воздействия.[65] У детей и подростков вероятность развития лейкемии, вызванной радиацией, в два раза выше, чем у взрослых; лучевое воздействие до рождения имеет в десять раз больший эффект.[65]
Ионизирующее излучение также используется в некоторых видах медицинская визуализация. В промышленно развитых странах медицинская визуализация приносит населению почти такую же дозу радиации, как и естественный фон. Ядерная медицина Методы включают введение радиоактивных фармацевтических препаратов непосредственно в кровоток. Лучевая терапия преднамеренно доставлять высокие дозы радиации к опухолям и окружающим тканям в качестве средства лечения заболевания. Подсчитано, что 0,4% раковых заболеваний в 2007 г. в США были вызваны КТ, выполненными в прошлом, и что эта цифра может возрасти до 1,5–2% с темпами использования КТ в тот же период времени.[71]
Воздействие газообразного радона в жилых помещениях имеет такой же риск рака, как и пассивное курение.[65] Воздействие малых доз, например проживание рядом с атомная электростанция, как правило, считается, что они не оказывают или оказывают очень незначительное влияние на развитие рака.[65] Радиация является более мощным источником рака, когда она сочетается с другими вызывающими рак агентами, такими как воздействие газообразного радона и курение табака.[65]
Редкие причины
Трансплантация органов

Развитие донорских опухолей от трансплантация органов чрезвычайно редко. Основной причиной опухолей, связанных с трансплантацией органов, по-видимому, является: злокачественная меланома, который не был обнаружен во время извлечения органов.[72] Также были сообщения о Саркома Капоши возникает после трансплантации из-за опухолевого роста инфицированных вирусом донорских клеток.[73]
Травма
Физические травмы, приводящие к раку, относительно редки.[74] Утверждения, что переломы костей, например, приводят к раку костей, никогда не были доказаны.[74] Точно так же физическая травма не считается причиной рака шейки матки, груди или мозга.[74] Одним из признанных источников является частое и длительное прикладывание к телу горячих предметов. Возможно, что повторяющиеся ожоги одной и той же части тела, например, нанесенные Кангер и обогреватели kairo (уголь грелки для рук ), может вызвать рак кожи, особенно если присутствуют канцерогенные химические вещества.[74]
Частое употребление обжигающего горячего чая может вызвать рак пищевода.[74] Обычно считается, что рак возникает или поощряется ранее существовавший рак во время процесса восстановления травмы, а не рак, вызванный непосредственно травмой.[74] Однако повторяющиеся повреждения одних и тех же тканей могут способствовать чрезмерной пролиферации клеток, что в свою очередь увеличивает вероятность раковой мутации.
Передача от матери к плоду
В Соединенных Штатах ежегодно около 3500 беременных женщин заболевают злокачественными новообразованиями, и трансплацентарная передача острый лейкоз, лимфома, меланома и карцинома от матери к плоду.[75] За исключением редких случаев передачи, которые происходят во время беременности и лишь незначительного количества доноров органов, рак, как правило, не является серьезным заболеванием. трансмиссивная болезнь. Основная причина этого - отторжение тканевого трансплантата, вызванное: MHC несовместимость.[75] У людей и других позвоночных иммунная система использует антигены MHC, чтобы различать «собственные» и «чужие» клетки, потому что эти антигены различаются от человека к человеку. Когда встречаются не собственные антигены, иммунная система реагирует против соответствующей клетки. Такие реакции могут защитить от приживления опухолевых клеток за счет удаления имплантированных клеток.
Рекомендации
- ^ Фергюсон Л. Р., Чен Х., Коллинз А. Р., Коннелл М., Дамиа Г., Дасгупта С. и др. (Декабрь 2015 г.). «Геномная нестабильность при раке человека: молекулярные знания и возможности терапевтического воздействия и профилактики с помощью диеты и питания». Семинары по биологии рака. 35 Дополнение (Suppl): S5 – S24. Дои:10.1016 / j.semcancer.2015.03.005. ЧВК 4600419. PMID 25869442.
- ^ а б c Roukos DH (апрель 2009 г.). «Полногеномные исследования ассоциации: насколько предсказуемым является риск рака у человека?». Экспертный обзор противоопухолевой терапии. 9 (4): 389–92. Дои:10.1586 / эра.09.12. PMID 19374592.
- ^ Стюарт Б.В., Wild CP, ред. (2014). «Раковая этиология». Всемирный доклад о раке, 2014 г.. Всемирная организация здоровья. С. 16–54. ISBN 978-9283204299.
- ^ Рак и окружающая среда: что нужно знать и что делать. Публикация NIH № 03-2039: Национальные институты здоровья. 2003.
Рак развивается в течение нескольких лет и имеет множество причин. Несколько факторов, как внутри, так и вне организма, способствуют развитию рака. В этом контексте ученые называют «окружающей средой» все, что взаимодействует с людьми вне тела.
CS1 maint: location (связь) - ^ Кравченко Я., Акушевич И, Мантон К.Г. (2009). Паттерны смертности и заболеваемости раком среди населения США: междисциплинарный подход. Берлин: Springer. ISBN 978-0-387-78192-1.
Период, термин среда относится не только к воздуху, воде и почве, но также к веществам и условиям дома и на рабочем месте, включая диету, курение, алкоголь, наркотики, воздействие химикатов, солнечный свет, ионизирующее излучение, электромагнитные поля, инфекционные агенты и т. д. , экономические и поведенческие факторы - все это аспекты нашей окружающей среды.
- ^ Долл Р., Пето Р. (июнь 1981 г.). «Причины рака: количественные оценки предотвратимых рисков рака в Соединенных Штатах сегодня». Журнал Национального института рака. 66 (6): 1191–308. Дои:10.1093 / jnci / 66.6.1192. PMID 7017215.
- ^ Уайтмен, Дэвид С .; Уилсон, Луиза Ф. (октябрь 2016 г.). «Доли рака, обусловленные изменяемыми факторами: глобальный обзор». Эпидемиология рака. 44: 203–221. Дои:10.1016 / j.canep.2016.06.013. ISSN 1877-783X. PMID 27460784.
- ^ а б c d е Ананд П., Куннумаккара А.Б., Куннумакара А.Б., Сундарам С., Харикумар К.Б., Тхаракан С.Т., Лай О.С., Сунг Б., Аггарвал Б.Б. (сентябрь 2008 г.). «Рак - это предотвратимое заболевание, требующее серьезных изменений в образе жизни». Фармацевтические исследования. 25 (9): 2097–116. Дои:10.1007 / s11095-008-9661-9. ЧВК 2515569. PMID 18626751.
- ^ а б Всемирный доклад о раке, 2014 г.. Всемирная организация здоровья. 2014. С. Глава 1.1. ISBN 978-9283204299.
- ^ "Информационный бюллетень № 297 о раке". Всемирная организация здоровья. Февраль 2014. Получено 10 июн 2014.
- ^ Ходжсон С (январь 2008 г.). «Механизмы наследственной предрасположенности к раку». Журнал науки B Чжэцзянского университета. 9 (1): 1–4. Дои:10.1631 / jzus.B073001. ЧВК 2170461. PMID 18196605.
- ^ а б Всемирный доклад о раке, 2014 г.. Всемирная организация здоровья. 2014. С. Глава 5.5. ISBN 978-9283204299.
- ^ Эймс, Брюс Н .; Золото, Лоис Свирски (17 января 2000). «Парацельс паранауке: отвлечение от рака окружающей среды». Мутационные исследования / Фундаментальные и молекулярные механизмы мутагенеза. 447 (1): 3–13. Дои:10.1016 / S0027-5107 (99) 00194-3. ISSN 0027-5107. PMID 10686303.
- ^ «Национальный институт профессиональной безопасности и здоровья - профессиональный рак». Национальный институт безопасности и гигиены труда США. Получено 13 октября 2007.
- ^ а б c «ВОЗ призывает к профилактике рака через здоровые рабочие места» (Пресс-релиз). Всемирная организация здоровья. 27 апреля 2007 г.. Получено 13 октября 2007.
- ^ Иригарай П., Ньюби Дж. А., Клапп Р., Харделл Л., Ховард В., Монтанье Л., Эпштейн С., Белпом Д. (декабрь 2007 г.). «Факторы, связанные с образом жизни, и факторы окружающей среды, вызывающие рак: обзор». Биомедицина и фармакотерапия. 61 (10): 640–58. Дои:10.1016 / j.biopha.2007.10.006. PMID 18055160.
- ^ Хейккиля К., Нюберг С.Т., Теорелл Т., Франссон Э.И., Альфредссон Л., Бьорнер Дж. Б. и др. (Февраль 2013). «Рабочий стресс и риск рака: метаанализ 5700 случаев рака у 116 000 европейских мужчин и женщин». BMJ. 346: f165. Дои:10.1136 / bmj.f165. ЧВК 3567204. PMID 23393080.
- ^ «Доля смертей от рака, связанных с табаком». Наш мир в данных. Получено 5 марта 2020.
- ^ а б Sasco AJ, Secretan MB, Straif K (август 2004 г.). «Табакокурение и рак: краткий обзор последних эпидемиологических данных». Рак легких. 45 Дополнение 2: S3–9. Дои:10.1016 / j.lungcan.2004.07.998. PMID 15552776.
- ^ Бисальский HK, Буэно де Мескита B, Chesson A, Chytil F, Grimble R, Hermus RJ, Köhrle J, Lotan R, Norpoth K, Pastorino U, Thurnham D (1998). «Заявление Европейского консенсуса по раку легких: факторы риска и профилактика. Группа экспертов по раку легких». Ca. 48 (3): 167–76, обсуждение 164–6. Дои:10.3322 / canjclin.48.3.167. PMID 9594919.
- ^ а б Купер Х., Боффетта П., Адами Х.О. (сентябрь 2002 г.). «Употребление табака и причина рака: ассоциация по типу опухоли». Журнал внутренней медицины. 252 (3): 206–24. Дои:10.1046 / j.1365-2796.2002.01022.x. PMID 12270001.
- ^ а б Купер Х., Адами Х.О., Боффетта П. (июнь 2002 г.). «Употребление табака, причины рака и влияние на здоровье населения». Журнал внутренней медицины. 251 (6): 455–66. Дои:10.1046 / j.1365-2796.2002.00993.x. PMID 12028500. S2CID 9172672.
- ^ Тун MJ, Джемал A (октябрь 2006 г.). «Насколько снижение смертности от рака в США связано с сокращением курения табака?». Контроль над табаком. 15 (5): 345–7. Дои:10.1136 / tc.2006.017749. ЧВК 2563648. PMID 16998161.
- ^ Дубей С., Пауэлл, Калифорния (май 2008 г.). «Обновление рака легких 2007». Американский журнал респираторной медицины и реанимации. 177 (9): 941–6. Дои:10.1164 / rccm.200801-107UP. ЧВК 2720127. PMID 18434333.
- ^ Проктор Р.Н. (май 2004 г.). «Глобальная эпидемия курения: история и статус». Клинический рак легких. 5 (6): 371–6. Дои:10.3816 / CLC.2004.n.016. PMID 15217537.
- ^ Кук А., Фергесон Дж., Булхи А., Казале Т. Б. (2015). «Электронная сигарета: хорошее, плохое и уродливое». Журнал аллергии и клинической иммунологии. На практике. 3 (4): 498–505. Дои:10.1016 / j.jaip.2015.05.022. PMID 26164573.
- ^ Эбберт, Джон О .; Агунвамба, Аменах А .; Руттен, Лила Дж. (Январь 2015 г.). «Консультации пациентов по использованию электронных сигарет». Труды клиники Мэйо. 90 (1): 128–134. Дои:10.1016 / j.mayocp.2014.11.004. ISSN 1942-5546. PMID 25572196.
- ^ а б c d е Мальтони CF, Голландия JF (2000). «Глава 16: Физические канцерогены». В Bast RC, Kufe DW, Pollock RE и др. (ред.). Holland-Frei Cancer Medicine (5-е изд.). Гамильтон, Онтарио: B.C. Декер. ISBN 978-1-55009-113-7. Получено 31 января 2011.
- ^ Основная патология Роббинса. Кумар, Виней, 1944-, Роббинс, Стэнли Л. (Стэнли Леонард), 1915-2003. (8-е изд.). Филадельфия, Пенсильвания: Saunders / Elsevier. 2007. С. Таблица 6–2. ISBN 978-1416029731. OCLC 69672074.CS1 maint: другие (связь)
- ^ а б c Куши Л.Х., Байерс Т., Дойл С., Бандера Э.В., Маккаллоу М., Мактирнан А., Ганслер Т., Эндрюс К.С., Тун М.Дж. (2006). «Рекомендации Американского онкологического общества по питанию и физической активности для профилактики рака: снижение риска рака с помощью здорового питания и физической активности». Ca. 56 (5): 254–81, викторина 313–4. Дои:10.3322 / canjclin.56.5.254. PMID 17005596.
- ^ Куши Л. Х., Дойл С., Маккалоу М., Рок К. Л., Демарк-Ванефрид В., Бандера Е. В., Гапстур С., Патель А. В., Эндрюс К., Ганслер Т. (январь 2012 г.). «Рекомендации Американского онкологического общества по питанию и физической активности для профилактики рака: снижение риска рака с помощью здорового питания и физической активности». Ca. 62 (1): 30–67. Дои:10.3322 / caac.20140. PMID 22237782.
- ^ Вики А, Хагманн Дж (2011). «Диета и рак». Швейцарский медицинский еженедельник. 141: w13250. Дои:10.4414 / smw.2011.13250. PMID 21904992.
- ^ «МАИР: МАИР укрепляет свои выводы о некоторых канцерогенных личных привычках и воздействиях в семье» (PDF). Международное агентство по изучению рака - Всемирная организация здравоохранения. 2009.
- ^ Schütze M, Boeing H, Pischon T, Rehm J, Kehoe T, Gmel G и др. (Апрель 2011 г.). «Связанное с алкоголем бремя рака в восьми европейских странах на основании результатов проспективного когортного исследования». BMJ. 342: d1584. Дои:10.1136 / bmj.d1584. ЧВК 3072472. PMID 21474525.
- ^ Боффетта (август 2006 г.). «Бремя рака, связанное с употреблением алкоголя». Международный журнал рака. 119 (4): 884–7. Дои:10.1002 / ijc.21903. HDL:2434/22728. PMID 16557583.
- ^ «Употребление алкоголя и риск рака». pubs.niaaa.nih.gov. Получено 2018-03-22.
- ^ Терувату Дж. А., Джаруга П., Натх Р. Г., Диздароглу М., Брукс П. Дж. (2005). «Полиамины стимулируют образование мутагенных аддуктов 1, N2-пропанодезоксигуанозина из ацетальдегида». Исследования нуклеиновых кислот. 33 (11): 3513–20. Дои:10.1093 / нар / gki661. ЧВК 1156964. PMID 15972793.
- ^ Poschl G (май 2004 г.). «Алкоголь и рак». Алкоголь и алкоголизм. 39 (3): 155–165. Дои:10.1093 / alcalc / agh057. PMID 15082451.
- ^ Стюарт Б. (2014). Всемирный доклад о раке, 2014 г.. Всемирная организация здоровья. С. 124–33. ISBN 9789283204299.
- ^ Фергюсон Л. Р. (февраль 2010 г.). «Мясо и рак». Наука о мясе. 84 (2): 308–313. Дои:10.1016 / j.meatsci.2009.06.032. PMID 20374790.
- ^ «Отчет о колоректальном раке за 2011 год: еда, питание, физическая активность и профилактика колоректального рака» (PDF). Всемирный фонд исследований рака и Американский институт исследований рака. 2011.
- ^ Пак С., Бэ Дж, Нам Б.Х., Ю К.Й. (2008). «Этиология рака в Азии». Азиатско-Тихоокеанский журнал профилактики рака. 9 (3): 371–80. PMID 18990005. Архивировано из оригинал (PDF) на 2011-09-04. Получено 2014-07-17.
- ^ Бреннер Х, Ротенбахер Д., Арндт В. (2009). «Эпидемиология рака желудка». Эпидемиология рака. Методы молекулярной биологии. 472. С. 467–77. Дои:10.1007/978-1-60327-492-0_23. ISBN 978-1-60327-491-3. ЧВК 2166976. PMID 19107449.
- ^ Буэлл П., Данн Дж. Э. (май 1965 г.). «Смертность от рака среди японцев Issei и Nisei из Калифорнии». Рак. 18 (5): 656–64. Дои:10.1002 / 1097-0142 (196505) 18: 5 <656 :: AID-CNCR2820180515> 3.0.CO; 2-3. PMID 14278899.
- ^ Паркин, Д. М .; Хлат, М. (май 1996 г.). «Исследования рака у мигрантов: обоснование и методология». Европейский журнал рака (Оксфорд, Англия: 1990). 32A (5): 761–771. Дои:10.1016/0959-8049(96)00062-7. ISSN 0959-8049. PMID 9081351.
- ^ а б c d е ж Басен-Энгквист К., Чанг М. (февраль 2011 г.). «Ожирение и риск рака: недавний обзор и доказательства». Текущие онкологические отчеты. 13 (1): 71–6. Дои:10.1007 / s11912-010-0139-7. ЧВК 3786180. PMID 21080117.
- ^ Альзахрани Б., Исели Т.Дж., Хеббард Л.В. (апрель 2014 г.). «Невирусные причины рака печени: играет ли роль воспаление, вызванное ожирением?». Письма о раке. 345 (2): 223–9. Дои:10.1016 / j.canlet.2013.08.036. PMID 24007864.
- ^ Гилберт Калифорния, Слингерленд Дж. М. (14 января 2013 г.). «Цитокины, ожирение и рак: новое понимание механизмов, связывающих ожирение с риском и прогрессированием рака». Ежегодный обзор медицины. 64 (1): 45–57. Дои:10.1146 / annurev-med-121211-091527. PMID 23121183.
- ^ а б c d е ж грамм час я j Хендерсон Б.Е., Бернштейн Л., Росс Р.К. (2000). «Глава 13: Гормоны и этиология рака». В Bast RC, Kufe DW, Pollock RE и др. (ред.). Holland-Frei Cancer Medicine (5-е изд.). Гамильтон, Онтарио: B.C. Декер. ISBN 978-1-55009-113-7. Получено 27 января 2011.
- ^ Роулендс М.А., Ганнелл Д., Харрис Р., Ваттен Л.Дж., Холли Д.М., Мартин Р.М. (май 2009 г.). «Циркулирующие пептиды инсулиноподобного фактора роста и риск рака простаты: систематический обзор и метаанализ». Международный журнал рака. 124 (10): 2416–29. Дои:10.1002 / ijc.24202. ЧВК 2743036. PMID 19142965.
- ^ Де Мартель, Кэтрин; Ферле, Жак; Франчески, Сильвия; Винья, Жером; Брей, Фредди; Форман, Дэвид; Пламмер, Мартин (2012-06-01). «Глобальное бремя рака, связанного с инфекциями в 2008 году: обзор и синтетический анализ». Ланцет онкологии. 13 (6): 607–615. Дои:10.1016 / S1470-2045 (12) 70137-7. ISSN 1470-2045. PMID 22575588.
- ^ Де Паоли П., Карбон А (октябрь 2013 г.). «Канцерогенные вирусы и солидный рак без достаточных доказательств причинной связи». Международный журнал рака. 133 (7): 1517–29. Дои:10.1002 / ijc.27995. PMID 23280523.
- ^ Ананд П., Куннумаккара А.Б., Куннумакара А.Б., Сундарам С., Харикумар К.Б., Тхаракан С.Т., Лай О.С., Сунг Б., Аггарвал Б.Б. (сентябрь 2008 г.). «Рак - это предотвратимое заболевание, требующее серьезных изменений в образе жизни». Фармацевтические исследования. 25 (9): 2097–116. Дои:10.1007 / s11095-008-9661-9. ЧВК 2515569. PMID 18626751.
- ^ «Вирус папилломы человека (ВПЧ) и рак». CDC. 2 января 2018 г.. Получено 22 марта, 2018.
- ^ Мюнгер К., Болдуин А., Эдвардс К.М., Хаякава Х., Нгуен С.Л., Оуэнс М., Грейс М., Хах К. (ноябрь 2004 г.). «Механизмы онкогенеза, вызванного вирусом папилломы человека». Журнал вирусологии. 78 (21): 11451–60. Дои:10.1128 / JVI.78.21.11451-11460.2004. ЧВК 523272. PMID 15479788.
- ^ а б Сун MW, Thung SN, Acs G (2000). Вирусы гепатита. BC Decker.
- ^ Pagano JS, Blaser M, Буэндиа М.А., Дамания Б., Халили К., Рааб-Трауб Н., Ройзман Б. (декабрь 2004 г.). «Инфекционные агенты и рак: критерии причинной связи». Семинары по биологии рака. 14 (6): 453–71. Дои:10.1016 / j.semcancer.2004.06.009. PMID 15489139.
- ^ Хатакеяма, Масанори (9 декабря 2005 г.). «Helicobacter pylori CagA: новая парадигма бактериального канцерогенеза». Наука о раке. 96 (12): 835–843. Дои:10.1111 / j.1349-7006.2005.00130.x. PMID 16367902.
- ^ Самарас В., Рафаилидис П.И., Мурцуку Е.Г., Пеппас Г., Фалагас М.Э. (июнь 2010 г.). «Хронические бактериальные и паразитарные инфекции и рак: обзор» (PDF). Журнал инфекций в развивающихся странах. 4 (5): 267–81. Дои:10.3855 / jidc.819. PMID 20539059.
- ^ Мустакки, Пьеро (2000). Паразиты. BC Decker.
- ^ Pallis AG, Syrigos KN (декабрь 2013 г.). «Рак легкого у никогда не куривших: характеристики заболевания и факторы риска». Критические обзоры в онкологии / гематологии. 88 (3): 494–503. Дои:10.1016 / j.critrevonc.2013.06.011. PMID 23921082.
- ^ Танигучи К., Карин М. (февраль 2014 г.). «IL-6 и родственные цитокины как решающие связующие звенья между воспалением и раком». Семинары по иммунологии. 26 (1): 54–74. Дои:10.1016 / j.smim.2014.01.001. PMID 24552665.
- ^ Колотта Ф, Аллавена П., Сика А., Гарланда С., Мантовани А. (июль 2009 г.). «Воспаление, связанное с раком, седьмой признак рака: связь с генетической нестабильностью». Канцерогенез. 30 (7): 1073–81. Дои:10.1093 / carcin / bgp127. PMID 19468060.
- ^ Мантовани А (июнь 2010 г.). «Молекулярные пути, связывающие воспаление и рак». Современная молекулярная медицина. 10 (4): 369–73. Дои:10.2174/156652410791316968. PMID 20455855.
- ^ а б c d е ж грамм час я j k л Маленький JB (2000). «Глава 14: Ионизирующее излучение». В Kufe DW, Pollock RE, Weichselbaum RR, Bast RC, Gansler TS, Holland JF, Frei E (eds.). Противораковая медицина (6-е изд.). Гамильтон, Онтарио: Британская Колумбия Декер. ISBN 978-1-55009-113-7.
- ^ "IARC classifies radiofrequency electromagnetic fields as possibly carcinogenic to humans" (PDF). Всемирная организация здоровья.
- ^ "IARC Monographs- Classifications". monographs.iarc.fr. Архивировано из оригинал на 2017-06-10. Получено 2018-03-13.
- ^ "Cell Phones and Cancer Risk - National Cancer Institute". Cancer.gov. 2013-05-08. Получено 2013-12-15.
- ^ а б Cleaver JE, Mitchell DL (2000). "15. Ultraviolet Radiation Carcinogenesis". In Bast RC, Kufe DW, Pollock RE, et al. (ред.). Holland-Frei Cancer Medicine (5-е изд.). Hamilton, Ontario: B.C. Декер. ISBN 978-1-55009-113-7. Получено 31 января 2011.
- ^ Yamanaka R, Hayano A, Kanayama T (January 2017). "Radiation-Induced Meningiomas: An Exhaustive Review of the Literature". Мировая нейрохирургия. 97: 635–644.e8. Дои:10.1016/j.wneu.2016.09.094. PMID 27713063.
- ^ Brenner DJ, Hall EJ (November 2007). "Computed tomography--an increasing source of radiation exposure". Медицинский журнал Новой Англии. 357 (22): 2277–84. Дои:10.1056/NEJMra072149. PMID 18046031.
- ^ Dingli D, Nowak MA (September 2006). «Биология рака: инфекционные опухолевые клетки». Природа. 443 (7107): 35–6. Bibcode:2006Natur.443...35D. Дои:10.1038 / 443035a. ЧВК 2711443. PMID 16957717.
- ^ Barozzi P, Luppi M, Facchetti F, Mecucci C, Alù M, Sarid R, Rasini V, Ravazzini L, Rossi E, Festa S, Crescenzi B, Wolf DG, Schulz TF, Torelli G (May 2003). "Post-transplant Kaposi sarcoma originates from the seeding of donor-derived progenitors". Природа Медицина. 9 (5): 554–61. Дои:10.1038/nm862. PMID 12692543.
- ^ а б c d е ж Gaeta JF (2000). "Chapter 17: Trauma and Inflammation". In Bast RC, Kufe DW, Pollock RE, et al. (ред.). Holland-Frei Cancer Medicine (5-е изд.). Hamilton, Ontario: B.C. Декер. ISBN 978-1-55009-113-7. Получено 27 января 2011.
- ^ а б Tolar J, Neglia JP (June 2003). "Transplacental and other routes of cancer transmission between individuals". Журнал детской гематологии / онкологии. 25 (6): 430–4. Дои:10.1097/00043426-200306000-00002. PMID 12794519.
