Крымско-Конго геморрагическая лихорадка - Crimean–Congo hemorrhagic fever
| Крымско-Конго геморрагическая лихорадка | |
|---|---|
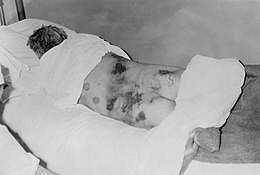 | |
| Мужчина с диагнозом Крымско-Конго геморрагическая лихорадка, 1969 г. | |
| Специальность | Инфекционное заболевание |
| Симптомы | Высокая температура, мышечные боли, Головная боль, рвота, понос, кровотечение в кожу[1] |
| Осложнения | Печеночная недостаточность[1] |
| Обычное начало | Быстрый[1] |
| Продолжительность | Две недели[1] |
| Диагностический метод | Обнаружение антитела, вирус РНК, или сам вирус[1] |
| Дифференциальный диагноз | Лихорадка денге, Ку-лихорадка,[2] Болезнь, вызванная вирусом Эбола[3] |
| лечение | Поддерживающая терапия, рибавирин[1] |
| Прогноз | Риск смерти ~ 25%[1] |
Крымско-Конго геморрагическая лихорадка (CCHF) это вирусное заболевание.[1] Симптомы CCHF могут включать: высокая температура, мышечные боли, Головная боль, рвота, понос, и кровотечение в кожу.[1] Симптомы появляются менее чем через две недели после заражения.[1] Осложнения могут включать: печеночная недостаточность.[1] У тех, кто выжил, выздоровление обычно происходит примерно через две недели после начала болезни.[1]
Вирус CCHF обычно распространяется поставить галочку укусы или контакт с домашний скот переносчик болезни.[1] К группам повышенного риска заражения относятся: фермеры и те, кто работает в бойни.[1] Вирус также может передаваться между людьми через телесные жидкости.[1] Диагноз ставится путем обнаружения антитела, вирус РНК, или сам вирус.[1] Это тип вирусная геморрагическая лихорадка.[1]
Профилактика предполагает избегание укусов клещей.[1] А вакцина не имеется в продаже.[1] Лечение обычно с поддерживающая терапия.[1] Лекарство рибавирин также может помочь.[1]
Это происходит в Африке, Балканы, Ближний Восток и Азия.[1] Часто это происходит в вспышки.[1] В 2013 Иран, Россия, индюк, и Узбекистан задокументировано более пятидесяти случаев.[2] Риск смерти среди пострадавших составляет от 10 до 40%.[1] Впервые он был обнаружен в 1940-х годах.[4]
Признаки и симптомы
Заболевание у человека - тяжелая форма геморрагическая лихорадка.[5] Обычно через 1–3 дня период инкубации после укуса клеща или через 5-6 дней после контакта с инфицированной кровью или тканями, грипп -подобные симптомы, которые могут исчезнуть через неделю.[нужна цитата ] До 75% случаев признаки кровотечение могут появиться в течение 3–5 дней от начала болезни при плохом сдерживании первых симптомов: нестабильность настроения, волнение, умственное замешательство и горло петехии; и вскоре после носового кровотечения, рвоты и черного стула. В печень становится опухшим и болезненным. Диссеминированное внутрисосудистое свертывание может возникнуть, а также острая почечная недостаточность, шок, и иногда острый респираторный дистресс-синдром.[нужна цитата ] Обычно люди начинают выздоравливать через 9–10 дней после появления первых симптомов. К концу второй недели болезни умирают до 30% инфицированных.[нужна цитата ]
Причина
Вирусология
| Ортонаировирус крымско-конголезской геморрагической лихорадки | |
|---|---|
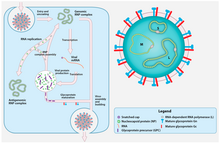 | |
| Вирион и цикл репликации вируса Крымско-Конго геморрагической лихорадки (CCHFV). | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Царство: | Рибовирия |
| Королевство: | Орторнавиры |
| Тип: | Негарнавирикота |
| Класс: | Ellioviricetes |
| Порядок: | Буньявиралес |
| Семья: | Nairoviridae |
| Род: | Ортонаировирус |
| Виды: | Ортонаировирус крымско-конголезской геморрагической лихорадки |
В Ортонаировирус Крымско-Конго геморрагической лихорадки (CCHFV) является представителем рода Ортонаировирус, семья Nairoviridae из РНК-вирусы.[6]
Вирионы 80–120 нанометры (нм) в диаметре и равны плеоморфный. В вирионе нет рибосом-хозяев. Каждый вирион содержит три копии генома. Оболочка является однослойной и образована из липидного бислоя толщиной 5 нм. Не имеет выступов. Белки оболочки образуют небольшие выступы длиной ~ 5–10 нм. Нуклеокапсиды нитевидные, круглые, длиной 200–3000 нм.[7]Вирус может проникнуть в клетку, используя белок клеточной поверхности. нуклеолин.[8]
Молекулярная биология
Геном круговой, отрицательный смысл РНК в трех частях - Маленькая (S), Средняя (M) и Большая (L). Сегмент L имеет длину 11–14,4 килобаз, а сегменты M и S - 4,4–6,3 и 1,7–2,1 килобаз соответственно. Сегмент L кодирует РНК-полимераза, сегмент M кодирует конверт гликопротеины (Gc и Gn), а сегмент S кодирует белок нуклеокапсида.[7] Частота мутаций для трех частей генома оценивалась как 1,09×10−4, 1.52×10−4 и 0,58×10−4 замен / участок / год для сегментов S, M и L.[9]
Популяционная генетика
CCHFV является наиболее генетически разнообразным из арбовирусы: Его нуклеотидные последовательности часто различаются между разными штаммами, от 20% вариабельности для вирусного S-сегмента до 31% для M-сегмента.[10] Вирусы с разными последовательностями можно найти в одном географическом районе; близкородственные вирусы были изолированы из широко разнесенных регионов, что позволяет предположить, что распространение вируса произошло, возможно, от клещей, переносимых перелетными птицами или в результате международной торговли домашним скотом. Перегруппировка сегментов генома во время коинфекция клещей или позвоночных, вероятно, сыграли роль в создании разнообразия этого вируса.[нужна цитата ]
На основании данных о последовательностях было выделено семь генотипов CCHFV: Африка 1 (Сенегал ), Африка 2 (Демократическая Республика Конго и Южная Африка), Африка 3 (юг и запад Африки), Европа 1 (Албания, Болгария, Косово, Россия и индюк ), Европа 2 (Греция ), Азия 1 (средний Восток, Иран и Пакистан ) и Азия 2 (Китай, Казахстан, Таджикистан и Узбекистан ).[нужна цитата ]
Передача инфекции

Клещи одновременно являются «резервуаром окружающей среды» и вектор для вируса, переносящего его от диких животных к домашним животным и людям. Виды клещей, идентифицированные как инфицированные вирусом, включают: Рефлекс аргаса, Гиаломма анатолическая, Детрит гиаломмы, Hyalomma marginatum marginatum и Rhipicephalus sanguineus.[нужна цитата ]Не менее 31 вида клещей из этих родов Гемафизалис и Гиаломма на юго-востоке Ирана был обнаружен переносчик вируса.[11]
Дикие животные и мелкие млекопитающие, особенно Европейский заяц, Среднеафриканский ежики и многокорпусные крысы являются «усиливающими хозяевами» вируса. Птицы в целом устойчивы к CCHF, за исключением страусы. Домашние животные, такие как овцы, козы и крупный рогатый скот, могут вырабатывать высокие титры вируса в крови, но не заболевают.[12]
«Спорадическая инфекция» человека обычно вызывается Гиаломма укус клеща. Животные могут передавать вирус людям, но обычно это является частью кластера болезней. Когда возникают кластеры болезни, это обычно происходит после того, как люди вылечили, разделали или съели зараженный скот, особенно жвачные животные и страусы. Вспышки произошли в скотобойни а также в других местах, где рабочие подвергались воздействию инфицированной крови человека или животных и фомиты[нужна цитата ] Люди могут заразить людей, и вспышки болезни также происходят в медицинских учреждениях через зараженную кровь и нечистые медицинские инструменты.[13]
Профилактика
Там, где инфекция клещами млекопитающих является обычным явлением, сельскохозяйственные правила требуют снимать клещи с сельскохозяйственных животных перед транспортировкой или доставкой на убой. Рекомендуются индивидуальные меры по предотвращению клещей, такие как использование репеллентов от насекомых, соответствующая одежда и осмотр тела на предмет прилипших клещей.[нужна цитата ]
Когда лихорадочный пациентам с признаками кровотечения требуется реанимация или интенсивная терапия, выделение вещества тела следует принять меры предосторожности.[нужна цитата ]
Вакцина
С 1970-х годов несколько испытаний вакцины против CCHF по всему миру были прекращены из-за высокой токсичности.[14]
По состоянию на март 2011 г.[Обновить], единственной доступной и, вероятно, отчасти эффективной вакциной CCHF был препарат инактивированного антигена, который затем использовался в Болгарии.[14] В научной литературе нет публикаций, связанных с этой вакциной, которую турецкий вирусолог назвал подозрительной как из-за устаревшей технологии, так и мозг мыши были использованы для его изготовления.[15] В настоящее время разрабатываются новые вакцины, но спорадический характер заболевания даже в эндемичных странах предполагает, что проведение крупных испытаний эффективности вакцины будет затруднено. Поиск волонтеров может оказаться сложной задачей, учитывая рост антивакцинация настроения и устойчивость населения к вакцинации против заразных болезней. Необходимо тщательно определить количество людей, которые будут вакцинированы, и продолжительность наблюдения за ними для подтверждения защиты. С другой стороны, многие ученые полагают, что лечение CCHF с помощью рибавирин является более практичным, чем профилактика, но некоторые недавно проведенные клинические испытания, похоже, опровергают предположения об эффективности препарата.[14]В 2011 г. турецкий исследовательская группа во главе с Университет Эрджиес успешно разработала первую нетоксичную профилактическую вакцину, прошедшую клинические испытания. По состоянию на 2012 год вакцина ожидала одобрения FDA США.[15]
После эпидемии лихорадки Эбола ВОЗ приступила к реализации «Программы обеспечения готовности к исследованиям и разработкам». новые патогены с эпидемическим потенциалом, против которого нет лекарств.[16] CCHF был главным приоритетом в первоначальном списке с декабря 2015 года и вторым по состоянию на январь 2017 года.[17]
лечение
Лечение в основном поддерживающий. Рибавирин эффективен in vitro[18] и использовался внутрь во время вспышек заболеваний,[нужна цитата ] но есть неуверенные доказательства в поддержку его использования.[19]
По состоянию на 2011 г.[Обновить] использование Иммуноглобулин препараты остались недоказанными, а инженерия антител, которая вселила надежды на моноклональное антитело терапия, осталась в зачаточном состоянии.[14]
В вооруженных силах США есть специальные запасы рибавирин для защиты персонала, развернутого в Афганистан и Ирак от CCHF.[нужна цитата ]
Эпидемиология
CCHD чаще всего возникает среди сельскохозяйственных рабочих после укуса инфицированного клеща и в меньшей степени среди рабочих бойни, подвергшихся воздействию крови и тканей инфицированного домашнего скота, а также медицинского персонала при контакте с жидкостями организма инфицированных людей.[10]
Географическое распространение
По состоянию на 2013 год[Обновить] северная граница CCHF была 50 градусов северной широты, к северу от которой Гиаломма клещей не обнаружено.[5]Согласно карте ВОЗ от 2008 года, клещи Hyalomma встречались к югу от этой широты на всем евразийском континенте и в Африке, за исключением островов Шри-Ланки, Индонезии и Японии.[20] Серологические или вирусологические доказательства CCHF были широко распространены в Азии, Восточной Европе, на Ближнем Востоке (кроме Израиля, Ливана и Иордании), в Центральной Африке, Западной Африке, Южной Африке и на Мадагаскаре.[20]
В 2008 г. регистрировалось более 50 случаев в год только из 4 стран: Турции, Ирана, России и Узбекистана. 5-49 случаев в год присутствовали в Южной Африке, Центральной Азии, включая Пакистан и Афганистан (но за исключением Туркменистана), на Ближнем Востоке только в ОАЭ и балканских странах, ограниченных Румынией, Болгарией, Сербией, Черногорией и Косово-Албанией.[20]
На карте 2014 года, составленной CDC, эндемичные районы (красным цветом) в Африке и на Ближнем Востоке практически не изменились, но разные для Балкан, включая все страны бывшей Югославии, а также Грецию, но уже не Румынию. Первые случаи заболевания зафиксированы в северо-западных регионах Индии, Раджастане и Гуджарате.[21]
Вспышки
С 1995 по 2013 год в Республике Косово было зарегистрировано 228 случаев CCHF с летальностью 25,5%.[22]
В период с 2002 по 2008 год Министерство здравоохранения Турции сообщило о 3 128 случаях CCHF, при 5% смертности.[нужна цитата ] В июле 2005 г. власти сообщили о 41 случае CCHF в центральной части Турции. Провинция Йозгат, с одной смертью.[требуется разъяснение ] По состоянию на август 2008 года, всего за год было зарегистрировано 50 смертей в различных городах Турции из-за CCHF.[требуется разъяснение ]
В сентябре 2010 г. сообщалось о вспышке болезни в Пакистане. Хайбер-Пахтунхва провинция. Плохая диагностика и ведение записей привели к неопределенности масштабов вспышки, хотя в некоторых отчетах указано более 100 случаев с летальным исходом более 10%.[нужна цитата ]
В январе 2011 г. первые случаи заболевания людей CCHF в Индии были зарегистрированы в Сананд, Гуджарат, Индия, с 4 зарегистрированными смертельными случаями, в том числе индексный пациент, лечащий врач и медсестра.[23]
По состоянию на май 2012 г.[Обновить]Сообщается, что в Иране этим заболеванием заразился 71 человек, в результате чего 8 человек погибли.[24]
В октябре 2012 года британец умер от болезни в Королевская бесплатная больница В Лондоне. Ранее он был помещен в Больница общего профиля Гартнавел в Глазго, после возвращения рейсом из Кабул в Афганистан.[25]
В июле 2013 года в селе Карияна в Бабре из-за КГЗ погибли семь человек. Taluka, Амрелиский район, Гуджарат, Индия.[26][27]
В августе 2013 г. фермер из г. Агаго, Уганда лечилась в Больница Калонго для подтвержденной инфекции CCHF. Смерть трех других лиц в северный регион предположительно были вызваны вирусом.[28] Другой неродственный пациент с CCHF поступил в Госпиталь Мулаго в тот же день. В Министерство здравоохранения объявили 19-го, что вспышка находится под контролем, но второй пациент, 27-летняя женщина из Нансана умер 21-го числа. Считается, что она заразилась вирусом от своего мужа, который вернулся в Кампалу после лечения от CCHF в Джуба, южный Судан.[29]
В июне 2014 года случаи были диагностированы в Казахстане. Десять человек, включая бригаду скорой помощи, были госпитализированы в больницу на юге Казахстана с подозрением на ЗДН.[нужна цитата ] В июле 2014 года в медицинском комплексе Хаятабад (HMC), Пакистан, был обнаружен 8-й человек, инфицированный CCHF. Восемь пациентов, включая медсестру и 6 граждан Афганистана, умерли в период с апреля по июль 2014 года.[30]
По состоянию на 2015 год[Обновить], зарегистрированы единичные подтвержденные случаи из Бхудж, Амрели, Сананд, Идар и Ваднагар в Гуджарате, Индия. В ноябре 2014 года у врача и рабочего в северном Гуджарате результат теста на болезнь оказался положительным. В последующие недели еще три человека умерли от CCHF.[31] В марте 2015 года в Гуджарате от CCHF умер еще один человек.[32]По состоянию на 2015 год среди домашнего скота CCHF был признан «широко распространенным» в Индии, всего через 4 года после того, как был диагностирован первый случай заболевания человека.[33]
В августе 2016 года первый локальный случай CCHF в Западной Европе произошел в Западной Испании. 62-летний мужчина, укушенный клещом в Испании, умер 25 августа, заразив медсестру.[34] Укус клеща произошел в провинция Авила, 300 км от г. провинция Касерес, где вирусная РНК CCHF от клещей была амплифицирована в 2010 г.[35]По состоянию на июль 2017 г.[Обновить] неясно, какая именно экология привела к испанским случаям.[36]
В августе 2016 года ряд пакистанских источников новостей выразил обеспокоенность по поводу болезни.[37][38] В период с января по октябрь 2016 г. в Пакистане были зарегистрированы вспышки CCHF с наибольшим числом случаев заболевания и смертей в августе 2016 г., незадолго до фестиваля Ид-аль-Адха (13–15 сентября 2016 г.). Было высказано предположение, что фестиваль может сыграть важную роль, поскольку люди могут контактировать с домашними или импортированными животными, потенциально инфицированными вирусом CCHF.[39] Пакистанский NIH показал, что корреляции нет, и что случаи CCHF совпадали с пиком распространения клещей в течение предшествующих 8–10 лет.[40]
5 февраля 2020 года произошла вспышка заболевания в центральном районе Мали. Зараженные - из регионов Дуэнца и Мопти. На данный момент умерло 7 человек.[41][нуждается в обновлении ]
История
Вирус мог появиться примерно в 1500–1100 годах до нашей эры. Считается, что изменение климата и методов ведения сельского хозяйства примерно в это время могло быть причиной его эволюции.[9]
В XII веке был зарегистрирован случай геморрагической болезни из современной Таджикистан возможно, был первым известным случаем Крымско-Конго геморрагической лихорадки.[нужна цитата ] В течение Крымская война, болезнь была известна как «крымская лихорадка» и заразилась многими, в том числе Флоренс Найтингейл.[42]
В 1944 году советские ученые впервые идентифицировали болезнь, которую они назвали Крымской геморрагической лихорадкой. Крым.[43] Они установили его вирусную этиологию, но в то время не смогли выделить возбудителя.
В феврале 1967 г. вирусологи Джон П. Вудалл, Дэвид Симпсон, Гислен Куртуа и другие опубликовали первые отчеты о вирусе, который они назвали вирусом Конго.[44][45] В 1956 году вирус Конго был впервые выделен врачом Гислен Куртуа, руководителем провинциальной медицинской лаборатории. Stanleyville, в Бельгийское Конго. Штамм V3010, выделенный Куртуа, был отправлен в Фонд Рокфеллера Вирусная лаборатория (RFVL) в Нью-Йорке, который был идентичен другому штамму из Уганда, но ни одному другому вирусу в то время.[нужна цитата ]
В июне 1967 г. советский вирусолог. Михаил Чумаков зарегистрировал изолят от смертельного случая, произошедшего в Самарканд в Каталоге вирусов, переносимых членистоногими.[46]В 1969 году было опубликовано, что российский штамм, который Чумаков отправил в RFVL, идентичен вирусу Конго.[47]
В 1973 г. Международный комитет по таксономии вирусов принял Вирус Крымско-Конго геморрагической лихорадки как официальное название.[48]
Эти отчеты включают записи о появлении вируса или антител к вирусу из Греции, Португалии, Южной Африки, Мадагаскар (первая изоляция оттуда), Магриб, Дубай, Саудовская Аравия, Кувейт и Ирак.[49][50][51]
использованная литература
- ^ а б c d е ж г час я j k л м п о п q р s т ты v ш Икс «Крымско-Конго геморрагическая лихорадка». Всемирная организация здоровья. Январь 2013. В архиве из оригинала 13 июля 2017 г.. Получено 18 июля 2017.
- ^ а б Бергер С (2017). Крымско-Конго геморрагическая лихорадка: глобальный статус: издание 2017 г.. GIDEON Informatics Inc. стр. 7. ISBN 9781498815567. В архиве из оригинала от 10.09.2017.
- ^ «Инфекция, вызванная вирусом Эбола - Отличия | Лучшая практика BMJ». bestpractice.bmj.com. Получено 21 мая 2018.
- ^ Мэджилл Эй Джей (2013). Hunter's Tropical Medicine и Emerging Infectious Disease, Expert Consult - Online and Print, 9: Hunter's Tropical Medicine and Emerging Infectious Disease.. Elsevier Health Sciences. п. 334. ISBN 978-1416043904. В архиве из оригинала от 04.08.2017.
- ^ а б «Крымско-Конго геморрагическая лихорадка, Информационный бюллетень № 208». КТО. Январь 2013. В архиве из оригинала на 2015-05-20. Получено 2015-05-19.
- ^ Таксономия вирусов: выпуск 2018 г., EC 50, Вашингтон, округ Колумбия, июль 2018 г., ратификация электронной почты, октябрь 2018 г. (MSL № 33) https://talk.ictvonline.org/taxonomy/
- ^ а б Картер С.Д., Сёртиз Р., Уолтер С.Т., Ариза А., Бержерон Э., Никол С.Т. и др. (Октябрь 2012 г.). «Структура, функция и эволюция нуклеокапсидного белка вируса Крымско-Конго геморрагической лихорадки». Журнал вирусологии. 86 (20): 10914–23. Дои:10.1128 / JVI.01555-12. ЧВК 3457148. PMID 22875964.
- ^ Сяо Х, Фэн Й, Чжу З., Димитров Д.С. (июль 2011 г.). «Выявление предполагаемого фактора проникновения вируса Крымско-Конго геморрагической лихорадки». Сообщения о биохимических и биофизических исследованиях. 411 (2): 253–8. Дои:10.1016 / j.bbrc.2011.06.109. ЧВК 3155881. PMID 21723257.
- ^ а б Кэрролл С.А., Берд Б.Х., Роллин П.Е., Никол С.Т. (июнь 2010 г.). «Древние общие предки вируса Крымско-Конго геморрагической лихорадки». Молекулярная филогенетика и эволюция. 55 (3): 1103–10. Дои:10.1016 / j.ympev.2010.01.006. PMID 20074652.
- ^ а б Бенте Д.А., Форрестер Н.Л., Уоттс Д.М., Маколи А.Дж., Уайтхаус, Калифорния, Брей М. (октябрь 2013 г.). «Крымско-Конго геморрагическая лихорадка: история, эпидемиология, патогенез, клинический синдром и генетическое разнообразие». Противовирусные исследования. 100 (1): 159–89. Дои:10.1016 / j.antiviral.2013.07.006. PMID 23906741.
- ^ Мехраваран А., Моради М., Телмадаррай З., Мостафави Е., Моради А.Р., Хакифируз С. и др. (Февраль 2013). «Молекулярное обнаружение вируса Крымско-Конго геморрагической лихорадки (ККГЛ) у клещей из юго-восточного Ирана». Клещи и клещевые болезни. 4 (1–2): 35–8. Дои:10.1016 / j.ttbdis.2012.06.006. PMID 23238248.
- ^ Ergönül O, Celikbaş A, Dokuzoguz B, Eren S, Baykam N, Esener H (июль 2004 г.). «Характеристики пациентов с Крымско-Конго геморрагической лихорадкой во время недавней вспышки в Турции и влияние пероральной терапии рибавирином». Клинические инфекционные болезни. 39 (2): 284–7. Дои:10.1086/422000. PMID 15307042.
- ^ Отдел патогенов и патологий с серьезными последствиями, Отделение специальных вирусных патогенов (5 марта 2014 г.). «Передача Крымско-Конго геморрагической лихорадки (КГЛ)». CDC. В архиве с оригинала от 28 апреля 2014 г.
- ^ а б c d Keshtkar-Jahromi M, Kuhn JH, Christova I., Bradfute SB, Jahrling PB, Bavari S (май 2011 г.). «Крымско-Конго геморрагическая лихорадка: текущие и будущие перспективы вакцин и методов лечения». Противовирусные исследования. 90 (2): 85–92. Дои:10.1016 / j.antiviral.2011.02.010. PMID 21362441.
- ^ а б sitesi, milliyet.com.tr Türkiye'nin lider haber. "Keneye aşı müjdesi". В архиве из оригинала 19.12.2013.
- ^ Киени М (20 мая 2015 г.). «После лихорадки Эбола появляется план для ускорения исследований и разработок». Сеть блогов Scientific American. В архиве из оригинала 20 декабря 2016 г.. Получено 13 декабря 2016.
- ^ "Программа НИОКР. Список приоритетных болезней". Всемирная организация здоровья. Январь 2017 г. В архиве с оригинала 10 сентября 2017 г.. Получено 13 июля 2017.
- ^ Watts DM, Ussery MA, Nash D, Peters CJ (ноябрь 1989 г.). «Ингибирование вирусной инфекционности крымско-конголезской геморрагической лихорадки in vitro с помощью рибавирина». Американский журнал тропической медицины и гигиены. 41 (5): 581–5. Дои:10.4269 / ajtmh.1989.41.581. PMID 2510529.
- ^ Джонсон С., Хеншке Н., Мааян Н., Миллс И., Бакли Б.С., Какуру А., Маршалл Р. и др. (Кокрановская группа по инфекционным заболеваниям) (июнь 2018 г.). «Рибавирин для лечения геморрагической лихорадки Крымское Конго». Кокрановская база данных систематических обзоров. 6: CD012713. Дои:10.1002 / 14651858.CD012713.pub2. ЧВК 5994605. PMID 29869797.
- ^ а б c «Географическое распространение Крымско-Конго геморрагической лихорадки (КГЛ)». КТО. 2008 г. В архиве из оригинала от 13.05.2016.
- ^ Отдел патогенов и патологий с серьезными последствиями, Отделение специальных вирусных патогенов (5 марта 2014 г.). «Карта распространения Крымско-Конго геморрагической лихорадки (КГЛ)». CDC. В архиве с оригинала 18 июня 2017 г.
- ^ Файс Л., Якупи Х, Ахмети С., Хумолли И., Дедушай И., Авшич-Люпанц Т. (2014). «Молекулярная эпидемиология вируса Крымско-Конго геморрагической лихорадки в Косово». PLOS забытые тропические болезни. 8 (1): e2647. Дои:10.1371 / journal.pntd.0002647. ЧВК 3886908. PMID 24416468.
- ^ Сайед Халике Ахмед, Танвир А Сиддики, Анурадха Маскаренхас, Анурадха Маскаренхас, Танвир А Сиддики, Сайед Халике Ахмед: Пуна, Ахмадабад Смертельный вирус, впервые появившийся в Индии, убил троих в Гуджарате В архиве 2011-03-04 на Wayback Machine indianexpress.com, 19 января 2011 г.
- ^ «Архивная копия». Архивировано из оригинал на 2016-03-05. Получено 2012-05-19.CS1 maint: заархивированная копия как заголовок (ссылка на сайт)
- ^ «Лихорадка Конго: пациент умирает в больнице». Новости BBC. 6 октября 2012 г. В архиве из оригинала 7 октября 2012 г.
- ^ "Конго лихорадка: семь человек умирают в Амрели за неделю для мобильного сайта". IndiaTv. Indiatvnews. 2013-07-15. В архиве из оригинала от 04.03.2016. Получено 2015-03-28.
- ^ «Подтверждена лихорадка Конго в деревне Амрели». Времена Индии.
- ^ Бирябарема Э (17 августа 2013 г.). «Трое умирают в Уганде от лихорадки, похожей на Эбола: Министерство здравоохранения». Yahoo News. Рейтер. В архиве из оригинала от 20 августа 2013 г.. Получено 16 августа 2013.
- ^ Отто А. (22 августа 2013 г.). «Особая тревога по поводу крымской лихорадки». Наблюдатель. Кампала. В архиве из оригинала 14 июля 2014 г.. Получено 26 августа 2013.
- ^ Хан Х (2014-07-11). «Исходящие вспышки: Восьмой пациент умер от геморрагической лихорадки Конго в HMC». В архиве из оригинала 13 июля 2014 г.. Получено 13 июля 2014.
- ^ «Представители здравоохранения подтверждают смерть мужчины из Джайсалмера от лихорадки Конго». Мобильный сайт "Таймс оф Индия". 26 января 2015. В архиве из оригинала 2 апреля 2015 г.. Получено 30 марта 2015.
- ^ «Житель Катча умер от лихорадки Конфо». Индийский экспресс. 29 марта 2015 года. В архиве с оригинала 3 апреля 2015 г.. Получено 29 марта, 2015.
- ^ «Крымско-Конго геморрагическая лихорадка распространяется по Индии - Новости вспышки сегодня». 9 октября 2015. В архиве из оригинала от 20 декабря 2015 г.
- ^ «Первый местный случай клещевой болезни убил человека в Испании». Ученый американец. нет данных В архиве из оригинала от 02.09.2016. Получено 2016-09-03.
- ^ Negredo A, de la Calle-Prieto F, Palencia-Herrejón E, Mora-Rillo M, Astray-Mochales J, Sánchez-Seco MP, et al. (Июль 2017 г.). «Автохтонная Крымско-Конго геморрагическая лихорадка в Испании». Медицинский журнал Новой Англии. 377 (2): 154–161. Дои:10.1056 / NEJMoa1615162. PMID 28700843.
- ^ Шпенглер-младший, Бенте Д.А. (июль 2017 г.). «Крымско-Конго геморрагическая лихорадка в Испании - новоприбывшие или молчаливый резидент?». Медицинский журнал Новой Англии. 377 (2): 106–108. Дои:10.1056 / NEJMp1707436. ЧВК 5922251. PMID 28700846.
- ^ «Вирус Конго: врачи предостерегают от вспышки болезни». Экспресс Трибуна. 17 августа 2016 г. В архиве из оригинала от 6 сентября 2016 г.
- ^ «Карачи: вирус Конго уносит еще одну жизнь - Пакистан - Dunya News». В архиве из оригинала от 04.09.2016.
- ^ Карим А.М., Хуссейн И., Ли Дж.Х., Пак К.С., Ли С.Х. (апрель 2017 г.). «Эпиднадзор за Крымско-Конго геморрагической лихорадкой в Пакистане». Ланцет. Инфекционные заболевания. 17 (4): 367–368. Дои:10.1016 / S1473-3099 (17) 30119-6. PMID 28346174.
- ^ Алам М.М., Хуршид А., Рана М.С., Амир У.Б., Салман М., Ахмад М. (август 2017 г.). «Эпиднадзор за Крымско-Конго геморрагической лихорадкой в Пакистане». Ланцет. Инфекционные заболевания. 17 (8): 806. Дои:10.1016 / S1473-3099 (17) 30403-6. PMID 28741546.
- ^ «7 человек погибли в результате вспышки лихорадки в Конго в Мали». medicalxpress.com. Получено 8 февраля 2020.
- ^ Кромвель, Джудит Лиссауэр, Флоренс Найтингейл, феминистка, МакФарланд, 2013 г., стр.149
- ^ «Природная очаговость зоонозных инфекций в Крыму». Мир Животных. В архиве из оригинала от 23.09.2016.
- ^ Симпсон Д.И., Найт Э.М., Куртуа Дж., Уильямс М.С., Вайнбрен МП, Кибукамусоке Дж. У. (февраль 1967 г.). «Вирус Конго: ранее не описанный вирус, встречающийся в Африке. I. Изоляция человека - клинические заметки». Восточноафриканский медицинский журнал. 44 (2): 86–92. PMID 6040759.
- ^ Вудалл Дж. П., Уильямс М.С., Симпсон Д.И. (февраль 1967). «Вирус Конго: еще не описанный вирус, встречающийся в Африке. II. Идентификационные исследования». Восточноафриканский медицинский журнал. 44 (2): 93–8. PMID 6068614.
- ^ Чумаков М.П., Бутенко А.М., Шалунова Н.В., Мартьянова Л.И., Смирнова С.Е., Башкирцев Ю.В. и др. (Май – июнь 1968 г.). «[Новые данные о вирусном возбудителе Крымской геморрагической лихорадки]». Вопросы вирусологии (по-русски). 13 (3): 377. PMID 4235803.
- ^ Casals J (май 1969). «Антигенное сходство вируса, вызывающего Крымскую геморрагическую лихорадку, и вируса Конго». Труды Общества экспериментальной биологии и медицины. 131 (1): 233–6. Дои:10.3181/00379727-131-33847. PMID 5770109. S2CID 30654789.
- ^ Ergönül O, Whitehouse CA (2007). «Личные размышления, Джек Вудол». Геморрагическая лихорадка Конго: глобальная перспектива. Нидерланды: Спрингер. п.23. ISBN 978-1-4020-6105-9.
- ^ Кроукрофт Н.С., Морган Д., Браун Д. (март 2002 г.). «Вирусные геморрагические лихорадки в Европе - эффективный контроль требует скоординированных действий». Европейское наблюдение. 7 (3): 31–2. Дои:10.2807 / esm.07.03.00343-ru. PMID 12631941.
- ^ Аль-Тикрити С.К., Аль-Ани Ф., Джурджи Ф.Дж., Тантави Х., Аль-Мослих М., Аль-Джанаби Н. и др. (1981). «Конго / Крымская геморрагическая лихорадка в Ираке». Бюллетень Всемирной организации здравоохранения. 59 (1): 85–90. ЧВК 2396030. PMID 6790183.
- ^ Окорие Т.Г. (март 1991 г.). «Сравнительные исследования переносчиков различных стадий Amblyomma variegatum Fabricius и Hyalomma rufipes Koch в отношении вируса Конго после внутрицеломной инокуляции». Ветеринарная паразитология. 38 (2–3): 215–23. Дои:10.1016 / 0304-4017 (91) 90131-э. PMID 1907050.
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |
- Ergönül O (апрель 2006 г.). «Крымско-Конго геморрагическая лихорадка». Ланцет. Инфекционные заболевания. 6 (4): 203–14. Дои:10.1016 / S1473-3099 (06) 70435-2. ЧВК 7185836. PMID 16554245.
- Информационный бюллетень Всемирной организации здравоохранения
