Общая анестезия - General anaesthesia
Эта статья нужны дополнительные цитаты для проверка. (Февраль 2015 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
| Общая анестезия | |
|---|---|
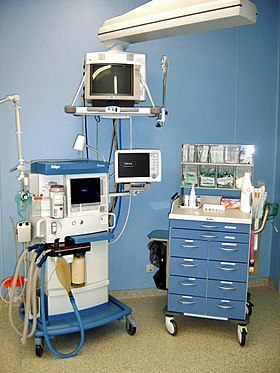 Оборудование, используемое для анестезии в операционной | |
| MeSH | D000768 |
| MedlinePlus | 007410 |
Общая анестезия или же Общая анестезия (видеть орфографические различия ) - это медицинская кома с потерей защитных рефлексы в результате введения одного или нескольких общих анестетиков. Он проводится для того, чтобы позволить медицинские процедуры, которые в противном случае были бы для пациента невыносимо болезненными; или если характер самой процедуры не позволяет пациенту бодрствовать.
Разнообразие наркотики могут управляться с общей целью обеспечения бессознательное состояние, амнезия, обезболивание, потеря рефлексов автономная нервная система, а в некоторых случаях паралич из скелетные мышцы. Оптимальную комбинацию лекарств для каждого конкретного пациента и процедуры обычно выбирает специалист. анестезиолог или другой поставщик, например практикующий врач операционного отделения, практикующий анестезиолог, аспирант или же медсестра-анестезиолог (в зависимости от местной практики) после консультации с пациентом и хирургом, стоматологом или другим практикующим врачом, выполняющим оперативную процедуру.
История
Попытки создать состояние общей анестезии можно проследить на протяжении всей записанной истории в трудах древних Шумеры, Вавилоняне, Ассирийцы, Египтяне, Греки, Римляне, Индейцы, и Китайский. Вовремя Средний возраст, ученые и другие ученые добились значительных успехов в Восточный мир, в то время как их европейские коллеги также добились важных успехов.
В эпоха Возрождения увидел значительный прогресс в анатомия и хирургическая техника. Однако, несмотря на весь этот прогресс, операция оставалась последней инстанцией. Во многом из-за связанных боль, многие пациенты предпочли верную смерть, нежели операцию. Хотя было много споров о том, кто заслуживает наибольшей признательности за открытие общей анестезии, несколько научных открытий в конце 18-го и начале 19-го веков сыграли решающую роль в конечном внедрении и развитии современных методов анестезии.
В конце 19 века произошли два огромных скачка, которые вместе позволили перейти к современной хирургии. Признание микробная теория болезни быстро привели к развитию и применению антисептик техники в хирургии. Антисептика, которая вскоре уступила место асептика, снизил общий болезненность и смертность хирургических операций с гораздо более приемлемой скоростью, чем в предыдущие эпохи. Одновременно с этим произошел значительный прогресс в фармакология и физиология что привело к развитию общей анестезии и купированию боли. 14 ноября 1804 г. Ханаока Сейшу Японский врач стал первым, кто успешно провел операцию под общим наркозом.
В 20 веке безопасность и эффективность общей анестезии повысились за счет рутинного использования интубация трахеи и другие продвинутые управление дыхательными путями техники. Значительный прогресс в мониторинг и новые анестетики с улучшенным фармакокинетический и фармакодинамический характеристики также способствовали этой тенденции. Наконец, стандартизированные программы обучения анестезиологов и медсестры-анестезиологи возник в этот период.
Цель
Общая анестезия имеет множество целей, в том числе:
- Бессознательное состояние (потеря сознания)
- Анальгезия (потеря реакции на боль)
- Амнезия (потеря памяти)
- Неподвижность (потеря двигательных рефлексов)
- Паралич (расслабление скелетных мышц и нормальное расслабление мышц)
Общая анестезия не должна использоваться в качестве профилактики у пациентов с анафилаксией, вызванной контрастным веществом.[1]
Биохимический механизм действия
В биохимический механизм действия общих анестетиков не совсем понятно[2][нужна цитата ]. Теории должны объяснять функцию анестезии у животных и растений.[3] Чтобы вызвать бессознательное состояние, анестетики имеют множество участков действия и влияют на Центральная нервная система (ЦНС) на нескольких уровнях. Общие области центральной нервной системы, функции которых прерываются или изменяются во время общей анестезии, включают кора головного мозга, таламус, ретикулярная активирующая система, и спинной мозг. Современные теории анестезированного состояния идентифицируют не только целевые участки в ЦНС, но также нейронные сети и петли, прерывание которых связано с бессознательным состоянием.[4] Потенциальные фармакологические мишени общих анестетиков: ГАМК, глутамат рецепторы, потенциалзависимые ионные каналы, и глицин и серотонин рецепторы.
Галотан было обнаружено, что это ГАМК агонист,[5] и кетамин является Антагонист рецептора NMDA.[6]
Преанестетическая оценка
Перед запланированной процедурой анестезиолог просматривает медицинские записи и / или беседует с пациентом, чтобы определить наилучшее сочетание лекарств и дозировок, а также степень, в которой мониторинг потребуется для обеспечения безопасной и эффективной процедуры. Ключевые факторы в этой оценке - возраст пациента, индекс массы тела, медицинский и хирургический анамнез, текущие лекарства и время голодания.[7][8] Тщательный и точный ответ на вопросы важен, чтобы анестезиолог мог выбрать правильные препараты и процедуры. Например, пациенту, который употребляет значительное количество алкоголь или же запрещенные наркотики могут получить недостаточное лечение, если они не раскроют этот факт, и это может привести к осведомленность об анестезии или во время операции гипертония.[9][10] Обычно используемые лекарства могут взаимодействовать с анестетиками, и отказ от раскрытия информации об их использовании может увеличить риск для пациента.
Важным аспектом предварительной анестезиологической оценки является оценка состояния пациента. дыхательные пути, включающий осмотр ротовой полости и визуализацию мягких тканей глотка.[11] Состояние зубов и расположение зубные коронки проверяются, гибкость шеи и разгибание головы.[12][13]
Премедикация
Перед введением общего анестетика анестезиолог может ввести одно или несколько препаратов, которые дополняют или улучшают качество или безопасность анестетика.
Одна из часто используемых премедикаций - это клонидин, альфа-2-адренергический агонист.[14][15] Премедикация клонидином снижает потребность в средствах для индукции анестезии, в летучих средствах для поддержания общей анестезии и в послеоперационных анальгетиках.[нужна цитата ] Он также уменьшает послеоперационную дрожь, послеоперационная тошнота и рвота, и появление бред.[нужна цитата ] У детей премедикация клонидином не менее эффективна, чем бензодиазепины и имеет менее серьезные побочные эффекты.[нужна цитата ] Однако для полного эффекта перорального клонидина может потребоваться до 45 минут.[16] и недостатки включают гипотония и брадикардия.[нужна цитата ]
Мидазолам, бензодиазепин, характеризующийся быстрым началом и короткой продолжительностью действия, эффективен для снижения предоперационная тревога, включая тревога разлуки у детей.[17] Дексмедетомидин и некоторые атипичный антипсихотик агенты могут использоваться у детей, не склонных к сотрудничеству.[18]
Мелатонин был признан эффективным в качестве премедикации анестезией как у взрослых, так и у детей из-за его гипнотический, анксиолитик, успокаивающее, антиноцицептивный, и противосудорожное средство характеристики. В отличие от мидазолама, мелатонин не ухудшает психомоторные навыки или мешают выздоровлению. Восстановление происходит быстрее после премедикации мелатонином, чем после мидазолама, а также снижается частота послеоперационных осложнений. волнение и бред.[19] Премедикация мелатонином также снижает необходимую индукционную дозу пропофол и тиопентал натрия.[19]
Другой пример премедикации анестетиком - это предоперационное введение бета-адренергические антагонисты снизить частоту послеоперационных гипертония, сердечная аритмия, или же инфаркт миокарда.[нужна цитата ] Анестезиологи могут назначить противорвотное средство агент, такой как ондансетрон, дроперидол, или же дексаметазон для предотвращения послеоперационной тошноты и рвоты,[нужна цитата ] или подкожно гепарин или же эноксапарин снизить частоту глубокие венозные тромбы.[нужна цитата ] Другие широко используемые средства премедикации включают: опиоиды Такие как фентанил или же суфентанил, гастрокинетический такие агенты, как метоклопрамид, и антагонисты гистамина Такие как фамотидин.
Немедикаментозные преанестезиологические вмешательства включают воспроизведение расслабляющей музыки, массаж, а также снижение уровня окружающего света и шума, чтобы поддерживать цикл сна-бодрствования.[20] Эти методы особенно полезны для детей и пациентов с ограниченными интеллектуальными возможностями. Сведение к минимуму сенсорной стимуляции или отвлечения видеоиграми может помочь уменьшить беспокойство до или во время введения общей анестезии. Необходимы более масштабные высококачественные исследования, чтобы подтвердить наиболее эффективные нефармакологические подходы к снижению этого типа беспокойства.[21] Не показано, что присутствие родителей во время премедикации и индукции анестезии снижает тревожность у детей.[21] Рекомендуется, чтобы родителей, желающих присутствовать, не отговаривали, а родителей, которые предпочитают не присутствовать, не следует активно поощрять к посещению.[21]
Этапы анестезии
Классификация Геделя, представлен Артур Эрнест Гедель в 1937 г.,[22] описывает четыре этапа анестезии. Несмотря на появление новых анестетиков и методов доставки, которые привели к более быстрому наступлению анестезии и восстановлению после нее (в некоторых случаях полностью обходя некоторые стадии), принципы остаются.
- Этап 1
- Этап 1, также известный как индукция, это период между введением индукционных агентов и потерей сознания. На этом этапе пациент переходит от обезболивания без амнезии к обезболиванию с амнезией. В это время пациенты могут вести беседу.
- 2 этап
- Этап 2, также известный как этап возбуждения, это период после потери сознания, отмеченный возбужденной и бредовой деятельностью. На этом этапе пациент дыхание и частота сердцебиения может стать нерегулярным. Кроме того, могут быть неконтролируемые движения, рвота, приостановка дыхания, и расширение зрачков. Поскольку сочетание спастических движений, рвоты и нерегулярного дыхания может нарушить проходимость дыхательных путей пациента, используются быстродействующие препараты, чтобы минимизировать время на этой стадии и как можно быстрее достичь стадии 3.
- 3 этап
- На стадии 3, также известной как хирургическая анестезияскелетные мышцы расслабляются, рвота прекращается, возникает угнетение дыхания, и движения глаз замедляются, а затем прекращаются. Пациент без сознания и готов к операции. Этот этап разделен на четыре плоскости:
- Глаза закатываются, затем фиксируются;
- Утрачиваются роговичные и гортанные рефлексы;
- Зрачки расширяются, теряется световой рефлекс;
- Возникает межреберный паралич и поверхностное брюшное дыхание.
- 4 этап
- Стадия 4, также известная как передозировка, возникает, когда вводится слишком много анестезирующего препарата относительно количества хирургической стимуляции, и у пациента наблюдается тяжелая мозговой ствол или же медуллярный депрессия, приводящая к остановке дыхания и возможному сердечно-сосудистому коллапсу. Эта стадия смертельна без сердечно-сосудистой и респираторной поддержки.
Индукция
Общая анестезия обычно проводится в медицинское учреждение, чаще всего в операционная или в специальной анестезиологической комнате рядом с театром. Однако его также можно проводить в других местах, например эндоскопия люкс радиология или же кардиология отделение, отделение неотложной помощи, или скорая помощь, или на месте катастрофа где извлечение пациента невозможно или нецелесообразно.
Анестетики можно вводить различными путями, включая: вдыхание, инъекция (внутривенный, внутримышечный, или же подкожный ), устный, и ректальный. Как только они войдут в сердечно-сосудистая система, агенты транспортируются в свои биохимические места действия в центральный и автономный нервная система.
Большинство общих анестетиков вводятся либо внутривенно, либо путем ингаляции. Внутривенная инъекция работает быстрее, чем ингаляция, и требуется около 10–20 секунд, чтобы вызвать полное бессознательное состояние. Это сводит к минимуму фазу возбуждения (стадия 2) и, таким образом, уменьшает осложнения, связанные с введением анестезии.[нужна цитата ] Обычно используемые агенты для внутривенной индукции включают: пропофол, тиопентал натрия, этоидат, метогекситал, и кетамин. Ингаляционная анестезия может быть выбран, когда получить внутривенный доступ трудно (например, у детей), когда ожидается сложность поддержания проходимости дыхательных путей или когда пациент предпочитает это. Севофлуран является наиболее часто используемым средством для ингаляционной индукции, потому что он менее раздражает трахеобронхиальное дерево чем другие агенты.[нужна цитата ]
В качестве примера последовательность индукционных препаратов:
- Предварительная оксигенация для наполнения легких кислородом, чтобы обеспечить более длительный период апноэ во время интубации, не влияя на уровень кислорода в крови
- Фентанил для системной анальгезии для интубации
- Пропофол для седации для интубации
- Переход с кислорода на смесь кислорода и ингаляционный анестетик
Ларингоскопия и интубация очень стимулируют, а индукция притупляет реакцию на эти маневры, одновременно вызывая состояние, близкое к коме, чтобы предотвратить осознание.
Физиологический мониторинг
Несколько мониторинг Технологии позволяют контролировать введение, поддержание и выход из наркоза.
- Непрерывный электрокардиография (ЭКГ или ЭКГ): Электроды помещаются на кожу пациента, чтобы контролировать частоту сердечных сокращений и ритм. Это также может помочь анестезиологу определить ранние признаки сердца. ишемия. Обычно в отведениях II и V5 проводят мониторинг аритмий и ишемии соответственно.
- Непрерывный пульсоксиметрия (SpO2): устройство помещается, обычно на палец, для раннего обнаружения падения пациента. гемоглобин насыщение кислородом (гипоксемия ).
- Мониторинг артериального давления: Есть два метода измерения артериального давления пациента. Первый и наиболее распространенный - это неинвазивный мониторинг артериального давления (НИАД). Это предполагает размещение манжета для измерения артериального давления вокруг руки, предплечья или ноги пациента. Аппарат снимает показания артериального давления через регулярные заданные промежутки времени на протяжении всей операции. Второй метод - это инвазивный мониторинг артериального давления (ИДД). Этот метод предназначен для пациентов с серьезными заболеваниями сердца или легких, в критическом состоянии и для тех, кто подвергается серьезным процедурам, таким как кардиохирургия или операция по трансплантации, или когда ожидается большая кровопотеря. Он предполагает размещение специального вида пластика. канюля в артерии, обычно в запястье (лучевая артерия ) или пах (бедренная артерия ).
- Измерение концентрации агента: анестезиологические аппараты обычно имеют мониторы для измерения процента используемых ингаляционных анестетиков, а также концентрации выдыхаемого воздуха. Эти мониторы включают измерения кислород, углекислый газ, и ингаляционные анестетики (например., оксид азота, изофлуран ).
- Измерение кислорода: Почти во всех контурах есть сигнализация в случае нарушения подачи кислорода пациенту. Сигнал тревоги срабатывает, если доля вдыхаемого кислорода падает ниже установленного порога.
- А сигнализация отключения цепи или же сигнализация низкого давления указывает на неспособность контура достичь заданного давления во время механическая вентиляция.
- Капнография измеряет количество углекислый газ выдыхаемый пациентом в процентах или мм рт. ст., что позволяет анестезиологу оценить адекватность вентиляция. MmHg обычно используется, чтобы позволить провайдеру увидеть более тонкие изменения.
- Измерение температуры различать переохлаждение или лихорадки, и для раннего выявления злокачественная гипертермия.
- Электроэнцефалография, энтропийный мониторинг, или другие системы могут использоваться для проверки глубины анестезии. Это снижает вероятность осведомленность об анестезии и передозировки.
Управление дыхательными путями
Пациенты, находящиеся под наркозом, теряют защитные рефлексы дыхательных путей (например, кашель), проходимость дыхательных путей, а иногда и регулярное дыхание из-за действия анестетиков, опиоиды, или же миорелаксанты.Для поддержания открытых дыхательных путей и регулирования дыхания некоторые формы дыхательная трубка вводится после того, как пациент потерял сознание. механическая вентиляция, эндотрахеальная трубка часто используется, хотя есть альтернативные устройства, которые могут помочь в дыхании, такие как маски для лица или ларингеальная маска дыхательные пути Как правило, полная механическая вентиляция используется только в том случае, если требуется вызвать очень глубокое состояние общей анестезии перед большой процедурой и / или у глубоко больного или травмированного пациента. При этом индукция общей анестезии обычно приводит к апноэ и требует вентиляции до тех пор, пока лекарства не закончатся и не начнется самостоятельное дыхание. Другими словами, вентиляция может потребоваться как для индукции, так и для поддержания общей анестезии или только во время индукции. Однако механическая вентиляция может обеспечить вентиляционную поддержку во время спонтанного дыхания, чтобы обеспечить достаточное количество газа. обмен.
Общая анестезия также может быть вызвана спонтанным дыханием пациента и, следовательно, поддержанием собственной оксигенации, что может быть полезно в определенных сценариях (например, при затрудненном прохождении дыхательных путей или при бесконтактной хирургии). Самопроизвольная вентиляция традиционно поддерживается с помощью ингаляционных агентов (например, галотана или севофлурана), что называется газовой или ингаляционной индукцией. Самостоятельную вентиляцию легких также можно поддерживать с помощью внутривенной анестезии (например, пропофолом). Внутривенная анестезия для поддержания спонтанного дыхания имеет определенные преимущества по сравнению с ингаляционными средствами (например, подавление гортанных рефлексов), однако требует тщательного титрования. Самопроизвольное дыхание с использованием внутривенной анестезии и высокопроизводительного назального кислорода (STRIVE Hi) - это метод, который использовался при затрудненных и затрудненных дыхательных путях.[23]
Управление глазами
Общая анестезия снижает тоническое сокращение из orbicularis oculi мышца, вызывая лагофтальм, или неполное закрытие глаза у 59% пациентов.[24] Кроме того, снижается образование слезы и стабильность слезной пленки, что приводит к высыханию эпителия роговицы и снижению лизосомный защита. Защита, предоставляемая Феномен Белла (при котором глазное яблоко во время сна поворачивается вверх, защищая роговицу) также теряется. Требуется тщательное управление, чтобы снизить вероятность травмы глаз во время наркоза.[25]
Нервно-мышечная блокада

- Пропофол, снотворное
- Эфедрин, в случае гипотония
- Фентанил, за обезболивание
- Атракуриум, за нервно-мышечный блок
- Гликопиррония бромид (здесь под торговым наименованием Robinul), уменьшающие секрецию
Паралич или временное расслабление мышц с нервно-мышечный блокатор, является неотъемлемой частью современной анестезии. Первым лекарством, использованным для этой цели, был кураре, представленный в 1940-х годах, который сейчас заменен лекарствами с меньшим количеством побочных эффектов и, как правило, с меньшей продолжительностью действия. Расслабление мышц позволяет проводить операции в полости тела, такой как брюшная полость и грудная клетка, без необходимости очень глубокой анестезии, а также облегчает эндотрахеальная интубация.
Ацетилхолин, естественный нейротрансмиттер на нервномышечное соединение, заставляет мышцы сокращаться, когда он высвобождается из нервных окончаний. Миорелаксанты действуют, предотвращая прикрепление ацетилхолина к его рецептору. Паралич дыхательных мышц - диафрагма и межреберные мышцы грудной клетки - требует применения какой-либо формы искусственного дыхания. Потому что мышцы гортань также парализованы, дыхательные пути обычно необходимо защитить с помощью эндотрахеальная трубка.
Паралич легче всего контролировать с помощью стимулятора периферических нервов. Это устройство периодически посылает короткие электрические импульсы через кожу по периферическому нерву, в то время как наблюдается сокращение мышцы, обеспечиваемой этим нервом. Действие миорелаксантов обычно отменяется в конце операции путем антихолинэстераза препараты, которые назначают в сочетании с мускариновыми холинолитик препараты для минимизации побочных эффектов. Новые средства, снимающие нервно-мышечную блокаду, такие как Sugammadex также могут быть использованы. Примеры используемых сегодня релаксантов скелетных мышц: панкуроний, рокуроний, векуроний, цисатракурий, атракурий, мивакурий, и сукцинилхолин.
Обслуживание
Продолжительность действия агентов для внутривенной индукции обычно составляет от 5 до 10 минут, после чего происходит спонтанное восстановление сознания. Чтобы продлить бессознательное состояние на требуемую продолжительность (обычно на время операции), необходимо поддерживать анестезию. Это достигается, позволяя пациенту дышать тщательно контролируемой смесью кислорода, иногда оксид азота, а летучий анестетик агента, или путем введения лекарства (обычно пропофол ) через внутривенный катетер. Вдыхаемые агенты часто дополняются внутривенными анестетиками, такими как опиоиды (обычно фентанил или производное фентанила) и успокаивающие (обычно пропофол или мидазолам). Однако при использовании анестетиков на основе пропофола добавление ингаляционных средств не требуется.
По окончании операции введение анестетиков прекращают. Восстановление сознания происходит, когда концентрация анестетика в головном мозге падает ниже определенного уровня (обычно в пределах от 1 до 30 минут, в зависимости от продолжительности операции).
В 1990-х годах был разработан новый метод поддержания анестезии. Глазго, Шотландия. Называется целевая контролируемая инфузия (TCI), он включает использование управляемого компьютером шприца (насоса) для инфузии пропофола на протяжении всей операции, что устраняет необходимость в летучих анестетиках и позволяет фармакологическим принципам более точно определять количество используемого препарата, устанавливая желаемое концентрация препарата. Преимущества включают более быстрое восстановление после анестезии, снижение частоты послеоперационной тошноты и рвоты и отсутствие триггера для злокачественная гипертермия. В настоящее время TCI не разрешен в Соединенных Штатах, но вместо него обычно используется шприцевой насос, доставляющий определенную дозу лекарства.[нужна цитата ]
Иногда для лечения побочных эффектов или предотвращения осложнений используются другие лекарства. Они включают гипотензивные средства для лечения повышенного артериального давления; эфедрин или же фенилэфрин для лечения пониженного давления; сальбутамол лечить астма, ларингоспазм, или же бронхоспазм; и адреналин или же дифенгидрамин для лечения аллергических реакций. Глюкокортикоиды или же антибиотики иногда назначают для предотвращения воспаления и инфекции соответственно.
Возникновение
Возникновение - это возвращение к исходной физиологической функции всех систем органов после прекращения действия общих анестетиков. Эта стадия может сопровождаться временными неврологическими явлениями, такими как: возбужденное появление (острая спутанность сознания), афазия (нарушение производства или понимания речи) или очаговое нарушение сенсорной или моторной функции. Дрожь также довольно часто встречается и может иметь клиническое значение, поскольку вызывает увеличение кислород потребление, углекислый газ производство, сердечный выброс, частота сердцебиения, и системное артериальное давление. Предлагаемый механизм основан на наблюдении, что спинной мозг восстанавливается быстрее, чем мозг. Это приводит к раскрепощенным спинальным рефлексам, проявляющимся в виде клонический активность (дрожь). Эта теория подтверждается тем фактом, что доксапрам, а ЦНС стимулятор, в некоторой степени эффективен при устранении послеоперационной дрожи.[26] Сердечно-сосудистые события, такие как повышение или снижение артериального давления, быстрое сердцебиение, или другой сердечные аритмии также распространены при выходе из наркоза, как и респираторные симптомы, такие как одышка.
Послеоперационный уход

Больницы стремятся к безболезненному пробуждению от наркоза. Хотя это и не является прямым результатом общей анестезии, послеоперационная боль купируется в блок восстановления анестезии с региональная анальгезия или устно, трансдермальный, или же парентеральный медикамент. Пациентам можно давать опиоиды, а также другие лекарства, такие как стероидные противовоспалительные препараты и ацетаминофен.[27] Иногда опиоидные препараты вводятся самим пациентом с помощью системы, называемой контролируемый пациентом анальгетик.[28] Пациент нажимает кнопку, чтобы активировать шприц и получить заданную дозу или «болюс» препарата, обычно сильнодействующего опиоида, такого как морфий, фентанил, или же оксикодон (например, один миллиграмм морфина). Затем устройство PCA «блокируется» на заранее установленный период, чтобы лекарство начало действовать. Если пациент становится слишком сонным или находится под действием седативных средств, он больше не просит. Это дает аспект отказоустойчивости, которого не хватает в методах непрерывной инфузии. Если эти лекарства не могут эффективно справиться с болью, местный анестетик может быть введен непосредственно в нерв в ходе процедуры, называемой блокада нерва.[29][30]
В отделении восстановления отслеживаются многие жизненно важные функции, в том числе насыщение кислородом,[31][32] сердечный ритм и дыхание,[31][33] артериальное давление,[31] и внутренняя температура тела.
Постанестетическая дрожь обычное дело. Было показано, что дрожь не только вызывает дискомфорт и усиливает боль, но и увеличивает потребление кислорода. катехоламин выброс, сердечный выброс, частота сердечных сокращений, артериальное давление и внутриглазное давление.[34] Для уменьшения дрожи используется ряд методов, таких как теплые одеяла,[35][36] или обертывание пациента простыней, в которой циркулирует теплый воздух, что называется Bair Hugger.[37][38] Если дрожь не купируется с помощью внешних согревающих устройств, можно использовать такие препараты, как дексмедетомидин,[39][40] или другие α2-агонисты, холинолитики, стимуляторы центральной нервной системы или кортикостероиды.[27][41]
Во многих случаях опиоиды, используемые для общей анестезии, могут вызывать послеоперационные кишечная непроходимость, даже после неабдоминальных операций. Администрация μ-опиоид антагонист Такие как альвимопан сразу после операции может помочь уменьшить тяжесть и продолжительность кишечной непроходимости.[42]
Основное осложнение общей анестезии: злокачественная гипертермия.[43][44] В больницах есть процедуры и лекарства для оказания неотложной помощи, чтобы справиться с этим опасным осложнением.[45]
Периоперационная смертность
Наиболее периоперационная смертность связано с осложнения от операции, например кровотечение, сепсис, и отказ жизненно важных органов. Текущие оценки периоперационной смертности при процедурах, связанных с общей анестезией, варьируются от одного из 53 до одного из 5417.[46][47] Однако канадец 1997 года ретроспективный обзор из 2 830 000 оральная хирургия процедуры в Онтарио в период с 1973 по 1995 год зарегистрировано только четыре смерти в случаях, когда челюстно-лицевой хирург или зубной врач со специальной подготовкой в области анестезии назначают общий наркоз или глубокую седацию. Авторы подсчитали, что общий уровень смертности составляет 1,4 на 1 000 000 человек.[48]
Смертность, напрямую связанная с анестезиологическим лечением, очень редка, но может быть вызвана: легочная аспирация содержимого желудка,[49] удушье,[50] или же анафилаксия.[51] Это, в свою очередь, может быть результатом неисправности оборудование для анестезии или, чаще, человеческая ошибка. Исследование 1978 года показало, что 82% предотвратимых неудач с анестезией были результатом человеческой ошибки.[52] В 1954 году обзор 599 548 хирургических процедур в 10 больницах США в период с 1948 по 1952 год показал, что 384 смертельных случая были связаны с анестезией. смертность 0,064%.[53] В 1984 году после телевизионной программы, в которой рассказывалось о неудачах с анестезией в США, американский анестезиолог Эллисон С. Пирс назначен Комитет по безопасности анестезиологических пациентов и управлению рисками в рамках Американское общество анестезиологов.[54] Этому комитету было поручено определить и уменьшить причины связанных с анестезией болезненность и смертность.[54] Результатом этого комитета является Фонд безопасности пациентов при анестезии, который был создан в 1985 году как независимая некоммерческая корпорация с целью, «чтобы ни один пациент не пострадал от анестезии».[55]
Как и периоперационной смертности в целом, смертность, относящаяся к управлению общим наркозом, является спорным.[56] Оценки частоты периоперационной смертности, напрямую связанной с анестезией, варьируются от 1 на 6 795 до 1 на 200 200.[46]
Смотрите также
Рекомендации
- ^ Бём И., Наирз К., Морелли Дж., Сильва Хасембанк Келлер П., Хверхаген Дж. Т. (2017). «Общая анестезия для пациентов с анафилаксией, вызванной контрастным веществом в анамнезе: полезная профилактика?». Br J Radiol. 90 (1079): 20160647. Дои:10.1259 / bjr.20160647. ЧВК 5963380. PMID 28876979.
- ^ Евтович-Тодорович V (сентябрь 2016 г.). «Общие анестетики и нейротоксичность: что мы знаем?». 34 (3). Anesthesiol Clin. Дои:10.1016 / j.anclin.2016.04.001. PMID 27521190. Получено 11 мая 2020. Цитировать журнал требует
| журнал =(помощь) - ^ Фрейзер, Дженнифер (26 января 2018 г.). «Растения, как и люди, поддаются анестезии». Scientific American. Получено 26 января 2018.
- ^ Шнайдер Г (2007). «Поиск структур и механизмов, контролирующих бессознательное состояние, вызванное анестезией». Анестезиология. 107 (2): 195–198. Дои:10.1097 / 01.anes.0000271869.27956.d1. PMID 17667560.
- ^ Ли Х, Пирс Р.А. (февраль 2000 г.). «Влияние галотана на кинетику рецептора ГАМК (А): доказательства замедленного расщепления агониста». Журнал неврологии. 20 (3): 899–907. Дои:10.1523 / JNEUROSCI.20-03-00899.2000. ЧВК 6774186. PMID 10648694.
- ^ Харрисон Н.Л., Симмондс М.А. (февраль 1985 г.). «Количественные исследования некоторых антагонистов N-метил D-аспартата в срезах коры головного мозга крыс». Британский журнал фармакологии. 84 (2): 381–91. Дои:10.1111 / j.1476-5381.1985.tb12922.x. ЧВК 1987274. PMID 2858237.
- ^ Ледерман Д., Ишвар Дж., Фельдман Дж., Шапиро В. (август 2019 г.). «Анестезиологические соображения при резекции легкого: предоперационная оценка, интраоперационные проблемы и послеоперационная анальгезия». Анналы трансляционной медицины. 7 (15): 356. Дои:10.21037 / атм.2019.03.67. ЧВК 6712248. PMID 31516902.
- ^ Идзумо В., Хигучи Р., Ядзава Т., Уэмура С., Шиихара М., Ямамото М. (октябрь 2019 г.). «Оценка предоперационных факторов риска постпанкреатэктомического кровотечения». Архив хирургии Лангенбека. 404 (8): 967–974. Дои:10.1007 / s00423-019-01830-w. ЧВК 6935390. PMID 31650216.
- ^ Будворт Л., Прествич А., Лоутон Р., Коце А., Келлар И. (4 февраля 2019 г.). «Предоперационные вмешательства для употребления алкоголя и других развлекательных веществ: систематический обзор и метаанализ». Границы в психологии. 10: 34. Дои:10.3389 / fpsyg.2019.00034. ЧВК 6369879. PMID 30778307.
- ^ Siriphuwanun V, Punjasawadwong Y, Saengyo S, Rerkasem K (18 октября 2018 г.). «Заболеваемость и факторы, связанные с периоперационной остановкой сердца у пациентов с травмами, получающих анестезию». Политика управления рисками и здравоохранения. 11: 177–187. Дои:10.2147 / rmhp.s178950. ЧВК 6201994. PMID 30425598.
- ^ Mushambi MC, Jaladi S (июнь 2016 г.). «Обеспечение проходимости дыхательных путей и обучение акушерской анестезии». Текущее мнение в анестезиологии. 29 (3): 261–7. Дои:10.1097 / ACO.0000000000000309. PMID 26844863. S2CID 27527932.
- ^ Рехак А., Уоттерсон Л. М. (ноябрь 2019 г.). «Институциональная готовность к предотвращению и лечению связанных с анестезией событий« не могу интубировать, не могу насыщать кислородом »в учебных больницах Австралии и Новой Зеландии». Анестезия. 75 (6): 767–774. Дои:10.1111 / anae.14909. PMID 31709522.
- ^ Schieren M, Kleinschmidt J, Schmutz A, Loop T, Staat M, Gatzweiler KH и др. (Декабрь 2019 г.). «Сравнение сил, действующих на резцы верхней челюсти во время интубации трахеи, с различными методами ларингоскопии: исследование слепого манекена». Анестезия. 74 (12): 1563–1571. Дои:10.1111 / anae.14815. PMID 31448404.
- ^ Bergendahl H, Lönnqvist PA, Eksborg S (февраль 2006 г.). «Клонидин в педиатрической анестезии: обзор литературы и сравнение с бензодиазепинами для премедикации». Acta Anaesthesiologica Scandinavica. 50 (2): 135–43. Дои:10.1111 / j.1399-6576.2006.00940.x. PMID 16430532. Архивировано из оригинал 16 декабря 2012 г.
- ^ Дахмани С., Брашер С., Стани И., Голмард Дж., Схири А., Бруно Б. и др. (Апрель 2010 г.). «Премедикация клонидином превосходит бензодиазепины. Метаанализ опубликованных исследований». Acta Anaesthesiologica Scandinavica. 54 (4): 397–402. Дои:10.1111 / j.1399-6576.2009.02207.x. PMID 20085541. S2CID 205430269.
- ^ Розенбаум А., Каин З.Н., Ларссон П., Лённквист П.А., Вольф А.Р. (сентябрь 2009 г.). «Место премедикации в педиатрической практике». Детская анестезия. 19 (9): 817–28. Дои:10.1111 / j.1460-9592.2009.03114.x. PMID 19691689.
- ^ Кокс Р., Немиш Ю., Юэн А., Кроу М. Дж. (Декабрь 2006 г.). «Обновленная клиническая информация, основанная на фактах: приводит ли премедикация пероральным мидазоламом к улучшению поведенческих результатов у детей?». Канадский журнал анестезии. 53 (12): 1213–9. Дои:10.1007 / BF03021583. PMID 17142656.
- ^ Бозкурт П. (июнь 2007 г.). «Премедикация педиатрического больного - анестезия для несговорчивого ребенка». Текущее мнение в анестезиологии. 20 (3): 211–5. Дои:10.1097 / ACO.0b013e328105e0dd. PMID 17479023. S2CID 25446995.
- ^ а б Naguib M, Gottumukkala V, Goldstein PA (январь 2007 г.). «Мелатонин и анестезия: клиническая перспектива». Журнал исследований шишковидной железы. 42 (1): 12–21. Дои:10.1111 / j.1600-079X.2006.00384.x. PMID 17198534.
- ^ Mencía SB, López-Herce JC, Freddi N (май 2007 г.). «Обезболивание и седация у детей: практический подход к наиболее частым ситуациям» (PDF). Jornal de Pediatria. 83 (2 доп.): С71-82. Дои:10.2223 / JPED.1625. PMID 17530139.
- ^ а б c Манянде А., Сина А.М., Ип П., Чхой С., Миддлтон П. (июль 2015 г.). «Немедикаментозные вмешательства для содействия введению анестезии у детей» (PDF). Кокрановская база данных систематических обзоров (7): CD006447. Дои:10.1002 / 14651858.CD006447.pub3. PMID 26171895.
- ^ Hewer CL (август 1937 г.). «Этапы и признаки общей анестезии». Британский медицинский журнал. 2 (3996): 274–6. Дои:10.1136 / bmj.2.3996.274. ЧВК 2087073. PMID 20780832.
- ^ Бут А.В., Видхани К., Ли П.К., Томсетт К.М. (март 2017 г.). «Спонтанное дыхание с использованием внутривенной анестезии и назального кислорода Hi-flow (STRIVE Hi) поддерживает оксигенацию и проходимость дыхательных путей во время лечения обструкции дыхательных путей: обсервационное исследование». Британский журнал анестезии. 118 (3): 444–451. Дои:10.1093 / bja / aew468. ЧВК 5409133. PMID 28203745.
- ^ Подрядчик С., Хардман Дж. Г. (2006). «Травма при наркозе». Повышение квалификации в области анестезии, неотложной помощи и боли. 6 (2): 67–70. Дои:10.1093 / bjaceaccp / mkl004.
- ^ Наир П.Н., Белый Э (2014). «Уход за глазом во время наркоза и интенсивной терапии». Анестезия и интенсивная терапия. 15: 40–43. Дои:10.1016 / j.mpaic.2013.11.008.
- ^ Основы анестезии, 5-е издание Авторы: Роберт К. Стултинг и Рональд Д. Миллер ISBN 978-0-443-06801-0
- ^ а б Лопес, М. Б. (2018). "12.1.2018". Румынский журнал анестезии и интенсивной терапии. 25 (1): 73–81. Дои:10.21454 / rjaic.7518.251.xum. ЧВК 5931188. PMID 29756066.
- ^ Райпал С., Гордон Д. Б., Пеллино Т. А., Страйер А. Л., Брост Д., Трост Г. Р. и др. (Апрель 2010 г.). «Сравнение периоперационной пероральной мультимодальной анальгезии с IV PCA для хирургии позвоночника». Журнал заболеваний и методов позвоночника. 23 (2): 139–45. Дои:10.1097 / BSD.0b013e3181cf07ee. PMID 20375829. S2CID 5319313.
- ^ Schnabel A, Reichl SU, Weibel S, Zahn PK, Kranke P, Pogatzki-Zahn E, Meyer-Frießem CH (октябрь 2019 г.). Кокрановская группа по анестезии (ред.). «Блокада приводящего канала для лечения послеоперационной боли у взрослых, перенесших операцию на колене». Кокрановская база данных систематических обзоров. 2019 (10). Дои:10.1002 / 14651858.CD012262.pub2. ЧВК 6814953. PMID 31684698.
- ^ Шарма А., Гоэль А.Д., Шарма П.П., Вьяс В., Агравал С.П. (октябрь 2019 г.). «Эффект блокады поперечной мышцы живота на обезболивание у пациентов, перенесших трансплантацию печени: систематический обзор и метаанализ». Турецкий журнал анестезиологии и реанимации. 47 (5): 359–366. Дои:10.5152 / tjar.2019.60251. ЧВК 6756312. PMID 31572985.
- ^ а б c Олсен Р.М., Аасванг Е.К., Мейхофф К.С., Диссинг Соренсен HB (октябрь 2018 г.). «На пути к автоматизированной мультимодальной системе поддержки принятия клинических решений в постанестезиологическом отделении». Компьютеры в биологии и медицине. 101: 15–21. Дои:10.1016 / j.compbiomed.2018.07.018. PMID 30092398.
- ^ Петерсен К., Веттерслев Дж., Мейхофф С.С. (август 2018 г.). «Периоперационная гипероксия и послеоперационные сердечные осложнения у взрослых, перенесших внесердечные операции: протокол систематического обзора». Acta Anaesthesiologica Scandinavica. 62 (7): 1014–1019. Дои:10.1111 / aas.13123. PMID 29664117.
- ^ Орбах-Зингер С., Бизман И., Фирман С., Лев С., Гат Р., Ашвал Э. и др. (Октябрь 2019 г.). «Периоперационный неинвазивный мониторинг сердечного выброса у рожениц, перенесших кесарево сечение со спинальной анестезией и профилактической капельницей фенилэфрина: проспективное обсервационное когортное исследование». Журнал материнско-фетальной и неонатальной медицины. 32 (19): 3153–3159. Дои:10.1080/14767058.2018.1458835. PMID 29683007. S2CID 5039625.
- ^ Махаджан Р.П., Гровер В.К., Шарма С.Л., Сингх Х. (март 1987 г.). «Изменение внутриглазного давления при мышечной гиперактивности после общей анестезии». Анестезиология. 66 (3): 419–21. Дои:10.1097/00000542-198703000-00030. PMID 3826703.
- ^ Shaw CA, Steelman VM, DeBerg J, Schweizer ML (май 2017 г.). «Эффективность активного и пассивного нагревания для предотвращения непреднамеренного переохлаждения у пациентов, получающих нейроаксиальную анестезию: систематический обзор и метаанализ рандомизированных контролируемых исследований». Журнал клинической анестезии. 38: 93–104. Дои:10.1016 / j.jclinane.2017.01.005. ЧВК 5381733. PMID 28372696.
- ^ Олдерсон П., Кэмпбелл Г., Смит А.Ф., Варттиг С., Николсон А., Льюис С.Р. (июнь 2014 г.). Кокрановская анестезия, группа интенсивной и неотложной помощи (ред.). «Теплоизоляция для предотвращения непреднамеренного переохлаждения в период операции». Кокрановская база данных систематических обзоров (6): CD009908. Дои:10.1002 / 14651858.CD009908.pub2. PMID 24895945.
- ^ Стангер Р., Коливас К., Кэсси Дж. Г., Робинсон И. А., Армстронг П. (август 2009 г.). «Прогнозирование эффективности конвекционного нагревания у детей под наркозом». Британский журнал анестезии. 103 (2): 275–82. Дои:10.1093 / bja / aep160. PMID 19541677.
- ^ Вагнер К., Суонсон Э, Раймонд С.Дж., Смит С.Е. (июнь 2008 г.). «Сравнение двух систем конвективного обогрева во время крупных абдоминальных и ортопедических операций». Канадский журнал анестезии. 55 (6): 358–63. Дои:10.1007 / BF03021491. PMID 18566199.
- ^ Чжан Дж, Чжан Х, Ван Х, Чжоу Х, Тиан Т, Ву А (22 августа 2017 г.). «Дексмедетомидин как нейроаксиальный адъювант для предотвращения периоперационной дрожи: метаанализ рандомизированных контролируемых исследований». PLOS ONE. 12 (8): e0183154. Bibcode:2017PLoSO..1283154Z. Дои:10.1371 / journal.pone.0183154. ЧВК 5567500. PMID 28829798.
- ^ Чжан X, Ван Д., Ши М., Ло И (апрель 2017 г.). «Эффективность и безопасность дексмедетомидина в качестве адъюванта при эпидуральной аналгезии и анестезии: систематический обзор и метаанализ рандомизированных контролируемых испытаний». Клинические исследования лекарств. 37 (4): 343–354. Дои:10.1007 / s40261-016-0477-9. PMID 27812971. S2CID 5512397.
- ^ Английский W (2002). «Послеоперационная дрожь, причины, профилактика и лечение (письмо)». Обновление в анестезии (15). Архивировано из оригинал 29 мая 2011 г.. Получено 8 сентября 2010.
- ^ Лесли JB, Viscusi ER, Pergolizzi JV, Panchal SJ (2011). «Анестезиологические процедуры: роль анестезиолога в восстановлении желудочно-кишечного тракта и послеоперационном Ileus». Достижения профилактической медицины. 2011: 976904. Дои:10.4061/2011/976904. ЧВК 3168940. PMID 21991449.
- ^ Ким К.С., Крисс Р.С., Тауц Т.Дж. (декабрь 2019 г.). «Злокачественная гипертермия: клинический обзор». Достижения в анестезии. 37: 35–51. Дои:10.1016 / j.aan.2019.08.003. PMID 31677658.
- ^ Бальдо Б.А., Роуз М.А. (октябрь 2019 г.). «Анестезиолог, опиоидные анальгетики и токсичность серотонина: механистический и клинический обзор». Британский журнал анестезии. 0 (1): 44–62. Дои:10.1016 / j.bja.2019.08.010. PMID 31653394.
- ^ Поллок Н., Лангтонт Е., Стоуэлл К., Симпсон С., МакДоннелл Н. (август 2004 г.). «Безопасная продолжительность послеоперационного наблюдения за пациентами, предрасположенными к злокачественной гипертермии». Анестезия и интенсивная терапия. 32 (4): 502–9. Дои:10.1177 / 0310057X0403200407. PMID 15675210.
- ^ а б Lagasse RS (декабрь 2002 г.). «Безопасность анестезии: модель или миф? Обзор опубликованной литературы и анализ текущих исходных данных». Анестезиология. 97 (6): 1609–17. Дои:10.1097/00000542-200212000-00038. PMID 12459692. S2CID 32903609.
- ^ Arbous MS, Meursing AE, van Kleef JW, de Lange JJ, Spoormans HH, Touw P et al. (Февраль 2005 г.). «Влияние характеристик управления анестезией на тяжелую заболеваемость и смертность». Анестезиология. 102 (2): 257–68, викторина 491–2. Дои:10.1097/00000542-200502000-00005. HDL:1874/12590. PMID 15681938.
- ^ Нканса П.Дж., Хаас Д.А., Сасо Массачусетс (июнь 1997 г.). «Смертность при амбулаторной анестезии в стоматологии в Онтарио». Хирургия полости рта, стоматология, патология полости рта, радиология полости рта и эндодонтия. 83 (6): 646–51. Дои:10.1016 / S1079-2104 (97) 90312-7. PMID 9195616.
- ^ Энгельхардт Т., Вебстер Н.Р. (сентябрь 1999 г.). "Pulmonary aspiration of gastric contents in anaesthesia" (PDF). Британский журнал анестезии. 83 (3): 453–60. Дои:10.1093/bja/83.3.453. PMID 10655918.
- ^ Parker RB (July 1956). "Maternal death from aspiration asphyxia". Британский медицинский журнал. 2 (4983): 16–9. Дои:10.1136/bmj.2.4983.16. ЧВК 2034767. PMID 13329366.
- ^ Dewachter P, Mouton-Faivre C, Emala CW (November 2009). "Anaphylaxis and anesthesia: controversies and new insights". Анестезиология. 111 (5): 1141–50. Дои:10.1097/ALN.0b013e3181bbd443. PMID 19858877.
- ^ Cooper JB, Newbower RS, Long CD, McPeek B (December 1978). "Preventable anesthesia mishaps: a study of human factors". Анестезиология. 49 (6): 399–406. Дои:10.1097/00000542-197812000-00004. PMID 727541.[постоянная мертвая ссылка ]
- ^ Beecher HK, Todd DP (July 1954). "A study of the deaths associated with anesthesia and surgery: based on a study of 599, 548 anesthesias in ten institutions 1948-1952, inclusive". Анналы хирургии. 140 (1): 2–35. Дои:10.1097/00000658-195407000-00001. ЧВК 1609600. PMID 13159140.
- ^ а б Guadagnino C (2000). "Improving anesthesia safety". Narberth, Pennsylvania: Physician's News Digest, Inc. Archived from оригинал 15 августа 2010 г.. Получено 8 сентября 2010.
- ^ Stoelting RK (2010). «История фонда». Indianapolis, IN: Anesthesia Patient Safety Foundation. Получено 8 сентября 2010.
- ^ Cottrell, J.E. (2003). "Uncle Sam, Anesthesia-Related Mortality and New Directions: Uncle Sam Wants You!". Информационный бюллетень ASA. 67 (1). Архивировано из оригинал 31 июля 2010 г.. Получено 8 сентября 2010.
внешняя ссылка
- Chloroform: The molecular lifesaver An article at University of Bristol providing interesting facts about chloroform.
- In detail about Общая анестезия
- Australian & New Zealand College of Anaesthetists Monitoring Standard
- Royal College of Anaesthetists Patient Information page
