Лептоспироз - Leptospirosis
| Лептоспироз | |
|---|---|
| Другие имена | Крысиная лихорадка,[1] полевая лихорадка,[2] желтизна крысолова,[3] претибиальная лихорадка[4] |
 | |
| Лептоспира увеличен в 200 раз с темнопольный микроскоп. | |
| Специальность | Инфекционное заболевание |
| Симптомы | Никто, головные боли, мышечные боли, лихорадка[5] |
| Осложнения | Кровотечение из легких, менингит, почечная недостаточность[5][6] |
| Обычное начало | От одной до двух недель[7] |
| Причины | Лептоспира обычно распространяется грызуны[8] |
| Факторы риска | Контакт с инфицированными животными или загрязненной водой[8] |
| Диагностический метод | Анализ крови на антитела против бактерии или ее ДНК[5] |
| Дифференциальный диагноз | Малярия, брюшной тиф, риккетсиоз, денге[9] |
| Профилактика | Средства индивидуальной защиты, меры гигиены, доксициклин[7] |
| лечение | Доксициклин, пенициллин, цефтриаксон[8] |
| Прогноз | Риск смерти ~ 7,5%[10] |
| Частота | Один миллион человек в год[7][11] |
| Летальные исходы | 58900 в год[11] |
Лептоспироз это заражение крови вызвано бактериями Лептоспира.[8] Признаки и симптомы могут варьироваться от нулевых до легких (головные боли, мышечные боли, и лихорадка ) до тяжелой (кровотечение в легких или менингит ).[5] Болезнь Вейля, острая тяжелая форма лептоспироза, приводит к тому, что инфицированный человек становится желтушный (кожа и глаза становятся желтыми), развиваются почечная недостаточность, и кровотечение.[6] Кровотечение из легких, связанное с лептоспирозом, известно как «синдром тяжелого легочного кровотечения».[5]
Более десяти генетических типов Лептоспира вызывают заболевание у людей.[12] Как дикие, так и домашние животные могут распространять болезнь, чаще всего грызуны.[8] Бактерии передаются людям через моча животных, или вода и почва, загрязненные мочой животных, вступающие в контакт с глаза, рот, нос или разрывы в кожа.[8] В развивающихся странах болезнь чаще всего встречается у фермеров и людей с низким доходом, которые живут в районах с плохими санитарными условиями.[5] В развитых странах это происходит во время сильных ливней и существует риск сточные воды рабочие[13] и тем, кто занимается активным отдыхом в теплых и влажных местах.[5] Диагноз обычно ставится путем тестирования на антитела против бактерий или обнаружение бактериальных ДНК в крови.[5]
Усилия по предотвращению заболевания включают в себя защитное снаряжение для блокировки контакта при работе с потенциально инфицированными животными, мытье после контакта и сокращение количества грызунов в районах, где люди живут и работают.[7] В антибиотик доксициклин эффективно предотвращает заражение лептоспирозом.[7] Человеческие вакцины имеют ограниченную полезность;[14] вакцины для других животных более доступны.[15] Лечение инфицированных проводится антибиотиками, такими как доксициклин, пенициллин, или цефтриаксон.[8] Общий риск смерти составляет 5–10%.[10] Однако, когда поражены легкие, риск смерти увеличивается до 50–70%.[8]
По оценкам, ежегодно происходит один миллион тяжелых случаев лептоспироза, в результате чего около 58 900 случаев смерти.[11] Заболевание чаще всего встречается у тропический области мира, но может произойти где угодно.[7] Вспышки может возникнуть после сильного дождя.[7] Заболевание впервые было описано врачом. Адольф Вайль в 1886 году в Германии.[16][17]
Признаки и симптомы
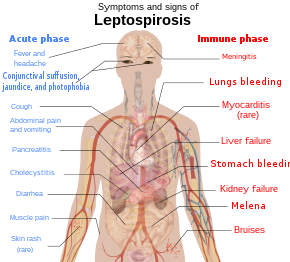

Симптомы лептоспироза обычно появляются через одну-две недели после заражения.[7] но период инкубации может быть до месяца.[18] Болезнь двухфазный в большинстве симптоматических случаев. Симптомы первой фазы (острая или лептоспиремическая фаза) длятся от пяти до семи дней. Во второй фазе (иммунная фаза) симптомы исчезают по мере выработки антител против бактерий.[8] Во второй фазе развиваются дополнительные симптомы.[19] Фазы болезни могут не различаться, особенно у пациентов с тяжелым заболеванием.[20] У 90% инфицированных наблюдаются легкие симптомы, а у 10% - тяжелый лептоспироз.[21]
Лептоспиральная инфекция у людей вызывает ряд симптомы, хотя у некоторых инфицированных может не быть. Заболевание начинается внезапно с повышения температуры тела, сопровождающегося ознобом, сильной головной болью, сильной боль в мышцах и боли в животе.[5][18] Головная боль, вызванная лептоспирозом, вызывает пульсирующую боль и обычно локализуется в области головы с обеих сторон. временный или лобной регионы. У человека также может быть боль за глазами и чувствительность к свету. Мышечная боль обычно связана с икроножная мышца и поясницу. Наиболее характерным признаком лептоспироза является конъюнктивальный прилив (конъюнктивит без экссудат ) который редко встречается в других фебрильный болезни. Другие характерные особенности глаза включают: субконъюнктивальное кровотечение и желтуха. Сыпь при лептоспирозе встречается редко. При обнаружении альтернативных диагнозов, таких как лихорадка денге и лихорадка чикунгунья следует считать. Сухой кашель наблюдается у 20–57% больных лептоспирозом. Таким образом, этот клинический признак может ввести врача в заблуждение, чтобы диагностировать заболевание как респираторное заболевание. Дополнительно, желудочно-кишечный такие симптомы как тошнота часто возникают рвота, боль в животе и диарея. Рвота и диарея могут способствовать обезвоживание. Боль в животе может быть вызвана бескаменный холецистит или воспаление поджелудочной железы.[18] Редко лимфатический узел, печень, и селезенка может быть увеличенным и ощутимым.[8]
Симптомы исчезнут в течение одного-трех дней.[7] После этого начинается иммунная фаза, которая может длиться от четырех до 30 дней и может быть чем угодно, от головного мозга до почечных осложнений.[22] Отличительной чертой второй фазы является воспаление оболочек, покрывающих мозг.[7] Признаки и симптомы менингита включают сильную головную боль и скованность шеи.[7] Поражение почек связано со снижением диуреза или его отсутствием.[7]
Классическая форма тяжелого лептоспироза, известная как болезнь Вейля, характеризуется поражением печени (вызывающим желтуху), почечная недостаточность и кровотечение, которое случается у 5–10% инфицированных.[7] Также может произойти повреждение легких и головного мозга. Для тех, у кого есть признаки воспаление оболочек головного мозга и самого мозга, измененный уровень сознания может случиться. Различные неврологические проблемы, такие как паралич половины тела, полное воспаление всего горизонтального отдела спинного мозга, и мышечная слабость из-за иммунного повреждения нервов, снабжающих мышцы осложнения. Признаки кровотечения, такие как нетравматические синяки размером 1 мм (0,039 дюйма), нетравматические синяки более 1 см (0,39 дюйма), кровотечение из носа, черный стул из-за желудочного кровотечения, рвота кровью и кровотечение из легких также можно найти. Продление протромбиновое время в проверка коагуляции связано с сильным проявлением кровотечения. Однако, низкое количество тромбоцитов не связан с сильным кровотечением.[18] Легочное кровотечение - это альвеолярное кровотечение (кровотечение в альвеолы легких), что приводит к массивному кашель с кровью, и вызывая острый респираторный дистресс-синдром, где риск смерти более 50%.[18] Редко, воспаление сердечной мышцы, воспаление оболочек, покрывающих сердце, аномалии в естественном кардиостимуляторе сердца и аномальные сердечные ритмы может возникнуть.[8]
Причина
Бактерии
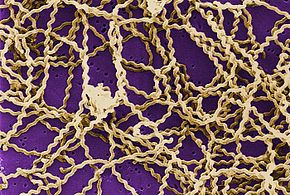
Лептоспироз вызывается спирохета бактерии, принадлежащие к род Лептоспира, которые аэробный,[8] правша спиральный,[12] и 6–20микрометры длинная.[7] подобно Грамотрицательный бактерии Лептоспира есть внешняя мембрана усыпанный липополисахарид (LPS) на поверхности, внутренняя мембрана и слой пептидогликан клеточная стенка. Однако, в отличие от грамотрицательных бактерий, пептидогликановый слой в Лептоспира лежит ближе к внутренней, чем к внешней мембране. Это приводит к образованию жидкой внешней мембраны, слабо связанной с клеточной стенкой.[23] К тому же, Лептоспира есть жгутик расположен в периплазма, связанный с движением в стиле штопор.[7] Хеморецепторы на полюсах бактерии ощущают различные субстраты и меняют направление своего движения.[12] Бактерии традиционно визуализируются с помощью темнопольная микроскопия без окрашивания.[7]
Всего 66 видов Лептоспира был идентифицирован. Основываясь на их геномной последовательности, они делятся на два клады и четыре субклада: P1, P2, S1 и S2.[24] 19 членов субклада P1 включают 8 видов, которые могут вызывать тяжелые заболевания у человека: L. alexanderi, L. borgpetersenii, L. interrogans, Л. киршнери, L. mayottensis, L. noguchii, L. santarosai, и L. weilii.[12][24] В кладу P2 входит 21 вид, которые могут вызывать легкие заболевания у человека. Остальные 26 видов составляют субклады S1 и S2, которые включают «сапрофиты», которые, как известно, потребляют разлагающееся вещество (сапротрофное питание ).[24] Патогенный Лептоспира не размножаются в окружающей среде. Лептоспира требуют высокой влажности для выживания, но могут оставаться живыми в таких средах, как стоячая вода или загрязненная почва. Бактерия может быть уничтожена при температуре 50 ° C (122 ° F) и может быть инактивирована на 70%.этиловый спирт, 1% гипохлорит натрия, формальдегид, моющие средства и кислоты.[25]
Лептоспира также классифицируются на основе их серовар. Разнообразный сахарный состав липополисахарида на поверхности бактерий отвечает за антигенное различие между сероварами.[12] Более 250 патогенных сероваров Лептоспира распознаются, при этом близкородственные серовары собраны в более чем 26 патогенных серогрупп.[8] Штаммы разных видов Лептоспира могут быть членами одной серогруппы из-за горизонтальный перенос генов генов биосинтеза ЛПС между разными видами.[12]
Передача инфекции
Бактерии можно найти в прудах, реках, лужах, канализации, сельскохозяйственных полях и влажной почве.[7] Патогенный Лептоспира были найдены в виде водных биопленки, что может способствовать выживанию в окружающей среде.[26]
Лептоспира живут в почках различных диких и домашних животных. Когда животные проглатывают бактерии, они циркулируют в кровотоке, а затем попадают в почки через клубочковый или перитубулярные капилляры. Затем бактерии переходят в люмен из почечные канальцы и колонизировать кисть границы из проксимальный извитый каналец. Это вызывает постоянное выделение бактерий с мочой, не вызывая у животного серьезных болезненных последствий. Эти отношения между животным и бактериями известны как комменсальные отношения, а животное известно как хозяин резервуара.[18]
Лептоспира встречаются в основном у млекопитающих.[5] Однако рептилии и хладнокровные животные такие, как лягушки, змеи, черепахи и жабы, заражены инфекцией.[15] Неизвестно, являются ли они резервуарами заражения человека.[18][15] Крысы, мыши и кроты важны основные хосты, но другие млекопитающие, включая собак, оленей, кроликов, ежей, коров, овец, свиней, енотов, опоссумов и скунсов, также могут переносить болезнь.[15] В Африке несколько диких животных-хозяев были идентифицированы как переносчики, в том числе полосатый мангуст, Египетская лиса, Руса олень, и землеройки.[27] Существуют различные механизмы, с помощью которых животные могут заразить друг друга. Собаки могут слизывать мочу зараженного животного с травы или почва, или выпить из зараженной лужи.[нужна цитата ] Домашние собаки, прикованные к дому, заразились лептоспирозом, по-видимому, в результате вылизывания мочи инфицированных мышей в доме.[нужна цитата ] Лептоспироз также может передаваться через сперму инфицированных животных.[15] Бактерии, постоянно присутствующие в моче животных, могут сохраняться годами.[15]
Люди - это случайный хозяин из Лептоспира.[5] Люди заражаются при контакте с водой или влажной почвой, содержащей мочу инфицированных животных.[7] Бактерии попадают через порезы, ссадины,[7] проглатывание зараженной пищи или контакт с слизистая оболочка тела (например, рта, носа и глаз).[28] К профессиям, подверженным риску заражения лептоспирозом, относятся фермеры, рыбаки, сборщики мусора и работники сточных вод.[5] Заболевание также связано с приключенческий туризм и развлекательные мероприятия.[5] Это распространено среди любителей водных видов спорта в определенных областях, в том числе триатлон, воды рафтинг, гребля на каноэ и плавание, поскольку длительное погружение в воду способствует проникновению бактерий.[5] Однако, Лептоспира не могут проникнуть через неповрежденную кожу.[8] Заболевание не распространяется между людьми, а распространение бактерий в период восстановления крайне редко встречается у человека.[8] После заражения человека бактериальные выделения из почек обычно сохраняются до 60 дней.[25]
Редко лептоспироз может передаваться через пересадку органа.[29] Заражение через плацента во время беременности тоже возможно.[30][31][32] Это может вызвать выкидыш и инфекция в младенцы.[33]
Патогенез

Патогенез лептоспироза остается малоизученным, несмотря на исследования.[7][28] Бактерии попадают в организм человека через отверстия в коже или слизистой оболочке, а затем попадают в кровоток. Позже бактерии прикрепляются к эндотелиальный клетки кровеносных сосудов и внеклеточный матрикс (сложная сеть белков и углеводов, присутствующих между клетками). Бактерии используют свои жгутики для перемещения между слоями клеток. Они связываются с такими клетками, как фибробласты, макрофаги, эндотелиальные клетки и эпителиальные клетки почек. Они также связываются с несколькими белками человека, такими как белки комплемента, тромбин, фибриноген, и плазминоген используя поверхностный лептоспираль иммуноглобулиноподобный (Lig) белки, такие как LigB и LipL32, гены которых обнаружены у всех патогенных видов.[12][28]
Через врожденная иммунная система, эндотелиальные клетки капилляров в организме человека активируются присутствием этих бактерий. Эндотелиальные клетки производят цитокины и антимикробные пептиды против бактерий. Эти продукты регулируют каскад коагуляции и движения белых кровяных телец.[12] Макрофаги, представленные в организме человека, способны поглотить Лептоспира. Однако, Лептоспира могут жить и размножаться в цитоплазматический матрикс после проглатывания макрофагами.[12] Люди с тяжелым лептоспирозом могут испытывать высокий уровень цитокинов, таких как интерлейкин 6, фактор некроза опухоли альфа (TNF-α) и интерлейкин 10. Высокий уровень цитокинов вызывает сепсис -подобные симптомы, которые опасны для жизни, а не помогают бороться с инфекцией.[21] Обнаружено, что у тех, кто имеет высокий риск сепсиса во время лептоспирозной инфекции, HLA-DQ6 генотип, возможно, из-за суперантиген активация, которая повреждает органы тела.[18]
Гуморальный иммунитет это основной иммунный ответ против Лептоспира клетки. Агглютинирующие антитела, такие как иммуноглобулин М и иммуноглобулин G производятся против бактерий. Такие антитела в основном направлены против LPS.[28] Лептоспира LPS только активирует толл-подобный рецептор 2 (TLR2) в моноциты в людях. Молекула липида А бактерий не распознается человеком. TLR4 рецепторы. Следовательно, отсутствие Лептоспира распознавание рецепторами TLR4, вероятно, способствует развитию лептоспироза у людей.[12]
Хотя в организме человека существуют различные механизмы борьбы с бактериями, Лептоспира хорошо приспособлен к такому воспалительному заболеванию, которое оно создает. В кровотоке он может активировать плазминоген хозяина, чтобы стать плазмин который разрушает внеклеточный матрикс, разрушает фибрин сгустки и дополнительные белки (C3b и C5 ) избежать опсонизация. Он также может нанять регулирующих органов, таких как Фактор H, C4b -связывающий белок, фактор H-подобный связывающий белок, и витронектин чтобы предотвратить активацию комплекс мембранной атаки на его поверхности. Он также выделяет протеазы для разрушения белков комплемента, таких как C3. Он может связываться с тромбином, что снижает образование фибрина. Снижение образования фибрина увеличивает риск кровотечения.[12] Лептоспира также выделяет сфингомиелиназа и гемолизин которые нацелены на красные кровяные тельца.[7]
Лептоспира быстро распространяется по всем органам через кровоток.[12] В основном они поражают печень. Они вторгаются в пространство между гепатоциты, вызывая апоптоз. Поврежденные гепатоциты и межклеточные соединения гепатоцитов вызывают утечку желчи в кровоток, вызывая повышенный уровень билирубин, что приводит к желтухе. Перегружен синусоиды печени и перисинусоидальные пространства не поступало. Между тем в легких петехии или откровенные кровотечение можно найти на альвеолярная перегородка и промежутки между альвеолами.[18] Лептоспира выделяет токсины, которые вызывают от легкой до тяжелой почечной недостаточности или интерстициальный нефрит.[28] Почечная недостаточность может полностью восстановиться или привести к атрофия и фиброз.[18] Воспаление сердечных мышц, коронарных артерий и аорта редко.[22]
Диагностика


Лабораторные тесты
Для инфицированных полный анализ крови может показать высокое количество лейкоцитов и низкое количество тромбоцитов. Когда низкий уровень гемоглобина присутствует вместе с низкое количество лейкоцитов и тромбоцитопения, подавление костного мозга следует считать.[18] Скорость оседания эритроцитов и С-реактивный белок также может быть повышенным.[8]
Почки обычно поражаются лептоспирозом. Кровь мочевина и креатинин уровни будут повышены. Лептоспироз увеличивает выведение калия с мочой, что приводит к низкий уровень калия[18] и низкий уровень натрия в крови.[8][18] Анализ мочи может выявить наличие белка, белые кровяные клетки и микроскопические гематурия.[8] Поскольку бактерии оседают в почках, посев мочи будет положительным на лептоспироз, начиная со второй недели болезни и до 30 дней заражения.[8]
Для пациентов с поражением печени: трансаминазы и прямой билирубин повышены в функциональные пробы печени. Серогруппа Icterohaemorrhagiae связана с желтухой и повышенным уровнем билирубина. Гемолитическая анемия способствует желтухе. Особенность лептоспироза - острая. гемолитическая анемия и сопряженный гипербилирубинемия, особенно у пациентов с дефицит глюкозо-6-фосфатдегидрогеназы.[18] Аномальный сыворотка амилаза и уровни липазы (связанные с панкреатитом) обнаруживаются у тех, кто попадает в больницу из-за лептоспироза. Нарушение функции почек с клиренс креатинина менее 50 мл / мин связано с повышенными ферментами поджелудочной железы.[18]
Тем, у кого сильная головная боль и есть признаки менингита, рекомендуется: поясничная пункция можно попробовать. Если заражен, спинномозговая жидкость (CSF) экзамен показывает лимфоцитарный преобладание с количеством клеток около 500 / мм3, белок от 50 до 100 мг / мл и нормальный уровень глюкозы. Эти результаты согласуются с асептический менингит.[18]
Серологические тесты
Быстрое обнаружение Лептоспира можно сделать путем количественного определения антител IgM с использованием ELISA. Обычно L. biflexa антиген используется для обнаружения антител IgM. Этот тест может быстро определить диагноз и помочь в раннем лечении. Однако специфичность теста зависит от типа используемого антигена и наличия антител от предыдущих инфекций. Наличие других заболеваний, таких как Вирус Эпштейна-Барра инфекция, вирусная гепатит, и цитомегаловирус инфекция может вызвать ложноположительные результаты.[18] Были разработаны другие быстрые скрининговые тесты, такие как индикаторные полоски, латекс и слайд-тесты агглютинации.[8]
Микроскопический тест агглютинации (МАТ) является эталонным тестом для диагностики лептоспироза.[18] MAT - это тест, в котором серийные разведения сывороток пациентов смешивают с различными сероварами Лептоспира. Затем смесь исследуют под темнопольный микроскоп искать агглютинация. Результатом является максимальное разбавление, при котором происходит агглютинация 50%.[18] МАТ титры от 1: 100 до 1: 800 являются диагностическими для лептоспироза.[8] Четырехкратное или большее повышение титра двух сывороток, взятых при появлении симптомов и от трех до 10 дней начала заболевания, подтверждает диагноз. Во время острой фазы заболевания МАТ неспецифична для выявления серотипа Лептоспира из-за перекрестной реактивности между сероварами.[18] в выздоравливающий В фазе MAT более специфичен для определения типов сероваров.[18] MAT требует панели живых антигенов и требует кропотливой работы.[22]
Молекулярные тесты
Лептоспира ДНК можно амплифицировать с помощью полимеразной цепной реакции (ПЦР) из сыворотки, мочи, водянистая влага, CSF и образцы вскрытия.[18] ПЦР может обнаружить Лептоспира ДНК в крови еще до развития антител. Поскольку ПЦР обнаруживает присутствие Лептоспира ДНК, она полезна даже после начала лечения антибиотиками.[8]
Изображения
У тех, у кого есть поражение легких, рентген грудной клетки может продемонстрировать диффузное помутнение альвеол.[18]
Диагностические критерии
В 1982 г. Всемирная организация здоровья (ВОЗ) предложили критерии Фейна для диагностики лептоспироза. Он состоит из трех частей: A (клинические данные), B (эпидемиологические факторы) и C (лабораторные данные и бактериологические данные). Поскольку исходные критерии Фейна включали культивирование и МАТ только в части C, которая является сложной и сложной для выполнения, в 2004 году были предложены модифицированные критерии Фейна, включающие ИФА и тесты агглютинации на слайдах, которые легче выполнять. В 2012 году модифицированные критерии Фейна (с поправками) были предложены для включения одышка и кровохарканье при диагнозе. В 2013 году Индия рекомендовала модифицированные критерии Фейна для диагностики лептоспироза.[34]
Профилактика


Уровень лептоспироза можно снизить за счет улучшения жилищных, инфраструктурных и санитарных стандартов. Усилия по борьбе с грызунами и проекты по смягчению последствий наводнений также могут помочь предотвратить это.[18] Правильное использование средства индивидуальной защиты (СИЗ) людей с высоким риском профессионального заражения в большинстве случаев могут предотвратить заражение лептоспирозом.[18]
Не существует вакцины для человека, пригодной для использования во всем мире.[14] Только Куба, Япония, Франция и Китай одобрили использование вакцин против лептоспироза, и они вводятся только тем, кто работает с повышенным риском, а также в ответ на наводнения и эпидемии.[18][14][35] Вакцины состоят из убитых Лептоспира, и они придают иммунитет только серовару, содержащемуся в вакцине.[35] Побочные эффекты, такие как тошнота, покраснение в месте инъекции сообщалось об отеке после введения вакцины. Поскольку иммунитет, вызванный одним Лептоспира серовар защищает только от этого конкретного, трехвалентный вакцины разработаны.[18] Иммунитет после вакцинации сохраняется около года.[35]
Доксициклин дается раз в неделю в качестве профилактика и эффективен в снижении частоты инфекций лептоспирозом среди лиц с высоким риском в районах, подверженных наводнениям.[36] Согласно одному исследованию, это снизило количество случаев лептоспироза у военнослужащих, проходящих учения в джунглях. В другом исследовании он уменьшил количество симптоматических случаев после заражения лептоспирозом в условиях сильных дождей в эндемичный области.[18]
лечение
Большинство случаев лептоспируса разрешаются спонтанно. Раннее начало приема антибиотиков может предотвратить развитие тяжелого заболевания. Таким образом, в условиях ограниченных ресурсов лечение антибиотиками можно начинать при подозрении на лептоспироз после сбора анамнеза и обследования.[18]
При легком лептоспирозе рекомендуются антибиотики, такие как доксициклин, азитромицин, ампициллин и амоксициллин были основаны исключительно на in vitro тестирование.[8] В 2001 году ВОЗ рекомендовала пероральный доксициклин (от 2 мг / кг до 100 мг каждые 12 часов) в течение пяти-семи дней для пациентов с легким лептоспирозом. Тетрациклин в таких случаях также можно использовать ампициллин и амоксициллин.[37] Однако в районах, где риккетсия и лептоспироз являются эндемическими, азитромицин и доксициклин являются препаратами выбора.[8]
На основании исследования 1988 г. внутривенный (IV) бензилпенициллин (также известный как пенициллин G) рекомендуется для лечения тяжелого лептоспироза.[8] Внутривенный бензилпенициллин (от 30 мг / кг до 1,2 г каждые шесть часов) применяют в течение пяти-семи дней. Амоксициллин, ампициллин и эритромицин также могут использоваться в тяжелых случаях.[37] Цефтриаксон (1 г внутривенно каждые 24 часа в течение семи дней) также эффективен при тяжелом лептоспирозе.[18][8][38] Цефотаксим (1 г внутривенно каждые шесть часов в течение семи дней) и доксициклин (сначала 200 мг, затем 100 мг внутривенно каждые 12 часов в течение семи дней) столь же эффективны, как бензилпенициллин (1,5 миллиона единиц внутривенно каждые шесть часов в течение семи дней).[8][39] Следовательно, нет доказательств различий в снижении смертности при сравнении бензилпенициллина с цефтриаксоном или цефотаксимом.[8] Другое исследование, проведенное в 2007 году, также не показало разницы в эффективности доксициклина (200 мг вначале, затем 100 мг перорально каждые 12 часов в течение семи дней) или азитромицина (2 г в первый день, а затем 1 г в день в течение еще двух дней) при подозрении на лептоспироз. . Разницы в разрешении лихорадки не было, азитромицин переносится лучше, чем доксициклин.[40][41][42]
Амбулаторно назначают доксициклин или азитромицин. Доксициклин может сократить продолжительность лептоспироза на два дня, улучшить симптомы и предотвратить выделение организмов с мочой. Азитромицин и амоксициллин назначают беременным женщинам и детям.[18] Редко Реакция Яриша – Герксхаймера может развиться в первые несколько часов после приема антибиотиков.[8] Однако, по мнению метаанализ проведенного в 2012 году, польза антибиотиков при лечении лептоспироза была неясной, хотя использование антибиотиков может сократить продолжительность болезни на два-четыре дня.[8][41] Другой метаанализ, проведенный в 2013 году, пришел к аналогичному выводу.[8][42]
Для людей с тяжелым лептоспирозом, включая истощение калия с нарушением функции почек, внутривенная гидратация и добавки калия могут предотвратить обезвоживание и гипокалиемия. Когда острая почечная недостаточность происходит раннее начало гемодиализ или перитонеальный диализ может помочь улучшить выживаемость. Для людей с дыхательной недостаточностью интубация трахеи с низким дыхательный объем улучшает выживаемость.[18]
Кортикостероиды были предложены для подавления воспаления при лептоспирозе, потому что Лептоспира инфекция может вызвать высвобождение химические сигналы которые продвигают воспаление кровеносных сосудов в легких. Однако недостаточно доказательств, чтобы определить, полезно ли использование кортикостероидов.[8][43]
Прогноз
Общий риск смерти от лептоспироза составляет 5–10%.[10] У больных желтухой летальность может возрасти до 15%.[25] Для инфицированных, у которых наблюдается спутанность сознания и неврологические признаки, существует высокий риск смерти.[18] Другие факторы, повышающие риск смерти, включают снижение диуреза, возраст старше 36 лет и дыхательную недостаточность.[18] При надлежащем уходе большинство инфицированных полностью выздоравливает. У пациентов с острой почечной недостаточностью после выздоровления может наблюдаться стойкое легкое поражение почек.[18] У пациентов с тяжелым поражением легких риск смерти составляет 50–70%.[8]
В одном исследовании 30% пациентов, выздоровевших от острого лептоспироза, жаловались на длительную усталость, недомогание, слабость, боли в мышцах и головные боли. У 21% этих пациентов эти симптомы продолжались более 2 лет.[18] Проблемы с глазами возникают у 10% вылечившихся от лептоспироза.[25] Эти осложнения варьируются от легких передний увеит до тяжелого панувеита (затрагивающего все три сосудистых слоя глаза) после выздоровления. У 80% инфицированных Лептоспира ДНК обнаруживается в водянистой влаге глаза.[18] Проблемы с глазами обычно имеют хороший прогноз после лечения или они проходят самостоятельно.[25]
Эпидемиология
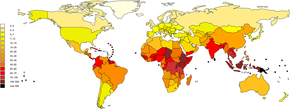
По оценкам, ежегодно происходит один миллион тяжелых случаев лептоспироза, при этом 58 900 случаев смерти. На тяжелые случаи лептоспироза приходится 5-15%.[11] Лептоспироз встречается как в городской, так и в сельской местности в тропический, субтропический, и умеренный регионы.[10] Глобальное бремя лептоспироза для здоровья можно измерить год жизни с поправкой на инвалидность (ДАЛИ). Показатель составляет 42 на 100 000 человек в год, что больше, чем при других заболеваниях, таких как бешенство и филяриоз.[7]
Заболевание постоянно наблюдается в некоторых частях Азии, Океании, Карибского бассейна, Латинской Америки и Африки.[25] Антарктида - единственное место, не пораженное лептоспирозом.[25] В Соединенных Штатах ежегодно регистрируется от 100 до 150 случаев лептоспироза.[44] В 1994 г. лептоспироз перестал быть болезнью, подлежащей регистрации в США, за исключением 36 штатов / территорий, где он распространен, таких как Гавайи, Техас, Калифорния и Пуэрто-Рико.[45] Около 50% зарегистрированных случаев произошли в Пуэрто-Рико. В январе 2013 года лептосприоз был восстановлен как заболевание, подлежащее регистрации на национальном уровне в Соединенных Штатах.[44]
Глобальные показатели заболеваемости лептоспирозом недооцениваются, поскольку в большинстве затронутых стран отсутствует уведомление или уведомление не является обязательным.[18] Другими проблемами являются отличие клинических признаков лептоспироза от других болезней и отсутствие лабораторных диагностических услуг.[46] Социально-экономический статус многих людей в мире тесно связан с недоеданием; последующее отсутствие микроэлементы может привести к повышенному риску заражения и смерти из-за инфекции лептоспироза.[47] Микроэлементы, такие как утюг, кальций, и магний представляют собой важные области для будущих исследований.[47]

Число случаев лептоспироза напрямую связано с количеством выпавших осадков, что делает болезнь сезонной в умеренном климате и круглогодичной в тропическом климате.[7] Риск заражения лептоспирозом зависит от риска распространения болезни в обществе и частоты заражения.[18] В сельской местности сельское хозяйство и животноводство являются основными факторами риска заболевания лептоспирозом.[5] Плохое жилье и неадекватная санитария также увеличивают риск заражения.[18] В тропических и полутропических регионах болезнь часто переходит в широко распространенный после проливных дождей или после наводнения.[7]
История
Заболевание впервые было описано Адольф Вайль в 1886 году, когда он сообщил об «остром инфекционном заболевании с увеличением селезенки, желтухой и нефрит."[17] До описания Вейля болезнь была известна как «рисовое поле». желтуха «в древнекитайском тексте« осенняя лихорадка »,« семидневная лихорадка »,[48] и "Нанукаями высокая температура"[49] в Японии; в Европе и Австралии болезнь ассоциировалась с определенными профессиями и получила такие названия, как «болезнь тростника», «болезнь свиного стада» и «Шламмфибер"(грязевая лихорадка).[48] Исторически это было известно как «черная желтуха»,[50] или «лихорадка молочной фермы» в Новой Зеландии.[51] Лептоспироз считался причиной эпидемии среди Коренные американцы вдоль побережья того, что сейчас Новая Англия в течение 1616–1919 гг. Заболевание, скорее всего, было доведено до Новый мир европейцами.[52]
Лептоспира впервые наблюдался в 1907 г. вскрытие срез ткани почек, сделанный Артуром Стимсоном с использованием окрашивание отложением серебра техника. Он назвал организм Spirocheta interrogans потому что бактерии напоминали вопросительный знак.[48][53] В 1908 году японская исследовательская группа под руководством Риокичи Инада и Ютака Ито впервые определила эту бактерию как возбудителя лептоспироза.[54] и отметил его присутствие у крыс в 1916 году.[55] Японские рабочие угольных шахт часто болеют лептоспирозом. В Японии организм получил название Spirocheta icterohaemorrhagiae. Японская группа также экспериментировала с первыми исследованиями лептоспирусной иммунизации морских свинок. Они продемонстрировали, что, вводя инфицированным морские свинки с сывороткой выздоравливающих людей или коз, пассивный иммунитет может быть предоставлен морским свинкам. В 1917 году японская группа открыла крыс как переносчиков лептоспироза.[48] Не зная о работе японской группы, две немецкие группы независимо и почти одновременно опубликовали свою первую демонстрацию передачи лептоспиральной инфекции у морских свинок в октябре 1915 года. Они назвали организм Spirochaeta nodosa и Spirochaeta Icterogenes соответственно.[48]
Впоследствии лептоспироз был признан болезнью всех видов млекопитающих. В 1933 году голландские рабочие сообщили об изоляции Leptospira canicola который особенно заражает собак. В 1940 году в России впервые был обнаружен штамм, специфически поражающий крупный рогатый скот.[48] В 1942 г. солдаты на Форт-Брэгг, Северная Каролина, были зарегистрированы инфекционные заболевания, вызвавшие сыпь на их берцовые кости. Позже выяснилось, что причиной этого заболевания является лептоспироз.[18] К 1950-м годам количество сероваров, инфицировавших различных млекопитающих, значительно увеличилось. В 1980-х годах лептоспироз был признан ветеринарным заболеванием, имеющим большое экономическое значение.[48]
В 1982 году насчитывалось около 200 сероваров Лептоспира доступны для классификации. В Международный комитет по систематической бактериологии подкомитет по таксономии Лептоспира предложил разделить эти серовары на две большие группы: L. interrogans содержащие патогенные серовары и L. biflexa содержащие сапрогитные серовары.[48] В 1979 году семейство лептоспиральных Leptospiraceae было предложено. В том же году, Лептоспира иллини был реклассифицирован как новый род Лептонема.[48] В 2002 году был придуман «синдром Лептангамуши» для описания ряда перекрывающихся симптомов лептоспироза с Хантавирусная геморрагическая лихорадка с почечным синдромом, и скраб тиф вызванный Ориентиа цуцугамуши.[56][57] В 2005 году, Лептоспира парва был классифицирован как Turneriella.[48] С участием Гибридизация ДНК-ДНК технологии, L. interrogans был разделен на семь видов. Больше Лептоспира виды были обнаружены с тех пор.[48] ВОЗ учредила Справочную группу по эпидемиологии бремени лептоспироза (LERG) для обзора последних эпидемиологических данных о лептоспирозе, разработки модели передачи болезни и выявления пробелов в знаниях и исследованиях. Первое совещание было проведено в 2009 году. В 2011 году LERG подсчитала, что ежегодный уровень заболеваемости лептоспирозом в мире составляет от 5 до 14 случаев на 100 000 населения.[18]
Другие животные
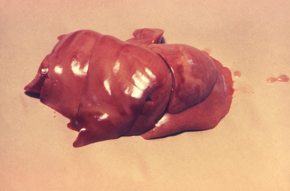

У инфицированных животных могут отсутствовать симптомы легкой или тяжелой степени;[58] Симптомы могут варьироваться в зависимости от вида животного.[15][58] У некоторых животных бактерии живут в репродуктивном тракте, что приводит к передаче инфекции во время спаривания.[15]
Животные также имеют сходные клинические признаки по сравнению с людьми. У собак клинические признаки могут появиться через 5–15 дней. У кошек инкубационный период может быть продлен. Лептоспироз может вызывать аборты у крупного рогатого скота через 2–12 недель, а у свиней - через 1–4 недели. У резервуарных хозяев болезнь протекает в более легкой форме. Чаще всего поражаются почки, печень и репродуктивная система, но могут поражаться и другие органы.[25] У собак острые клинические признаки включают лихорадку, потеря аппетита, дрожь, мышечные боли, слабость и симптомы мочеиспускания. Также могут присутствовать рвота, диарея и боль в животе. На слизистых оболочках могут быть петехии и экхимозы. У собак также может наблюдаться кровотечение из легких. При хронических проявлениях у пораженной собаки симптомы могут отсутствовать. У животных, умерших от лептоспироза, почки могут быть опухшими с серыми и белыми пятнами, крапчатый, или рубцевание. Их печень может быть увеличена на участки смерть клетки. Петехии и экхимозы могут обнаруживаться в различных органах.[25][59] Воспаление кровеносных сосудов, воспаление сердца, менингеальных слоев, покрывающих головной и спинной мозг, и увеит также возможны.[15] Рецидивирующий увеит у лошадей (ЕСВ) - наиболее распространенное заболевание, связанное с Лептоспира инфекция лошадей в Северной Америке и может привести к слепоте.[60][61] ERU - это аутоиммунное заболевание, связанное с антителами против Лептоспира белки LruA и LruB перекрестно реагируют с белками глаза.[60] Прямой эфир Лептоспира может быть извлечен из водянистой или стекловидного тела многих лошадей с Лептоспира-ассоциированный ЕСВ.[61] Риск смерти или инвалидности у инфицированных животных варьируется в зависимости от вида и возраста животных. У взрослых свиней и крупного рогатого скота репродуктивные признаки являются наиболее частыми признаками лептоспироза. До 40% коров могут иметь самопроизвольный аборт. У молодых животных обычно развивается более тяжелое заболевание. Около 80% собак могут выжить после лечения, но выживаемость снижается, если поражены легкие.[25]
ИФА и микроскопические тесты агглютинации чаще всего используются для диагностики лептоспироза у животных. Бактерии можно обнаружить в крови, моче, молоке, печени, почках или других образцах тканей с помощью иммунофлуоресценция или иммуногистохимический или методы полимеразной цепной реакции. Окрашивание серебром или окрашивание иммунозолотым серебром используется для обнаружения Лептоспира в срезах тканей. Организмы плохо окрашиваются Окраска по Граму. Темнопольная микроскопия может использоваться для обнаружения Лептоспира в жидкостях организма, но он не чувствителен и не специфичен для обнаружения организма. Положительный посев на лептоспироз является окончательным, но его наличие ограничено, и результаты посева могут занять 13–26 недель, что ограничивает его полезность. Для серологической диагностики лептоспироза у животных предпочтительны парные образцы в остром периоде и в период выздоровления. Положительный серологический образец абортированного плода также указывает на лептоспироз.[25]
Различные антибиотики, такие как доксициклин, пенициллины, дигидрострептомицин, и стрептомицин использовались для лечения лептоспироза у животных. При тяжелом заболевании может потребоваться жидкостная терапия, переливание крови и респираторная поддержка. Для лошадей с ERU первичное лечение - противовоспалительные препараты.[25][15]
Вакцины против лептоспироза доступны для таких животных, как свиньи, собаки, крупный рогатый скот, овцы и козы. Вакцины для крупного рогатого скота обычно содержат Лептоспира серовар Hardjo и Pomona, вакцины для собак обычно содержат серовар Icterohaemorrhagiae и Canicola. Вакцины, содержащие несколько сероваров, не работают для крупного рогатого скота так же, как вакцины, содержащие один серовар, однако поливалентные вакцины продолжают продаваться.[15] Изоляция инфицированных животных и профилактические антибиотики также эффективны для предотвращения передачи лептоспироза между животными. Экологический контроль и санитария также снижают скорость передачи.[25][15]
использованная литература
- ^ Бергер С (2018). Лептоспироз: глобальный статус. GIDEON Informatics Inc. стр. 7. ISBN 9781498820318.
- ^ Медицинский словарь Мосби (9-е изд.). Elsevier Health Sciences. 2013. с. 697. ISBN 9780323112581. В архиве из оригинала 8 сентября 2017 г.. Получено 21 февраля 2016.
- ^ Маккей Дж. Э. (2001). Комплексное лечение собак. Миннетонка, Миннесота: Творческий паб. Международный. п. 97. ISBN 9781559717830.
- ^ Джеймс В.Д., Элстон Д.М., Бергер Т.Г., Эндрюс Г.К. (2006). Болезни кожи Эндрюса: клиническая дерматология. Сондерс Эльзевир. ISBN 978-0-7216-2921-6.:290
- ^ а б c d е ж г час я j k л м п о Су З.М., Хан Н.А., Сиддики Р. (январь 2020 г.). «Лептоспироз: возрастающее значение в развивающихся странах». Acta Tropica. 201: 105183. Дои:10.1016 / j.actatropica.2019.105183. PMID 31542372.
- ^ а б Макбрайд А.Дж., Атанацио Д.А., Рейс М.Г., Ко А.И. (октябрь 2005 г.). "Лептоспироз". Современное мнение об инфекционных заболеваниях. 18 (5): 376–86. Дои:10.1097 / 01.qco.0000178824.05715.2c. PMID 16148523. S2CID 220576544.
- ^ а б c d е ж г час я j k л м п о п q р s т ты v ш Икс Карпагам КБ, Ганеш Б (январь 2020 г.). «Лептоспироз: забытая тропическая зоонозная инфекция, имеющая значение для общественного здравоохранения - обновленный обзор». Европейский журнал клинической микробиологии и инфекционных заболеваний. 39 (5): 835–846. Дои:10.1007 / s10096-019-03797-4. PMID 31898795. S2CID 209669669.
- ^ а б c d е ж г час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг Лейн, Элисон Б; Доре, Майкл М (2016). «Лептоспироз: клинический обзор доказательной диагностики, лечения и профилактики». Всемирный журнал клинических инфекционных болезней. 6 (4): 61. Дои:10.5495 / wjcid.v6.i4.61. ISSN 2220-3176.
- ^ Фаррар Дж., Хотез П., Юнгханс Т., Канг Дж., Лаллоо Д., Белый Нью-Джерси (2013). Электронная книга Мэнсона по тропическим болезням. Elsevier Health Sciences. п. 438. ISBN 9780702053061. В архиве из оригинала 8 сентября 2017 г.. Получено 2 сентября 2017.
- ^ а б c d Евангелиста К.В., Кобурн Дж. (Сентябрь 2010 г.). «Лептоспира как новый патоген: обзор его биологии, патогенеза и иммунных ответов хозяина». Будущая микробиология. 5 (9): 1413–25. Дои:10.2217 / fmb.10.102. ЧВК 3037011. PMID 20860485.
- ^ а б c d Коста Ф., Хаган Дж. Э., Кальканьо Дж., Кейн М., Торгерсон П., Мартинес-Сильвейра М.С. и др. (2015). «Глобальная заболеваемость и смертность от лептоспироза: систематический обзор». PLOS забытые тропические болезни. 9 (9): e0003898. Дои:10.1371 / journal.pntd.0003898. ЧВК 4574773. PMID 26379143.
- ^ а б c d е ж г час я j k л Picardeau M (май 2017 г.). «Вирулентность зоонозного возбудителя лептоспироза: все еще terra incognita?». Обзоры природы. Микробиология. 15 (5): 297–307. Дои:10.1038 / nrmicro.2017.5. PMID 28260786. S2CID 11626842.
- ^ Chan, O. Y .; Chia, S.E .; Nadarajah, N .; Снг, Э. Х. (16 октября 1987 г.). «Риск лептоспироза у работников коммунальных служб и канализации». Анналы Медицинской академии, Сингапур. 16 (4): 586–90. PMID 3446001.
- ^ а б c Тейшейра А.Ф., Фернандес Л.Г., Кавенаг М.Ф., Такахаши М.Б., Сантос Дж.С., Пассалия Ф.Дж. и др. (Июль 2019). «Адъювантные лептоспиральные вакцины: проблемы и будущее развитие новых лептоспирозных вакцин». Вакцина. 37 (30): 3961–3973. Дои:10.1016 / j.vaccine.2019.05.087. PMID 31186193.
- ^ а б c d е ж г час я j k л Эллис WA (2015). «Лептоспироз животных». Актуальные темы микробиологии и иммунологии. 387: 99–137. Дои:10.1007/978-3-662-45059-8_6. ISBN 978-3-662-45058-1. PMID 25388134.
- ^ Slack A (июль 2010 г.). "Лептоспироз". Австралийский семейный врач. 39 (7): 495–8. PMID 20628664.
- ^ а б Вейль А. (1886 г.). «Über eine eigenthümliche, mit Milztumor, Icterus und Nephritis einhergehende, острый Infektionskrankheit» [О странном остром инфекционном заболевании, сопровождающемся отеком селезенки, желтухой и нефритом]. Deutsches Archiv für Klinische Medizin (на немецком). 39: 209–232.
- ^ а б c d е ж г час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль я ан ао ap Хааке Д.А., Леветт П.Н. (25 мая 2015 г.). «Лептоспироз у человека». Актуальные темы микробиологии и иммунологии. 387 (387): 65–97. Дои:10.1007/978-3-662-45059-8_5. ISBN 978-3-662-45058-1. ЧВК 4442676. PMID 25388133.
- ^ «Информационный бюллетень о лептоспирозе». Европейский центр профилактики и контроля заболеваний. Получено 5 сентября 2020.
- ^ Вагонер Дж. Дж., Пинский Б. А. (октябрь 2016 г.). «Молекулярная диагностика лептоспироза человека». Современное мнение об инфекционных заболеваниях. 29 (5): 440–5. Дои:10.1097 / QCO.0000000000000295. ЧВК 5127924. PMID 27537829.
- ^ а б Кальеро Дж., Вильянуэва С.Ю., Мацуи М. (20 июня 2018 г.). «Патофизиология лептоспироза: буря цитокинов». Границы клеточной и инфекционной микробиологии. 8 (204): 204. Дои:10.3389 / fcimb.2018.00204. ЧВК 6019470. PMID 29974037.
- ^ а б c Беннетт Дж. Э., Рафаэль Д., Мартин Дж. Б., Барт Дж. К. (2015). «223». Принципы и практика инфекционных заболеваний Манделла, Дугласа и Беннета (Восьмое изд.). Эльзевир. С. 2541–2549. ISBN 978-1-4557-4801-3.
- ^ Кэмерон CE (2015). «Лептоспиральное строение, физиология и метаболизм». Актуальные темы микробиологии и иммунологии. 387: 21–41. Дои:10.1007/978-3-662-45059-8_3. ISBN 978-3-662-45058-1. PMID 25388131.
- ^ а б c Кайми К., Руйбал П. (февраль 2020 г.). «Leptospira spp., Род на стадии разнообразия и расширения геномных данных». Инфекция, генетика и эволюция. 81: 104241. Дои:10.1016 / j.meegid.2020.104241. PMID 32061688.
- ^ а б c d е ж г час я j k л м Спиклер А. Р., Ледом Ларсон К. Р. (октябрь 2013 г.). «Лептоспироз (Информационный бюллетень)» (PDF). Центр продовольственной безопасности и общественного здоровья. В архиве (PDF) из оригинала 24 ноября 2014 г.. Получено 15 марта 2019.
- ^ Барраган В., Оливас С., Кейм П., Пирсон Т. (октябрь 2017 г.). «Критические пробелы в знаниях в нашем понимании круговорота окружающей среды и передачи Leptospira spp». Прикладная и экологическая микробиология. 83 (19). Дои:10.1128 / AEM.01190-17. ЧВК 5601346. PMID 28754706.
- ^ Аллан К.Дж., Биггс Х.М., Халлидей Дж. Э., Казвала Р. Р., Маро В. П., Кливленд С., Крамп Дж. А. (2015). «Эпидемиология лептоспироза в Африке: систематический обзор забытого зооноза и парадигма« единого здоровья »в Африке». PLOS забытые тропические болезни. 9 (9): e0003899. Дои:10.1371 / journal.pntd.0003899. ЧВК 4569256. PMID 26368568.
- ^ а б c d е Чин В.К., Басир Р., Нордин С.А., Абдулла М., Секави З. (март 2019 г.). "Патология и уклонение от иммунитета хозяина во время лептоспироза человека: обзор". Международная микробиология. 23 (2): 127–136. Дои:10.1007 / s10123-019-00067-3. PMID 30875033. S2CID 78095369.
- ^ Song AT, Abas L, Andrade LC, Andraus W, D'Albuquerque LA, Abdala E (февраль 2016 г.). «Первое сообщение о лептоспирозе после трансплантации печени». Инфекционное заболевание трансплантата. 18 (1): 137–40. Дои:10.1111 / тид.12490. PMID 26671230.
- ^ Пулият Дж., Сингх С. (октябрь 2012 г.). «Лептоспироз при беременности». Европейский журнал клинической микробиологии и инфекционных заболеваний. 31 (10): 2491–6. Дои:10.1007 / s10096-012-1625-7. PMID 22549729. S2CID 14033595.
- ^ Карлес Г., Монтойя Е., Жоли Ф., Пено С. (1995). «[Лептоспироз и беременность. Одиннадцать случаев во Французской Гайане]». Journal de Gynécologie, Obstétrique et Biologie de la Reproduction. 24 (4): 418–21. PMID 7650320.
- ^ Koe SL, Tan KT, Tan TC (февраль 2014 г.). «Лептоспироз при беременности с патологическими изменениями кардиотокографии плода». Сингапурский медицинский журнал. 55 (2): e20-4. Дои:10.11622 / smedj.2013194. ЧВК 4291937. PMID 24712035.
- ^ Шакед Ю., Шпильберг О., Самра Д., Самра Ю. (август 1993 г.). «Лептоспироз при беременности и его влияние на плод: история болезни и обзор». Клинические инфекционные болезни. 17 (2): 241–3. Дои:10.1093 / Clinids / 17.2.241. PMID 8399874.
- ^ Кумар СС (2013). "7" (PDF). Индийские рекомендации по диагностике и лечению лептоспироза человека. Индия. С. 23–29. Архивировано из оригинал (PDF) 25 декабря 2016 г.. Получено 16 ноября 2019.
- ^ а б c Сюй И, Е Цюй (апрель 2018 г.). «Вакцины против лептоспироза человека в Китае». Человеческие вакцины и иммунотерапевтические препараты. 14 (4): 984–993. Дои:10.1080/21645515.2017.1405884. ЧВК 5893195. PMID 29148958.
- ^ Abd Rahim MA, Zaki AM, Atil A, Azme MH, Him NA, Rahim SS, Jeffree MS, Ahmad N, Hassan MR. «Эффективность антибиотикопрофилактики лептоспироза у взрослых: систематический обзор». Малазийский журнал прикладных наук. 3 (2): 46–56. Получено 1 марта 2020.
- ^ а б Рекомендуемые ВОЗ стратегии профилактики инфекционных заболеваний и борьбы с ними. Всемирная организация здравоохранения - Департамент по контролю, профилактике и искоренению инфекционных заболеваний. 2001. с. 104. Архивировано с оригинал 5 мая 2019 г.
- ^ Panaphut T, Domrongkitchaiporn S, Vibhagool A, Thinkamrop B, Susaengrat W (июнь 2003 г.). «Цефтриаксон в сравнении с пенициллином натрия g для лечения тяжелого лептоспироза». Клинические инфекционные болезни. 36 (12): 1507–13. Дои:10.1086/375226. PMID 12802748.
- ^ Супуттамонгкол Ю., Ниваттаякуль К., Суттинонт С., Лосуваналук К., Лимпайбоун Р., Чиеракул В. и др. (Ноябрь 2004 г.). «Открытое рандомизированное контролируемое исследование пенициллина, доксициклина и цефотаксима у пациентов с тяжелым лептоспирозом». Клинические инфекционные болезни. 39 (10): 1417–24. Дои:10.1086/425001. PMID 15546074.
- ^ Phimda K, Hoontrakul S, Suttinont C, Chareonwat S, Losuwanaluk K, Chueasuwanchai S и др. (Сентябрь 2007 г.). «Доксициклин против азитромицина для лечения лептоспироза и сыпного тифа». Противомикробные препараты и химиотерапия. 51 (9): 3259–63. Дои:10.1128 / AAC.00508-07. ЧВК 2043199. PMID 17638700.
- ^ а б Бретт-Майор Д.М., Колдрен Р. (февраль 2012 г.). «Антибиотики от лептоспироза». Кокрановская база данных систематических обзоров (2): CD008264. Дои:10.1002 / 14651858.CD008264.pub2. PMID 22336839.
- ^ а б Чаран Дж., Саксена Д., Мулла С., Ядав П. (май 2013 г.). «Антибиотики для лечения лептоспироза: систематический обзор и метаанализ контролируемых исследований». Международный журнал профилактической медицины. 4 (5): 501–10. ЧВК 3733179. PMID 23930159.
- ^ Родриго К., Лакшита де Сильва Н., Гунаратне Р., Самарасекара К., Виджесингхе I, Парттипан Б., Раджапаксе С. (декабрь 2014 г.). «Высокие дозы кортикостероидов при тяжелом лептоспирозе: систематический обзор». Труды Королевского общества тропической медицины и гигиены. 108 (12): 743–50. Дои:10.1093 / trstmh / tru148. PMID 25266477.
- ^ а б «Медицинские работники - Техническая информация по лептоспирозу». Центры по контролю и профилактике заболеваний (CDC). 9 ноября 2017. Архивировано с оригинал 11 января 2019 г.. Получено 28 апреля 2019.
- ^ Guerra MA (сентябрь 2013 г.). «Лептоспироз: перспективы общественного здравоохранения». Биологические препараты. 41 (5): 295–7. Дои:10.1016 / j.biologicals.2013.06.010. ЧВК 4629849. PMID 23850378.
- ^ "ВОЗ | Справочная группа по эпидемиологии бремени лептоспироза (LERG)". www.who.int. В архиве из оригинала 17 ноября 2017 г.. Получено 30 ноября 2017.
- ^ а б Герман Х.С., Мехта С., Карденас В.Б., Стюарт-Ибарра А.М., Финкельштейн Ю.Л. (июль 2016 г.). «Микроэлементы и лептоспироз: обзор современных данных». PLOS забытые тропические болезни. 10 (7): e0004652. Дои:10.1371 / journal.pntd.0004652. ЧВК 4936698. PMID 27387046.
- ^ а б c d е ж г час я j k Адлер Б (2015). «История лептоспироза и лептоспир». Актуальные темы микробиологии и иммунологии. 387: 1–9. Дои:10.1007/978-3-662-45059-8_1. ISBN 978-3-662-45058-1. PMID 25388129.
- ^ Иллюстрированный медицинский словарь Дорланда. Филадельфия: Эльзевир / Сондерс. 2012. с. 1231. ISBN 9781455709854. В архиве из оригинала 8 сентября 2017 г.. Получено 21 февраля 2016.
- ^ Клэпхэм Д. (2004). Малые источники воды: практическое руководство. Рутледж. п. 125. ISBN 9781134457496. В архиве из оригинала 8 сентября 2017 г.. Получено 21 февраля 2016.
- ^ Рождество BW, Теннент РБ, Линдси PG (май 1974 г.). «Лихорадка молочной фермы в Новой Зеландии: локальная вспышка лептоспироза человека». Медицинский журнал Новой Зеландии. 79 (514): 901–4. PMID 4527727.
- ^ Марр Дж. С., Кэти Дж. Т. (февраль 2010 г.). "Новая гипотеза причины эпидемии среди коренных американцев, Новая Англия, 1616-1619 гг.". Возникающие инфекционные заболевания. 16 (2): 281–6. Дои:10.3201 / eid1602.090276. ЧВК 2957993. PMID 20113559.
- ^ Стимсон AM (1907). «Замечание об организме, обнаруженном в тканях желтой лихорадки». Отчеты общественного здравоохранения. 22 (18): 541. Дои:10.2307/4559008. JSTOR 4559008.
- ^ Инада Р., Ито И (1908). «Отчет об открытии возбудителя (нового вида спирохеты) болезни Вейля». Токио Иджишинси. 1915: 351–60.
- ^ Инада Р., Идо Й, Хоки Р., Канеко Р., Ито Х. (март 1916 г.). «Этиология, способ заражения и специфическая терапия болезни Вейля (спирохотоз Icterohæmorrhagica)». Журнал экспериментальной медицины. 23 (3): 377–402. Дои:10.1084 / jem.23.3.377. ЧВК 2125418. PMID 19867994.
- ^ Панис-Мондольфи А.Е., Родригес-Моралес А.Дж., Блом Дж., Маркес М., Вилламил-Гомес В.Е. (июль 2016 г.). «Синдром ЧикДенМазика: проблема диагностики арбовирусных инфекций в условиях сопутствующих эпидемий». Анналы клинической микробиологии и противомикробных препаратов. 15 (1): 42. Дои:10.1186 / s12941-016-0157-x. ЧВК 4957883. PMID 27449770.
- ^ «284184004: синдром Лептангамуши (расстройство)». Архивировано из оригинал 18 ноября 2019 г.. Получено 18 ноября 2019.
- ^ а б "Лептоспироз" (PDF). Центр продовольственной безопасности и общественного здоровья. Октябрь 2013. В архиве (PDF) из оригинала 24 ноября 2014 г.. Получено 8 ноября 2014.
- ^ Клопфляйш Р., Кон Б., Плог С., Вайнгарт С., Нёклер К., Майер-Шолль А., Грубер А.Д. (декабрь 2010 г.). «Возникающий легочный геморрагический синдром у собак: похож на лептоспиральный легочный геморрагический синдром человека?». Международная ветеринарная медицина. 2010: 928541. Дои:10.4061/2010/928541. ЧВК 3025382. PMID 21274452.
- ^ а б Цуэрнер Р.Л. (2015). "Ответ хозяина на Лептоспира инфекция". Актуальные темы микробиологии и иммунологии. 387: 223–50. Дои:10.1007/978-3-662-45059-8_9. ISBN 978-3-662-45058-1. PMID 25388137.
- ^ а б Divers TJ, Chang YF, Irby NL, Smith JL, Carter CN (май 2019 г.). «Лептоспироз: важное инфекционное заболевание североамериканских лошадей». Ветеринарный журнал лошадей. 51 (3): 287–292. Дои:10.1111 / evj.13069. PMID 30629756. S2CID 58578433.
внешние ссылки
- "Лептоспироз". НАС.Центр по контролю и профилактике заболеваний. 21 ноября 2018.
- "Лептоспира". Браузер таксономии NCBI. 171.
| Классификация | |
|---|---|
| Внешние ресурсы |
