Дефицит глюкозо-6-фосфатдегидрогеназы - Glucose-6-phosphate dehydrogenase deficiency
| Дефицит глюкозо-6-фосфатдегидрогеназы | |
|---|---|
| Другие имена | Фавизм[1] |
 | |
| Глюкозо-6-фосфатдегидрогеназа | |
| Специальность | Медицинская генетика |
| Симптомы | Желтоватая кожа, темная моча, одышка[1] |
| Осложнения | Анемия, желтуха новорожденных[2][1] |
| Обычное начало | Через несколько дней после срабатывания триггера[2] |
| Причины | Генетический (Х-сцепленный рецессивный )[1] |
| Факторы риска | Вызваны инфекции, некоторые лекарства, стресс, продукты, такие как бобы[1][3] |
| Диагностический метод | На основании симптомов, анализа крови, генетическое тестирование[2] |
| Дифференциальный диагноз | Дефицит пируваткиназы, наследственный сфероцитоз, серповидноклеточная анемия[2] |
| лечение | Избегание триггеров, лекарств от инфекций, прекращение приема лекарств-нарушителей, переливание крови[3] |
| Частота | 400 миллионов[1] |
| Летальные исходы | 33,000 (2015)[4] |
Дефицит глюкозо-6-фосфатдегидрогеназы (G6PDD) является врожденная ошибка обмена веществ что предрасполагает к распад красных кровяных телец.[1] В большинстве случаев у пораженных нет симптомов.[3] После определенного триггера такие симптомы, как желтоватая кожа, темная моча, одышка, может развиться чувство усталости.[1][2] Осложнения могут включать: анемия и желтуха новорожденных.[2] У некоторых людей никогда не бывает симптомов.[3]
Это Х-сцепленный рецессивный расстройство, приводящее к дефектному глюкозо-6-фосфатдегидрогеназа фермент.[1] Распад эритроцитов может быть вызван: инфекции, определенные лекарства, стресс или продукты, такие как бобы.[1][3] В зависимости от конкретного мутация тяжесть состояния может быть разной.[2] Диагноз основывается на симптомах и подтверждается анализами крови и генетическое тестирование.[2]
Важно избегать триггеров.[3] Лечение острых эпизодов может включать прием лекарств от инфекции, прекращение приема лекарств, вызывающих нарушение, или переливание крови.[3] Желтуху у новорожденных можно лечить с помощью били огни.[2] Перед приемом некоторых лекарств, таких как: примахин, принимаются.[2]
Во всем мире этим заболеванием страдают около 400 миллионов человек.[1] Это особенно распространено в некоторых частях Африки, Азии, Средиземноморье, а Средний Восток.[1] Мужчины болеют чаще, чем женщины.[1] Считается, что в 2015 году это привело к смерти 33 000 человек.[4]
Признаки и симптомы
Большинство людей с дефицитом G6PD бессимптомный.

Большинство людей, у которых развиваются симптомы, - мужчины из-за Х-связанный тип наследования, но женщины-носители могут пострадать из-за неблагоприятных лионизация, где случайная инактивация Х-хромосомы в определенных клетках создает популяцию G6PD-дефицитных красные кровяные клетки сосуществование с незатронутыми эритроцитами. У женщины с одной пораженной Х-хромосомой наблюдается дефицит примерно половины эритроцитов. Однако в редких случаях, включая двойной X-дефицит, соотношение может быть намного больше половины, что делает человека почти таким же чувствительным, как и мужчины.
Распад красных кровяных телец (также известный как гемолиз ) при дефиците G6PD может проявляться несколькими способами, в том числе следующими:
- Длительный неонатальная желтуха, возможно, приведет к ядерная желтуха (возможно, самое серьезное осложнение дефицита G6PD)
- Гемолитические кризы в ответ на:
- Болезнь (особенно инфекции)
- Определенный наркотики (см. ниже)
- Определенные продукты, особенно бобы, откуда слово фавизм происходит
- Некоторые химические вещества
- Диабетический кетоацидоз
- Гемоглобинурия (красная или коричневая моча)
- Очень серьезные кризисы могут вызвать острая почечная недостаточность
Фавизм является гемолитической реакцией на потребление фасоли, также известной как бобы. Хотя все люди с фавизмом демонстрируют дефицит G6PD, не все люди с дефицитом G6PD проявляют фавизм. Известно, что это состояние чаще встречается у младенцев и детей, и генетический вариант G6PD может влиять на химическую чувствительность.[5] Помимо этого, особенности химической связи между фавизмом и G6PD до конца не изучены.
Причина
Триггеры
Носители основной мутации не проявляют никаких симптомов, если их эритроциты не подвергаются воздействию определенных триггеров, которые могут быть четырех основных типов:
- Еда (фасоль - это клеймо триггер для носителей мутации G6PD),
- Некоторые лекарства, включая аспирин, хинин и другие противомалярийные препараты полученный из хинина.
- Шарики от моли (нафталин )[6]
- Стресс от бактериальный или вирусная инфекция.[7]
Наркотики
Многие вещества потенциально вредны для людей с дефицитом G6PD. Вариабельность реакции на эти вещества затрудняет индивидуальные прогнозы. Противомалярийные препараты которые могут вызвать острый гемолиз у людей с дефицитом G6PD, включают: примахин, памахин, хлорохин, и гидроксихлорохин.[8] Имеются данные о том, что другие противомалярийные средства также могут усугублять дефицит G6PD, но только в более высоких дозах. Сульфаниламиды (такие как сульфаниламид, сульфаметоксазол, и мафенид ), тиазолесульфон, метиленовый синий, и нафталин также следует избегать людям с дефицитом G6PD, поскольку они противодействуют синтезу фолиевой кислоты, как следует анальгетики (такие как феназопиридин и ацетанилид ) и несколько несульфаминовых антибиотиков (налидиксовая кислота, нитрофурантоин, изониазид, дапсон, и фуразолидон ).[9][10][11] Хна известно, что он вызывает гемолитический криз у младенцев с дефицитом G6PD.[12] Расбурикасе также противопоказан при дефиците G6PD. Высокая доза внутривенный витамин C также известно, что он вызывает гемолиз у носителей с дефицитом G6PD;[13][14] таким образом, тестирование на дефицит G6PD является рутинным перед введением доз 25 г или более.
Генетика
Два варианта (G6PD A- и G6PD Mediterranean) наиболее распространены в популяциях людей. G6PD A- встречается у 10% африканцев и афроамериканцев, в то время как G6PD Mediterranean преобладает на Ближнем Востоке. Известное распространение мутировавшего аллеля в значительной степени ограничено людьми средиземноморского происхождения (испанцы, итальянцы, греки, армяне, евреи-сефарды и другие семитские народы).[15] Считается, что оба варианта проистекают из сильного защитного эффекта от Плазмодий falciparum и Плазмодий вивакс малярия.[16] Это особенно часто встречается у курдского еврейского населения, где примерно 1 из 2 мужчин страдает этим заболеванием, и такое же количество женщин являются носителями.[7] Это также распространено в афроамериканец, Саудовский, Сардинский мужчины, некоторые африканские группы населения и азиатские группы.[7]
Все мутации, вызывающие дефицит G6PD, обнаруживаются на длинном плече Х хромосома, на полосе Xq28. Ген G6PD охватывает около 18,5 килобазы.[10] Хорошо известны и описаны следующие варианты и мутации:
| Описательные мутации | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Мутация | Ген | Протеин | |||||||
| Обозначение | Короткое имя | Изоформа G6PD-белок | OMIM-код | Тип | Подтип | Должность | Должность | Изменение структуры | Изменение функции |
| G6PD-A (+) | Gd-A (+) | G6PD A | +305900.0001 | Нуклеотидный полиморфизм | А →г | 376 (Экзон 5) | 126 | Аспарагин →Аспарагиновая кислота (ASN126ASP) | Нет дефекта фермента (вариант) |
| G6PD-A (-) | Gd-A (-) | G6PD A | +305900.0002 | Замена нуклеотида | г →А | 376 (Экзон 5) и 202 | 68 и 126 | Валин →Метионин (VAL68MET) Аспарагин →Аспарагиновая кислота (ASN126ASP) | |
| G6PD-Средиземноморье | Gd-Med | G6PD B | +305900.0006 | Замена нуклеотида | C →Т | 563 (Экзон 6) | 188 | Серин →Фенилаланин (SER188PHE) | II класс |
| G6PD-Кантон | Gd-Canton | G6PD B | +305900.0021 | Замена нуклеотида | г →Т | 1376 | 459 | Аргинин →Лейцин (ARG459LEU) | II класс |
| G6PD-Chatham | Б-г-Чатам | G6PD | +305900.0003 | Замена нуклеотида | г →А | 1003 | 335 | Аланин →Треонин (ALA335THR) | II класс |
| G6PD-Cosenza | Gd-Cosenza | G6PD B | +305900.0059 | Замена нуклеотида | г →C | 1376 | 459 | Аргинин →Пролин (ARG459PRO) | G6PD-активность <10%, следовательно, большая часть пациентов. |
| G6PD-Mahidol | Gd-Mahidol | G6PD | +305900.0005 | Замена нуклеотида | г →А | 487 (Экзон 6) | 163 | Глицин →Серин (GLY163SER) | III класс |
| G6PD-Орисса | Б-г-Орисса | G6PD | +305900.0047 | Замена нуклеотида | C →г | 131 | 44 | Аланин →Глицин (ALA44GLY) | Поражено место связывания НАДФ. Более высокая стабильность, чем у других вариантов. |
| G6PD-Asahi | Б-г-Асахи | G6PD A- | +305900.0054 | Замена нуклеотида (несколько) | А →г ± г →А | 376 (Экзон 5) 202 | 126 68 | Аспарагин →Аспарагиновая кислота (ASN126ASP) Валин →Метионин (VAL68MET) | III класс. |
Патофизиология
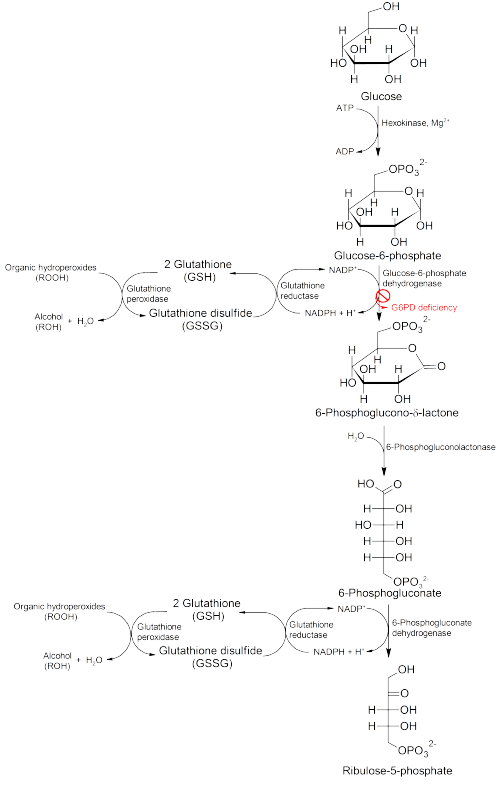
Глюкозо-6-фосфатдегидрогеназа (G6PD) представляет собой фермент в пентозофосфатный путь (см. изображение, также известное как шунтирующий путь HMP). G6PD конвертирует глюкозо-6-фосфат в 6-фосфоглюконо-δ-лактон и является ферментом, ограничивающим скорость этого метаболический путь что поставляет сокращение энергии для клеток, поддерживая уровень восстановленной формы кофермент никотинамидадениндинуклеотидфосфат (НАДФН). НАДФН, в свою очередь, поддерживает подачу уменьшенного глутатион в клетках, который используется для удаления свободных радикалов, вызывающих окислительный повреждение.
Путь G6PD / NADPH - это только источник восстановленного глутатиона в красных кровяных тельцах (эритроциты ). Роль эритроцитов в качестве переносчиков кислорода подвергает их значительному риску повреждения от окисляющих свободных радикалов, за исключением защитного эффекта G6PD / NADPH / глутатиона.
Следовательно, люди с дефицитом G6PD подвержены риску гемолитическая анемия в штатах окислительный стресс. Окислительный стресс может быть результатом инфекции и химического воздействия медикамент и определенные продукты. Бобы, например, бобы, содержат высокий уровень Vicine, божественный, коницин и изурамил, все из которых создают окислители.[17]
Когда все остальное уменьшено глутатион потребляется, ферменты и другие белки (в том числе гемоглобин ) впоследствии повреждаются окислителями, что приводит к перекрестному связыванию и отложению белка в красном клеточные мембраны. Поврежденные эритроциты фагоцитированный и изолированы (выведены из обращения) в селезенка. Гемоглобин метаболизируется до билирубин (вызывая желтуха при высоких концентрациях). Эритроциты редко распадаются в кровотоке, поэтому гемоглобин редко выводится непосредственно из организма. почка, но это может произойти в тяжелых случаях, вызывая острая травма почек.
Дефицит G6PD в альтернативном пути вызывает накопление глюкозы, и, таким образом, происходит увеличение конечные продукты с улучшенным гликированием (ВОЗРАСТ). Дефицит также снижает количество НАДФН, который необходим для образования оксида азота (NO). Высокая распространенность сахарный диабет 2 типа и гипертония у афро-карибских жителей на Западе может быть напрямую связано с распространением дефицита G6PD в этих популяциях.[18]
Хотя женщины-носители могут иметь легкую форму дефицита G6PD (в зависимости от степени инактивации незатронутой Х-хромосомы - см. лионизация ) описаны гомозиготные самки; у этих самок встречается редкий иммунное расстройство названный хроническая гранулематозная болезнь (CGD).
Диагностика
Диагноз обычно подозревают, когда у пациентов из определенных этнических групп (см. Эпидемиологию) развиваются анемия, желтуха и симптомы гемолиз после проблем по любой из вышеперечисленных причин, особенно при наличии положительного семейного анамнеза.
Как правило, тесты включают:
- Полный анализ крови и ретикулоцит считать; при активном дефиците G6PD, Тела Heinz можно увидеть в красные кровяные клетки на мазок крови;
- Ферменты печени (чтобы исключить другие причины желтуха );
- Лактатдегидрогеназа (повышенный уровень гемолиза и маркер тяжести гемолиза)
- Гаптоглобин (уменьшился гемолиз);
- А "прямой антиглобулиновый тест "(Тест Кумбса) - он должен быть отрицательным, так как гемолиз в G6PD не является иммуноопосредованным;
Когда есть достаточные основания подозревать G6PD, прямой тест на G6PD является "Точечный флуоресцентный тест Бейтлера ", который в значительной степени заменил более старый тест (тест обесцвечивания красителя Мотульского). Другие возможности - прямое тестирование ДНК и / или секвенирование гена G6PD.
В Флуоресцентный точечный тест Бейтлера это быстрый и недорогой тест, который визуально определяет НАДФН производства G6PD под ультрафиолетовое излучение. Когда пятно крови не флюоресцирует, тест положительный; он может быть ложноотрицательным у пациентов с активным гемолизом. Следовательно, это можно сделать только через 2–3 недели после гемолитического эпизода.
Когда макрофаг в селезенке идентифицирует эритроциты с тельцом Хайнца, он удаляет осадок и небольшой кусочек мембраны, что приводит к характеристике "кусать клетки ". Однако, если образуется большое количество тельцов Хайнца, как в случае дефицита G6PD, некоторые тельца Хайнца, тем не менее, будут видны при просмотре эритроцитов, окрашенных кристаллическим фиолетовым. Этот простой и недорогой тест может привести к первоначальному презумпция дефицита G6PD, что может быть подтверждено другими тестами.
Классификация
В Всемирная организация здоровья классифицирует генетические варианты G6PD на пять классов, первые три из которых являются состояниями дефицита.[19]
- Класс I: тяжелый дефицит (активность <10%) с хронической (несфероцитарной) гемолитической анемией.
- Класс II: тяжелый дефицит (активность <10%) с периодическим гемолизом
- Класс III: умеренный дефицит (активность 10-60%), гемолиз только со стрессорами
- Класс IV: вариант без дефицита, без клинических последствий
- Класс V: повышенная активность ферментов, без клинических последствий
Дифференциальный диагноз
Дефицит 6-фосфоглюконатдегидрогеназы (6PGD) имеет схожие симптомы и часто ошибочно принимается за дефицит G6PD, поскольку пораженный фермент находится в одном и том же пути, однако эти заболевания не связаны и могут быть обнаружены у одного человека.
лечение
Самая важная мера - это профилактика - отказ от лекарств и продуктов, вызывающих гемолиз. Вакцинация против некоторых распространенных патогенов (например, гепатит А и гепатит Б ) может предотвратить атаки, вызванные инфекцией.[20]
В острой фазе гемолиза, переливание крови может быть необходимо, или даже диализ в острая почечная недостаточность. Переливание крови является важной симптоматической мерой, так как перелитые эритроциты обычно не имеют дефицита G6PD и будут жить нормальной продолжительностью жизни в кровотоке реципиента. Пострадавшим следует избегать таких лекарств, как аспирин.
Некоторым пациентам может быть полезно удаление селезенка (спленэктомия ),[21] так как это важное место разрушения эритроцитов. Фолиевая кислота следует использовать при любом расстройстве с высокой активностью эритроцитов. Несмотря на то что витамин Е и селен обладают антиоксидантными свойствами, их использование не снижает выраженности дефицита G6PD.
Прогноз
Люди с дефицитом G6PD, по-видимому, не заболевают какими-либо заболеваниями чаще, чем другие люди, и могут иметь меньший риск заражения, чем другие люди. ишемическая болезнь сердца и цереброваскулярное заболевание.[22]
Эпидемиология
Дефицит G6PD является вторым по распространенности дефектом ферментов человека после ALDH2 дефицит, присутствующий у более чем 400 миллионов человек во всем мире.[23] Дефицит G6PD привел к 4 100 случаям смерти в 2013 году и 3 400 случаям смерти в 1990 году.[24] Больше всего страдают жители Африки, Ближнего Востока и Южной Азии, в том числе те, кто имеет эти предки.[25][26] Побочным эффектом этого заболевания является то, что оно защищает от малярия,[27] в частности форма малярии, вызванная Плазмодий falciparum, самая смертоносная форма малярии. Аналогичная связь существует между малярией и серповидноклеточная анемия. Одна теория, объясняющая это, заключается в том, что клетки, инфицированные Плазмодий паразиты выводятся быстрее селезенка. Это явление может дать носителям дефицита G6PD эволюционное преимущество за счет повышения их приспособленности в эндемичных по малярии средах. Исследования in vitro показали, что Плазмодий falciparum очень чувствителен к окислительному повреждению. Это основа для другой теории, заключающейся в том, что генетический дефект придает устойчивость из-за того, что хозяин с дефицитом G6PD имеет более высокий уровень окислительных агентов, которые, хотя обычно переносятся хозяином, смертельны для паразита.[28]
История
Современное понимание этого состояния началось с анализа пациентов, проявлявших чувствительность к примахин.[29] Обнаружение дефицита G6PD во многом зависело от тестирования заключенных-добровольцев в Государственная тюрьма Иллинойса, тип исследования, который сегодня считается неэтичным и не может быть проведен. Когда некоторым заключенным вводили препарат примахин, у некоторых начиналось гемолитическая анемия но другие этого не сделали. Несмотря на эти результаты, военные США широко применяли препарат во время корейской войны, чтобы предотвратить рецидив инфекции, вызванный Плазмодий вивакс гипнозоиты. Многочисленные случаи гемолитической анемии наблюдались у американских солдат североафриканского и средиземноморского происхождения.[30]
После изучения механизма через Cr51 При тестировании было окончательно показано, что гемолитический эффект примахина был вызван внутренним дефектом эритроцитов.[31]
Общество и культура
И в легендах, и в мифологии фавизм известен с древних времен. Священники разных Греко-римская эпоха культам было запрещено есть или даже упоминать бобы, и Пифагор было строгое правило, чтобы присоединиться к обществу Пифагорейцы нужно было ругаться с фасолью.[32] Предположительно, этот запрет был вызван тем, что бобы напоминали мужские гениталии, но возможно, что это произошло из-за веры в то, что бобы и люди были созданы из одного материала.[33]
использованная литература
- ^ а б c d е ж г час я j k л м «Дефицит глюкозо-6-фосфатдегидрогеназы». Домашний справочник по генетике. 6 декабря 2017 г.. Получено 10 декабря 2017.
- ^ а б c d е ж г час я j «Дефицит глюкозо-6-фосфатдегидрогеназы». NORD (Национальная организация по редким заболеваниям). 2017. Получено 11 декабря 2017.
- ^ а б c d е ж г «Дефицит глюкозо-6-фосфатдегидрогеназы». Информационный центр по генетическим и редким заболеваниям (GARD). 2017. Получено 10 декабря 2017.
- ^ а б ГББ 2015 Смертность и причины смерти, соавторы. (8 октября 2016 г.). «Ожидаемая продолжительность жизни на глобальном, региональном и национальном уровнях, смертность от всех причин и смертность от конкретных причин для 249 причин смерти, 1980–2015 годы: систематический анализ для исследования глобального бремени болезней 2015 года». Ланцет. 388 (10053): 1459–1544. Дои:10.1016 / с0140-6736 (16) 31012-1. ЧВК 5388903. PMID 27733281.
- ^ Луццатто, Л. "ДЕГИДРОГЕНАЗА ГЛЮКОЗЫ-6-ФОСФАТА". Продвинутая медицина-Двенадцать: Материалы конференции, состоявшейся в Королевском колледже врачей Лондона, 11–14 февраля 1985 г. Vol. 21. Черчилль Ливингстон, 1986.
- ^ «Триггеры кризиса G6PD» (PDF). Сиднейский местный округ здравоохранения.
- ^ а б c Дефицит глюкозо-6-фосфатдегидогеназы (G6PD) на сайте Консорциума еврейских генетических болезней (JGDC) [1].В архиве 1 июля 2017 г. Wayback Machine
- ^ Джонс и Бартлетт; Издатели, Джонс и Бартлетт (2010). Справочник медсестры по лекарствам, 2010 г.. Джонс и Бартлетт Обучение. п. 497. ISBN 978-0-7637-7900-9.
- ^ Фрэнк Дж. Э. (октябрь 2005 г.). «Диагностика и лечение дефицита G6PD». Am Fam Врач. 72 (7): 1277–82. PMID 16225031.
- ^ а б Уоррелл, Дэвид А .; Тимоти М. Кокс; Джон Д. Ферт; Эдвард Дж. Бенц (2005). Оксфордский учебник медицины, том третий. Издательство Оксфордского университета. С. 720–725. ISBN 978-0-19-857013-4.
- ^ Полный список лекарств и химических веществ, которые потенциально вредны при дефиците G6PD, можно найти в Beutler E (декабрь 1994 г.). «Дефицит G6PD». Кровь. 84 (11): 3613–36. Дои:10.1182 / blood.V84.11.3613.bloodjournal84113613. PMID 7949118.[постоянная мертвая ссылка ].
- ^ Раупп П., Хассан Дж. А., Варугезе М., Кристианссон Б. (2001). «Хна вызывает опасный для жизни гемолиз при дефиците глюкозо-6-фосфатдегидрогеназы». Arch. Дис. Ребенок. 85 (5): 411–2. Дои:10.1136 / adc.85.5.411. ЧВК 1718961. PMID 11668106.
- ^ Рис, округ Колумбия; Келси, H; Ричардс, JD (27 марта 1993 г.). «Острый гемолиз, вызванный высокой дозой аскорбиновой кислоты при дефиците глюкозо-6-фосфатдегидрогеназы». BMJ (под ред. Клинических исследований). 306 (6881): 841–2. Дои:10.1136 / bmj.306.6881.841. ЧВК 1677333. PMID 8490379.
- ^ Mehta, JB; Сингхал, SB; Мехта, Британская Колумбия (13 октября 1990 г.). «Гемолиз, вызванный аскорбиновой кислотой при дефиците G-6-PD». Ланцет. 336 (8720): 944. Дои:10.1016 / 0140-6736 (90) 92317-б. PMID 1976956. S2CID 30959794.
- ^ «Фавизм | генетическое заболевание».
- ^ Кумар, Винай; Аббас, Абул К .; Фаусто, Нельсон; Астер, Джон (28 мая 2009 г.). Патологическая основа болезни Роббинса и Котрана, Профессиональное издание: Консультации экспертов - Интернет (Патология Роббинса) (Kindle Locations 33351-33354). Elsevier Health. Kindle Edition.
- ^ Шевион, Мордехай; Навок, Тиква; Глейзер, Гад; Магер, Джейкоб (1982-10-01). "Химия соединений, вызывающих фавизм". Европейский журнал биохимии. 127 (2): 405–409. Дои:10.1111 / j.1432-1033.1982.tb06886.x. ISSN 1432-1033. PMID 7140776.
- ^ Гаскин Р.С., Эствик Д., Педди Р. (2001). «Дефицит G6PD: его роль в высокой распространенности гипертонии и сахарного диабета». Этническая принадлежность и болезнь. 11 (4): 749–54. PMID 11763298.
- ^ Рабочая группа ВОЗ (1989 г.). «Дефицит глюкозо-6-фосфатдегидрогеназы». Бюллетень Всемирной организации здравоохранения. 67 (6): 601–11. ЧВК 2491315. PMID 2633878.
- ^ Монга А., Маккар Р.П., Арора А., Мукхопадхьяй С., Гупта А.К. (июль 2003 г.). «Отчет о клиническом случае: острый гепатит Е с сопутствующим дефицитом глюкозо-6-фосфатдегидрогеназы». Может ли J заразить Dis. 14 (4): 230–1. Дои:10.1155/2003/913679. ЧВК 2094938. PMID 18159462.
- ^ Гамильтон Дж. В., Джонс Ф. Г., МакМаллин М. Ф. (август 2004 г.). «Глюкозо-6-фосфатдегидрогеназа Гвадалахара - случай хронической несфероцитарной гемолитической анемии в ответ на спленэктомию и роль спленэктомии в этом заболевании». Гематология. 9 (4): 307–9. Дои:10.1080/10245330410001714211. PMID 15621740. S2CID 71268494.
- ^ thefreedictionary.com> дефицит глюкозо-6-фосфатдегидрогеназы цитируется: Gale Encyclopedia of Medicine. Авторское право 2008 г.
- ^ Cappellini MD, Fiorelli G (январь 2008 г.). «Дефицит глюкозо-6-фосфатдегидрогеназы». Ланцет. 371 (9606): 64–74. Дои:10.1016 / S0140-6736 (08) 60073-2. PMID 18177777. S2CID 29165746.
- ^ ГББ 2013 Смертность и причины смерти, соавторы (17 декабря 2014 г.). «Глобальная, региональная и национальная возрастная и половая смертность от всех причин и причин смерти от 240 причин смерти, 1990–2013 годы: систематический анализ для исследования глобального бремени болезней 2013». Ланцет. 385 (9963): 117–71. Дои:10.1016 / S0140-6736 (14) 61682-2. ЧВК 4340604. PMID 25530442.
- ^ Gelabert, Pere; Олальде, Иньиго; де-Диос, Тони; Чивит, Серги; Лалуэса-Фокс, Карлес (2017). «Малярия была слабой силой отбора у древних европейцев». Научные отчеты. 7 (1): 1377. Bibcode:2017НатСР ... 7.1377G. Дои:10.1038 / s41598-017-01534-5. ISSN 2045-2322. ЧВК 5431260. PMID 28469196.
- ^ Раздел FAQ по G-6-PD
- ^ Мехта А., Мейсон П.Дж., Вуллиами Т.Дж. (2000). «Дефицит глюкозо-6-фосфатдегидрогеназы». Передовая практика и исследования в клинической гематологии. 13 (1): 21–38. Дои:10.1053 / бэха.1999.0055. ЧВК 2398001. PMID 10916676.
- ^ Нельсон, Дэвид Л .; Кокс, Майкл М. (13 февраля 2013 г.). Принципы биохимии Ленингера (6-е изд.). Бейзингсток, Англия: Высшее образование Макмиллан. п. 576. ISBN 978-1-4641-0962-1.
- ^ Алвинг А.С., Карсон П.Е., Фланаган С.Л., Икес К.Э. (сентябрь 1956 г.). «Ферментативная недостаточность в чувствительных к примахину эритроцитах». Наука. 124 (3220): 484–5. Bibcode:1956 г., наука ... 124..484C. Дои:10.1126 / science.124.3220.484-а. PMID 13360274.
- ^ Бэрд К. (2015). «Истоки и последствия игнорирования дефицита G6PD и токсичности примахина при малярии Plasmodium vivax». Pathog Glob Health. 109 (3): 93–106. Дои:10.1179 / 2047773215Y.0000000016. ЧВК 4455359. PMID 25943156.
- ^ Beutler E (январь 2008 г.). «Дефицит глюкозо-6-фосфатдегидрогеназы: историческая перспектива». Кровь. 111 (1): 16–24. Дои:10.1182 / кровь-2007-04-077412. PMID 18156501.
- ^ Саймунс, Ф.Дж. (30 августа 1996 г.). «8». Растения жизни, растения смерти. Университет Висконсин Press. п. 216. ISBN 978-0299159047.
- ^ Рендалл, Стивен; Ридвег, Кристоф (2005). Пифагор: его жизнь, учение и влияние. Итака, Нью-Йорк: Издательство Корнельского университета. ISBN 978-0-8014-4240-7.
внешние ссылки
| Классификация | |
|---|---|
| Внешние ресурсы |
