Миелиновый протеин ноль - Myelin protein zero
Миелиновый протеин ноль (P0, МПЗ) представляет собой одинарную мембрану гликопротеин[5] который у человека кодируется МПЗ ген. P0 - главный структурный компонент миелиновой оболочки в периферическая нервная система (ПНС).[6] Нулевой миелиновый белок выражается Шванновские клетки и составляет более 50% всех белков периферической нервной системы, что делает его наиболее распространенным белком, экспрессируемым в ПНС.[6] Мутации нулевого белка миелина могут вызывать дефицит миелина и связаны с невропатии любить Болезнь Шарко – Мари – Зуба и Болезнь Дежерина – Соттаса.[7]
Структура
| Миелин-PO_C | |||||||||
|---|---|---|---|---|---|---|---|---|---|
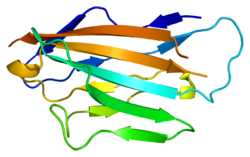
 Структура внеклеточного домена нулевого миелинового белка с мечеными бета-цепями. Нити D, E, B и A составляют один бета-лист, нити A ', G, F, C, C', C '' составляют другой бета-лист. | |||||||||
| Идентификаторы | |||||||||
| Символ | Миелин-PO_C | ||||||||
| Pfam | PF10570 | ||||||||
| ИнтерПро | IPR019566 | ||||||||
| OPM суперсемейство | 193 | ||||||||
| Белок OPM | 3oai | ||||||||
| Мембранома | 213 | ||||||||
| |||||||||
У человека ген, кодирующий нулевой миелиновый белок, расположен на хромосома 1 рядом с Даффи Локус или антиген / хемокиновый рецептор Даффи. Ген имеет длину около 7000 оснований и разделен на 6 экзонов. В общей сложности нулевой миелиновый белок состоит из 219 аминокислот.[6] и имеет много основных аминокислотных остатков.[8]
Нулевой миелиновый белок состоит из внеклеточный N-концевой домен (аминокислоты 1-124), одиночный трансмембранный область (125-150), а меньшая положительно заряженная внутриклеточный регион (151-219).[6][9][10] Его цитоплазматический домен сильно заряжен положительно, но предположительно не складывается в глобулярную структуру.[11] Внеклеточный домен структурно похож на иммуноглобулин домен[8] и поэтому белок считается принадлежащим к суперсемейство иммуноглобулинов[12]
Помимо того, что он существует в качестве мономера, нулевой миелиновый белок, как известно, также образует димеры и тетрамеры с другими нулевыми молекулами миелинового белка у позвоночных.[13]
Функция
В миелиновой оболочки представляет собой многослойную мембрану, уникальную для нервной системы, которая действует как изолятор, значительно увеличивая скорость проведения аксональных импульсов. Миелиновый белок нулевой, отсутствует в центральной нервной системе,[14] является основным компонентом миелин оболочка в периферийный нервы. Мутации, которые нарушают функцию нулевого белка миелина, могут привести к снижению экспрессии миелина и дегенерации миелиновой оболочки в периферической нервной системе.[15] В настоящее время постулируется, что нулевая экспрессия белка миелина вызывается сигналами от аксона. Однако более подробная информация о регуляции нулевого белка миелина неизвестна.[6]
Постулируется, что нулевой миелиновый белок является структурный элемент в образовании и стабилизации миелина периферических нервов.[9] Также предполагается, что нулевой миелиновый белок служит молекулой клеточной адгезии, удерживая вместе несколько слоев миелина.[10] Когда миелинизирующая клетка несколько раз оборачивает свою мембрану вокруг аксона, генерируя несколько слоев миелина, нулевой миелиновый белок помогает удерживать эти слои компактными, выступая в качестве «клея», удерживающего слои миелина вместе.[11] Он делает это, удерживая свою характеристическую катушку структура вместе электростатическими взаимодействиями[8] положительно заряженного внутриклеточного домена с кислый липиды в цитоплазматический грань противоположного бислоя.[14] и взаимодействием между гидрофобный шаровидные «головы» прилегающих внеклеточных домены.[14]
Функция нулевого белка миелина аналогична функции других белков с доменами иммуноглобина, таких как полииммуноглобин и белок Т4. Эти белки функционируют как связывающие и адгезионные молекулы и участвуют в гомотипических взаимодействиях или взаимодействиях, в которых участвуют два подобных белка.[9] Нулевой миелиновый белок удерживает вместе миелиновую оболочку, участвуя в гомотипических взаимодействиях с другими нулевыми белками миелинового белка. Внеклеточный домен нулевого миелинового белка связывается с миелином сфинголипид мембрана и скрепляет миелиновые слои, используя гомотипические взаимодействия с другими нулевыми внеклеточными доменами миелинового белка,[7] и с внеклеточными остатками триптофана, взаимодействующими с мембраной.[8]
Также было продемонстрировано, что нулевой миелиновый белок взаимодействовать с другими белками, такими как периферический миелиновый белок 22.[16] Однако на данный момент цель этих взаимодействий еще не определена.[16]
Связь с невропатией
Известно, что мутации нулевого миелинового белка вызывают дегенерацию миелина и невропатия.[7] Считается, что мутации, которые снижают адгезионную функцию нулевого миелинового белка или его способность участвовать в гомеотипических взаимодействиях с другими нулевыми белками миелина, вызывают невропатию.[17] Мутации нулевого миелинового белка могут привести к проблемам с развитием миелина в раннем возрасте или к дегенерации миелина на аксоне в более позднем возрасте.[12] Некоторые мутации могут вызывать невропатию в младенчестве, например Болезнь Держерина-Соттаса в то время как другие мутации могут вызывать невропатию в течение первых двух десятилетий жизни, например Болезнь Шарко-Мари-Тута.[7] Добавление заряженной аминокислоты или изменение остатка цистеина во внеклеточной мембране может привести к раннему началу невропатии. Усечение цитоплазматического домена или изменение третичной структуры нулевого миелинового белка также может привести к невропатии.[7] поскольку было продемонстрировано, что цитоплазматический домен необходим для гомотипических взаимодействий.[12]
использованная литература
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000158887 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000056569 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Magnaghi V, Cavarretta I, Galbiati M, Martini L, Melcangi RC (ноябрь 2001 г.). «Нейроактивные стероиды и белки периферического миелина». Исследование мозга. Обзоры исследований мозга. 37 (1–3): 360–71. Дои:10.1016 / s0165-0173 (01) 00140-0. PMID 11744100.
- ^ а б c d е Shy ME (март 2006 г.). «Периферические невропатии, вызванные мутациями нулевого миелинового белка». Журнал неврологических наук. 242 (1–2): 55–66. Дои:10.1016 / j.jns.2005.11.015. PMID 16414078.
- ^ а б c d е Shy ME, Jáni A, Krajewski K, Grandis M, Lewis RA, Li J, Shy RR, Balsamo J, Lilien J, Garbern JY, Kamholz J (февраль 2004 г.). «Фенотипическая кластеризация при мутациях MPZ». Мозг. 127 (Pt 2): 371–84. Дои:10.1093 / мозг / awh048. PMID 14711881.
- ^ а б c d Шапиро Л., Дойл Дж. П., Хенсли П., Колман Д. Р., Хендриксон В. А. (сентябрь 1996 г.). «Кристаллическая структура внеклеточного домена из P0, основного структурного белка миелина периферических нервов». Нейрон. 17 (3): 435–49. Дои:10.1016 / s0896-6273 (00) 80176-2. PMID 8816707.
- ^ а б c Лемке Г., Аксель Р. (март 1985 г.). «Выделение и последовательность кДНК, кодирующей основной структурный белок периферического миелина». Ячейка. 40 (3): 501–8. Дои:10.1016/0092-8674(85)90198-9. PMID 2578885.
- ^ а б Лемке Г., Ламар Е., Паттерсон Дж. (Март 1988 г.). «Выделение и анализ гена, кодирующего периферический миелиновый белок ноль». Нейрон. 1 (1): 73–83. Дои:10.1016/0896-6273(88)90211-5. PMID 2483091.
- ^ а б Хан Х, Мюллюкоски М., Рускамо С., Ван С., Курсула П. (январь 2013 г.). «Миелин-специфические белки: структурно разнообразная группа молекул, взаимодействующих с мембраной». БиоФакторы. 39 (3): 233–41. Дои:10.1002 / biof.1076. PMID 23780694.
- ^ а б c Kamholz JA, Brucal M, Li J, Shy M (2007), «Нулевой миелиновый протеин и CMT1B: рассказ о двух фенотипах», Молекулярная неврология, Elsevier, стр. 463–474, Дои:10.1016 / b978-012369509-3.50031-7, ISBN 9780123695093
- ^ Томпсон А.Дж., Кронин М.С., Киршнер Д.А. (март 2002 г.). «Нулевой миелиновый белок существует в виде димеров и тетрамеров в нативных мембранах периферического нерва Xenopus laevis». Журнал неврологических исследований. 67 (6): 766–71. Дои:10.1002 / jnr.10167. PMID 11891790.
- ^ а б c Сакамото Ю., Китамура К., Йошимура К., Нисидзима Т., Уэмура К. (март 1987 г.). «Полная аминокислотная последовательность белка PO в миелине периферических нервов крупного рогатого скота». Журнал биологической химии. 262 (9): 4208–14. PMID 2435734.
- ^ Киршнер Д.А., Иноуе Х., Сааведра Р.А. (ноябрь 1996 г.). «Мембранная адгезия в периферическом миелине: хорошие и плохие обертывания с белком P0». Структура. 4 (11): 1239–44. Дои:10.1016 / s0969-2126 (96) 00132-3. PMID 8939762.
- ^ а б Д'Урсо Д., Эрхардт П., Мюллер Х.В. (май 1999 г.). «Периферический миелиновый протеин 22 и нулевой протеин: новая ассоциация миелина периферической нервной системы» (PDF). Журнал неврологии. 19 (9): 3396–403. Дои:10.1523 / JNEUROSCI.19-09-03396.1999. ЧВК 6782240. PMID 10212299.
- ^ Парейсон, Давиде; Марчези, Кьяра; Сальсано, Этторе (2013), «Доминантный синдром Шарко – Мари – Тута и родственные расстройства», Справочник по клинической неврологии, Эльзевьер, 115: 817–845, Дои:10.1016 / b978-0-444-52902-2.00047-3, ISBN 9780444529022, PMID 23931817
дальнейшее чтение
- Патель П.И., Лупски-младший (апрель 1994 г.). «Болезнь Шарко-Мари-Тута: новая парадигма механизма наследственного заболевания». Тенденции в генетике. 10 (4): 128–33. Дои:10.1016/0168-9525(94)90214-3. PMID 7518101.
- Роа BB, Лупски-младший (1995). Молекулярная генетика невропатии Шарко-Мари-Тута. Достижения в генетике человека. 22. С. 117–52. Дои:10.1007/978-1-4757-9062-7_3. ISBN 978-1-4757-9064-1. PMID 7762451.
- Нелис Э., Хайтес Н., Ван Брокховен С. (1999). «Мутации в генах периферического миелина и связанных генах при наследственных периферических невропатиях». Человеческая мутация. 13 (1): 11–28. Дои:10.1002 / (SICI) 1098-1004 (1999) 13: 1 <11 :: AID-HUMU2> 3.0.CO; 2-A. PMID 9888385.
- Ватанабэ М., Ямамото Н., Окоши Н., Нагата Х., Коно Й., Хаяси А., Тамаока А., Сёдзи С. (сентябрь 2002 г.). «Кортикостероид-зависимая асимметричная нейропатия с нулевой мутацией гена миелинового белка». Неврология. 59 (5): 767–9. Дои:10.1212 / wnl.59.5.767. PMID 12221176.
- Хаттори Н, Ямамото М., Йошихара Т., Коике Х., Накагава М., Йошикава Х, Охниши А., Хаясака К., Онодера О, Баба М., Ясуда Х, Сайто Т., Накашима К., Кира Дж, Кадзи Р., Ока Н., Собуэ Дж. (Январь 2003 г.). «Демиелинизирующие и аксональные особенности болезни Шарко-Мари-Тута с мутациями белков, связанных с миелином (PMP22, MPZ и Cx32): клинико-патологическое исследование 205 японских пациентов». Мозг. 126 (Pt 1): 134–51. Дои:10.1093 / мозг / awg012. PMID 12477701.
- Shy ME (март 2006 г.). «Периферические невропатии, вызванные мутациями нулевого миелинового белка». Журнал неврологических наук. 242 (1–2): 55–66. Дои:10.1016 / j.jns.2005.11.015. PMID 16414078.
- Хаясака К., Нанао К., Тахара М., Сато В., Такада Дж., Миура М., Уэмура К. (октябрь 1991 г.). «Выделение и определение последовательности кДНК, кодирующей основной структурный белок периферического миелина человека». Сообщения о биохимических и биофизических исследованиях. 180 (2): 515–8. Дои:10.1016 / S0006-291X (05) 81094-0. PMID 1719967.
- Оврие Р.А., МакЛеод Дж. Г., Кончин Т. Е. (февраль 1987 г.). «Гипертрофические формы наследственной моторной и сенсорной нейропатии. Исследование гипертрофической болезни Шарко-Мари-Тута (HMSN тип I) и болезни Дежерина-Сотта (HMSN тип III) в детстве». Мозг. 110 (Pt 1) (1): 121–48. Дои:10.1093 / мозг / 110.1.121. PMID 3467805.
- Тачи Н., Исикава Ю., Минами Р. (1985). «Два случая врожденной нейропатии гипомиелинизации». Мозг и развитие. 6 (6): 560–5. Дои:10.1016 / s0387-7604 (84) 80101-1. PMID 6099985.
- Хаясака К., Химоро М., Ван И, Таката М., Миносима С., Симидзу Н., Миура М., Уэмура К., Такада Г. (сентябрь 1993 г.). «Структура и хромосомная локализация гена, кодирующего нулевой белок миелина человека (MPZ)». Геномика. 17 (3): 755–8. Дои:10.1006 / geno.1993.1400. PMID 7503936.
- Су И, Брукс Д.Г., Ли Л., Леперк Дж., Трофаттер Дж. А., Раветч Дж. В., Лебо Р. В. (ноябрь 1993 г.). "Нулевой ген миелинового белка мутировал у пациентов типа 1B Шарко-Мари-Зуб". Труды Национальной академии наук Соединенных Штатов Америки. 90 (22): 10856–60. Bibcode:1993ПНАС ... 9010856С. Дои:10.1073 / пнас.90.22.10856. ЧВК 47877. PMID 7504284.
- Химоро М., Йошикава Х., Мацуи Т., Мицуи Ю., Такахаши М., Кайдо М., Нисимура Т., Савайши И., Такада Г., Хаясака К. (сентябрь 1993 г.). «Новая мутация гена миелина P0 в родословной нейропатии Шарко-Мари-Тута 1». Международная биохимия и молекулярная биология. 31 (1): 169–73. PMID 7505151.
- Хаясака К., Химоро М., Савайши И., Нанао К., Такахаши Т., Такада Г., Николсон Г.А., Оврие Р.А., Тачи Н. (ноябрь 1993 г.). «Мутация de novo гена миелина P0 при болезни Дежерина-Соттаса (наследственная моторная и сенсорная нейропатия III типа)». Природа Генетика. 5 (3): 266–8. Дои:10.1038 / ng1193-266. PMID 7506095.
- Pham-Dinh D, Fourbil Y, Blanquet F, Mattéi MG, Roeckel N, Latour P, Chazot G, Vandenberghe A, Dautigny A (декабрь 1993 г.). «Главный нулевой ген периферического миелинового белка: структура и локализация в кластере генов рецепторов Fc гамма на хромосоме 1q21.3-q23 человека». Молекулярная генетика человека. 2 (12): 2051–4. Дои:10.1093 / hmg / 2.12.2051. PMID 7509228.
- Томас Ф. П., Лебо Р. В., Росоклия Г., Динг XS, Лавлейс Р. Э., Латов Н., Хейс А. П. (1994). "Томакулезная невропатия в хромосоме 1 синдром Шарко-Мари-Тута". Acta Neuropathologica. 87 (1): 91–7. Дои:10.1007 / BF00386259. PMID 7511317.
- Нелис Э., Тиммерман В., Де Йонге П., Ванденберге А., Фам-Динь Д., Даутиньи А., Мартин Дж. Дж., Ван Брокховен С. (декабрь 1994 г.). «Быстрый скрининг генов миелина у пациентов с CMT1 с помощью анализа SSCP: выявление новых мутаций и полиморфизмов в гене P0». Генетика человека. 94 (6): 653–7. Дои:10.1007 / bf00206959. PMID 7527371.
- Hilmi S, Fournier M, Valeins H, Gandar JC, Bonnet J (февраль 1995 г.). «Гликопротеин миелина P0: идентификация сайта, фосфорилированного in vitro и in vivo эндогенными протеинкиназами». Журнал нейрохимии. 64 (2): 902–7. Дои:10.1046 / j.1471-4159.1995.64020902.x. PMID 7530295.
- Раутенштраус Б., Нелис Э., Грел Х., Пфайффер Р.А., Ван Брокховен С. (сентябрь 1994 г.). «Идентификация инсерционной мутации de novo в P0 у пациента с фенотипом синдрома Дежерина-Соттаса (DSS)». Молекулярная генетика человека. 3 (9): 1701–2. Дои:10.1093 / hmg / 3.9.1701. PMID 7530550.
- Латур П., Бланке Ф., Нелис Е., Боннебуш С., Чапон Ф., Дирасон П., Олланьон Е., Даутиньи А., Фам-Динь Д., Шазо Г. (1995). «Мутации в гене нулевого белка миелина, связанные с болезнью Шарко-Мари-Тута типа 1B». Человеческая мутация. 6 (1): 50–4. Дои:10.1002 / humu.1380060110. PMID 7550231.
внешние ссылки
- GeneReviews / NCBI / NIH / UW запись о невропатии Шарко-Мари-Тута типа 1
- GeneReviews / NCBI / NIH / UW запись о невропатии Шарко-Мари-Тута 2 типа
- Миелин + белок + ноль в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Обзор всей структурной информации, доступной в PDB для UniProt: P25189 (Миелиновый белок P0) на PDBe-KB.