Nucleus accumbens - Nucleus accumbens
| Nucleus accumbens | |
|---|---|
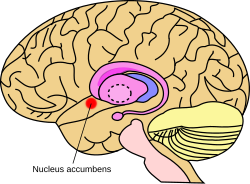 Примерное расположение прилежащего ядра в головном мозге | |
 Nucleus accumbens мозга мыши | |
| Подробности | |
| Часть | Мезолимбический путь Базальный ганглий (Вентральное полосатое тело ) |
| Запчасти | Оболочка прилежащего ядра Ядро прилежащего ядра |
| Идентификаторы | |
| латинский | прилежащее ядро септи |
| Акроним (ы) | NAc или NAcc |
| MeSH | D009714 |
| NeuroNames | 277 |
| НейроЛекс Я БЫ | birnlex_727 |
| TA98 | A14.1.09.440 |
| TA2 | 5558 |
| FMA | 61889 |
| Анатомические термины нейроанатомии | |
В прилежащее ядро (NAc или же NAcc; также известный как прилежащее ядро, или ранее как прилежащее ядро септи, латинский за "ядро рядом с перегородка ") - это регион в базальный передний мозг ростральный к преоптическая область из гипоталамус.[1] Прилежащее ядро и обонятельный бугорок коллективно формируют брюшное полосатое тело. Вентральное полосатое тело и спинное полосатое тело коллективно формируют полосатое тело, который является основным компонентом базальный ганглий.[2] В дофаминергические нейроны из мезолимбический путь проект на ГАМКергический средние шиповатые нейроны прилежащего ядра и обонятельного бугорка.[3][4] Каждый полушарие головного мозга имеет собственное прилежащее ядро, которое можно разделить на две структуры: ядро прилежащего ядра и оболочку прилежащего ядра. Эти подструктуры имеют разную морфологию и функции.
Различные субрегионы NAcc (ядро против оболочки) и субпопуляции нейронов в каждом регионе (D1-типа против D2-тип средние шиповатые нейроны) отвечают за различные когнитивные функции.[5][6] В целом прилежащее ядро играет важную роль в когнитивной обработке мотивация, отвращение, награда (т.е. стимулирующая значимость, удовольствие, и положительное подкрепление ), и подкрепление обучение (например, Павловско-инструментальный перевод );[4][7][8][9][10] следовательно, он играет важную роль в зависимость.[4][8] Кроме того, часть ядра прилежащего ядра центрально участвует в индукции медленный сон.[11][12][13][14] Прилежащее ядро играет меньшую роль в обработке страх (форма отвращения), импульсивность, а эффект плацебо.[15][16][17] Он участвует в кодировании новых моторные программы также.[4]
Структура
Прилежащее ядро - это совокупность нейронов, которая описывается как имеющая внешнюю оболочку и внутреннее ядро.[4]
Вход
Основной глутаматергический входы в прилежащее ядро включают префронтальная кора (особенно предлимбическая кора и инфралимбическая кора ), базолатеральная миндалина, вентральная гиппокамп, таламический ядра (в частности срединные таламические ядра и интраламинарные ядра таламуса ), и глутаматергические проекции из вентральная тегментальная область (ВТА).[18] Прилежащее ядро получает дофаминергические входы от вентральной области покрышки, которые соединяются через мезолимбический путь. Прилежащее ядро часто описывают как часть кортико-базальные ганглии-таламо-кортикальная петля.[19]
Дофаминергические входы от VTA модулируют активность ГАМКергический нейроны в прилежащем ядре. Эти нейроны прямо или косвенно активируются эйфорический наркотики (например, амфетамин, опиаты и т. д.) и участвуя в полезном опыте (например, сексе, музыке, упражнениях и т. д.).[20][21]
Другой важный источник входных данных - CA1 и вентральный субикулум из гиппокамп к дорсомедиальный область прилежащего ядра. Незначительная деполяризация клеток в прилежащем ядре коррелирует с положительностью нейронов гиппокампа, что делает их более возбудимыми. Коррелированные клетки этих возбужденных состояний нейронов со средними шипами в прилежащем ядре в равной степени распределяются между субикулумом и CA1. Обнаружено, что нейроны субикулума гиперполяризованы (увеличивают негативность), в то время как нейроны CA1 «колеблются» (срабатывают> 50 Гц) для выполнения этого прайминга.[22]
Прилежащее ядро - одна из немногих областей, которые получают гистаминергические проекции от туберомаммиллярное ядро (единственный источник гистамин нейроны головного мозга).[23]
Выход
Выходные нейроны прилежащего ядра посылают аксональные проекции к базальный ганглий и вентральный аналог бледный шар, известный как брюшной паллидум (ВП). Вице-президент, в свою очередь, проецирует на медиальное дорсальное ядро спинного таламус, который проецируется в префронтальную кору, а также в полосатое тело. Другие эффекты от прилежащего ядра включают связи с хвост вентральной тегментальной области,[24] черная субстанция, а ретикулярная формация из мосты.[1]
Ракушка
В оболочка прилежащего ядра (Оболочка NAcc) является субструктурой прилежащего ядра. Оболочка и ядро вместе образуют все прилежащее ядро.
Место расположения: Оболочка является внешней областью прилежащего ядра и, в отличие от ядра, считается частью расширенная миндалина, расположенный на его ростральном полюсе.
Типы ячеек: Нейроны в прилежащем ядре в основном средние шиповатые нейроны (MSN), содержащие в основном D1-типа (т.е. DRD1 и DRD5 ) или же D2-тип (т.е. DRD2, DRD3, и DRD4 ) дофаминовые рецепторы. Субпопуляция MSN содержит рецепторы как D1-типа, так и D2-типа, при этом примерно 40% полосатых MSN экспрессируют оба DRD1 и DRD2 мРНК.[19][25][26] Эти NAcc MSN смешанного типа с рецепторами как D1-типа, так и D2-типа в основном ограничены оболочкой NAcc.[19] Нейроны в оболочке по сравнению с ядром имеют меньшую плотность дендритные шипы, меньше конечных сегментов и меньше сегментов ответвлений, чем в ядре. Оболочечные нейроны проецируются на субкомиссуральную часть брюшной паллидум а также вентральной тегментальной области и обширными областями в гипоталамус и расширенная миндалевидное тело.[27][28][29]
Функция: Оболочка прилежащего ядра участвует в когнитивной обработке награда, включая субъективные "симпатичные" реакции на определенные приятные стимулы, мотивационная значимость, и положительное подкрепление.[4][5][30][31] Также было показано, что эта оболочка NAcc является посредником специфический павловско-инструментальный перевод, явление, в котором классически обусловленный раздражитель изменяет оперантное поведение.[32][9][10] «Гедонистическая точка» или центр удовольствия, который отвечает за компонент удовольствия или «симпатии» некоторых внутренних наград, также расположен в небольшом отсеке внутри медиальной оболочки NAcc.[30][33][34] Наркотики, вызывающие привыкание оказывают большее влияние на высвобождение дофамина в оболочке, чем в ядре.[4]
Основной
В ядро прилежащего ядра (Ядро NAcc) - внутренняя субструктура прилежащего ядра.
Место расположения: Ядро прилежащего ядра является частью брюшное полосатое тело, расположенный внутри базальных ганглиев.Типы ячеек: Ядро NAcc состоит в основном из нейронов со средними шипами, содержащими в основном дофаминовые рецепторы D1-типа или D2-типа. Средние шиповатые нейроны D1-типа опосредуют когнитивные процессы, связанные с вознаграждением,[5][35][36] тогда как нейроны со средними шипами D2-типа опосредуют познание, связанное с отвращением.[6] Нейроны в ядре, по сравнению с нейронами в оболочке, имеют повышенную плотность дендритных шипов, сегментов ветвей и терминальных сегментов. Из ядра нейроны проецируются на другие подкорковые области, такие как бледный шар и черная субстанция. ГАМК является одним из основных нейротрансмиттеров в NAcc, и Рецепторы ГАМК также в изобилии.[27][29]
Функция: Ядро прилежащего ядра участвует в когнитивной обработке двигательная функция связанных с вознаграждением и подкреплением и регулированием медленный сон.[4][11][12][13] В частности, ядро кодирует новые двигательные программы, которые облегчают получение заданной награды в будущем.[4] Нейроны непрямого пути (т. Е. D2-типа) в ядре NAcc, ко-экспрессирующие аденозин А2А рецепторы в зависимости от активации способствуют медленноволновому сну.[11][12][13] Ядро NAcc также было показано как посредник общий павловско-инструментальный перевод, феномен, при котором классически обусловленный раздражитель изменяет оперантное поведение.[32][9][10]
Типы клеток
Приблизительно 95% нейронов в NAcc являются ГАМКергическими нейронами со средним шипом (MSN), которые в основном экспрессируют рецепторы D1-типа или D2-типа;[20] около 1–2% остальных типов нейронов - крупные аспины. холинергический интернейроны еще 1-2% - ГАМКергические интернейроны.[20]По сравнению с GABAergic MSN в оболочке, в ядре есть повышенная плотность дендритных шипов, сегментов ветвей и терминальных сегментов. Из ядра нейроны проецируются на другие подкорковые области, такие как бледный шар и черная субстанция. ГАМК является одним из основных нейротрансмиттеров в NAcc, и рецепторы ГАМК также широко распространены.[27][29] Эти нейроны также являются главными проекционными или выходными нейронами прилежащего ядра.
Нейрохимия
Некоторые из нейротрансмиттеров, нейромодуляторов и гормонов, которые передают сигнал через рецепторы в прилежащем ядре, включают:
Дофамин: Дофамин выделяется в прилежащее ядро после воздействия поощрительные стимулы, включая рекреационные наркотики подобно замещенные амфетамины, кокаин, никотин и морфий.[37][38]
Фенэтиламин и тирамин: Фенэтиламин и тирамин являются следы аминов которые синтезируются в нейронах, которые выражают гидроксилаза ароматической аминокислоты (AADC) фермент, который включает все дофаминергические нейроны.[39] Оба соединения действуют как дофаминергические нейромодуляторы которые регулируют обратный захват и высвобождение дофамина в Nacc посредством взаимодействия с VMAT2 и TAAR1 в конце аксона мезолимбических дофаминовых нейронов.
Глюкокортикоиды и дофамин: Глюкокортикоид рецепторы - единственные кортикостероид рецепторы в оболочке прилежащего ядра. L-ДОПА, стероиды и, в частности, глюкокортикоиды в настоящее время известны как единственные известные эндогенные соединения, которые могут вызывать психотические проблемы, поэтому понимание гормонального контроля над дофаминергическими проекциями в отношении рецепторов глюкокортикоидов может привести к новым методам лечения психотических симптомов. Недавнее исследование показало, что подавление глюкокортикоидных рецепторов привело к уменьшению высвобождения дофамина, что может привести к будущим исследованиям с участием антиглюкокортикоидных препаратов для потенциального облегчения психотических симптомов.[40]
ГАМК: Недавнее исследование на крысах, которые использовали агонисты и антагонисты ГАМК, показало, что ГАМКА рецепторы в оболочке NAcc имеют ингибирующий контроль над поворотным поведением под влиянием дофамина, и ГАМКB рецепторы иметь тормозящий контроль над поворотным поведением, опосредованный ацетилхолин.[27][41]
Глутамат: Исследования показали, что местная блокада глутаматергический Рецепторы NMDA в ядре NAcc нарушено пространственное обучение.[42] Другое исследование показало, что как NMDA, так и AMPA (оба рецепторы глутамата ) играют важную роль в регулировании инструментального обучения.[43]
Серотонин (5-HT): В целом, 5-HT синапсы более многочисленны и имеют большее количество синаптических контактов в оболочке NAcc, чем в ядре. Они также больше и толще и содержат более крупные плотные сердцевинные везикулы, чем их аналоги в сердцевине.
Функция
Награда и подкрепление
Прилежащее ядро, являясь одной из частей системы вознаграждения, играет важную роль в обработке поощрительных стимулов, подкрепляющих стимулов (например, еда и вода), а также тех, которые являются одновременно поощрительными и подкрепляющими (вызывающие привыкание наркотики, секс и упражнения).[4][44] Преобладающая реакция нейронов прилежащего ядра на вознаграждение сахароза это торможение; обратное верно в ответ на введение аверсива хинин.[45] Существенные данные фармакологических манипуляций также предполагают, что снижение возбудимости нейронов в прилежащем ядре является полезным, как, например, было бы верно в случае μ-опиоидный рецептор стимуляция.[46] В сигнал зависимости уровня кислорода в крови (ЖИРНЫЙ) в прилежащем ядре избирательно увеличивается при восприятии приятных, эмоционально возбуждающих картинок и во время мысленных образов приятных эмоциональных сцен. Однако, поскольку BOLD считается косвенной мерой регионального сетевого возбуждения к ингибированию, степень, в которой BOLD измеряет процессинг, зависящий от валентности, неизвестен.[47][48] Из-за большого количества входов NAcc из лимбических регионов и сильных выходов NAcc в моторные регионы, прилежащее ядро было описано Гордоном Могенсеном как интерфейс между лимбической и моторной системами.[49][50]

Прилежащее ядро причинно связано с переживанием удовольствия. Микроинъекции агонистов μ-опиоидов, δ-опиоидные агонисты или же κ-опиоидные агонисты в ростродорсальном квадранте медиальной оболочки усиливают «симпатию», в то время как более каудальные инъекции могут подавлять реакции отвращения, симпатии или и то, и другое.[30] Области прилежащего ядра, которым можно приписать причинную роль в производстве удовольствия, ограничены как анатомически, так и химически, поскольку кроме опиоидных агонистов только эндоканнабиноиды может усилить симпатию. В прилежащем ядре в целом дофамин, Агонист рецептора ГАМК или же Антагонисты AMPA изменить только мотивацию, в то время как то же самое верно для опиоидов и эндоканнабиноидов за пределами горячей точки в медиальной оболочке. Ростро-каудальный градиент существует для усиления аппетитных реакций по сравнению с реакциями страха, последний из которых традиционно считается требующим только функции рецептора D1, а первый из которых требует функции как D1, так и D2. Одна интерпретация этого открытия, гипотеза растормаживания, постулирует, что ингибирование прилежащих MSN (которые являются ГАМКергическими) растормаживает нижележащие структуры, делая возможным проявление аппетитного или консумативного поведения.[52] Мотивационные эффекты антагонистов AMPA и, в меньшей степени, агонистов GABA, анатомически гибки. Стрессовые условия могут расширить области, вызывающие страх, в то время как знакомая среда может уменьшить размер области, вызывающей страх. Кроме того, кортикальный вход от орбитофронтальная кора (OFC) смещает реакцию в сторону аппетитного поведения, и инфралимбический входной сигнал, эквивалентный субгенуальной поясной коре человека, подавляет реакцию независимо от валентности.[30]
Прилежащее ядро не является ни необходимым, ни достаточным для инструментального обучения, хотя манипуляции могут повлиять на выполнение задач инструментального обучения. Одна из задач, в которой эффект поражения NAcc очевиден, - это Павлово-инструментальный перенос (PIT), где сигнал в сочетании с конкретным или общим вознаграждением может усилить инструментальную реакцию. Поражения ядра NAcc ухудшают производительность после девальвации и подавляют эффект общего PIT. С другой стороны, повреждения оболочки только ухудшают эффект специфического PIT. Считается, что это различие отражает согласованные и аппетитные условные реакции в оболочке NAcc и ядре NAcc, соответственно.[53]
В дорсальном полосатом теле наблюдается дихотомия между D1-MSN и D2-MSN, при этом первые усиливают и усиливают локомоцию, а вторые - отталкивающие и уменьшающие локомоцию. Такое различие традиционно считалось применимым и к прилежащему ядру, но данные фармакологических и оптогенетических исследований противоречивы. Более того, подмножество NAcc MSN экспрессируют как D1, так и D2 MSN, и фармакологическая активация D1 по сравнению с рецепторами D2 не обязательно должна точно активировать нервные популяции. В то время как большинство исследований не показывают влияния селективной оптогенетической стимуляции D1 или D2 MSN на двигательную активность, в одном исследовании сообщается об уменьшении базальной локомоции при стимуляции D2-MSN. В двух исследованиях сообщалось о снижении усиливающих эффектов кокаина при активации D2-MSN, в одном исследовании сообщалось об отсутствии эффекта. Сообщалось также, что активация NAcc D2-MSN усиливает мотивацию, по оценке PIT, а активность рецептора D2 необходима для усиливающих эффектов стимуляции VTA.[54] В исследовании 2018 года сообщается, что активация D2 MSN усиливает мотивацию за счет ингибирования вентрального паллидума, тем самым подавляя VTA.[55]
Материнское поведение
An фМРТ Исследование, проведенное в 2005 году, показало, что, когда крысы-матери находились рядом со своими детенышами, области мозга, участвующие в подкреплении, включая прилежащее ядро, были очень активными.[56] Уровень дофамина увеличивается в прилежащем ядре во время материнского поведения, в то время как поражения в этой области нарушают материнское поведение.[57] Когда женщинам показывают фотографии неродственных младенцев, фМРТ показывают повышенную активность мозга в прилежащем ядре и прилежащем хвостатом ядре, пропорционально тому, насколько женщины находят этих младенцев «милыми».[58]
Отвращение
Активация MSN типа D1 в прилежащем ядре участвует в вознаграждении, тогда как активация MSN типа D2 в прилежащем ядре способствует отвращение.[6]
Медленный сон
В конце 2017 года исследования грызунов, использовавших оптогенетический и хемогенетический Методы обнаружили, что нейроны с шипами среднего звена непрямого пути (т.е. типа D2) в ядре прилежащего ядра, коэкспрессирующие аденозин А2А рецепторы и проект брюшной паллидум участвуют в регулировании медленный сон.[11][12][13][14] В частности, оптогенетическая активация этих нейронов ядра NAcc непрямого пути индуцирует медленный сон, а хемогенетическая активация тех же нейронов увеличивает количество и продолжительность эпизодов медленноволнового сна.[12][13][14] Хемогенетическое ингибирование этих нейронов ядра NAcc подавляет сон.[12][13] Напротив, нейроны со средними шипами D2-типа в оболочке NAcc, которые экспрессируют аденозин A2А рецепторы не играют никакой роли в регуляции медленноволнового сна.[12][13]
Клиническое значение
Зависимость
Современные модели зависимости от хронического употребления наркотиков включают изменения в экспрессия гена в мезокортиколимбическая проекция.[20][59][60] Самое важное факторы транскрипции производят эти изменения ΔFosB, циклический аденозинмонофосфат (лагерь ) связывающий белок элемент ответа (CREB ) и ядерный фактор каппа B (NFκB ).[20] ΔFosB является наиболее значимым фактором транскрипции генов при зависимости, поскольку его популярный или генетическая сверхэкспрессия в прилежащем ядре необходимо и достаточно для многих нейронных адаптаций и поведенческих эффектов (например, зависимое от экспрессии увеличение самоуправление и поощрение поощрения ) замечен в наркомании.[20][35][61] Сверхэкспрессия ΔFosB связана с зависимостью от спирт (этанол), каннабиноиды, кокаин, метилфенидат, никотин, опиоиды, фенциклидин, пропофол, и замещенные амфетамины, среди прочего.[20][59][61][62][63] Повышение экспрессии ΔJunD прилежащего ядра может снижать или, при большом увеличении, даже блокировать большинство нейронных изменений, наблюдаемых при хроническом злоупотреблении наркотиками (т.е. изменений, опосредованных ΔFosB).[20]
ΔFosB также играет важную роль в регулировании поведенческих реакций на естественные награды, такие как вкусная еда, секс и упражнения.[20][21] Естественные вознаграждения, такие как наркотики, вызывающие злоупотребление, индуцируют ΔFosB в прилежащем ядре, и хроническое получение этих вознаграждений может привести к аналогичному патологическому состоянию зависимости из-за сверхэкспрессии ΔFosB.[20][21][44] Следовательно, ΔFosB также является ключевым фактором транскрипции, участвующим в зависимости от естественных вознаграждений;[20][21][44] в частности, ΔFosB в прилежащем ядре имеет решающее значение для усиливающих эффектов сексуального вознаграждения.[21] Исследования взаимодействия между естественными и лекарственными вознаграждениями показывают, что психостимуляторы и сексуальное поведение действуют на аналогичные биомолекулярные механизмы, индуцируя ΔFosB в прилежащем ядре, и обладают эффектами перекрестной сенсибилизации, которые опосредуются через ΔFosB.[44][64]
Как и в случае с лекарственными препаратами, немедикаментозные поощрения также увеличивают уровень внеклеточного дофамина в оболочке NAcc. Вызванное лекарством высвобождение дофамина в оболочке NAcc и ядре NAcc обычно не подвержено привыкание (т.е. развитие переносимость лекарств: уменьшение высвобождения дофамина от будущего воздействия лекарственного средства в результате повторного воздействия препарата); Напротив, повторное воздействие лекарств, которые вызывают высвобождение дофамина в оболочке и ядре NAcc, обычно приводит к сенсибилизация (т. е. количество дофамина, которое высвобождается в NAcc в результате будущего воздействия препарата, увеличивается в результате повторного воздействия препарата). Сенсибилизация высвобождения дофамина в оболочке NAcc после многократного воздействия лекарств служит для усиления ассоциаций стимул-лекарство (т.е. классическое кондиционирование что происходит, когда употребление наркотиков постоянно сочетается со стимулами окружающей среды), и эти ассоциации становятся менее склонными к вымирание (т.е. «отучиться» от этих классически обусловленных ассоциаций между употреблением наркотиков и стимулами окружающей среды становится все труднее). После многократного спаривания эти классически обусловленные стимулы окружающей среды (например, контексты и объекты, которые часто сочетаются с употреблением наркотиков) часто становятся сигналы наркотиков которые функционируют как вторичные арматуры употребления наркотиков (то есть, как только эти ассоциации установлены, воздействие парного стимула окружающей среды запускает тяга или желание употребить наркотик, с которым они стали ассоциироваться ).[27][38]
В отличие от лекарств, высвобождение дофамина в оболочке NAcc многими типами полезных немедикаментозных стимулов обычно вызывает привыкание после многократного воздействия (т. Е. Количество дофамина, которое высвобождается в результате будущего воздействия полезного немедикаментозного стимула, обычно уменьшается. в результате многократного воздействия этого стимула).[27][38]
Депрессия
В апреле 2007 года две исследовательские группы сообщили о вставке электродов в прилежащее ядро, чтобы использовать глубокая стимуляция мозга лечить тяжелые депрессия.[65] В 2010 году эксперименты показали, что глубокая стимуляция прилежащего ядра мозга позволила уменьшить симптомы депрессии у 50% пациентов, которые не ответили на другие виды лечения, такие как электрошоковой терапии.[66] Nucleus accumbens также использовался в качестве мишени для лечения небольших групп пациентов с рефрактерным к терапии обсессивно-компульсивным расстройством.[67]
Абляция
Для лечения зависимости и в попытке лечить психические заболевания радиочастотная абляция прилежащего ядра. Результаты неубедительны и противоречивы.[68][69]
Эффект плацебо
Было показано, что активация NAcc происходит в ожидании эффективности лекарства, когда пользователю дают плацебо, что указывает на важную роль прилежащего ядра в эффект плацебо.[16][70]
Дополнительные изображения
Дофамин и серотонин
Коронарный срез МРТ, показывающий прилежащее ядро, обведенное красным

Сагиттальный срез МРТ с выделением (красным) прилежащего ядра.
Смотрите также
Рекомендации
- ^ а б Карлсон Н.Р. (2013). Физиология поведения (11-е изд.). Бостон: Пирсон.[страница нужна ]
- ^ Nucleus Accumbens
- ^ Икемото S (ноябрь 2010 г.). «Схема вознаграждения мозга за пределами мезолимбической дофаминовой системы: нейробиологическая теория». Неврология и биоповеденческие обзоры. 35 (2): 129–50. Дои:10.1016 / j.neubiorev.2010.02.001. ЧВК 2894302. PMID 20149820.
Недавние исследования внутричерепного самостоятельного введения нейрохимических веществ (лекарств) показали, что крысы учатся самостоятельно вводить различные препараты в мезолимбические структуры дофамина - заднюю вентральную тегментальную область, прилежащее ядро медиальной оболочки и медиальный обонятельный бугорок. ... В 1970-х годах было признано, что обонятельный бугорок содержит стриарный компонент, который заполнен ГАМКергическими средними шиповидными нейронами, получающими глутаматергические входные сигналы от кортикальных областей и дофаминергические входные сигналы от ВТА и проецирующиеся в вентральный паллидум так же, как прилежащее ядро.
Рисунок 3: Вентральное полосатое тело и самостоятельное введение амфетамина - ^ а б c d е ж грамм час я j Маленка Р.К., Нестлер Э.Дж., Хайман С.Е. (2009). Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: основа клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. С. 147–148, 367, 376. ISBN 978-0-07-148127-4.
Нейроны VTA DA играют решающую роль в мотивации, поведении, связанном с вознаграждением (глава 15), внимании и множественных формах памяти. Такая организация DA-системы, широкая проекция из ограниченного числа клеточных тел, позволяет скоординированно реагировать на новые мощные награды. Таким образом, действуя в различных конечных областях, дофамин придает мотивационную значимость («желание») самой награде или связанным с ней сигналам (область оболочки прилежащего ядра), обновляет значение, придаваемое различным целям, в свете этого нового опыта (орбитальная префронтальная кора), помогает консолидировать несколько форм памяти (миндалевидное тело и гиппокамп) и кодирует новые двигательные программы, которые облегчат получение этой награды в будущем (основная область прилежащего ядра и дорсальное полосатое тело). В этом примере дофамин модулирует обработку сенсомоторной информации в различных нейронных цепях, чтобы максимизировать способность организма получать будущие вознаграждения. ...
Схема вознаграждения мозга, на которую нацелены наркотики, вызывающие привыкание, обычно обеспечивает получение удовольствия и укрепление поведения, связанного с естественными подкреплениями, такими как еда, вода и сексуальный контакт. Дофаминовые нейроны в VTA активируются пищей и водой, а высвобождение дофамина в NAc стимулируется присутствием естественных подкрепляющих веществ, таких как еда, вода или половой партнер. ...
NAc и VTA являются центральными компонентами схемы, лежащей в основе вознаграждения и памяти о вознаграждении. Как упоминалось ранее, активность дофаминергических нейронов в VTA, по-видимому, связана с предсказанием вознаграждения. NAc участвует в обучении, связанном с подкреплением и модуляцией моторных ответов на стимулы, которые удовлетворяют внутренние гомеостатические потребности. Оболочка NAc, по-видимому, особенно важна для начальных действий лекарства в рамках схемы вознаграждения; наркотики, вызывающие привыкание, оказывают большее влияние на высвобождение дофамина в оболочке, чем в ядре NAc. - ^ а б c Депутат Саддориса, Ф. Каччапалья, Ф. Вайтман, Р. М. Карелли (август 2015 г.). «Дифференциальная динамика высвобождения дофамина в ядре Accumbens ядра и оболочке выявляет дополнительные сигналы для прогнозирования ошибок и мотивации». Журнал неврологии. 35 (33): 11572–82. Дои:10.1523 / JNEUROSCI.2344-15.2015. ЧВК 4540796. PMID 26290234.
Здесь мы обнаружили, что высвобождение дофамина в прилежащем ядре (первичная мишень дофаминовых нейронов среднего мозга) в реальном времени сильно различается между субрегионами ядра и оболочки. В основном динамика дофамина согласуется с теориями, основанными на обучении (такими как ошибка предсказания вознаграждения), тогда как в оболочке дофамин согласуется с теориями, основанными на мотивации (например, значимостью стимулов).
- ^ а б c Calipari ES, Bagot RC, Purushothaman I, Davidson TJ, Yorgason JT, Peña CJ, Walker DM, Pirpinias ST, Guise KG, Ramakrishnan C, Deisseroth K, Nestler EJ (март 2016 г.). «Визуализация in vivo идентифицирует временную сигнатуру шиповидных нейронов D1 и D2 в кокаиновой награде». Труды Национальной академии наук Соединенных Штатов Америки. 113 (10): 2726–31. Bibcode:2016PNAS..113.2726C. Дои:10.1073 / pnas.1521238113. ЧВК 4791010. PMID 26831103.
Повышенная активность мезолимбической дофаминовой системы является центральным механизмом, лежащим в основе подкрепляющих и вознаграждающих действий злоупотребляемых наркотиков, включая кокаин, а также компульсивного поиска наркотиков, который развивается с течением времени и характеризует состояние зависимости (10–12). Действие дофамина в NAc опосредуется преимущественно через активацию дофаминовых рецепторов D1 или D2, которые экспрессируются в основном неперекрывающимися популяциями нейронов со средними шипами (MSN) (13). Эти два подтипа MSN оказывают противоположное влияние на поведение, при этом оптогенетическая активация нейронов D1-типа способствует положительному подкреплению и увеличивает образование ассоциаций кокаинового вознаграждения и контекста, а активация нейронов D2-типа вызывает отвращение и снижает вознаграждение кокаином (14, 15). ; связанные различия в поведенческих реакциях наблюдаются в ответ на агонисты или антагонисты рецепторов D1 по сравнению с D2 (16). ... Предыдущая работа продемонстрировала, что оптогенетическая стимуляция D1 MSN способствует вознаграждению, тогда как стимуляция D2 MSN вызывает отвращение.
- ^ Венцель Дж. М., Раушер Н. А., Чир Дж. Ф., Олесон Е.Б. (январь 2015 г.). «Роль фазового высвобождения дофамина в прилежащем ядре в кодировании отвращения: обзор нейрохимической литературы». ACS Chemical Neuroscience. 6 (1): 16–26. Дои:10.1021 / cn500255p. ЧВК 5820768. PMID 25491156.
Таким образом, стимулы, вызывающие страх, способны по-разному изменять фазовую передачу дофамина в субрегионах NAcc. Авторы предполагают, что наблюдаемое повышение уровня дофамина оболочки NAcc, вероятно, отражает общую мотивационную значимость, возможно, из-за облегчения состояния страха, вызванного CS, когда УЗ (удар ногой) не применяется. Это рассуждение подтверждается отчетом Будыгина с коллегами.112 показывая, что у анестезированных крыс прекращение защемления хвоста приводит к увеличению высвобождения дофамина в панцире.
- ^ а б Маленка Р.К., Нестлер Э.Дж., Хайман С.Е. (2009). «Глава 10: Нейронный и нейроэндокринный контроль внутренней среды». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: основа клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. п. 266. ISBN 978-0-07-148127-4.
Дофамин действует в прилежащем ядре, придавая мотивационное значение стимулам, связанным с вознаграждением.
- ^ а б c Саламоне Дж. Д., Пардо М., Йон С. Е., Лопес-Крус Л., Сан-Мигель Н., Корреа М. (2016). «Мезолимбический допамин и регуляция мотивированного поведения». Актуальные темы поведенческой нейронауки. 27: 231–57. Дои:10.1007/7854_2015_383. ISBN 978-3-319-26933-7. PMID 26323245.
Значительные доказательства указывают на то, что accumbens DA важен для павловского подхода и передачи от Павлова к инструментам [(PIT)] ... PIT - это поведенческий процесс, который отражает влияние стимулов, обусловленных Павловым (CS), на инструментальную реакцию. Например, демонстрация Павловской CS в паре с едой может повысить результативность инструментального поведения, подкрепленного едой, такого как нажатие на рычаг. PIT, зависящий от результата, возникает, когда Павловский безусловный стимул (US) и инструментальное подкрепление являются одним и тем же стимулом, тогда как общий PIT, как говорят, возникает, когда Павловский US и подкрепление различны. ... Более свежие данные показывают, что ядро и оболочка прилегающих к телу, по-видимому, опосредуют различные аспекты PIT; повреждения оболочки и инактивация снижали PIT, специфичный для исхода, в то время как повреждения ядра и инактивация подавляли общую PIT (Corbit and Balleine 2011). Эти различия между ядром и панцирем, вероятно, связаны с разными анатомическими входами и бледными выходами, связанными с этими прилежащими подобластями (Root et al. 2015). Эти результаты привели Corbit and Balleine (2011) к предположению, что accumbens core опосредует общие возбуждающие эффекты сигналов, связанных с вознаграждением. PIT обеспечивает фундаментальный поведенческий процесс, посредством которого условные стимулы могут оказывать активирующее действие на инструментальную реакцию
- ^ а б c Корбит Л.Х., Баллейн Б.В. (2016). «Процессы обучения и мотивации, способствующие передаче инструментальных средств Павлова и их нейронные основы: дофамин и не только». Актуальные темы поведенческой нейронауки. 27: 259–89. Дои:10.1007/7854_2015_388. ISBN 978-3-319-26933-7. PMID 26695169.
Такие эффекты предполагают, что определенные мотивационные состояния ограничивают возбуждающие эффекты процессов стимулирования Павлова на инструментальную производительность ... Поведенческие данные подтверждаются свидетельствами того, что отдельные нейронные цепи, сосредоточенные на ядре и оболочке NAc, опосредуют общие и специфические формы передачи, соответственно, и текущая работа начинает объяснять, как павловские и инструментальные процессы обучения, которые происходят независимо и в разное время, интегрированы в нейронные цепи, управляющие поведенческим контролем.
- ^ а б c d Cherasse Y, Urade Y (ноябрь 2017 г.). «Диетический цинк действует как модулятор сна». Международный журнал молекулярных наук. 18 (11): 2334. Дои:10.3390 / ijms18112334. ЧВК 5713303. PMID 29113075.
Совсем недавно лаборатория Фуллера также обнаружила, что сну может способствовать активация гамма-аминомасляной кислоты-эргической (ГАМКергической) популяции нейронов, расположенных в парафациальной зоне [11,12], в то время как роль нейронов, экспрессирующих ГАМКергический A2AR, прилежащего ядра [13] и полосатого тела только что выявлено [14,15].
- ^ а б c d е ж грамм Валенсия Гарсия S, Форт П. (февраль 2018 г.). "Nucleus Accumbens, новая область регулирования сна посредством интеграции мотивационных стимулов". Acta Pharmacologica Sinica. 39 (2): 165–166. Дои:10.1038 / aps.2017.168. ЧВК 5800466. PMID 29283174.
Прилежащее ядро включает контингент нейронов, специфически экспрессирующих подтип постсинаптических рецепторов A2A (A2AR), что делает их возбудимыми под действием аденозина, его природного агониста, наделенного мощными способствующими засыпанию свойствами [4]. ... В обоих случаях большая активация нейронов, экспрессирующих A2AR, в NAc способствует медленноволновому сну (SWS) за счет увеличения количества и продолжительности эпизодов. ... После оптогенетической активации ядра наблюдали аналогичное продвижение SWS, тогда как при активации A2AR-экспрессирующих нейронов внутри оболочки не было индуцировано значительных эффектов.
- ^ а б c d е ж грамм Оиши Ю., Сюй Кью, Ван Л., Чжан Б.Дж., Такахаши К., Таката Ю., Ло Ю.Дж., Черасс Ю., Шиффманн С.Н., де Кершов д'Эксарде А., Ураде И., Ку В.М., Хуанг З.Л., Лазарус М. (сентябрь 2017 г.). «Медленноволновой сон у мышей контролируется подмножеством нейронов ядра прилежащего ядра». Nature Communications. 8 (1): 734. Bibcode:2017НатКо ... 8..734О. Дои:10.1038 / s41467-017-00781-4. ЧВК 5622037. PMID 28963505.
Здесь мы показываем, что хемогенетическая или оптогенетическая активация возбуждающих нейронов непрямого пути, экспрессирующих аденозиновый рецептор A2A, в центральной области NAc сильно индуцирует медленный сон. Хемогенетическое ингибирование нейронов непрямого пути NAc предотвращает индукцию сна, но не влияет на гомеостатический откат сна.
- ^ а б c Юань XS, Ван Л., Донг Х., Цюй В.М., Ян С.Р., Черасс Ю., Лазарус М., Шиффманн С.Н., д'Эксарде АК, Ли RX, Хуанг З.Л. (октябрь 2017 г.). «Нейроны рецептора 2A контролируют сон в активном периоде с помощью нейронов парвальбумина во внешнем бледном глобусе». eLife. 6: e29055. Дои:10.7554 / eLife.29055. ЧВК 5655138. PMID 29022877.
- ^ Schwienbacher I, Fendt M, Richardson R, Schnitzler HU (ноябрь 2004 г.). «Временная инактивация прилежащего ядра нарушает приобретение и выражение испуга, вызванного страхом, у крыс». Исследование мозга. 1027 (1–2): 87–93. Дои:10.1016 / j.brainres.2004.08.037. PMID 15494160.
- ^ а б Zubieta JK, Stohler CS (март 2009 г.). «Нейробиологические механизмы реакции на плацебо». Летопись Нью-Йоркской академии наук. 1156 (1): 198–210. Bibcode:2009НЯСА1156..198Z. Дои:10.1111 / j.1749-6632.2009.04424.x. ЧВК 3073412. PMID 19338509.
- ^ Basar K, Sesia T, Groenewegen H, Steinbusch HW, Visser-Vandewalle V, Temel Y (декабрь 2010 г.). «Прилежащее ядро и импульсивность». Прогресс в нейробиологии. 92 (4): 533–57. Дои:10.1016 / j.pneurobio.2010.08.007. PMID 20831892.
- ^ Гипсон С.Д., Купчик Ю.М., Каливас П.В. (январь 2014 г.). «Быстрая, преходящая синаптическая пластичность при зависимости». Нейрофармакология. 76 Pt B: 276–86. Дои:10.1016 / j.neuropharm.2013.04.032. ЧВК 3762905. PMID 23639436.
В упрощенной схеме PFC-NAc-VTA NAc служит «шлюзом», через который информация о направлении поведенческого выхода обрабатывается от лимбической коры к моторным подсхемам. Считается, что переход к навязчивому поиску наркотиков происходит из-за нарушенной способности этой подсистемы эффективно обрабатывать информацию о негативных непредвиденных обстоятельствах окружающей среды, что приводит к неспособности подавлять доминантные реакции, связанные с наркотиками; тем самым наркоман становится склонным к рецидиву.
Рисунок 1: Глутаматергические афференты к прилежащему ядру, участвующие в аддиктивном поведении - ^ а б c Ягер Л.М., Гарсия А.Ф., Вунш А.М., Фергюсон С.М. (август 2015 г.). «Все аспекты полосатого тела: роль в наркомании». Неврология. 301: 529–541. Дои:10.1016 / j.neuroscience.2015.06.033. ЧВК 4523218. PMID 26116518.
[Стриатум] получает дофаминергические входы из вентральной тегментальной области (VTA) и черной субстанции (SNr), а глутаматергические входы из нескольких областей, включая кору, гиппокамп, миндалевидное тело и таламус (Swanson, 1982; Phillipson and Griffiths, 1985; Finch, 1996; Groenewegen et al., 1999; Britt et al., 2012). Эти глутаматергические входы соприкасаются с головками дендритных шипов полосатых ГАМКергических нейронов проекции шипов (MSN), тогда как дофаминергические входные синапсы на шейке позвоночника, обеспечивая важное и сложное взаимодействие между этими двумя входами в модуляции активности MSN ... Следует также отметить, что существует небольшая популяция нейронов в NAc, которые коэкспрессируют рецепторы D1 и D2, хотя это в значительной степени ограничено оболочкой NAc (Bertran-Gonzalez et al., 2008). ... Нейроны в подразделениях ядра NAc и оболочки NAc также различаются функционально. Ядро NAc участвует в обработке условных стимулов, тогда как оболочка NAc более важна в обработке безусловных стимулов; Традиционно считается, что эти две популяции полосатого тела MSN оказывают противоположное влияние на продукцию базальных ганглиев. Активация dMSN вызывает общее возбуждение таламуса, приводящее к положительной петле корковой обратной связи; тем самым действуя как сигнал «идти» к началу поведения. Однако активация iMSN вызывает чистое ингибирование таламической активности, что приводит к отрицательной петле корковой обратной связи и, следовательно, служит «тормозом» для подавления поведения ... также появляется все больше свидетельств того, что iMSN играют роль в мотивации и зависимости ( Lobo, Nestler, 2011; Grueter et al., 2013). ... Вместе эти данные предполагают, что iMSN обычно действуют, чтобы сдерживать поведение, связанное с приемом наркотиков, и рекрутирование этих нейронов на самом деле может защищать от развития компульсивного употребления наркотиков.
- ^ а б c d е ж грамм час я j k Робисон А.Дж., Нестлер Э.Д. (октябрь 2011 г.). «Транскрипционные и эпигенетические механизмы зависимости». Обзоры природы. Неврология. 12 (11): 623–37. Дои:10.1038 / nrn3111. ЧВК 3272277. PMID 21989194.
ΔFosB был напрямую связан с несколькими зависимостями поведения ... Важно отметить, что генетическая или вирусная сверхэкспрессия ΔJunD, доминантно-отрицательного мутанта JunD, который противодействует ΔFosB- и другой AP-1-опосредованной транскрипционной активности, в NAc или OFC блокирует их. ключевые эффекты воздействия наркотиков14,22–24. Это указывает на то, что ΔFosB необходим и достаточен для многих изменений, вызываемых в мозге хроническим воздействием лекарств. ΔFosB также индуцируется в MSN NAc D1-типа при хроническом потреблении нескольких естественных наград, включая сахарозу, пищу с высоким содержанием жира, секс, бег колеса, где он способствует этому потреблению.14,26–30. Это означает, что ΔFosB участвует в регуляции естественного вознаграждения в нормальных условиях и, возможно, во время состояний, подобных патологическому привыканию. ... 95% нейронов NAc представляют собой ГАМКергические MSN (нейроны со средними шипами), которые можно далее дифференцировать на те MSN, которые экспрессируют рецептор дофамина D1 (MSN типа D1) и экспрессируют динорфин и вещество P, а также те, которые экспрессируют дофамин D2 рецептора (MSN D2-типа) и экспрессируют энкефалин132. Лекарственная индукция ΔFosB133,134, а влияние ΔFosB и G9a на морфологию и поведение клеток различается между MSN D1-типа и D2-типа.135, и нейрональная активность этих двух типов клеток оказывает противоположное влияние на полезные свойства кокаина.131. ... Около 1–2% нейронов NAc представляют собой аспиновые большие холинергические интернейроны, которые, как было показано, играют важную роль в вознаграждении за кокаин.130, и примерно такое же количество ГАМКергических интернейронов, функции которых менее изучены.
- ^ а б c d е Блюм К., Вернер Т., Карнес С., Карнес П., Бовиррат А., Джордано Дж., Оскар-Берман М., Голд М. (2012). «Секс, наркотики и рок-н-ролл: гипотеза о распространенной мезолимбической активации как функции полиморфизма генов вознаграждения». Журнал психоактивных препаратов. 44 (1): 38–55. Дои:10.1080/02791072.2012.662112. ЧВК 4040958. PMID 22641964.
Было обнаружено, что ген deltaFosB в NAc имеет решающее значение для усиления эффектов сексуального вознаграждения. Питчерс и его коллеги (2010) сообщили, что сексуальный опыт вызывает накопление DeltaFosB в нескольких лимбических областях мозга, включая NAc, медиальную префронтальную кору, VTA, хвостатую часть и скорлупу, но не в медиальном преоптическом ядре. Затем индукция c-Fos, нижестоящей (репрессированной) мишени DeltaFosB, была измерена у опытных половым путем и наивных животных. Количество индуцированных спариванием клеток c-Fos-IR было значительно снижено у животных, имевших опыт сексуальной жизни, по сравнению с контрольными животными, не подвергавшимися сексуальному воздействию. Наконец, уровнями DeltaFosB и его активностью в NAc манипулировали с помощью вирусно-опосредованного переноса генов, чтобы изучить его потенциальную роль в опосредовании сексуального опыта и облегчении сексуальной активности, вызванном опытом. Животные со сверхэкспрессией DeltaFosB продемонстрировали улучшенное облегчение сексуальной активности с сексуальным опытом по сравнению с контрольной группой. Напротив, экспрессия DeltaJunD, доминантно-негативного партнера по связыванию DeltaFosB, ослабляла индуцированное сексуальным опытом облегчение сексуальной активности и замедляла долгосрочное поддержание фасилитации по сравнению с группой со сверхэкспрессией DeltaFosB. В совокупности эти данные подтверждают критическую роль экспрессии DeltaFosB в NAc в усиливающих эффектах сексуального поведения и индуцированного сексуальным опытом облегчения сексуальной активности. ... и наркомания, и сексуальная зависимость представляют собой патологические формы нейропластичности наряду с появлением аберрантного поведения, включающего каскад нейрохимических изменений, главным образом в цепях вознаграждения мозга.
- ^ Гото Y, О'Доннелл П. (февраль 2001 г.). «Синхронная активность в гиппокампе и прилежащем ядре in vivo». Журнал неврологии. 21 (4): RC131. Дои:10.1523 / jneurosci.21-04-j0003.2001. ЧВК 6762233. PMID 11160416.
- ^ Маленка Р.К., Нестлер Э.Дж., Хайман С.Е. (2009). «Глава 6: Широко распространяющиеся системы: моноамины, ацетилхолин и орексин». В Sydor A, Brown RY (ред.). Молекулярная нейрофармакология: основа клинической неврологии (2-е изд.). Нью-Йорк: McGraw-Hill Medical. С. 175–176. ISBN 978-0-07-148127-4.
В головном мозге гистамин синтезируется исключительно нейронами с их клеточными телами в туберомаммиллярном ядре (TMN), которое находится в задней части гипоталамуса. У человека примерно 64000 гистаминергических нейронов на каждой стороне. Эти клетки проецируются по всему головному и спинному мозгу. Области, которые получают особенно плотные проекции, включают кору головного мозга, гиппокамп, неостриатум, прилежащее ядро, миндалевидное тело и гипоталамус. ... В то время как наиболее охарактеризованная функция гистаминовой системы в головном мозге - регуляция сна и возбуждения, гистамин также участвует в обучении и памяти ... Также оказывается, что гистамин участвует в регуляции питания и энергетического баланса.
- ^ Барро М., Сесак С.Р., Жорж Ф., Пистис М., Хонг С., Джоу Т.К. (октябрь 2012 г.). «Торможение дофаминовых систем: новая основная структура ГАМК для мезолимбических и нигростриатальных функций». Журнал неврологии. 32 (41): 14094–101. Дои:10.1523 / JNEUROSCI.3370-12.2012. ЧВК 3513755. PMID 23055478.
- ^ Ферре С., Луис К., Джастинова З., Кирос С., Орру М., Наварро Дж., Канела Е. И., Франко Р., Голдберг С. Р. (июнь 2010 г.). «Взаимодействие аденозин-каннабиноидных рецепторов. Влияние на стриатальную функцию». Br. J. Pharmacol. 160 (3): 443–453. Дои:10.1111 / j.1476-5381.2010.00723.x. ЧВК 2931547. PMID 20590556.
Два класса MSN, которые гомогенно распределены в полосатом теле, можно различить по их выходной связности и экспрессии дофаминовых и аденозиновых рецепторов и нейропептидов. В дорсальном полосатом теле (в основном представленном хвостатым ядром-скорлупой) энкефалинергические MSN соединяют полосатое тело с бледным шаром (латеральный бледный шар) и экспрессируют пептид энкефалин и высокую плотность рецепторов дофамина D2 и аденозина A2A (они также экспрессируют аденозин. A1 рецепторы), в то время как динорфинергические MSN соединяют полосатое тело с черной субстанцией (pars compacta и reticulata) и энтопедункулярным ядром (medial globus pallidus) и экспрессируют пептиды динорфин и вещество P, а также дофамин D1 и аденозин A1, но не рецепторы A2A ... Эти два различных фенотипа MSN также присутствуют в вентральном полосатом теле (в основном представленном прилежащим ядром и обонятельным бугорком). Однако, хотя они фенотипически идентичны своим дорсальным собратьям, у них есть некоторые различия с точки зрения связности. Во-первых, не только энкефалинэргические, но и динорфинэргические MSNs проецируются на вентральный аналог латерального бледного глобуса, вентральный бледный шар, который, фактически, имеет характеристики как латерального, так и медиального бледного шара в его афферентной и эфферентной связности. В дополнение к вентральному паллидуму, медиальному бледному шару и черной субстанции-VTA, вентральное полосатое тело посылает проекции на расширенную миндалину, латеральный гипоталамус и тегментальное ядро педункулопонтина. ... Также важно упомянуть, что небольшой процент MSNs имеют смешанный фенотип и экспрессируют рецепторы D1 и D2 (Surmeier et al., 1996).
- ^ Ниси А., Куроива М., Шуто Т. (июль 2011 г.). «Механизмы модуляции передачи сигналов рецептора дофамина d (1) в нейронах полосатого тела». Фронт нейроанат. 5: 43. Дои:10.3389 / fnana.2011.00043. ЧВК 3140648. PMID 21811441.
Дофамин играет критически важную роль в регуляции психомоторных функций мозга (Bromberg-Martin et al., 2010; Cools, 2011; Gerfen and Surmeier, 2011). Рецепторы дофамина представляют собой суперсемейство рецепторов, связанных с гепталическим G-белком, и подразделяются на две категории, D1-подобные (D1, D5) и D2-подобные (D2, D3, D4) рецепторы, в зависимости от функциональных свойств стимулировать аденилатциклазу. (AC) через Gs / olf и ингибировать AC через Gi / o, соответственно ... Было продемонстрировано, что рецепторы D1 образуют гетероолигомер с рецепторами D2, и что гетероолигомер рецептора D1-D2 предпочтительно соединяется с Gq / PLC-сигнализация (Рашид и др., 2007a, b). Экспрессия дофаминовых рецепторов D1 и D2 в значительной степени сегрегирована в нейронах прямого и непрямого пути в дорсальном полосатом теле, соответственно (Gerfen et al., 1990; Hersch et al., 1995; Heiman et al., 2008). Однако известно, что некоторая часть нейронов со средними шипами экспрессирует как рецепторы D1, так и D2 (Hersch et al., 1995). Анализ экспрессии генов с использованием метода ОТ-ПЦР отдельных клеток показал, что 40% нейронов со средними шипами экспрессируют мРНК рецепторов D1 и D2 (Surmeier et al., 1996).
- ^ а б c d е ж Shirayama Y, Chaki S (октябрь 2006 г.). «Нейрохимия прилежащего ядра и ее связь с депрессией и антидепрессивным действием у грызунов». Современная нейрофармакология. 4 (4): 277–91. Дои:10.2174/157015906778520773. ЧВК 2475798. PMID 18654637.
- ^ Meredith GE, Agolia R, Arts MP, Groenewegen HJ, Zahm DS (сентябрь 1992 г.). «Морфологические различия между проекционными нейронами ядра и оболочки в прилежащем ядре крысы». Неврология. 50 (1): 149–62. Дои:10.1016 / 0306-4522 (92) 90389-к. PMID 1383869.
- ^ а б c Мередит Г.Е., Пеннарц С.М., Гроеневеген HJ (1993). «Клеточная основа для химической передачи сигналов в прилежащем ядре». Химическая передача сигналов в базальных ганглиях. Прогресс в исследованиях мозга. 99. С. 3–24. Дои:10.1016 / s0079-6123 (08) 61335-7. ISBN 978-0-444-81562-0. PMID 7906426.
- ^ а б c d Берридж К.С., Крингельбах М.Л. (май 2015 г.). «Системы удовольствия в мозгу». Нейрон. 86 (3): 646–64. Дои:10.1016 / j.neuron.2015.02.018. ЧВК 4425246. PMID 25950633.
- ^ Балики М.Н., Мансур А., Бариа А.Т., Хуанг Л., Бергер С.Е., Филдс Н.Л., Апкарян А.В. (октябрь 2013 г.). «Разделение прилежащего человека на предполагаемое ядро и оболочку разъединяет кодирование ценностей вознаграждения и боли». Журнал неврологии. 33 (41): 16383–93. Дои:10.1523 / JNEUROSCI.1731-13.2013. ЧВК 3792469. PMID 24107968.
Недавние данные показывают, что инактивация рецепторов D2 в непрямом стриатопаллидном пути у грызунов необходима как для приобретения, так и для выражения аверсивного поведения, а активация рецептора D1 прямого пути контролирует обучение, основанное на вознаграждении (Hikida et al., 2010; Hikida et al. ., 2013). Похоже, мы можем сделать вывод, что прямые и непрямые пути NAc через рецепторы D1 и D2 подчиняют различные роли ожидания и оценки в оболочке и ядре NAc, что согласуется с наблюдениями относительно пространственной сегрегации и разнообразия ответов дофаминергических нейронов среднего мозга. для условий вознаграждения и отвращения, одни кодируют мотивационную ценность, другие - мотивационную значимость, каждая из которых связана с отдельными сетями мозга и играет определенную роль в мотивационном контроле (Bromberg-Martin et al., 2010; Cohen et al., 2012; Lammel et al., 2013). ... Таким образом, предыдущие результаты в сочетании с текущими наблюдениями предполагают, что ответ NAc pshell отражает сигнал прогнозирования / ожидания или значимости, а ответ NAc pcore является оценочным ответом (сигнал прогнозирования вознаграждения), который сигнализирует об отрицательном значении подкрепления. прекращения боли (т. е. ожидаемого обезболивания).
- ^ а б Картони Э., Пуглиси-Аллегра С., Бальдассарр Г (ноябрь 2013 г.). «Три принципа действия: Павловско-инструментальная гипотеза переноса». Границы поведенческой нейробиологии. 7: 153. Дои:10.3389 / fnbeh.2013.00153. ЧВК 3832805. PMID 24312025.
- ^ Ричард Дж. М., Кастро, округ Колумбия, Дифеличеантонио АГ, Робинсон М.Дж., Берридж К.С. (ноябрь 2013 г.). «Отображение мозговых цепей вознаграждения и мотивации: по стопам Энн Келли». Неврология и биоповеденческие обзоры. 37 (9 Pt A): 1919–31. Дои:10.1016 / j.neubiorev.2012.12.008. ЧВК 3706488. PMID 23261404.
Рисунок 3: Нейронные цепи, лежащие в основе мотивированного «желания» и гедонистического «симпатии». - ^ Берридж К.С., Робинсон Т.Э., Олдридж Дж. В. (февраль 2009 г.). «Разделение компонентов вознаграждения:« симпатия »,« желание »и обучение». Текущее мнение в фармакологии. 9 (1): 65–73. Дои:10.1016 / j.coph.2008.12.014. ЧВК 2756052. PMID 19162544.
- ^ а б Nestler EJ (декабрь 2013 г.). «Клеточная основа памяти при зависимости». Диалоги в клинической неврологии. 15 (4): 431–43. ЧВК 3898681. PMID 24459410.
НЕСМОТРЯ НА ВАЖНОСТЬ МНОГОЧИСЛЕННЫХ ПСИХОСОЦИАЛЬНЫХ ФАКТОРОВ, В СВОЕЙ ОСНОВНОЙ ЦЕЛЕ НАРКОЗАВИСИМОСТЬ ВКЛЮЧАЕТ БИОЛОГИЧЕСКИЙ ПРОЦЕСС: способность многократного воздействия наркотика, вызывающего злоупотребление, вызывать изменения в уязвимом мозге, которые вызывают компульсивный поиск и прием наркотиков, а также потерю контроля над употреблением наркотиков, которые определяют состояние зависимости. ... Большое количество литературы продемонстрировало, что такая индукция ΔFosB в нейронах NAc D1-типа увеличивает чувствительность животного к лекарству, а также естественное вознаграждение и способствует самостоятельному введению лекарства, предположительно посредством процесса положительного подкрепления ... Например, , субрегионы оболочки и ядра NAc обнаруживают различия в индуцированной лекарствами синаптической пластичности, как и D1- по сравнению с D2-типами средние шиповатые нейроны в каждой подобласти.60,63,64,67
- ^ Думитриу Д., Лаплант К., Гроссман Ю.С., Диас К., Янссен В.Г., Руссо С.Дж., Моррисон Дж. Х., Нестлер Э.Д. (май 2012 г.). «Субрегиональная, дендритная компартмент и специфичность подтипа шипов в регуляции кокаином дендритных шипов в прилежащем ядре». Журнал неврологии. 32 (20): 6957–66. Дои:10.1523 / JNEUROSCI.5718-11.2012. ЧВК 3360066. PMID 22593064.
Устойчивое изменение плотности позвоночника в ядре, но не в оболочке, хорошо согласуется с устоявшейся идеей о том, что оболочка преимущественно участвует в развитии зависимости, в то время как ядро опосредует долгосрочное выполнение усвоенного поведения, связанного с зависимостью (Ito et al., 2004 ; Di Chiara, 2002; Meredith et al., 2008). В соответствии с идеей, что ядро NAc является локусом длительной нейропластичности, вызванной лекарственными средствами, несколько исследований показали, что электрофизиологические изменения в ядре сохраняются дольше, чем их аналоги в оболочке. ... Кроме того, представленные здесь данные подтверждают идею о том, что оболочка NAc предпочтительно участвует в немедленном вознаграждении за наркотики, в то время как ядро может играть более явную роль в долгосрочных аспектах зависимости.
- ^ Pontieri FE, Tanda G, Di Chiara G (декабрь 1995 г.). «Внутривенный кокаин, морфин и амфетамин преимущественно увеличивают внеклеточный дофамин в« оболочке »по сравнению с« ядром »прилежащего ядра крысы». Труды Национальной академии наук Соединенных Штатов Америки. 92 (26): 12304–8. Bibcode:1995ПНАС ... 9212304П. Дои:10.1073 / пнас.92.26.12304. JSTOR 2369093. ЧВК 40345. PMID 8618890.
- ^ а б c Ди Кьяра Джи (декабрь 2002 г.). «Оболочка прилежащего ядра и дофамин ядра: различная роль в поведении и зависимости». Поведенческие исследования мозга. 137 (1–2): 75–114. Дои:10.1016 / s0166-4328 (02) 00286-3. PMID 12445717.
- ^ Эйден Л. Е., Вэйхэ Э (январь 2011 г.). «VMAT2: динамический регулятор моноаминергической нейрональной функции мозга, взаимодействующий с наркотиками, вызывающими злоупотребление». Летопись Нью-Йоркской академии наук. 1216 (1): 86–98. Bibcode:2011НЯСА1216 ... 86Е. Дои:10.1111 / j.1749-6632.2010.05906.x. ЧВК 4183197. PMID 21272013.
VMAT2 является везикулярным переносчиком ЦНС не только для биогенных аминов DA, NE, EPI, 5-HT и HIS, но, вероятно, также для следовых аминов TYR, PEA и тиронамина (THYR) ... [Следы аминергических] нейронов в ЦНС млекопитающих можно идентифицировать как нейроны, экспрессирующие VMAT2 для хранения, и биосинтетический фермент декарбоксилазу ароматических аминокислот (AADC).
- ^ Барро М., Маринелли М., Абрус Д. Н., Руже-Пон Ф., Ле Моаль М., Piazza PV (март 2000 г.). «Дофаминергическая гиперчувствительность оболочки прилежащего ядра зависит от гормонов». Европейский журнал нейробиологии. 12 (3): 973–9. Дои:10.1046 / j.1460-9568.2000.00996.x. PMID 10762327.
- ^ Акияма Г., Икеда Х, Мацудзаки С., Сато М., Морибе С., Кошикава Н., Охлаждение А. Р. (июнь 2004 г.). «Рецепторы GABAA и GABAB в оболочке прилежащего ядра по-разному модулируют опосредованное рецептором допамина и ацетилхолина поворотное поведение». Нейрофармакология. 46 (8): 1082–8. Дои:10.1016 / j.neuropharm.2004.02.007. PMID 15111014.
- ^ Смит-Роу С.Л., Садегиан К., Келли А.Е. (август 1999 г.). «Пространственное обучение и производительность в лабиринте с лучевой рукой ухудшаются после блокады рецептора N-метил-D-аспартата (NMDA) в субрегионах полосатого тела». Поведенческая неврология. 113 (4): 703–17. Дои:10.1037/0735-7044.113.4.703. PMID 10495079.
- ^ Giertler C, Bohn I, Hauber W (март 2005 г.). «Вовлечение рецепторов NMDA и AMPA / KA в ядро прилежащего ядра в инструментальном обучении, управляемом подсказками, предсказывающими вознаграждение». Европейский журнал нейробиологии. 21 (6): 1689–702. Дои:10.1111 / j.1460-9568.2005.03983.x. PMID 15845096.
- ^ а б c d е ж грамм час я j k л м п о п q Олсен CM (декабрь 2011 г.). «Естественные награды, нейропластичность и немедикаментозные зависимости». Нейрофармакология. 61 (7): 1109–22. Дои:10.1016 / j.neuropharm.2011.03.010. ЧВК 3139704. PMID 21459101.
Перекрестная сенсибилизация также является двунаправленной, поскольку введение амфетамина в анамнезе способствует сексуальному поведению и усиливает связанное с этим повышение NAc DA ... Как описано для пищевого вознаграждения, сексуальный опыт также может привести к активации связанных с пластичностью сигнальных каскадов.Фактор транскрипции delta FosB увеличивается в NAc, PFC, дорсальном полосатом теле и VTA после повторного полового поведения (Wallace et al., 2008; Pitchers et al., 2010b). Это естественное увеличение delta FosB или вирусная избыточная экспрессия delta FosB в NAc модулирует сексуальную активность, а блокада NAc delta FosB ослабляет это поведение (Hedges et al., 2009; Pitchers et al., 2010b). Более того, вирусная сверхэкспрессия delta FosB усиливает обусловленное предпочтение места для окружающей среды в сочетании с сексуальным опытом (Hedges et al., 2009). ...
Таблица 1 - ^ Дэй Джей Джей, Карелли Р.М. (апрель 2007 г.). «Прилежащее ядро и Павловское вознаграждение». Нейробиолог. 13 (2): 148–59. Дои:10.1177/1073858406295854. ЧВК 3130622. PMID 17404375.
В соответствии с другими сообщениями (Nicola and others 2004; Taha and Fields 2006) преобладающим ответом нейронов NAc на инфузии сахарозы было снижение активности (рис. 2). Как видно из рисунка 2, одни и те же нейроны проявляли противоположные реакции, когда аверсивный раствор хинина вводился внутрь. Одна из гипотез предполагает, что ингибирование, наблюдаемое во время доставки вознаграждения, происходит среди ГАМК-содержащих нейронов NAc, которые проецируются на важные моторные области, такие как вентральный паллидум (VP).
- ^ Карлезон WA, Томас MJ (2009). «Биологические субстраты награды и отвращения: гипотеза активности прилежащего ядра». Нейрофармакология. 56 Дополнение 1: 122–32. Дои:10.1016 / j.neuropharm.2008.06.075. ЧВК 2635333. PMID 18675281.
При совместном рассмотрении эти исследования предоставили два важных доказательства, которые сыграли важную роль в формулировании нашей текущей рабочей гипотезы: во-первых, что дофамин-зависимое вознаграждение ослабляется блокадой D2-подобных рецепторов, которые являются ингибирующими рецепторами, преимущественно выраженными. в NAc на MSN непрямого пути; и, во-вторых, событий, которые, как ожидается, снизят общую возбудимость NAc (например, стимуляция Gi-связанных опиоидных рецепторов, снижение стимуляции возбуждающих рецепторов NMDA, снижение возбуждающего входа), достаточно для вознаграждения. Эта интерпретация привела к разработке модели вознаграждения, в которой критическим событием является уменьшение активации MSN в NAc.
- ^ Коста В.Д., Ланг П.Дж., Сабатинелли Д., Версаче Ф., Брэдли М.М. (сентябрь 2010 г.). «Эмоциональные образы: оценка удовольствия и возбуждения в цепи вознаграждения мозга». Картирование человеческого мозга. 31 (9): 1446–57. Дои:10.1002 / hbm.20948. ЧВК 3620013. PMID 20127869.
- ^ Sabatinelli D, Bradley MM, Lang PJ, Costa VD, Versace F (сентябрь 2007 г.). «Удовольствие, а не заметность активируют прилежащее ядро человека и медиальную префронтальную кору». Журнал нейрофизиологии. 98 (3): 1374–9. Дои:10.1152 / ян.00230.2007. PMID 17596422.
- ^ Могенсон Г.Дж., Джонс Д.Л., Йим С.Ю. (1980). «От мотивации к действию: функциональный интерфейс между лимбической системой и двигательной системой». Прогресс в нейробиологии. 14 (2–3): 69–97. Дои:10.1016/0301-0082(80)90018-0. PMID 6999537.
- ^ Харт Дж., Люнг Б.К., Баллейн Б.В. (февраль 2014 г.). «Дорсальный и вентральный потоки: особая роль полосатых субрегионов в приобретении и выполнении целенаправленных действий». Нейробиология обучения и памяти. 108: 104–18. Дои:10.1016 / j.nlm.2013.11.003. ЧВК 4661143. PMID 24231424.
- ^ Кастро, округ Колумбия, Коул С.Л., Берридж К.С. (2015). «Роли латерального гипоталамуса, прилежащего ядра и брюшной паллидума в еде и голоде: взаимодействие между гомеостатической схемой и схемой вознаграждения». Границы системной нейробиологии. 9: 90. Дои:10.3389 / fnsys.2015.00090. ЧВК 4466441. PMID 26124708.
- ^ Берридж К.С., Крингельбах М.Л. (июнь 2013 г.). «Неврология аффекта: мозговые механизмы удовольствия и неудовольствия». Текущее мнение в нейробиологии. 23 (3): 294–303. Дои:10.1016 / j.conb.2013.01.017. ЧВК 3644539. PMID 23375169.
- ^ Инь ХХ, Остлунд С.Б., Баллейн Б.В. (октябрь 2008 г.). «Обучение, направленное на вознаграждение, помимо допамина в прилежащем ядре: интегративные функции сетей кортико-базальных ганглиев». Европейский журнал нейробиологии. 28 (8): 1437–48. Дои:10.1111 / j.1460-9568.2008.06422.x. ЧВК 2756656. PMID 18793321.
- ^ Соарес-Кунья С., Коимбра Б., Суза Н., Родригес А.Дж. (сентябрь 2016 г.). "Переоценка D1- и D2-нейронов полосатого тела в поощрении и отвращении" (PDF). Неврология и биоповеденческие обзоры. 68: 370–386. Дои:10.1016 / j.neubiorev.2016.05.021. HDL:1822/47044. PMID 27235078.
- ^ Соарес-Кунья С., Коимбра Б., Домингес А.В., Васконселос Н., Соуза Н., Родригес А.Дж. (19 апреля 2018 г.). «Микросхема Nucleus Accumbens, лежащая в основе повышения мотивации, вызванного D2-MSN». eNeuro. 5 (2): ENEURO.0386–18.2018. Дои:10.1523 / ENEURO.0386-18.2018. ЧВК 5957524. PMID 29780881.
Оптогенетическая активация D2-MSN снижала активность вентрального паллида (VP), снижая подавляющий тон к VTA, что приводило к увеличению дофаминергической активности. Важно отметить, что оптогенетическая активация концов D2-MSN в VP была достаточной, чтобы повторить усиление мотивации.
- ^ Феррис К.Ф., Кулкарни П., Салливан Дж. М., Хардер Дж. А., Посланник Т. Л., Фебо М. (январь 2005 г.). «Сосание щенком полезнее, чем кокаин: данные функциональной магнитно-резонансной томографии и трехмерного компьютерного анализа». Журнал неврологии. 25 (1): 149–56. arXiv:1510.02343. Дои:10.1523 / jneurosci.3156-04.2005. ЧВК 6725197. PMID 15634776.
- ^ Нуман М (январь 2007 г.). «Мотивационные системы и нейронные схемы материнского поведения у крысы». Психобиология развития. 49 (1): 12–21. Дои:10.1002 / dev.20198. PMID 17186513.
- ^ Glocker ML, Langleben DD, Ruparel K, Loughead JW, Valdez JN, Griffin MD, Sachser N, Gur RC (июнь 2009 г.). «Схема ребенка модулирует систему вознаграждения мозга у нерожавших женщин». Труды Национальной академии наук Соединенных Штатов Америки. 106 (22): 9115–9. Bibcode:2009PNAS..106.9115G. Дои:10.1073 / pnas.0811620106. JSTOR 40482823. ЧВК 2690007. PMID 19451625.
- ^ а б Хайман С.Е., Маленка Р.С., Нестлер Е.Дж. (2006). «Нейронные механизмы зависимости: роль обучения и памяти, связанных с вознаграждением». Ежегодный обзор нейробиологии. 29: 565–98. Дои:10.1146 / annurev.neuro.29.051605.113009. PMID 16776597.
- ^ Штайнер Х., Ван Вэйс В. (январь 2013 г.). «Регулирование генов, связанных с зависимостью: риски воздействия когнитивных усилителей по сравнению с другими психостимуляторами». Прогресс в нейробиологии. 100: 60–80. Дои:10.1016 / j.pneurobio.2012.10.001. ЧВК 3525776. PMID 23085425.
- ^ а б Ruffle JK (ноябрь 2014 г.). «Молекулярная нейробиология зависимости: что такое (Δ) FosB?». Американский журнал злоупотребления наркотиками и алкоголем. 40 (6): 428–37. Дои:10.3109/00952990.2014.933840. PMID 25083822.
ΔFosB является важным фактором транскрипции, участвующим в молекулярных и поведенческих механизмах привыкания после многократного воздействия наркотиков. Образование ΔFosB во многих областях мозга и молекулярный путь, ведущий к образованию комплексов AP-1, хорошо изучены. Установление функционального назначения ΔFosB позволило дополнительно определить некоторые ключевые аспекты его молекулярных каскадов, включая такие эффекторы, как GluR2 (87,88), Cdk5 (93) и NFkB (100). Более того, многие из этих выявленных молекулярных изменений теперь напрямую связаны со структурными, физиологическими и поведенческими изменениями, наблюдаемыми после хронического воздействия лекарств (60,95,97,102). Эпигенетические исследования открыли новые горизонты исследований молекулярной роли ΔFosB, а недавние достижения продемонстрировали роль ΔFosB, действующего на ДНК и гистоны, действительно как молекулярный переключатель (34).
- ^ Kanehisa Laboratories (29 октября 2014 г.). «Алкоголизм - Homo sapiens (человек)». KEGG Pathway. Получено 31 октября 2014.
- ^ Ким Й., Тейлан М.А., Барон М., Сэндс А., Нэрн А.С., Грингард П. (февраль 2009 г.). «Метилфенидат-индуцированное образование дендритных шипов и экспрессия DeltaFosB в прилежащем ядре». Труды Национальной академии наук Соединенных Штатов Америки. 106 (8): 2915–20. Bibcode:2009ПНАС..106.2915К. Дои:10.1073 / pnas.0813179106. ЧВК 2650365. PMID 19202072.
- ^ Кувшины К.К., Виалу В., Нестлер Э.Дж., Лавиолетт С.Р., Леман М.Н., Кулен Л.М. (февраль 2013 г.). «Естественные и лекарственные вознаграждения воздействуют на общие механизмы нейронной пластичности с ΔFosB в качестве ключевого посредника». Журнал неврологии. 33 (8): 3434–42. Дои:10.1523 / JNEUROSCI.4881-12.2013. ЧВК 3865508. PMID 23426671.
Наркотики, вызывающие злоупотребление, вызывают нейропластичность в естественном пути вознаграждения, особенно в прилежащем ядре (NAc), тем самым вызывая развитие и проявление аддиктивного поведения. ... В совокупности эти результаты демонстрируют, что злоупотребление наркотиками и поведение, основанное на естественном вознаграждении, воздействуют на общие молекулярные и клеточные механизмы пластичности, которые контролируют уязвимость к наркомании, и что эта повышенная уязвимость опосредуется ΔFosB и его нижележащими транскрипционными мишенями. ... Сексуальное поведение очень полезно (Tenk et al., 2009), а сексуальный опыт вызывает сенсибилизированное поведение, связанное с наркотиками, включая перекрестную сенсибилизацию к локомоторной активности, вызванной амфетамином (Amph) (Bradley and Meisel, 2001; Pitchers et al. ., 2010a) и увеличенное вознаграждение Amph (Pitchers et al., 2010a). Более того, сексуальный опыт вызывает нейрональную пластичность в NAc, аналогичную той, которая вызывается воздействием психостимуляторов, включая увеличение плотности дендритных шипов (Meisel and Mullins, 2006; Pitchers et al., 2010a), изменение трафика рецепторов глутамата и снижение синаптической силы в префронтальной коре -отвечающие нейроны оболочки NAc (Pitchers et al., 2012). Наконец, периоды воздержания от сексуального опыта оказались критическими для усиления вознаграждения Amph, спиногенеза NAc (Pitchers et al., 2010a) и трафика глутаматных рецепторов (Pitchers et al., 2012). Эти результаты показывают, что природное вознаграждение и награда за лекарство имеют общие механизмы нервной пластичности.
- ^ Мозговые электроды помогают лечить депрессию, Обзор технологий, 26 апреля 2007 г.
- ^ Bewernick BH, Hurlemann R, Matusch A, Kayser S, Grubert C, Hadrysiewicz B, Axmacher N, Lemke M, Cooper-Mahkorn D, Cohen MX, Brockmann H, Lenartz D, Sturm V, Schlaepfer TE (январь 2010 г.). «Глубокая стимуляция мозга Nucleus accumbens снижает вероятность депрессии и тревожности при устойчивой к лечению депрессии». Биологическая психиатрия. 67 (2): 110–6. Дои:10.1016 / j.biopsych.2009.09.013. PMID 19914605.
- ^ Ooms P, Mantione M, Figee M, Schuurman PR, van den Munckhof P, Denys D (февраль 2014 г.). «Глубокая стимуляция мозга при обсессивно-компульсивных расстройствах: долгосрочный анализ качества жизни». Журнал неврологии, нейрохирургии и психиатрии. 85 (2): 153–8. Дои:10.1136 / jnnp-2012-302550. PMID 23715912.
- ^ "Спорная хирургия для лечения наркозависимости сгорает центр удовольствия мозга" Автор Майя Салавиц. 13 декабря 2012 г.
- ^ "Китай запрещает необратимую мозговую процедуру" Автор Замиска Николас. 28 апреля 2008 г. The Wall Street Journal
- ^ Скотт Д.Д., Столер С.С., Эгнатук К.М., Ван Х., Коппе Р.А., Зубиета Дж.К. (июль 2007 г.). «Индивидуальные различия в реакции на вознаграждение объясняют ожидания и эффекты, вызванные плацебо». Нейрон. 55 (2): 325–36. Дои:10.1016 / j.neuron.2007.06.028. PMID 17640532. Сложить резюме – Cell Press (18 июля 2007 г.).
внешняя ссылка
- Роль прилежащего ядра в цепи вознаграждения. Часть «Мозг сверху донизу». на thebrain.mcgill.ca
- Nucleus Accumbens - база данных, ориентированная на клетки
- Окрашенные изображения срезов головного мозга, содержащие «ядро% 20accumbens» на Проект BrainMaps



