Фосфоинозитид-3-киназа - Phosphoinositide 3-kinase
| Фосфатидилинозитол-4,5-бисфосфат-3-киназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
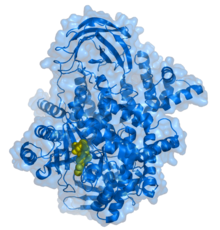 Ингибитор PIK-93 (желтый) связывается с гамма-субъединицей PI3K 110.[1] | |||||||||
| Идентификаторы | |||||||||
| Символ | PI3K | ||||||||
| Pfam | PF00454 | ||||||||
| ИнтерПро | IPR000403 | ||||||||
| УМНАЯ | SM00146 | ||||||||
| PROSITE | PDOC00710 | ||||||||
| SCOP2 | 3гмм / Объем / СУПФАМ | ||||||||
| OPM суперсемейство | 265 | ||||||||
| Белок OPM | 3 мл9 | ||||||||
| |||||||||
| Фосфоинозитид-3-киназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Номер ЕС | 2.7.1.137 | ||||||||
| Количество CAS | 115926-52-8 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
Фосфоинозитид-3-киназы (PI3K), также называемый фосфатидилинозитол-3-киназы, семья ферменты участвует в клеточных функциях, таких как рост, пролиферация, дифференциация, подвижность, выживание и внутриклеточный транспорт, которые, в свою очередь, участвуют в развитии рака.
PI3K представляют собой семейство родственных внутриклеточных преобразователь сигнала ферменты, способные фосфорилировать 3 положение гидроксил группа инозитол кольцо фосфатидилинозитол (PtdIns).[2] Путь, с онкоген PIK3CA и ген-супрессор опухоли PTEN, участвует в чувствительности раковых опухолей к инсулин и IGF1, И в ограничение калорий.[3][4]
Открытие
Открытие PI3K Льюис Кэнтли и его коллеги начали с идентификации ранее неизвестной фосфоинозитидкиназы, связанной с полиома средний белок T.[5] Они наблюдали уникальную субстратную специфичность и хроматографические свойства продуктов липидкиназы, что привело к открытию, что эта фосфоинозитидкиназа обладает беспрецедентной способностью фосфорилировать фосфоинозитиды в 3'-положении инозитолового кольца.[6] Впоследствии Кэнтли и его коллеги продемонстрировали, что in vivo фермент предпочитает PtdIns (4,5) P2 в качестве субстрата, производя новый фосфоинозитид. PtdIns (3,4,5) P3[7] ранее идентифицированные в нейтрофилах[8]
Классы
Семейство PI3K делится на четыре разных класса: I класс, II класс, III класс, и Класс IV. Классификации основаны на первичной структуре, нормах и in vitro специфичность липидного субстрата.[9]
I класс
PI3K класса I катализируют превращение фосфатидилинозитол (4,5) -бисфосфат (PI (4,5) P2) в фосфатидилинозит (3,4,5) -трисфосфат (PI (3,4,5) P3) in vivo. В пробирке они также показали преобразование фосфатидилинозитол (PI) в фосфатидилинозитол 3-фосфат (PI3P) и фосфатидилинозитол 4-фосфат (PI4P) в фосфатидилинозитол (3,4) -бисфосфат (PI (3,4) P2), эти реакции крайне нежелательны in vivo.[10][11][12][13] PI3K активируется G-белковые рецепторы и рецепторы тирозинкиназы.[9]
PI3K класса I гетеродимерный молекулы, состоящие из регуляторных и каталитических подразделение; далее они делятся на подмножества IA и IB по сходству последовательностей. PI3K класса IA состоят из гетеродимера между каталитической субъединицей p110 и регуляторной субъединицей p85.[14] Существует пять вариантов регуляторной субъединицы p85, обозначенных p85α, p55α, p50α, p85β, и p55γ. Есть также три варианта каталитической субъединицы p110, обозначенные как каталитическая субъединица p110α, β или δ. Первые три регуляторные субъединицы представляют собой сплайсинговые варианты одного и того же гена (Pik3r1), а два других экспрессируются другими генами (Pik3r2 и Pik3r3, p85β и p55γ соответственно). Наиболее экспрессируемая регуляторная субъединица - p85α; все три каталитические субъединицы экспрессируются отдельными генами (Pik3ca, Pik3cb, и Pik3cd за p110α, p110β, и p110δ, соответственно). Первые две изоформы p110 (α и β) экспрессируются во всех клетках, но p110δ экспрессируется в основном в лейкоциты, и было высказано предположение, что он развивался параллельно с адаптивной иммунной системой. Регуляторный p101 и каталитический p110γ подразделения включают класс IB PI3Ks и кодируются одним геном каждый (Pik3cg за p110γ и Pik3r5 для p101).
Субъединицы p85 содержат SH2 и SH3 домены (Онлайн-менделевское наследование в человеке (OMIM): 171833 ). Домены SH2 преимущественно связываются с фосфорилированными остатками тирозина в контексте аминокислотной последовательности Y-X-X-M.[15][16]
Классы II и III

II класс и III PI3K отличаются от класса I своей структурой и функцией. Отличительной особенностью PI3K класса II является C-концевой домен C2. В этом домене отсутствуют критические Жерех остатки для координации связывания Ca2+, что предполагает, что PI3K класса II связывают липиды в Ca2+-независимо.
Класс II включает три каталитические изоформы (C2α, C2β и C2γ), но, в отличие от классов I и III, не содержит регуляторных белков. Класс II катализирует производство PI (3) P из PI и PI (3,4) P2 из ПИ (4) П; однако мало что известно об их роли в иммунных клетках. ПИ (3,4) П2 однако, как было показано, играет роль в фазе инвагинации клатрин-опосредованного эндоцитоза.[17] C2α и C2β экспрессируются через тело, но экспрессия C2γ ограничена гепатоциты.
PI3K класса III производят только PI (3) P из PI [9] но по структуре они больше похожи на класс I, поскольку существуют как гетеродимеры каталитического (Vps34 ) и регуляторную (Vps15 / p150) субъединицы. Класс III, по-видимому, в первую очередь участвует в перемещении белков и везикул. Однако есть доказательства того, что они могут способствовать эффективности нескольких процессов, важных для иммунных клеток, в том числе: фагоцитоз.
IV класс
Группу более отдаленно связанных ферментов иногда называют PI3K класса IV. Он состоит из атаксия, телеангиэктазия, мутировавшая (Банкомат), атаксия, телеангиэктазия и Rad3-связанные (ATR), ДНК-зависимая протеинкиназа (ДНК-ПК) и мишень рапамицина у млекопитающих (mTOR). Это протеинкиназы серин / треонин.
Гены человека
| группа | ген | белок | псевдонимы | Номер ЕС |
|---|---|---|---|---|
| каталитический класс 1 | PIK3CA | PI3K, каталитический, альфа-полипептид | p110-α | 2.7.1.153 |
| PIK3CB | PI3K, каталитический, бета-полипептид | p110-β | ||
| PIK3CG | PI3K, каталитический, гамма-полипептид | p110-γ | ||
| PIK3CD | PI3K, каталитический, дельта-полипептид | p110-δ | ||
| регулирующий класс 1 | ПИК3Р1 | PI3K, регуляторная субъединица 1 (альфа) | p85-α | Нет данных |
| ПИК3Р2 | PI3K, регуляторная субъединица 2 (бета) | p85-β | ||
| ПИК3Р3 | PI3K, регуляторная субъединица 3 (гамма) | p55-γ | ||
| ПИК3Р4 | PI3K, регуляторная субъединица 4 | p150 | ||
| ПИК3Р5 | PI3K, регуляторная субъединица 5 | p101 | ||
| ПИК3Р6 | PI3K, регуляторная субъединица 6 | стр. 87 | ||
| 2 класс | PIK3C2A | PI3K, класс 2, альфа-полипептид | PI3K-C2α | 2.7.1.154 |
| PIK3C2B | PI3K, класс 2, бета-полипептид | PI3K-C2β | ||
| PIK3C2G | PI3K, класс 2, гамма-полипептид | PI3K-C2γ | ||
| 3 класс | PIK3C3 | PI3K, класс 3 | Vps34 | 2.7.1.137 |
Механизм
Различные 3-фосфорилированные фосфоинозитиды которые производятся PI3K (PtdIns3P, PtdIns (3,4) P2, PtdIns (3,5) P2, и PtdIns (3,4,5) P3 ) функционируют в механизме, с помощью которого отобранная группа сигнальных белков, содержащих PX домены, домены гомологии плекстрина (Домены PH), FYVE домены или другие фосфоинозитид-связывающие домены привлекаются к различным клеточным мембранам.
Функция
PI3K связаны с чрезвычайно разнообразной группой клеточных функций, включая рост, пролиферацию, дифференцировку, подвижность, выживание и внутриклеточный трафик. Многие из этих функций связаны со способностью PI3K класса I активировать протеинкиназа B (PKB, он же Akt) как в Путь PI3K / AKT / mTOR. В p110δ и p110γ изоформы регулируют различные аспекты иммунных ответов. PI3K также являются ключевым компонентом сигнальный путь инсулина. Следовательно, существует большой интерес к роли передачи сигналов PI3K в сахарный диабет.
Механизм
В домен гомологии плекстрина из AKT связывается напрямую с PtdIns (3,4,5) P3 и PtdIns (3,4) P2, которые производятся активированными PI3K.[18] Поскольку PtdIns (3,4,5) P3 и PtdIns (3,4) P2 ограничены плазматической мембраной, это приводит к транслокации AKT на плазматическую мембрану. Точно так же фосфоинозитид-зависимая киназа-1 (PDK1 или, что редко называют PDPK1) также содержит домен гомологии плекстрина, который непосредственно связывается с PtdIns (3,4,5) P3 и PtdIns (3,4) P2, заставляя его также перемещаться на плазматическую мембрану при активации PI3K. . Взаимодействие активированных PDK1 и AKT позволяет AKT фосфорилироваться PDK1 по треонину 308, что приводит к частичной активации AKT. Полная активация AKT происходит при фосфорилировании серина 473 комплексом TORC2 mTOR протеинкиназа.
В Путь PI3K / AKT Было показано, что он необходим для чрезвычайно разнообразной клеточной активности, в первую очередь для клеточной пролиферации и выживания. Например, было показано, что он участвует в защите астроцитов от апоптоза, индуцированного церамидами.[19]
Было идентифицировано множество других белков, которые регулируются PtdIns (3,4,5) P3, включая Тирозинкиназа Брутона (БТК), общий рецептор фосфоинозитидов-1 (GRP1) и О-связанная N-ацетилглюкозамин (O-GlcNAc) трансфераза.
PtdIns (3,4,5) P3 также активирует факторы обмена гуанин-нуклеотидов (GEF), которые активируют GTPase Rac1,[20] ведущий к актин полимеризация и перестройка цитоскелета.[21]
Рак
В класс IA PI3K p110α мутирует при многих видах рака. Многие из этих мутаций повышают активность киназы. Это единственная наиболее мутированная киназа в глиобластоме, наиболее злокачественной первичной опухоли головного мозга.[22] Птицы (3,4,5)п3 фосфатаза PTEN который противодействует передаче сигналов PI3K, отсутствует во многих опухолях. Кроме того, рецептор эпидермального фактора роста EGFR который функционирует выше PI3K, мутационно активируется или сверхэкспрессируется при раке.[22][23] Следовательно, активность PI3K вносит значительный вклад в клеточная трансформация и развитие рак.
Обучение и память
PI3K также участвуют в долгосрочное потенцирование (ДП). Вопрос о том, необходимы ли они для экспрессии или индукции LTP, все еще обсуждается. В нейронах CA1 гиппокампа мыши определенные PI3K образуют комплекс с Рецепторы AMPA и разделены на постсинаптическую плотность глутаматергических синапсов.[24] PI3K фосфорилируются на Рецептор NMDA -зависимая активность CaMKII,[25] и затем он способствует встраиванию субъединиц AMPA-R GluR1 в плазматическую мембрану. Это говорит о том, что PI3K необходимы для экспрессии LTP. Кроме того, ингибиторы PI3K отменяют экспрессию LTP в CA1 гиппокампа крысы, но не влияют на ее индукцию.[26] Примечательно, что зависимость экспрессии LTP на поздней фазе от PI3Ks, по-видимому, снижается со временем.[27]
Однако другое исследование показало, что ингибиторы PI3K подавляют индукцию, но не экспрессию LTP в CA1 гиппокампа мыши.[28] В Путь PI3K также привлекает многие другие белки ниже по течению, в том числе mTOR,[29] GSK3β,[30] и PSD-95.[29] В Путь PI3K-mTOR приводит к фосфорилированию p70S6K, киназа, которая способствует трансляционной деятельности,[31][32] дальнейшее предположение, что PI3Ks необходимы вместо этого для фазы синтеза белка индукции LTP.
PI3K взаимодействуют с субстрат рецептора инсулина (IRS), чтобы регулировать поглощение глюкозы посредством серии событий фосфорилирования.
PI 3-киназы как протеинкиназы
Многие PI3K обладают активностью серин / треонинкиназы. in vitro; однако неясно, играет ли это какую-то роль in vivo.[нужна цитата ]
Торможение
Все PI3K ингибируются препаратами. вортманнин и LY294002, хотя некоторые члены семейства PI3K класса II демонстрируют пониженную чувствительность. Вортманнин показывает лучшую эффективность, чем LY294002 по позициям мутации горячих точек (GLU542, GLU545 и HIS1047)[33][34]
Ингибиторы PI3K как терапевтические средства
В качестве вортманнин и LY294002 широкий диапазон ингибиторы PI3Ks и ряд неродственных белков в более высоких концентрациях, они слишком токсичны для использования в качестве терапевтических средств.[нужна цитата ] Таким образом, ряд фармацевтических компаний разработали ингибиторы, специфичные для изоформы PI3K. По состоянию на январь 2019 года три ингибитора PI3K одобрены FDA для рутинного клинического применения у людей: ингибитор PIK3CD Idelalisib (Июль 2014 г., NDA 206545 ), двойной ингибитор PIK3CA и PIK3CD копанлисиб (Сентябрь 2017 г., NDA 209936 ), и двойной ингибитор PIK3CD и PIK3CG Дувелисиб (Сентябрь 2018 г., NDA 211155 ). Совместное ингибирование этого пути с другими путями, такими как MAPK или PIM, было выделено как многообещающая противораковая терапевтическая стратегия, которая может дать преимущество перед монотерапевтическим подходом за счет обхода компенсаторной передачи сигналов, замедления развития резистентности и потенциально позволяющего уменьшить дозирование.[35][36][37][38][39][40]
Смотрите также
Рекомендации
- ^ PDB: 2chz; Knight ZA, Gonzalez B, Feldman ME, Zunder ER, Goldenberg DD, Williams O, et al. (Май 2006 г.). «Фармакологическая карта семейства PI3-K определяет роль p110alpha в передаче сигналов инсулина». Клетка. 125 (4): 733–47. Дои:10.1016 / j.cell.2006.03.035. ЧВК 2946820. PMID 16647110.
- ^ «мио-инозитол». Архивировано из оригинал на 2011-08-06. Получено 2006-01-28.
- ^ Гизе Н (2009). «Перегрузка клеточного пути предотвращает реакцию рака на ограничение питания». PhysOrg.com. Получено 2009-04-22.
- ^ Калаани, штат Нью-Йорк, Сабатини Д.М. (апрель 2009 г.). «Опухоли с активацией PI3K устойчивы к диетическим ограничениям». Природа. 458 (7239): 725–31. Bibcode:2009Натура.458..725K. Дои:10.1038 / природа07782. ЧВК 2692085. PMID 19279572.
- ^ Whitman M, Kaplan DR, Schaffhausen B, Cantley L, Roberts TM (1985). «Ассоциация активности фосфатидилинозитол киназы с полиомой мидд-Т, компетентной для трансформации». Природа. 315 (6016): 239–42. Bibcode:1985 Натур. 315..239Вт. Дои:10.1038 / 315239a0. PMID 2987699.
- ^ Уитмен М., Даунс С.П., Киллер М., Келлер Т., Кэнтли Л. (апрель 1988 г.). «Фосфатидилинозитолкиназа типа I производит новый инозитолфолипид, фосфатидилинозитол-3-фосфат». Природа. 332 (6165): 644–6. Bibcode:1988Натура.332..644Вт. Дои:10.1038 / 332644a0. PMID 2833705.
- ^ Оже К.Р., Серуниан Л.А., Солтофф С.П., Либби П., Кэнтли Л.К. (апрель 1989 г.). «PDGF-зависимое фосфорилирование тирозина стимулирует продукцию новых полифосфоинозитидов в интактных клетках». Клетка. 57 (1): 167–75. Дои:10.1016/0092-8674(89)90182-7. PMID 2467744.
- ^ Трейнор-Каплан А.Е., Харрис А.Л., Томпсон Б.Л., Тейлор П., Склар Л.А. (июль 1988 г.). «Инозитолтетракисфосфат-содержащий фосфолипид в активированных нейтрофилах». Природа. 334 (6180): 353–6. Bibcode:1988Натура.334..353Т. Дои:10.1038 / 334353a0. PMID 3393226.
- ^ а б c Ливерс SJ, Vanhaesebroeck B, Waterfield MD (апрель 1999 г.). «Передача сигналов через фосфоинозитид-3-киназы: липиды в центре внимания». Текущее мнение в области клеточной биологии. 11 (2): 219–25. Дои:10.1016 / S0955-0674 (99) 80029-5. PMID 10209156.
- ^ Фруман Д.А., Чиу Х., Хопкинс Б.Д., Багродиа С., Кэнтли Л.С., Абрахам Р.Т. (август 2017 г.). «Путь PI3K при заболеваниях человека». Клетка. 170 (4): 605–635. Дои:10.1016 / j.cell.2017.07.029. ЧВК 5726441. PMID 28802037.
- ^ Жан С., Кигер А.А. (март 2014 г.). «Краткий обзор классов фосфоинозитид-3-киназ». Журнал клеточной науки. 127 (Pt 5): 923–8. Дои:10.1242 / jcs.093773. ЧВК 3937771. PMID 24587488.
- ^ Ванхаэсбрук Б., Стивенс Л., Хокинс П. (февраль 2012 г.). «Сигнализация PI3K: путь к открытию и пониманию». Обзоры природы. Молекулярная клеточная биология. 13 (3): 195–203. Дои:10.1038 / nrm3290. PMID 22358332.
- ^ Оккенхауг К. (январь 2013 г.). «Передача сигналов семейством фосфоинозитид-3-киназ в иммунных клетках». Ежегодный обзор иммунологии. 31 (2): 675–704. Дои:10.1146 / аннурев-иммунол-032712-095946. ЧВК 4516760. PMID 23330955.
- ^ Карпентер К.Л., Дакворт Британская Колумбия, Оже К.Р., Коэн Б., Шаффхаузен Б.С., Кэнтли Л.С. (ноябрь 1990 г.). «Очистка и характеристика фосфоинозитид-3-киназы из печени крысы». Журнал биологической химии. 265 (32): 19704–11. PMID 2174051.
- ^ Songyang Z, Shoelson SE, Chaudhuri M, Gish G, Pawson T., Haser WG и др. (Март 1993 г.). «Домены SH2 распознают специфические фосфопептидные последовательности». Клетка. 72 (5): 767–78. Дои:10.1016 / 0092-8674 (93) 90404-Е. PMID 7680959.
- ^ Йоаким М., Хоу В., Сонъян З., Лю Ю., Кантли Л., Шаффхаузен Б. (сентябрь 1994 г.). «Генетический анализ домена SH2 фосфатидилинозитол-3-киназы выявляет детерминанты специфичности». Молекулярная и клеточная биология. 14 (9): 5929–38. Дои:10.1128 / MCB.14.9.5929. ЧВК 359119. PMID 8065326.
- ^ Posor Y, Eichhorn-Grünig M, Haucke V (июнь 2015 г.). «Фосфоинозитиды в эндоцитозе». Biochimica et Biophysica Acta (BBA) - Молекулярная и клеточная биология липидов. 1851 (6): 794–804. Дои:10.1016 / j.bbalip.2014.09.014. PMID 25264171.
- ^ Franke TF, Kaplan DR, Cantley LC, Toker A (январь 1997 г.). «Прямая регуляция продукта протоонкогена Akt фосфатидилинозитол-3,4-бисфосфатом». Наука. 275 (5300): 665–8. Дои:10.1126 / science.275.5300.665. PMID 9005852.
- ^ Гомес Дель Пульгар Т., Де Себальос М.Л., Гусман М., Веласко Г. (сентябрь 2002 г.). «Каннабиноиды защищают астроциты от апоптоза, вызванного церамидами, через путь фосфатидилинозитол-3-киназы / протеинкиназы B». Журнал биологической химии. 277 (39): 36527–33. Дои:10.1074 / jbc.M205797200. PMID 12133838.
- ^ Welch HC, Coadwell WJ, Стивенс LR, Hawkins PT (июль 2003 г.). «Фосфоинозитид-3-киназа-зависимая активация Rac». Письма FEBS. 546 (1): 93–7. Дои:10.1016 / с0014-5793 (03) 00454-х. PMID 12829242.
- ^ Jaffe AB, зал A (2005). «Rho GTPases: биохимия и биология». Ежегодный обзор клеточной биологии и биологии развития. 21: 247–69. Дои:10.1146 / annurev.cellbio.21.020604.150721. PMID 16212495.
- ^ а б Бликер Ф. Е., Ламба С., Занон С., Моленаар Р. Дж., Хулсебос Т. Дж., Трост Д. и др. (Сентябрь 2014 г.). «Мутационное профилирование киназ при глиобластоме». BMC Рак. 14: 718. Дои:10.1186/1471-2407-14-718. ЧВК 4192443. PMID 25256166.
- ^ Bleeker FE, Molenaar RJ, Leenstra S (май 2012 г.). «Последние достижения в молекулярном понимании глиобластомы». Журнал нейроонкологии. 108 (1): 11–27. Дои:10.1007 / s11060-011-0793-0. ЧВК 3337398. PMID 22270850.
- ^ Man HY, Wang Q, Lu WY, Ju W, Ahmadian G, Liu L и др. (Май 2003 г.). «Активация PI3-киназы необходима для вставки рецептора AMPA во время LTP mEPSCs в культивируемых нейронах гиппокампа». Нейрон. 38 (4): 611–24. Дои:10.1016 / S0896-6273 (03) 00228-9. PMID 12765612.
- ^ Джойал Дж. Л., Буркс Д. Д., Понс С., Материя В. Ф., Влахос С. Дж., Уайт М. Ф., Сакс ДБ (ноябрь 1997 г.). «Кальмодулин активирует фосфатидилинозитол-3-киназу». Журнал биологической химии. 272 (45): 28183–6. Дои:10.1074 / jbc.272.45.28183. PMID 9353264.
- ^ Санна П.П., Каммаллери М., Бертон Ф., Симпсон К., Лютьенс Р., Блум Ф. Э., Франческони В. (май 2002 г.). «Фосфатидилинозитол-3-киназа необходима для экспрессии, но не для индукции или поддержания долгосрочной потенциации в области CA1 гиппокампа». Журнал неврологии. 22 (9): 3359–65. Дои:10.1523 / JNEUROSCI.22-09-03359.2002. ЧВК 6758361. PMID 11978812.
- ^ Карпова А., Санна П.П., Бехниш Т. (февраль 2006 г.). «Участие нескольких зависимых от фосфатидилинозитол 3-киназы путей в сохранении поздней фазы долгосрочной потенциации экспрессии». Неврология. 137 (3): 833–41. Дои:10.1016 / j.neuroscience.2005.10.012. PMID 16326012.
- ^ Опазо П., Ватабе А.М., Грант С.Г., О'Делл Т.Дж. (май 2003 г.). «Фосфатидилинозитол-3-киназа регулирует индукцию долгосрочной потенциации посредством внеклеточных сигналов, связанных с независимыми от киназы механизмами». Журнал неврологии. 23 (9): 3679–88. Дои:10.1523 / JNEUROSCI.23-09-03679.2003. ЧВК 6742185. PMID 12736339.
- ^ а б Ян ПК, Ян Ч., Хуанг СС, Сюй К.С. (февраль 2008 г.). «Активация фосфатидилинозитол-3-киназы необходима для индуцированной стресс-протоколом модификации синаптической пластичности гиппокампа». Журнал биологической химии. 283 (5): 2631–43. Дои:10.1074 / jbc.M706954200. PMID 18057005.
- ^ Пино С., Тагибиглу С., Брэдли С., Вонг Т.П., Лю Л., Лу Дж. И др. (Март 2007 г.). «LTP ингибирует LTD в гиппокампе посредством регуляции GSK3beta». Нейрон. 53 (5): 703–17. Дои:10.1016 / j.neuron.2007.01.029. PMID 17329210.
- ^ Токер А., Cantley LC (июнь 1997 г.). «Передача сигналов через липидные продукты фосфоинозитид-3-ОН киназы». Природа. 387 (6634): 673–6. Bibcode:1997Натура.387..673Т. Дои:10.1038/42648. PMID 9192891.
- ^ Cammalleri M, Lütjens R, Berton F, King AR, Simpson C, Francesconi W, Sanna PP (ноябрь 2003 г.). «Ограниченная по времени роль дендритной активации пути mTOR-p70S6K в индукции поздней фазы долгосрочной потенциации в CA1». Труды Национальной академии наук Соединенных Штатов Америки. 100 (24): 14368–73. Bibcode:2003PNAS..10014368C. Дои:10.1073 / pnas.2336098100. ЧВК 283598. PMID 14623952.
- ^ Кумар Д.Т., Досс К.Г. (01.01.2016). Изучение ингибирующего эффекта вортманнина в мутации горячей точки на кодоне 1047 киназного домена PIK3CA: подход молекулярного докинга и молекулярной динамики. Достижения в химии белков и структурной биологии. 102. С. 267–97. Дои:10.1016 / bs.apcsb.2015.09.008. ISBN 9780128047958. PMID 26827608.
- ^ Судхакар Н., Прия Досс К.Г., Тирумал Кумар Д., Чакраборти С., Ананд К., Суреш М. (2016-01-02). «Расшифровка влияния соматических мутаций в экзоне 20 и экзоне 9 гена PIK3CA на опухоли груди среди индийских женщин с помощью метода молекулярной динамики». Журнал биомолекулярной структуры и динамики. 34 (1): 29–41. Дои:10.1080/07391102.2015.1007483. PMID 25679319.
- ^ Мэлоун Т., Шефер Л., Саймон Н., Хиви С., Каффе С., Финн С. и др. (Март 2020 г.). «Современные перспективы нацеливания на киназы PIM для преодоления механизмов лекарственной устойчивости и уклонения от иммунитета при раке». Фармакология и терапия. 207: 107454. Дои:10.1016 / j.pharmthera.2019.107454. PMID 31836451.
- ^ Лущак С., Кумар С., Сатьядеван В.К., Симпсон Б.С., Гейтли К.А., Уитакер ХК, Хиви С. (2020). «Ингибирование киназы PIM: совместные терапевтические подходы при раке простаты». Передача сигналов и таргетная терапия. 5: 7. Дои:10.1038 / с41392-020-0109-у. ЧВК 6992635. PMID 32025342.
- ^ Хиви С., Доулинг П., Мур Г., Барр М. П., Келли Н., Махер С. Г. и др. (Январь 2018). «Разработка и характеристика панели фосфатидилинозитид-3-киназы - млекопитающих-мишеней устойчивых к ингибитору рапамицина линий клеток рака легких». Научные отчеты. 8 (1): 1652. Дои:10.1038 / s41598-018-19688-1. ЧВК 5786033. PMID 29374181.
- ^ Хиви С., Кафф С., Финн С., Янг В., Райан Р., Николсон С. и др. (Ноябрь 2016 г.). «В поисках синергизма: исследование стратегии совместного ингибирования PI3K / mTOR / MEK при НМРЛ». Oncotarget. 7 (48): 79526–79543. Дои:10.18632 / oncotarget.12755. ЧВК 5346733. PMID 27765909.
- ^ Хиви С., Годвин П., Бэрд А.М., Барр М.П., Умедзава К., Каффе С. и др. (Октябрь 2014 г.). «Стратегическое нацеливание на ось PI3K-NFκB в цисплатин-резистентном НМРЛ». Биология и терапия рака. 15 (10): 1367–77. Дои:10.4161 / cbt.29841. ЧВК 4130730. PMID 25025901.
- ^ Хиви С., О'Бирн К.Дж., Гейтли К. (апрель 2014 г.). «Стратегии совместного нацеливания пути PI3K / AKT / mTOR в NSCLC». Отзывы о лечении рака. 40 (3): 445–56. Дои:10.1016 / j.ctrv.2013.08.006. PMID 24055012.
дальнейшее чтение
- Ванхаэсбрук Б., Ливерс С.Дж., Ахмади К., Тиммс Дж., Катсо Р., Дрисколл П.С. и др. (2001). «Синтез и функция 3-фосфорилированных липидов инозита». Ежегодный обзор биохимии. 70: 535–602. Дои:10.1146 / annurev.biochem.70.1.535. PMID 11395417. [1]
- Шильд С., Вирт М., Райхерт М., Шмид Р.М., Заур Д., Шнайдер Г. (декабрь 2009 г.). «Передача сигналов PI3K поддерживает экспрессию c-myc для регулирования транскрипции E2F1 в клетках рака поджелудочной железы». Молекулярный канцерогенез. 48 (12): 1149–58. Дои:10.1002 / mc.20569. PMID 19603422.
- Уильямс Р., Берндт А., Миллер С., Хон В. К., Чжан Х (август 2009 г.). «Форма и гибкость фосфоинозитид-3-киназ». Сделки Биохимического Общества. 37 (Пт 4): 615–26. Дои:10.1042 / BST0370615. PMID 19614567.
- Куарежма А.Дж., Сиверт Р., Никерсон Дж. А. (апрель 2013 г.). «Регулирование экспорта мРНК с помощью пути передачи сигнала киназы PI3 / AKT». Молекулярная биология клетки. 24 (8): 1208–21. Дои:10.1091 / mbc.E12-06-0450. ЧВК 3623641. PMID 23427269.
внешняя ссылка
- Ресурс Eukaryotic Linear Motif класс мотива MOD_PIKK_1
- Протеопедия Фосфоинозитид-3-киназы изучить структуру в интерактивном 3D
- PI-3 + киназа в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Сигнальный путь PI3K / Akt
