Иделалисиб - Idelalisib
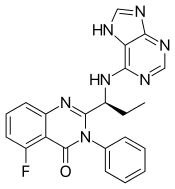 Состав Иделалисиба | |
| Клинические данные | |
|---|---|
| Произношение | /аɪˈdɛлəлɪsɪб/ глаз-DEL-ə-li-sib |
| Торговые наименования | Зиделиг |
| Другие имена | GS-1101, CAL-101 |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a614040 |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Устно (таблетки ) |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Связывание с белками | >84%[2] |
| Метаболизм | Альдегидоксидаза (~70%), CYP3A4 (~30%);[3] UGT1A4 (незначительный) |
| Метаболиты | GS-563117 (неактивный in vitro) |
| Начало действия | ТМаксимум = 1,5 часа |
| Устранение период полураспада | 8,2 часов |
| Экскреция | Кал (78%), моча (14%) |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.235.089 |
| Химические и физические данные | |
| Формула | C22ЧАС18FN7О |
| Молярная масса | 415.432 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
Иделалисиб, продается под торговой маркой Зиделиг, это лекарство, используемое для лечения некоторых рак крови.[2][1]
Вещество действует как ингибитор фосфоинозитид-3-киназы; более конкретно, он блокирует P110δ, дельта-изоформа фермента фосфоинозитид-3-киназа.[4][5] Он был разработан Gilead Sciences. Годовой объем продаж Иделалисиба составил 168 миллионов долларов (доллар США ) в течение 2016 года по сравнению со 132 миллионами долларов США в 2015 году.[6]
Медицинское использование
Иделалисиб - препарат второго ряда для пациентов, у которых хронический лимфолейкоз (CLL) рецидив. Используется в сочетании с ритуксимаб,[7] Иделалисиб следует применять пациентам, для которых применение ритуксимаба в отдельности считается подходящей терапией из-за других существующих заболеваний.[7] Это оказывается эффективным и приводит к улучшению лимфаденопатия и спленомегалия. Однако при приеме идеалалисиба количество лимфоцитов снижается до нормального уровня. Не рекомендуется в качестве лечения первой линии.[2]
Он также одобрен для лечения фолликулярная B-клеточная неходжкинская лимфома (FL) и рецидив малая лимфоцитарная лимфома (SLL), оба у пациентов, которые ранее получали как минимум два системных лечения.[2]
Побочные эффекты
Клинические симптомы включают: понос, высокая температура, усталость, тошнота, кашель, пневмония, боль в животе, озноб и сыпь. Лабораторные отклонения могут включать: нейтропения, гипертриглицеридемия, гипергликемия и повышенный уровень ферментов печени. Безопасность и эффективность иделалисиба для лечения рецидивов ФЛ и рецидивов SLL были установлены в клинических испытаниях с участием 123 участников с медленно растущими (вялотекущими) неходжкинскими лимфомами. Все участники получали иделалисиб, и их оценивали на предмет полного или частичного исчезновения рака после лечения (уровень объективного ответа, или ЧОО). Результаты показали, что у 54% участников с рецидивом FL и у 58% участников с SLL наблюдалась ЧОО.[8]
На этикетке иделалисиба в США есть предупреждение в рамке описание токсичности, которая может быть серьезной и смертельной, в том числе токсичность печени, суровый понос, воспаление толстой кишки, воспаление легочной ткани (пневмонит ) и перфорация кишечника, и производитель был обязан установить Стратегия оценки и снижения рисков (REMS), с помощью которого можно управлять риском токсичности.[9]
В марте 2016 года, когда были сделаны отчеты о трех продолжающихся клинических испытаниях серьезных побочных эффектов и смертей, в основном из-за инфекций, Европейское агентство по лекарственным средствам начало обзор препарата и связанных с ним рисков.[10] 21 марта 2016 г. Gilead Sciences (производитель иделалисиба) предупредил медицинских работников о снижении общей выживаемости и повышенном риске серьезных инфекций у пациентов с ХЛЛ и вялотекущей неходжкинской лимфомой (iNHL), получавших идеалализиб.[11] Компания также сообщила, что прекратила шесть клинических испытаний у пациентов с ХЛЛ, SLL и iNHL из-за увеличения частоты побочных эффектов, включая летальные исходы.[12] В 2016 году EMA рекомендовало людям, принимающим иделалисиб, давать лекарства от легочной инфекции. Pneumocystis jirovecii пневмония и это следует продолжать до 6 месяцев после прекращения приема иделалисиба. Кроме того, за людьми следует наблюдать на предмет признаков инфекции.[13]
Фармакология
Механизм действия
PI3Kδ киназа выражается в нормальных и злокачественных В-клетки. Подавляя его, иделалисиб вызывает апоптоз и предотвращает пролиферацию клеточных линий, полученных из злокачественных В-клеток, и клеток первичной опухоли. Он также подавляет несколько клеточных сигнальные пути, включая B-клеточный рецептор (BCR) сигнализация и CXCR4 и CXCR5 передачи сигналов, которые участвуют в транспортировке и наведении В-клеток на лимфатический узел и Костный мозг.[2]
Профиль привязки
Иделалисиб - это конкурентный ингибитор из АТФ сайт связывания PI3Kδ каталитический домен. Его in vitro эффективность и избирательность по отношению к другим Изоформы PI3K класса I следующее:[14]
| PI3K изоформа | IC50, нМ | IC50селективность на основе PI3Kδ |
|---|---|---|
| PI3Kα | 8,600 | 453 |
| PI3Kβ | 4,000 | 211 |
| PI3Kγ | 2,100 | 110 |
| PI3Kδ | 19 | 1 |
История
Нормативный
В июле 2014 года FDA и EMA одобрили иделалисиб для лечения различных типов лейкемии.[8][15] FDA также одобрило иделалисиб для лечения пациентов с рецидивом фолликулярная B-клеточная неходжкинская лимфома и рецидив малая лимфоцитарная лимфома. Idelalisib предназначен для использования у пациентов, которые ранее получали как минимум два системных лечения.
Рекомендации
- ^ а б «Зыделиг ЕПАР». Европейское агентство по лекарствам (EMA). Получено 21 октября 2020.
- ^ а б c d е «Зиделигиделалисиб таблетка, покрытая пленочной оболочкой». DailyMed. 22 октября 2018 г.. Получено 21 октября 2020.
- ^ «Обзор клинической фармакологии и биофармацевтики: Зиделиг (идеалалисиб)» (PDF). Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. п. 6. Получено 15 апреля 2016.
- ^ Spreitzer H (13 мая 2013 г.). «Neue Wirkstoffe - Ibrutinib und Idelalisib». Österreichische Apothekerzeitung (на немецком языке) (10/2013): 34.
- ^ Ву М., Акинлей А., Чжу Х (май 2013 г.). «Новые средства от хронического лимфолейкоза». Журнал гематологии и онкологии. 6: 36. Дои:10.1186/1756-8722-6-36. ЧВК 3659027. PMID 23680477.
- ^ «Годовые продажи иделалисиба указаны с использованием годового отчета глобальных фармацевтических компаний, составленного компанией PharmaCompass». Фармакомпас. Получено 21 января, 2019.
- ^ а б Furman RR, Sharman JP, Coutre SE, Cheson BD, Pagel JM, Hillmen P и др. (Март 2014 г.). «Иделалисиб и ритуксимаб при рецидиве хронического лимфолейкоза». Медицинский журнал Новой Англии. 370 (11): 997–1007. Дои:10.1056 / NEJMoa1315226. ЧВК 4161365. PMID 24450857.
- ^ а б «FDA одобряет Zydelig для трех типов рака крови» (Пресс-релиз). Управление по контролю за продуктами и лекарствами. 23 июля 2014 г.[мертвая ссылка ]
- ^ «Сообщения для прессы - FDA одобряет Zydelig для трех типов рака крови». www.fda.gov. Получено 2016-03-14.
- ^ "Европейское агентство по лекарственным средствам - Новости и события - EMA рассматривает лекарство от рака Zydelig". www.ema.europa.eu. Получено 2016-03-14.
- ^ «Важное предупреждение о лекарствах: снижение общей выживаемости и повышение риска серьезных инфекций у пациентов, получающих ЗИДЕЛИГ (идеалалисиб)» (PDF). Gilead Sciences, Inc. 21 марта 2016 г.. Получено 19 апреля 2016.
- ^ «Безопасность и доступность лекарств - FDA предупреждает медицинских работников о клинических испытаниях зиделига (иделалисиба) в сочетании с другими противораковыми лекарствами». Центр FDA по оценке и исследованию лекарственных средств. Получено 19 апреля 2016.
- ^ «ЧМП подтверждает рекомендации по применению Зиделига». Европейское агентство по лекарствам (EMA). 15 сентября 2016 г.
- ^ «Отчет об оценке комитета по лекарственным средствам для человека: Зиделиг (иделалисиб)» (PDF). Европейское агентство по лекарственным средствам. п. 17. Получено 19 апреля 2016.
- ^ «Европейское агентство по лекарственным средствам рекомендует одобрить два новых варианта лечения редких видов рака» (Пресс-релиз). Европейское агентство по лекарственным средствам. 25 июля 2014 г.
внешняя ссылка
- «Иделалисиб». Портал информации о наркотиках. Национальная медицинская библиотека США.
