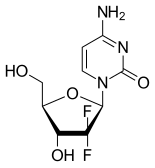
Гемцитабин - Gemcitabine
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | /dʒɛмˈsаɪтəбяп/ |
| Торговые наименования | Гемзар, другие[1] |
| Другие имена | 2 ', 2'-дифтор 2'-дезоксицитидин, dFdC |
| AHFS /Drugs.com | Монография |
| Беременность категория |
|
| Маршруты администрация | Внутривенно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Связывание с белками | <10% |
| Устранение период полураспада | Короткие настои: 32–94 минуты. Длительные настои: 245–638 минут |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.124.343 |
| Химические и физические данные | |
| Формула | C9ЧАС11F2N3О4 |
| Молярная масса | 263.201 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| (проверить) | |
Гемцитабин, продается под торговой маркой Гемзар, среди прочего,[1] это химиотерапевтические препараты используется для лечения ряда типов рак.[2] Эти виды рака включают рак молочной железы, рак яичников, немелкоклеточный рак легкого, панкреатический рак, и Рак мочевого пузыря.[2][3] Это дается медленное введение в вену.[2]
Общие побочные эффекты включают: подавление костного мозга, проблемы с печенью и почками, тошнота, лихорадка, сыпь, одышка, язвы во рту, диарея, невропатия и выпадение волос.[2] Использовать во время беременность скорее всего, нанесет вред ребенку.[2] Гемцитабин находится в аналог нуклеозида семья лекарства.[2] Он работает, блокируя создание новых ДНК, что приводит к гибели клеток.[2]
Гемцитабин был запатентован в 1983 году и одобрен для медицинского применения в 1995 году.[4] Универсальные версии были представлены в Европе в 2009 году и в США в 2010 году.[5][6] Это на Список основных лекарственных средств Всемирной организации здравоохранения.[7]
Медицинское использование
Гемцитабин используется в различных карциномы. Он используется только как средство первой линии для панкреатический рак, и в сочетании с цисплатин для продвинутых или метастатических Рак мочевого пузыря и продвинутый или метастатический немелкоклеточный рак легкого. Он используется в качестве лечения второй линии в сочетании с карбоплатин для рак яичников и в сочетании с паклитаксел для рак молочной железы который является метастатическим или не может быть удален хирургическим путем.[8][9][10]
Это обычно используется не по назначению лечить холангиокарцинома[11] и другие желчные пути раки.[12]
Его вводят путем инъекции в вену на химиотерапия клиника.[2]
Противопоказания и лекарственные взаимодействия
Прием гемцитабина также может повлиять на фертильность у мужчин и женщин, половую жизнь и менструацию. Женщины, принимающие гемцитабин, не должны беременеть, а беременные и кормящие женщины не должны его принимать.[13]
По состоянию на 2014 г. лекарственные взаимодействия не изучались.[9][8]
Побочные эффекты
Гемцитабин - это химиотерапия препарат, который убивает любые делящиеся клетки.[8] Раковые клетки делятся быстро, и поэтому гемцитабин нацелен на более высокие скорости, но многие важные клетки также быстро делятся, включая клетки кожи, волосистой части головы, слизистой оболочки желудка и костного мозга, что приводит к побочным эффектам.[14]:265
На этикетке гемцитабина содержится предупреждение о том, что он может подавлять функцию костного мозга и вызывать потеря лейкоцитов, потеря тромбоцитов, и потеря красных кровяных телец и что его следует осторожно использовать людям с заболеваниями печени, почек или сердечно-сосудистой системы. Люди, принимающие его, не должны принимать живые вакцины. На этикетке с предупреждением также указано, что это может вызвать синдром задней обратимой энцефалопатии, что это может вызвать синдром утечки капилляров, что это может вызвать тяжелые заболевания легких, такие как отек легких, пневмония, и респираторный дистресс-синдром у взрослых, и что это может повредить сперму.[8][15]
Очень частые (они развиваются более чем у 10% людей) побочные эффекты включают затрудненное дыхание, низкое количество лейкоцитов и красных кровяных телец и тромбоцитов, рвоту и тошноту, повышенные трансаминазы, сыпь и зуд на коже, выпадение волос, кровь и белок в моче, гриппоподобные симптомы и отек.[8][13]
Общие побочные эффекты (встречающиеся у 1–10% людей) включают лихорадку, потерю аппетита, головную боль, проблемы со сном, усталость, кашель, насморк, диарею, язвы во рту и губах, потливость, боли в спине и мышечные боли.[8]
Тромботическая тромбоцитопеническая пурпура (ТТП) - редкий, но серьезный побочный эффект, связанный с гемцитабином, а также с другими определенными химиотерапевтическими препаратами. ТТП - это заболевание крови, которое может привести к микроангиопатическая гемолитическая анемия (MAHA), неврологические нарушения, лихорадка и почечные заболевания.[16]
Фармакология
Гемцитабин - это гидрофильный и должны транспортироваться в клетки через молекулярные транспортеры для нуклеозиды (наиболее распространенными переносчиками гемцитабина являются SLC29A1, SLC28A1 и SLC28A3).[17][18] После попадания в клетку гемцитабин сначала модифицируется путем присоединения фосфат к нему, и поэтому он становится монофосфатом гемцитабина (dFdCMP).[17][18] Это этап определения ставки что катализируется фермент дезоксицитидинкиназа (ДВК).[17][18] Еще два фосфата добавляются другими ферментами. После присоединения трех фосфатов гемцитабин, наконец, становится фармакологически активным как гемцитабинтрифосфат (dFdCTP).[17]
После трехкратного фосфорилированный, гемцитабин может маскироваться под дезоксицитидинтрифосфат и включается в новые цепи ДНК, синтезируемые как клетка. копирует.[2][17][18]
Когда гемцитабин включен в ДНК, он позволяет добавить к нему нативное или нормальное нуклеозидное основание. Это приводит к «замаскированному обрыву цепи», поскольку гемцитабин является «дефектным» основанием, но из-за соседнего нативного нуклеозида он ускользает от нормальной системы репарации клетки (базисно-эксцизионная пластика ). Таким образом, включение гемцитабина в ДНК клетки создает непоправимую ошибку, которая приводит к ингибированию дальнейшего синтеза ДНК и, таким образом, к гибели клетки.[2][17][18]
Форма гемцитабина с двумя присоединенными фосфатами (dFdCDP) также обладает активностью; подавляет фермент рибонуклеотидредуктаза (RNR), который необходим для создания новых нуклеотидов ДНК. Недостаток нуклеотидов заставляет клетку поглощать больше компонентов, необходимых для производства нуклеотидов извне клетки, что также увеличивает поглощение гемцитабина.[2][17][18][19]
Химия
Гемцитабин - синтетический пиримидин нуклеозид пролекарство —А аналог нуклеозида в которой водород атомы на 2 'углерода дезоксицитидин заменены на фтор атомы.[2][20][21]
Синтез, описанный и изображенный ниже, является оригинальным синтезом, выполненным в лабораториях Eli Lilly Company. Синтез начинается с энантиочистого D-глицеральдегида (R) -2 в качестве исходного материала, который можно получить из D-маннита за 2-7 шагов. Затем фтор вводится методом «строительного блока» с использованием этилбромдифторацетата. Затем реакция Реформатского в стандартных условиях даст смесь анти / син-диастереомеров 3: 1 с одним основным продуктом. Разделение диастереомеров проводят с помощью ВЭЖХ, что дает анти-3-гемцитабин с выходом 65%.[20][21] По крайней мере, два других метода полного синтеза также были разработаны различными группами.[21]

История
Гемцитабин был впервые синтезирован в Ларри Хертель лаборатория в Эли Лилли и компания в начале 1980-х гг. Он был задуман как противовирусный препарат, но доклинические испытания показали, что он убивает лейкозные клетки in vitro.[22]
В начале 1990-х годов гемцитабин изучался в клинических испытаниях. Испытания рака поджелудочной железы показали, что гемцитабин значительно увеличивает продолжительность жизни в течение одного года, и он был одобрен в Великобритании в 1995 году.[8] и одобрен FDA в 1996 году для лечения рака поджелудочной железы.[3] В 1998 году гемцитабин получил одобрение FDA для лечения немелкоклеточного рака легких, а в 2004 году он был одобрен для лечения метастатического рака груди.[3]
Европейские марки были согласованы EMA в 2008 году.[23]
К 2008 году мировые продажи гемцитабина Lilly составили около 1,7 миллиарда долларов; в то время срок действия ее патентов в США истекал в 2013 г., а европейских патентов - в 2009 г.[24] Первый дженерик, выпущенный в Европе в 2009 году,[5] в США возникли проблемы с патентами, что привело к признанию недействительным ключевого патента Lilly на метод изготовления препарата.[25][26] Компании-производители дженериков начали продавать препарат в США в 2010 году, когда истек срок действия патента на само химическое вещество.[26][6] Патентные тяжбы в Китае стали там заголовками и были урегулированы в 2010 году.[27]
Общество и культура
По состоянию на 2017 год гемцитабин продавался по всему миру под многими торговыми марками: Abine, Accogem, Acytabin, Antoril, axigem, Bendacitabin, Biogem, Boligem, Celzar, Citegin, Cytigem, Cytogem, Daplax, DBL, Demozar, Dercin, Emcamogar. , Fotinex, Gebina, Gemalata, Gembin, Gembine, Gembio, Gemcel, Gemcetin, Gemcibine, Gemcikal, Gemcipen, Gemcired, Gemcirena, Gemcit, Gemcitabin, Гемцитабина, Gemcitabine, Gemcitabin, Gemcitabina, Gemcitabine, Gemcitabin, Gemcitabin , Gemmis, Gemnil, Gempower, Gemsol, Gemstad, Gemstada, Gemtabine, Gemtavis, Gemtaz, Gemtero, Gemtra, Gemtro, Gemvic, Gemxit, Gemzar, Gentabim, Genuten, Genvir, Geroam, Gosanzredos, Gestmanztisi, Gosanztisi, Gestmanztisi, Gestmanztisi, Gestmanztisi , Haxanit, Jemta, Kalbezar, Medigem, Meditabine, Nabigem, Nallian, Oncogem, Oncoril, Pamigeno, Ribozar, Santabin, Sitagem, Symtabin, Yu Jie, Ze Fei и Zefei.[1]
Исследование
Поскольку он имеет клиническую ценность и полезен только при внутривенном введении, методы его изменения, чтобы его можно было вводить перорально, были предметом исследований.[28][29][30]
Исследования в фармакогеномика и фармакогенетика продолжается. По состоянию на 2014 год было неясно, могут ли генетические тесты быть полезными для определения дозировки и какие люди лучше всего реагируют на гемцитабин.[17] Однако похоже, что вариации в экспрессии белков (SLC29A1, SLC29A2, SLC28A1, и SLC28A3 ), используемый для транспорта гемцитабина в клетку, приводит к изменению его активности. Точно так же гены, экспрессирующие белки, которые приводят к его инактивации (дезоксицитидин дезаминаза, цитидин дезаминаза, и NT5C ) и которые выражают другие его внутриклеточные мишени (RRM1, RRM2, и RRM2B ) приводят к вариациям реакции на препарат.[17] Также продолжаются исследования, чтобы понять, как сами мутации рака поджелудочной железы определяют реакцию на гемцитабин.[31]
Он был изучен как средство от Саркома Капоши, распространенный рак у людей с СПИД что является редкостью в развитом мире, но не редкостью в развивающемся мире.[32]
Смотрите также
использованная литература
- ^ а б c "Международные бренды гемцитабина". Drugs.com. В архиве из оригинала 25 мая 2014 г.. Получено 6 мая 2017.
- ^ а б c d е ж г час я j k л «Гемцитабина гидрохлорид». Американское общество фармацевтов систем здравоохранения. В архиве из оригинала 2 февраля 2017 г.. Получено 8 декабря 2016.
- ^ а б c Национальный институт рака (2006-10-05). «Одобрение FDA для гемцитабина гидрохлорида». Национальный институт рака. В архиве из оригинала 5 апреля 2017 г.. Получено 22 апреля 2017.
- ^ Фишер Дж, Ганеллин ЧР (2006). Открытие лекарств на основе аналогов. Джон Вили и сыновья. п. 511. ISBN 9783527607495.
- ^ а б Майерс, Калиша (13 марта 2009 г.). «Гемцитабин от Actavis выпущен на рынки ЕС по истечении срока действия патента». FierceBiotech. В архиве из оригинала от 11 сентября 2017 года.
- ^ а б «Пресс-релиз: Hospira выпускает двухграммовый флакон гемцитабина гидрохлорида для инъекций». Хоспира через News-Medical.Net. 16 ноября 2010 г. В архиве из оригинала 2 октября 2015 г.
- ^ Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ а б c d е ж г "Британский лейбл". Сборник электронных лекарств Великобритании. 5 июня 2014. Архивировано с оригинал 10 июля 2017 г.. Получено 6 мая 2017.
- ^ а б «Лейбл США» (PDF). FDA. Июнь 2014 г. В архиве (PDF) из оригинала 16 февраля 2017 г.. Получено 6 мая 2017. Для обновлений этикеток см. Индексная страница FDA для NDA 020509 В архиве 2017-04-29 в Wayback Machine
- ^ Чжан XW, Ма YX, Сунь Y, Цао YB, Ли Q, Сюй Калифорния (июнь 2017 г.). «Гемцитабин в комбинации со вторым цитотоксическим агентом в лечении первой линии местнораспространенного или метастатического рака поджелудочной железы: систематический обзор и метаанализ». Таргетированная онкология. 12 (3): 309–321. Дои:10.1007 / s11523-017-0486-5. PMID 28353074. S2CID 3833614.
- ^ Пленц Р.Р., Малек Н.П. (декабрь 2016 г.). «Системная терапия холангиокарциномы». Висцеральная медицина. 32 (6): 427–430. Дои:10.1159/000453084. ЧВК 5290432. PMID 28229078.
- ^ Джайн А., Квонг Л.Н., Джавле М. (ноябрь 2016 г.). «Геномное профилирование рака желчных путей и его значение для клинической практики». Современные варианты лечения в онкологии. 17 (11): 58. Дои:10.1007 / s11864-016-0432-2. PMID 27658789. S2CID 25477593.
- ^ а б Поддержка Macmillan Cancer. «Гемцитабин». Поддержка Macmillan Cancer. В архиве из оригинала 25 марта 2017 г.. Получено 6 мая 2017.
- ^ Рэйчел Эйрли (2009). Химиотерапия рака. Вили-Блэквелл. ISBN 978-0-470-09254-5.
- ^ Сиддалл Э., Хатри М., Радхакришнан Дж. (Июль 2017 г.). «Синдром капиллярной утечки: этиология, патофизиология и лечение». Kidney International. 92 (1): 37–46. Дои:10.1016 / j.kint.2016.11.029. PMID 28318633.
- ^ Kasi PM (январь 2011 г.). «Тромботическая тромбоцитопеническая пурпура и гемцитабин». Отчеты о случаях в онкологии. 4 (1): 143–8. Дои:10.1159/000326801. ЧВК 3114619. PMID 21691573.
- ^ а б c d е ж г час я Alvarellos ML, Lamba J, Sangkuhl K, Thorn CF, Wang L, Klein DJ, Altman RB, Klein TE (ноябрь 2014 г.). «Резюме PharmGKB: путь гемцитабина». Фармакогенетика и геномика. 24 (11): 564–74. Дои:10.1097 / fpc.0000000000000086. ЧВК 4189987. PMID 25162786.
- ^ а б c d е ж Mini E, Nobili S, Caciagli B, Landini I, Mazzei T (май 2006 г.). «Клеточная фармакология гемцитабина». Анналы онкологии. 17 Дополнение 5: ст. 7-12. Дои:10.1093 / annonc / mdj941. PMID 16807468.
- ^ Cerqueira NM, Фернандес PA, Ramos MJ (2007). «Понимание инактивации рибонуклеотидредуктазы гемцитабином». Химия. 13 (30): 8507–15. Дои:10.1002 / chem.200700260. PMID 17636467.
- ^ а б Браун К., Веймут-Уилсон А., Линклау Б. (апрель 2015 г.). «Линейный синтез гемцитабина». Исследование углеводов. 406: 71–5. Дои:10.1016 / j.carres.2015.01.001. PMID 25681996.
- ^ а б c Браун К., Дикси М., Уэймут-Уилсон А., Линклау Б. (март 2014 г.). «Синтез гемцитабина». Исследование углеводов. 387: 59–73. Дои:10.1016 / j.carres.2014.01.024. PMID 24636495.
- ^ Снидер, Уолтер (2005). Открытие лекарств: история. Нью-Йорк: Вили. п. 259. ISBN 978-0-471-89979-2.
- ^ «Гемзар». Европейское агентство по лекарственным средствам. 24 сентября 2008 г. В архиве из оригинала от 11 сентября 2017 года.
- ^ Майерс, Калиша (18 августа 2009 г.). «Патент на лекарство от рака Гемзар Лилли аннулирован». FiercePharma. В архиве из оригинала от 11 сентября 2017 года.
- ^ Холман, Кристофер М. (лето 2011 г.). «Непредсказуемость патентного права и ее влияние на фармацевтические инновации» (PDF). Обзор закона Миссури. 76 (3): 645–693. Архивировано из оригинал (PDF) на 2017-09-11. Получено 2017-05-06.
- ^ а б Равичер, Дэниел Б. (28 июля 2010 г.). "О патентной борьбе за родовой Гемзар". В поисках альфы. В архиве из оригинала от 9 декабря 2012 г.
- ^ Ван М., Александр Д. (2015). «Анализ дел о нарушении фармацевтических патентов в Великом Китае». В Rader RR et al. (ред.). Право, политика и извлечение доходов от интеллектуальной собственности. Издательство Кембриджских ученых. п. 119. ISBN 9781443879262. В архиве из оригинала от 11.09.2017.
- ^ Dyawanapelly S, Kumar A, Chourasia MK (2017). «Уроки, извлеченные из гемцитабина: влияние терапевтических систем-носителей и конъюгатов препаратов гемцитабина на терапию рака». Критические обзоры терапевтических систем-носителей лекарственных средств. 34 (1): 63–96. Дои:10.1615 / CritRevTherDrugCarrierSyst.2017017912. PMID 28322141.
- ^ Бирхану Г., Джавар Х.А., Сейджафари Э., Занди-Карими А. (апрель 2017 г.). «Нанотехнология доставки гемцитабина для лечения рака поджелудочной железы». Биомедицина и фармакотерапия. 88: 635–643. Дои:10.1016 / j.biopha.2017.01.071. PMID 28142120.
- ^ Дубей Р.Д., Санежа А., Гупта П.К., Гупта П.Н. (октябрь 2016 г.). «Последние достижения в стратегиях доставки лекарств для улучшения терапевтической эффективности гемцитабина». Европейский журнал фармацевтических наук. 93: 147–62. Дои:10.1016 / j.ejps.2016.08.021. PMID 27531553.
- ^ Пишваян MJ, Броды JR (март 2017). «Терапевтическое значение молекулярного подтипирования рака поджелудочной железы». Онкология. 31 (3): 159–66, 168. PMID 28299752. В архиве из оригинала от 3 июля 2017 г.
- ^ Krown SE (сентябрь 2011 г.). «Стратегии лечения саркомы Капоши в Африке к югу от Сахары: проблемы и возможности». Текущее мнение в области онкологии. 23 (5): 463–8. Дои:10.1097 / cco.0b013e328349428d. ЧВК 3465839. PMID 21681092.
внешние ссылки
- «Гемцитабин». Портал информации о наркотиках. Национальная медицинская библиотека США.
