Доксорубицин - Doxorubicin - Wikipedia
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | /ˌdɒksəˈрuбɪsɪп/ |
| Торговые наименования | Адриамицин, Caelyx, Myocet, другие |
| AHFS /Drugs.com | Монография |
| MedlinePlus | a682221 |
| Данные лицензии |
|
| Беременность категория |
|
| Маршруты администрация | внутривенный, внутрипузырный |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетический данные | |
| Биодоступность | 5% (внутрь) |
| Связывание с белками | 75%[1] |
| Метаболизм | Печень |
| Устранение период полураспада | Трехфазный; 12 минут, 3,3 часа, 30 часов. Среднее: 1–3 часа[1][2] |
| Экскреция | Моча (5–12%), фекалии (40–50%)[1] |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.041.344 |
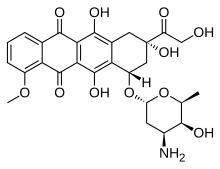
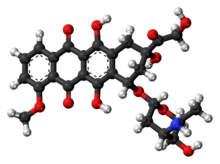
| Химические и физические данные | |
| Формула | C27ЧАС29NО11 |
| Молярная масса | 543.525 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
| | |
Доксорубицин, продается под торговой маркой Адриамицин среди прочего, это химиотерапевтические препараты используется для лечения рак.[3] Это включает в себя рак молочной железы, Рак мочевого пузыря, Саркома Капоши, лимфома, и острый лимфолейкоз.[3] Часто используется вместе с другими химиотерапевтическими агентами.[3] Доксорубицин предоставляется инъекция в вену.[3]
Общие побочные эффекты включают: потеря волос, подавление костного мозга, рвота, сыпь и воспаление рта.[3] Другие серьезные побочные эффекты могут включать: аллергические реакции Такие как анафилаксия, повреждение сердца, повреждение тканей в месте укола, отзыв радиации, и связанные с лечением лейкемия.[3] Люди часто в течение нескольких дней испытывают покраснение мочи.[3] Доксорубицин находится в антрациклин и противоопухолевый антибиотик семейство лекарств.[3] Частично это работает, нарушая функцию ДНК.[4]
Доксорубицин был одобрен для медицинского применения в США в 1974 году.[3] Это на Список основных лекарственных средств Всемирной организации здравоохранения.[5][6] Версии, которые пегилированный И в липосомы также доступны; однако дороже.[6] Доксорубицин изначально был получен из бактерии Streptomyces peucetius.[7]
Медицинское использование
Доксорубицин обычно используется для лечения некоторых лейкемии и Лимфома Ходжкина, а также рак мочевой пузырь, грудь, желудок, легкое, яичники, щитовидная железа, саркома мягких тканей, множественная миелома, и другие.[2][8] Обычно используемые доксорубицинсодержащие режимы являются AC (Адриамицин, циклофосфамид ), ТАС (таксотер, AC), ABVD (Адриамицин, блеомицин, винбластин, дакарбазин ), BEACOPP, НАРЕЗАТЬ (циклофосфамид, гидроксидаунорубицин, винкристин, преднизон ) и FAC (5-фторурацил, адриамицин, циклофосфамид).[2]
Доксил (см. Ниже) используется в основном для лечения рака яичников, когда заболевание прогрессировало или рецидивировало после химиотерапия на основе платины, или для лечения СПИД -связанные с Саркома Капоши.[9]
Липосомальная форма
Существует пегилированный (с покрытием из полиэтиленгликоля) липосома -инкапсулированная форма доксорубицина, продаваемая как Доксил. Он был разработан для лечения Саркома Капоши, СПИД -зависимый рак, который вызывает рост поражений под кожей, на слизистой оболочке рта, носа и горла или в других органах. В полиэтиленгликоль покрытие приводит к предпочтительной концентрации доксорубицина в коже. Однако это также приводит к побочному эффекту, называемому ладонная подошвенная эритродизестезия (СИЗ), более известный как синдром ладони-стопы.
После приема этой формы доксорубицина небольшое количество препарата может вытекать из капилляров в ладонях рук и подошвах ног. Результатом этой утечки является покраснение, болезненность и шелушение кожи, которые могут быть неудобными и даже болезненными. При клинических испытаниях при 50 мг / м2 При приеме препарата каждые 4 недели у половины людей развился синдром ладони-стопы. Скорость этого побочного эффекта ограничивает дозу данного препарата, которую можно вводить по сравнению с обычным доксорубицином в той же схеме лечения, тем самым ограничивая потенциальную замену. Замена была бы желательна, поскольку инкапсулированный в липосомы доксорубицин менее кардиотоксичен, чем неинкапсулированный доксорубицин. Эта инкапсулированная в липосомы форма также одобрена FDA для лечения рака яичников и множественной миеломы.[10][11]
Непегилированный липосомальный доксорубицин, называемый Myocet, одобрен в Европе и Канаде для лечения метастатического рака молочной железы в сочетании с циклофосфамид, но не был одобрен FDA для использования в США. В отличие от Doxil, липосомы Myocet не имеют покрытия из полиэтиленгликоля и, следовательно, не вызывают такого же синдрома кистей и стоп. Сведение к минимуму этого побочного эффекта может позволить произвести замену доксорубицином один к одному (1: 1) в той же схеме лечения, тем самым повышая безопасность без потери эффективности. Как и доксил, липосомальная инкапсуляция доксорубицина ограничивает кардиотоксичность. Теоретически, ограничивая кардиотоксичность доксорубицина за счет липосомальной инкапсуляции, его можно безопасно использовать в одновременной комбинации с другими кардиотоксическими химиотерапевтическими препаратами, такими как трастузумаб. Существует предупреждение FDA в черном ящике о том, что трастузумаб нельзя использовать в одновременной комбинации с доксорубицином, только в последовательной комбинации. Хотя одновременная комбинация трастузумаба и доксорубицина в клинических исследованиях показала лучший ответ опухоли, комбинация привела к неприемлемой кардиотоксичности, включая риск сердечной недостаточности, проявляющейся в виде хроническая сердечная недостаточность (CHF). Опубликованные результаты исследования фазы II показали, что миоцет, трастузумаб и паклитаксел можно безопасно использовать одновременно без сердечного риска, измеряемого по снижению LVEF функции, при этом обеспечивая превосходный ответ опухоли. Это открытие является основой для продолжающегося исследования фазы III для утверждения FDA.[10]
Побочные эффекты
Кардиотоксичность
Самый опасный побочный эффект доксорубицина - это дилатационная кардиомиопатия, что приводит к хроническая сердечная недостаточность. Частота кардиомиопатии зависит от ее кумулятивной дозы, с частотой около 4%, когда доза доксорубицина составляет 500–550 мг / м 2.2, 18% при дозе 551–600 мг / м2 и 36% при дозе более 600 мг / м2.[12] Считается, что доксорубицин вызывает кардиомиопатию несколькими способами, в том числе: окислительный стресс, подавление генов сократительных белков и p53 -опосредованный апоптоз.[12]
Кардиомиопатия, вызванная доксорубицином, обычно приводит к дилатационной кардиомиопатии с увеличением всех четырех камер сердца.[13] Это приводит как к систолической, так и к диастолической дисфункции.[13] В конце концов, это может привести к сердечной недостаточности, что приводит к 50% смертности.[13] Эффективного лечения кардиомиопатии, вызванной препаратом, на 2010 г. не существует.[13] Наркотик дексразоксан в некоторых случаях может использоваться для снижения риска кардиотоксичности доксорубицина.[14]
Другой
Еще одно частое и потенциально смертельное осложнение доксорубицина - это: тифлит, острая опасная для жизни инфекция кишечника.[15] Кроме того, у некоторых людей может развиться СИЗ, характеризующийся кожными высыпаниями на ладонях или подошвах ног, отеком, болью и эритема.[9] Из-за этих побочных эффектов и его красного цвета доксорубицин получил прозвище «красный дьявол».[16][17] или «красная смерть».[18]
Химиотерапия может вызвать реактивацию гепатит Б, и схемы, содержащие доксорубицин, не являются исключением.[19][20]
Доксорубицин и некоторые химиотерапевтические препараты (включая циклофосфамид) вызывают диспигментацию. Другие группы лекарств, вызывающих эту проблему, включают противомалярийные препараты, амиодарон, тяжелые металлы (но не железо), тетрациклины, и нейролептики.[21]
Биосинтез
Доксорубицин (DXR) представляет собой 14-гидроксилированный версия даунорубицин, непосредственный предшественник DXR в его биосинтетический путь.
Даунорубицин более широко встречается как натуральный продукт потому что его производят различные дикого типа напряжения из Streptomyces. Напротив, только один известный не-дикого типа разновидность, Streptomyces peucetius подвид цезий Первоначально было обнаружено, что ATCC 27952 способен продуцировать более широко используемый доксорубицин.[22] Этот штамм был создан Arcamone et al. в 1969 г. мутирующий штамм, продуцирующий даунорубицин, но не DXR, по крайней мере, в определяемых количествах.[23] Впоследствии группа Хатчинсона показала, что в особых условиях окружающей среды или путем введения генетические модификации, другие штаммы Streptomyces может производить доксорубицин.[24] Его группа также клонированный многие из гены необходимы для производства DXR, хотя не все из них полностью охарактеризованы. В 1996 году группа Штроля обнаружила, изолировала и охарактеризовала dox A, ген кодирование фермент который превращает даунорубицин в DXR.[25]
К 1999 году они произвели рекомбинантный dox A, a оксидаза цитохрома P450, и обнаружил, что это катализирует несколько шагов в DXR биосинтез, включая шаги, ведущие к даунорубицину.[26] Это было важно, потому что стало ясно, что все штаммы, продуцирующие даунорубицин, имеют необходимые гены производить DXR, гораздо более терапевтически важный из двух. Группа Хатчинсона продолжила разработку методов увеличения выхода DXR из ферментация процесс, используемый в его коммерческом производстве, не только путем введения кодировки dox A плазмиды, но также путем введения мутаций для деактивации ферменты которые шунтируют предшественники DXR в менее полезные продукты, например, подобные баумицину гликозиды.[22] Некоторые тройные мутанты, которые тоже чрезмерно выраженный dox A, смогли удвоить выход DXR. Это представляет более чем академический интерес, потому что в то время DXR стоил около 1,37 миллиона долларов за кг, а текущее производство в 1999 году составляло 225 кг в год.[27]
Более эффективные производственные технологии снизили цену до 1,1 миллиона долларов за килограммлипосомальный формулировка. Хотя DXR можно производить полусинтетически из даунорубицина процесс включает электрофильный бромирование и несколько шагов, и урожай плохой.[28] Поскольку даунорубицин производится ферментация, было бы идеально, если бы бактерии может завершить синтез DXR более эффективно.
Механизм действия
Доксорубицин взаимодействует с ДНК посредством вставка и ингибирование макромолекулярных биосинтез.[4][30][31] Это тормозит развитие топоизомераза II, фермент, который расслабляет суперспирали в ДНК для транскрипция.[32] Доксорубицин стабилизирует комплекс топоизомеразы II после того, как он разорвал цепь ДНК для репликации, предотвращая повторное запечатывание двойной спирали ДНК и тем самым останавливая процесс репликация.[4] Он также может увеличивать производство свободных радикалов хинонового типа, что способствует его цитотоксичности.[8]
Часть плоского ароматического хромофора молекулы интеркалирует между двумя парами оснований ДНК, в то время как шестичленный сахар даунозамин находится в малой бороздке и взаимодействует с фланкирующими парами оснований, непосредственно прилегающими к сайту интеркаляции, о чем свидетельствуют несколько кристаллических структур.[29][33]
К вставка доксорубицин также может вызывать гистон выселение из транскрипционно активного хроматин.[34][35] Как результат, Ответ на повреждение ДНК, эпигеном и транскриптом дерегулированы в клетках, подвергшихся воздействию доксорубицина.[34]
История
В 1950-х годах итальянская исследовательская компания Фармиталия Исследовательские лаборатории начали организованную попытку найти противораковые соединения из почвенных микробов. Образец почвы был изолирован от территории, окружающей Кастель-дель-Монте, замок 13 века. Новый штамм Streptomyces peucetius, который продуцировал красный пигмент, был изолирован, и антибиотик из этой бактерии оказался эффективным против опухолей у мышей. Поскольку группа французских исследователей открыла одно и то же соединение примерно в одно и то же время, две группы назвали соединение даунорубицин, объединяя имя Дауни, доримское племя, которое занимало территорию Италии, где находилось изолированное соединение, с французского слова для Рубин, рубин, описывая цвет.[36][37][38] Клинические испытания начались в 1960-х годах, и препарат оказался успешным при лечении острого лейкоза и лимфомы. Однако к 1967 году было признано, что даунорубицин может вызывать фатальную сердечную токсичность.[39]
Исследователи из Farmitalia вскоре обнаружили, что изменения в биологической активности могут быть вызваны незначительными изменениями в структуре соединения. Напряжение Streptomyces был изменен с использованием N-нитрозо-N-метилуретан, и этот новый штамм продуцировал другой антибиотик красного цвета. Они назвали это новое соединение адриамицином в честь Адриатическое море, и название было позже изменено на доксорубицин, чтобы соответствовать установленному соглашению об именах.[23] Доксорубицин показал лучшую активность, чем даунорубицин, против опухолей мышей, особенно солидных опухолей. Он также показал более высокий терапевтический индекс, но кардиотоксичность остался.[40]
Доксорубицин и даунорубицин вместе можно рассматривать как соединения-прототипы для антрациклины. Последующие исследования привели к появлению многих других антрациклиновых антибиотиков или аналогов, и в настоящее время известно более 2000 аналогов доксорубицина. К 1991 году 553 из них прошли проверку в рамках программы проверки в Национальный институт рака (NCI).[36] В 2016 году GPX-150 получил орфанный препарат обозначение FDA США.[41]
Общество и культура
Имена
Он также известен как гидроксидаунорубицин и гидроксидауномицин.[42]
Он продается под разными торговыми марками, включая Adriamycin PFS, Adriamycin RDF или Rubex.[2]
Составы
Доксорубицин светочувствителен, и контейнеры часто закрывают алюминиевым пакетом и / или коричневой вощеной бумагой, чтобы на него не влиял свет.[2] Доксорубицин также доступен в липосома -инкапсулированные формы как Доксил (пегилированный форма), Myocet (непегилированная форма) и Caelyx, хотя эти формы также необходимо вводить внутривенно.[2]
Дефицит
С 2011 по март 2014 года поставки Доксила были ограничены.[43] В 2011 году Doxil стал доступен только в очень ограниченных количествах из-за производственных проблем со сторонним производителем. Johnson & Johnson (JNJ) через свою дочернюю компанию Janssen Products, LP, получала поставки доксила от контрактного производителя Ben Venue Laboratories (расположенного в Бедфорде, штат Огайо), подразделения Boehringer Ingelheim GmbH Германии.[44] Проблемы начались, когда Ben Venue временно остановил производство из-за проблем с контролем качества.[45]
В феврале 2012 года, чтобы решить проблему нехватки доксила, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) разрешило временный ввоз Lipodox, который содержит тот же активный ингредиент, что и доксил, и производится Sun Pharma Global FZE (Sun), дочерней компанией Индийская компания Sun Pharmaceutical Industries Ltd.[46] Агентство заявило, что намерено продолжать разрешать импорт Lipodox до тех пор, пока Sun не произведет достаточное количество дженерика Doxil для удовлетворения спроса.[47]
FDA одобрило первую генерическую версию Doxil, произведенную Sun, в феврале 2013 года. Он будет доступен во флаконах по 20 и 50 миллиграммов.[48]
Исследование
Комбинированная терапия эксперименты с сиролимус (рапамицин) и доксорубицин показали себя многообещающими при лечении Акт -положительный лимфомы у мышей.[49]
В 2006 году исследования на животных соединили мышиный моноклональное антитело с доксорубицином создал иммуноконъюгат что удалось устранить ВИЧ-1 инфекция у мышей. Текущее лечение с антиретровирусная терапия (АРТ) по-прежнему оставляет очаги ВИЧ в организме хозяина. Иммуноконъюгат потенциально может обеспечить дополнительное лечение к АРТ для устранения антиген-экспрессирующих Т-клетки.[50][51]
Противомалярийная активность
Имеются некоторые доказательства противомалярийной активности доксорубицина и аналогичных соединений. В 2009 году было обнаружено, что соединение, сходное по структуре с доксорубицином, ингибирует плазмепсин II, уникальный фермент малярийного паразита. Плазмодий falciparum.[52] Фармацевтическая компания GlaxoSmithKline (GSK) позже идентифицировал доксорубицин в составе набора соединений, подавляющих рост паразитов. [53]
Флуоресценция
Также известно, что доксорубицин является флуоресцентным. Это часто использовалось для характеристики концентраций доксорубицина и открыло возможность использования молекулы в качестве тераностический агент. Однако существуют значительные ограничения, поскольку известно, что спектр флуоресценции доксорубицина зависит от множества факторов, включая pH среды, растворителя. диэлектрическая постоянная и другие. Флуоресценция доксорубицина подавляется связыванием с ДНК и экранируется инкапсуляцией мицелл. Также известно, что при высоких концентрациях он самозатухает. Напротив, связывание гистонов усиливает флуоресценцию.[54][55]
Смотрите также
Рекомендации
- ^ а б c «(доксорубицин) дозировка, показания, взаимодействия, побочные эффекты и многое другое». Ссылка на Medscape. WebMD. В архиве из оригинала 16 апреля 2014 г.. Получено 15 апреля 2014.
- ^ а б c d е ж Брейфилд, А, изд. (19 декабря 2013 г.). «Доксорубицин». Мартиндейл: полный справочник лекарств. Фармацевтическая пресса. Получено 15 апреля 2014.
- ^ а б c d е ж грамм час я «Доксорубицина гидрохлорид». Американское общество фармацевтов систем здравоохранения. В архиве из оригинала 11 октября 2016 г.. Получено 12 января 2017.
- ^ а б c Такар, О; Sriamornsak, P; Дасс, CR (февраль 2013 г.). «Доксорубицин: обновленная информация о противораковом молекулярном действии, токсичности и новых системах доставки лекарств». Журнал фармации и фармакологии. 65 (2): 157–70. Дои:10.1111 / j.2042-7158.2012.01567.x. PMID 23278683. S2CID 34737360.
- ^ Всемирная организация здоровья (2019). Типовой список основных лекарственных средств Всемирной организации здравоохранения: 21-й список 2019 г.. Женева: Всемирная организация здравоохранения. HDL:10665/325771. WHO / MVP / EMP / IAU / 2019.06. Лицензия: CC BY-NC-SA 3.0 IGO.
- ^ а б Британский национальный формуляр: BNF 69 (69 изд.). Британская медицинская ассоциация. 2015. стр. 583. ISBN 9780857111562.
- ^ Равина, Энрике (2011). Эволюция открытия лекарств: от традиционных лекарств к современным лекарствам. Джон Вили и сыновья. п. 291. ISBN 9783527326693. В архиве из оригинала 18 сентября 2017 г.
- ^ а б Росси, S, изд. (2013). Австралийский справочник по лекарствам (Издание 2013 г.). Аделаида: Австралийский фонд руководства по лекарствам. ISBN 978-0-9805790-9-3.
- ^ а б "Информация о продукте DOXIL В архиве 21 сентября 2007 г. Wayback Machine ", Ortho Biotech Products, L.P.. Проверено 19 апреля, 2007.
- ^ а б «Липосомальный доксорубицин (Caelyx, Myocet)». Поддержка Macmillan Cancer. 1 апреля 2009 г. В архиве из оригинала 29 ноября 2009 г.. Получено 27 ноября 2009.
- ^ «Доксорубицин липосомальный». Chemocare. Кливлендская клиника. В архиве из оригинала от 2 января 2010 г.. Получено 27 ноября 2009.
- ^ а б Чатерджи, Кану; Цзяньцин Чжан; Норман Хонбо; Джоэл С. Карлинер (январь 2010 г.). «Доксорубициновая кардиомиопатия». Кардиология. 115 (2): 155–162. Дои:10.1159/000265166. ЧВК 2848530. PMID 20016174.
- ^ а б c d Кану Чаттерджи; Цзяньцин Чжан; Норман Хонбо; Джоэл С. Карлинер (2010). «Доксорубициновая кардиомиопатия». Кардиология. 115 (2): 155–162. Дои:10.1159/000265166. ЧВК 2848530. PMID 20016174.
- ^ «Монография дексразоксана гидрохлорида для профессионалов - Drugs.com». Drugs.com. Американское общество фармацевтов систем здравоохранения. Получено 1 августа 2018.
- ^ Качмарек А., Бринкман Б.М., Хейндрикс Л., Ванденабеле П., Крыско Д.В. Дж. (2012). «Тяжесть мукозита тонкого кишечника, вызванного доксорубицином, регулируется путями TLR-2 и TLR-9». Дж. Патол. 226 (4): 598–608. Дои:10.1002 / path.3009. PMID 21960132. S2CID 206325412.
- ^ "Серия препаратов для амбулаторной онкологии: доксорубицин - печально известный красный дьявол".
- ^ Блох, Ричард; Блох, Аннет. «25 наиболее часто задаваемых вопросов». Борьба с раком. Онкологический фонд Р. А. Блоха. Архивировано из оригинал 26 июня 2007 г.. Получено 28 июн 2007.
- ^ Groopman, Джером Э. (2007). Как думают врачи. Бостон: Хоутон Миффлин. п.49. ISBN 978-0-618-61003-7.
- ^ Йео В., Лам К.С., Зи Б. и др. (Ноябрь 2004 г.). «Реактивация гепатита В у пациентов с гепатоцеллюлярной карциномой, проходящих системную химиотерапию». Энн Онкол. 15 (11): 1661–6. Дои:10.1093 / annonc / mdh430. PMID 15520068.
- ^ Диллон Р., Хиршфилд GM, Эллисон М.Э., Рег К.П. (2008). «Смертельная реактивация гепатита В после химиотерапии лимфомы». BMJ. 337: a423. Дои:10.1136 / bmj.39490.680498.BE. PMID 18595895. S2CID 11661945.
- ^ "Image Challenge | NEJM". В архиве из оригинала 16 марта 2013 г.. Получено 1 сентября 2011.
- ^ а б Ломовская Н., Оттен С.Л., Дои-Катаяма Ю. и др. (1999). "Избыточное производство доксорубицина в Streptomyces peucetius: клонирование и характеристика генов dnrU-кеторедуктазы и dnrV и гена гидроксилазы цитохрома P-450 doxA ». J. Bacteriol. 181 (1): 305–18. Дои:10.1128 / JB.181.1.305-318.1999. ЧВК 103563. PMID 9864344.
- ^ а б Аркамоне Ф., Кассинелли Дж., Фантини Дж. И др. (1969). «Адриамицин, 14-гидроксидауномицин, новый противоопухолевый антибиотик от S. peucetius var. цезий". Биотехнология Биоенг. 11 (6): 1101–10. Дои:10.1002 / бит. 260110607. PMID 5365804. S2CID 21897153.
- ^ Гримм А., Маддури К., Али А., Хатчинсон CR (1994). «Характеристика генов Streptomyces peucetius ATCC 29050, кодирующих доксорубицин-поликетидсинтазу». Ген. 151 (1–2): 1–10. Дои:10.1016/0378-1119(94)90625-4. PMID 7828855.
- ^ Диккенс ML, Штрол WR (1996). «Выделение и характеристика гена из штамма C5 Streptomyces sp., Который придает способность превращать дауномицин в доксорубицин Streptomyces lividans TK24». J. Bacteriol. 178 (11): 3389–95. Дои:10.1128 / jb.178.11.3389-3395.1996. ЧВК 178102. PMID 8655530.
- ^ Вальчак Р.Дж., Диккенс М.Л., Пристли Н.Д., Штрол В.Р. (1999). «Очистка, свойства и характеристика рекомбинантного штамма Streptomyces sp. C5 DoxA, цитохрома P-450, катализирующего несколько стадий биосинтеза доксорубицина». J. Bacteriol. 181 (1): 298–304. Дои:10.1128 / JB.181.1.298-304.1999. ЧВК 103562. PMID 9864343.
- ^ Хатчинсон CR, Коломбо AL (1999). «Генная инженерия производства доксорубицина в Streptomyces peucetius: обзор». J. Ind. Microbiol. Биотехнология. 23 (1): 647–52. Дои:10.1038 / sj.jim.2900673. PMID 10455495. S2CID 27337697.
- ^ Лаун Дж. В. (1993). «Антрациклиновые и антрахиноновые противораковые агенты: текущее состояние и последние разработки». Pharmacol. Ther. 60 (2): 185–214. Дои:10.1016 / 0163-7258 (93) 90006-У. PMID 8022857.
- ^ а б Фредерик К.А., Уильямс Л.Д., Угетто Г. и др. (Март 1990 г.). «Структурное сравнение комплексов противораковое лекарственное средство-ДНК: адриамицин и дауномицин». Биохимия. 29 (10): 2538–49. Дои:10.1021 / bi00462a016. PMID 2334681. Кристаллическая структура доступна для скачивания в виде PDB В архиве 2008-01-14 на Wayback Machine файл.
- ^ Форнари Ф.А., Рэндольф Дж. К., Ялович Дж. К., Ритке М.К., Гевирц Д.А. (апрель 1994 г.). «Вмешательство доксорубицина в раскручивание ДНК в клетках опухоли молочной железы MCF-7». Мол Фармакол. 45 (4): 649–56. PMID 8183243.
- ^ Momparler RL, Karon M, Siegel SE, Avila F (август 1976 г.). «Влияние адриамицина на синтез ДНК, РНК и белка в бесклеточных системах и интактных клетках». Рак Res. 36 (8): 2891–5. PMID 1277199. В архиве из оригинала от 5 февраля 2009 г.
- ^ Поммье, Y; Лев, Э; Чжан, Х; Маршан, К. (май 2010 г.). «ДНК-топоизомеразы и их отравление противоопухолевыми и антибактериальными препаратами». Химия и биология. 17 (5): 421–33. Дои:10.1016 / j.chembiol.2010.04.012. ЧВК 7316379. PMID 20534341.
- ^ Пиграмма В.Дж., Фуллер В., Гамильтон Л.Д. (январь 1972 г.). «Стереохимия интеркаляции: взаимодействие дауномицина с ДНК». Природа Новая Биология. 235 (53): 17–9. Дои:10.1038 / newbio235017a0. PMID 4502404.
- ^ а б Панг Б., Цяо X, Янссен Л., Велдс А., Гротуис Т., Керкховен Р., Ньивланд М., Оваа Х., Роттенберг С., ван Теллинген О., Янссен Дж., Хуйгенс П., Цварт В., Нифьес Дж. (2013). «Лекарственное выселение гистонов из открытого хроматина способствует химиотерапевтическим эффектам доксорубицина». Nature Communications. 4 (5): 1908. Bibcode:2013НатКо ... 4.1908P. Дои:10.1038 / ncomms2921. ЧВК 3674280. PMID 23715267.
- ^ Панг Б., де Йонг Дж., Цяо Х, Весселс Л.Ф., Нифджес Дж. (2015). «Химическое профилирование генома с помощью противораковых препаратов определяет специфичность мишени». Природа Химическая Биология. 11 (7): 472–80. Дои:10.1038 / nchembio.1811. PMID 25961671.
- ^ а б Weiss RB (декабрь 1992 г.).«Антрациклины: найдем ли мы когда-нибудь лучший доксорубицин?». Семинары по онкологии. 19 (6): 670–86. PMID 1462166.
- ^ Баруффа Г (1966). «Клинические испытания малярии Plasmodium falciparum с сульфонамидом длительного действия». Пер. R. Soc. Троп. Med. Hyg. 60 (2): 222–4. Дои:10.1016/0035-9203(66)90030-7. PMID 5332105.
- ^ Согласно предварительной ссылке, первая публикация: Camerino B, Palamidessi G (1960) Derivati della parazina II. Сульфонамдопир (на итальянском языке). Газз Чим Итал 90: 1802–1815
- ^ Тан С, Тасака Х, Ю. КП, Мерфи М.Л., Карновский Д.А. (март 1967). «Дауномицин, противоопухолевый антибиотик, в лечении неопластических заболеваний. Клиническая оценка с особым акцентом на лейкоз у детей». Рак. 20 (3): 333–53. Дои:10.1002 / 1097-0142 (1967) 20: 3 <333 :: AID-CNCR2820200302> 3.0.CO; 2-K. PMID 4290058.
- ^ Ди Марко А., Гаэтани М., Скарпинато Б. (февраль 1969 г.). «Адриамицин (NSC-123,127): новый антибиотик с противоопухолевой активностью». Рак Chemother Rep. 53 (1): 33–7. PMID 5772652.
- ^ Исследуемое лекарство от саркомы GPX-150 получает статус орфанного препарата. 2016 г. В архиве 2016-01-24 в Wayback Machine
- ^ «Доксорубицин: информация о лекарствах MedlinePlus». medlineplus.gov. Получено 12 июля 2020.
- ^ «Нехватка лекарств, доксорубицин». Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. В архиве из оригинала 16 февраля 2014 г.. Получено 22 февраля 2014.
- ^ Питер Лофтус (21 июля 2011 г.). "J&J не хватает доксила против рака". Wall Street Journal. В архиве из оригинала от 9 сентября 2017 года.
- ^ "Ben Venue Laboratories - добровольное отключение". Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. 30 ноября 2011 г. В архиве из оригинала 20 февраля 2014 г.. Получено 22 февраля 2014.
- ^ Харрис, Гардинер (21 февраля 2012 г.). «Поставки из-за рубежа для облегчения нехватки двух противораковых препаратов». Нью-Йорк Таймс. В архиве из оригинала 11 марта 2014 г.. Получено 22 февраля 2014.
- ^ Юхананов, Анна (21 февраля 2012 г.). «FDA действует, чтобы остановить нехватку двух противораковых препаратов». Рейтер. В архиве из оригинала 27 февраля 2014 г.. Получено 22 февраля 2014.
- ^ «Ожидается, что одобрение FDA генерической версии противоракового препарата Doxil поможет решить проблему дефицита» (Пресс-релиз). НАС. Управление по контролю за продуктами и лекарствами (FDA). 4 февраля 2013 г. Архивировано с оригинал 28 февраля 2014 г.. Получено 22 февраля 2014.
- ^ Wendel H, De Stanchina E, Фридман J, Малина A, Ray S, Kogan S, Кордон-Кардо С, Пеллетье Дж, Лоу С. (2004). «Передача сигналов выживания с помощью Akt и eIF4E в онкогенезе и терапии рака». Природа. 428 (6980): 332–7. Bibcode:2004 Натур 428..332 Вт. Дои:10.1038 / природа02369. PMID 15029198. S2CID 4426215.CS1 maint: несколько имен: список авторов (связь)
- ^ Йоханссон С., Гольденберг Д., Гриффитс Г., Варен Б., Хинкула Дж. (2006). «Устранение ВИЧ-1 инфекции путем лечения доксорубицин-конъюгированным антителом против оболочки». СПИД. 20 (15): 1911–1915. Дои:10.1097 / 01.aids.0000247111.58961.60. PMID 16988511. S2CID 42286690.
- ^ Мицуясу, Рональд (май 2013 г.). «Лечение ВИЧ: уроки терапии рака». Текущее мнение о ВИЧ и СПИДе. 8 (3): 224–229. Дои:10.1097 / COH.0b013e32835ef0a1. ISSN 1746-630X. ЧВК 3789644. PMID 23454863.
- ^ Фридман Р., Кафлиш А. (2009). «Открытие ингибиторов плазмепсина с помощью стыковки на основе фрагментов и оценки консенсуса». ChemMedChem. 4 (8): 1317–26. Дои:10.1002 / cmdc.200900078. PMID 19472268. S2CID 14642593. Архивировано из оригинал 5 января 2013 г.
- ^ Gamo F-J; и другие. (2010). «Тысячи химических отправных точек для идентификации противомалярийного свинца». Природа. 465 (7296): 305–310. Bibcode:2010Натура.465..305Г. Дои:10.1038 / природа09107. PMID 20485427. S2CID 1143258.
- ^ Карукстис К., Томпсон Э, Уайлз Дж, Розенфельд Р. (1998). «Расшифровка сигнатуры флуоресценции дауномицина и доксорубицина». Биофизическая химия. 73 (3): 249–263. Дои:10.1016 / s0301-4622 (98) 00150-1. PMID 9700924.
- ^ Мохан П., Рапопорт Н. (2010). «Доксорубицин как молекулярный нанотераностический агент: влияние инкапсуляции доксорубицина в мицеллы или наноэмульсии на опосредованную ультразвуком внутриклеточную доставку и ядерный оборот». Молекулярная фармацевтика. 7 (6): 1959–1973. Дои:10.1021 / mp100269f. ЧВК 2997862. PMID 20957997.
внешняя ссылка
- «Доксорубицин». Портал информации о наркотиках. Национальная медицинская библиотека США.

