Глюкокиназа - Glucokinase
| Глюкокиназа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Номер ЕС | 2.7.1.2 | ||||||||
| Количество CAS | 9001-36-9 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| БРЕНДА | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
Глюкокиназа (EC 2.7.1.2 ) является фермент что облегчает фосфорилирование из глюкоза к глюкозо-6-фосфат. Глюкокиназа встречается в клетки в печень и поджелудочная железа людей и большинства других позвоночные. В каждом из этих органов он играет важную роль в регуляции углевод метаболизм действуя как датчик глюкозы, вызывая сдвиги в метаболизме или функции клеток в ответ на повышение или понижение уровня глюкозы, например, после еды или когда голодание. Мутации из ген поскольку этот фермент может вызывать необычные формы сахарный диабет или же гипогликемия.
Глюкокиназа (ГК) представляет собой гексокиназа изофермент, связанные с гомологично по крайней мере трем другим гексокиназам.[4] Все гексокиназы могут опосредовать фосфорилирование глюкозы до глюкозо-6-фосфата (G6P), что является первым шагом обоих гликоген синтез и гликолиз. Однако глюкокиназа закодированный отдельным ген и его отличительный кинетический свойства позволяют ему выполнять другой набор функций. Глюкокиназа имеет более низкое сродство к глюкозе, чем другие гексокиназы, и ее активность локализована в нескольких типах клеток, в результате чего три другие гексокиназы являются более важными факторами подготовки глюкозы для гликолиза и синтеза гликогена для большинства тканей и органов. Из-за этого пониженного сродства активность глюкокиназы при обычных условиях физиологические условия, существенно меняется в зависимости от концентрации глюкозы.[5]
Номенклатура
Альтернативные названия этого фермента: гексокиназа человека IV, гексокиназа D и АТФ: D-гексозо-6-фосфотрансфераза, EC 2.7.1.1 (ранее 2.7.1.2). Общее название глюкокиназа происходит от ее относительной специфичности в отношении глюкозы в физиологических условиях.
Немного биохимики утверждали, что следует отказаться от названия глюкокиназа как вводящего в заблуждение, так как этот фермент может фосфорилировать другие гексозы в нужных условиях, а в составе есть отдаленно связанные ферменты. бактерии с более абсолютной специфичностью для глюкозы, которая лучше заслуживает названия и EC 2.7.1.2.[5][6] Тем не менее, глюкокиназа остается предпочтительным названием в контексте лекарство и млекопитающие физиология.
Другая глюкозокиназа млекопитающих, АДФ-специфическая глюкокиназа, был обнаружен в 2004 году.[7] Этот ген отличается и похож на ген у примитивных организмов. Это зависит от ADP а не АТФ (что предполагает возможность более эффективного функционирования во время гипоксия ), а метаболическая роль и важность еще предстоит выяснить.
Катализ
Субстраты и продукты
Главный субстрат физиологического значения глюкокиназы глюкоза, и самое главное товар является глюкозо-6-фосфат (G6P). Другой необходимый субстрат, из которого получают фосфат, - это аденозинтрифосфат (АТФ), который преобразуется в аденозиндифосфат (АДФ) при удалении фосфата. Реакция, катализируемая глюкокиназой:
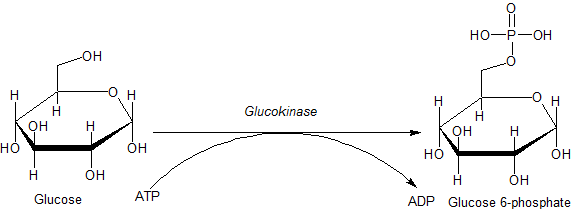
АТФ участвует в реакции в форме комплекса с магний (Mg) как кофактор. Кроме того, при определенных условиях глюкокиназа, как и другие гексокиназы, может индуцировать фосфорилирование других гексозы (6 углерода сахара ) и подобные молекулы. Таким образом, общая реакция глюкокиназы более точно описывается как:[6]
Среди гексозных субстратов есть манноза, фруктоза, и глюкозамин, но сродство глюкокиназы к ним требует концентраций, не обнаруживаемых в клетках для значительной активности.[8]
Кинетика
Два важных кинетический По своим свойствам глюкокиназа отличается от других гексокиназ, что позволяет ей выполнять особую роль сенсора глюкозы.
- Глюкокиназа имеет более низкое сродство к глюкозе, чем другие гексокиназы. Глюкокиназа изменяет конформацию и / или функцию параллельно с повышением концентрации глюкозы в физиологически важном диапазоне 4–10 ммоль / л (72–180 мг /дл ). Он наполовину насыщен при концентрации глюкозы около 8 ммоль / л (144 мг / дл).[9][10]
- Глюкокиназа не ингибируется ее продуктом, глюкозо-6-фосфатом.[9] Это позволяет непрерывно выводить сигнал (например, запускать инсулин релиз) среди значительных количеств своего продукта[10]
Эти две особенности позволяют ему регулировать метаболический путь, «управляемый поставками». То есть скорость реакции зависит от предложения глюкозы, а не от спроса на конечные продукты.
Еще одно отличительное свойство глюкокиназы - умеренная сотрудничество с глюкозой, с Коэффициент Хилла (пЧАС) около 1,7.[10] Глюкокиназа имеет только один сайт связывания для глюкозы и является единственным мономерным регуляторным ферментом, который, как известно, проявляет кооперативность с субстратом. Постулируется, что природа кооперативности включает «медленный переход» между двумя различными состояниями фермента с разной скоростью активности. Если доминантное состояние зависит от концентрации глюкозы, оно будет производить очевидную кооперативность, аналогичную наблюдаемой.[11]
Из-за этой кооперативности кинетическое взаимодействие глюкокиназы с глюкозой не соответствует классическому Кинетика Михаэлиса-Ментен. А не Kм для глюкозы точнее описать уровень половинного насыщения S0.5, которая представляет собой концентрацию, при которой фермент является насыщенным и активным на 50%.
В S0.5 и nH экстраполировать на "точка перегиба" кривой, описывающей активность фермента как функцию концентрации глюкозы около 4 ммоль / л.[12] Другими словами, при концентрации глюкозы около 72 мг / дл, что близко к нижнему пределу нормального диапазона, активность глюкокиназы наиболее чувствительна к небольшим изменениям концентрации глюкозы.
Кинетическая взаимосвязь с другим субстратом, MgATP, может быть описана классической кинетикой Михаэлиса-Ментен со сродством примерно 0,3–0,4 ммоль / л, что значительно ниже типичной внутриклеточной концентрации 2,5 ммоль / л. Тот факт, что почти всегда имеется избыток доступного АТФ, означает, что концентрация АТФ редко влияет на активность глюкокиназы.
Максимальная удельная активность (kКот, также известная как скорость оборота) глюкокиназы при насыщении обоими субстратами составляет 62 / с.[9]
Оптимум pH глюкокиназы человека был идентифицирован только недавно, и он неожиданно высок и составляет 8,5-8,7.[13]
А «минимальная математическая модель» был разработан на основе вышеупомянутой кинетической информации для прогнозирования скорости фосфорилирования глюкозы бета-клетками (BGPR) нормальной («дикого типа») глюкокиназы и известных мутаций. BGPR для глюкокиназы дикого типа составляет около 28% при концентрации глюкозы 5 ммоль / л, что указывает на то, что фермент работает на 28% емкости при обычном пороговом уровне глюкозы для запуска высвобождения инсулина.
Механизм
В сульфгидрил группы из нескольких цистеины окружают сайт связывания глюкозы. Все, кроме cys 230, необходимы для каталитического процесса, образуя несколько дисульфидные мостики при взаимодействии с субстратами и регуляторами. По крайней мере, в бета-клетках соотношение активных и неактивных молекул глюкокиназы, по крайней мере, частично определяется балансом окисление сульфгидрильных групп или восстановление дисульфидных мостиков.
Эти сульфгидрильные группы весьма чувствительны к окислительному статусу клеток, что делает глюкокиназу одним из компонентов, наиболее уязвимых к окислительному стрессу, особенно в бета-клетках.
Интерактивная карта проезда
Нажмите на гены, белки и метаболиты ниже, чтобы ссылки на соответствующие статьи.[§ 1]
- ^ Интерактивную карту путей можно редактировать на WikiPathways: «ГликолизГлюконеогенез_WP534».
Структура
| ||||||||||||||||||||||||||||
Глюкокиназа - это мономерный белок 465 аминокислоты и молекулярный вес около 50 кД. Есть как минимум две щели, одна для активный сайт, связывающий глюкозу и MgATP, а другой - для предполагаемого аллостерический активатор что еще не было идентифицировано.[15][16]
Это примерно половина размера других гексокиназ млекопитающих, которые сохраняют определенную димерную структуру. Несколько последовательностей и трехмерная структура ключевых активных сайтов. Например, связывающий АТФ домен является общим с гексокиназами, бактериальными глюкокиназами и другими белками, и общая структура называется актиновая складка.
Генетика
Глюкокиназа человека кодируется GCK ген на хромосома 7. Этот сингл аутосомный ген имеет 10 экзоны.[17][18] Гены глюкокиназы у других животных гомологичны человеческим. GCK.[9][19]
Отличительная особенность гена в том, что он начинается с двух промоутер регионы.[20] Первый экзон с 5'-конца содержит две тканеспецифичные промоторные области. Транскрипция может начинаться с любого промотора (в зависимости от ткани), так что один и тот же ген может продуцировать несколько разные молекулы в печени и в других тканях. Два изоформы глюкокиназы различаются всего на 13–15 аминокислоты на N-концевой конец молекулы, что дает лишь минимальную разницу в структуре. Две изоформы имеют одинаковые кинетические и функциональные характеристики.[5]
Первый промотор с 5'-конца, называемый «вышестоящим» или нейроэндокринным промотором, активен в клетках островков поджелудочной железы, нервной ткани и энтероцитах (тонкий кишечник клетки) для производства «нейроэндокринной изоформы» глюкокиназы.[20] Второй промотор, "нижестоящий" или промотор печени, активен в гепатоциты и направляет производство «изоформы печени».[21] Два промотора имеют небольшую гомологию последовательностей или не имеют ее и разделены 30 kбп последовательность, которая, как еще не было показано, вызывает какие-либо функциональные различия между изоформами.[5] Два промотора функционально исключительны и регулируются разными наборами регуляторных факторов, так что экспрессия глюкокиназы может регулироваться отдельно в разных типах тканей.[5] Эти два промотора соответствуют двум широким категориям функции глюкокиназы: в печени глюкокиназа действует как ворота для «массовой обработки» доступной глюкозы, в то время как в нейроэндокринных клетках она действует как сенсор, запускающий клеточные реакции, которые влияют на организм: широкий углеводный обмен.
Распределение по системам органов
Глюкокиназа была обнаружена в специфических клетках четырех типов тканей млекопитающих: печени, поджелудочной железы, тонкий кишечник, и мозг. Все они играют решающую роль в реагировании на повышение или понижение уровня глюкоза в крови.
- Преобладающими клетками печени являются гепатоциты, причем GK находится исключительно в этих клетках. В течение пищеварение углеводной пищи, когда глюкоза в крови много и инсулин уровни высокие, гепатоциты удаляют глюкозу из крови и хранят ее в виде гликоген. После завершения переваривания и всасывания печень производит глюкозу из субстратов, не содержащих глюкозу (глюконеогенез ) и гликоген (гликогенолиз ) и экспортирует его в кровь, чтобы поддерживать адекватный уровень глюкозы в крови во время голодания. Поскольку активность GK быстро возрастает по мере увеличения концентрации глюкозы, она служит центральным метаболическим переключателем для переключения метаболизма углеводов в печени между состояниями питания и голодания. Фосфорилирование глюкозы до глюкозо-6-фосфата с помощью GK способствует хранению глюкозы в виде гликогена и утилизации путем гликолиза. Отдельный промотор печени позволяет регулировать глюкокиназу в гепатоцитах иначе, чем в нейроэндокринных клетках.
- Нейроэндокринные клетки поджелудочной железы, кишечника и мозга имеют некоторые общие аспекты производства, регуляции и функции глюкокиназы.[22] В данном контексте эти ткани все вместе называются «нейроэндокринными» клетками.
- Бета-клетки и альфа-клетки поджелудочной железы островки
- Выпуск бета-клеток инсулин в ответ на повышение уровня глюкозы. Инсулин позволяет многим типам клеток импортировать и использовать глюкозу и сигнализирует печени о синтезе гликогена. Альфа-клетки производят меньше глюкагон в ответ на повышение уровня глюкозы и больше глюкагона, если уровень глюкозы в крови низкий. Глюкагон служит сигналом для печени расщеплять гликоген и выделять глюкозу в кровь. Глюкокиназа в бета-клетках служит датчиком глюкозы, усиливая секрецию инсулина при повышении уровня глюкозы в крови.
- В бета-клетках поджелудочной железы глюкокиназа является ключевым ферментом-регулятором. Глюкокиназа очень важна в регуляции секреции инсулина и известна как сенсор бета-клеток поджелудочной железы. Мутации в гене, кодирующем глюкокиназу, могут вызывать как гипергликемию, так и гипогликемию из-за своей центральной роли в регуляции высвобождения инсулина.[23]
- Чувствительный к глюкозе нейроны из гипоталамус
- В ответ на повышение или понижение уровня глюкозы клетки гипоталамуса поляризуются или деполяризуются. Среди нейроэндокринных реакций Центральная нервная система к гипогликемия активация адренергический ответы автономная нервная система. Глюкокиназа, вероятно, и здесь служит сигналом глюкозы. Глюкокиназа также была обнаружена в клетках передней гипофиз.
- Энтероциты тонкой кишки
- Это наименее изученная из сенсорных систем глюкокиназы. Кажется вероятным, что реакция на поступающую глюкозу во время пищеварения играет роль в инкретин усиление секреции инсулина во время еды или генерация сигналов насыщения от кишечника к мозгу.
- Бета-клетки и альфа-клетки поджелудочной железы островки
Распространение среди видов
Глюкокиназа печени встречается широко, но не повсеместно у позвоночных. Структура гена и аминокислотная последовательность высоко консервативны среди большинства млекопитающих (например, глюкокиназа крысы и человека гомологична более чем на 80%). Однако есть некоторые необычные исключения: например, он не был обнаружен в кошки и летучие мыши хотя некоторые рептилии, птицы, амфибии, и рыбы иметь это. Происходит ли аналогичное действие глюкокиназы в поджелудочной железе и других органах, еще не установлено. Было высказано предположение, что присутствие глюкокиназы в печени отражает легкость, с которой углеводы могут быть включены в организм животных. диеты.
Функция и регулирование
Большая часть глюкокиназы у млекопитающих находится в печени, а глюкокиназа обеспечивает примерно 95% активности гексокиназы в гепатоцитах. Фосфорилирование глюкозы до глюкозо-6-фосфат (G6P) глюкокиназой является первым шагом обоих гликоген синтез и гликолиз в печени.
Когда доступно достаточное количество глюкозы, синтез гликогена продолжается на периферии гепатоцитов до тех пор, пока клетки не наполнятся гликогеном. Затем избыток глюкозы в большей степени превращается в триглицериды на экспорт и хранение в жировой ткань. Активность глюкокиназы в цитоплазме повышается и падает с доступной глюкозой.
G6P, продукт глюкокиназы, является основным субстратом синтеза гликогена, а глюкокиназа имеет тесную функциональную и регуляторную связь с синтезом гликогена. При максимальной активности GK и гликогенсинтаза по-видимому, располагается в тех же периферических областях цитоплазмы гепатоцитов, в которых происходит синтез гликогена. Поставка G6P влияет на скорость синтеза гликогена не только в качестве основного субстрата, но и путем прямой стимуляции гликогенсинтазы и ингибирования гликогенфосфорилаза.
Активность глюкокиназы может быстро увеличиваться или уменьшаться в ответ на изменения в поставке глюкозы, обычно возникающие в результате еды и голодания. Регулирование происходит на нескольких уровнях и на нескольких скоростях, и на него влияют многие факторы, которые влияют в основном на два основных механизма:
- Активность глюкокиназы может быть увеличена или уменьшена за несколько минут под действием регуляторный белок глюкокиназы (ГКРП). На действие этого белка влияют небольшие молекулы, такие как глюкоза и фруктоза.
- Количество глюкокиназы можно увеличить за счет синтеза нового белка. Инсулин является основным сигналом для усиления транскрипции, действуя главным образом посредством фактора транскрипции, называемого белок, связывающий регуляторный элемент стерола -1c (SREBP1c), кроме печени. Это происходит в течение часа после повышения уровня инсулина, как после углеводной еды.[нужна цитата ]
Транскрипционный
Инсулин, действующий через белок, связывающий регуляторный элемент стерола -1c (SREBP1c) считается наиболее важным прямым активатором транскрипции гена глюкокиназы в гепатоцитах. SREBP1c - это молния базовая спираль-петля-спираль (bHLHZ) трансактиватор. Трансактиваторы этого класса связываются с последовательностью «Е-бокса» генов ряда регуляторных ферментов. Промотор печени в первом экзоне гена глюкокиназы включает такой E-бокс, который, по-видимому, является основным элементом инсулинового ответа гена в гепатоцитах. Ранее считалось, что SREBP1c должен присутствовать для транскрипции глюкокиназы в гепатоцитах, однако недавно было показано, что транскрипция глюкокиназы обычно осуществляется у мышей с нокаутом SREBP1c. SREBP1c увеличивается в ответ на диету с высоким содержанием углеводов, что, как предполагается, является прямым следствием частого повышения уровня инсулина. Повышенную транскрипцию можно обнаружить менее чем через час после воздействия на гепатоциты повышенного уровня инсулина.
Фруктозо-2,6-бисфосфат (F2,6P
2) также стимулирует транскрипцию GK, по-видимому, посредством Akt2, а не SREBP1c. Неизвестно, является ли этот эффект одним из последующих эффектов активации рецепторов инсулина или независимым от действия инсулина. Уровни F2,6P
2 играют другие усиливающие роли в гликолизе в гепатоцитах.
Другие трансакционные факторы, которые, как предполагается, играют роль в регуляции транскрипции клеток печени, включают:
- Ядерный фактор печени-4-альфа (HNF4α ) представляет собой орфанный ядерный рецептор, важный для транскрипции многих генов ферментов углеводного и липидного обмена. Это активирует GCK транскрипция.
- Верхний стимулирующий фактор 1 (USF1 ) Другой молния базовая спираль-петля-спираль (bHLHZ) трансактиватор.
- Ядерный фактор печени 6 (HNF6 ) является гомеодоменным регулятором транскрипции «однократного класса». HNF6 также участвует в регуляции транскрипции глюконеогенный ферменты, такие как глюкозо-6-фосфатаза и фосфоенолпируваткарбоксикиназа.
Гормонально-диетический
Инсулин на сегодняшний день является наиболее важным из гормонов, которые прямо или косвенно влияют на экспрессию и активность глюкокиназы в печени. Инсулин, по-видимому, влияет как на транскрипцию, так и на активность глюкокиназы множеством прямых и непрямых путей. При подъеме воротная вена уровень глюкозы увеличивает активность глюкокиназы, сопутствующее повышение инсулина усиливает этот эффект на индукция синтеза глюкокиназы. Транскрипция глюкокиназы начинает расти в течение часа после повышения уровня инсулина. Транскрипция глюкокиназы становится почти невыявимой при длительном голодании, тяжелой углеводной недостаточности или нелеченном инсулино-дефицитном диабете.
Механизмы, с помощью которых инсулин индуцирует глюкокиназу, могут включать как основные внутриклеточные пути действия инсулина, так и каскад киназ, регулируемых внеклеточными сигналами (ERK 1/2), и каскад фосфоинозитид-3-киназ (PI3-K). Последний может работать через трансактиватор FOXO1.
Однако, как и следовало ожидать, учитывая его антагонистический эффект на синтез гликогена, глюкагон и его внутриклеточный второй посланник лагерь подавляет транскрипцию и активность глюкокиназы даже в присутствии инсулина.
Другие гормоны, такие как трийодтиронин (Т
3) и глюкокортикоиды в определенных обстоятельствах оказывают разрешающее или стимулирующее действие на глюкокиназу. Биотин и ретиноевая кислота увеличить транскрипцию мРНК GCK, а также активность GK. Жирные кислоты в значительных количествах усиливают активность ГК в печени, в то время как длинноцепочечный ацил-КоА тормозит это.
Печеночный
Глюкокиназа может быть быстро активирована и инактивирована в гепатоцитах новым регуляторным белком (регуляторный белок глюкокиназы ), который поддерживает неактивный резерв GK, который может быстро стать доступным в ответ на повышение уровня глюкозы в воротной вене.[24]
ГКРП перемещается между ядро и цитоплазма гепатоцитов и может быть привязан к микрофиламенту цитоскелет. Он образует обратимые комплексы 1: 1 с GK и может перемещать его из цитоплазмы в ядро. Он действует как конкурентный ингибитор глюкозы, так что активность фермента снижается почти до нуля при связывании. GK: комплексы GKRP секвестрируются в ядре, в то время как уровни глюкозы и фруктозы низкие. Ядерная секвестрация может служить для защиты GK от деградации цитоплазматической протеазы. GK может быстро высвобождаться из GKRP в ответ на повышение уровня глюкозы. В отличие от GK в бета-клетках, GK в гепатоцитах не связан с митохондриями.
Фруктоза в крошечных (микромолярных) количествах (после фосфорилирования кетогексокиназа к фруктозо-1-фосфат (F1P)) ускоряет выпуск ГК из ГКРП. Эта чувствительность к присутствию небольшого количества фруктозы позволяет GKRP, GK и кетогексокиназе действовать как «система восприятия фруктозы», которая сигнализирует о том, что смешанная углеводная еда переваривается, и ускоряет утилизацию глюкозы. Тем не мение, фруктозо-6-фосфат (F6P) усиливает связывание GK посредством GKRP. F6P снижает фосфорилирование глюкозы GK, когда гликогенолиз или же глюконеогенез в стадии реализации. F1P и F6P связываются с одним и тем же сайтом на GKRP. Предполагается, что они продуцируют 2 разные конформации GKRP, одна способна связывать GK, а другая нет.
Панкреатический
Хотя большая часть глюкокиназы в организме находится в печени, меньшие количества в бета- и альфа-клетках поджелудочной железы, некоторых нейронах гипоталамуса и определенных клетках (энтероцитах) кишечника играют все более важную роль в регуляции углеводного обмена. В контексте функции глюкокиназы эти типы клеток вместе называются нейроэндокринными тканями, и у них есть общие аспекты регуляции и функции глюкокиназы, особенно общий нейроэндокринный промотор. Из нейроэндокринных клеток бета-клетки островков поджелудочной железы являются наиболее изученными и изученными. Вероятно, что многие из регуляторных отношений, обнаруженных в бета-клетках, будут также существовать в других нейроэндокринных тканях с глюкокиназой.
Сигнал для инсулина
На островке бета-клетки, активность глюкокиназы служит основным контролем секреции инсулин в ответ на повышение уровня глюкозы в крови. Когда G6P потребляется, увеличивающееся количество АТФ запускает серию процессов, которые приводят к высвобождению инсулина. Одним из непосредственных последствий учащения клеточного дыхания является повышение НАДН и НАДФН концентрации (вместе именуемые НАД (Ф) Н). Этот сдвиг в окислительно-восстановительном статусе бета-клеток приводит к увеличению внутриклеточного кальций уровни, закрытие KАТФ каналы деполяризация клеточной мембраны, слияние секреторных гранул инсулина с мембраной и выброс инсулина в кровь.
Именно как сигнал для высвобождения инсулина глюкокиназа оказывает наибольшее влияние на уровень сахара в крови и общее направление метаболизма углеводов. Глюкоза, в свою очередь, влияет как на непосредственную активность, так и на количество глюкокиназы, продуцируемой бета-клетками.
Регулирование в бета-клетках
Глюкоза немедленно усиливает активность глюкокиназы за счет эффекта кооперативности.
Второй важный быстрый регулятор активности глюкокиназы в бета-клетках происходит за счет прямого белок-белкового взаимодействия между глюкокиназой и «бифункциональным ферментом» (фосфофруктокиназа-2 / фруктоза-2,6-бисфосфатаза), который также играет роль в регуляции гликолиза. . Эта физическая ассоциация стабилизирует глюкокиназу в каталитически благоприятной конформации (несколько противоположной эффекту связывания GKRP), что усиливает ее активность.
Всего за 15 минут глюкоза может стимулировать GCK транскрипция и синтез глюкокиназы посредством инсулина. Инсулин вырабатывается бета-клетками, но часть его действует на бета-клетки B-типа. рецепторы инсулина, обеспечивая автокринный усиление активности глюкокиназы с положительной обратной связью. Дальнейшая амплификация происходит под действием инсулина (через рецепторы А-типа) для стимуляции собственной транскрипции.
Транскрипция GCK ген инициируется через "вышестоящий" или нейроэндокринный промотор. Этот промотор, в отличие от промотора печени, имеет элементы, гомологичные другим промоторам индуцированных инсулином генов. Среди возможных трансакционных факторов - Pdx-1 и PPARγ. Pdx-1 представляет собой фактор транскрипции гомеодомена, участвующий в дифференцировке поджелудочной железы. PPARγ - это ядерный рецептор, который реагирует на препараты глитазона повышением чувствительности к инсулину.
Связь с секреторными гранулами инсулина
Большая часть, но не вся глюкокиназа, обнаруженная в цитоплазме бета-клеток, связана с секреторными гранулами инсулина и митохондриями. «Связанная» доля быстро падает в ответ на повышение секреции глюкозы и инсулина. Было высказано предположение, что связывание служит цели, аналогичной цели печеночного регуляторного белка глюкокиназы, - защите глюкокиназы от деградации, так что она быстро становится доступной по мере повышения уровня глюкозы. Эффект заключается в усилении ответа глюкокиназы на глюкозу быстрее, чем это может сделать транскрипция.[25]
Подавление глюкагона в альфа-клетках
Также было высказано предположение, что глюкокиназа играет роль в чувствительности к глюкозе панкреатической железой. альфа-клетки, но доказательства менее последовательны, и некоторые исследователи не нашли доказательств активности глюкокиназы в этих клетках. Альфа-клетки встречаются в островках поджелудочной железы в смеси с бета-клетками и другими клетками. В то время как бета-клетки реагируют на повышение уровня глюкозы, секретируя инсулин, альфа-клетки реагируют снижением уровня глюкозы. глюкагон секреция. Когда концентрация глюкозы в крови падает до гипогликемический уровни, альфа-клетки выделяют глюкагон. Глюкагон - это белковый гормон, который блокирует действие инсулина на гепатоциты, вызывая гликогенолиз, глюконеогенез и снижая активность глюкокиназы в гепатоцитах. Степень, в которой подавление глюкозы глюкагона является прямым эффектом глюкозы через глюкокиназу в альфа-клетках или косвенным эффектом, опосредованным инсулином или другими сигналами от бета-клеток, все еще остается неопределенной.
Гипоталамический
Пока все нейроны использовать глюкозу в качестве топлива, некоторые нейроны, чувствительные к глюкозе изменяют скорость их возбуждения в ответ на повышение или понижение уровня глюкозы. Эти нейроны, чувствительные к глюкозе, сосредоточены в основном в вентромедиальное ядро и дугообразное ядро из гипоталамус, которые регулируют многие аспекты гомеостаза глюкозы (особенно реакцию на гипогликемию), использование топлива, сытость и аппетит, и масса поддержание. Эти нейроны наиболее чувствительны к изменениям глюкозы в диапазоне 0,5–3,5 ммоль / л глюкозы.
Глюкокиназа была обнаружена в головном мозге в основном в тех же областях, которые содержат нейроны, чувствительные к глюкозе, включая оба ядра гипоталамуса. Ингибирование глюкокиназы устраняет реакцию вентромедиального ядра на прием пищи. Однако уровень глюкозы в мозге ниже, чем в плазме, обычно 0,5–3,5 ммоль / л. Хотя этот диапазон соответствует чувствительности нейронов, чувствительных к глюкозе, он ниже оптимальной чувствительности к перегибу для глюкокиназы. Предположение, основанное на косвенных доказательствах и предположениях, состоит в том, что нейрональная глюкокиназа каким-то образом подвергается воздействию уровня глюкозы в плазме даже в нейронах.
Энтероциты и инкретин
Хотя было показано, что глюкокиназа присутствует в определенных клетках (энтероцитах) тонкий кишечник и желудок, его функции и регуляция не изучены. Было высказано предположение, что и здесь глюкокиназа служит сенсором глюкозы, позволяя этим клеткам обеспечивать один из самых ранних метаболических ответов на поступающие углеводы. Предполагается, что эти клетки участвуют в инкретин функции.
Клиническое значение
Поскольку инсулин является одним из, если не самым важным, регуляторов синтеза глюкокиназы, сахарный диабет всех типов снижает синтез и активность глюкокиназы по ряду механизмов. Активность глюкокиназы чувствительна к окислительному стрессу клеток, особенно бета-клеток.
Около 200 мутации глюкокиназы человека ген GCK были обнаружены, которые могут изменять эффективность связывания и фосфорилирования глюкозы, увеличивая или уменьшая чувствительность секреции инсулина бета-клетками в ответ на глюкозу и производя клинически значимые гипергликемия или же гипогликемия.
Сахарный диабет
GCK мутации снижают функциональную эффективность молекулы глюкокиназы. Гетерозиготность для аллелей с пониженной активностью фермента приводит к более высокому порогу высвобождения инсулина и стойкой легкой гипергликемии. Это состояние называется зрелость начало диабета молодых, тип 2 (MODY2). Самый последний обзор GCK Мутация, которая наблюдалась у пациентов, заявляет о 791 мутации, 489 из которых, как полагают, вызывают диабет MODY и, следовательно, снижают функциональную эффективность молекулы глюкокиназы.[26]
Гомозиготность за GCK аллели с пониженной функцией могут вызывать тяжелый врожденный дефицит инсулина, что приводит к стойкому неонатальный диабет.
Гиперинсулинемическая гипогликемия
Было обнаружено, что некоторые мутации усиливают секрецию инсулина. Гетерозиготность для увеличения функциональных мутаций снижает порог глюкозы, который запускает высвобождение инсулина. Это создает гипогликемию различной формы, в том числе временную или стойкую. врожденный гиперинсулинизм, или пост или реактивная гипогликемия появляясь в более старшем возрасте. Самый последний обзор GCK мутации, которые наблюдались у пациентов, заявили о 17 GCK мутации, вызывающие гиперинсулинемическую гипогликемию.[26]
Гомозиготность мутаций по усилению функции не обнаружена.
Исследование
Несколько Фармацевтические компании исследуют молекулы, которые активируют глюкокиназу, в надежде, что она будет полезна при лечении диабет 2 типа.[27][28][29]
Рекомендации
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000041798 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Каваи С., Мукаи Т., Мори С., Миками Б., Мурата К. (апрель 2005 г.). «Гипотеза: структуры, эволюция и предок глюкозокиназ в семействе гексокиназ». Журнал биологии и биоинженерии. 99 (4): 320–30. Дои:10.1263 / jbb.99.320. PMID 16233797.
- ^ а б c d е Iynedjian PB (январь 2009 г.). «Молекулярная физиология глюкокиназы млекопитающих». Клеточные и молекулярные науки о жизни. 66 (1): 27–42. Дои:10.1007 / s00018-008-8322-9. ЧВК 2780631. PMID 18726182.
- ^ а б Карденас ML (2004). «Сравнительная биохимия глюкокиназы». В Matschinsky FM, Magnuson MA (ред.). Глюкокиназа и гликемическая болезнь: от основ до новых методов лечения (границы диабета). Базель: S. Karger AG (Швейцария). С. 31–41. ISBN 3-8055-7744-3.
- ^ Ронимус Р.С., Морган Х.В. (март 2004 г.). «Клонирование и биохимическая характеристика новой АДФ-зависимой глюкокиназы мыши». Сообщения о биохимических и биофизических исследованиях. 315 (3): 652–8. Дои:10.1016 / j.bbrc.2004.01.103. PMID 14975750.
- ^ Магнусон М.А., Мачинский Ф.М. (2004). «Глюкокиназа как сенсор глюкозы: прошлое, настоящее и будущее». В Matschinsky FM, Magnuson MA (ред.). Глюкокиназа и гликемическая болезнь: от основ до новых методов лечения (границы диабета). Базель: S. Karger AG (Швейцария). С. 18–30. ISBN 3-8055-7744-3.
- ^ а б c d Белл GI, Cuesta-Munoz A, Matschinsky FM (2002). «Глюкокиназа». Энциклопедия молекулярной медицины. Хобокен: Джон Уайли и сыновья. ISBN 978-0-471-37494-7.
- ^ а б c Мачинский FM (февраль 1996 г.). «Лекция Бантинга, 1995. Урок метаболической регуляции, вдохновленный парадигмой глюкокиназного сенсора». Сахарный диабет. 45 (2): 223–41. Дои:10.2337 / диабет.45.2.223. PMID 8549869.
- ^ Heredia VV, Thomson J, Nettleton D, Sun S (июнь 2006 г.). "Индуцированные глюкозой конформационные изменения глюкокиназы опосредуют аллостерическую регуляцию: временный кинетический анализ". Биохимия. 45 (24): 7553–62. Дои:10.1021 / bi060253q. PMID 16768451.
- ^ Matschinsky FM, Glaser B, Magnuson MA (март 1998 г.). «Глюкокиназа бета-клеток поджелудочной железы: устранение разрыва между теоретическими концепциями и экспериментальными реалиями». Сахарный диабет. 47 (3): 307–15. Дои:10.2337 / диабет.47.3.307. PMID 9519733.
- ^ Шимчикова Д., Хенеберг П. (август 2019 г.). «Идентификация щелочного оптимума pH глюкокиназы человека из-за коррекции АТФ-опосредованного смещения результатов ферментных анализов». Научные отчеты. 9 (1): 11422. Bibcode:2019НатСР ... 911422С. Дои:10.1038 / s41598-019-47883-1. ЧВК 6684659. PMID 31388064.
- ^ Лунин В.В., Ли Й., Шраг Дж. Д., Яннуцци П., Сиглер М., Мэтт А (октябрь 2004 г.). «Кристаллические структуры АТФ-зависимой глюкокиназы Escherichia coli и ее комплекса с глюкозой». Журнал бактериологии. 186 (20): 6915–27. Дои:10.1128 / JB.186.20.6915-6927.2004. ЧВК 522197. PMID 15466045.
- ^ Махалингам Б., Куэста-Муньос А., Дэвис Э.А., Матчинский Ф.М., Харрисон Р.В., Вебер ИТ (сентябрь 1999 г.). «Структурная модель человеческой глюкокиназы в комплексе с глюкозой и АТФ: последствия для мутантов, вызывающих гипо- и гипергликемию». Сахарный диабет. 48 (9): 1698–705. Дои:10.2337 / диабет.48.9.1698. PMID 10480597.
- ^ Камата К., Мицуя М., Нисимура Т., Эйки Дж., Нагата И. (март 2004 г.). «Структурные основы аллостерической регуляции мономерного аллостерического фермента глюкокиназы человека». Структура. 12 (3): 429–38. Дои:10.1016 / j.str.2004.02.005. PMID 15016359.
Красивые структурные изображения, иллюстрирующие конформационные изменения и потенциальные регуляторные механизмы
- ^ Мацутани А., Янссен Р., Донис-Келлер Х., Пермутт Массачусетс (февраль 1992 г.). «Полиморфный (СА) n повторяющийся элемент отображает ген глюкокиназы человека (GCK) на хромосому 7р». Геномика. 12 (2): 319–25. Дои:10.1016 / 0888-7543 (92) 90380-Б. PMID 1740341.
- ^ Стоффель М., Фрогель П., Такеда Дж., Зуали Х., Вионнет Н., Ниши С. и др. (Август 1992 г.). «Ген глюкокиназы человека: выделение, характеристика и идентификация двух миссенс-мутаций, связанных с ранним началом инсулиннезависимого (типа 2) сахарного диабета». Труды Национальной академии наук Соединенных Штатов Америки. 89 (16): 7698–702. Bibcode:1992PNAS ... 89.7698S. Дои:10.1073 / пнас.89.16.7698. ЧВК 49778. PMID 1502186.
- ^ Уилсон Дж. Э. (2004). «Семейство генов гексокиназы». В Matschinsky FM, Magnuson MA (ред.). Глюкокиназа и гликемическая болезнь: от основ до новых методов лечения (границы диабета). Базель: S. Karger AG (Швейцария). С. 18–30. ISBN 3-8055-7744-3.
- ^ а б Iynedjian PB, Pilot PR, Nouspikel T, Milburn JL, Quaade C, Hughes S, et al. (Октябрь 1989 г.). «Дифференциальная экспрессия и регуляция гена глюкокиназы в печени и островках Лангерганса». Труды Национальной академии наук Соединенных Штатов Америки. 86 (20): 7838–42. Bibcode:1989PNAS ... 86.7838I. Дои:10.1073 / pnas.86.20.7838. ЧВК 298166. PMID 2682629.
- ^ Iynedjian PB, Jotterand D, Nouspikel T, Asfari M, Pilot PR (декабрь 1989 г.). «Транскрипционная индукция гена глюкокиназы инсулином в культивируемых клетках печени и его репрессия системой глюкагон-цАМФ». Журнал биологической химии. 264 (36): 21824–9. PMID 2557341.
- ^ Джеттон Т.Л., Лян И., Петтефер С.К., Циммерман Е.С., Кокс Ф.Г., Хорват К. и др. (Февраль 1994). «Анализ активности промотора глюкокиназы выше по течению у трансгенных мышей и идентификация глюкокиназы в редких нейроэндокринных клетках мозга и кишечника». Журнал биологической химии. 269 (5): 3641–54. PMID 8106409.
- ^ Глойн А.Л. (ноябрь 2003 г.). «Мутации глюкокиназы (GCK) при гипер- и гипогликемии: диабет зрелого возраста у молодых, стойкий неонатальный диабет и гиперинсулинемия в младенчестве». Человеческая мутация. 22 (5): 353–62. Дои:10.1002 / humu.10277. PMID 14517946.
- ^ Карденас ML (1995). «Глюкокиназа»: ее регуляция и роль в метаболизме печени (подразделение молекулярной биологии). R G Landes. ISBN 1-57059-207-1.
Это наиболее подробное лечение глюкокиназы печени.
- ^ Арден С., Харботтл А., Балтруш С., Тидж М., Агиус Л. (сентябрь 2004 г.). «Глюкокиназа является неотъемлемым компонентом гранул инсулина в чувствительных к глюкозе секреторных клетках инсулина и не перемещается во время стимуляции глюкозой». Сахарный диабет. 53 (9): 2346–52. Дои:10.2337 / диабет.53.9.2346. PMID 15331544.
- ^ а б Šimčíková D, Kocková L, Vackářová K, Těšínský M, Heneberg P (август 2017 г.). «Доказательная адаптация подходов к биоинформатике для оптимизации методов, которые предсказывают эффекты несинонимичных аминокислотных замен в глюкокиназе». Научные отчеты. 7 (1): 9499. Дои:10.1038 / s41598-017-09810-0. ЧВК 5573313. PMID 28842611.
- ^ Коглан М., Лейтон Б. (февраль 2008 г.). «Активаторы глюкокиназы в лечении диабета». Заключение эксперта по исследуемым препаратам. 17 (2): 145–67. Дои:10.1517/13543784.17.2.145. PMID 18230050. S2CID 21028951.
- ^ Matschinsky FM (май 2009 г.). «Оценка потенциала активаторов глюкокиназы в терапии диабета». Обзоры природы. Открытие наркотиков. 8 (5): 399–416. Дои:10.1038 / nrd2850. PMID 19373249. S2CID 40490126.
- ^ Филипски К.Дж., Пфефферкорн Я.А. (август 2014 г.). «Патентный обзор активаторов глюкокиназы и разрушителей взаимодействия глюкокиназы и регуляторных белков глюкокиназы: 2011-2014». Экспертное заключение о терапевтических патентах. 24 (8): 875–91. Дои:10.1517/13543776.2014.918957. PMID 24821087. S2CID 39201131.
внешняя ссылка
- Glaser B (24 января 2013 г.). «Семейный гиперинсулинизм». GeneReviews. Сиэтл, Вашингтон: Вашингтонский университет, Сиэтл. PMID 20301549. NBK1375.
- Де Леон Д.Д., Стэнли, Калифорния (23 января 2014 г.). «Постоянный неонатальный сахарный диабет». В Adam MP, Ardinger HH, Pagon RA, et al. (ред.). GeneReview. Сиэтл, Вашингтон: Вашингтонский университет, Сиэтл. PMID 20301620. NBK1447.
внешняя ссылка
- Глюкокиназа в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)








