Молекулярная генетика - Molecular genetics
эта статья нужны дополнительные цитаты для проверка. (Январь 2012 г.) (Узнайте, как и когда удалить этот шаблон сообщения) |
| Часть набор на |
| Генетика |
|---|
 |
| Ключевые компоненты |
| История и темы |
| Исследование |
| Персонализированная медицина |
| Персонализированная медицина |
Молекулярная генетика - это подраздел биологии, изучающий, как различия в структурах или экспрессии молекул ДНК проявляются как различия между организмами. Молекулярная генетика часто применяет «исследовательский подход» для определения структуры и / или функции генов в геноме организма с использованием генетические экраны.[1][2] Область исследования основана на слиянии нескольких разделов биологии: классической Менделирующее наследование, клеточная биология, молекулярная биология, биохимия, и биотехнология. Исследователи ищут мутации в гене или вызывают мутации в гене, чтобы связать последовательность гена с определенным фенотипом. Молекулярная генетика - это мощная методология связи мутаций с генетическими состояниями, которая может помочь в поиске методов лечения различных генетических заболеваний.
История
Для того чтобы молекулярная генетика развивалась как дисциплина, потребовалось несколько научных открытий. Открытие ДНК как средства передачи генетического кода жизни от одной клетки к другой и от поколения к поколению имело важное значение для идентификации молекулы, ответственной за наследственность. Уотсон и Крик (в сочетании с Франклин и Уилкинс ) разобрался в структуре ДНК, краеугольный камень молекулярной генетики.[3] Изоляция эндонуклеаза рестрикции в Кишечная палочка Арбером и Линном в 1969 году открыли сферу генная инженерия.[4] Рестрикционные ферменты использовали для линеаризации ДНК для разделения с помощью электрофорез и Саузерн-блоттинг позволяет идентифицировать определенные сегменты ДНК через зонды гибридизации.[5][6] В 1971 году Берг использовал рестрикционные ферменты для создания первого рекомбинантная ДНК молекула и первая рекомбинантная ДНК плазмида.[7] В 1972 году Коэн и Бойер создали первый рекомбинантный ДНК-организм, вставив рекомбинантные ДНК-плазмиды в Кишечная палочка, теперь известный как бактериальная трансформация, и проложили путь к молекулярному клонированию.[8] Развитие Секвенирование ДНК техники в конце 1970-х, сначала Максамом и Гилбертом, а затем Фредерик Сэнгер, сыграла решающую роль в молекулярно-генетических исследованиях и позволила ученым начать проводить генетический скрининг, чтобы связать генотипические последовательности с фенотипами..[9] Полимеразной цепной реакции (ПЦР) с использованием полимеразы Taq, изобретенной Муллисом в 1985 году, позволила ученым создать миллионы копий определенной последовательности ДНК, которые можно было бы использовать для трансформации или манипулировать с помощью агарозный гель разделение.[10] Десять лет спустя был секвенирован первый полный геном (Haemophilus influenzae ) с последующим секвенированием генома человека через Проект "Геном человека" в 2001.[11] Кульминацией всех этих открытий стала новая область под названием геномика который связывает молекулярную структуру гена с белком или РНК, кодируемыми этим сегментом ДНК, и функциональную экспрессию этого белка в организме.[12] Сегодня, благодаря применению молекулярно-генетических методов, геномика изучается на многих модельных организмах, и данные собираются в компьютерных базах данных, таких как NCBI и Ансамбль. Компьютерный анализ и сравнение генов внутри и между разными видами называется биоинформатика, и связывает генетические мутации в эволюционном масштабе.[13]
Центральная догма
На этом изображении показан пример центральной догмы с использованием транскрибируемой, а затем транслируемой цепи ДНК и показаны важные ферменты, используемые в процессах.
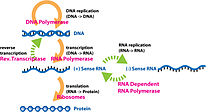
В Центральная догма является основой всей генетики и играет ключевую роль в изучении молекулярной генетики. Центральная догма гласит, что ДНК реплицируется, ДНК транскрибируется в РНК, а РНК транслируется в белки.[14]. Наряду с Центральной Догмой, генетический код используется для понимания того, как РНК транслируется в белки. Репликация ДНК и транскрипция с ДНК на мРНК происходит в митохондрии в то время как трансляция с РНК на белки происходит в рибосома[15]. Генетический код состоит из четырех пар оснований: аденина, цитозина, урацила и гуанина и является избыточным, что означает, что несколько комбинаций этих пар оснований (которые считываются в трех экземплярах) производят одну и ту же аминокислоту.[16]. Протеомика и геномика области биологии, возникшие в результате изучения молекулярной генетики и центральной догмы[17].
Методы
Прогрессивная генетика
Прогрессивная генетика это метод молекулярной генетики, используемый для идентификации генов или генетических мутаций, которые вызывают определенные фенотип. В генетический скрининг, случайные мутации генерируются с мутагены (химические вещества или радиация) или транспозоны и люди проходят скрининг на определенный фенотип. Часто может последовать вторичный анализ в форме отбора. мутагенез где желаемый фенотип трудно наблюдать, например, в бактериях или культурах клеток. Ячейки могут быть преобразованный используя ген для устойчивость к антибиотикам или флуоресцентный репортер так что мутанты с желаемым фенотипом выбираются из немутантов.[18]
Мутанты, проявляющие интересующий фенотип, изолированы и проверка дополнения может быть выполнено, чтобы определить, является ли фенотип результатом более чем одного гена. Затем мутантные гены характеризуются как доминирующий (что приводит к увеличению функциональности), рецессивный (показывая потерю функции), или эпистатический (мутантный ген маскирует фенотип другого гена). Наконец, местоположение и конкретный характер мутации отображаются с помощью последовательность действий.[19] Прямая генетика - это беспристрастный подход, который часто приводит ко многим неожиданным открытиям, но может быть дорогостоящим и отнимать много времени. Модельные организмы, такие как червь нематода Caenorhabditis elegans плодовая муха Drosophila melanogaster, и данио Данио Рерио были успешно использованы для изучения фенотипов, возникающих в результате генных мутаций.[20]

Обратная генетика
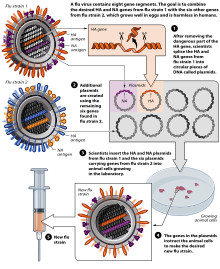
Обратная генетика - это термин для методов молекулярной генетики, используемых для определения фенотипа в результате преднамеренной мутации в интересующем гене. Фенотип используется для определения функции немутантной версии гена. Мутации могут быть случайными или преднамеренными изменениями интересующего гена. Мутации могут быть неверно воспринимаемая мутация вызванный заменой нуклеотида, добавлением или удалением нуклеотида, чтобы вызвать мутация сдвига рамки или полное добавление / удаление гена или генного сегмента. Удаление определенного гена создает нокаут гена где ген не экспрессируется и приводит к потере функции (например, нокаутные мыши ). Мутации, связанные с неправильным восприятием, могут вызвать полную потерю функции или привести к частичной потере функции, известной как нокдаун. Нокдаун также может быть достигнут РНК-интерференция (РНКи).[22] В качестве альтернативы гены могут быть заменены в геном организма (также известный как трансген ) для создания генная нокаутация и приводит к увеличению функциональности хоста.[23] Хотя эти методы имеют некоторую врожденную предвзятость в отношении решения связать фенотип с конкретной функцией, они намного быстрее с точки зрения производства, чем прямая генетика, потому что интересующий ген уже известен.
Смотрите также
- Комплементация (генетика)
- Повреждение ДНК (естественное)
- Теория повреждений ДНК старения
- Эпигенетика
- Картирование генов
- Генетический код
- Генетическая рекомбинация
- Геномный импринтинг
- История генетики
- Гомологичная рекомбинация
- Мутагенез
- Регулирование экспрессии генов
- Хронология истории генетики
- Трансформация (генетика)
Источники и примечания
- ^ Уотерс, Кен (2013), «Молекулярная генетика», в Залте, Эдвард Н. (ред.), Стэнфордская энциклопедия философии (Издание осень 2013 г.), Исследовательская лаборатория метафизики, Стэнфордский университет., получено 2019-10-07
- ^ Альбертс, Брюс (18 ноября 2014 г.). Молекулярная биология клетки (Шестое изд.). Нью-Йорк, штат Нью-Йорк. ISBN 9780815344322. OCLC 887605755.
- ^ Тобин, Мартин Дж. (15 апреля 2003 г.). «25 апреля 1953 года». Американский журнал респираторной медицины и реанимации. 167 (8): 1047–1049. Дои:10.1164 / rccm.2302011. ISSN 1073-449X. PMID 12684243.
- ^ "Обзор рестрикционных ферментов | Изучение науки в Scitable". www.nature.com. Получено 2019-10-07.
- ^ Ригетти, Пьер Джорджио (24 июня 2005 г.). «Электрофорез: марш грошей, марш грошей». Журнал хроматографии А. 1079 (1–2): 24–40. Дои:10.1016 / j.chroma.2005.01.018. PMID 16038288.
- ^ "Саузерн-блоттинг | Центр обучения MyBioSource". Получено 2019-11-11.
- ^ "Профессор Пол Берг | Биографическое резюме". WhatisBiotechnology.org. Получено 2019-10-07.
- ^ "Герберт В. Бойер и Стэнли Н. Коэн". Институт истории науки. 2016-06-01. Получено 2019-10-07.
- ^ «Секвенирование ДНК | генетика». Энциклопедия Британника. Получено 2019-10-07.
- ^ «Изобретение ПЦР». Bitesize Bio. 2007-10-24. Получено 2019-10-07.
- ^ «Хронология: организмы, чей геном секвенирован». твой геном. Получено 2019-10-07.
- ^ "Что такое геномика?". EMBL-EBI Поезд онлайн. 2011-09-09. Получено 2019-10-07.
- ^ «Что такое биоинформатика? Предлагаемое определение и обзор области». Методы информации в медицине. 40 (2). 2001. Дои:10.1055 / с-008-38405. ISSN 0026-1270.
- ^ "Центральная догма | Протокол". www.jove.com. Получено 2020-12-04.
- ^ «Транскрипция, перевод и тиражирование». www.atdbio.com. Получено 2020-12-04.
- ^ "Генетический код". Genome.gov. Получено 2020-12-04.
- ^ «Краткое руководство по геномике». Genome.gov. Получено 2020-12-04.
- ^ «Отбор или просмотр в направленной эволюции», Направленная эволюция селективных ферментов, John Wiley & Sons, Ltd, 2016 г., стр. 27–57, Дои:10.1002 / 9783527655465.ch2, ISBN 978-3-527-65546-5
- ^ Шнеебергер, Корбинян (20 августа 2014 г.). «Использование секвенирования следующего поколения для изоляции мутантных генов от прямого генетического скрининга». Природа Обзоры Генетика. 15 (10): 662–676. Дои:10.1038 / nrg3745. ISSN 1471-0056. PMID 25139187. S2CID 1822657.
- ^ Лоусон, Натан Д .; Вулф, Скотт А. (19 июля 2011 г.). «Прямые и обратные генетические подходы к анализу развития позвоночных у рыбок данио». Клетка развития. 21 (1): 48–64. Дои:10.1016 / j.devcel.2011.06.007. ISSN 1534-5807. PMID 21763608.
- ^ Кучер, Лена М. (2014). «Прямой и обратный мутагенез у C. elegans». WormBook: 1–26. Дои:10.1895 / wormbook.1.167.1. ЧВК 4078664. PMID 24449699.
- ^ Харди, Серж; Леганьё, Винсент; Аудик, Янн; Пайлард, Люк (октябрь 2010 г.). «Обратная генетика у эукариот». Биология клетки. 102 (10): 561–580. Дои:10.1042 / BC20100038. ЧВК 3017359. PMID 20812916.
- ^ Дойл, Альфред; МакГарри, Майкл П .; Ли, Нэнси А .; Ли, Джеймс Дж. (Апрель 2012 г.). «Создание трансгенных и нокаутных / нокаутных по генам мышей моделей болезней человека». Трансгенные исследования. 21 (2): 327–349. Дои:10.1007 / s11248-011-9537-3. ISSN 0962-8819. ЧВК 3516403. PMID 21800101.
дальнейшее чтение
- Сайты и базы данных по генетике, цитогенетике и онкологии, в Атлас генетики и цитогенетики в онкологии и гематологии
- Джереми В. Дейл и Саймон Ф. Парк. 2010. Молекулярная генетика бактерий, 5-е издание. ISBN 978-0470741849
внешние ссылки
 СМИ, связанные с Молекулярная генетика в Wikimedia Commons
СМИ, связанные с Молекулярная генетика в Wikimedia Commons- NCBI: https://www.ncbi.nlm.nih.gov/About/primer/genetics_molecular.html
