Фагосома - Phagosome
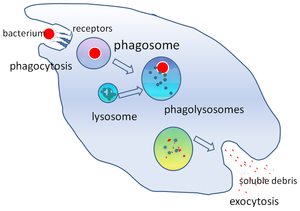
В клеточная биология, а фагосома это везикул формируется вокруг частицы, охваченной фагоцит через фагоцитоз. К профессиональным фагоцитам относятся: макрофаги, нейтрофилы, и дендритные клетки (DC). Фагосома образуется путем слияния клеточная мембрана вокруг микроорганизм, а стареющая клетка или апоптотическая клетка. Фагосомы имеют мембраносвязанные белки набирать и сливаться с лизосомы сформировать зрелый фаголизосомы. Лизосомы содержат гидролитические ферменты и активные формы кислорода (ROS), которые убивают и переваривают патогены. Фагосомы также могут образовываться в непрофессиональных фагоцитах, но они могут охватывать только меньший диапазон частиц и не содержат АФК. Полезные материалы (например, аминокислоты ) из переваренных частиц перемещаются в цитозоль, а отходы удаляются экзоцитоз. Формирование фагосом имеет решающее значение для гомеостаза тканей и как врожденной, так и адаптивной защиты хозяина от патогенов.
Однако некоторые бактерии может использовать фагоцитоз в качестве стратегии вторжения. Они либо воспроизводятся внутри фаголизосомы. (например. Coxiella виды)[1] или сбежать в цитоплазма до того, как фагосома сливается с лизосомой (например, Риккетсия виды).[2]Многие микобактерии, в том числе Микобактерии туберкулеза[3][4]и Mycobacterium avium paratuberculosis,[5] может манипулировать хозяином макрофаг для предотвращения слияния лизосом с фагосомами и создания зрелых фаголизосом. Такое неполное созревание фагосомы поддерживает среду, благоприятную для патогенов внутри нее.[6]
Формирование
Фагосомы достаточно велики, чтобы разлагать целые бактерии или апоптотический и стареющие клетки, которые обычно имеют диаметр> 0,5 мкм.[7] Это означает, что фагосома на несколько порядков больше, чем эндосома, который измеряется в нанометры.
Фагосомы образуются, когда патогены или опсонины связываются с трансмембранными рецепторами, которые случайным образом распределены на поверхности фагоцитов. При связывании срабатывает сигнализация "снаружи-внутрь" актин полимеризация и псевдоподия образование, которое окружает и сливается с микроорганизмом. Протеинкиназа C, фосфоинозитид-3-киназа, и фосфолипаза C (PLC) необходимы для сигнализации и управления интернализацией частиц.[8] Больше рецепторов клеточной поверхности может связываться с частицей по механизму, похожему на застежку-молнию, когда патоген окружен, увеличивая связывание жадность.[9] Рецептор Fc (FcR), рецепторы комплемента (CR), рецептор маннозы и Dectin-1 являются фагоцитарными рецепторами, что означает, что они могут вызывать фагоцитоз, если они экспрессируются в нефагоцитарных клетках, таких как фибробласты.[10] Другие белки, такие как Толл-подобные рецепторы участвуют в распознавании паттернов патогенов и часто задействуются в фагосомах, но не вызывают специфического запуска фагоцитоза в нефагоцитарных клетках, поэтому они не считаются фагоцитарными рецепторами.
Опсонизация
Опсонины - это молекулярные метки, такие как антитела и дополняет которые прикрепляются к патогенам и регулируют фагоцитоз. Иммуноглобулин G (IgG) является основным типом антител, присутствующих в сыворотка. Это часть адаптивная иммунная система, но он ссылается на врожденный ответ путем привлечения макрофагов к фагоцитозу патогенов. Антитело связывается с микробами с переменной Fab домен, и домен Fc связывается с рецепторами Fc (FcR), чтобы вызвать фагоцитоз.
Комплемент-опосредованная интернализация имеет гораздо менее значительные мембранные выступы, но нижестоящая передача сигналов обоих путей сходится, чтобы активировать Rho GTPases.[11] Они контролируют полимеризацию актина, которая необходима для слияния фагосомы с эндосомами и лизосомами.
Нефагоцитарные клетки
Другие непрофессиональные фагоциты обладают некоторой степенью фагоцитарной активности, например, эпителиальные клетки щитовидной железы и мочевого пузыря, которые могут поглощать эритроциты, и эпителиальные клетки сетчатки, которые усваивают стержни сетчатки.[7] Однако непрофессиональные фагоциты не экспрессируют специфические фагоцитарные рецепторы, такие как FcR, и имеют гораздо более низкую скорость интернализации.
Некоторые инвазивные бактерии также могут вызывать фагоцитоз в нефагоцитарных клетках, чтобы опосредовать захват организма хозяином. Например, Шигелла может секретировать токсины, которые изменяют цитоскелет хозяина и проникают в базолатеральную сторону энтероциты.[12]
Структура
Поскольку мембрана фагосомы образована путем слияния плазматической мембраны, основной состав фосфолипидный бислой та же. Затем эндосомы и лизосомы сливаются с фагосомой, чтобы внести свой вклад в мембрану, особенно когда поглощенная частица очень большая, например, паразит.[13] Они также доставляют различные мембранные белки в фагосому и модифицируют структуру органелл.
Фагосомы могут поглощать искусственные малоплотные латекс бусинки, а затем очищены сахароза градиент концентрации, позволяющий изучить структуру и состав.[14] Процесс созревания также можно охарактеризовать путем очистки фагосом в разные моменты времени. Ранние фагосомы характеризуются Rab5, который переходит в Rab7 по мере созревания пузырьков в поздние фагосомы.
Процесс созревания
Возникающая фагосома по своей природе не является бактерицидной. По мере созревания он становится более кислым от pH 6,5 до pH 4 и приобретает характерные белковые маркеры и гидролитические ферменты. Различные ферменты действуют при различных оптимальных значениях pH, образуя диапазон, поэтому каждый из них работает на узких стадиях процесса созревания. Активность ферментов можно точно настроить, изменив уровень pH, что обеспечивает большую гибкость. Фагосома движется микротрубочки из цитоскелет, сливаясь с эндосомами и лизосомами последовательно в динамическом "поцелуй и беги" манера.[15] Этот внутриклеточный транспорт зависит от размера фагосом. Органеллы большего размера (диаметром около 3 мкм) очень устойчиво транспортируются от периферии клетки к перинуклеарной области, тогда как органеллы меньшего размера (диаметром около 1 мкм) перемещаются более двунаправленно взад и вперед между центром клетки и периферией клетки.[16] Вакуолярные протонные насосы (v-АТФаза) доставляются к фагосомам для подкисления компартмента органелл, создавая более враждебную среду для патогенов и облегчая деградацию белка. Бактериальные белки денатурируются при низком pH и становятся более доступными для протеаз, на которые не влияет кислая среда. Позднее ферменты рециркулируются из фаголизосомы перед перевариванием, поэтому они не теряются. Состав фосфолипидной мембраны также изменяется по мере созревания фагосомы.[14]
Слияние может занять от нескольких минут до часов в зависимости от содержимого фагосомы; Слияние, опосредованное FcR или рецептором маннозы, длится менее 30 минут, но фагосомам, содержащим латексные шарики, может потребоваться несколько часов для слияния с лизосомами.[7] Предполагается, что состав фагосомной мембраны влияет на скорость созревания. Микобактерии туберкулеза имеет очень гидрофобный клеточная стенка, который, как предполагается, предотвращает рециклинг мембран и рекрутирование факторов слияния, поэтому фагосома не сливается с лизосомами, и бактерия избегает деградации.[17]
Молекулы меньшего размера в просвете переносятся путем слияния быстрее, чем молекулы большего размера, что предполагает образование небольшого водного канала между фагосомой и другими пузырьками во время «поцелуя и бегства», через который допускается только ограниченный обмен.[7]
Регулирование термоядерного синтеза
Вскоре после интернализации F-актин деполимеризуется из новообразованной фагосомы, поэтому он становится доступным для эндосом для слияния и доставки белков.[7] Процесс созревания делится на раннюю и позднюю стадии в зависимости от характерных белковых маркеров, регулируемых малыми Rab GTPases. Rab5 присутствует на ранних фагосомах и контролирует переход к поздним фагосомам, маркированным Rab7.[18]
Rab5 привлекает киназу PI-3 и другие связывающие белки, такие как Vps34, на мембрану фагосомы, поэтому эндосомы могут доставлять белки к фагосоме. Rab5 частично участвует в переходе к Rab7 через комплекс CORVET и комплекс HOPS у дрожжей.[18] Точный путь созревания у млекопитающих не совсем понятен, но предполагается, что HOPS может связывать Rab7 и вытеснять ингибитор диссоциации гуанозиновых нуклеотидов (GDI).[19] Rab11 участвует в переработке мембран.[20]
Фаголизосома
Фагосома сливается с лизосомами с образованием фаголизосомы, которая обладает различными бактерицидными свойствами. Фаголизосома содержит реактивный кислород и азотные виды (ROS и RNS) и гидролитические ферменты. Компартмент также является кислым из-за протонных насосов (v-АТФаз), которые транспортируют H+ через мембрану, используемую для денатурации бактериальных белков.
Точные свойства фаголизосом варьируются в зависимости от типа фагоцита. Те, что находятся в дендритных клетках, обладают более слабыми бактерицидными свойствами, чем те, что находятся в макрофагах и нейтрофилах. Также макрофаги делятся на провоспалительные «киллеры» M1 и «ремонтные» M2. Фаголизосомы M1 могут метаболизировать аргинин в высокореактивный оксид азота, в то время как M2 использует аргинин для производства орнитин для ускорения пролиферации клеток и восстановления тканей.[21]
Функция
Распад патогенов
Макрофаги и нейтрофилы - это профессиональные фагоциты, отвечающие за большую часть деградации патогенов, но они имеют разные бактерицидные методы. Нейтрофилы имеют гранулы, которые сливаются с фагосомой. Гранулы содержат НАДФН оксидаза и миелопероксидаза, которые производят токсичные производные кислорода и хлора для уничтожения патогенов в окислительный взрыв. Протеазы и антимикробные пептиды также попадают в фаголизосомы. Макрофаги не имеют гранул и больше полагаются на закисление фаголизосом, гликозидазы, и протеазы для переваривания микробов.[20] Фагосомы в дендритных клетках менее кислые и обладают гораздо более слабой гидролитической активностью из-за более низкой концентрации лизосомных протеаз и даже наличия ингибиторов протеаз.
Воспаление
Формирование фагосом связано с воспаление через общие сигнальные молекулы. Киназа PI-3 и PLC участвуют как в механизме интернализации, так и в запуске воспаления.[8] Эти два белка, наряду с Rho GTPases, являются важными компонентами врожденного иммунного ответа, вызывая цитокин производство и активация MAP киназа сигнальный каскад. Провоспалительные цитокины, включая ИЛ-1β, Ил-6, TNFα, и Ил-12 все производятся.[7]
Этот процесс жестко регулируется, а воспалительная реакция зависит от типа частицы внутри фагосомы. Апоптотические клетки, инфицированные патогеном, вызывают воспаление, но поврежденные клетки, которые деградируют как часть нормального тканевого обмена, не вызывают. Ответ также различается в зависимости от опсонин-опосредованного фагоцитоза. FcR и реакции, опосредованные рецептором маннозы, продуцируют провоспалительные активные формы кислорода и арахидоновая кислота молекул, но реакции, опосредованные CR, не приводят к этим продуктам.[7]
Презентация антигена
Незрелые дендритные клетки (ДК) могут фагоцитозировать, но зрелые ДК не могут из-за изменений в Rho GTPases, участвующих в ремоделировании цитоскелета.[20] Фагосомы ДК менее гидролитичны и кислые, чем фагосомы макрофагов и нейтрофилов, поскольку ДК в основном участвуют в презентация антигена а не деградация патогенов. Они должны удерживать фрагменты белка подходящего размера для специфического распознавания бактериями, поэтому пептиды разлагаются лишь частично.[20] Пептиды из бактерий попадают в Главный комплекс гистосовместимости (MHC). Пептидные антигены представлены лимфоциты, где они привязаны к Рецепторы Т-клеток и активирует Т-клетки, преодолевая разрыв между врожденным и адаптивным иммунитетом.[8] Это характерно для млекопитающие, птицы, и челюстная рыба, как насекомые не обладают адаптивным иммунитетом.[22]

Питательный
Древние одноклеточные организмы, такие как амеба использовать фагоцитоз как способ приобретения питательных веществ, а не как иммунную стратегию. Они поглощают другие более мелкие микробы и переваривают их внутри фагосомы со скоростью около одной бактерии в минуту, что намного быстрее, чем профессиональные фагоциты.[23] Для почвенной амебы Dictyostelium discoideum, их основной источник пищи - бактерии Легионелла пневмофила, что приводит к болезнь легионеров в людях.[24] Созревание фагосом у амебы очень похоже на созревание макрофагов, поэтому они используются в качестве модельного организма для изучения этого процесса.[15]
Очистка тканей
Фагосомы разрушают стареющие клетки и апоптотические клетки для поддержания тканевого гомеостаза. Эритроциты имеют одну из самых высоких скоростей оборота в организме, и они фагоцитируются макрофагами в печень и селезенка. в эмбрион, процесс удаления мертвых клеток недостаточно изучен, но он не выполняется макрофагами или другими клетками, происходящими из гемопоэтические стволовые клетки.[25] Только у взрослого человека апоптотические клетки фагоцитируются профессиональными фагоцитами. Воспаление вызывается только определенными возбудитель- или же молекулярные паттерны, связанные с повреждениями (PAMPs или DAMPs) удаление стареющих клеток не вызывает воспаления.[13]
Аутофагосома
Аутофагосомы отличаются от фагосом тем, что они в основном используются для избирательной деградации поврежденных цитозольных органелл, таких как митохондрии (митофагия ). Однако, когда клетка голодает или испытывает стресс, аутофагосомы также могут неизбирательно разрушать органеллы, чтобы обеспечить клетку аминокислотами и другими питательными веществами.[26] Аутофагия не ограничивается профессиональными фагоцитами, она впервые обнаружена у крыс. гепатоциты от клеточного биолога Кристиан де Дюв.[27] Аутофагосомы имеют двойную мембрану, внутреннюю из охваченной органеллы, а внешняя мембрана предположительно образована из эндоплазматический ретикулум или Промежуточное отделение ЭР-Гольджи (ERGIC).[28] Аутофагосома также сливается с лизосомами для разрушения своего содержимого. Когда М. туберкулез подавляют закисление фагосом, Интерферон гамма может вызвать аутофагию и спасти процесс созревания.[29]
Бактериальное уклонение и манипуляции
Многие бактерии эволюционировали, чтобы уклониться от бактерицидных свойств фагосом или даже использовать фагоцитоз в качестве стратегии инвазии.
- Микобактерии туберкулеза нацелены на макрофаги M2 в нижних отделах дыхательного пути, которые не производят АФК.[30] М. туберкулез могут также манипулировать сигнальными путями, секретируя фосфатазы, такие как PtpA и SapM, которые нарушают рекрутирование белка и блокируют закисление фагосом.[7][31]
- Легионелла пневмофила может реконструировать мембрану фагосомы, чтобы имитировать везикулы в других частях секреторного пути, поэтому лизосомы не распознают фагосомы и не сливаются с ней. Бактерия выделяет токсины, которые мешают передаче хозяина, поэтому Легионелла-содержащая вакуоль привлекает мембранные белки, обычно обнаруживаемые в эндоплазматическом ретикулуме или ERGIC.[32] Это перенаправляет секреторные везикулы к модифицированной фагосоме и доставляет питательные вещества к бактерии.
- Listeria monocytogenes выделяет порообразующий белок листериолизин О так бактерия может покинуть фагосому и попасть в цитозоль. Листериолизин активируется кислой средой фагосомы.[33] Кроме того, Листерия секретируют два фермента фосфолипазы C, которые способствуют ускользанию от фагосом.
Смотрите также
Рекомендации
- ^ Hackstadt T, Williams JC (май 1981 г.). «Биохимическая стратагема облигатного паразитирования эукариотических клеток Coxiella burnetii». Труды Национальной академии наук Соединенных Штатов Америки. 78 (5): 3240–4. Дои:10.1073 / пнас.78.5.3240. ЧВК 319537. PMID 6942430.
- ^ Винклер HH (1990). «Виды риккетсий (как организмы)». Ежегодный обзор микробиологии. 44: 131–153. Дои:10.1146 / annurev.micro.44.1.131.
- ^ Макмикинг Дж. Д., Тейлор Г. А., Маккинни Дж. Д. (октябрь 2003 г.). «Иммунный контроль туберкулеза с помощью IFN-гамма-индуцибельного LRG-47». Наука. 302 (5645): 654–9. Bibcode:2003Наука ... 302..654М. Дои:10.1126 / science.1088063. PMID 14576437.
- ^ Vandal OH, Pierini LM, Schnappinger D, Nathan CF, Ehrt S (август 2008 г.). «Мембранный белок сохраняет внутрибактериальный pH при внутрифагосомных микобактериях туберкулеза». Природа Медицина. 14 (8): 849–54. Дои:10,1038 / нм.1795. ЧВК 2538620. PMID 18641659.
- ^ Kuehnel MP, Goethe R, Habermann A, Mueller E, Rohde M, Griffiths G, Valentin-Weigand P (август 2001 г.). «Характеристика внутриклеточной выживаемости Mycobacterium avium ssp. Paratuberculosis: фагосомный pH и фузогенность в макрофагах J774 по сравнению с другими микобактериями». Клеточная микробиология. 3 (8): 551–66. Дои:10.1046 / j.1462-5822.2001.00139.x. PMID 11488816.
- ^ Тессема MZ, Koets AP, Rutten VP, Gruys E (ноябрь 2001 г.). «Как Mycobacterium avium subsp. Paratuberculosis противостоит внутриклеточной деградации?». Ветеринарный квартал. 23 (4): 153–62. Дои:10.1080/01652176.2001.9695105. PMID 11765232.
- ^ а б c d е ж грамм час Адерем А., Андерхилл DM (апрель 1999 г.). «Механизмы фагоцитоза в макрофагах». Ежегодный обзор иммунологии. 17 (1): 593–623. Дои:10.1146 / annurev.immunol.17.1.593. PMID 10358769.
- ^ а б c Адерем А (июнь 2003 г.). «Фагоцитоз и воспалительная реакция». Журнал инфекционных болезней. 187 Приложение 2 (s2): S340-5. Дои:10.1086/374747. PMID 12792849.
- ^ Дюпюи А.Г., Карон Э. (июнь 2008 г.). «Интегрин-зависимый фагоцитоз: переход от микроадгезии к новым концепциям». Журнал клеточной науки. 121 (11): 1773–83. Дои:10.1242 / jcs.018036. PMID 18492791.
- ^ Андерхилл Д.М., Озинский А. (апрель 2002 г.). «Фагоцитоз микробов: сложность в действии». Ежегодный обзор иммунологии. 20 (1): 825–52. Дои:10.1146 / annurev.immunol.20.103001.114744. PMID 11861619.
- ^ Каплан Г. (август 1977 г.). «Различия в режиме фагоцитоза с рецепторами Fc и C3 в макрофагах». Скандинавский журнал иммунологии. 6 (8): 797–807. Дои:10.1111 / j.1365-3083.1977.tb02153.x. PMID 561436.
- ^ Келер Х., Родригес С.П., Маккормик Б.А. (март 2002 г.). «Взаимодействие Shigella flexneri с базолатеральным мембранным доменом поляризованного модельного эпителия кишечника: роль липополисахарида в клеточной инвазии и в активации митоген-активированной протеинкиназы ERK». Инфекция и иммунитет. 70 (3): 1150–8. Дои:10.1128 / IAI.70.3.1150-1158.2002. ЧВК 127798. PMID 11854195.
- ^ а б Дежарден М., Хоуд М., Ганьон Э (октябрь 2005 г.). «Фагоцитоз: запутанный путь от питания к адаптивному иммунитету». Иммунологические обзоры. 207 (1): 158–65. Дои:10.1111 / j.0105-2896.2005.00319.x. PMID 16181334.
- ^ а б Дежарден М., Селис Дж. Э., ван Меер Дж., Диплингер Х., Джараус А., Гриффитс Дж., Хубер Л. А. (декабрь 1994 г.). «Молекулярная характеристика фагосом». Журнал биологической химии. 269 (51): 32194–200. PMID 7798218.
- ^ а б Gotthardt D, Warnatz HJ, Henschel O, Brückert F, Schleicher M, Soldati T (октябрь 2002 г.). «Рассечение процесса созревания фагосом с высоким разрешением позволяет выявить различные фазы мембранного переноса». Молекулярная биология клетки. 13 (10): 3508–20. Дои:10.1091 / mbc.E02-04-0206. ЧВК 129962. PMID 12388753.
- ^ Келлер С., Бергхофф К., Кресс Х (декабрь 2017 г.). «Фагосомный транспорт сильно зависит от размера фагосом». Научные отчеты. 7 (1): 17068. Bibcode:2017НатСР ... 717068K. Дои:10.1038 / s41598-017-17183-7. ЧВК 5719076. PMID 29213131.
- ^ де Шастелье С., Тило Л. (сентябрь 1997 г.). «Созревание фагосом и слияние с лизосомами в зависимости от свойств поверхности и размера фагоцитарной частицы». Европейский журнал клеточной биологии. 74 (1): 49–62. PMID 9309390.
- ^ а б Fairn GD, Grinstein S (август 2012 г.). «Как зарождающиеся фагосомы созревают, чтобы стать фаголизосомами». Тенденции в иммунологии. 33 (8): 397–405. Дои:10.1016 / j.it.2012.03.003. PMID 22560866.
- ^ Кинчен Дж. М., Равичандран К. С. (апрель 2010 г.). «Идентификация двух эволюционно консервативных генов, регулирующих процессинг поглощенных апоптотических клеток». Природа. 464 (7289): 778–82. Bibcode:2010Натура.464..778K. Дои:10.1038 / природа08853. ЧВК 2901565. PMID 20305638.
- ^ а б c d Савина А, Амигорена С (октябрь 2007 г.). «Фагоцитоз и презентация антигенов в дендритных клетках». Иммунологические обзоры. 219 (1): 143–56. Дои:10.1111 / j.1600-065X.2007.00552.x. PMID 17850487.
- ^ Компакт-диск Миллса (5 мая 2015 г.). «Анатомия открытия: макрофаги m1 и m2». Границы иммунологии. 6: 212. Дои:10.3389 / fimmu.2015.00212. ЧВК 4419847. PMID 25999950.
- ^ Варр GW (1997). «Адаптивная иммунная система рыб». Развитие биологической стандартизации. 90: 15–21. PMID 9270830.
- ^ Коссон П., Солдати Т. (июнь 2008 г.). «Ешь, убей или умри: когда амеба встречается с бактериями». Текущее мнение в микробиологии. 11 (3): 271–6. Дои:10.1016 / j.mib.2008.05.005. PMID 18550419.
- ^ Соломон Дж. М., Руппер А., Карделли Дж. А., Исберг Р. Р. (май 2000 г.). «Внутриклеточный рост Legionella pneumophila в Dictyostelium discoideum, системе для генетического анализа взаимодействий хозяин-патоген». Инфекция и иммунитет. 68 (5): 2939–47. Дои:10.1128 / iai.68.5.2939-2947.2000. ЧВК 97507. PMID 10768992.
- ^ Личанская AM, Хьюм Д.А. (июнь 2000 г.). «Происхождение и функции фагоцитов эмбриона» (PDF). Экспериментальная гематология. 28 (6): 601–11. Дои:10.1016 / s0301-472x (00) 00157-0. PMID 10880746.
- ^ Ding WX, Yin XM (июль 2012 г.). «Митофагия: механизмы, патофизиологические роли и анализ». Биологическая химия. 393 (7): 547–64. Дои:10.1515 / hsz-2012-0119. ЧВК 3630798. PMID 22944659.
- ^ Кастро-Обрегон С (2010). «Открытие лизосом и аутофагии». Природное образование. 3 (9): 49.
- ^ Ge L, Schekman R (январь 2014 г.). «Промежуточный отсек ER-Golgi питает фагофорную мембрану». Аутофагия. 10 (1): 170–2. Дои:10.4161 / авто.26787. ЧВК 4389871. PMID 24220263.
- ^ Гутьеррес М.Г., Мастер СС, Сингх С.Б., Тейлор Г.А., Коломбо М.И., Деретич В. (декабрь 2004 г.). «Аутофагия - это защитный механизм, ингибирующий выживаемость БЦЖ и Mycobacterium tuberculosis в инфицированных макрофагах». Клетка. 119 (6): 753–66. Дои:10.1016 / j.cell.2004.11.038. PMID 15607973.
- ^ Cambier CJ, Takaki KK, Larson RP, Hernandez RE, Tobin DM, Urdahl KB, Cosma CL, Ramakrishnan L (январь 2014 г.). «Микобактерии манипулируют набором макрофагов за счет скоординированного использования мембранных липидов». Природа. 505 (7482): 218–22. Дои:10.1038 / природа12799. ЧВК 3961847. PMID 24336213.
- ^ Вонг Д., Чао Дж. Д., Ав-Гей Y (февраль 2013 г.). «Фосфатазы, секретируемые Mycobacterium tuberculosis: от патогенеза к мишеням для разработки противотуберкулезных препаратов». Тенденции в микробиологии. 21 (2): 100–9. Дои:10.1016 / j.tim.2012.09.002. PMID 23084287.
- ^ Рой С.Р., Каган Дж.С. (1 января 2013 г.). Уклонение от слияния лизосом фагосом и создание репликативной органеллы внутриклеточным патогеном Legionella pneumophila. Landes Bioscience.
- ^ Портной Д.А., Ауэрбух В., Гломски И.Ю. (август 2002 г.). «Клеточная биология инфекции Listeria monocytogenes: пересечение бактериального патогенеза и клеточного иммунитета». Журнал клеточной биологии. 158 (3): 409–14. Дои:10.1083 / jcb.200205009. ЧВК 2173830. PMID 12163465.
