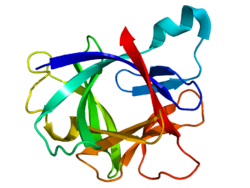
Интерлейкин 1 бета - Interleukin 1 beta
Интерлейкин 1 бета (ИЛ-1β) также известный как лейкоцитарный пироген, лейкоцитарный эндогенный медиатор, фактор мононуклеарных клеток, фактор активации лимфоцитов и другие имена, это цитокин белок что у людей кодируется IL1B ген.[5][6][7][8] Есть два гена интерлейкин-1 (Ил-1): ИЛ-1 альфа и ИЛ-1 бета (этот ген). Предшественник IL-1β расщепляется цитозольным каспаза 1 (интерлейкин 1 бета конвертаза) с образованием зрелого IL-1β.
Функция
Лихорадочное свойство лейкоцитов человека пироген (интерлейкин 1) был очищен Динарелло в 1977 г. (PNAS) с удельной активностью 10–20 нанограмм / кг. В 1979 году Динарелло сообщил, что очищенный лейкоцитарный пироген человека представляет собой ту же молекулу, которая была описана Игалом Гери в 1972 году.[9][10][11] Он назвал его фактором активации лимфоцитов (LAF), потому что это митоген лимфоцитов. Лишь в 1984 году было обнаружено, что интерлейкин 1 состоит из двух разных белков, которые теперь называются интерлейкин-1 альфа и интерлейкин-1 бета.[6]
IL-1β входит в состав интерлейкинов 1 семейства из цитокины. Этот цитокин вырабатывается активированными макрофагами в виде пропротеина, который протеолитически перерабатывается до активной формы посредством каспаза 1 (CASP1 / ICE). Этот цитокин является важным медиатором воспалительная реакция, и участвует в различных клеточных действиях, включая пролиферацию, дифференцировку и апоптоз. Индукция циклооксигеназа-2 (PTGS2 / COX2) этим цитокином в Центральная нервная система (ЦНС) способствует воспалительному боль гиперчувствительность. Этот ген и восемь других генов семейства интерлейкинов 1 образуют кластер генов цитокинов на хромосома 2.[12]
IL-1β в сочетании с IL-23 индуцировал экспрессию IL-17, IL-21 и IL-22 клетками γδT. Эта индукция экспрессии происходит при отсутствии дополнительных сигналов. Это свидетельствует о том, что IL-1β участвует в модуляции аутоиммунного воспаления. [13]
Описан различный комплекс инфламмасом - цитозольный молекулярный комплекс. Инфламмасома распознает сигналы опасности и активирует провоспалительный процесс и выработку IL-1β и IL-18. Инфламмасома типа NLRP3 (содержит три домена: пириновый домен, нуклеотид-связывающий домен и лейцин-богатый повтор) активируется различными стимулами, и зарегистрировано несколько заболеваний, связанных с активацией NLRP3, таких как сахарный диабет 2 типа , Болезнь Альцгеймера, ожирение и атеросклероз.[14]
Характеристики
Молекулярная масса протеолитически процессированного IL-1β составляет 17,5 кДа.IL-1β имеет следующую аминокислотную последовательность:
- APVRSLNCTL RDSQQKSLVM SGPYELKALH LQGQDMEQQV VFSMSFVQGE ESNDKIPVAL GLKEKNLYLS CVLKDDKPTL QLESVDPKNY PKKKMEKRFV FNKIEINNKL EFESAQFPNGT QFESAQFPNW YISGTS
Физиологическая активность, определенная по дозозависимой пролиферации мышиных клеток D10S, составляет 2,5 × 10.8 до 7,1 х 108 ед. / мг.
Клиническое значение
Повышенная продукция IL-1β вызывает ряд различных аутовоспалительные синдромы, в первую очередь моногенные условия, называемые Криопирин-ассоциированные периодические синдромы (CAPS) из-за мутаций рецептора инфламмасомы NLRP3, который запускает процессинг IL-1B.[15]
Кишечник дисбактериоз было замечено, чтобы вызвать остеомиелит зависимым от IL-1β образом.[16]
Присутствие IL-1β также было обнаружено у пациентов с рассеянный склероз (хроническое аутоиммунное заболевание центральной нервной системы). Однако точно не известно, какие клетки продуцируют IL-1β. Лечение рассеянного склероза с помощью глатирамера ацетат или же натализумаб также было показано, что он снижает присутствие IL-1β или его рецептора.[17]
Роль инфламмасомы и IL-1β в канцерогенезе
Предполагается, что несколько типов инфламмасом играют роль в онкогенезе благодаря своим иммуномодулирующим свойствам, модуляции микробиоты кишечника, дифференцировке и апоптозу. Чрезмерная экспрессия IL-1β, вызванная инфламмасомами, может привести к канцерогенезу. Некоторые данные предполагают, что полиморфизм инфламмасомы NLRP3 связан со злокачественными новообразованиями, такими как рак толстой кишки и меланома. Сообщалось, что секреция IL-1β была увеличена в клеточной линии аденокарциномы легкого A549. В другом исследовании также было показано, что IL-1β вместе с IL-8 играет важную роль в химической устойчивости злокачественной мезотелиомы плевры, индуцируя экспрессию трансмембранных транспортеров. [18] Другое исследование показало, что ингибирование экспрессии инфламмасомы и IL-1β снижает развитие раковых клеток в меланоме.[19]
Дегенерация сетчатки
Было показано, что семейство IL-1 играет важную роль в воспалении при многих дегенеративных заболеваниях, таких как возрастная дегенерация желтого пятна, диабетическая ретинопатия и пигментный ретинит. Значительно повышенный уровень протеина IL-1β был обнаружен в стекловидном теле пациента с диабетической ретинопатией. Роль IL-1β была исследована как потенциальная терапевтическая мишень для лечения диабетической ретинопатии. Однако системное использование канакинумаб не оказали значительного эффекта. Роль IL-1β в возрастной дегенерации желтого пятна у пациентов не была доказана, но на многих моделях животных и исследованиях in vitro была продемонстрирована роль IL-1β в пигментированных эпителиальных клетках сетчатки и повреждении фоторецепторных клеток. Активация воспаления NLRP3 каспаза-1 которые катализируют расщепление неактивного цитозольного предшественника про-ИЛ-1β до его зрелой формы ИЛ-1β. Формы пигментированных эпителиальных клеток сетчатки кровяной барьер сетчатки в сетчатке человека, который важен для метаболической активности сетчатки, целостности и подавления инфильтрации иммунных клеток. Было показано, что клетки пигментированного эпителия сетчатки человека могут секретировать IL-1β при воздействии окислительный стресс. Воспалительная реакция приводит к повреждению клеток сетчатки и инфильтрации клеток иммунной системы. Воспалительный процесс, включая активацию NLRP3, является одной из причин возрастной дегенерации желтого пятна и других заболеваний сетчатки, которые приводят к потере зрения.[20][21][22]
Терапия, нацеленная на интерлейкин 1 бета
Канакинумаб представляет собой человеческое моноклональное антитело, нацеленное на IL-1B, одобренное во многих странах для лечения криопирин-ассоциированные периодические синдромы.
Рилонацепт ловушка ИЛ-1, разработанная Регенерон нацеленный на IL-1B, и одобрен в США как Arcalyst.[23]
Орфографическое примечание
Поскольку многие авторы научных рукописей допускают незначительную ошибку, используя гомоглиф, диез (ß) вместо бета (β), упоминания «IL-1ß» [так в оригинале] часто превращаются в «IL-1ss» [так в оригинале] при автоматическом перекодирование (потому что ß перекодируется в ss). Вот почему так много упоминаний последнего появляется в результатах веб-поиска.
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000125538 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000027398 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Auron PE, Webb AC, Rosenwasser LJ, Mucci SF, Rich A, Wolff SM, Dinarello CA (декабрь 1984 г.). «Нуклеотидная последовательность кДНК предшественника интерлейкина 1 человека». Труды Национальной академии наук Соединенных Штатов Америки. 81 (24): 7907–11. Bibcode:1984PNAS ... 81.7907A. Дои:10.1073 / пнас.81.24.7907. ЧВК 392262. PMID 6083565.
- ^ а б «Катаболин» - это название, данное Джереми Саклатвалой для IL-1 alpha. Марч С.Дж., Мосли Б., Ларсен А., Черретти Д.П., Бредт Г., Прайс В. и др. (1985). «Клонирование, последовательность и экспрессия двух различных человеческих комплементарных ДНК интерлейкина-1». Природа. 315 (6021): 641–7. Bibcode:1985Натура.315..641М. Дои:10.1038 / 315641a0. PMID 2989698. S2CID 4240002.
- ^ Кларк Б.Д., Коллинз К.Л., Ганди М.С., Уэбб А.С., Аурон П.Е. (октябрь 1986 г.). «Геномная последовательность проинтерлейкина 1 бета человека: возможная эволюция гена проинтерлейкина 1 альфа с обратной транскрипцией». Исследования нуклеиновых кислот. 14 (20): 7897–914. Дои:10.1093 / nar / 14.20.7897. ЧВК 311823. PMID 3490654.
- ^ Бенси Дж., Раугей Дж., Палла Е., Каринчи В., Торнезе Буонамасса Д., Мелли М. (1987). «Ген интерлейкина-1 бета человека». Ген. 52 (1): 95–101. Дои:10.1016/0378-1119(87)90398-2. PMID 2954882.
- ^ Гери I, Гершон Р.К., Ваксман Б.Х. (июль 1972 г.). «Усиление ответа Т-лимфоцитов на митогены. I. Отвечающая клетка». Журнал экспериментальной медицины. 136 (1): 128–42. Дои:10.1084 / jem.136.1.128. ЧВК 2139184. PMID 5033417.
- ^ Гери I, Ваксман Б.Х. (июль 1972 г.). «Усиление ответа Т-лимфоцитов на митогены. II. Клеточный источник потенцирующего медиатора (ов)». Журнал экспериментальной медицины. 136 (1): 143–55. Дои:10.1084 / jem.136.1.143. ЧВК 2139186. PMID 5033418.
- ^ Гери I, Хандшумахер Р. Э. (март 1974 г.). «Усиление ответа Т-лимфоцитов на митогены. III. Свойства медиатора (ов) из прилипших клеток». Клеточная иммунология. 11 (1–3): 162–9. Дои:10.1016/0008-8749(74)90016-1. PMID 4549027.
- ^ «Энтрез Ген: интерлейкин 1, бета IL1B».
- ^ Саттон, Кэролайн Э .; Лалор, Стивен Дж .; Суини, Шерил М .; Бреретон, Коринна Ф .; Lavelle, Ed C .; Миллс, Кингстон Х.Г. (август 2009 г.). «Интерлейкин-1 и IL-23 индуцируют врожденную продукцию IL-17 из γδ Т-клеток, усиливая ответы Th17 и аутоиммунитет». Иммунитет. 31 (2): 331–341. Дои:10.1016 / j.immuni.2009.08.001. ISSN 1074-7613. PMID 19682929.
- ^ Абдерразак А., Сыровец Т., Куши Д., Эль-Хадри К., Фриге Б., Симмет Т., Руис М. (апрель 2015 г.). «Инфламмасома NLRP3: от датчика сигнала опасности до регулирующего узла окислительного стресса и воспалительных заболеваний». Редокс Биология. 4: 296–307. Дои:10.1016 / j.redox.2015.01.008. ЧВК 4315937. PMID 25625584.
- ^ Мастерс С.Л., Саймон А., Аксентьевич И., Кастнер Д.Л. (2009). «Ужас аутовоспалительного заболевания: молекулярная патофизиология аутовоспалительного заболевания (*)». Ежегодный обзор иммунологии. 27: 621–68. Дои:10.1146 / annurev.immunol.25.022106.141627. ЧВК 2996236. PMID 19302049.
- ^ Люкенс Дж. Р., Гурунг П., Фогель П., Джонсон Г. Р., Картер Р. А., МакГолдрик Д. Д. и др. (Декабрь 2014 г.). «Диетическое изменение микробиома влияет на аутовоспалительное заболевание». Природа. 516 (7530): 246–9. Bibcode:2014Натура.516..246л. Дои:10.1038 / природа13788. ЧВК 4268032. PMID 25274309.
- ^ Лин СС, Эдельсон Б.Т. (июнь 2017 г.). «Новое понимание роли IL-1β в экспериментальном аутоиммунном энцефаломиелите и рассеянном склерозе». Журнал иммунологии. 198 (12): 4553–4560. Дои:10.4049 / jimmunol.1700263. ЧВК 5509030. PMID 28583987.
- ^ Милошевич В. и др. Аутокринные цепи Wnt / IL-1β / IL-8 контролируют химиорезистентность в инициирующих клетках мезотелиомы, индуцируя ABCB5.Int. J. Рак, https://doi.org/10.1002/ijc.32419
- ^ Мусави М., Парсаманеш Н., Бахрами А., Аткин С.Л., Сахебкар А. (ноябрь 2018 г.). «Роль инфламмасомы NLRP3 в развитии рака». Молекулярный рак. 17 (1): 158. Дои:10.1186 / s12943-018-0900-3. ЧВК 6240225. PMID 30447690.
- ^ Биан З.М., Филд М.Г., Элнер С.Г., Каленберг Дж.М., Элнер В.М. (май 2018 г.). «Определенные рецепторы CD40L опосредуют активацию инфламмасом и секрецию IL-1β и MCP-1 в культивируемых клетках пигментного эпителия сетчатки человека». Экспериментальные исследования глаз. 170: 29–39. Дои:10.1016 / j.exer.2018.02.014. ЧВК 5924621. PMID 29454857.
- ^ Ценг В.А., Тейн Т., Киннунен К., Лашкари К., Грегори М.С., Д'Амор П.А., Ксандер Б.Р. (январь 2013 г.). «Активация инфламмасомы NLRP3 в пигментных эпителиальных клетках сетчатки путем дестабилизации лизосом: последствия для возрастной дегенерации желтого пятна». Исследовательская офтальмология и визуализация. 54 (1): 110–20. Дои:10.1167 / iovs.12-10655. ЧВК 3544415. PMID 23221073.
- ^ Wooff Y, Man SM, Aggio-Bruce R, Natoli R, Fernando N (16.07.2019). «Члены семейства IL-1 опосредуют гибель клеток, воспаление и ангиогенез при дегенеративных заболеваниях сетчатки». Границы иммунологии. 10: 1618. Дои:10.3389 / fimmu.2019.01618. ЧВК 6646526. PMID 31379825.
- ^ (PDF) https://www.accessdata.fda.gov/drugsatfda_docs/label/2008/125249lbl.pdf. Получено 5 октября 2020. Отсутствует или пусто
| название =(помощь)
дальнейшее чтение
- Смирнова М.Г., Киселев С.Л., Гнучев Н.В., Бирчалл Дж. П., Пирсон Дж. П. (2003). «Роль провоспалительных цитокинов, фактора некроза опухоли альфа, интерлейкина-1 бета, интерлейкина-6 и интерлейкина-8 в патогенезе отита с выпотом». Европейская сеть цитокинов. 13 (2): 161–72. PMID 12101072.
- Гриффин В.С., Мрак Р.Э. (август 2002 г.). «Интерлейкин-1 в генезе и прогрессировании, а также риск развития нейрональной дегенерации при болезни Альцгеймера». Журнал биологии лейкоцитов. 72 (2): 233–8. ЧВК 3835694. PMID 12149413.
- Аренд WP (2003). «Баланс между IL-1 и IL-1Ra при болезни». Отзывы о цитокинах и факторах роста. 13 (4–5): 323–40. Дои:10.1016 / S1359-6101 (02) 00020-5. PMID 12220547.
- Чакраворти М., Гош А., Чоудхури А., Сантра А., Хембрум Дж., Ройчоудхури С. (февраль 2004 г.). «Этнические различия в распределении аллелей генов IL8 и IL1B в популяциях из восточной Индии». Человеческая биология. 76 (1): 153–9. Дои:10.1353 / ступица.2004.0016. PMID 15222686. S2CID 2816300.
- Джозеф AM, Кумар М., Митра Д. (январь 2005 г.). «Неф:« необходимый и усиливающий фактор »при ВИЧ-инфекции». Текущие исследования ВИЧ. 3 (1): 87–94. Дои:10.2174/1570162052773013. PMID 15638726.
- Маруяма Й., Стенвинкель П., Линдхольм Б. (2005). «Роль интерлейкина-1бета в развитии недостаточности питания у пациентов с хронической почечной недостаточностью». Очищение крови. 23 (4): 275–81. Дои:10.1159/000086012. PMID 15925866. S2CID 72570361.
- Милошевич V и др. (Январь 2020 г.). «Аутокринные цепи Wnt / IL-1β / IL-8 контролируют химиорезистентность в инициирующих клетках мезотелиомы, индуцируя ABCB5». Int. J. Рак. 146 (1): 192–207. Дои:10.1002 / ijc.32419.
- Рой Д., Саркар С., Фелти К. (январь 2006 г.). «Уровни ИЛ-1 бета контролируют стимулирующий / ингибирующий рост раковых клеток». Границы биологических наук. 11: 889–98. Дои:10.2741/1845. PMID 16146780. S2CID 23009646.
- Коупленд К.Ф. (декабрь 2005 г.). «Модуляция транскрипции ВИЧ-1 цитокинами и хемокинами». Мини-обзоры по медицинской химии. 5 (12): 1093–101. Дои:10.2174/138955705774933383. PMID 16375755.
- Prinz C, Schwendy S, Voland P (сентябрь 2006 г.). "H. pylori и рак желудка: перенос глобального бремени". Всемирный журнал гастроэнтерологии. 12 (34): 5458–64. Дои:10.3748 / wjg.v12.i34.5458. ЧВК 4088226. PMID 17006981.
- Камангар Ф., Ченг С., Абнет СС, Рабкин С.С. (октябрь 2006 г.). «Полиморфизм интерлейкина-1B и риск рака желудка - метаанализ». Эпидемиология, биомаркеры и профилактика рака. 15 (10): 1920–8. Дои:10.1158 / 1055-9965.EPI-06-0267. PMID 17035400.
внешняя ссылка
- IL1B + белок, + человеческий в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.