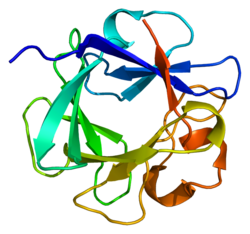
FGF4 - FGF4
Фактор роста фибробластов 4 это белок что у людей кодируется FGF4 ген.[5][6]
Белок, кодируемый этим геном, является членом фактор роста фибробластов (FGF) семья. Члены семьи FGF обладают широким митогенный и активности клеток и участвуют во множестве биологических процессов, включая эмбриональное развитие, рост клеток, морфогенез, восстановление тканей, рост опухоли и инвазия. Этот ген был идентифицирован по его онкогенной трансформирующей активности. Этот ген и FGF3 - еще один онкогенный фактор роста - расположены близко к хромосоме 11. Коамплификация обоих генов была обнаружена в различных типах опухолей человека. Исследования гомолога мышей предполагают функцию морфогенеза костей и развития конечностей с помощью звукового ежа (SHH ) сигнальный путь.[6]
Функция
Во время эмбрионального развития белок FGF4 массой 21 кДа функционирует как сигнальная молекула, которая участвует во многих важных процессах.[7][8] Исследования с использованием мышей с нокаутом гена Fgf4 показали дефекты развития у эмбрионов как in vivo, так и in vitro, показывая, что FGF4 способствует выживанию и росту внутренней клеточной массы во время постимплантационной фазы развития, действуя как аутокринный или паракринный лиганд.[7] FGFs, продуцируемые в апикальном эктодермальном гребне (AER), критичны для правильного роста передних и задних конечностей.[9] Передача сигналов FGF в AER участвует в регуляции количества пальцев конечностей и гибели клеток в межпальцевом суставе. мезенхима.[10] Когда динамика передачи сигналов FGF и регуляторные процессы изменяются, постаксиальная полидактилия и кожная синдактилия, возникают две фенотипические аномалии, вместе известные как полисиндактилия, может возникнуть в конечностях. Полисиндактилия наблюдается, когда избыток Fgf4 экспрессируется в зачатках конечностей мышей дикого типа. В мутантных зачатках конечностей, не экспрессирующих Fgf8, экспрессия Fgf4 все еще приводит к полисиндактилии, но Fgf4 также способен восстанавливать все дефекты скелета, которые возникают из-за отсутствия Fgf8. Следовательно, ген Fgf4 компенсирует потерю гена Fgf8, показывая, что FGF4 и FGF8 выполняют сходные функции в формировании паттерна скелета конечностей и развитии конечностей.[10] Исследования эмбрионов с нокдауном Fgf4 рыбок данио продемонстрировали, что когда передача сигналов Fgf4 ингибируется, имеет место рандомизированное формирование паттерна слева направо в печени, поджелудочной железе и сердце, показывая, что Fgf4 является критическим геном, участвующим в формировании формирования паттерна слева направо висцеральных органов. Более того, в отличие от роли FGF4 в развитии конечностей, FGF4 и FGF8 имеют разные роли и функционируют независимо в процессе формирования лево-правого паттерна висцеральных органов.[11]Также было продемонстрировано, что сигнальный путь Fgf управляет идентичностью задней кишки во время развития желудочно-кишечного тракта, и повышающая регуляция Fgf4 в плюрипотентных стволовых клетках используется для направления их дифференцировки для генерации кишечных Органоиды и ткани in vitro.[12]
использованная литература
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000075388 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000050917 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Галланд Ф, Стефанова М, Лафаж М, Бирнбаум Д (июль 1992 г.). «Локализация 5 'конца онкогена MCF2 на хромосоме 15q15 ---- q23 человека». Цитогенетика и клеточная генетика. 60 (2): 114–6. Дои:10.1159/000133316. PMID 1611909.
- ^ а б «Ген Entrez: фактор роста 4 фибробластов FGF4 (белок 1, трансформирующий секретор гепарина, онкоген саркомы Капоши)».
- ^ а б Feldman B, Poueymirou W., Papaioannou VE, DeChiara TM, Goldfarb M (январь 1995 г.). «Потребность в FGF-4 для постимплантационного развития мышей». Наука. 267 (5195): 246–9. Дои:10.1126 / science.7809630. PMID 7809630. S2CID 31312392.
- ^ Юань Х., Корби Н., Базилико С., Дейли Л. (ноябрь 1995 г.). «Специфическая для развития активность энхансера FGF-4 требует синергетического действия Sox2 и Oct-3». Гены и развитие. 9 (21): 2635–45. Дои:10.1101 / gad.9.21.2635. PMID 7590241.
- ^ Boulet AM, Moon AM, Arenkiel BR, Capecchi MR (сентябрь 2004 г.). «Роли Fgf4 и Fgf8 в инициации и отрастании зачатка конечностей». Биология развития. 273 (2): 361–72. Дои:10.1016 / j.ydbio.2004.06.012. PMID 15328019.
- ^ а б Лу П, Миновада Дж., Мартин Г. Р. (январь 2006 г.). «Повышение экспрессии Fgf4 в зачатке конечности мыши вызывает полисиндактилию и устраняет дефекты скелета, которые возникают в результате потери функции Fgf8». Развитие. 133 (1): 33–42. Дои:10.1242 / dev.02172. PMID 16308330.
- ^ Ямаути Х., Миякава Н., Мияке А., Ито Н. (август 2009 г.). «Fgf4 необходим для формирования левого-правого паттерна висцеральных органов у рыбок данио». Биология развития. 332 (1): 177–85. Дои:10.1016 / j.ydbio.2009.05.568. PMID 19481538.
- ^ Ланкастер М.А., Кноблич Ю.А. (2014). «Органогенез в блюде: моделирование развития и заболевания с помощью органоидных технологий». Наука. 345 (6194): 1247125. Дои:10.1126 / science.1247125. PMID 25035496. S2CID 16105729.
дальнейшее чтение
- Полномочия CJ, McLeskey SW, Wellstein A (сентябрь 2000 г.). «Факторы роста фибробластов, их рецепторы и сигнализация». Эндокринный рак. 7 (3): 165–97. CiteSeerX 10.1.1.323.4337. Дои:10.1677 / erc.0.0070165. PMID 11021964.
- Тайра М., Йошида Т., Миягава К., Сакамото Х., Терада М., Сугимура Т. (май 1987 г.). «последовательность кДНК трансформирующего гена человека hst и идентификация кодирующей последовательности, необходимой для трансформирующей активности». Труды Национальной академии наук Соединенных Штатов Америки. 84 (9): 2980–4. Дои:10.1073 / пнас.84.9.2980. ЧВК 304784. PMID 2953031.
- Делли Бови П., Куратола А.М., Керн Ф.Г., Греко А., Иттманн М., Базилико С. (август 1987 г.). «Онкоген, выделенный трансфекцией ДНК саркомы Капоши, кодирует фактор роста, который является членом семейства FGF». Ячейка. 50 (5): 729–37. Дои:10.1016 / 0092-8674 (87) 90331-Х. PMID 2957062. S2CID 30018932.
- Йошида Т., Миягава К., Одагири Х., Сакамото Х., Литтл П.Ф., Терада М., Сугимура Т. (октябрь 1987 г.). «Геномная последовательность hst, трансформирующего гена, кодирующего белок, гомологичный факторам роста фибробластов, и белок, кодируемый int-2». Труды Национальной академии наук Соединенных Штатов Америки. 84 (20): 7305–9. Дои:10.1073 / пнас.84.20.7305. ЧВК 299281. PMID 2959959.
- Вада А., Сакамото Х., Катох О, Ёсида Т., Йокота Дж., Литтл П.Ф., Сугимура Т., Терада М. (декабрь 1988 г.). «Два гомологичных онкогена, HST1 и INT2, близко расположены в геноме человека». Сообщения о биохимических и биофизических исследованиях. 157 (2): 828–35. Дои:10.1016 / S0006-291X (88) 80324-3. PMID 2974287.
- Хюбнер К., Феррари АС, Делли Бови П., Кроче С.М., Базилико С. (1989). «Связанный с FGF онкоген, K-FGF, картируется в области хромосомы человека 11q13, возможно, рядом с int-2». Онкогенные исследования. 3 (3): 263–70. PMID 3060803.
- Аделаида Дж., Маттей М.Г., Марикс I, Рейбо Ф., Планш Дж., Де Лапейриер О, Бирнбаум Д. (апрель 1988 г.). «Хромосомная локализация онкогена hst и его совместная амплификация с онкогеном int.2 в меланоме человека». Онкоген. 2 (4): 413–6. PMID 3283658.
- Орниц Д.М., Сюй Дж., Колвин Д.С., МакИвен Д.Г., Макартур Калифорния, Кулиер Ф., Гао Дж., Гольдфарб М. (июнь 1996 г.). «Рецепторная специфичность семейства факторов роста фибробластов». Журнал биологической химии. 271 (25): 15292–7. Дои:10.1074 / jbc.271.25.15292. PMID 8663044.
- Tanaka S; и другие. (1998). «Содействие пролиферации стволовых клеток трофобласта с помощью FGF-4». Наука. 282 (5396): 2072–2075. Дои:10.1126 / science.282.5396.2072. PMID 9851926.
- Хелланд Р., Берглунд Г.И., Отлевски Дж., Апостолук В., Андерсен О.А., Уиллассен Н.П., Смалас А.О. (январь 1999 г.). «Структуры высокого разрешения трех новых комплексов трипсин-сквош-ингибитор: подробное сравнение с другими трипсинами и их комплексами». Acta Crystallographica Раздел D. 55 (Pt 1): 139–48. Дои:10.1107 / S090744499801052X. PMID 10089404.
- Беллоста П., Ивахори А., Плотников А.Н., Елисеенкова А.В., Базилико С., Мохаммади М. (сентябрь 2001 г.). «Идентификация рецепторов и сайтов связывания гепарина в факторе роста фибробластов 4 с помощью структурного мутагенеза». Молекулярная и клеточная биология. 21 (17): 5946–57. Дои:10.1128 / MCB.21.17.5946-5957.2001. ЧВК 87313. PMID 11486033.
- Бритто Дж. А., Эванс Р. Д., Хейворд Р. Д., Джонс Б. М. (декабрь 2001 г.). «От генотипа к фенотипу: дифференциальная экспрессия генов FGF, FGFR и TGFbeta характеризует развитие краниоскелета человека и отражает клиническую картину синдромов FGFR». Пластическая и реконструктивная хирургия. 108 (7): 2026–39, обсуждение 2040–6. Дои:10.1097/00006534-200112000-00030. PMID 11743396.
- Ямамото Х., Очия Т., Тамамуси С., Торияма-Баба Х., Такахама Й., Хираи К., Сасаки Х., Сакамото Х., Сайто И., Ивамото Т., Какидзоэ Т., Терада М. (январь 2002 г.). «Активация гена HST-1 / FGF-4 индуцирует сперматогенез и предотвращает индуцированную адриамицином токсичность для яичек». Онкоген. 21 (6): 899–908. Дои:10.1038 / sj.onc.1205135. PMID 11840335.
- Зиевертс А.М., Мартенс Дж.В., Дорссерс Л.С., Клин Дж. Г., Фоекенс Дж. А. (апрель 2002 г.). «Дифференциальные эффекты факторов роста фибробластов на экспрессию генов активатора плазминогена и систем инсулиноподобных факторов роста фибробластами груди человека». Тромбоз и гемостаз. 87 (4): 674–83. Дои:10.1055 / с-0037-1613065. PMID 12008951.
- Ко КР, Охта К., Накамаэ Х., Хино М., Ямане Т., Такубо Т., Тацуми Н. (октябрь 2002 г.). «Дифференциальные эффекты фактора роста фибробластов-4, эпидермального фактора роста и трансформирующего фактора роста-бета1 на функциональное развитие стромальных слоев при остром миелоидном лейкозе». Исследование лейкемии. 26 (10): 933–8. Дои:10.1016 / S0145-2126 (02) 00033-4. PMID 12163055.
- Лопес-Санчес К., Климент V, Шенвольф Г.К., Альварес И.С., Гарсия-Мартинес V (август 2002 г.). «Индукция кардиогенеза узлом Генсена и факторами роста фибробластов». Исследования клеток и тканей. 309 (2): 237–49. Дои:10.1007 / s00441-002-0567-2. PMID 12172783. S2CID 11783465.
- Ван П., Branch DR, Bali M, Schultz GA, Goss PE, Jin T (октябрь 2003 г.). «Гомеодоменный белок OCT3 POU как потенциальный активатор транскрипции для фактора роста фибробластов-4 (FGF-4) в клетках рака груди человека». Биохимический журнал. 375 (Pt 1): 199–205. Дои:10.1042 / BJ20030579. ЧВК 1223663. PMID 12841847.
- Ременьи А., Линс К., Ниссен Л.Дж., Рейнбольд Р., Шелер Х.Р., Вильманнс М. (август 2003 г.). «Кристаллическая структура тройного комплекса POU / HMG / ДНК предполагает дифференциальную сборку Oct4 и Sox2 на двух энхансерах». Гены и развитие. 17 (16): 2048–59. Дои:10.1101 / gad.269303. ЧВК 196258. PMID 12923055.
- Хираи К., Сасаки Х., Ямамото Х., Сакамото Х., Кубота Й, Какидзоэ Т., Терада М., Очия Т. (март 2004 г.). «HST-1 / FGF-4 защищает мужские половые клетки от апоптоза в условиях теплового стресса». Экспериментальные исследования клеток. 294 (1): 77–85. Дои:10.1016 / j.yexcr.2003.11.012. PMID 14980503.
- Григорьева Е.В., Шевченко А.И., Мазурок Н.А., Елисафенко Е.А., Железова А.И., Шилов А.Г., Дыбан П.А., Дыбан А.П., Нониашвили Е.М., Слободянюк С.Ю., Нестерова Т.Б., Брокдорф Н., Закян С.М. (2009). «FGF4 независимое происхождение стволовых клеток трофобласта от обыкновенной полевки». PLOS ONE. 4 (9): e7161. Дои:10.1371 / journal.pone.0007161. ЧВК 2744875. PMID 19777059.
- Boulet AM, Capecchi MR (ноябрь 2012 г.). «Передача сигналов от FGF4 и FGF8 необходима для осевого удлинения эмбриона мыши». Биология развития. 371 (2): 235–45. Дои:10.1016 / j.ydbio.2012.08.017. ЧВК 3481862. PMID 22954964.