Стволовая клетка - Stem cell
| Стволовая клетка | |
|---|---|
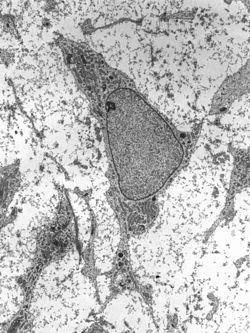 Передача инфекции электронная микрофотография из мезенхимальные стволовые клетки отображение типичного ультраструктурный характеристики | |
| Подробности | |
| Идентификаторы | |
| латинский | Cellula praecursoria |
| MeSH | D013234 |
| TH | H1.00.01.0.00028, H2.00.01.0.00001 |
| FMA | 63368 |
| Анатомическая терминология | |
В многоклеточные организмы, стволовые клетки находятся недифференцированный или частично дифференцированный клетки которые можно разделить на различные типы ячеек и размножаться бесконечно, чтобы производить больше одинаковых стволовых клеток. Это самый ранний тип клеток в клеточная линия.[1] Они есть в обоих эмбриональный и взрослые организмы, но у каждого из них свойства немного разные. Их обычно отличают от клетки-предшественники, который не может делиться бесконечно, и предшественник или бластные клетки, которые обычно преданы дифференцировке в один тип клеток.
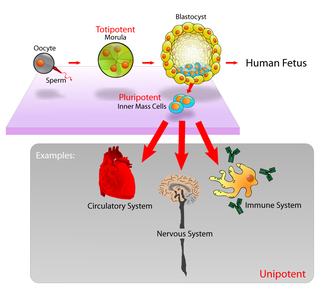
В млекопитающие, примерно 50–150 клеток составляют внутренняя клеточная масса вовремя бластоциста стадия эмбрионального развития, около 5–14 дней. Они обладают способностью к стволовым клеткам. В естественных условиях, они в конечном итоге дифференцируются во все типы клеток тела (что делает их плюрипотентный ). Этот процесс начинается с разделения на три ростковые отростки - в эктодерма, мезодерма и энтодерма - на гаструляция сцена. Однако когда они изолированы и культурный in vitro, они могут сохраняться на стадии стволовых клеток и известны как эмбриональные стволовые клетки (ESC).
Взрослые стволовые клетки находятся в нескольких избранных местах тела, известных как ниши, например, в Костный мозг или же гонады. Они существуют для восполнения быстро потерянных типов клеток и являются мультипотентный или унипотентные, то есть они дифференцируются только на несколько типов клеток или на один тип клеток. У млекопитающих они включают, среди прочего, гемопоэтические стволовые клетки, которые восполняют кровь и иммунные клетки, базальные клетки, которые поддерживают кожу эпителий, и мезенхимальные стволовые клетки, которые поддерживают кости, хрящ, мышечные и жировые клетки. Взрослые стволовые клетки составляют небольшое количество клеток; их значительно меньше, чем клеток-предшественников и терминально дифференцированных клеток, в которые они дифференцируются.[1]
Исследования стволовых клеток основаны на открытиях канадских биологов Эрнест А. Маккалох, Джеймс Э. Тилль и Эндрю Дж. Беккер в Университет Торонто в 1960-е гг.[2][3] По состоянию на 2016 год[Обновить], единственный установленный лечебная терапия с использованием стволовых клеток является трансплантация гемопоэтических стволовых клеток,[4] впервые выполнен в 1958 году французским онкологом Жорж Мате. Однако с 1998 г. стало возможным культивировать и дифференцировать эмбриональные стволовые клетки человека (в линии стволовых клеток ). Процесс выделения этих клеток был спорный, потому что это обычно приводит к разрушению эмбриона. Источники для выделения ESC были ограниченный в некоторых европейских странах и Канаде, но другие, такие как Великобритания и Китай, продвинули исследование.[5] Перенос ядра соматической клетки это клонирование метод, который можно использовать для создания клонированного эмбриона для использования его эмбриональных стволовых клеток в терапии стволовыми клетками.[6] В 2006 году японская команда под руководством Шинья Яманака открыли метод преобразования зрелых клеток тела обратно в стволовые клетки. Их назвали индуцированные плюрипотентные стволовые клетки (ИПСК).[7]
История
Период, термин стволовая клетка был придуман Теодор Бовери и Валентин Хеккер в конце 19 века[8]. Пионерские работы по теории стволовых клеток крови были проведены в начале 20 века. Артур Паппенгейм, Александр Максимов, Эрнст Нойман[8].
Ключевые свойства стволовой клетки были впервые определены Эрнест МакКаллох и Джеймс Тилль в Университете Торонто в начале 1960-х. Они открыли кроветворные стволовые клетки, гемопоэтические стволовые клетки (HSC), благодаря своей новаторской работе на мышах. Маккаллох и Тилль начали серию экспериментов, в которых клетки костного мозга вводили облученным мышам. Они наблюдали уплотнения в селезенке мышей, которые были линейно пропорциональны количеству введенных клеток костного мозга. Они предположили, что каждая шишка (колония) была клоном, возникшим из одной клетки костного мозга (стволовой клетки). В последующей работе Маккалок и Тилль, к которым присоединились аспирант Энди Беккер и старший научный сотрудник Лу Симинович, подтвердили, что каждый кусок на самом деле возник из одной клетки. Их результаты опубликованы в Природа в 1963 году. В том же году Симинович был ведущим исследователем в исследованиях, которые обнаружили, что колониеобразующие клетки способны к самообновлению, что является ключевым определяющим свойством стволовых клеток, которое теоретизировали Тилль и МакКаллох.[9]
Первая терапия с использованием стволовых клеток была пересадка костного мозга в исполнении французского онколога Жорж Мате в 1958 г. на пяти рабочих на Ядерный институт Винча в Югославия кто пострадал от авария с критичностью. Все рабочие выжили.[10]
В 1981 году британские биологи впервые выделили и успешно культивировали эмбриональные стволовые (ES) клетки с использованием бластоцист мыши. Мартин Эванс и Мэтью Кауфман. Это позволило сформировать мышиные генетические модели, систему, в которой гены мышей удаляются или изменяются с целью изучения их функции при патологии. К 1998 году эмбриональные стволовые клетки были впервые выделены американским биологом. Джеймс Томсон, что позволило использовать новые методы трансплантации или различные типы клеток для тестирования новых методов лечения. В 2006 г. Шинья Яманака Команда ученых из Киото, Япония, преобразовала фибробласты в плюрипотентные стволовые клетки, изменив экспрессию только четырех генов. Этот подвиг представляет собой происхождение индуцированных плюрипотентных стволовых клеток, известных как iPS-клетки.[7]
Характеристики
Классическое определение стволовой клетки требует, чтобы она обладала двумя свойствами:
- Самообновление: умение проходить многочисленные циклы из рост клеток и деление клеток, известный как распространение клеток, сохраняя при этом недифференцированное состояние.
- Потенция: способность к различать на специализированные типы клеток. В самом строгом смысле для этого требуется, чтобы стволовые клетки были либо тотипотент или же плюрипотентный - иметь возможность давать начало любому типу зрелых клеток, хотя мультипотентный или же всесильный клетки-предшественники иногда называют стволовыми клетками. Помимо этого, говорят, что функция стволовых клеток регулируется по механизму обратной связи.
Самообновление
Два механизма обеспечивают поддержание популяции стволовых клеток (не уменьшение ее размера):
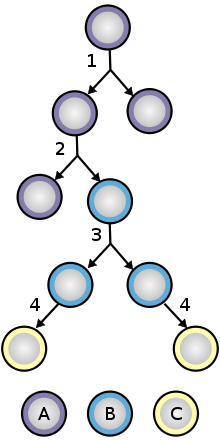
1. Асимметричное деление клеток: стволовая клетка делится на одну материнскую клетку, которая идентична исходной стволовой клетке, и другую дочернюю клетку, которая дифференцируется.
Когда стволовые клетки самообновляются, они делятся и не нарушают недифференцированное состояние. Это самообновление требует контроля клеточного цикла, а также поддержания мультипотентности или плюрипотентности, которые все зависит от стволовых клеток.[11]
2. Стохастическая дифференциация: когда одна стволовая клетка растет и делится на две дифференцированные дочерние клетки, другая стволовая клетка подвергается митоз и производит две стволовые клетки, идентичные оригиналу.
Использование стволовых клеток теломераза, белок, восстанавливающий теломеры, чтобы защитить свою ДНК и увеличить предел деления клеток ( Лимит Хейфлика ).[12]
Значение потенции

A: Колонии стволовых клеток, которые еще не дифференцировались.
B: Нерв ячеек, пример тип ячейки после дифференциации.
Потенция определяет потенциал дифференцировки (способность дифференцироваться в разные типы клеток) стволовой клетки.[13]
- Тотипотент (также известные как всемогущие) стволовые клетки могут дифференцироваться на эмбриональные и внеэмбриональные типы клеток. Такие клетки могут построить полноценный жизнеспособный организм.[13] Эти клетки производятся из слияние яйцеклетки и сперматозоида. Клетки, продуцируемые несколькими первыми делениями оплодотворенной яйцеклетки, также являются тотипотентными.[14]
- Плюрипотентный стволовые клетки являются потомками тотипотентных клеток и могут дифференцироваться почти во все клетки,[13] т.е. клетки, полученные из любого из трех ростковые отростки.[15]
- Мультипотентный стволовые клетки могут дифференцироваться в несколько типов клеток, но только из близкородственного семейства клеток.[13]
- Олигопотент стволовые клетки могут дифференцироваться только в несколько типов клеток, такие как лимфоидные или миелоидные стволовые клетки.[13]
- Унипотентный клетки могут производить только один тип клеток, свои собственные,[13] но обладают свойством самообновления, что отличает их от не стволовых клеток (например, клетки-предшественники, который не может самообновляться).
Идентификация
На практике стволовые клетки идентифицируют по тому, могут ли они регенерировать ткань. Например, определяющий тест на костный мозг или гемопоэтические стволовые клетки (HSC) - это способность трансплантировать клетки и спасать человека без HSC. Это показывает, что клетки могут производить новые клетки крови в течение длительного времени. Также должна быть возможность выделить стволовые клетки от пересаженного человека, которые сами могут быть трансплантированы другому человеку без HSC, что демонстрирует способность стволовых клеток к самообновлению.
Свойства стволовых клеток можно проиллюстрировать in vitro, используя такие методы, как клоногенные анализы, в котором отдельные клетки оцениваются на предмет их способности дифференцироваться и самообновляться.[16][17] Стволовые клетки также можно выделить по наличию в них особого набора маркеров клеточной поверхности. Тем не мение, in vitro условия культивирования могут изменять поведение клеток, делая неясным, будут ли клетки вести себя аналогичным образом. in vivo. Существуют серьезные споры о том, действительно ли некоторые предполагаемые популяции взрослых клеток являются стволовыми клетками.[18]
Эмбриональный
Эмбриональные стволовые клетки (ESC) - это ячейки внутренняя клеточная масса из бластоциста, сформированный до имплантация в матке.[19] В эмбриональное развитие человека то бластоциста стадия достигается через 4–5 дней после оплодотворение, при этом состоит из 50–150 ячеек. ESC плюрипотентный и порождают в процессе разработки все производные от трех ростковые отростки: эктодерма, энтодерма и мезодерма. Другими словами, они могут развиться в каждый из более чем 200 типов клеток взрослого человека. тело при достаточной и необходимой стимуляции для определенного типа клеток. Они не способствуют внеэмбриональные оболочки или в плацента.
Во время эмбрионального развития клетки внутренней клеточной массы непрерывно делятся и становятся более специализированными. Например, часть эктодермы в дорсальной части эмбриона специализируется как «нейроэктодерма ', который станет будущим Центральная нервная система.[20][страница нужна ] Позже в разработке нейруляция заставляет нейроэктодерму формировать нервная трубка. На стадии нервной трубки передняя часть подвергается энцефализация для создания или «моделирования» основной формы мозга. На этом этапе развития основной тип клеток ЦНС рассматривается как нервная стволовая клетка.
Нервные стволовые клетки самообновляются и в какой-то момент переходят в клетки-предшественники радиальной глии (РГП). Рано сформированные RGP самообновляются за счет симметричного деления с образованием коллектора группы клетки-предшественники. Эти клетки переходят в нейрогенный заявить и начать делить асимметрично для создания большого разнообразия множества различных типов нейронов, каждый из которых имеет уникальную экспрессию генов, морфологические и функциональные характеристики. Процесс генерации нейронов из радиальных глиальных клеток называется нейрогенез. Радиальная глиальная клетка имеет отличительную биполярную морфологию с сильно удлиненными отростками, охватывающими толщину стенки нервной трубки. Он разделяет некоторые глиальный характеристики, в первую очередь выражение глиальный фибриллярный кислый белок (GFAP).[21][22] Радиальная глиальная клетка - это первичная нервная стволовая клетка развивающейся позвоночное животное ЦНС, и ее клеточное тело находится в желудочковая зона, примыкающий к развивающейся желудочковая система. Нервные стволовые клетки преданы нейрональным линиям (нейроны, астроциты, и олигодендроциты ), и, таким образом, их эффективность ограничена.[20]
На сегодняшний день почти во всех исследованиях использовались эмбриональные стволовые клетки мыши (mES) или эмбриональные стволовые клетки человека (hES), полученные из ранней внутренней клеточной массы. Оба обладают основными характеристиками стволовых клеток, но для поддержания недифференцированного состояния им требуется очень разная среда. ES-клетки мыши выращивают на слое желатин как внеклеточный матрикс (для поддержки) и требуют наличия фактор ингибирования лейкемии (LIF) в сыворотке. Лекарственный коктейль, содержащий ингибиторы GSK3B и Путь MAPK / ERK, названный 2i, также, как было показано, поддерживает плюрипотентность в культуре стволовых клеток.[23] ЭСК человека выращивают на фидерном слое эмбриональных клеток мыши. фибробласты и требуют присутствия основного фактора роста фибробластов (bFGF или FGF-2).[24] Без оптимальных условий культивирования или генетических манипуляций,[25] эмбриональные стволовые клетки быстро дифференцируются.
Эмбриональная стволовая клетка человека также определяется экспрессией нескольких факторов транскрипции и белков клеточной поверхности. Факторы транскрипции Октябрь-4, Наног, и Sox2 образуют ядро регуляторной сети, которая обеспечивает подавление генов, ведущих к дифференцировке и поддержанию плюрипотентности.[26] Антигенами клеточной поверхности, наиболее часто используемыми для идентификации hES-клеток, являются гликолипиды. стадия специфического эмбрионального антигена 3 и 4, и кератансульфатные антигены Tra-1-60 и Tra-1-81. Молекулярное определение стволовой клетки включает гораздо больше белков и продолжает оставаться предметом исследований.[27]
Используя эмбриональные стволовые клетки человека для производства специализированных клеток, таких как нервные клетки или клетки сердца, в лаборатории, ученые могут получить доступ к клеткам взрослого человека, не отбирая ткани у пациентов. Затем они могут подробно изучить эти специализированные взрослые клетки, чтобы попытаться распознать осложнения заболеваний или изучить реакции клеток на предлагаемые новые лекарства.
Из-за их комбинированных способностей неограниченного роста и плюрипотентности эмбриональные стволовые клетки остаются теоретически потенциальным источником регенеративная медицина и замена тканей после травмы или болезни.,[28] однако в настоящее время нет одобренных методов лечения с использованием ES-клеток. Первое испытание на людях было одобрено Управлением по контролю за продуктами и лекарствами США в январе 2009 года.[29] Однако испытание на людях началось только 13 октября 2010 г. в Атланте по поводу исследование травм спинного мозга. 14 ноября 2011 г. компания, проводившая судебное разбирательство (Корпорация Geron ) объявил, что прекратит дальнейшее развитие своих программ стволовых клеток.[30] Дифференциация ES-клеток в пригодные для использования клетки при одновременном предотвращении отторжения трансплантата - это лишь некоторые из препятствий, с которыми все еще сталкиваются исследователи эмбриональных стволовых клеток.[31] Эмбриональные стволовые клетки, будучи плюрипотентными, требуют определенных сигналов для правильной дифференцировки - при введении непосредственно в другое тело ES-клетки будут дифференцироваться во множество различных типов клеток, вызывая тератома. Этические соображения относительно использования тканей нерожденного человека - еще одна причина отсутствия одобренных методов лечения с использованием эмбриональных стволовых клеток. Многие страны в настоящее время имеют мораторий или ограничения на исследования человеческих ES-клеток или производство новых человеческих линий ES-клеток.
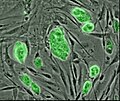
Мышь эмбриональный стволовые клетки с флуоресцентным маркером

Колония эмбриональных стволовых клеток человека на фидерном слое эмбриональных фибробластов мыши
Мезенхимальные стволовые клетки
Известно, что мезенхимальные стволовые клетки (МСК) мультипотентны, и их можно обнаружить во взрослых тканях, например, в мышцах, печени, костном мозге. Мезенхимальные стволовые клетки обычно функционируют как структурная опора в различных органах, как упоминалось выше, и контролируют движение веществ. МСК могут дифференцироваться на множество категорий клеток, как иллюстрация адипоцитов, остеоцитов и хондроцитов, происходящих из мезодермального слоя.[32] Когда слой мезодермы обеспечивает увеличение скелетных элементов тела, таких как хрящ или кость. Термин «мезо» означает средний, происходит от греческого слова «инфузия», означающий, что мезенхимальные клетки способны перемещаться и перемещаться на раннем этапе эмбрионального роста между эктодермальным и энтодермальным слоями. Этот механизм помогает заполнять пространство, таким образом, ключ к заживлению ран у взрослых организмов, которые связаны с мезенхимальными клетками дермы (кожи), костей или мышц.[33]
Известно, что мезенхимальные стволовые клетки необходимы для регенеративной медицины. Они широко изучаются в клинические испытания. Поскольку они легко выделяются и получают высокий выход, высокую пластичность, что позволяет облегчить воспаление и стимулировать рост клеток, дифференцировку клеток и восстановление тканей, полученных в результате иммуномодуляции и иммуносупрессии. МСК поступают из костного мозга, что требует агрессивной процедуры, когда дело доходит до определения количества и качества выделенных клеток, и это зависит от возраста донора. При сравнении уровней МСК в аспиратах костного мозга и строме костного мозга, аспираты, как правило, имеют более низкие показатели МСК, чем строма. Известно, что МСК неоднородны и экспрессируют высокий уровень плюрипотентных маркеров по сравнению с другими типами стволовых клеток, такими как эмбриональные стволовые клетки.[32]
Контроль клеточного цикла
Эмбриональные стволовые клетки (ЭСК) обладают способностью неограниченно делиться, сохраняя при этом свои плюрипотентность, что стало возможным благодаря специализированным механизмам клеточный цикл контроль.[34] По сравнению с распространением соматические клетки, ESC обладают уникальными характеристиками клеточного цикла, такими как быстрое деление клеток, вызванное укорочением Фаза G1, отсутствующий Фаза G0, и модификации в контрольные точки клеточного цикла - который оставляет клетки в основном в S фаза в любой момент времени.[34][35] Быстрое деление ESC демонстрируется их коротким временем удвоения, которое колеблется от 8 до 10 часов, тогда как время удвоения соматических клеток составляет примерно 20 часов или больше.[36] По мере дифференциации клеток эти свойства изменяются: фазы G1 и G2 удлиняются, что приводит к более длинным циклам деления клеток. Это указывает на то, что специфическая структура клеточного цикла может способствовать установлению плюрипотентности.[34]
В частности, поскольку фаза G1 - это фаза, в которой клетки обладают повышенной чувствительностью к дифференцировке, укороченный G1 является одной из ключевых характеристик ESC и играет важную роль в поддержании недифференцированных клеток. фенотип. Хотя точный молекулярный механизм остается понятным лишь частично, несколько исследований показали, как быстро ESC проходят через G1 и, возможно, другие фазы.[35]
Клеточный цикл регулируется сложной сетью циклины, циклин-зависимые киназы (Cdk), ингибиторы циклин-зависимых киназ (Cdkn), карманные белки семейства ретинобластомы (Rb) и другие дополнительные факторы.[36] Основополагающее понимание отличительной регуляции клеточного цикла ESC было получено в исследованиях на мышиных ESCs (mESCs).[35] mESCs показали клеточный цикл с сильно сокращенной фазой G1, что позволило клеткам быстро переключаться между фазой M и фазой S. В соматическом клеточном цикле осцилляторная активность комплексов Cyclin-Cdk наблюдается в последовательном действии, которое контролирует важнейшие регуляторы клеточного цикла, чтобы вызвать однонаправленные переходы между фазами: Циклин D и Cdk4 / 6 активны в фазе G1, а Циклин E и Cdk2 активны во время поздней фазы G1 и фазы S; и Циклин А и Cdk2 активны в фазе S и G2, а Циклин Б и Cdk1 активны в фазах G2 и M.[36] Однако в mESCs эта обычно упорядоченная и колебательная активность комплексов Cyclin-Cdk отсутствует. Скорее, комплекс Cyclin E / Cdk2 конститутивно активен на протяжении всего цикла, сохраняя белок ретинобластомы (пРб) гиперфосфорилированный и поэтому неактивен. Это обеспечивает прямой переход от фазы M к поздней фазе G1, что приводит к отсутствию циклинов D-типа и, следовательно, к укороченной фазе G1.[35] Активность Cdk2 важна как для регуляции клеточного цикла, так и для принятия решений о судьбе клеток в mESCs; Подавление активности Cdk2 продлевает прогрессирование фазы G1, устанавливает клеточный цикл, подобный соматическим клеткам, и индуцирует экспрессию маркеров дифференцировки.[37]
В человеческих ESC (hESC) продолжительность G1 резко сокращается. Это было связано с высокими уровнями мРНК G1-связанных генов Cyclin D2 и Cdk4 и низкими уровнями регуляторных белков клеточного цикла, которые ингибируют прогрессирование клеточного цикла в G1, таких как стр.21CipP1, стр. 27Кип1, и p57Kip2.[34][38] Кроме того, регуляторы активности Cdk4 и Cdk6, такие как члены семейства ингибиторов Ink (p15, p16, p18 и p19), экспрессируются на низких уровнях или не экспрессируются совсем. Таким образом, подобно mESC, hESC демонстрируют высокую активность Cdk, при этом Cdk2 демонстрирует самую высокую киназную активность. Также подобно mESCs, hESCs демонстрируют важность Cdk2 в регуляции фазы G1, показывая, что переход G1 в S задерживается, когда активность Cdk2 ингибируется, а G1 останавливается, когда Cdk2 сбивается.[34] Однако, в отличие от мЭСК, чЭСК имеют функциональную фазу G1. hESCs показывают, что активности комплексов Cyclin E / Cdk2 и Cyclin A / Cdk2 зависят от клеточного цикла, и контрольная точка Rb в G1 является функциональной.[36]
ESC также характеризуются нефункциональностью контрольной точки G1, хотя контрольная точка G1 имеет решающее значение для поддержания стабильности генома. В ответ на Повреждение ДНК, ESC не останавливаются в G1 для восстановления повреждений ДНК, а вместо этого зависят от контрольных точек S и G2 / M или подвергаются апоптозу. Отсутствие контрольной точки G1 в ESC позволяет удалять клетки с поврежденной ДНК, тем самым избегая потенциальных мутаций из-за неточной репарации ДНК.[34] В соответствии с этой идеей, ESC сверхчувствительны к повреждению ДНК, чтобы минимизировать мутации, передаваемые следующему поколению.[36]
Плода
Примитивные стволовые клетки, расположенные в органах плоды называются фетальными стволовыми клетками.[39]
Есть два типа фетальных стволовых клеток:
- Собственно стволовые клетки плода происходят из тканей самого плода и обычно получают после аборт. Эти стволовые клетки не бессмертны, но имеют высокий уровень деления и мультипотентны.
- Внеэмбриональные стволовые клетки плода происходят из внеэмбриональные оболочки, и обычно не отличаются от взрослых стволовых клеток. Эти стволовые клетки приобретаются после рождения, они не бессмертны, но имеют высокий уровень клеточного деления и плюрипотентны.[40]
Взрослый
Взрослые стволовые клетки, также называемые соматический (от греческого σωματικóς, «тела») стволовые клетки - это стволовые клетки, которые поддерживают и восстанавливают ткань, в которой они находятся.[41] Их можно встретить как у детей, так и у взрослых.[42]
Есть три известных доступных источника аутологичный взрослые стволовые клетки человека:
- Костный мозг, который требует извлечения сбор урожая, то есть сверление в кости (обычно бедренная кость или же гребень подвздошной кости ).
- Жировая ткань (жировые клетки), которую необходимо извлечь путем липосакции.[43]
- Кровь, которая требует извлечения через аферез, при этом кровь берется у донора (аналогично донорской крови) и проходит через машину, которая извлекает стволовые клетки и возвращает другие части крови донору.
Стволовые клетки также можно взять из пуповинная кровь сразу после рождения. Из всех типов стволовых клеток аутологичный сбор представляет собой наименьший риск. По определению, аутологичные клетки получают из собственного тела, точно так же, как человек может хранить свою кровь для плановых хирургических процедур.
Плюрипотентные взрослые стволовые клетки встречаются редко и, как правило, в небольшом количестве, но их можно найти в пуповинной крови и других тканях.[44] Костный мозг - богатый источник взрослых стволовых клеток,[45] которые использовались для лечения нескольких состояний, включая цирроз печени,[46] хроническая ишемия конечностей[47] сердечная недостаточность в конечной стадии.[48] Количество стволовых клеток костного мозга снижается с возрастом и больше у мужчин, чем у женщин в репродуктивном возрасте.[49] На сегодняшний день большое количество исследований стволовых клеток взрослых нацелено на определение их активности и способности к самообновлению.[50] Повреждения ДНК с возрастом накапливаются как в стволовых клетках, так и в клетках, составляющих среду стволовых клеток. Считается, что это накопление отвечает, по крайней мере частично, за усиление дисфункции стволовых клеток с возрастом (см. Теория повреждений ДНК старения ).[51]
Большинство взрослых стволовых клеток ограничены по происхождению (мультипотентный ) и обычно обозначаются по их тканевому происхождению (мезенхимальные стволовые клетки стволовые клетки, полученные из жировой ткани, эндотелиальные стволовые клетки, стволовые клетки пульпы зуба, так далее.).[52][53] Клетки Muse (многолинейные дифференцирующиеся устойчивые к стрессу клетки) представляют собой недавно открытый тип плюрипотентных стволовых клеток, обнаруженный во многих тканях взрослого человека, включая жировую ткань, дермальные фибробласты и костный мозг. Хотя клетки Muse встречаются редко, их можно идентифицировать по выражению SSEA-3, маркер недифференцированных стволовых клеток и общие маркеры мезенхимальных стволовых клеток, такие как CD105. При культивировании в суспензии единичных клеток клетки будут генерировать кластеры, похожие на эмбриоидные тельца по морфологии, а также по экспрессии генов, включая канонические маркеры плюрипотентности. 4 октября, Sox2, и Наног.[54]
Лечение взрослых стволовыми клетками успешно применялось в течение многих лет для лечения лейкемии и родственного рака костей / крови с помощью трансплантации костного мозга.[55] Взрослые стволовые клетки также используются в ветеринарии для лечения травм сухожилий и связок у лошадей.[56]
Использование взрослых стволовых клеток в исследованиях и терапии не совсем так. спорный как использование эмбриональные стволовые клетки, потому что производство взрослых стволовых клеток не требует разрушения эмбрион. Кроме того, в случаях, когда взрослые стволовые клетки получены от предполагаемого реципиента ( аутотрансплантат ) риск отказа практически отсутствует. Следовательно, правительство США выделяет больше средств на исследования стволовых клеток взрослых.[57]
С ростом потребности в стволовых клетках взрослого человека как для исследовательских, так и для клинических целей (обычно на курс лечения требуется 1–5 миллионов клеток на 1 кг веса тела) становится чрезвычайно важным преодолеть разрыв между необходимостью увеличения количества клеток in vitro. и способность использовать факторы, лежащие в основе репликативного старения. Известно, что взрослые стволовые клетки имеют ограниченную продолжительность жизни in vitro и вступают в репликативное старение почти незаметно после начала культивирования in vitro.[58]
Амниотический
Мультипотентные стволовые клетки также встречаются в амниотическая жидкость. Эти стволовые клетки очень активны, быстро разрастаются без питателей и не являются канцерогенными. Амниотические стволовые клетки являются мультипотентными и могут дифференцироваться в клетках адипогенной, остеогенной, миогенной, эндотелиальной, печеночной, а также нейрональной линий.[59]Амниотические стволовые клетки - предмет активных исследований.
Использование стволовых клеток из амниотическая жидкость преодолевает этические возражения против использования человеческих эмбрионов в качестве источника клеток. Римский католик обучение запрещает использование эмбриональных стволовых клеток в экспериментах; соответственно, Ватикан газета "Оссерваторе Романо «амниотические стволовые клетки назвали« будущим медицины ».[60]
Возможен сбор амниотических стволовых клеток для доноров или для аутологичного использования: первый в США банк амниотических стволовых клеток[61][62] был открыт в 2009 году в Медфорде, Массачусетс, компанией Центр Биоячеек Корпорация[63][64][65] и сотрудничает с различными больницами и университетами по всему миру.[66]
Индуцированный плюрипотентный
У взрослых стволовых клеток есть ограничения по их активности; В отличие от эмбриональные стволовые клетки (ЭСК), они не способны дифференцироваться в клетки всех трех ростковые отростки. Таким образом, они считаются мультипотентный.
Тем не мение, перепрограммирование позволяет создавать плюрипотентные клетки, индуцированные плюрипотентные стволовые клетки (ИПСК) из взрослых клеток. Это не взрослые стволовые клетки, а соматические клетки (например, эпителиальные клетки), перепрограммированные для образования клеток с плюрипотентными способностями. Использование генетического перепрограммирования с белком факторы транскрипции, были получены плюрипотентные стволовые клетки с ESC-подобными способностями.[67][68][69] Первая демонстрация индуцированных плюрипотентных стволовых клеток была проведена Шинья Яманака и его коллеги в Киотский университет.[70] Они использовали факторы транскрипции 3 октября / 4, Sox2, c-Myc, и Klf4 репрограммировать мышиные фибробласты в плюрипотентные клетки.[67][71] Последующие исследования использовали эти факторы для индукции плюрипотентности фибробластных клеток человека.[72] Юйин Юй, Джеймс Томсон, и их коллеги по Университет Висконсина-Мэдисона использовали другой набор факторов, Oct4, Sox2, Nanog и Lin28, и проводили свои эксперименты с использованием клеток человека крайняя плоть.[67][73] Однако они смогли воспроизвести Яманака открытие, что индуцирование плюрипотентности в человеческих клетках возможно.
Индуцированные плюрипотентные стволовые клетки отличаются от эмбриональных стволовых клеток. У них много схожих свойств, например плюрипотентность и дифференцирующий потенциал, выражение плюрипотентность гены эпигенетический узоры эмбриоидное тело и тератома формирование и жизнеспособный химера формирование[70][71] но в этих свойствах есть много различий. Хроматин ИПСК, по-видимому, более «закрытый» или метилированный, чем хроматин ЭСК.[70][71] Точно так же паттерн экспрессии генов между ESC и iPSC, или даже iPSC, происходящий из разного происхождения.[70] Таким образом, возникают вопросы о "полноте" перепрограммирование и соматическая память индуцированных плюрипотентных стволовых клеток. Несмотря на это, индукция плюрипотентности соматических клеток представляется жизнеспособной.
В результате успеха этих экспериментов, Ян Вилмут, который помог создать первое клонированное животное Овечка Долли, объявил, что оставит перенос ядра соматической клетки как направление исследования.[74]
IPSC значительно помогли области медицины, найдя множество способов лечения болезней. Поскольку человеческий IPSCc дал преимущество в создании моделей пробирки для изучения токсинов и патогенеза.[75]
Кроме того, индуцированные плюрипотентные стволовые клетки обеспечивают несколько терапевтических преимуществ. Как и ESC, они плюрипотентный. Таким образом, у них есть большой потенциал дифференциации; теоретически они могут производить любую клетку в человеческом теле (если перепрограммирование чтобы плюрипотентность была "полной").[70] Более того, в отличие от ESC, они потенциально могут позволить врачам создать линию плюрипотентных стволовых клеток для каждого отдельного пациента.[76] Замороженные образцы крови можно использовать в качестве ценного источника индуцированных плюрипотентных стволовых клеток.[77] Стволовые клетки, специфичные для пациента, позволяют выявить побочные эффекты перед медикаментозным лечением, а также снизить риск отторжения трансплантации.[76] Несмотря на их ограниченное терапевтическое использование в настоящее время, ИПСК создают потенциал для будущего использования в лечении и исследованиях.
Контроль клеточного цикла
Ключевые факторы, контролирующие клеточный цикл, также регулируют плюрипотентность. Таким образом, манипулирование соответствующими генами может поддерживать плюрипотентность и перепрограммировать соматические клетки до индуцированного плюрипотентного состояния.[36] Однако репрограммирование соматических клеток часто малоэффективно и считается стохастический.[78]
Идея о том, что более быстрый клеточный цикл является ключевым компонентом плюрипотентности, может повысить эффективность перепрограммирования. Методы улучшения плюрипотентности посредством манипуляции с регуляторами клеточного цикла включают: сверхэкспрессию Cyclin D / Cdk4, фосфорилирование Sox2 на S39 и S253, сверхэкспрессия Cyclin A и Cyclin E, нокдаун Rb и нокдаун членов Cip / Кип семья или семья Инк.[36] Более того, эффективность репрограммирования коррелирует с числом клеточных делений, произошедших во время стохастической фазы, о чем свидетельствует растущая неэффективность репрограммирования старых или медленно ныряющих клеток.[79]
Происхождение
Линия - важная процедура для анализа развивающихся эмбрионов. Поскольку клеточные линии показывают взаимосвязь между клетками при каждом делении. Это помогает в процессе анализа клонов стволовых клеток, что помогает распознать эффективность стволовых клеток, продолжительность жизни и другие факторы. С помощью метода клеточной линии мутантные гены могут быть проанализированы в клонах стволовых клеток, которые могут помочь в генетических путях. Эти пути могут регулировать работу стволовых клеток.[80]
Чтобы обеспечить самообновление, стволовые клетки подвергаются двум типам деления клеток (см. Деление и дифференциация стволовых клеток диаграмму). Симметричное деление дает две идентичные дочерние клетки, обе наделенные свойствами стволовых клеток. Асимметричное деление, с другой стороны, дает только одну стволовую клетку и клетка-предшественница с ограниченным потенциалом самообновления. Прародители могут пройти несколько раундов клеточного деления, прежде чем окончательно дифференцирующий в зрелую клетку. Возможно, что молекулярное различие между симметричными и асимметричными делениями заключается в дифференциальной сегрегации белков клеточной мембраны (таких как рецепторы ) между дочерними клетками.[81]
Альтернативная теория состоит в том, что стволовые клетки остаются недифференцированными из-за сигналов окружающей среды в их конкретных ниша. Стволовые клетки дифференцируются, когда они покидают эту нишу или больше не получают эти сигналы. Исследования в Дрозофила germarium идентифицировали сигналы декапентаплегический и адгезивные соединения, которые препятствуют дифференцировке стволовых клеток гермария.[82][83]
Терапии
Терапия стволовыми клетками - это использование стволовых клеток для лечения или предотвращения заболевания или состояния. Пересадка костного мозга это форма терапии стволовыми клетками, которая используется в течение многих лет, поскольку доказала свою эффективность в клинических испытаниях.[84][85]
Имплантация стволовых клеток может помочь в укреплении левого желудочка сердца, а также в сохранении сердечной ткани пациентам, перенесшим сердечные приступы в прошлом.[86]
Преимущества
Лечение стволовыми клетками может снизить симптомы заболевания или состояния, которое лечится. Снижение симптомов может позволить пациентам снизить потребление лекарств от болезни или состояния. Лечение стволовыми клетками также может дать обществу знания для дальнейшего понимания стволовых клеток и будущих методов лечения.[87][88]
Недостатки
Лечение стволовыми клетками может потребовать иммуносупрессия из-за необходимости облучения перед трансплантацией для удаления предыдущих клеток человека или из-за того, что иммунная система пациента может нацеливаться на стволовые клетки. Один из способов избежать второй возможности - использовать стволовые клетки того же пациента, которого лечат.
Плюрипотентность некоторых стволовых клеток также может затруднить получение определенного типа клеток. Также трудно получить точный необходимый тип клеток, потому что не все клетки в популяции дифференцируются равномерно. Недифференцированные клетки могут создавать ткани, отличные от желаемых типов.[89]
Некоторые стволовые клетки после трансплантации образуют опухоли;[90] плюрипотентность связана с образованием опухолей, особенно в эмбриональных стволовых клетках, собственных стволовых клетках плода, индуцированных плюрипотентных стволовых клетках. Собственно стволовые клетки плода, несмотря на мультипотентность, образуют опухоли.[91]
Туризм стволовых клеток
Туризм со стволовыми клетками - это интернет-индустрия, в которой процедуры со стволовыми клетками рекламируются общественности как проверенное лекарство.[92] в большинстве случаев это приводит к тому, что пациенты и семьи путешествуют за границу для получения процедур, которые не доказаны, или являются частью клинических испытаний, одобренных FDA. Эти процедуры не прошли проверку клинических исследований и не имеют строгой научной поддержки. Хотя для широкой публики эта реклама может показаться авторитетной, для переводчиков и ученых это приводит к эксплуатации уязвимых пациентов. Этим процедурам не хватает воспроизводимости, необходимой строгости. Хотя этот термин может означать путешествия на большие расстояния, в последние годы в США произошел взрывной рост «клиник стволовых клеток», что хорошо задокументировано. Эти виды деятельности очень прибыльны для клиники, но не приносят пользы для пациентов, иногда испытывающих трудности. такие осложнения, как опухоли позвоночника[93], смерть или финансовый крах, все это задокументировано в научной литературе[94]. Существует большой интерес к просвещению общественности и пациентов, семей и врачей, которые имеют дело с пациентами, обращающимися в клиники стволовых клеток.[95].
Несмотря на большой интерес общественности к использованию стволовых клеток, среди всех ученых стволовых клеток, включая Международное общество исследования стволовых клеток, крупнейшая академическая организация ученых и сторонников исследований стволовых клеток в мире[96]. Терапия стволовыми клетками все еще находится в стадии разработки, и хотя во всем мире проводится множество исследований.[97]. Строгие испытания стволовых клеток все еще продолжаются, и пациенты должны быть осведомлены о неэтичных клиниках в США или за рубежом, которые предлагают процедуры стволовыми клетками в качестве лекарства, когда это все еще расследуется.[98].
Исследование
Некоторые из фундаментальных патенты покрывающие человеческие эмбриональные стволовые клетки принадлежат Фонд исследований выпускников Висконсина (WARF) - это патенты 5,843,780, 6,200,806 и 7,029,913, изобретенные Джеймс А. Томсон. WARF не применяет эти патенты против академических ученых, но применяет их против компаний.[99]
В 2006 г. запрос на Бюро патентов и товарных знаков США (USPTO) о пересмотре трех патентов была подана Общественный Патентный Фонд от имени своего клиента, некоммерческая группа по надзору за патентами Consumer Watchdog (ранее - Фонд защиты прав налогоплательщиков и потребителей).[99] В процессе повторной экспертизы, который включает в себя несколько раундов обсуждения между ВПТЗ США и сторонами, ВПТЗ США первоначально согласовало с Consumer Watchdog и отклонило все претензии во всех трех патентах,[100] однако в ответ WARF внесла поправки в формулы всех трех патентов, чтобы сделать их более узкими, и в 2008 году USPTO признало измененные формулы во всех трех патентах патентоспособными. Решение по одному из патентов (7 029 913) может быть обжаловано, а по двум другим - нет.[101][102] Consumer Watchdog подала апелляцию на выдачу патента '913 в Совет по патентным апелляциям и вмешательствам USPTO (BPAI), который удовлетворил апелляцию, и в 2010 году BPAI решило, что измененные формулы патента' 913 не подлежат патентованию.[103] Тем не менее, WARF смогла возобновить судебное преследование по делу и сделала это, снова изменив требования патента 913, чтобы сделать их более узкими, и в январе 2013 года измененные требования были разрешены.[104]
В июле 2013 года Consumer Watchdog объявила, что подаст апелляцию на решение удовлетворить требования патента 913 в США. Апелляционный суд федерального округа (CAFC), федеральный апелляционный суд, рассматривающий патентные дела.[105] На слушаниях в декабре 2013 года CAFC подняла вопрос о том, была ли у Consumer Watchdog правовой статус подавать апелляцию; дело не могло продолжаться, пока эта проблема не была решена.[106]
Расследования

Заболевания и состояния, при которых исследуется лечение стволовыми клетками, включают:
- Сахарный диабет[107]
- Андрогенная алопеция и выпадение волос[108][109]
- Ревматоидный артрит[107]
- болезнь Паркинсона[107]
- Болезнь Альцгеймера[107]
- Остеоартроз[107]
- Гладить и травматическое повреждение мозга ремонт[110]
- Нарушение обучаемости из-за врожденное заболевание[111]
- Повреждение спинного мозга ремонт[112]
- Инфаркт сердца[113]
- Анти-рак лечение[114]
- Облысение разворот[115]
- Заменить отсутствующий зубы[116]
- Ремонт слушание[117]
- Восстановить зрение[118] и отремонтировать повреждение роговица[119]
- Боковой амиотрофический склероз[120]
- болезнь Крона[121]
- Лечение раны[122]
- Мужское бесплодие из-за отсутствия сперматогониальных стволовых клеток.[123] В недавних исследованиях ученые нашли способ решить эту проблему, перепрограммировав клетку и превратив ее в сперматозоид. Другие исследования доказали восстановление сперматогенеза путем введения клеток ИПСК человека в яички мышей. Это может означать конец азооспермия.[124]
- Женское бесплодие: ооциты, полученные из эмбриональных стволовых клеток. Ученые обнаружили стволовые клетки яичников - редкий тип клеток (0,014%), обнаруженный в яичниках. Их можно использовать для лечения не только бесплодия, но и преждевременной недостаточности яичников.[125]
Ведутся исследования по разработке различных источников стволовых клеток и применению лечения стволовыми клетками для нейродегенеративные заболевания и условия, сахарный диабет, сердечное заболевание, и другие условия.[126] Также ведутся исследования по созданию органоиды использование стволовых клеток, что позволит лучше понять развитие человека, органогенез, и моделирование болезней человека.[127]
В последние годы благодаря способности ученых изолировать и культивировать эмбриональные стволовые клетки и с растущей способностью ученых создавать стволовые клетки, используя перенос ядра соматической клетки и методы создания индуцированные плюрипотентные стволовые клетки, закрались споры, оба связаны с политика абортов и чтобы клонирование человека.
Гепатотоксичность и вызванное лекарственным средством поражение печени является причиной значительного числа неудач в разработке новых лекарств и их вывода с рынка, что подчеркивает необходимость проведения скрининговых анализов, таких как полученные из стволовых клеток гепатоцитоподобные клетки, которые способны обнаруживать токсичность на ранней стадии разработка лекарств процесс.[128]
Смотрите также
Рекомендации
- ^ а б Атала А., Ланза Р. (31 декабря 2012 г.). Справочник по стволовым клеткам. Академическая пресса. п. 452. ISBN 978-0-12-385943-3.
- ^ Беккер AJ, McCULLOCH EA, Till JE (февраль 1963 г.). «Цитологическая демонстрация клональной природы колоний селезенки, полученных из трансплантированных клеток костного мозга мыши». Природа. 197 (4866): 452–4. Bibcode:1963Натура.197..452Б. Дои:10.1038 / 197452a0. HDL:1807/2779. PMID 13970094. S2CID 11106827.
- ^ Симинович Л., Маккулок Э.А., Тиль Дж. Э. (декабрь 1963 г.). «Распределение колониеобразующих клеток среди колоний селезенки». Журнал клеточной и сравнительной физиологии. 62 (3): 327–36. Дои:10.1002 / jcp.1030620313. HDL:1807/2778. PMID 14086156. S2CID 43875977.
- ^ Мюллер А.М., Хупперц С., Хеншлер Р. (июль 2016 г.). «Гематопоэтические стволовые клетки в регенеративной медицине: заблудшие или в пути?». Трансфузионная медицина и гемотерапия. 43 (4): 247–254. Дои:10.1159/000447748. ЧВК 5040947. PMID 27721700.
- ^ Ральстон, Мишель (17 июля 2008 г.). «Исследования стволовых клеток во всем мире». Форум Pew о религии и общественной жизни. Pew Research Center. Архивировано из оригинал 9 ноября 2008 г.. Получено 13 апреля, 2009.
- ^ Tuch BE (сентябрь 2006 г.). «Стволовые клетки - клиническое обновление» (PDF). Австралийский семейный врач. 35 (9): 719–21. PMID 16969445.
- ^ а б Феррейра Л. (03.01.2014). «Стволовые клетки: краткая история и перспективы». Стволовые клетки: краткая история и перспективы - наука в новостях. WordPress. Получено 3 декабря 2019.
- ^ а б «О происхождении термина» стволовая клетка"". Стволовая клетка. Получено 2020-11-04.
- ^ Макферсон К. «Случайное открытие стволовых клеток». Новости США. Университет Саскачевана. Получено 3 декабря 2019.
- ^ Авария на реакторе Винча, 1958 г. В архиве 27 января 2011 г. Wayback Machine, составленный Wm. Роберт Джонстон
- ^ Шэнхуэй, Х. Э., Накада, Д., и Моррисон, С. Дж. (2009). Механизмы самообновления стволовых клеток. Ежегодный обзор клетки и развития, 25, 377–406.
- ^ Конг Ю.С., Райт В.Е., Шей Дж.В. (сентябрь 2002 г.). «Теломераза человека и ее регуляция». Обзоры микробиологии и молекулярной биологии. 66 (3): 407–25, содержание. Дои:10.1128 / MMBR.66.3.407-425.2002. ЧВК 120798. PMID 12208997.
- ^ а б c d е ж Schöler HR (2007). «Возможности стволовых клеток: перечень». У Николауса Кнопфлера, Дагмар Шипански, Стефана Лоренца Зоргнера (ред.). Человеческие биотехнологии как социальный вызов. Издательство Ashgate. п. 28. ISBN 978-0-7546-5755-2.
- ^ Миталипов С., Вольф Д. (2009). «Тотипотентность, плюрипотентность и ядерное репрограммирование». Инженерия стволовых клеток. Достижения в области биохимической инженерии / биотехнологии. 114. С. 185–99. Bibcode:2009esc..book..185M. Дои:10.1007/10_2008_45. ISBN 978-3-540-88805-5. ЧВК 2752493. PMID 19343304.
- ^ Ulloa-Montoya F, Verfaillie CM, Hu WS (июль 2005 г.). «Системы культивирования плюрипотентных стволовых клеток». Журнал биологии и биоинженерии. 100 (1): 12–27. Дои:10.1263 / jbb.100.12. PMID 16233846.
- ^ Friedenstein AJ, Deriglasova UF, Kulagina NN, Panasuk AF, Rudakowa SF, Luriá EA, Ruadkow IA (1974). «Предшественники фибробластов в различных популяциях гемопоэтических клеток, обнаруженные методом анализа колоний in vitro». Экспериментальная гематология. 2 (2): 83–92. PMID 4455512.
- ^ Фриденштейн А.Ю., Горская Ю.Ф., Кулагина Н.Н. (сентябрь 1976 г.). «Предшественники фибробластов в нормальных и облученных кроветворных органах мышей». Экспериментальная гематология. 4 (5): 267–74. PMID 976387.
- ^ Сехар Л., Бишт Н. (01.09.2006). «Терапия стволовыми клетками». Аполлон Медицина. 3 (3): 271–276. Дои:10.1016 / S0976-0016 (11) 60209-3.
- ^ Томсон Дж. А., Ицковиц-Элдор Дж., Шапиро С. С., Вакниц М. А., Свиергиль Дж. Дж., Маршалл В. С., Джонс Дж. М. (ноябрь 1998 г.). «Линии эмбриональных стволовых клеток, полученные из бластоцист человека». Наука. 282 (5391): 1145–7. Bibcode:1998Научный ... 282.1145Т. Дои:10.1126 / science.282.5391.1145. PMID 9804556.
- ^ а б Гилберт С.Ф. (2014). Биология развития (Десятое изд.). Сандерленд, Массачусетс: Sinauer. ISBN 978-0878939787.
- ^ Ракич П. (октябрь 2009 г.). «Эволюция неокортекса: взгляд из биологии развития». Обзоры природы. Неврология. 10 (10): 724–35. Дои:10.1038 / nrn2719. ЧВК 2913577. PMID 19763105.
- ^ Noctor SC, Flint AC, Weissman TA, Dammerman RS, Kriegstein AR (февраль 2001 г.). «Нейроны, происходящие из радиальных глиальных клеток, устанавливают радиальные единицы в неокортексе». Природа. 409 (6821): 714–20. Bibcode:2001Натура.409..714Н. Дои:10.1038/35055553. PMID 11217860. S2CID 3041502.
- ^ Ying QL, Wray J, Nichols J, Batlle-Morera L, Doble B, Woodgett J, Cohen P, Smith A (май 2008 г.). «Основное состояние самообновления эмбриональных стволовых клеток». Природа. 453 (7194): 519–23. Bibcode:2008Натура.453..519л. Дои:10.1038 / природа06968. ЧВК 5328678. PMID 18497825.
- ^ «Культура эмбриональных стволовых клеток человека (hESC)». Национальные институты здоровья. Архивировано из оригинал на 2010-01-06. Получено 2010-03-07.
- ^ Палаты I, Колби Д., Робертсон М., Николс Дж., Ли С., Твиди С., Смит А. (май 2003 г.). «Клонирование функциональной экспрессии Nanog, фактора поддержания плюрипотентности в эмбриональных стволовых клетках». Клетка. 113 (5): 643–55. Дои:10.1016 / S0092-8674 (03) 00392-1. HDL:1842/843. PMID 12787505. S2CID 2236779.
- ^ Бойер Л.А., Ли Т.И., Коул М.Ф., Джонстон С.Е., Левин С.С., Цукер Дж.П., Гюнтер М.Г., Кумар Р.М., Мюррей Х.Л., Дженнер Р.Г., Гиффорд Д.К., Мелтон Д.А., Джениш Р., Янг Р.А. (сентябрь 2005 г.). «Основная схема регуляции транскрипции в эмбриональных стволовых клетках человека». Клетка. 122 (6): 947–56. Дои:10.1016 / j.cell.2005.08.020. ЧВК 3006442. PMID 16153702.
- ^ Адевуми О., Афлатуниан Б., Арлунд-Рихтер Л., Амит М., Эндрюс П. В., Бейтон Г. и др. (Международная инициатива по стволовым клеткам) (июль 2007 г.). «Характеристика линий эмбриональных стволовых клеток человека Международной инициативой по стволовым клеткам». Природа Биотехнологии. 25 (7): 803–16. Дои:10.1038 / nbt1318. PMID 17572666. S2CID 13780999.
- ^ Махла RS (2016). «Применение стволовых клеток в регенеративной медицине и терапии болезней». Международный журнал клеточной биологии. 2016 (7): 1–24. Дои:10.1155/2016/6940283. ЧВК 4969512. PMID 27516776.
- ^ Уинслоу Р., Манди А. (23 января 2009 г.). «Первое испытание эмбриональных стволовых клеток одобрено FDA». Журнал "Уолл Стрит.
- ^ "Терапия эмбриональными стволовыми клетками в опасности? Клинические испытания Geron завершены". ScienceDebate.com. Получено 2011-12-11.
- ^ Ву, округ Колумбия, Бойд А.С., Вуд К.Дж. (май 2007 г.). «Трансплантация эмбриональных стволовых клеток: возможность применения в заместительной клеточной терапии и регенеративной медицине». Границы биологических наук. 12 (8–12): 4525–35. Дои:10.2741/2407. PMID 17485394. S2CID 6355307.
- ^ а б Зомер HD, Видане А.С., Гонсалвес Н.Н., Амброзио CE (2015-09-28). «Мезенхимальные и индуцированные плюрипотентные стволовые клетки: общие сведения и клинические перспективы». Стволовые клетки и клонирование. 8: 125–34. Дои:10.2147 / SCCAA.S88036. ЧВК 4592031. PMID 26451119.
- ^ Каплан А.И. (сентябрь 1991 г.). «Мезенхимальные стволовые клетки». Журнал ортопедических исследований. 9 (5): 641–50. Дои:10.1002 / jor.1100090504. PMID 1870029. S2CID 22606668.
- ^ а б c d е ж Коледова З., Кремер А., Кафкова Л.Р., Дивоки В. (ноябрь 2010 г.). «Регуляция клеточного цикла в эмбриональных стволовых клетках: центросомные решения о самообновлении». Стволовые клетки и развитие. 19 (11): 1663–78. Дои:10.1089 / scd.2010.0136. PMID 20594031.
- ^ а б c d Барта Т, Долезалова Д, Голубцова З, Хампл А (март 2013). «Регуляция клеточного цикла в человеческих эмбриональных стволовых клетках: ссылки на адаптацию к культуре клеток». Экспериментальная биология и медицина. 238 (3): 271–5. Дои:10.1177/1535370213480711. PMID 23598972. S2CID 2028793.
- ^ а б c d е ж грамм Завери Л., Дхаван Дж. (2018). «Езда на велосипеде навстречу судьбе: соединение плюрипотентности с клеточным циклом». Границы клеточной биологии и биологии развития. 6: 57. Дои:10.3389 / fcell.2018.00057. ЧВК 6020794. PMID 29974052.
- ^ Коледова З., Кафкова Л.Р., Калабкова Л., Кристоф В., Долезель П., Дивоки В. (февраль 2010 г.). «Ингибирование Cdk2 продлевает прогрессирование фазы G1 в эмбриональных стволовых клетках мыши». Стволовые клетки и развитие. 19 (2): 181–94. Дои:10.1089 / scd.2009.0065. PMID 19737069.
- ^ Беккер К.А., Гуле П.Н., Терриен Дж. А., Лиан Дж. Б., Штейн Дж. Л., ван Вейнен А. Дж., Стейн Г. С. (декабрь 2006 г.). «Самообновление эмбриональных стволовых клеток человека поддерживается за счет укороченной фазы клеточного цикла G1». Журнал клеточной физиологии. 209 (3): 883–93. Дои:10.1002 / jcp.20776. PMID 16972248. S2CID 24908771.
- ^ Арифф Бонгсо; Энг Хин Ли, ред. (2005). «Стволовые клетки: их определение, классификация и источники». Стволовые клетки: от настольного компьютера к постели больного. World Scientific. п.5. ISBN 978-981-256-126-8. OCLC 443407924.
- ^ Мур, К.Л., Т.В.Н. Персо и А.Г. Торчиа. До нашего рождения: основы эмбриологии и врожденных пороков. Филадельфия, Пенсильвания: Сондерс, Эльзевир. 2013. Печать
- ^ "Стволовые клетки" Клиника Мэйо. Фонд медицинского образования и исследований Мэйо без даты Web. 23 марта 2013 г.
- ^ Jiang Y, Jahagirdar BN, Reinhardt RL, Schwartz RE, Keene CD, Ortiz-Gonzalez XR, Reyes M, Lenvik T, Lund T, Blackstad M, Du J, Aldrich S, Lisberg A, Low WC, Largaespada DA, Verfaillie CM ( Июль 2002 г.). «Плюрипотентность мезенхимальных стволовых клеток, полученных из костного мозга взрослых». Природа. 418 (6893): 41–9. Дои:10.1038 / природа00870. PMID 12077603. S2CID 47162269.
- ^ Кафлин Р.П., Олдвейлер А., Микельсон Д.Т., Мурман СТ (октябрь 2017 г.). «Техника трансплантации жировых стволовых клеток при дегенеративном заболевании суставов». Методы артроскопии. 6 (5): e1761 – e1766. Дои:10.1016 / j.eats.2017.06.048. ЧВК 5795060. PMID 29399463.
- ^ Ратайчак MZ, Machalinski B, Wojakowski W, Ratajczak J, Kucia M (май 2007 г.). «Гипотеза эмбрионального происхождения плюрипотентных стволовых клеток Oct-4 (+) в костном мозге и других тканях взрослых». Лейкемия. 21 (5): 860–7. Дои:10.1038 / sj.leu.2404630. PMID 17344915.
- ^ Нарасипура С.Д., Войцеховски Дж. К., Чарльз Н., Лисвельд Дж. Л., Король М. Р. (январь 2008 г.). «Микропробирка с покрытием P-Selectin для обогащения CD34 + гемопоэтических стволовых клеток и клеток-предшественников из костного мозга человека». Клиническая химия. 54 (1): 77–85. Дои:10.1373 / Clinchem.2007.089896. PMID 18024531.
- ^ Тераи С., Исикава Т., Омори К., Аояма К., Марумото Ю., Урата Ю., Йокояма Ю., Утида К., Ямасаки Т., Фудзи Ю., Окита К., Сакаида И. (октябрь 2006 г.). «Улучшение функции печени у пациентов с циррозом печени после инфузионной терапии аутологичных клеток костного мозга». Стволовые клетки. 24 (10): 2292–8. Дои:10.1634 / стволовые клетки.2005-0542. PMID 16778155. S2CID 5649484.
- ^ Субрамманийан Р., Амалорпаванатан Дж., Шанкар Р., Раджкумар М., Баскар С., Манджунатх С.Р., Сентилкумар Р., Муруган П., Шринивасан В.Р., Абрахам С. (сентябрь 2011 г.). «Применение аутологичных мононуклеарных клеток костного мозга у шести пациентов с хронической критической ишемией конечностей в результате диабета: наш опыт». Цитотерапия. 13 (8): 993–9. Дои:10.3109/14653249.2011.579961. PMID 21671823.
- ^ Мадхусанкар Н (2007). «Использование стволовых клеток, полученных из костного мозга, у пациентов с сердечно-сосудистыми заболеваниями». Журнал стволовых клеток и регенеративной медицины. 3 (1): 28–9. ЧВК 3908115. PMID 24693021.
- ^ Дедепия В.Д., Рао Й.Й., Джаякришнан Г.А., Партибан Дж. К., Баскар С., Манджунатх С. Р., Сентилкумар Р., Абрахам С. Дж. (2012). «Индекс CD34 + клеток и мононуклеарных клеток в костном мозге у пациентов с травмой спинного мозга разных возрастных групп: сравнительный анализ». Исследование костного мозга. 2012: 1–8. Дои:10.1155/2012/787414. ЧВК 3398573. PMID 22830032.
- ^ Гарднер Р.Л. (март 2002 г.). «Стволовые клетки: сила, пластичность и общественное восприятие». Журнал анатомии. 200 (Pt 3): 277–82. Дои:10.1046 / j.1469-7580.2002.00029.x. ЧВК 1570679. PMID 12033732.
- ^ Беренс А., ван Дерсен Дж. М., Рудольф К. Л., Шумахер Б. (март 2014 г.). «Влияние повреждения генома и старения на функцию стволовых клеток». Природа клеточной биологии. 16 (3): 201–7. Дои:10.1038 / ncb2928. ЧВК 4214082. PMID 24576896.
- ^ Баррилло Б., Финни Д. Г., Прокоп Д. Д., О'Коннор К. К. (ноябрь 2006 г.). «Обзор: инженерия ex vivo живых тканей с помощью взрослых стволовых клеток». Тканевая инженерия. 12 (11): 3007–19. CiteSeerX 10.1.1.328.2873. Дои:10.1089 / десять.2006.12.3007. PMID 17518617.
- ^ Гимбл Дж. М., Кац А. Дж., Баннелл Б. А. (май 2007 г.). «Стволовые клетки жирового происхождения для регенеративной медицины». Циркуляционные исследования. 100 (9): 1249–60. Дои:10.1161 / 01.RES.0000265074.83288.09. ЧВК 5679280. PMID 17495232.
- ^ Курода Я., Китада М., Вакао С., Нисикава К., Танимура Ю., Макиносима Х, Года М., Акаси Х., Инуцука А., Нива А, Сигемото Т., Набешима Ю., Накахата Т., Набешима Ю., Фудзиёси Ю., Дезава М. (май 2010 г. ). «Уникальные мультипотентные клетки в популяциях мезенхимальных клеток взрослого человека». Труды Национальной академии наук Соединенных Штатов Америки. 107 (19): 8639–43. Bibcode:2010PNAS..107.8639K. Дои:10.1073 / pnas.0911647107. ЧВК 2889306. PMID 20421459.
- ^ "Пересадка костного мозга". ucsfchildrenshospital.org.
- ^ Кейн, Эд (2008-05-01). «Терапия стволовыми клетками перспективна при травмах и заболеваниях мягких тканей лошади». DVM Newsmagazine. Получено 2008-06-12.
- ^ «Часто задаваемые вопросы о стволовых клетках». Министерство здравоохранения и социальных служб США. 2004-07-14. Архивировано из оригинал на 2009-01-09.
- ^ Оливейра PH, да Силва CL, Кабрал JM (2014). «Геномная нестабильность в стволовых клетках человека: текущее состояние и будущие проблемы». Стволовые клетки. 32 (11): 2824–2832. Дои:10.1002 / шток.1796. PMID 25078438. S2CID 41335566.
- ^ Де Коппи П., Барч Г., Сиддики М.М., Сюй Т., Сантос С.К., Перин Л., Мостославский Г., Серр А.С., Снайдер Е.Ю., Ю Дж.Дж., Фурт М.Э., Сокер С., Атала А. (январь 2007 г.). «Выделение линий амниотических стволовых клеток с потенциалом терапии». Природа Биотехнологии. 25 (1): 100–6. Дои:10.1038 / nbt1274. PMID 17206138. S2CID 6676167.
- ^ «Газета Ватикана называет новый источник стволовых клеток« будущим медицины »:: Католическое информационное агентство (CNA)». Католическое информационное агентство. 2010-02-03. Получено 2010-03-14.
- ^ «Центр биоклеток европейской биотехнологической компании открывает первое в США предприятие по сохранению амниотических стволовых клеток в Медфорде, штат Массачусетс». Рейтер. 2009-10-22. Архивировано из оригинал на 2009-10-30. Получено 2010-03-14.
- ^ «Европейский центр Biocell открывает офис в Медфорде - Daily Business Update». Бостонский глобус. 2009-10-22. Получено 2010-03-14.
- ^ "Тикер". BostonHerald.com. 2009-10-22. Получено 2010-03-14.
- ^ «Центр Biocell открывает банк амниотических стволовых клеток в Медфорде». Массовые новости бизнеса в сфере высоких технологий. 2009-10-23. Архивировано из оригинал на 2012-10-14. Получено 2012-08-26.
- ^ «Первый в мире банк амниотических стволовых клеток открывается в Медфорде». wbur.org. Получено 2010-03-14.
- ^ «Корпорация Biocell Center в партнерстве с крупнейшей сетью местных больниц Новой Англии предлагает уникальный ...» Медфорд, Массачусетс: Prnewswire.com. Получено 2010-03-14.
- ^ а б c «Изготовление эмбриональных стволовых клеток человека». Экономист. 2007-11-22.
- ^ Бренд М, Палка Дж, Коэн А (2007-11-20). «Клетки кожи могут превращаться в эмбриональные стволовые клетки». Национальное общественное радио.
- ^ «Прорыв, который радикально изменит дебаты о стволовых клетках». Час новостей с Джимом Лерером. 2007-11-20.
- ^ а б c d е Kimbrel EA, Lanza R (декабрь 2016 г.). «Плюрипотентные стволовые клетки: последние 10 лет». Регенеративная медицина. 11 (8): 831–847. Дои:10.2217 / rme-2016-0117. PMID 27908220.
- ^ а б c Такахаши К., Яманака С. (август 2006 г.). «Индукция плюрипотентных стволовых клеток из эмбриональных и взрослых культур фибробластов мыши с помощью определенных факторов». Клетка. 126 (4): 663–76. Дои:10.1016 / j.cell.2006.07.024. HDL:2433/159777. PMID 16904174. S2CID 1565219.
- ^ Такахаши К., Танабе К., Охнуки М., Нарита М., Ичисака Т., Томода К., Яманака С. (ноябрь 2007 г.). «Индукция плюрипотентных стволовых клеток из фибробластов взрослого человека определенными факторами». Клетка. 131 (5): 861–72. Дои:10.1016 / j.cell.2007.11.019. HDL:2433/49782. PMID 18035408. S2CID 8531539.
- ^ Ю. Дж., Водяник М. А., Смуга-Отто К., Антосевич-Бурже Дж., Френ Дж. Л., Тиан С., Ни Дж., Джонсдоттир Г. А., Руотти В., Стюарт Р., Слуквин И. И., Томсон Дж. А. (декабрь 2007 г.). «Индуцированные линии плюрипотентных стволовых клеток, полученные из соматических клеток человека». Наука. 318 (5858): 1917–20. Bibcode:2007Научный ... 318.1917Y. Дои:10.1126 / science.1151526. PMID 18029452. S2CID 86129154.
- ^ "Его вдохновение исходит из исследования профессора Шинья Яманака в Киотский университет, который предлагает способ создания стволовых клеток человеческого эмбриона без необходимости в человеческих яйцеклетках, которых очень мало, и без необходимости создавать и уничтожать клонированные человеческие эмбрионы, что категорически противостоит движению за жизнь ".Highfield R (16 ноября 2007 г.). «Создатель Dolly профессор Ян Уилмут избегает клонирования». Телеграф. Лондон.
- ^ Мальдонадо М., Луу Р.Дж., Ико Дж., Оспина А., Мён Д., Ши ХП, Нам Дж. (Сентябрь 2017 г.). «Специфическая механомодуляция клонов и стадий развития индуцированной дифференцировки плюрипотентных стволовых клеток». Исследования стволовых клеток и терапия. 8 (1): 216. Дои:10.1186 / s13287-017-0667-2. ЧВК 5622562. PMID 28962663.
- ^ а б Робинтон Д.А., Дейли GQ (январь 2012 г.). «Перспективы индуцированных плюрипотентных стволовых клеток в исследованиях и терапии». Природа. 481 (7381): 295–305. Bibcode:2012Натура.481..295р. Дои:10.1038 / природа10761. ЧВК 3652331. PMID 22258608.
- ^ Стерк Дж., Давлати М.М., Гао К., Мэтцель Д., Ханна Дж., Соммер К.А., Мостославский Г., Яениш Р. (июль 2010 г.). «Перепрограммирование клеток периферической крови человека в индуцированные плюрипотентные стволовые клетки». Стволовая клетка. 7 (1): 20–4. Дои:10.1016 / j.stem.2010.06.002. ЧВК 2917234. PMID 20621045. Сложить резюме – ScienceDaily.
- ^ Чен Х, Хартман А, Го С (01.09.2015). «Выбор клеточной судьбы посредством динамического клеточного цикла». Текущие отчеты о стволовых клетках. 1 (3): 129–138. Дои:10.1007 / s40778-015-0018-0. ЧВК 5487535. PMID 28725536.
- ^ Хиндли С., Филпотт А. (апрель 2013 г.). «Клеточный цикл и плюрипотентность». Биохимический журнал. 451 (2): 135–43. Дои:10.1042 / BJ20121627. ЧВК 3631102. PMID 23535166.
- ^ "Анализ происхождения стволовых клеток | StemBook". www.stembook.org. Получено 2020-04-20.
- ^ Бекманн Дж., Шайца С., Вернет П., Фишер Дж. К., Гибель Б. (июнь 2007 г.). «Асимметричное деление клеток в компартменте человеческих гемопоэтических стволовых клеток и клеток-предшественников: идентификация асимметрично сегрегационных белков». Кровь. 109 (12): 5494–501. Дои:10.1182 / кровь-2006-11-055921. PMID 17332245.
- ^ Се Т., Spradling AC (июль 1998 г.). «decapentaplegic необходим для поддержания и деления стволовых клеток зародышевой линии в яичнике дрозофилы». Клетка. 94 (2): 251–60. Дои:10.1016 / S0092-8674 (00) 81424-5. PMID 9695953. S2CID 11347213.
- ^ Song X, Zhu CH, Doan C, Xie T (июнь 2002 г.). «Стволовые клетки зародышевой линии закреплены сращениями в нишах яичников дрозофилы». Наука. 296 (5574): 1855–7. Bibcode:2002Sci ... 296.1855S. Дои:10.1126 / science.1069871. PMID 12052957. S2CID 25830121.
- ^ Ян Мурнаган для исследования стволовых клеток. Обновлено: 16 декабря 2013 г. Зачем проводить трансплантацию стволовых клеток?
- ^ Трансплантация костного мозга и трансплантация стволовых клеток периферической крови На веб-сайте Национального института рака. Bethesda, MD: Национальные институты здравоохранения, Министерство здравоохранения и социальных служб США, 2010 г. Цитировано 24 августа 2010 г.
- ^ Stamm C, Westphal B, Kleine HD, Petzsch M, Kittner C, Klinge H и др. (Январь 2003 г.). «Аутологичная трансплантация стволовых клеток костного мозга для регенерации миокарда». Ланцет. 361 (9351): 45–6. Дои:10.1016 / S0140-6736 (03) 12110-1. PMID 12517467. S2CID 23858666.
- ^ «Последние преимущества стволовых клеток в 2020 году - Poseidonia Healthcare». Посейдония Здравоохранение. 2020-03-17. Получено 2020-08-22.
- ^ Мастер Z, Маклеод М., Мендес I (март 2007 г.). «Преимущества, риски и этические соображения при переводе исследований стволовых клеток в клиническое применение при болезни Паркинсона». Журнал медицинской этики. 33 (3): 169–73. Дои:10.1136 / jme.2005.013169. JSTOR 27719821. ЧВК 2598267. PMID 17329391.
- ^ Мур К.Л., Persaud TV, Torchia MG (2013). До нашего рождения: основы эмбриологии и врожденных пороков. Филадельфия, Пенсильвания: Сондерс, Эльзевир.
- ^ Бернадин Хили, доктор медицины. «Почему эмбриональные стволовые клетки устарели» Новости США и мировой отчет. Проверено 17 августа, 2015.
- ^ «Стволовые клетки плода вызывают опухоль у мальчика-подростка».
- ^ https://pubmed.ncbi.nlm.nih.gov/30063299/?from_term=stem+cell+tourism&from_sort=date&from_size=200&from_pos=13
- ^ https://pubmed.ncbi.nlm.nih.gov/27331440/?from_term=stem+cell+tourism+spinal+cord&from_sort=date&from_size=200&from_pos=3
- ^ https://pubmed.ncbi.nlm.nih.gov/27331440/?from_term=stem+cell+tourism&from_sort=date&from_size=200&from_pos=33
- ^ https://pubmed.ncbi.nlm.nih.gov/26322563/?from_term=stem+cell+tourism&from_sort=date&from_size=200&from_pos=43
- ^ https://www.isscr.org/news-publicationsss/isscr-news-articles/blog-detail/stem-cells-in-focus/2019/11/12/communicating-about-unproven-stem-cell-treatments- публике
- ^ https://pubmed.ncbi.nlm.nih.gov/25651226/?from_term=stem+cell+tourism+spinal+cord&from_sort=date&from_size=200&from_pos=4
- ^ https://pubmed.ncbi.nlm.nih.gov/27227162/?from_term=stem+cell+tourism&from_sort=date&from_size=200&from_pos=35
- ^ а б Регаладо, Антонио, Дэвид П. Гамильтон (июль 2006 г.). «Как университетские патенты могут ограничивать исследователя стволовых клеток». Журнал "Уолл Стрит. Проверено 24 июля, 2006 г.
- ^ Стивен Дженей для патентных бариста, 3 апреля 2007 г. Патенты WARF на стволовые клетки были подавлены в первом раунде
- ^ Стивен Дженей для патентных бариста, 3 марта 2008 г. Дин! WARF выигрывает раунд 2, поскольку патент на стволовые клетки подтвержден
- ^ Констанс Холден для науки сейчас. 12 марта 2008 г. WARF получает 3 из 3 по патентам
- ^ Стивен Г. Кунин за патентный пост-грант. 10 мая 2010 г. BPAI отклоняет патентные претензии WARF на стволовые клетки в апелляции Inter Partes на повторную экспертизу
- ^ Ведомство США по патентам и товарным знакам. Совет по патентным апелляциям и вмешательствам. Фонд защиты прав налогоплательщиков и потребителей, заявитель и заявитель V. Патент Исследовательского фонда выпускников Висконсина, патентообладатель и ответчик. Апелляция 2012-011693, Контроль повторной экспертизы 95 / 000,154. Патент 7,029,913 Решение по апелляции В архиве 2013-02-20 в Wayback Machine
- ^ Сотрудники GenomeWeb, 3 июля 2013 г. Контроль потребителей, PPF объявляет недействительным патент WARF на стволовые клетки
- ^ Антуанетта Конски для персонализированного медицинского бюллетеня. 3 февраля 2014 г. Правительство США и ВПТЗ США призывают федеральный округ отклонить апелляцию по поводу стволовых клеток
- ^ а б c d е Основы стволовых клеток: каковы потенциальные возможности использования стволовых клеток человека и препятствия, которые необходимо преодолеть, прежде чем эти потенциальные применения будут реализованы?. В информации о стволовых клетках в Интернете. Bethesda, MD: Национальные институты здравоохранения, Министерство здравоохранения и социальных служб США, 2009 г., процитировано в воскресенье, 26 апреля 2009 г.
- ^ «Лечение выпадения волос с помощью стволовых клеток и PRP-терапии». Стволовые клетки LA. 2019-02-20. Получено 2020-05-30.
- ^ Джентиле, Пьетро; Гаркович, Симона; Бьелли, Алессандра; Шоли, Мария Джованна; Орланди, Аугусто; Сервелли, Валерио (ноябрь 2015 г.). «Влияние плазмы с высоким содержанием тромбоцитов на рост волос: рандомизированное плацебо-контролируемое исследование». Трансляционная медицина стволовых клеток. 4 (11): 1317–1323. Дои:10.5966 / sctm.2015-0107. ISSN 2157-6564. ЧВК 4622412. PMID 26400925.
- ^ Стейнберг, Дуглас (ноябрь 2000 г.) Стволовые клетки используются для восполнения запасов органов thescientist.com
- ^ ISRAEL21c: израильские ученые устраняют врожденные дефекты мозга с помощью стволовых клеток 25 декабря 2008 г. (Исследователи из Еврейского университета Иерусалима-Хадасса Медикал под руководством профессора Джозефа Янаи)
- ^ Кан К.С., Ким С.В., О ЙХ, Ю ДжВ, Ким Ки, Пак Х.К., Сон СН, Хан Х. (2005). «37-летняя пациентка с травмой спинного мозга, которой трансплантировали мультипотентные стволовые клетки из крови человека с ЯК, с улучшенным сенсорным восприятием и подвижностью, как функционально, так и морфологически: тематическое исследование». Цитотерапия. 7 (4): 368–73. Дои:10.1080/14653240500238160. PMID 16162459. S2CID 33471639.
- ^ Strauer BE, Schannwell CM, Brehm M (апрель 2009 г.). «Терапевтические возможности стволовых клеток при сердечных заболеваниях». Минерва Кардиоангиологическая. 57 (2): 249–67. PMID 19274033.
- ^ Стволовые клетки используются для восполнения запасов органов thescientist.com, ноябрь 2000 г. Дуглас Стейнберг
- ^ Клонирование волос приближается к реальности как средство от облысения WebMD Ноябрь 2004 г.
- ^ Йен АХ, Шарп П.Т. (январь 2008 г.). «Стволовые клетки и тканевая инженерия зуба». Исследования клеток и тканей. 331 (1): 359–72. Дои:10.1007 / s00441-007-0467-6. PMID 17938970. S2CID 23765276.
- ^ «Генная терапия - первое лекарство от глухоты'". Новый ученый. 14 февраля 2005 г.
- ^ «Стволовые клетки, используемые для восстановления зрения». Новости BBC. 2005-04-28.
- ^ Hanson C, Hardarson T, Ellerström C, Nordberg M, Caisander G, Rao M, Hyllner J, Stenevi U (март 2013 г.). «Трансплантация эмбриональных стволовых клеток человека на частично поврежденную роговицу человека in vitro». Acta Ophthalmologica. 91 (2): 127–30. Дои:10.1111 / j.1755-3768.2011.02358.x. ЧВК 3660785. PMID 22280565.
- ^ Вастаг Б (апрель 2001 г.). «Стволовые клетки шагают ближе к клинике: паралич частично обращен вспять у крыс с болезнью, подобной БАС». JAMA. 285 (13): 1691–3. Дои:10.1001 / jama.285.13.1691. PMID 11277806.
- ^ Андерсон Кью (2008-06-15). «Осирис возвещает о своем продукте стволовых клеток для взрослых». Новости генной инженерии и биотехнологии. Мэри Энн Либерт, Inc. п. 13. Получено 2008-07-06.
(подзаголовок) Процимал разрабатывается по многим показаниям, РТПХ является наиболее продвинутым
- ^ Gurtner GC, Каллаган MJ, Longaker MT (2007). «Прогресс и потенциал регенеративной медицины». Ежегодный обзор медицины. 58: 299–312. Дои:10.1146 / annurev.med.58.082405.095329. PMID 17076602. По состоянию на 2009 год трансплантация костного мозга является единственным установленным применением стволовых клеток.
- ^ Ханна В., Гассей К., Орвиг К.Э. (2015). "Лечение мужского бесплодия стволовыми клетками: где мы сейчас и куда мы идем?". В Carrell D, Schlegel P, Racowsky C, Gianaroli L (ред.). Двухгодичный обзор бесплодия. С. 17–39. Дои:10.1007/978-3-319-17849-3_3. ISBN 978-3-319-17849-3. По состоянию на 2009 год трансплантация костного мозга является единственным установленным применением стволовых клеток.
- ^ Валли Х., Филлипс Б.Т., Шетти Г., Бирн Дж.А., Кларк А.Т., Мейстрих М.Л., Орвиг К.Э. (январь 2014 г.). «Стволовые клетки зародышевой линии: к регенерации сперматогенеза». Фертильность и бесплодие. 101 (1): 3–13. Дои:10.1016 / j.fertnstert.2013.10.052. ЧВК 3880407. PMID 24314923.
- ^ Белый Я., Вудс, округ Колумбия, Такай Й, Исихара О, Секи Х, Тилли Дж. Л. (февраль 2012 г.). «Формирование ооцитов митотически активными зародышевыми клетками, очищенными из яичников женщин репродуктивного возраста». Природа Медицина. 18 (3): 413–21. Дои:10,1038 / нм.2669. ЧВК 3296965. PMID 22366948.
- ^ Бубела Т, Ли MD, Хафез М., Бибер М., Аткинс Х. (ноябрь 2012 г.). «Вера больше, чем факт: ожидания, оптимизм и реальность для исследований трансляционных стволовых клеток». BMC Медицина. 10: 133. Дои:10.1186/1741-7015-10-133. ЧВК 3520764. PMID 23131007.
- ^ Адер М, Танака Э.М. (декабрь 2014 г.). «Моделирование человеческого развития в 3D-культуре». Текущее мнение в области клеточной биологии. 31: 23–8. Дои:10.1016 / j.ceb.2014.06.013. PMID 25033469.
- ^ Гринхо С, Хэй, округ Колумбия (2012). «Скрининг токсичности на основе стволовых клеток: последние достижения в области создания гепатоцитов». Фарм Мед. 26 (2): 85–89. Дои:10.1007 / BF03256896. S2CID 15893493. Архивировано из оригинал на 16.06.2012.
дальнейшее чтение
- Манзо, Карло [и др.]. Нарушение слабой эргодичности движения рецепторов в живых клетках, возникающих из-за случайной диффузности. "Physical Review X", 25 февраля 2015 г., т. 5, ном. 011021. DOI: 10.1103 / PhysRevX.5.011021
внешняя ссылка
| Библиотечные ресурсы о Стволовая клетка |



