Спектроскопия ядерного магнитного резонанса - Nuclear magnetic resonance spectroscopy
Эта статья включает в себя список общих Рекомендации, но он остается в основном непроверенным, потому что ему не хватает соответствующих встроенные цитаты. (Ноябрь 2016) (Узнайте, как и когда удалить этот шаблон сообщения) |
Спектроскопия ядерного магнитного резонанса, чаще всего известный как ЯМР-спектроскопия или же магнитно-резонансная спектроскопия (Г-ЖА), это спектроскопический техника для наблюдения за местными магнитными полями вокруг атомные ядра. Образец помещается в магнитное поле, и сигнал ЯМР создается путем возбуждения образца ядер с помощью радиоволны в ядерный магнитный резонанс, который обнаруживается чувствительными радиоприемниками. Внутримолекулярное магнитное поле вокруг атома в молекуле изменяет резонансную частоту, тем самым открывая доступ к деталям электронной структуры молекулы и ее отдельных функциональных групп. Поскольку поля уникальны или очень характерны для отдельных соединений, в современных органическая химия На практике спектроскопия ЯМР является окончательным методом идентификации мономолекулярных органические соединения. Точно так же биохимики используют ЯМР для идентификации белки и другие сложные молекулы. Помимо идентификации, ЯМР-спектроскопия предоставляет подробную информацию о структуре, динамике, состоянии реакции и химическом окружении молекул. Наиболее распространенные типы ЯМР: протон и углерод-13 ЯМР спектроскопия, но она применима к любому типу образца, содержащему ядра, обладающие вращение.
Спектры ЯМР уникальны, хорошо разрешены, поддаются анализу и часто хорошо предсказуемы для маленькие молекулы. Разные функциональные группы очевидно различимы, и идентичные функциональные группы с разными соседними заместителями по-прежнему дают различимые сигналы. ЯМР в значительной степени заменил традиционные влажная химия такие тесты как цветные реагенты или типичная хроматография для идентификации. Недостатком является то, что требуется относительно большое количество, 2–50 мг очищенного вещества, хотя оно может быть получено путем обработки. Желательно, чтобы образец был растворен в растворителе, потому что для анализа ЯМР твердых веществ требуется специальный вращение под магическим углом аппарат и может не давать столь же хорошо разрешенные спектры. Временной масштаб ЯМР относительно велик, и поэтому он не подходит для наблюдения быстрых явлений, поскольку дает только усредненный спектр. Хотя в спектре ЯМР действительно обнаруживаются большие количества примесей, существуют более эффективные методы обнаружения примесей, поскольку ЯМР по своей природе не очень чувствителен, хотя на более высоких частотах чувствительность выше.
Корреляционная спектроскопия - это развитие обычного ЯМР. В двумерный ЯМР, излучение сосредоточено вокруг одной частоты, и наблюдаются коррелированные резонансы. Это позволяет идентифицировать соседние заместители наблюдаемой функциональной группы, позволяя однозначно идентифицировать резонансы. Существуют также более сложные методы 3D и 4D и множество методов, предназначенных для подавления или усиления определенных типов резонансов. В ядерный эффект Оверхаузера (NOE) спектроскопии наблюдается релаксация резонансов. Поскольку NOE зависит от близости ядер, количественное определение NOE для каждого ядра позволяет построить трехмерную модель молекулы.
Спектрометры ЯМР относительно дороги; Обычно они есть в университетах, но в частных компаниях они встречаются реже. Между 2000 и 2015 годами стоимость ЯМР-спектрометра составляла около 500 000–5 миллионов долларов. доллар США.[2][3] Современные спектрометры ЯМР имеют очень прочные, большие и дорогие жидкий гелий -охлажденный сверхпроводящий магнит, потому что разрешение напрямую зависит от напряженности магнитного поля. Также доступны менее дорогие машины с постоянными магнитами и более низким разрешением, которые по-прежнему обеспечивают достаточную производительность для определенных приложений, таких как мониторинг реакции и быстрая проверка образцов. Есть даже настольные спектрометры ядерного магнитного резонанса. ЯМР можно наблюдать в магнитных полях менее миллитесла. ЯМР низкого разрешения дает более широкие пики, которые могут легко перекрывать друг друга, вызывая проблемы при разрешении сложных структур. Использование более сильных магнитных полей приводит к четкому разрешению пиков и является стандартом в промышленности.[4]
История
Заслуга за открытие ЯМР принадлежит Исидор Исаак Раби, получивший Нобелевскую премию по физике в 1944 г.[5] Группа Перселла в Гарвардский университет и группа Блоха на Стэндфордский Университет независимо разработал ЯМР-спектроскопию в конце 1940-х - начале 1950-х годов. Эдвард Миллс Перселл и Феликс Блох разделила 1952 Нобелевская премия по физике за свои открытия.[6]
Основные методы ЯМР

Резонансная частота
При помещении в магнитное поле активные ядра ЯМР (например, 1H или 13В) впитывают электромагнитное излучение на частотной характеристике изотоп.[7] Резонансная частота, энергия поглощенного излучения и интенсивность сигнала пропорциональны силе магнитного поля. Например, в 21 Тесла магнитное поле, ядра водорода (обычно называемые протонами) резонируют на частоте 900 МГц. Магнит на 21 Т обычно называют 900 МГц магнит, поскольку водород является наиболее часто обнаруживаемым ядром, однако разные ядра будут резонировать на разных частотах при этой напряженности поля пропорционально их ядерные магнитные моменты.
Обработка образцов
Спектрометр ЯМР обычно состоит из вращающегося держателя образца внутри очень сильного магнита, радиочастотного излучателя и приемника с зондом (антенный узел), который проходит внутри магнита и окружает образец, необязательно градиентных катушек для измерений диффузии, и электроника для управления системой. Вращение образца обычно необходимо для усреднения диффузионного движения, однако в некоторых экспериментах требуется стационарный образец, когда движение раствора является важной переменной. Например, измерения константы диффузии (диффузионно-упорядоченная спектроскопия или ДОСЫ)[8][9] выполняются с использованием стационарного образца с отделением, а проточные кюветы можно использовать для онлайн-анализа технологических потоков.
Дейтерированные растворители
Подавляющее большинство молекул в растворе - это молекулы растворителя, а большинство обычных растворителей - это углеводороды и поэтому содержат ЯМР-активные протоны. Чтобы избежать обнаружения только сигналов от атомов водорода растворителя, используются дейтерированные растворители, в которых 99 +% протонов заменены на дейтерий (водород-2). Наиболее широко используемым дейтерированным растворителем является дейтерохлороформ (CDCl3), хотя другие растворители могут использоваться по разным причинам, например, растворимость образца, желание контролировать водородная связь, или точки плавления или кипения. Химические сдвиги молекулы будут незначительно изменяться между растворителями, и используемый растворитель почти всегда будет сообщаться с химическими сдвигами. Спектры ЯМР часто калибруют по известному пику остаточных протонов растворителя вместо добавленного тетраметилсилана.
Прокладка и фиксатор
Чтобы обнаружить очень небольшие сдвиги частоты из-за ядерного магнитного резонанса, приложенное магнитное поле должно быть постоянным во всем объеме образца. Использование спектрометров ЯМР высокого разрешения прокладки для регулировки однородности магнитного поля до частей на миллиард (ppb ) объемом в несколько кубических сантиметров. Чтобы обнаружить и компенсировать неоднородность и дрейф магнитного поля, спектрометр поддерживает "блокировку" частоты дейтерия в растворителе с помощью отдельного блока синхронизации, который по сути является дополнительным передатчиком и ВЧ-процессором, настроенным на ядро блокировки (дейтерий). а не ядра интересующего образца.[10] В современных ЯМР-спектрометрах регулировка шиммирования осуществляется автоматически, хотя в некоторых случаях оператору приходится вручную оптимизировать параметры регулировочной шайбы, чтобы получить наилучшее возможное разрешение.[11][12]
Получение спектров
При возбуждении образца радиочастотным (60–1000 МГц) импульсом отклик ядерного магнитного резонанса - a спад свободной индукции (FID) - получается. Это очень слабый сигнал, и для его приема необходимы чувствительные радиоприемники. А преобразование Фурье выполняется для извлечения спектра частотной области из необработанного FID временной области. Спектр от одного ПИД имеет низкий соотношение сигнал шум, но он быстро улучшается при усреднении повторных измерений. Хороший 1Спектры ЯМР 1Н могут быть получены с 16 повторами, что занимает всего несколько минут. Однако для элементов тяжелее водорода время релаксации довольно велико, например около 8 секунд для 13C. Таким образом, получение количественных спектров тяжелых элементов может занять много времени, от десятков минут до часов.
После импульса ядра в среднем возбуждаются под определенным углом относительно магнитного поля спектрометра. Степень возбуждения можно контролировать с помощью ширины импульса, обычно прибл. 3-8 мкс для оптимального импульса 90 °. Ширина импульса может быть определена путем построения графика интенсивности (подписанной) как функции ширины импульса. Это следует за синусоида, и, соответственно, меняет знак при длительности импульса, соответствующей импульсам 180 ° и 360 °.
Время затухания возбуждения, обычно измеряемое в секундах, зависит от эффективности релаксации, которая быстрее для более легких ядер и в твердых телах и медленнее для более тяжелых ядер и в растворах, и они могут быть очень длинными в газах. Если второй импульс возбуждения посылается преждевременно до завершения релаксации, средний вектор намагниченности не распадется до основного состояния, что непредсказуемо влияет на силу сигнала. На практике площади пиков тогда не пропорциональны стехиометрии; можно различить только присутствие, но не количество функциональных групп. Эксперимент по восстановлению инверсии может быть проведен для определения времени релаксации и, следовательно, необходимой задержки между импульсами. Передаются импульс 180 ° с регулируемой задержкой и импульс 90 °. Когда импульс 90 ° точно гасит сигнал, задержка соответствует времени, необходимому для релаксации 90 °.[13] Восстановление инверсии полезно для количественного 13C, 2D и другие трудоемкие эксперименты.
Химический сдвиг
Вращающийся заряд создает магнитное поле, в результате чего возникает магнитный момент, пропорциональный спину. В присутствии внешнего магнитного поля существуют два спиновых состояния (для ядра со спином 1/2): одно со спином вверх и одно со спином вниз, где одно выравнивается с магнитным полем, а другое противостоит ему. Разница в энергии (ΔE) между двумя спиновыми состояниями увеличивается по мере увеличения напряженности поля, но эта разница обычно очень мала, что приводит к необходимости использования сильных магнитов ЯМР (1-20 Тл для современных ЯМР-инструментов). Облучение образца энергией, соответствующей точному разделению спиновых состояний определенного набора ядер, вызовет возбуждение этого набора ядер в состоянии с более низкой энергией до состояния с более высокой энергией.
Для ядер со спином 1/2 разность энергий между двумя спиновыми состояниями при данной напряженности магнитного поля пропорциональна их магнитному моменту. Однако, даже если все протоны имеют одинаковые магнитные моменты, они не дают резонансных сигналов с одинаковыми значениями частоты. Эта разница возникает из-за различий в электронном окружении интересующего ядра. При приложении внешнего магнитного поля эти электроны движутся в ответ на это поле и генерируют локальные магнитные поля, которые противостоят гораздо более сильному приложенному полю. Таким образом, это локальное поле «экранирует» протон от приложенного магнитного поля, которое, следовательно, должно быть увеличено для достижения резонанса (поглощения высокочастотной энергии). Такие приращения очень малы, обычно в частях на миллион (ppm). Например, пик протона от альдегида смещен на ок. 10 ppm по сравнению с пиком углеводородов, поскольку электроноакцепторная группа карбонил снимает защитную оболочку с протона за счет уменьшения локальной электронной плотности. Таким образом, разница между 2,3487 Тл и 2,3488 Тл составляет около 42 частей на миллион. Однако частотный масштаб обычно используется для обозначения сигналов ЯМР, несмотря на то, спектрометр может работать при развертке магнитного поля, и, таким образом, 42 частей на миллион составляет 4200 Гц для опорной частоты 100 МГц (РЧ).
Однако, учитывая, что расположение различных сигналов ЯМР зависит от напряженности внешнего магнитного поля и опорной частоты, то сигналы, как правило, сообщалось относительно опорного сигнала, как правило, что ТМС (тетраметилсилан ). Кроме того, поскольку распределение сигналов ЯМР зависит от поля, эти частоты делятся на частоту спектрометра. Однако, поскольку мы делим Гц на МГц, полученное число будет слишком маленьким, и поэтому оно умножается на миллион. Таким образом, эта операция дает номер локатора, называемый «химическим сдвигом» с единицами измерения частей на миллион.[14] В общем, химические сдвиги для протонов очень предсказуемы, поскольку сдвиги в первую очередь определяются более простыми эффектами экранирования (электронной плотностью), но на химические сдвиги для многих более тяжелых ядер сильнее влияют другие факторы, включая возбужденные состояния («парамагнитный» вклад в экранирование тензор).

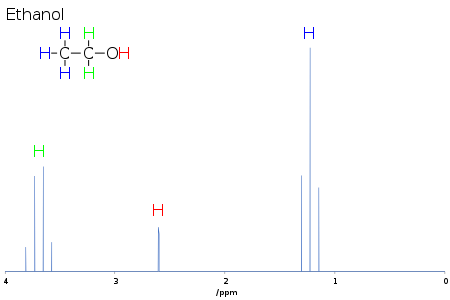
Химический сдвиг дает информацию о структуре молекулы. Преобразование необработанных данных в эту информацию называется назначение спектр. Например, для 1Спектр H-ЯМР этанола (CH3CH2OH), можно было бы ожидать сигналов при каждом из трех конкретных химических сдвигов: один для CЧАС3 группа, одна для CЧАС2 группа и один для OЧАС группа. Типичный CH3 группа имеет сдвиг около 1 ppm, CH2 присоединенный к ОН имеет сдвиг около 4 частей на миллион, а ОН имеет сдвиг где-нибудь от 2-6 частей на миллион в зависимости от используемого растворителя и количества водородная связь. В то время как атом O действительно оттягивает электронную плотность от присоединенного H через их взаимную сигма-связь, неподеленные пары электронов на O купают H своим экранирующим эффектом.
В парамагнитная спектроскопия ЯМР, измерения проводятся на парамагнитных образцах. Парамагнетизм вызывает самые разнообразные химические сдвиги. В 1Спектроскопия ЯМР 1Н, диапазон химического сдвига может достигать тысяч частей на миллион.[15]
Из-за молекулярного движения при комнатной температуре три метильных протона усреднить во время эксперимента ЯМР (который обычно требует нескольких РС ). Эти протоны становятся выродиться и образуют пик при том же химическом сдвиге.
Форма и площадь пиков также являются индикаторами химической структуры. В приведенном выше примере - протонный спектр этанола - CH3 Площадь пика в три раза больше, чем у пика ОН. Аналогично CH2 пик будет в два раза больше пика ОН, но только 2/3 площади пика СН3 вершина горы.
Программное обеспечение позволяет анализировать интенсивность сигналов пиков, которые в условиях оптимальной релаксации коррелируют с количеством протонов этого типа. Анализ интенсивности сигнала производится интеграция - математический процесс, вычисляющий площадь под кривой. Аналитик должен интегрировать пик, а не измерять его высоту, потому что пики также имеют ширина- и, следовательно, его размер зависит от площади, а не от высоты. Однако следует упомянуть, что количество протонов или любого другого наблюдаемого ядра пропорционально только интенсивности или интегралу сигнала ЯМР в самых простых одномерных экспериментах ЯМР. Например, в более сложных экспериментах, обычно используемых для получения углерод-13 В спектрах ЯМР интеграл сигналов зависит от скорости релаксации ядра и его скалярных и дипольных констант взаимодействия. Очень часто эти факторы плохо известны, поэтому интеграл сигнала ЯМР очень трудно интерпретировать в более сложных экспериментах по ЯМР.
J-муфта
| Множественность | Коэффициент интенсивности |
|---|---|
| Синглет (ы) | 1 |
| Дублет (г) | 1:1 |
| Триплет (т) | 1:2:1 |
| Квартет (q) | 1:3:3:1 |
| Квинтет | 1:4:6:4:1 |
| Секстет | 1:5:10:10:5:1 |
| Септет | 1:6:15:20:15:6:1 |
Некоторые из наиболее полезных сведений для определения структуры в одномерном спектре ЯМР получены из J-муфта или же скалярная связь (частный случай спин-спиновая связь ) между ЯМР-активными ядрами. Эта связь возникает из-за взаимодействия различных спиновых состояний через химические связи молекулы и приводит к расщеплению сигналов ЯМР. Для протона локальное магнитное поле немного отличается в зависимости от того, направлено ли соседнее ядро в сторону или против магнитного поля спектрометра, что дает два сигнала на протон вместо одного. Эти шаблоны расщепления могут быть сложными или простыми, а также могут быть легко интерпретируемыми или вводящими в заблуждение. Это соединение обеспечивает детальное понимание связи атомов в молекуле.
Соединение с п эквивалентных ядер (спин 1/2) расщепляет сигнал на п+1 мультиплет с соотношениями интенсивности, следующими Треугольник Паскаля как описано справа. Связь с дополнительными спинами приведет к дальнейшему разделению каждого компонента мультиплета, например. взаимодействие с двумя разными ядрами со спином 1/2 со значительно разными константами связи приведет к дуплет дуплетов (сокращение: дд). Обратите внимание, что связь между ядрами, которые химически эквивалентны (то есть, имеют одинаковый химический сдвиг), не влияет на спектры ЯМР, а связи между ядрами, которые находятся на расстоянии (обычно более 3 связей друг от друга для протонов в гибких молекулах), обычно слишком малы. вызвать наблюдаемые расщепления. Дальний связи более чем трех связей часто можно наблюдать в циклический и ароматный соединения, приводящие к более сложным схемам расщепления.
Например, в спектре протонов этанола, описанном выше, CH3 группа разделена на триплет с соотношением интенсивностей 1: 2: 1 двумя соседними CH2 протоны. Аналогично, CH2 разделен на квартет с соотношением интенсивностей 1: 3: 3: 1 по трем соседним CH3 протоны. В принципе, два CH2 протоны также снова будут разделены на дублет сформировать дуплет квартетов гидроксильным протоном, но межмолекулярный обмен кислого гидроксильного протона часто приводит к потере информации о сцеплении.
Связь с любыми ядрами со спином 1/2, такими как фосфор-31 или фтор-19, работает таким же образом (хотя величины констант связи могут быть очень разными). Но картины расщепления отличаются от описанных выше для ядер со спином больше 1/2, поскольку квантовое число спина имеет более двух возможных значений. Например, взаимодействие с дейтерием (ядром со спином 1) разбивает сигнал на 1: 1: 1 триплет потому что спин 1 имеет три состояния спина. Точно так же ядро со спином 3/2 расщепляет сигнал на 1: 1: 1: 1 квартет и так далее.
Связь в сочетании с химическим сдвигом (и интегрированием для протонов) говорит нам не только о химическом окружении ядер, но и о количестве соседний ЯМР-активные ядра в молекуле. В более сложных спектрах с множеством пиков при аналогичных химических сдвигах или в спектрах ядер, отличных от водорода, связывание часто является единственным способом различить разные ядра.

Связь второго порядка (или сильная)
В приведенном выше описании предполагается, что константа связи мала по сравнению с разницей в частотах ЯМР между неэквивалентными спинами. Если разделение сдвигов уменьшается (или увеличивается сила связи), картины интенсивности мультиплета сначала искажаются, а затем становятся более сложными и трудными для анализа (особенно, если задействовано более двух спинов). Усиление некоторых пиков в мультиплете достигается за счет остатка, который иногда почти исчезает в фоновом шуме, хотя интегральная площадь под пиками остается постоянной. Однако в большинстве высокопольных ЯМР искажения обычно невелики и характерные искажения (кровля) действительно может помочь идентифицировать связанные пики.
Некоторые из этих закономерностей можно проанализировать с помощью метод опубликовано Джон Попл,[16] хотя и имеет ограниченные возможности.
Эффекты второго порядка уменьшаются по мере увеличения разницы частот между мультиплетами, так что спектры ЯМР с высоким полем (т. Е. Высокочастотные) демонстрируют меньше искажений, чем спектры с более низкой частотой. Ранние спектры на 60 МГц были более подвержены искажениям, чем спектры более поздних машин, обычно работающих на частотах 200 МГц или выше.
Магнитная неэквивалентность
Более тонкие эффекты могут возникать, если химически эквивалентные спины (т.е. ядра, связанные симметрией и, следовательно, имеющие одинаковую частоту ЯМР) имеют разные отношения связи с внешними спинами. Спины, которые химически эквивалентны, но не являются неразличимыми (на основе их отношений сцепления), называются магнитно-неэквивалентными. Например, 4 H-центры 1,2-дихлорбензола делятся на две химически эквивалентные пары по симметрии, но являются отдельными членами одного из пары имеют разные связи со спинами, составляющими другую пару. Магнитная неэквивалентность может привести к очень сложным спектрам, которые можно проанализировать только с помощью компьютерного моделирования. Такие эффекты более распространены в спектрах ЯМР ароматических и других негибких систем, в то время как конформационное усреднение о связях C − C в гибких молекулах имеет тенденцию выравнивать связи между протонами на соседних атомах углерода, уменьшая проблемы с магнитной неэквивалентностью.
Корреляционная спектроскопия
Корреляционная спектроскопия является одним из нескольких типов двумерной спектроскопии ядерного магнитного резонанса (ЯМР) или 2D-ЯМР. Этот тип ЯМР-экспериментов известен прежде всего акроним, УЮТНЫЙ. Другие типы двумерного ЯМР включают J-спектроскопию, обменную спектроскопию (EXSY), Ядерный эффект Оверхаузера спектроскопия (NOESY), полная корреляционная спектроскопия (TOCSY) и эксперименты по гетероядерной корреляции, такие как HSQC, HMQC, и HMBC. В корреляционной спектроскопии излучение сосредоточено на пике отдельного ядра; если его магнитное поле коррелирует с другим ядром посредством сквозной связи (COSY, HSQC и т. д.) или связи через пространство (NOE), отклик также может быть обнаружен на частоте коррелированного ядра. Двумерные спектры ЯМР предоставляют больше информации о молекуле, чем одномерные спектры ЯМР, и особенно полезны при определении структуры молекулы. молекула, особенно для молекул, которые слишком сложны для работы с помощью одномерного ЯМР. Первый двумерный эксперимент, COZY, был предложен Жаном Джинером, профессором Свободного университета Брюсселя, в 1971 году.[17][18] Позже этот эксперимент был осуществлен Уолтером П. Ауэ, Энрико Бартольди и Ричард Р. Эрнст, опубликовавшие свои работы в 1976 г.[19]
Твердотельный ядерный магнитный резонанс

Разнообразие физических обстоятельств не позволяет изучать молекулы в растворах, и в то же время другими спектроскопическими методами на атомном уровне тоже. В твердофазных средах, таких как кристаллы, микрокристаллические порошки, гели, анизотропные растворы и т. Д., Именно диполярное взаимодействие и анизотропия химического сдвига становятся доминирующими в поведении ядерных спиновых систем. В традиционной ЯМР-спектроскопии в растворе эти дополнительные взаимодействия привели бы к значительному уширению спектральных линий. Разнообразие методов позволяет установить условия высокого разрешения, которые могут, по крайней мере, для 13Спектры C должны быть сопоставимы со спектрами ЯМР в растворе.
Двумя важными концепциями твердотельной ЯМР-спектроскопии высокого разрешения являются ограничение возможной ориентации молекул ориентацией образца и уменьшение анизотропных ядерных магнитных взаимодействий путем вращения образца. Из последнего подхода, быстрое вращение вокруг магический угол - очень известный метод, когда система состоит из ядер со спином 1/2. Скорость отжима ок. Используется 20 кГц, что требует специального оборудования. В настоящее время в ЯМР-спектроскопии используется ряд промежуточных методов с образцами частичного выравнивания или пониженной подвижности.
Приложения, в которых проявляются эффекты твердотельного ЯМР, часто связаны с исследованиями структуры мембранных белков, белковых фибрилл или всех видов полимеров и химическим анализом в неорганической химии, но также включают «экзотические» применения, такие как листья растений и топливные элементы. Например, Rahmani et al. исследовали влияние давления и температуры на самосборку бицеллярных структур с помощью спектроскопии ЯМР дейтерия.[21]
Биомолекулярная спектроскопия ЯМР
Белки
Многие инновации в спектроскопии ЯМР относятся к области белок ЯМР спектроскопия, важный метод в структурная биология. Общей целью этих исследований является получение трехмерных структур белка с высоким разрешением, аналогичных тем, которые могут быть достигнуты с помощью Рентгеновская кристаллография. В отличие от рентгеновской кристаллографии, ЯМР-спектроскопия обычно ограничивается белками меньше 35. кДа, хотя были решены более крупные конструкции. ЯМР-спектроскопия часто является единственным способом получить информацию с высоким разрешением о частично или полностью внутренне неструктурированные белки. Сейчас это обычный инструмент для определения Соответствие деятельности отношения где структура до и после взаимодействия, например, с кандидатом в лекарство сравнивается с его известной биохимической активностью. Белки порядки величины больше, чем небольшие органические молекулы, обсуждавшиеся ранее в этой статье, но также применимы основные методы ЯМР и некоторые теории ЯМР. Из-за гораздо большего количества атомов, присутствующих в молекуле белка по сравнению с небольшим органическим соединением, основные одномерные спектры становятся переполненными перекрывающимися сигналами до такой степени, что прямой спектральный анализ становится невозможным. Поэтому для решения этой проблемы были разработаны многомерные (2, 3 или 4D) эксперименты. Чтобы облегчить эти эксперименты, желательно изотопно маркируйте белок 13C и 15N потому что преобладающий изотоп природного происхождения 12C не является ЯМР-активным, и ядерный квадрупольный момент преобладающего встречающегося в природе 14Изотоп N препятствует получению информации с высоким разрешением от этого изотопа азота. Самый важный метод, используемый для определения структуры белков, использует NOE эксперименты для измерения расстояний между атомами внутри молекулы. Впоследствии полученные расстояния используются для создания трехмерной структуры молекулы путем решения геометрия расстояния проблема. ЯМР также можно использовать для получения информации о динамике и конформационной гибкости различных областей белка.
Нуклеиновые кислоты
"ЯМР нуклеиновой кислоты »- это использование ЯМР-спектроскопии для получения информации о структуре и динамике полинуклеиновые кислоты, Такие как ДНК или же РНК. По состоянию на 2003 г.[Обновить]почти половина всех известных структур РНК была определена с помощью ЯМР-спектроскопии.[22]
ЯМР-спектроскопия нуклеиновой кислоты и белка похожи, но существуют различия. Нуклеиновые кислоты имеют меньший процент атомов водорода, которые обычно наблюдаются в ЯМР-спектроскопии, и потому что двойные спирали нуклеиновых кислот жесткие и примерно линейные, они не складываются сами по себе, создавая «дальнодействующие» корреляции.[23] Типы ЯМР, обычно выполняемые с нуклеиновыми кислотами: 1H или протонный ЯМР, 13C ЯМР, 15N ЯМР, и 31P ЯМР. Двумерный ЯМР почти всегда используются методы, такие как корреляционная спектроскопия (COSY) и спектроскопия передачи полной когерентности (TOCSY) для обнаружения ядерных взаимодействий через сквозные связи, и ядерный эффект Оверхаузера спектроскопия (NOESY) для обнаружения взаимодействий между ядрами, которые находятся близко друг к другу в космосе.[24]
Параметры, взятые из спектра, в основном кросс-пики NOESY и константы связи, может использоваться для определения местных структурных особенностей, таких как гликозидная связь углы, двугранные углы (с использованием Уравнение Карплюса ) и конформации сахарной морщинки. Для крупномасштабной структуры эти локальные параметры должны быть дополнены другими структурными допущениями или моделями, потому что ошибки складываются при прохождении двойной спирали, и, в отличие от белков, двойная спираль не имеет компактной внутренней части и не сворачивается назад. сам. ЯМР также полезен для исследования нестандартных геометрий, таких как изогнутые спирали, не-Ватсона – Крика, и коаксиальная укладка. Это было особенно полезно при исследовании структуры природных олигонуклеотидов РНК, которые имеют тенденцию принимать сложные конформации, такие как стебель-петли и псевдоузлы. ЯМР также полезен для исследования связывания молекул нуклеиновой кислоты с другими молекулами, такими как белки или лекарственные препараты, путем наблюдения за тем, какие резонансы смещаются при связывании другой молекулы.[24]
Углеводы
Углеводный ЯМР спектроскопия решает вопросы о структуре и конформации углеводы. Анализ углеводов с помощью 1H ЯМР затруднен из-за ограниченного изменения функциональных групп, что приводит к резонансам 1H, сосредоточенным в узких полосах спектра ЯМР. Другими словами, имеется плохая спектральная дисперсия. Аномерные протонные резонансы отделены от других из-за того, что аномерные атомы углерода несут два атома кислорода. Для более мелких углеводов дисперсия аномерных протонных резонансов облегчает использование одномерных экспериментов TOCSY для исследования всей спиновой системы отдельных углеводных остатков.
Смотрите также
- Геометрия расстояния
- ЯМР поля Земли
- Магнитно-резонансная спектроскопия in vivo
- Функциональная магнитно-резонансная спектроскопия головного мозга
- ЯМР низкого поля
- Магнитно-резонансная томография
- ЯМР кристаллография
- База данных спектров ЯМР
- ЯМР трубка - включает раздел по пробоподготовке
- ЯМР-спектроскопия стереоизомеров
- Ядерно-магнитная резонансная спектроскопия белков
- Ядерный квадрупольный резонанс
- Магнит импульсного поля
- Протонно-усиленная ядерная индукционная спектроскопия
- Релаксация (ЯМР)
- Спектроскопия ядерного магнитного резонанса тройного резонанса
- ЯМР в нулевом поле
Связанные методы ядерная спектроскопия:
Рекомендации
- ^ Структурная биология: практическое применение ЯМР (PDF) (2-е изд.). Springer. 6 сентября 2012. с. 67. ISBN 978-1-4614-3964-6. Получено 7 декабря 2018.
- ^ Марк С. Райш (29 июня 2015 г.). "Подъем цен на приборы ЯМР спугнул пользователей". CEN.
- ^ "Принимая это выше". Ученый. 30 октября 2000 г.
- ^ Паудлер, Уильям (1974). Ядерный магнитный резонанс. Бостон: Серия химии Аллина и Бэкона. С. 9–11.
- ^ http://mriquestions.com/who-discovered-nmr.html
- ^ "История и теория установки ядерного магнитного резонанса". Аналитический центр Марка Уэйнрайта - Сиднейский университет Южного Уэльса. 9 декабря 2011. Архивировано с оригинал 27 января 2014 г.. Получено 9 февраля 2014.
- ^ Шах, Н; Саттар, А; Benanti, M; Холландер, S; Cheuck, L (январь 2006 г.). «Магнитно-резонансная спектроскопия как инструмент визуализации рака: обзор литературы». Журнал Американской остеопатической ассоциации. 106 (1): 23–27. PMID 16428685. Архивировано из оригинал на 2013-04-07.
- ^ Джонсон-младший, С.С. (1999). «Диффузионно-упорядоченная спектроскопия ядерного магнитного резонанса: принципы и приложения». Прогресс в спектроскопии ядерного магнитного резонанса. 34 (3–4): 203–256. Дои:10.1016 / S0079-6565 (99) 00003-5.
- ^ Neufeld, R .; Сталке, Д. (2015). «Точное определение молекулярной массы малых молекул с помощью DOSY-ЯМР с использованием внешних калибровочных кривых с нормализованными коэффициентами диффузии». Chem. Sci. 6 (6): 3354–3364. Дои:10.1039 / C5SC00670H. ЧВК 5656982. PMID 29142693.

- ^ http://nmr.chem.wsu.edu/tutorials/basics/lock/
- ^ «Центр ЯМР-спектроскопии: Замок». nmr.chem.wsu.edu.
- ^ «Артефакты ЯМР». www2.chemistry.msu.edu.
- ^ Парелла, Теодор. «ЭКСПЕРИМЕНТ ИНВЕРСИИ-ВОССТАНОВЛЕНИЯ». triton.iqfr.csic.es.
- ^ Джеймс Килер. «Глава 2: ЯМР и уровни энергии» (перепечатано в Кембриджский университет ). Понимание ЯМР-спектроскопии. Калифорнийский университет в Ирвине. Получено 2007-05-11.
- ^ Ott, J.C .; Wadepohl, H .; Эндерс, М .; Гаде, Л. Х. (2018). «Принятие решения протонного ЯМР до предела: предсказание и обнаружение гидридного резонанса в комплексе железа с промежуточным спином». Варенье. Chem. Soc. 140 (50): 17413–17417. Дои:10.1021 / jacs.8b11330. PMID 30486649.
- ^ Pople, J. A .; Bernstein, H.J .; Шнайдер, В. Г. (1957). «Анализ спектров ядерного магнитного резонанса». Может. J. Chem. 35: 65–81. Дои:10.1139 / v57-143.
- ^ Ауэ, В. П. (1976). «Двумерная спектроскопия. Приложение к ядерному магнитному резонансу». Журнал химической физики. 64 (5): 2229. Bibcode:1976ЖЧФ..64.2229А. Дои:10.1063/1.432450.
- ^ Джинер, Жан (2007). "Джинер, Жан: Воспоминания о первых днях 2D ЯМР". Энциклопедия магнитного резонанса. Дои:10.1002 / 9780470034590.emrhp0087. ISBN 978-0470034590.
- ^ Martin, G.E; Зектер А.С., Двумерные методы ЯМР для установления молекулярной связи; VCH Publishers, Inc: Нью-Йорк, 1988 (стр.59).
- ^ «Национальная установка сверхвысокого поля ЯМР для твердых тел». Получено 2014-09-22.
- ^ А. Рахмани, К. Найт и М. Р. Морроу. Реакция на гидростатическое давление двухцеллярных дисперсий, содержащих анионный липид: встречное пересечение под давлением. 2013, 29 (44), стр 13481–13490, Дои:10.1021 / la4035694
- ^ Фюртиг, Борис; Рихтер, Кристиан; Wöhnert, Jens; Швальбе, Харальд (2003). «ЯМР-спектроскопия РНК». ChemBioChem. 4 (10): 936–62. Дои:10.1002 / cbic.200300700. PMID 14523911.
- ^ Addess, Kenneth J .; Фейгон, Джули (1996). "Введение в 1H ЯМР-спектроскопия ДНК ». In Hecht, Sidney M. (ed.). Биоорганическая химия: нуклеиновые кислоты. Нью-Йорк: Издательство Оксфордского университета. ISBN 978-0-19-508467-2.
- ^ а б Wemmer, Дэвид (2000). «Глава 5: Структура и динамика ЯМР». В Блумфилде, Виктор А .; Crothers, Donald M .; Тиноко, Игнасио (ред.). Нуклеиновые кислоты: структура, свойства и функции. Саусалито, Калифорния: Научные книги университета. ISBN 978-0-935702-49-1.
дальнейшее чтение
- Джон Д. Робертс (1959). Ядерный магнитный резонанс: приложения к органической химии. Книжная компания McGraw-Hill. ISBN 9781258811662.
- J.A.Pople; В. Г. Шнайдер; Х. Дж. Бернштейн (1959). Ядерный магнитный резонанс высокого разрешения. Книжная компания McGraw-Hill.
- А. Абрагам (1961). Принципы ядерного магнетизма. Кларендон Пресс. ISBN 9780198520146.
- Чарльз П. Слихтер (1963). Принципы магнитного резонанса: на примерах из физики твердого тела. Харпер и Роу. ISBN 9783540084761.
- Джон Эмсли; Джеймс Фини; Лесли Ховард Сатклифф (1965). Спектроскопия ядерного магнитного резонанса высокого разрешения. Пергамон. ISBN 9781483184081.
внешняя ссылка
- Джеймс Килер. «Понимание ЯМР-спектроскопии» (перепечатано в Кембриджский университет ). Калифорнийский университет в Ирвине. Получено 2007-05-11.
- Основы ЯМР - Нетехнический обзор теории, оборудования и методов ЯМР от доктора Джозефа Хорнака, профессора химии в RIT.
- Библиотеки GAMMA и PyGAMMA - GAMMA - это библиотека C ++ с открытым исходным кодом, написанная для моделирования экспериментов по спектроскопии ядерного магнитного резонанса. PyGAMMA - это оболочка Python для GAMMA.
- расслабляться Программное обеспечение для анализа динамики ЯМР
- Vespa - VeSPA (Versatile Simulation, Pulses and Analysis) - это бесплатный программный пакет, состоящий из трех приложений Python. Эти инструменты на основе графического интерфейса пользователя предназначены для спектрального моделирования магнитного резонанса (МР), проектирования РЧ-импульсов, а также спектральной обработки и анализа данных МРТ.


