Метаболизм железа у человека - Human iron metabolism
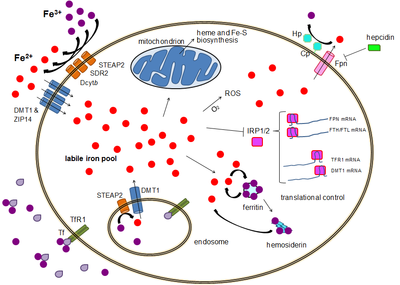
Метаболизм железа у человека это набор химических реакций, которые поддерживают гомеостаз человека из утюг на системном и клеточном уровне. Железо необходимо организму и потенциально токсично. Контроль уровня железа в организме является критически важной частью многих аспектов здоровья и болезней человека. Гематологи особенно интересовались системным железом метаболизм потому что железо необходимо для красные кровяные тельца, где содержится большая часть железа человеческого тела. Понимание метаболизма железа также важно для понимания болезней железная перегрузка, такие как наследственный гемохроматоз, и недостаток железа, такие как железодефицитная анемия.
Важность регулирования железа
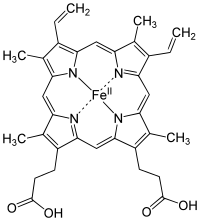
Железо является важным биоэлементом для большинства форм жизни, начиная с бактерии к млекопитающие. Его важность заключается в его способности опосредовать перенос электронов. В двухвалентном состоянии железо действует как донор электронов, а в железном состоянии он действует как акцептор. Таким образом, железо играет жизненно важную роль в катализ ферментативных реакций, включающих перенос электронов (восстановление и окисление, редокс ). Белки могут содержать железо в составе различных кофакторы, такие как железо-серные кластеры (Fe-S) и гем группы, обе из которых собраны в митохондрии.
Клеточное дыхание
Клеткам человека требуется железо для получения энергии в виде АТФ из многоступенчатого процесса, известного как клеточное дыхание, в частности, из окислительного фосфорилирования в митохондриальной кристы. Железо присутствует в железо-серных кластерах и гемовых группах электронная транспортная цепь белки, которые производят протонный градиент это позволяет АТФ-синтаза синтезировать АТФ (хемиосмос ).
Группы гема являются частью гемоглобин, белок, содержащийся в красных кровяных тельцах, который служит для транспортировки кислорода из легкие к другим тканям. Группы гема также присутствуют в миоглобин для хранения и распространения кислорода в мышечных клетках.
Транспорт кислорода
Организм человека нуждается в железе для транспортировки кислорода. Кислород (O2) требуется для функционирования и выживания почти всех типов клеток. Кислород переносится из легких в остальную часть тела, связанную с гем группа гемоглобин в красных кровяных тельцах. В клетках мышц железо связывает кислород с миоглобин, который регулирует его выпуск.
Токсичность
Железо также потенциально токсично. Его способность отдавать и принимать электроны означает, что он может катализировать превращение пероксид водорода в свободные радикалы. Свободные радикалы могут вызывать повреждение самых разных клеточных структур и в конечном итоге убивать клетку.[1]
Железо связано с белками или кофакторы такие как гем безопасно. Также в клетке практически нет действительно свободных ионов железа, так как они легко образуют комплексы с органическими молекулами. Однако некоторое количество внутриклеточного железа связано с комплексами с низким сродством и называется лабильным железом или «свободным» железом. Железо в таких комплексах может вызывать повреждения, как описано выше.[2]
Чтобы предотвратить такой ущерб, все формы жизни, использующие железо, связывают атомы железа с белки. Это связывание позволяет клеткам извлекать выгоду из железа, а также ограничивает его способность причинять вред.[1][3] Типичные внутриклеточные концентрации лабильного железа у бактерий составляют 10-20 мкмоль,[4] хотя в анаэробной среде они могут быть в 10 раз выше,[5] где свободные радикалы и активные формы кислорода реже. В клетках млекопитающих внутриклеточные концентрации лабильного железа обычно меньше 1 микромоля, менее 5 процентов от общего клеточного железа.[2]
Бактериальная защита

В ответ на системную бактериальную инфекцию иммунная система запускает процесс, известный как удержание железа. Если бактерии хотят выжить, они должны получать железо из окружающей среды. Бактерии, вызывающие заболевания, делают это разными способами, включая высвобождение связывающих железо молекул, называемых сидерофоры а затем реабсорбируют их для восстановления железа или удаляют железо из гемоглобина и трансферрин. Чем тяжелее бактерии должны работать, чтобы получить железо, тем больше метаболическая цена они должны платить. Это означает, что бактерии, лишенные железа, размножаются медленнее. Таким образом, контроль уровня железа является важной защитой от многих бактериальных инфекций. Некоторые виды бактерий разработали стратегии, позволяющие обойти эту защиту. Туберкулез вызывающие бактерии могут находиться внутри макрофаги, которые представляют собой богатую железом среду и Borrelia burgdorferi использует марганец вместо железа. Люди с повышенным содержанием железа, как, например, при гемохроматозе, более восприимчивы к некоторым бактериальным инфекциям.[6]
Хотя этот механизм является элегантным ответом на кратковременную бактериальную инфекцию, он может вызвать проблемы, если длится так долго, что организм лишается железа, необходимого для производства эритроцитов. Воспалительный цитокины стимулировать печень к выработке белка, регулирующего метаболизм железа гепсидин, что снижает доступное железо. Если уровни гепсидина повышаются из-за небактериальных источников воспаления, таких как вирусная инфекция, рак, аутоиммунные заболевания или другие хронические заболевания, то анемия хронического заболевания может привести. В этом случае удержание железа фактически ухудшает здоровье, препятствуя производству достаточного количества гемоглобинсодержащих красных кровяных телец.[3]
Магазины железа для тела
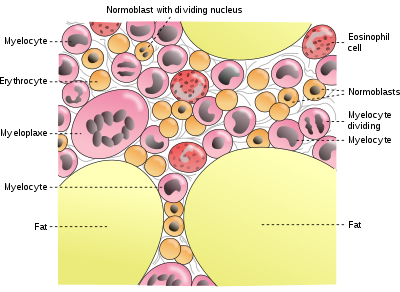
У большинства хорошо питающихся людей в промышленно развитых странах в организме содержится от 4 до 5 граммов железа (~ 38 мг железа / кг массы тела для женщин и ~ 50 мг железа / кг тела для мужчин).[7] Из этого о 2,5 г содержится в гемоглобине, необходимом для переноса кислорода через кровь (около 0,5 мг железа на мл крови),[8] а большая часть остального (примерно 2 грамма у взрослых мужчин и несколько меньше у женщин детородного возраста) содержится в ферритин комплексы, которые присутствуют во всех клетках, но наиболее часто встречаются в костном мозге, печень, и селезенка. Запасы ферритина в печени являются основным физиологическим источником резервного железа в организме. Запасы железа в промышленно развитых странах, как правило, ниже у детей и женщин детородного возраста, чем у мужчин и пожилых людей. Женщины, которым приходится использовать свои запасы, чтобы компенсировать потерю железа менструация, беременность или кормление грудью имеют более низкие запасы негемоглобина в организме, которые могут состоять из 500 мг, или даже меньше.
Из общего содержания железа в организме около 400 мг посвящен клеточным белкам, которые используют железо для важных клеточных процессов, таких как хранение кислорода (миоглобин) или выполнение окислительно-восстановительных реакций, производящих энергию (цитохромы ). Относительно небольшое количество (3–4 мг) циркулирует через плазма, связанный с трансферрином.[9] Из-за своей токсичности свободное растворимое железо сохраняется в организме в низкой концентрации.
Недостаток железа сначала влияет на запасы железа в организме, и истощение этих запасов считается относительно бессимптомным, хотя некоторые неопределенные и неспецифические симптомы были связаны с этим. Поскольку железо в первую очередь требуется для гемоглобина, железодефицитная анемия является первичным клиническим проявлением дефицита железа. Люди с дефицитом железа пострадают или умрут от повреждения органов задолго до того, как в их клетках закончится железо, необходимое для внутриклеточных процессов, таких как перенос электронов.
Макрофаги из ретикулоэндотелиальной системы хранить железо как часть процесса расщепления и обработки гемоглобина из захваченных красных кровяных телец. Железо также хранится в виде пигмента, называемого гемосидерин, который представляет собой плохо определенное отложение белка и железа, создаваемое макрофагами, в которых присутствует избыток железа, локально или системно, например, у людей с перегрузкой железом из-за частого разрушения клеток крови и необходимых переливаний, которых требует их состояние. Если устранить системную перегрузку железом, со временем гемосидерин медленно рассасывается макрофагами.
Механизмы регуляции железа
Гомеостаз человеческого железа регулируется на двух разных уровнях. Системные уровни железа уравновешиваются контролируемым всасыванием железа с пищей. энтероциты, ячейки, выстилающие внутреннюю часть кишечник и неконтролируемая потеря железа из-за слущивания эпителия, пота, травм и кровопотери. Кроме того, системное железо постоянно перерабатывается. Уровни клеточного железа по-разному контролируются разными типами клеток из-за экспрессии определенных регуляторных и транспортных белков железа.
Системная регуляция железа

Поглощение пищевого железа
Поглощение пищевого железа - это изменчивый и динамичный процесс. Количество поглощенного железа по сравнению с количеством проглоченного обычно невелико, но может варьироваться от 5% до 35% в зависимости от обстоятельств и типа железа. Эффективность абсорбции железа зависит от источника. Как правило, наиболее усваиваемые формы железа поступают из продуктов животного происхождения. Поглощение диетического железа в форме соли железа (как и в большинстве добавок) несколько варьируется в зависимости от потребности организма в железе и обычно составляет от 10% до 20% от потребления железа. Абсорбция железа из продуктов животного происхождения и некоторых растительных продуктов происходит в форме гемового железа и является более эффективной, позволяя абсорбировать от 15% до 35% от принятого количества. Гемовое железо у животных происходит из крови и гем-содержащих белков мяса и митохондрий, тогда как у растений гемовое железо присутствует в митохондриях всех клеток, которые используют кислород для дыхания.
Как и большинство минеральных питательных веществ, большая часть железа, усваиваемого из переваренной пищи или добавок, всасывается в организме. двенадцатиперстная кишка к энтероциты слизистой двенадцатиперстной кишки. В этих клетках есть особые молекулы, которые позволяют им перемещать железо в организм. Для всасывания пищевое железо может быть абсорбировано как часть белка, такого как гемовый белок, или железо должно находиться в своем двухвалентном Fe.2+ форма. Фермент редуктазы железа на энтероцитах кисть границы, дуоденальный цитохром B (Dcytb ), восстанавливает трехвалентное железо3+ в Fe2+.[10] Белок, называемый транспортером двухвалентного металла 1 (DMT1 ), который может транспортировать несколько двухвалентный металлов через плазматическую мембрану, а затем транспортирует железо через энтероциты. клеточная мембрана в камеру. Если железо связано с гемом, оно вместо этого транспортируется через апикальную мембрану посредством белок-носитель гема 1 (HCP1).[11]
Эти клетки слизистой оболочки кишечника могут накапливать железо в виде ферритин, что осуществляется Fe3+ связывание с апоферритином (в этом случае железо покидает организм, когда клетка умирает, и превращается в кал ), или клетка может высвободить его в организм через единственного известного экспортера железа у млекопитающих, ферропортин. Гефестин, а ферроксидаза который может окислять Fe2+ к Fe3+ и находится в основном в тонком кишечнике, помогает ферропортину переносить железо через базолатеральный конец клеток кишечника. Напротив, ферропортин посттрансляционно репрессируется гепсидин, пептидный гормон из 25 аминокислот. Организм регулирует уровень железа, регулируя каждый из этих шагов. Например, энтероциты синтезируют больше Dcytb, DMT1 и ферропортина в ответ на железодефицитную анемию.[12] Всасывание железа из рациона увеличивается в присутствии витамина С и уменьшается из-за избытка кальция, цинка или марганца.[13][нужна цитата ]
Скорость абсорбции железа в организме человека, по-видимому, зависит от множества взаимозависимых факторов, включая общие запасы железа, степень, в которой костный мозг производит новые эритроциты, концентрацию гемоглобина в крови и содержание кислорода в крови. кровь. Тело также поглощает меньше железа во время воспаление, чтобы лишить бактерии железа. Недавние открытия показывают, что регуляция ферропортина гепсидином ответственна за синдром хронической анемии.
Переработка и потеря железа
Большая часть железа в организме накапливается и перерабатывается ретикулоэндотелиальной системой, которая разрушает старые эритроциты. В отличие от поглощения и рециркуляции железа, не существует физиологического регулирующего механизма для выделение утюг. Люди теряют небольшую, но постоянную сумму из-за желудочно-кишечной кровопотери, потоотделения и отщепления клеток кожи и слизистая оболочка подкладка желудочно-кишечный тракт. Общая сумма потерь для здоровых людей в развитом мире составляет примерно 1 мг в день для мужчин и 1,5–2 мг в день для женщин с регулярными менструациями.[нужна цитата ] Люди с паразитарными инфекциями желудочно-кишечного тракта, которые чаще встречаются в развивающихся странах, часто теряют больше.[1] У тех, кто не может достаточно хорошо регулировать абсорбцию, возникают расстройства перегрузки железом. При этих заболеваниях токсичность железа начинает подавлять способность организма связывать и хранить его.[14]
Регуляция клеточного железа
Импорт железа
Большинство типов клеток поглощают железо в основном через рецептор-опосредованного эндоцитоза через рецептор трансферрина 1 (СКР1), рецептор трансферрина 2 (СКР2) и GAPDH. TFR1 имеет сродство к железу, связанному с трансферрином, в 30 раз выше, чем TFR2, и, таким образом, является основным участником этого процесса.[15][16] Многофункциональный гликолитический фермент более высокого порядка глицеральдегид-3-фосфатдегидрогеназа (GAPDH) также действует как рецептор трансферрина.[17][18] Связанное с трансферрином трехвалентное железо распознается этими рецепторами трансферрина, вызывая конформационные изменения, вызывающие эндоцитоз. Затем железо поступает в цитоплазму из эндосомы через импортер DMT1 после восстановления до своего двухвалентного состояния редуктазой семейства STEAP.[19]
Альтернативно, железо может поступать в клетку напрямую через импортеры двухвалентных катионов плазматической мембраны, такие как DMT1 и ZIP14 (Zrt-Irt-подобный белок 14).[20] И снова железо входит в цитоплазму в железистом состоянии после восстановления во внеклеточном пространстве редуктазой, такой как STEAP2, STEAP3 (в красных кровяных тельцах), Dcytb (в энтероцитах) и SDR2.[19]
Бассейн лабильного железа
В цитоплазме двухвалентное железо находится в растворимом хелатируемом состоянии, которое составляет пул лабильного железа (~ 0,001 мМ).[21] Считается, что в этом пуле железо связано с соединениями с малой массой, такими как пептиды, карбоксилаты и фосфаты, хотя некоторые из них могут находиться в свободной гидратированной форме (аква-ионы ).[21] В качестве альтернативы ионы железа могут быть связаны со специализированными белками, известными как металло-шапероны.[22] В частности, поли-r (C) -связывающие белки PCBP1 и PCBP2 по-видимому, опосредуют передачу свободного железа ферритину (для хранения) и негемовым ферментам железа (для использования в катализе).[20][23] Пул лабильного железа потенциально токсичен из-за способности железа генерировать активные формы кислорода. Железо из этого пула может поглощаться митохондриями через митоферрин для синтеза Fe-S кластеров и гемовых групп.[19]
Бассейн для хранения железа
Железо может храниться в ферритине как трехвалентное железо из-за ферроксидаза активность тяжелой цепи ферритина.[24] Дисфункциональный ферритин может накапливаться в виде гемосидерин, что может быть проблематично в случае перегрузки железом.[25] Пул железа, запасающего ферритин, намного больше, чем пул лабильного железа, в диапазоне концентраций от 0,7 до 3,6 мМ.[21]
Экспорт железа
Экспорт железа происходит в различных типах клеток, включая нейроны, эритроциты, макрофаги и энтероциты. Последние два особенно важны, поскольку от них зависят системные уровни железа. Есть только один известный экспортер железа, ферропортин.[26] Он переносит двухвалентное железо из клетки, как правило, с помощью церулоплазмин и / или Гефестин (в основном в энтероцитах), которые окисляют железо до его трехвалентного состояния, чтобы оно могло связывать ферритин во внеклеточной среде.[19] Гепсидин вызывает интернализацию ферропортина, уменьшая экспорт железа. Кроме того, гепсидин, по-видимому, подавляет как TFR1, так и DMT1 посредством неизвестного механизма.[27] Еще один игрок, помогающий ферропортину в экспорте клеточного железа, - это GAPDH.[28] Специфическая посттрансляционно модифицированная изоформа GAPDH рекрутируется на поверхность нагруженных железом клеток, где она рекрутирует апо-трансферрин в непосредственной близости от ферропортина, чтобы быстро хелатировать экструдированное железо.[29]
Экспрессия гепсидина, которая встречается только в определенных типах клеток, таких как гепатоциты, строго контролируется на уровне транскрипции и представляет собой связь между клеточным и системным гомеостазом железа из-за роли гепсидина как «привратника» высвобождения железа из энтероцитов в остальную часть тела.[19] Эритробласты производить эритроферрон, гормон, который ингибирует гепсидин и, таким образом, увеличивает доступность железа, необходимого для синтеза гемоглобина.[30]
Трансляционный контроль клеточного железа
Хотя определенный контроль существует на уровне транскрипции, регуляция уровней клеточного железа в конечном итоге контролируется на уровне трансляции посредством белки, связывающие железо-чувствительные элементы IRP1 и особенно IRP2.[31] Когда уровень железа низкий, эти белки могут связываться с железо-чувствительные элементы (IRE). IRE представляют собой структуры стволовых петель в нетранслируемых областях (UTR) мРНК.[19]
И ферритин, и ферропортин содержат IRE в своих 5 'UTR, так что при дефиците железа их трансляция репрессируется IRP2, предотвращая ненужный синтез запасного белка и вредный экспорт железа. Напротив, TFR1 и некоторые варианты DMT1 содержат IRE 3 'UTR, которые связывают IRP2 при дефиците железа, стабилизируя мРНК, что гарантирует синтез импортеров железа.[19]
Патология
Недостаток железа

Функциональный или реальный дефицит железа может быть вызван множеством причин. Эти причины можно сгруппировать в несколько категорий:
- Повышенная потребность в железе, которого не может удовлетворить диета.
- Повышенная потеря железа (обычно из-за потери крови).
- Недостаток питания. Это может происходить из-за недостатка железа в рационе или употребления продуктов, которые препятствуют усвоению железа. Наблюдалось ингибирование абсорбции, вызванное фитаты в отруби,[32] кальций из добавок или молочных продуктов,[33] и дубильные вещества из чая,[34] хотя во всех трех этих исследованиях эффект был небольшим, и авторы исследований, процитированных относительно отрубей и чая, отмечают, что эффект, вероятно, будет иметь заметный эффект только в том случае, если большая часть железа получена из растительных источников.
- Лекарства, снижающие кислотность: препараты, снижающие кислотность, снижают всасывание железа из пищи. Эти лекарства обычно используются при гастрите, рефлюксной болезни и язвах. Ингибиторы протонной помпы (ИПП), Н2-антигистаминные препараты, а антациды снижают метаболизм железа.[35]
- Повреждение слизистой оболочки кишечника. Примеры причин такого рода повреждений включают хирургическое вмешательство на двенадцатиперстной кишке или такие заболевания, как Крона или чревный литник которые сильно уменьшают доступную для поглощения площадь поверхности. Helicobacter pylori инфекции также снижают доступность железа.[36]
- Воспаление, приводящее к вызванному гепсидином ограничению высвобождения железа из энтероцитов (см. Выше).
- Также часто встречается у беременных женщин и у растущих подростков из-за плохого питания.
- Острая кровопотеря или острый цирроз печени вызывают нехватку трансферрина, что приводит к выделению железа из организма.
Железная перегрузка
Организм способен существенно уменьшить количество железа, которое он абсорбирует через слизистую. Похоже, что он не может полностью остановить процесс транспортировки железа. Кроме того, в ситуациях, когда избыток железа повреждает сам кишечник (например, когда дети едят большое количество таблеток железа, произведенных для потребления взрослыми), еще больше железа может попасть в кровоток и вызвать потенциально смертельный синдром перегрузки железом. Большое количество свободного железа в кровообращении вызовет повреждение критически важных клеток печени, сердце и другие метаболически активные органы.
Токсичность железа возникает, когда количество циркулирующего железа превышает количество трансферрина, доступного для его связывания, но организм способен энергично регулировать поглощение железа. Таким образом, токсичность железа при приеме внутрь обычно является результатом чрезвычайных обстоятельств, таких как чрезмерное употребление таблеток железа.[1][37] а не вариации в рацион питания. Тип острой токсичности от проглатывания железа вызывает, помимо других проблем, серьезное повреждение слизистой оболочки желудочно-кишечного тракта.
Избыток железа связан с более высоким уровнем заболеваемости и смертности. Например, пациенты с раком груди с низким ферропортин экспрессия (приводящая к более высоким концентрациям внутриклеточного железа) в среднем выживает в течение более короткого периода времени, в то время как высокая экспрессия ферропортина предсказывает 90% 10-летнюю выживаемость у пациентов с раком груди.[38] Точно так же генетические вариации генов транспортеров железа, которые, как известно, повышают уровень железа в сыворотке, также снижают срок жизни и среднее количество лет, проведенных в хорошем состоянии здоровья.[39] Было высказано предположение, что мутации, увеличивающие абсорбцию железа, такие как мутации, ответственные за гемохроматоз (см. Ниже), были выбраны во время Неолит раз, когда они предоставили селективное преимущество против железодефицитной анемии.[40] Повышение системного уровня железа становится патологическим в пожилом возрасте, что подтверждает мнение о том, что антагонистическая плейотропия или «гиперфункция» приводит к старению человека.[39]
Хроническая токсичность железа обычно является результатом более хронических синдромов перегрузки железом, связанных с генетическими заболеваниями, повторными переливаниями или другими причинами. В таких случаях запасы железа у взрослого человека могут достигать 50 граммов (в 10 раз больше нормального общего количества железа в организме) или больше. Наиболее частыми заболеваниями перегрузки железом являются: наследственный гемохроматоз (HH), вызванный мутациями в HFE ген, и более тяжелое заболевание ювенильный гемохроматоз (JH), вызванный мутациями в гемоювелин (HJV)[41] или гепсидин (HAMP). Точные механизмы большинства различных форм гемохроматоза взрослых, составляющих большинство генетических нарушений, связанных с перегрузкой железом, остаются нерешенными. Итак, хотя исследователи смогли идентифицировать генетические мутации, вызывающие несколько вариантов гемохроматоза у взрослых, теперь они должны обратить свое внимание на нормальное функционирование этих мутировавших генов.
Рекомендации
- ^ а б c Конрад М.Э., Umbreit JN (апрель 2000 г.). «Нарушения обмена железа». Медицинский журнал Новой Англии. 342 (17): 1293–4. Дои:10.1056 / NEJM200004273421716. PMID 10787338.
- ^ а б Кахлон О, Кабанчик З.И. (2002). «Лабильный пул железа: характеристика, измерение и участие в клеточных процессах». Свободная радикальная биология и медицина. 33 (8): 1037–1046. Дои:10.1016 / s0891-5849 (02) 01006-7. PMID 12374615.
- ^ а б Эндрюс NC (декабрь 1999 г.). «Нарушения обмена железа». Медицинский журнал Новой Англии. 341 (26): 1986–95. Дои:10.1056 / NEJM199912233412607. PMID 10607817.
- ^ Ян Ю., Уэйт-Кьюзик Дж. Г., Куппусами П., Юсеф А. Э. (январь 2013 г.). «Внутриклеточное свободное железо и его потенциальная роль в индуцированной сверхвысоким давлением инактивации Escherichia coli». Прикладная и экологическая микробиология. 79 (2): 722–724. Дои:10.1128 / aem.02202-12. ЧВК 3553779. PMID 23124235.
- ^ Ямамото Ю., Фукуи К., Кодзин Н., Охя Х, Кимура К., Камио Ю. (2004). «Регулирование внутриклеточного пула свободного железа с помощью Dpr обеспечивает устойчивость к кислороду Streptococcus mutans». Журнал бактериологии. 186 (18): 5997–6002. Дои:10.1128 / jb.186.18.5997-6002.2004. ЧВК 515136. PMID 15342568.
- ^ Ганц Т. (август 2003 г.). «Гепсидин, ключевой регулятор метаболизма железа и медиатор анемии воспаления». Кровь. 102 (3): 783–8. Дои:10.1182 / кровь-2003-03-0672. PMID 12663437.
- ^ Gropper, Sareen S .; Смит, Джек Л. (2013). Продвинутое питание и метаболизм человека (6-е изд.). Бельмонт, Калифорния: Уодсворт. п. 481. ISBN 978-1133104056.
- ^ Трасуэлл, А. Стюарт (15.07.2010). Азбука питания. Джон Вили и сыновья. п. 52. ISBN 9781444314229.
- ^ Камашелла К., Шриер С.Л. (07.11.2011). «Регулирование баланса железа». Своевременно. Получено 2012-03-11.
- ^ Маккай А.Т., Барроу Д., Латунде-Дада Г.О., Рольфс А., Сагер Г., Мудали Е., Мудали М., Ричардсон С., Барлоу Д., Бомфорд А., Питерс Т.Дж., Раджа К.Б., Ширали С., Хедигер М.А., Фарзане Ф., Симпсон Р.Дж. ( Март 2001 г.). «Железо-регулируемая редуктаза железа, связанная с абсорбцией пищевого железа». Наука. 291 (5509): 1755–9. Bibcode:2001Научный ... 291.1755M. Дои:10.1126 / science.1057206. PMID 11230685. S2CID 44351106.
- ^ Руо, Трейси А. (9 сентября 2005 г.). «Выявлен кишечник-переносчик гема». Клетка. 122 (5): 649–651. Дои:10.1016 / j.cell.2005.08.027. ISSN 0092-8674. PMID 16143096. S2CID 9180328.
- ^ Флеминг Р. Э., Бэкон Б. Р. (апрель 2005 г.). «Организация гомеостаза железа». Медицинский журнал Новой Англии. 352 (17): 1741–4. Дои:10.1056 / NEJMp048363. PMID 15858181.
- ^ "Утюг". Информационный бюллетень о расширении государственного университета Огайо. Государственный университет Огайо. Архивировано из оригинал 16 июня 2012 г.. Получено 25 июня, 2012.
- ^ Шриер С.Л., Бэкон Б.Р. (07.11.2011). «Синдромы перегрузки железом, отличные от наследственного гемохроматоза». Своевременно. Получено 2012-03-11.CS1 maint: использует параметр авторов (ссылка на сайт)
- ^ Кавабата Х., Жермен Р.С., Вуонг П.Т., Накамаки Т., Саид Дж.В., Кефлер Х.П. (июнь 2000 г.). «Рецептор трансферрина 2-альфа поддерживает рост клеток как в культивируемых клетках с хелатным железом, так и in vivo». Журнал биологической химии. 275 (22): 16618–25. Дои:10.1074 / jbc.M908846199. PMID 10748106.
- ^ West AP, Беннетт MJ, Селлерс VM, Andrews NC, Enns CA, Bjorkman PJ (декабрь 2000 г.). «Сравнение взаимодействий рецептора трансферрина и рецептора трансферрина 2 с трансферрином и белком наследственного гемохроматоза HFE». Журнал биологической химии. 275 (49): 38135–8. Дои:10.1074 / jbc.C000664200. PMID 11027676.
- ^ Кумар С., Шеоканд Н., Мхадешвар М.А., Радже С.И., Радже М. (январь 2012 г.). «Характеристика глицеральдегид-3-фосфатдегидрогеназы как нового рецептора трансферрина». Международный журнал биохимии и клеточной биологии. 44 (1): 189–99. Дои:10.1016 / j.biocel.2011.10.016. PMID 22062951.
- ^ Шеоканд Н., Кумар С., Малхотра Х, Тиллу В., Радже К.И., Радже М. (июнь 2013 г.). «Секретируемая глицеральдеги-3-фосфат [sic] дегидрогеназа является многофункциональным аутокринным рецептором трансферрина для приобретения клеточного железа». Biochimica et Biophysica Acta. 1830 (6): 3816–27. Дои:10.1016 / j.bbagen.2013.03.019. PMID 23541988.
- ^ а б c d е ж грамм Hentze MW, Muckenthaler MU, Galy B, Camaschella C (июль 2010 г.). «Двое в танго: регуляция метаболизма железа у млекопитающих». Клетка. 142 (1): 24–38. Дои:10.1016 / j.cell.2010.06.028. PMID 20603012. S2CID 23971474.
- ^ а б Lane, D.J.R .; Merlot, A.M .; Huang, M.L.-H .; Bae, D.-H .; Jansson, P.J .; Sahni, S .; Калиновский, D.S .; Ричардсон, Д. (Май 2015 г.). «Поглощение, перемещение и метаболизм клеточного железа: ключевые молекулы и механизмы и их роль в развитии болезней». Biochimica et Biophysica Acta (BBA) - Исследование молекулярных клеток. 1853 (5): 1130–1144. Дои:10.1016 / j.bbamcr.2015.01.021. PMID 25661197.
- ^ а б c Иегуда С., Мостофски Д.И., ред. (2010). Дефицит железа и перегрузка от фундаментальной биологии до клинической медицины. Питание и здоровье. Нью-Йорк, штат Нью-Йорк: Humana Press. п. 230. ISBN 9781934115220.
- ^ Финни Л.А., О'Халлоран ТВ (май 2003 г.). «Переходные металлы в клетке: выводы из химии рецепторов ионов металлов». Наука. 300 (5621): 931–6. Bibcode:2003Наука ... 300..931F. Дои:10.1126 / science.1085049. PMID 12738850. S2CID 14863354.
- ^ Филпотт, Кэролайн С .; Рю, Мун-Сон (22 июля 2014 г.). «Специальная доставка: распределение железа в цитозоле клеток млекопитающих». Границы фармакологии. 5: 173. Дои:10.3389 / fphar.2014.00173. ЧВК 4106451. PMID 25101000.
- ^ Arosio P, Levi S (август 2002 г.). «Ферритин, гомеостаз железа и окислительное повреждение». Свободная радикальная биология и медицина. 33 (4): 457–63. Дои:10.1016 / s0891-5849 (02) 00842-0. PMID 12160928.
- ^ Руо Т.А., Куперман С. (сентябрь 2006 г.). «Метаболизм железа в мозге». Семинары по детской неврологии. 13 (3): 142–8. Дои:10.1016 / j.spen.2006.08.002. PMID 17101452.
- ^ Ганц Т. (март 2005 г.). «Клеточное железо: ферропортин - единственный выход». Клеточный метаболизм. 1 (3): 155–7. Дои:10.1016 / j.cmet.2005.02.005. PMID 16054057.
- ^ Ду Ф, Цянь Ц., Цянь З.М., Ву XM, Се Х, Юнг У., Ке И (июнь 2011 г.). «Гепсидин напрямую ингибирует экспрессию рецептора трансферрина 1 в астроцитах через путь циклической АМФ-протеинкиназы А». Глия. 59 (6): 936–45. Дои:10.1002 / glia.21166. PMID 21438013. S2CID 25678955.
- ^ Борадия, Вишант Махендра; Радже, Манодж; Радже, Чая Айенгар (1 декабря 2014 г.). «Белок подрабатывает метаболизмом железа: глицеральдегид-3-фосфатдегидрогеназа (GAPDH)». Сделки Биохимического Общества. 42 (6): 1796–1801. Дои:10.1042 / BST20140220. PMID 25399609.
- ^ Шеоканд Н., Малхотра Х., Кумар С., Тиллу В.А., Чаухан А.С., Радже С.И., Радже М. (октябрь 2014 г.). «Находящийся под луной GAPDH на клеточной поверхности привлекает апотрансферрин для воздействия на выход железа из клеток млекопитающих». Журнал клеточной науки. 127 (Pt 19): 4279–91. Дои:10.1242 / jcs.154005. PMID 25074810.
- ^ Каутц Л., Юнг Дж., Валор Э.В., Ривелла С., Немет Е., Ганц Т. (июль 2014 г.). «Идентификация эритроферрона как эритроидного регулятора метаболизма железа». Природа Генетика. 46 (7): 678–84. Дои:10,1038 / нг.2996. ЧВК 4104984. PMID 24880340.
- ^ Мукенталер М.Ю., Гали Б., Хентце М.В. (2008). «Системный гомеостаз железа и регуляторная сеть железо-чувствительных элементов / железо-регуляторных белков (IRE / IRP)». Ежегодный обзор питания. 28: 197–213. Дои:10.1146 / annurev.nutr.28.061807.155521. PMID 18489257.
- ^ Холлберг L (1987). «Пшеничная клетчатка, фитаты и абсорбция железа». Сканд J Gastroenterol Suppl. 129: 73–9. Дои:10.3109/00365528709095855. PMID 2820048.
- ^ Линч С.Р. (2000). «Влияние кальция на усвоение железа». Nutr Res Rev. 13 (2): 141–58. Дои:10.1079/095442200108729043. PMID 19087437.
- ^ Disler PB, Lynch SR, Charlton RW, Torrance JD, Bothwell TH, Walker RB и др. (1975). «Влияние чая на усвоение железа». Кишечник. 16 (3): 193–200. Дои:10.1136 / гут.16.3.193. ЧВК 1410962. PMID 1168162.
- ^ "Своевременно".
- ^ Аннибале, Бруно; Капурсо, Габриэле; Мартино, Джина; Гросси, Кристина; Делле Фаве, Джанфранко (декабрь 2000 г.). «Железодефицитная анемия и инфекция Helicobacter pylori». Международный журнал противомикробных агентов. 16 (4): 515–519. Дои:10.1016 / s0924-8579 (00) 00288-0. PMID 11118871.
- ^ Рудольф CD (2003). Педиатрия Рудольфа. Нью-Йорк: McGraw-Hill, Medical Pub. Дивизия. ISBN 978-0-07-112457-7.
- ^ Pinnix, Zandra K .; Миллер, Лэнс Д .; Ван, Вэй; Д’Агостино, Ральф; Куте, Тим; Willingham, Mark C .; Хэтчер, Хизер; Тесфай, Лия; Суй, Гуанчжоу (2010-08-04). «Ферропортин и регуляция железа в прогрессировании и прогнозе рака груди». Научная трансляционная медицина. 2 (43): 43ra56. Дои:10.1126 / scitranslmed.3001127. ISSN 1946-6234. ЧВК 3734848. PMID 20686179.
- ^ а б Тиммерс, Пол Р. Х. Дж .; Уилсон, Джеймс Ф .; Джоши, Питер К .; Дилен, Джорис (июль 2020 г.). «Многофакторное геномное сканирование позволяет выявить новые локусы и метаболизм гема в процессе старения человека». Nature Communications. 11 (3570): 3570. Bibcode:2020НатКо..11.3570Т. Дои:10.1038 / с41467-020-17312-3. ЧВК 7366647. PMID 32678081.
- ^ Раметта, Рафаэла; Мерони, Марика; Донджованни, Паола (15 мая 2020 г.). «От окружающей среды к геному и обратно: урок мутаций HFE». Международный журнал молекулярных наук. 21 (10): 3505. Дои:10.3390 / ijms21103505. ЧВК 7279025. PMID 32429125.
- ^ Severyn CJ, Shinde U, Rotwein P (сентябрь 2009 г.). «Молекулярная биология, генетика и биохимия семейства отталкивающих молекул наведения». Биохимический журнал. 422 (3): 393–403. Дои:10.1042 / BJ20090978. ЧВК 4242795. PMID 19698085.
дальнейшее чтение
- Эндрюс С., Нортон I, Салунхе А.С., Гудлак Х, Али В.С., Мурад-Ага Х, Корнелис П. (2013). «Глава 7, Контроль метаболизма железа у бактерий». В Banci L (ред.). Металломика и клетка. Ионы металлов в науках о жизни. 12. Springer. С. 203–39. Дои:10.1007/978-94-007-5561-1_7. ISBN 978-94-007-5560-4. PMID 23595674. электронная книга ISBN 978-94-007-5561-1 ISSN 1559-0836 электронный-ISSN 1868-0402
- Эндрюс NC (май 2004 г.). «Анемия воспаления: связь цитокин-гепсидин». Журнал клинических исследований. 113 (9): 1251–3. Дои:10.1172 / JCI21441. ЧВК 398435. PMID 15124013.
- Camaschella C (декабрь 2005 г.). «Понимание гомеостаза железа посредством генетического анализа гемохроматоза и родственных заболеваний». Кровь. 106 (12): 3710–7. Дои:10.1182 / кровь-2005-05-1857. PMID 16030190.
- Фрейзер Д.М., Андерсон Г.Дж. (октябрь 2005 г.). «Импорт железа. I. Абсорбция железа в кишечнике и его регуляция». Американский журнал физиологии. Физиология желудочно-кишечного тракта и печени. 289 (4): G631–5. Дои:10.1152 / ajpgi.00220.2005. PMID 16160078.
- Инсел П., Росс Д., МакМахон К., Бернштейн М. (2011). "Утюг". Питание (4-е изд.). Садбери, Массачусетс: Джонс и Бартлетт Издательство. С. 510–514. ISBN 978-0-7637-7663-3. Получено 25 июня, 2012. См. Особенно стр. 513-514CS1 maint: использует параметр авторов (ссылка на сайт)
- Ламми-Киф CJ, Couch SC, Philipson EH, ред. (2008). «Диетическое разнообразие и модификация железа». Справочник по питанию и беременности. Питание и здоровье. Тотова, Нью-Джерси: Humana Press. С. 350–351. Дои:10.1007/978-1-59745-112-3. ISBN 978-1-59745-112-3. Получено 25 июня, 2012.
- Панель по микронутриентам; Подкомитеты по верхним референсным уровням питательных веществ и толкованию и использованию рекомендуемых диетических поступлений; Постоянный комитет по научной оценке рекомендуемых диетических рационов (2001). "Утюг". Нормы потребления витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка. Вашингтон, округ Колумбия: Совет по продовольствию и питанию, Институт медицины. С. 290–393. ISBN 978-0-309-07279-3. Получено 25 июня, 2012.
- Рейли C (2004). "Утюг". Пищевые микроэлементы. Оксфорд, Великобритания и Эймс, Айова: Blackwell Publishing. С. 35–81. ISBN 978-1-4051-1040-2. Получено 25 июня, 2012.
внешняя ссылка
- Подробный информационный бюллетень NIH по железу и питанию
- Институт заболеваний железа: некоммерческая группа, занимающаяся проблемами железа; на сайте есть полезные ссылки и информация о заболеваниях, связанных с железом.
- Интерактивный медицинский обучающий портал по метаболизму железа
- Информация о железе вне организма
