SCN8A - SCN8A
Натриевый канал, потенциал-gated, тип VIII, альфа-субъединица также известен как SCN8A или же Nav1.6 это мембрана белок закодировано SCN8A ген.[5] Nav1.6 представляет собой изоформу одного натриевого канала и является первичным напряженно-управляемый натриевый канал на узлы Ранвье. Каналы сконцентрированы в сенсорных и моторных аксонах периферической нервной системы и сгруппированы в узлах центральной нервной системы.[6][7][8]
Структура
Nav1.6 кодируется геном SCN8A, который содержит 27 экзонов и имеет размер 170 т.п.н. Напряжение закрытого натриевого канала состоит из 1980 остатков. Как и другие натриевые каналы, Nav1.6 представляет собой мономер, состоящий из четырех гомологичных доменов (I-IV) и 25 трансмембранных сегментов. SCN8A кодирует трансмембранные сегменты S3-S4, которые образуют внутриклеточную петлю.[9]
Функция
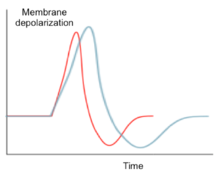
Как и другие ионные каналы натрия, Nav1.6 способствует распространению потенциала действия, когда мембранный потенциал является деполяризованный притоком Na+ ионы. Однако Nav1.6 способен выдерживать повторяющееся возбуждение и стрельбу. Высокочастотная характеристика возбуждения Nav1.6 вызвано постоянным и возобновляющимся натриевым током. Эта характеристика вызвана медленной активацией натриевого канала после реполяризации,[10] который допускает установившийся натриевый ток после начального распространения потенциала действия. Установившийся натриевый ток способствует деполяризации следующего потенциала действия. Кроме того, порог активации Nav1,6 ниже по сравнению с другими распространенными натриевыми каналами, такими как Nav1.2. Эта функция позволяет Nav1,6 каналов для быстрого восстановления после инактивации и поддержания высокого уровня активности.[11]
Nav1.6 экспрессируется главным образом в узлах Ранвье в миелинизированных аксонах, но также в высокой степени концентрируется на дистальном конце аксонного холма, в гранулярных клетках мозжечка и нейронах Пуркинье и в меньшей степени в немиелинизированных аксонах и дендритах.[11] Учитывая расположение Наv1.6, канал способствует порогу срабатывания данного нейрона, поскольку электрические импульсы от различных входов суммируются на аксональный бугорок чтобы достичь порога возбуждения перед распространением по аксону. Другие изоформы натриевых каналов экспрессируются на дистальном конце бугорка аксона, включая Nav1.1 и Nav1.2.[7]

NaV1,6 канала демонстрируют устойчивость к регуляции фосфорилирования белков. Натриевые каналы модулируются протеинкиназа А и протеинкиназа C (PKC) фосфорилирование, которое снижает пиковые токи натрия. Дофамин и ацетилхолин уменьшают натриевые токи в пирамидных нейронах гиппокампа за счет фосфорилирования. Точно так же рецепторы серотонина в префронтальной коре регулируются PKC, чтобы уменьшить натриевые токи.[10] Фосфорилированная регуляция натриевых каналов помогает замедлить инактивацию. Однако NaV1.6 каналов не имеют адекватных сайтов протеинкиназы. Сайты фосфорилирования по аминокислотным остаткам Ser573 и Ser687 обнаружены в других натриевых каналах, но не очень консервативны в NaV1.6. Отсутствие остатков серина приводит к способности канала постоянно и быстро срабатывать после инактивации.[13]
NaV1.6, наоборот, регулируется кальмодулином (CaM). CaM взаимодействует с изолейцин-глутаминовым (IQ) мотивом NaV1.6, чтобы отключить канал. Мотив IQ сворачивается в спираль при взаимодействии с CaM, и CaM инактивирует Na.V1,6 в зависимости от концентрации кальция. ЗатемV1.6 IQ демонстрирует умеренное сродство к CaM по сравнению с другими изоформами натриевых каналов, такими как NaV1.6. Разница в сродстве к CaM способствует увеличению NaV1.6 устойчивость к инактивации.[14]
Клиническое значение
Первую известную мутацию у человека обнаружили Кришна Вирама и Майкл Хаммер в 2012 году.[15] Геном ребенка с эпилептической энцефалопатией был секвенирован и выявил de novo миссенс-мутация, p.Asn1768Asp. Миссенс-мутации в Nav1.6 увеличил функцию канала за счет увеличения продолжительности постоянного натриевого тока и предотвратил полную инактивацию после гиперполяризации. 20% первоначального тока сохранялось через 100 мс после гиперполяризации, что приводило к повышенной возбудимости нейрона и увеличивало вероятность преждевременного или непреднамеренного срабатывания. Помимо эпилептической энцефалопатии, пациент имел задержку в развитии, аутизм, умственную отсталость и атаксию.
Конверсия натриевых каналов участвует в демиелинизации аксонов, связанных с рассеянным склерозом (РС). На ранних стадиях миелинизации незрелый NavВ 1,2 канала больше, чем Nav1,6 в аксонах. Однако зрелый Nav1,6 канала постепенно заменяют другие каналы по мере продолжения миелинизации, что позволяет увеличить скорость проводимости с учетом более низкого порога Nav1.6.[7] Однако в моделях MS конверсия натриевых каналов из зрелого Nav1,6 к Nav1.2 соблюдается.[16]
Смотрите также
- Натриевый канал
- паралитический - ортолог SCN8A в Дрозофила
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000196876 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000023033 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ «Ген Entrez: натриевые каналы SCN8A, управляемые по напряжению, тип VIII, альфа-субъединица».
- ^ Колдуэлл Дж. Х., Шаллер К. Л., Лашер Р. С., Пелеш Э., Левинсон С. Р. (май 2000 г.). «Натриевые каналы Na (v) 1.6 локализованы в узлах ранвье, дендритах и синапсах». Труды Национальной академии наук Соединенных Штатов Америки. 97 (10): 5616–20. Дои:10.1073 / pnas.090034797. ЧВК 25877. PMID 10779552.
- ^ а б c Бойко Т., Расбанд М.Н., Левинсон С.Р., Колдуэлл Дж. Х., Мандель Дж., Триммер Дж. С., Мэтьюз Дж. (Апрель 2001 г.). «Компактный миелин определяет дифференциальное нацеливание двух изоформ натриевых каналов в одном аксоне». Нейрон. 30 (1): 91–104. Дои:10.1016 / s0896-6273 (01) 00265-3. PMID 11343647. S2CID 7168889.
- ^ Цумака Э., Тишлер А.С., Сангамесваран Л., Эглен Р.М., Хантер Дж.С., Новакович С.Д. (апрель 2000 г.). «Дифференциальное распределение тетродотоксин-чувствительного натриевого канала rPN4 / NaCh6 / Scn8a в нервной системе». Журнал неврологических исследований. 60 (1): 37–44. Дои:10.1002 / (SICI) 1097-4547 (20000401) 60: 1 <37 :: AID-JNR4> 3.0.CO; 2-W. PMID 10723066.
- ^ О'Брайен Дж. Э., Мейслер М. Х. (октябрь 2013 г.). «Натриевый канал SCN8A (Nav1.6): свойства и мутации de novo при эпилептической энцефалопатии и умственной отсталости». Границы генетики. 4: 213. Дои:10.3389 / fgene.2013.00213. ЧВК 3809569. PMID 24194747.
- ^ а б Чен Ю., Ю. Ф. Х., Шарп Е. М., Бичем Д., Шойер Т., Каттералл, Вашингтон, США (август 2008 г.). «Функциональные свойства и дифференциальная нейромодуляция каналов Na (v) 1.6». Молекулярная и клеточная нейронауки. 38 (4): 607–15. Дои:10.1016 / j.mcn.2008.05.009. ЧВК 3433175. PMID 18599309.
- ^ а б Freeman SA, Desmazières A, Fricker D, Lubetzki C, Sol-Foulon N (февраль 2016 г.). «Механизмы кластеризации натриевых каналов и их влияние на проведение аксонального импульса». Клеточные и молекулярные науки о жизни. 73 (4): 723–35. Дои:10.1007 / s00018-015-2081-1. ЧВК 4735253. PMID 26514731.
- ^ Редди Чичили В.П., Сяо Й., Ситхараман Дж., Камминз Т.Р., Сивараман Дж. (2013). «Структурная основа модуляции нейронального потенциал-зависимого натриевого канала NaV1.6 с помощью кальмодулина». Научные отчеты. 3: 2435. Дои:10.1038 / srep02435. ЧВК 3743062. PMID 23942337.
- ^ Чен Й., Ю. Ф. Х., Шарп Е. М., Бичем Д., Шойер Т., Каттералл, Вашингтон. (Август 2008 г.). «Функциональные свойства и дифференциальная нейромодуляция каналов Na (v) 1.6». Молекулярная и клеточная нейронауки. 38 (4): 607–15. Дои:10.1016 / j.mcn.2008.05.009. ЧВК 3433175. PMID 18599309.
- ^ Редди Чичили, вице-президент, Сяо Ю., Ситхараман Дж., Камминз Т.Р., Сивараман Дж. (14 августа 2013 г.). «Структурная основа модуляции нейронального потенциал-зависимого натриевого канала NaV1.6 с помощью кальмодулина». Научные отчеты. 3: 2435. Дои:10.1038 / srep02435. ЧВК 3743062. PMID 23942337.
- ^ Вирама К.Р., О'Брайен Дж. Э., Мейслер М. Х., Ченг Х, Диб-Хадж С. Д., Ваксман С. Г., Талвар Д., Гирираджан С., Эйхлер Э. Э., Рестифо Л. Л., Эриксон Р. П., Хаммер М. Ф. (март 2012 г.). «De novo патогенная мутация SCN8A, идентифицированная с помощью полногеномного секвенирования семейного квартета, пораженного детской эпилептической энцефалопатией и SUDEP». Американский журнал генетики человека. 90 (3): 502–10. Дои:10.1016 / j.ajhg.2012.01.006. ЧВК 3309181. PMID 22365152.
- ^ Кранер М.Дж., Ньюкомб Дж., Блэк Д.А., Хартл С., Кузнер М.Л., Ваксман С.Г. (май 2004 г.). «Молекулярные изменения в нейронах при рассеянном склерозе: изменение аксональной экспрессии натриевых каналов Nav1.2 и Nav1.6 и обменника Na + / Ca2 +». Труды Национальной академии наук Соединенных Штатов Америки. 101 (21): 8168–73. Дои:10.1073 / pnas.0402765101. ЧВК 419575. PMID 15148385.
дальнейшее чтение
- Каттералл В.А., Голдин А.Л., Ваксман С.Г. (декабрь 2005 г.). "Международный союз фармакологии. XLVII. Номенклатура и взаимосвязь между структурой и функцией потенциалзависимых натриевых каналов". Фармакологические обзоры. 57 (4): 397–409. Дои:10.1124 / пр.57.4.4. PMID 16382098. S2CID 7332624.
- Берджесс Д.Л., Корман Д.К., Галт Дж., Пламмер Н.В., Джонс Дж. М., Спир Б., Мейслер М. Х. (август 1995 г.). "Мутация нового гена натриевого канала, Scn8a, при болезни моторной замыкательной пластинки мутанта мыши"'". Природа Генетика. 10 (4): 461–5. Дои:10.1038 / ng0895-461. PMID 7670495. S2CID 28941670.
- Пламмер Н.В., МакБерни М.В., Мейслер М.Х. (сентябрь 1997 г.). «Альтернативный сплайсинг натриевого канала SCN8A предсказывает усеченный двухдоменный белок в мозге плода и ненейронных клетках». Журнал биологической химии. 272 (38): 24008–15. Дои:10.1074 / jbc.272.38.24008. PMID 9295353.
- Пламмер Н.В., Галт Дж., Джонс Дж. М., Берджесс Д. Л., Спрунгер Л. К., Корман Д. К., Мейслер М. Х. (декабрь 1998 г.). «Организация экзона, кодирующая последовательность, физическое картирование и полиморфные внутригенные маркеры для гена человеческого нейронального натриевого канала SCN8A». Геномика. 54 (2): 287–96. Дои:10.1006 / geno.1998.5550. PMID 9828131.
- Анис Й., Нюрнберг Б., Височек Л., Рейсс Н., Наор З., Коэн-Армон М. (март 1999 г.). «Активация Go-белков деполяризацией мембраны, отслеживаемая фотоаффинной меткой in situ галфа-белков с помощью [alpha32P] GTP-азидоанилида». Журнал биологической химии. 274 (11): 7431–40. Дои:10.1074 / jbc.274.11.7431. PMID 10066808.
- Колдуэлл Дж. Х., Шаллер К. Л., Лэшер Р. С., Пелеш Э., Левинсон С. Р. (май 2000 г.). «Натриевые каналы Na (v) 1.6 локализованы в узлах ранвье, дендритах и синапсах». Труды Национальной академии наук Соединенных Штатов Америки. 97 (10): 5616–20. Дои:10.1073 / pnas.090034797. ЧВК 25877. PMID 10779552.
- Виттмак Е.К., Раш А.М., Кранер М.Дж., Гольдфарб М., Ваксман С.Г., Диб-Хадж С.Д. (июль 2004 г.). «Фактор 2B, гомологичный фактору роста фибробластов: ассоциация с Nav1.6 и избирательная колокализация в узлах Ранвье аксонов дорсального корешка». Журнал неврологии. 24 (30): 6765–75. Дои:10.1523 / JNEUROSCI.1628-04.2004. ЧВК 6729706. PMID 15282281.
- Раймонд С.К., Касл Дж., Гарретт-Энгеле П., Armor CD, Кан З., Циноремас Н., Джонсон Дж. М. (октябрь 2004 г.). «Экспрессия альтернативно сплайсированных генов альфа-субъединиц натриевых каналов. Уникальные паттерны сплайсинга наблюдаются в ганглиях задних корешков». Журнал биологической химии. 279 (44): 46234–41. Дои:10.1074 / jbc.M406387200. PMID 15302875.
- Дрюс В.Л., Либерман А.П., Мейслер М.Х. (февраль 2005 г.). «Множественные транскрипты натриевого канала SCN8A (Na (V) 1.6) с альтернативными 5'- и 3'-нетранслируемыми областями и начальная характеристика промотора SCN8A». Геномика. 85 (2): 245–57. Дои:10.1016 / j.ygeno.2004.09.002. PMID 15676283.
- Виттмак Е.К., Раш А.М., Хадмон А., Ваксман С.Г., Диб-Хадж С.Д. (июль 2005 г.). «Управляемый напряжением натриевый канал Nav1.6 модулируется митоген-активируемой протеинкиназой p38». Журнал неврологии. 25 (28): 6621–30. Дои:10.1523 / JNEUROSCI.0541-05.2005. ЧВК 6725417. PMID 16014723.
- Скьявон Э, Сакко Т., Кассулини Р.Р., Гуррола Г., Темпия Ф., Поссани Л.Д., Ванке Э. (июль 2006 г.). «Возрождающийся датчик тока и напряжения усиливает активацию токсином бета-скорпиона только в канале Nav1.6. Значение для нейронов Пуркинье мышей». Журнал биологической химии. 281 (29): 20326–37. Дои:10.1074 / jbc.M600565200. PMID 16702217.
- Сирахата Э., Ивасаки Х., Такаги М., Лин С., Беннетт В., Окамура Ю., Хаясака К. (сентябрь 2006 г.). «Анкирин-G регулирует инактивацию нейронального натриевого канала, Nav1.6». Журнал нейрофизиологии. 96 (3): 1347–57. Дои:10.1152 / jn.01264.2005. PMID 16775201.
- Блэк Дж. А., Ньюкомб Дж., Трапп Б. Д., Ваксман С. Г. (сентябрь 2007 г.). «Экспрессия натриевых каналов в бляшках хронического рассеянного склероза». Журнал невропатологии и экспериментальной неврологии. 66 (9): 828–37. Дои:10.1097 / nen.0b013e3181462841. PMID 17805013.
внешняя ссылка
- «Веб-сайт и реестр SCN8A». Университет Аризоны.
Эта статья включает текст из Национальная медицинская библиотека США, который находится в всеобщее достояние.