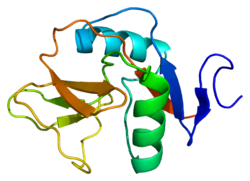
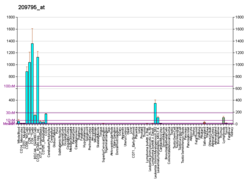
CD69 - CD69
CD69 (Cблеск Differentiation 69) является человеческим трансмембранным C-типом лектин белок закодировано CD69 ген. Это маркер ранней активации, который экспрессируется в гемопоэтических стволовых клетках, Т-клетках и многих других типах клеток иммунной системы.[5] Он также участвует в дифференцировке Т-клеток, а также в задержке лимфоцитов в лимфоидных органах.
Функция
Активация Т-лимфоцитов и естественных киллеров (NK) как in vivo, так и in vitro, индуцирует экспрессию CD69. Эта молекула, которая, по-видимому, является самым ранним индуцибельным гликопротеином клеточной поверхности, приобретенным во время активации лимфоидов, участвует в пролиферации лимфоцитов и функционирует как передающий сигнал рецептор в лимфоцитах, включая клетки естественных киллеров (NK), и тромбоциты (Cambiaggi et al., 1992 г.) [предоставлено OMIM].[6]
Строение и лиганды
Ген, кодирующий CD69, расположен в генном комплексе NK на хромосоме 6 и хромосоме 12 у мышей и людей соответственно.[7] Сигнальные пути активации в лимфоцитах, NK клетки, дендритные клетки и другие типы клеток активируют факторы транскрипции, такие как NF-κB, ЭРГ-1 (ген-1, связанный с трансформацией эритробластов), и АП-1 (белок-активатор), чтобы способствовать транскрипции гена CD69.[8][7] Белок CD69 подвергается посттрансляционным модификациям. А именно дифференциально гликозилированный для получения пептида 28 кДа или пептида 32 кДа. Два из этих пептидов случайным образом объединяются с образованием гомодимера, связанного дисульфидной связью.[7] Эти субъединицы имеют Лектиновый домен С-типа (CTLD) который связывает лиганды, трансмембранный домен и цитоплазматический хвост, который передает сигналы внутрь клетки.[7]
CD69 лишен характерного Ca2+ связывающих остатков в CTLD, что указывает на то, что он может связываться с белками, а не с углеводами, обычным лигандом CTLD.[9][7] Было показано, что CD69 связывается с Гал-1, белок, связывающий углеводы, расположенный на некоторых дендритных клетках и макрофагах, в дополнение к Мыл9 / 12.[8] Другие лиганды еще предстоит идентифицировать. Однако известно, что связывание лигандов инициирует Jak / Stat сигнальный путь, а также mTOR /HIF1-α путь.[9][8][7] Известно также, что CD69 взаимодействует и опосредует рецепторы S1P и LAT1, которые, среди прочего, влияют на выход лимфоцитов в лимфоидные органы.[10][8] Необходимо провести дополнительную работу, чтобы полностью охарактеризовать взаимодействия CD69-лиганд, а также метод передачи внутриклеточных сигналов CD69.
Дифференцировка Т-клеток
Экспрессия CD69 была связана с обоими регуляторные Т-клетки (Трег), Т-клетка памяти и Bcl6 вотCD69 ЗдравствуйПредшественники плазмобластов LZ GC B.[11] Предшественники Treg покидают тимус, экспрессируя CD69, и полностью дифференцируются в Treg-клетки в периферических тканях, когда они сталкиваются с антигенами и другими цитокинами, такими как Ил-2.[12] Через сигнальный путь JAK / STAT активация CD69 также индуцирует продукцию TGF-β а также IL-2, которые, как упоминалось выше, способствуют дифференцировке Treg-клеток.[8] Кроме того, известно, что CD69 активируется с помощью передачи сигналов NF-κB в начале иммунного ответа. Затем длительный иммунный ответ поддерживается неканоническим путем NF-κB, который, в свою очередь, связан с дифференцировкой Treg.[7]
Помимо дифференцировки Treg, CD69 является обычным маркером предшественников и зрелых резидентных Т-клеток памяти (TRM), которые локализуются в периферических тканях.[13][9] TGF-β также отвечает за развитие TRM, тем самым способствуя дифференцировке TRM аналогично дифференцировке Treg.[14]
Миграция лимфоцитов
Наиболее лимфоциты выражать сфингозин-1-фосфатные рецепторы (S1P1-5), которые G-белковые рецепторы расположен в клеточной мембране, которая связывается с лигандом сфингозин-1-фосфат (S1P). S1P - это метаболит сфинголипида, который присутствует в большом количестве в кровотоке и, связываясь с S1P1, способствует выходу лимфоцитов из лимфоидных органов, чтобы они могли перемещаться в пораженные ткани.[15][8] Однако, когда Т-лимфоциты активируются в лимфоидном органе через цитокин и TCR сигнализируя, CD69 экспрессируется и образует комплекс с S1P1 (не S1P3 или S1P5). Эта ассоциация зависит от взаимодействия между трансмембранным доменом CD69 и спиралью-4 S1P1. После образования этого комплекса S1P1 интернализуется и разрушается внутри клетки, подавляя ее способность связывать S1P и инициировать передачу сигналов ниже по течению. Это, в свою очередь, приводит к временной задержке лимфоцитов в лимфатических органах.[8] Считается, что задержка лимфоцитов в лимфатических узлах может увеличить шанс успешной активации лимфоцитов, особенно если исходный сигнал активации был слабым. Аналогичным образом CD69 экспрессируется в тимоциты после положительного отбора можно гарантировать, что Т-клетки полностью созреют в тимусе до поступления в кровоток.[10]
Некоторые исследования показали, что S1P1 и CD69 совместно регулируют, так что когда CD69 присутствует в большем количестве, это приводит к удалению S1P1 из мембраны, как упоминалось выше.[10] Однако, если S1P1 более распространен, чем CD69, как это было бы в случае зрелых Т-клеток, локализация CD69 в мембране снижается. Таким образом, регуляция экспрессии и локализации CD69 и S1P1 совместно влияет на выход и миграцию лимфоцитов.[10]
Смотрите также
Рекомендации
- ^ а б c ГРЧ38: Ансамбль выпуск 89: ENSG00000110848 - Ансамбль, Май 2017
- ^ а б c GRCm38: выпуск Ensembl 89: ENSMUSG00000030156 - Ансамбль, Май 2017
- ^ "Справочник человека по PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ "Ссылка на Mouse PubMed:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США.
- ^ Зиглер С.Ф., Рамсделл Ф., Олдерсон М.Р. (сентябрь 1994 г.). «Активационный антиген CD69». Стволовые клетки. 12 (5): 456–65. Дои:10.1002 / шток.5530120502. PMID 7804122. S2CID 22182832.
- ^ «Ген Энтреза: молекула CD69 CD69».
- ^ а б c d е ж грамм Радулович К., Нисс Дж. Х. (2015). «CD69 - важнейший регулятор воспаления кишечника: новая молекула-мишень для лечения ВЗК?». Журнал иммунологических исследований. 2015: 497056. Дои:10.1155/2015/497056. ЧВК 4352431. PMID 25759842.
- ^ а б c d е ж грамм Cibrián D, Sánchez-Madrid F (июнь 2017 г.). «CD69: от маркера активации к метаболическому привратнику». Европейский журнал иммунологии. 47 (6): 946–953. Дои:10.1002 / eji.201646837. ЧВК 6485631. PMID 28475283.
- ^ а б c Кимура М.Ю., Хаяшизаки К., Токойода К., Такамура С., Мотохаши С., Накаяма Т. (июль 2017 г.). «Решающая роль CD69 в аллергических воспалительных реакциях: система CD69-Myl9 в патогенезе воспаления дыхательных путей». Иммунологические обзоры. 278 (1): 87–100. Дои:10.1111 / imr.12559. PMID 28658550. S2CID 4327394.
- ^ а б c d Цистер Дж. Г., Шваб С. Р. (2012). «Выход сфингозин-1-фосфата и лимфоцитов из лимфоидных органов». Ежегодный обзор иммунологии. 30: 69–94. Дои:10.1146 / аннурев-иммунол-020711-075011. PMID 22149932.
- ^ Исэ, Ватару (17 апреля 2018 г.). «Т-фолликулярная клетка-помощник-зародышевый центр. Сила взаимодействия В-клеток регулирует проникновение в плазматические клетки или переработку клеточной судьбы зародышевого центра». Иммунитет. 48 (4): 702–715.e4. Дои:10.1016 / j.immuni.2018.03.027. PMID 29669250.
- ^ Гонсалес-Амаро Р., Марасуэла М. (апрель 2016 г.). «Т-регуляторные (Treg) и Т-хелперные 17 (Th17) лимфоциты при аутоиммунитете щитовидной железы». Эндокринный. 52 (1): 30–8. Дои:10.1007 / s12020-015-0759-7. PMID 26475497. S2CID 30154540.
- ^ Фарбер Д.Л., Юданин Н.А., Restifo Н.П. (январь 2014 г.). «Т-клетки памяти человека: генерация, компартментализация и гомеостаз». Обзоры природы. Иммунология. 14 (1): 24–35. Дои:10.1038 / nri3567. ЧВК 4032067. PMID 24336101.
- ^ Мюллер С.Н., Маккей Л.К. (февраль 2016 г.). «Резидентные Т-клетки памяти: местные специалисты по иммунной защите». Обзоры природы. Иммунология. 16 (2): 79–89. Дои:10.1038 / нет.2015.3. PMID 26688350. S2CID 3155731.
- ^ Гаррис С.С., Блахо В.А., Хла Т, Хан М.Х. (июль 2014 г.). «Передача сигналов рецептора 1 сфингозин-1-фосфата в Т-клетках: трафик и за его пределами». Иммунология. 142 (3): 347–53. Дои:10.1111 / imm.12272. ЧВК 4080950. PMID 24597601.
дальнейшее чтение
- Ли Кью, Лан Икс, Хан Х, Ван Дж. (Январь 2019 г.). «Экспрессия Tmem119 / Sall1 и Ccr2 / CD69 в FACS-сортированных популяциях клеток микроглии и моноцитов / макрофагов после внутримозгового кровоизлияния». Front Cell Neurosci. 12: 520. Дои:10.3389 / fncel.2018.00520. ЧВК 6333739. PMID 30687011.
- Cambiaggi C, Scupoli MT, Cestari T, Gerosa F, Carra G, Tridente G, Accolla RS (1992). «Конститутивная экспрессия CD69 в межвидовых Т-клеточных гибридах и определение локуса на хромосоме 12 человека». Иммуногенетика. 36 (2): 117–20. Дои:10.1007 / BF00215288. PMID 1612643. S2CID 20364822.
- Лопес-Кабрера М., Муньос Э., Бласкес М.В., Урса М.А., Сантис А.Г., Санчес-Мадрид Ф. (сентябрь 1995 г.). «Регуляция транскрипции гена, кодирующего рецептор лейкоцитов лектина С-типа человека AIM / CD69, и функциональная характеристика его элементов, чувствительных к фактору некроза опухоли альфа». Журнал биологической химии. 270 (37): 21545–51. Дои:10.1074 / jbc.270.37.21545. PMID 7665567.
- Безуска К., Неповим А., Хорват О, Посписил М., Хаманн Дж., Фейзи Т. (март 1995 г.). «Антиген CD 69 лимфоцитов человека представляет собой кальций-зависимый углевод-связывающий белок». Сообщения о биохимических и биофизических исследованиях. 208 (1): 68–74. Дои:10.1006 / bbrc.1995.1306. PMID 7887967.
- Сантис А.Г., Лопес-Кабрера М., Хаманн Дж., Штраус М., Санчес-Мадрид Ф. (июль 1994 г.). «Структура гена, кодирующего антиген CD69 активации ранних лимфоцитов человека: рецептор лектина С-типа, эволюционно связанный с семейством генов рецепторов, специфичных для естественных клеток-киллеров». Европейский журнал иммунологии. 24 (7): 1692–7. Дои:10.1002 / eji.1830240735. PMID 8026529.
- Зиглер С.Ф., Рамсделл Ф., Хьеррилд К.А., Армитаж Р.Дж., Грабштейн К.Х., Хеннен К.Б., Фарра Т., Фанслоу В.К., Шевач Е.М., Олдерсон М.Р. (июль 1993 г.). «Молекулярная характеристика антигена ранней активации CD69: мембранный гликопротеин типа II, относящийся к семейству антигенов активации естественных клеток-киллеров». Европейский журнал иммунологии. 23 (7): 1643–8. Дои:10.1002 / eji.1830230737. PMID 8100776.
- Лопес-Кабрера М., Сантис А.Г., Фернандес-Руис Э., Блахер Р., Эш Ф., Санчес-Матеос П., Санчес-Мадрид Ф. (август 1993 г.). «Молекулярное клонирование, экспрессия и хромосомная локализация самого раннего антигена активации лимфоцитов человека AIM / CD69, нового члена суперсемейства рецепторов передачи сигналов животных лектинов С-типа». Журнал экспериментальной медицины. 178 (2): 537–47. Дои:10.1084 / jem.178.2.537. ЧВК 2191117. PMID 8340758.
- Хаманн Дж., Фибиг Х., Штраус М (июнь 1993 г.). «Экспрессионное клонирование антигена ранней активации CD69, интегрального мембранного белка типа II с лектиновым доменом С-типа». Журнал иммунологии. 150 (11): 4920–7. PMID 8496594.
- Krowka JF, Cuevas B, Maron DC, Steimer KS, Ascher MS, Sheppard HW (январь 1996). «Экспрессия CD69 после стимуляции in vitro: быстрый метод количественной оценки нарушенных лимфоцитарных ответов у ВИЧ-инфицированных». Журнал синдромов приобретенного иммунодефицита и ретровирологии человека. 11 (1): 95–104. Дои:10.1097/00042560-199601010-00013. PMID 8528739.
- Яфрат А.Дж., Бронсон С., Сковронски Дж. (Февраль 1997 г.). «Разделимые функции Nef нарушают два аспекта аппарата рецепторов Т-клеток: экспрессию CD4 и передачу сигналов CD3». Журнал EMBO. 16 (4): 673–84. Дои:10.1093 / emboj / 16.4.673. ЧВК 1169669. PMID 9049297.
- Вэнс Б.А., Беннетт М.Дж., Уорд Й., Гресс Р.Г., Кирс КП (август 1999 г.). «Отчетливое, но необязательное N-гликозилирование белков CD69 человека». Архивы биохимии и биофизики. 368 (2): 214–20. Дои:10.1006 / abbi.1999.1322. PMID 10441371.
- Бласкес М.В., Мачо А., Ортис С., Лусена С., Лопес-Кабрера М., Санчес-Мадрид Ф., Муньос Е. (сентябрь 1999 г.). «Внеклеточный белок Tat 1 ВИЧ типа 1 индуцирует экспрессию CD69 посредством активации NF-kappaB: возможная корреляция с Tat-связывающими белками клеточной поверхности». Исследования СПИДа и ретровирусы человека. 15 (13): 1209–18. Дои:10.1089/088922299310304. PMID 10480634.
- Llera AS, Viedma F, Sánchez-Madrid F, Tormo J (март 2001 г.). «Кристаллическая структура лектин-подобного домена С-типа из рецептора CD69 кроветворных клеток человека». Журнал биологической химии. 276 (10): 7312–9. Дои:10.1074 / jbc.M008573200. PMID 11036086.
- Натараджан К., Савицкий М.В., Маргулис Д.Х., Мариуцца, РА (декабрь 2000 г.). «Кристаллическая структура человеческого CD69: лектиноподобный маркер активации C-типа гемопоэтических клеток». Биохимия. 39 (48): 14779–86. Дои:10.1021 / bi0018180. PMID 11101293.
- Лю X, Schrager JA, Lange GD, Marsh JW (август 2001 г.). «Nef-опосредованные ВИЧ клеточные фенотипы по-разному выражаются в зависимости от внутриклеточных концентраций Nef». Журнал биологической химии. 276 (35): 32763–70. Дои:10.1074 / jbc.M101025200. PMID 11438519.
- Diament D, Brunialti MK, Romero EC, Kallas EG, Salomao R (апрель 2002 г.). «Активация мононуклеарных клеток периферической крови, индуцированная гликолипопротеином Leptospira interrogans». Инфекция и иммунитет. 70 (4): 1677–83. Дои:10.1128 / IAI.70.4.1677-1683.2002. ЧВК 127819. PMID 11895929.
- Йошимура К., Ямагути М., Иикура М., Изуми С., Кудо К., Нагасе Х., Исии А., Уоллс А.Ф., Ра С., Ивата Т., Игараси Т., Ямамото К., Хираи К. (май 2002 г.). «Маркеры активации базофилов человека: экспрессия CD69 сильно и предпочтительно индуцируется IL-3». Журнал аллергии и клинической иммунологии. 109 (5): 817–23. Дои:10.1067 / mai.2002.123532. PMID 11994706.
- Pisegna S, Zingoni A, Pirozzi G, Cinque B, Cifone MG, Morrone S, Piccoli M, Frati L, Palmieri G, Santoni A (июль 2002 г.). «Src-зависимая активация Syk контролирует CD69-опосредованную передачу сигналов и функцию NK-клеток человека». Журнал иммунологии. 169 (1): 68–74. Дои:10.4049 / jimmunol.169.1.68. PMID 12077230.
- Лю С.К., Хуан К.Дж., Лин Ю.С., Йе Т.М., Лю Х.С., Лей Х.Й. (октябрь 2002 г.). «Временная инверсия соотношения CD4 / CD8 и аберрантная иммунная активация во время заражения вирусом денге». Журнал медицинской вирусологии. 68 (2): 241–52. Дои:10.1002 / jmv.10198. PMID 12210415. S2CID 21271659.
- Ферстер М., Хефнер Д., Крегель С. (октябрь 2002 г.). «Bcl-2-опосредованная регуляция CD69-индуцированного апоптоза эозинофилов человека: идентификация и характеристика нового рецепторного механизма и взаимосвязи с передачей сигналов, трансдуцированной CD95». Скандинавский журнал иммунологии. 56 (4): 417–28. Дои:10.1046 / j.1365-3083.2002.01111.x. PMID 12234263. S2CID 21934164.
- Вайгель Г., Грисмахер А., Карими А., Цукерманн А.О., Гримм М., Мюллер М.М. (октябрь 2002 г.). «Влияние терапии микофенолятмофетилом на активацию лимфоцитов у реципиентов трансплантата сердца». Журнал трансплантации сердца и легких. 21 (10): 1074–9. Дои:10.1016 / S1053-2498 (02) 00440-0. PMID 12398872.
внешняя ссылка
- CD69 + белок, + человек в Национальной медицинской библиотеке США Рубрики медицинской тематики (MeSH)
- Человек CD69 расположение генома и CD69 страница сведений о генах в Браузер генома UCSC.