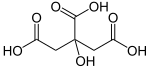
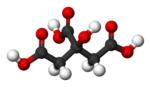
Лимонная кислота - Citric acid
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Лимонная кислота[1] | |||
| Систематическое название ИЮПАК 2-гидроксипропан-1,2,3-трикарбоновая кислота | |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.973 | ||
| Номер ЕС |
| ||
| Номер E | E330 (антиоксиданты, ...) | ||
| КЕГГ | |||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| |||
| |||
| Свойства | |||
| C6ЧАС8О7 | |||
| Молярная масса | 192.123 г / моль (безводный), 210,14 г / моль (моногидрат)[2] | ||
| Внешность | Кристаллическое белое твердое вещество | ||
| Запах | Без запаха | ||
| Плотность | 1.665 г / см3 (безводный) 1.542 г / см3 (18 ° C, моногидрат) | ||
| Температура плавления | 156 ° С (313 ° F, 429 К) | ||
| Точка кипения | 310 ° C (590 ° F, 583 K) разлагается от 175 ° C[3] | ||
| 54% ж / б (10 ° C) 59.2% ж / б (20 ° C) 64.3% ж / б (30 ° C) 68.6% ж / б (40 ° C) 70.9% ж / б (50 ° C) 73.5% ж / б (60 ° C) 76.2% ж / б (70 ° C) 78.8% ж / б (80 ° C) 81.4% ж / б (90 ° C) 84% ж / б (100 ° C)[4] | |||
| Растворимость | Растворим в ацетон, алкоголь, эфир, этилацетат, ДМСО Не растворим в C 6ЧАС 6, CHCl3, CS2, толуол[3] | ||
| Растворимость в этиловый спирт | 62 г / 100 г (25 ° C)[3] | ||
| Растворимость в амилацетат | 4.41 г / 100 г (25 ° C)[3] | ||
| Растворимость в диэтиловый эфир | 1.05 г / 100 г (25 ° C)[3] | ||
| Растворимость в 1,4-диоксан | 35.9 г / 100 г (25 ° C)[3] | ||
| журнал п | −1.64 | ||
| Кислотность (пKа) | пKа1 = 3.13[5] пKа2 = 4.76[5] пKа3 = 6.39,[6] 6.40[7] | ||
| 1.493–1.509 (20 ° C)[4] 1.46 (150 ° C)[3] | |||
| Вязкость | 6.5 сП (50% водн. соль)[4] | ||
| Структура | |||
| Моноклиника | |||
| Термохимия | |||
Теплоемкость (C) | 226.51 Дж / (моль · К) (26,85 ° C)[8] | ||
Стандартный моляр энтропия (S | 252.1 Дж / (моль · К)[8] | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | −1543.8 кДж / моль[4] | ||
| 1985,3 кДж / моль (474,5 ккал / моль, 2,47 ккал / г),[4] 1960.6 кДж / моль[8] 1972,34 кДж / моль (471,4 ккал / моль, 2,24 ккал / г) (моногидрат)[4] | |||
| Фармакология | |||
| A09AB04 (КТО) | |||
| Опасности | |||
| Основной опасности | Раздражитель кожи и глаз | ||
| Паспорт безопасности | HMDB | ||
| Пиктограммы GHS |  [5] [5] | ||
| Сигнальное слово GHS | Предупреждение | ||
| H319[5] | |||
| P305 + 351 + 338[5] | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 155 ° С (311 ° F, 428 К) | ||
| 345 ° С (653 ° F, 618 К) | |||
| Пределы взрываемости | 8%[5] | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 3000 мг / кг (крысы, перорально) | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
Лимонная кислота это слабый органическая кислота это имеет молекулярная формула C6ЧАС8О7. Это происходит естественно в цитрусовые. В биохимия, это промежуточное звено в цикл лимонной кислоты, что происходит в метаболизм из всех аэробные организмы.
Более двух миллионов тонн лимонной кислоты производятся каждый год. Он широко используется как подкислитель, как ароматизатор и хелатирующий агент.[9]
А цитрат производное лимонной кислоты; это соли, сложные эфиры, а многоатомный анион найдено в растворе. Пример первого: соль тринатрийцитрат; сложный эфир триэтилцитрат. Когда он входит в состав соли, формула цитрат-аниона записывается как C
6ЧАС
5О3−
7 или C
3ЧАС
5О (COO)3−
3.
Естественное происхождение и промышленное производство

Лимонная кислота содержится во многих фруктах и овощах, в первую очередь в цитрусовые. Лимоны и лаймы имеют особенно высокие концентрации кислоты; он может составлять до 8% от сухого веса этих фруктов (около 47г / л в соках[10]).[а] Концентрация лимонной кислоты в цитрусовых колеблется от 0,005Молл для апельсинов и грейпфрутов до 0,30 моль / л в лимонах и лаймах; эти значения варьируются в зависимости от вида в зависимости от сорт и обстоятельства, в которых был выращен плод.
Производство лимонной кислоты в промышленных масштабах началось в 1890 году на основе итальянского Цитрусовый фрукт промышленность, где сок обрабатывали гашеной известью (гидроксид кальция ) осадить цитрат кальция, который был выделен и преобразован обратно в кислоту с использованием разбавленных серная кислота.[11] В 1893 г. К. Вехмер обнаружил Пенициллий форма может производить лимонную кислоту из сахара. Однако производство лимонной кислоты с помощью микробов не имело промышленного значения до тех пор, пока Первая мировая война не нарушила экспорт итальянских цитрусовых.
В 1917 году американский пищевой химик Джеймс Карри обнаружил определенные штаммы плесени. Aspergillus niger могут быть эффективными производителями лимонной кислоты, а фармацевтическая компания Pfizer начал промышленное производство с использованием этой технологии два года спустя, а затем Citrique Belge в 1929 году. При этой технологии производства, которая до сих пор является основным промышленным способом получения лимонной кислоты, культуры А. нигер питаются сахароза или глюкоза -содержащая среда для получения лимонной кислоты. Источник сахара кукурузный крепкий ликер, патока, гидролизованная кукурузный крахмал, или другой недорогой сладкий раствор.[12] После того как плесень отфильтрована из полученного раствора, лимонная кислота выделяется осаждение его с гидроксидом кальция, чтобы получить соль цитрата кальция, из которой лимонную кислоту регенерируют обработкой серной кислотой, как при прямой экстракции из сока цитрусовых.
В 1977 г. был получен патент Lever Brothers для химического синтеза лимонной кислоты из аконитовой или изоцитрат / аллоизоцитратной солей кальция в условиях высокого давления; это давало лимонную кислоту с почти количественной конверсией при том, что казалось обратным, неферментативным. Реакция цикла Кребса.[13]
В 2018 году мировое производство превысило 2000000 тонн.[14] Более 50% этого объема произведено в Китае. Более 50% было использовано в качестве регулятор кислотности в напитках, около 20% - в других пищевых продуктах, 20% - в моющих средствах и 10% - в приложениях, отличных от пищевых, таких как косметика, фармацевтика и химическая промышленность.[нужна цитата ]
Химические характеристики


Лимонная кислота была впервые выделена в 1784 году химиком. Карл Вильгельм Шееле, который кристаллизовал его из лимонного сока.[15][11][16]Он может существовать либо в безводный (безводная) форма или как моногидрат. Безводная форма кристаллизируется из горячей воды, а моногидрат образуется при кристаллизации лимонной кислоты из холодной воды. Моногидрат можно превратить в безводную форму примерно при 78 ° C. Лимонная кислота также растворяется в абсолютном (безводном) этиловый спирт (76 частей лимонной кислоты на 100 частей этанола) при 15 ° C. Это разлагается с потерей углекислого газа выше примерно 175 ° C.
Лимонная кислота обычно считается трехосновной кислотой с pKа значения, экстраполированные на нулевую ионную силу, 2,92, 4,28 и 5,21 при 25 ° C.[17] ПКа гидроксильной группы было обнаружено с помощью 13Спектроскопия ЯМР 13С, равная 14,4.[18] Диаграмма видового состава показывает, что растворы лимонной кислоты буферные растворы между pH 2 и pH 8. В биологических системах с pH 7 присутствуют два вида - это цитрат-ион и моноводородцитрат-ион. В Буфер для гибридизации SSC 20X является примером общего использования.[19] Таблицы составлены для биохимических исследований[20] доступны.
С другой стороны, pH 1 мМ раствора лимонной кислоты будет около 3,2. PH фруктовых соков из цитрусовые например, апельсины и лимоны, зависит от концентрации лимонной кислоты, которая ниже при более высокой концентрации кислоты и наоборот.
Кислотные соли лимонной кислоты можно получить путем тщательного регулирования pH перед кристаллизацией соединения. См., Например, цитрат натрия.
Цитрат-ион образует комплексы с катионами металлов. В константы устойчивости для образования этих комплексов довольно большие из-за хелатный эффект. Следовательно, он образует комплексы даже с катионами щелочных металлов. Однако, когда хелатный комплекс образуется с использованием всех трех карбоксилатных групп, хелатные кольца имеют 7 и 8 членов, которые обычно менее стабильны термодинамически, чем хелатные кольца меньшего размера. Следовательно, гидроксильная группа может быть депротонирована, образуя часть более стабильного 5-членного кольца, как в цитрат железа (аммония), (NH
4)
5Fe (C
6ЧАС
4О
7)
2·2ЧАС
2О.[21]
Лимонная кислота может быть этерифицированный на одном или нескольких из карбоновая кислота функциональные группы в молекуле (с использованием различных спиртов) с образованием любого из множества моно-, ди-, три- и смешанных сложных эфиров.[нужна цитата ]
Биохимия
Цикл лимонной кислоты
Цитрат является промежуточным звеном в Цикл TCA (он же ТриCарбоновый Ацикл cid, или цикл Кребса, Сент-Дьёрдьи ), центральный метаболический путь для животных, растений и бактерий. Цитрат-синтаза катализирует конденсацию оксалоацетат с ацетил-КоА с образованием цитрата. Цитрат затем действует как субстрат для аконитаза и преобразуется в аконитовая кислота. Цикл завершается регенерацией оксалоацетата. Эта серия химических реакций является источником двух третей энергии, получаемой с пищей, у высших организмов. Ганс Адольф Кребс получил 1953 г. Нобелевская премия по физиологии и медицине за открытие.
Некоторые бактерии (особенно Кишечная палочка ) могут производить и потреблять цитрат внутри себя как часть своего цикла TCA, но не могут использовать его в качестве пищи, потому что им не хватает ферментов, необходимых для импорта его в клетку. После десятков тысяч эволюций в среде с минимальным содержанием глюкозы, которая также содержала цитрат во время Ричард Ленски с Долгосрочный эволюционный эксперимент, вариант Кишечная палочка развился благодаря способности расти в аэробных условиях на цитрате. Захари Блаунт, ученица Ленского и его коллеги изучали эти "Cit+" Кишечная палочка[22][23] как модель эволюции новых черт. Они обнаружили доказательства того, что в данном случае нововведение было вызвано редкой дупликационной мутацией из-за накопления нескольких предшествующих «потенцирующих» мутаций, идентичность и эффекты которых все еще изучаются. Эволюция Cit+ эта черта считается ярким примером роли исторической случайности в эволюции.
Другие биологические роли
Цитрат можно транспортировать из митохондрии и в цитоплазму, затем распадается на ацетил-КоА для синтез жирных кислот, и в оксалоацетат. Цитрат является положительным модулятором этого превращения и аллостерически регулирует фермент. ацетил-КоА карбоксилаза, который является ферментом, регулирующим превращение ацетил-КоА в малонил-КоА (этап обязательства в синтезе жирных кислот). Короче говоря, цитрат транспортируется в цитоплазму, превращается в ацетил-КоА, который затем превращается в малонил-КоА под действием ацетил-КоА-карбоксилазы, которая аллостерически модулируется цитратом.
Высокие концентрации цитозольного цитрата могут подавлять фосфофруктокиназа, катализатор лимитирующей стадии гликолиз. Этот эффект является преимуществом: высокие концентрации цитрата указывают на то, что существует большой запас молекул-предшественников биосинтеза, поэтому фосфофруктокиназа не должна продолжать отправлять молекулы своего субстрата, фруктозо-6-фосфат, в гликолиз. Цитрат действует, усиливая ингибирующий эффект высоких концентраций АТФ, еще один признак того, что нет необходимости проводить гликолиз.[24]
Цитрат - жизненно важный компонент костей, помогающий регулировать размер апатит кристаллы.[25]
Приложения
Еда и напитки

Поскольку это одна из наиболее сильных пищевых кислот, лимонная кислота используется в основном в качестве ароматизатора и консерванта в продуктах питания и напитках, особенно в безалкогольных напитках и конфетах.[11] В рамках Европейский Союз это обозначается Номер E E330. Цитратные соли различных металлов используются для доставки этих минералов в биологически доступной форме во многих пищевые добавки. Лимонная кислота имеет 247 ккал на 100 г.[26] В США требования к чистоте лимонной кислоты в качестве пищевой добавки определены Кодекс пищевых химикатов, который публикуется Фармакопея США (USP).
Лимонную кислоту можно добавлять в мороженое в качестве эмульгатора, чтобы жиры не расслаивались, в карамель, чтобы предотвратить кристаллизацию сахарозы, или в рецепты вместо свежего лимонного сока. Лимонная кислота используется с бикарбонат натрия в широком диапазоне шипучий формулы, как для приема внутрь (например, порошки и таблетки), так и для личной гигиены (например, соли для ванн, бомбы для ванн, и очистка смазывать ). Лимонная кислота, продаваемая в виде сухого порошка, обычно продается на рынках и в продуктовых магазинах как «кислая соль» из-за ее физического сходства с поваренной солью. Он используется в кулинарии как альтернатива уксусу или лимонному соку, где необходима чистая кислота. Лимонная кислота может использоваться в пищевой краситель чтобы сбалансировать уровень pH обычно основного красителя.[нужна цитата ]
Чистящее и хелатирующее средство
Лимонная кислота - отличный хелатирующий агент, связывая металлы, делая их растворимыми. Он используется для удаления и предотвращения накопления известковый налет от котлов и испарителей.[11] Его можно использовать для очистки воды, что делает его полезным для повышения эффективности мыла и моющих средств для стирки. Хелатируя металлы в жесткая вода, это позволяет этим чистящим средствам образовывать пену и лучше работать без необходимости смягчения воды. Лимонная кислота является активным ингредиентом некоторых моющих средств для ванной и кухни. Раствор с шестипроцентной концентрацией лимонной кислоты удалит пятна от жесткой воды со стекла, не протирая его. Лимонную кислоту можно использовать в шампуне для смывания воска и красителей с волос. Лимонная кислота, демонстрирующая ее хелатирующие способности, была первой успешной элюент используется для полного ионообменного разделения лантаноиды, в течение Манхэттенский проект в 1940-е гг. В 1950-х годах его заменили на гораздо более эффективные EDTA.
В промышленности он используется для растворения ржавчины со стали и пассивировать нержавеющая сталь.[27]
Косметика, фармацевтика, диетические добавки и продукты питания
Лимонная кислота используется как подкислитель в кремах, гелях и жидкостях. Используемый в пищевых продуктах и диетических добавках, он может быть классифицирован как технологическая добавка, если он был добавлен для технического или функционального эффекта (например, подкислитель, хелатор, загуститель и т. Д.). Если он по-прежнему присутствует в незначительных количествах, а технический или функциональный эффект больше не присутствует, он может быть освобожден от маркировки <21 CFR §101.100 (c)>.
Лимонная кислота - это альфа-гидроксикислота и является активным ингредиентом химического пилинга кожи.[нужна цитата ]
Лимонная кислота обычно используется в качестве буфера для увеличения растворимости коричневого. героин.[28]
Лимонная кислота используется в качестве одного из активных ингредиентов в производстве тканей для лица с противовирусными свойствами.[29]
Другое использование
В буферизация свойства цитратов используются для контроля pH в бытовых чистящих средствах и фармацевтические препараты.
Лимонная кислота используется как альтернатива белому уксусу без запаха при окрашивании в домашних условиях кислотные красители.
Цитрат натрия входит в состав Реагент Бенедикта, используется для качественной и количественной идентификации редуцирующих сахаров.
Лимонная кислота может использоваться как альтернатива азотной кислоте в пассивация из нержавеющая сталь.[30]
Лимонная кислота может использоваться как средство с меньшим запахом. остановить ванну как часть процесса разработки фотопленка. Фотографические разработчики являются щелочными, поэтому для нейтрализации и быстрого прекращения их действия используется мягкая кислота, но обычно используемая уксусная кислота оставляет в темной комнате сильный запах уксуса.[31]
Лимонная кислота / цитрат калия-натрия может использоваться как регулятор кислоты в крови.
Пайка поток. Лимонная кислота - отличный паяльный флюс,[32] либо в сухом виде, либо в виде концентрированного раствора в воде. Его следует удалить после пайки, особенно с тонких проводов, так как он имеет умеренную коррозию. Он быстро растворяется и смывается горячей водой.
Синтез твердых материалов из малых молекул
В материаловедении метод цитрат-геля - это процесс, аналогичный золь-гель метод, который представляет собой способ производства твердых материалов из небольших молекул. В процессе синтеза соли или алкоксиды металлов вводятся в раствор лимонной кислоты. Считается, что образование лимонных комплексов уравновешивает разницу в индивидуальном поведении ионов в растворе, что приводит к лучшему распределению ионов и предотвращает разделение компонентов на более поздних стадиях процесса. Поликонденсация этиленгликоля и лимонной кислоты начинается выше 100 ° С, что приводит к образованию геля цитрата полимера.
Безопасность
Хотя это и слабая кислота, воздействие чистой лимонной кислоты может вызвать побочные эффекты. Вдыхание может вызвать кашель, одышку или боль в горле. Передозировка может вызвать боль в животе и горло. Воздействие концентрированных растворов на кожу и глаза может вызвать покраснение и боль.[33] Длительное или повторяющееся употребление может вызвать эрозию зубной эмали.[33][34][35]
Компендиальный статус
Смотрите также
- Близкородственные кислоты изоазимонная кислота, аконитовая кислота, и пропан-1,2,3-трикарбоновая кислота (трикарбаллиловая кислота, карбаллиловая кислота)
- Кислоты в вине
использованная литература
- ^ ChemSpider перечисляет «лимонную кислоту» как подтвержденное экспертами название ИЮПАК.
- ^ CID 22230 от PubChem
- ^ а б c d е ж г "лимонная кислота". chemister.ru. Архивировано из оригинал 29 ноября 2014 г.. Получено 1 июня, 2014.
- ^ а б c d е ж CID 311 от PubChem
- ^ а б c d е ж Fisher Scientific, Лимонная кислота. Проверено 2 июня 2014.
- ^ «Данные для биохимических исследований». ZirChrom Separations, Inc. Получено 11 января, 2012.
- ^ «Константы ионизации органических кислот». Университет штата Мичиган. Получено 11 января, 2012.
- ^ а б c Лимонная кислота в Linstrom, Peter J .; Маллард, Уильям Г. (ред.); Веб-книга NIST Chemistry, стандартная справочная база данных NIST номер 69, Национальный институт стандартов и технологий, Гейтерсбург (Мэриленд), http://webbook.nist.gov (Дата обращения 2 июня 2014)
- ^ Аплеблат, Александр (2014). Лимонная кислота. Springer. ISBN 978-3-319-11232-9.
- ^ Пеннистон К.Л., Накада С.Ю., Холмс Р.П., Ассимос Д.Г. (2008). «Количественная оценка лимонной кислоты в лимонном соке, соке лайма и имеющихся в продаже фруктовых соках». Журнал эндоурологии. 22 (3): 567–570. Дои:10.1089 / конец.2007.0304. ЧВК 2637791. PMID 18290732.
- ^ а б c d Франк Х. Верхофф. "Лимонная кислота". Энциклопедия промышленной химии Ульмана. Вайнхайм: Wiley-VCH.
- ^ Lotfy, Walid A .; Ghanem, Khaled M .; Эль-Хелоу, Эхаб Р. (2007). "Производство лимонной кислоты по роману" Aspergillus niger изолировать: II. Оптимизация параметров процесса с помощью статистических экспериментальных планов ". Биоресурсные технологии. 98 (18): 3470–3477. Дои:10.1016 / j.biortech.2006.11.032. PMID 17317159.
- ^ US 4056567-В. Ламберти и Э. Гутьеррес
- ^ «Отчет о мировых рынках лимонной кислоты, 2011–2018 и 2019–2024 годы». prnewswire.com. 19 марта 2019 г.,. Получено 28 октября, 2019.
- ^ Шееле, Карл Вильгельм (1784). "Anmärkning om Citron-saft, samt sätt at crystalisera densamma" [Примечание о лимонном соке и способах его кристаллизации]. Kungliga Vetenskaps Academiens Nya Handlingar [Новые материалы Королевской академии наук]. 2-я серия (на шведском языке). 5: 105–109.
- ^ Грэм, Томас (1842). Элементы химии, включая приложения науки в искусстве. Ипполит Байер, иностранный продавец книг Королевского колледжа хирургов и Королевского общества, 219, Риджент-стрит. п.944. Получено 4 июня, 2010.
- ^ Голдберг, Роберт Н .; Кишор, Нанд; Леннен, Ребекка М. (2002). «Термодинамические величины для реакций ионизации буферов». J. Phys. Chem. Ref. Данные. 31 (1): 231–370. Bibcode:2002JPCRD..31..231G. Дои:10.1063/1.1416902. S2CID 94614267.
- ^ Сильва, Андре М. Н .; Конг, Сяоле; Гитлер, Роберт С. (2009). «Определение значения pKa гидроксильной группы в цитрате, малате и лактате α-гидроксикарбоксилатов с помощью 13C ЯМР: значение для координации металлов в биологических системах ». Биометаллы. 22 (5): 771–778. Дои:10.1007 / s10534-009-9224-5. PMID 19288211. S2CID 11615864.
- ^ Maniatis, T .; Fritsch, E. F .; Sambrook, J. 1982. Молекулярное клонирование: лабораторное руководство. Лаборатория Колд-Спринг-Харбор, Колд-Спринг-Харбор, Нью-Йорк.
- ^ Гомори, Г. (1955). «16 Подготовка буферов для использования в исследованиях ферментов». Методы в энзимологии Том 1. Методы в энзимологии. 1. стр.138–146. Дои:10.1016/0076-6879(55)01020-3. ISBN 9780121818012.
- ^ Matzapetakis, M .; Raptopoulou, C.P .; Tsohos, A .; Papaefthymiou, V .; Moon, S. N .; Салифоглу А. (1998). «Синтез, спектроскопические и структурные характеристики первого одноядерного водорастворимого комплекса железо-цитрат, (NH4)5Fe (C6ЧАС4О7)2· 2H2О ". Варенье. Chem. Soc. 120 (50): 13266–13267. Дои:10.1021 / ja9807035.
- ^ Пауэлл, Элвин (14 февраля 2014 г.). «59 000 поколений бактерий плюс морозильная камера дают потрясающие результаты». Phys.org. Получено 13 апреля, 2017.
- ^ Blount, Z. D .; Borland, C. Z .; Ленский, Р. Э. (4 июня 2008 г.). «Историческая случайность и эволюция ключевого нововведения в экспериментальной популяции Escherichia coli» (PDF). Труды Национальной академии наук. 105 (23): 7899–7906. Bibcode:2008PNAS..105.7899B. Дои:10.1073 / pnas.0803151105. ЧВК 2430337. PMID 18524956. Архивировано из оригинал (PDF) 21 октября 2016 г.. Получено 13 апреля, 2017.
- ^ Страйер, Люберт; Берг, Джереми; Тимочко, Джон (2003). «Раздел 16.2: Путь гликолиза строго контролируется». Биохимия (5. изд., Международное изд., 3. полиграфическое изд.). Нью-Йорк: Фриман. ISBN 978-0716746843.
- ^ Hu, Y.-Y .; Rawal, A .; Шмидт-Рор, К. (декабрь 2010 г.). «Прочно связанный цитрат стабилизирует нанокристаллы апатита в кости». Труды Национальной академии наук. 107 (52): 22425–22429. Bibcode:2010PNAS..10722425H. Дои:10.1073 / pnas.1009219107. ЧВК 3012505. PMID 21127269.
- ^ Гринфилд, Хизер; Саутгейт, D.A.T. (2003). Данные о составе пищевых продуктов: производство, управление и использование. Рим: ФАО. п. 146. ISBN 9789251049495.
- ^ https://www.astm.org/Standards/A967.htm
- ^ Strang J, Keaney F, Butterworth G, Noble A, Best D (апрель 2001 г.). «Различные формы героина и их связь с методами приготовления пищи: данные и объяснение употребления лимонного сока и других кислот». Неправильное использование субстанций. 36 (5): 573–88. Дои:10.1081 / ja-100103561. PMID 11419488. S2CID 8516420.
- ^ «Ткани, борющиеся с микробами». CNN. 14 июля 2004 г.. Получено 8 мая, 2008.
- ^ «Травление и пассивирование нержавеющей стали» (PDF). Euro-inox.org. Архивировано из оригинал (PDF) 12 сентября 2012 г.. Получено 2013-01-01.
- ^ Анчелл, Стив. "Поваренная книга темной комнаты: 3-е издание (мягкая обложка)". Focal Press. Получено 1 января, 2013.
- ^ "Исследование химии лимонной кислоты в военных паяльных устройствах" (PDF). 19 июня 1995 г.
- ^ а б "Лимонная кислота". Международные карты химической безопасности. NIOSH. 18 сентября 2018 г. Архивировано с оригинал 12 июля 2018 г.. Получено 9 сентября, 2017.
- ^ Дж. Чжэн; Ф. Сяо; Л. М. Цянь; З. Р. Чжоу (декабрь 2009 г.). «Эрозионное поведение эмали человеческого зуба в растворе лимонной кислоты». Tribology International. 42 (11–12): 1558–1564. Дои:10.1016 / j.triboint.2008.12.008.
- ^ «Влияние лимонной кислоты на зубную эмаль».
- ^ Секретариат Британской фармакопейной комиссии (2009 г.). «Индекс, BP 2009» (PDF). Архивировано из оригинал (PDF) 11 апреля 2009 г.. Получено 4 февраля, 2010.
- ^ «Японская фармакопея, пятнадцатое издание» (PDF). 2006. Архивировано с оригинал (PDF) 22 июля 2011 г.. Получено 4 февраля 2010.
- ^ Это не делает лимон особенно кислым. Это связано с тем, что в качестве слабой кислоты большинство молекул кислоты не диссоциировано, поэтому не способствует повышению кислотности внутри лимона или его сока.