Артемизинин - Artemisinin
 | |
 | |
| Клинические данные | |
|---|---|
| Произношение | /ɑːrтɪˈмɪsɪпɪп/ |
| Другие имена | Артемизинин, цинхаосу |
| Маршруты администрация | Устный |
| Код УВД | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.110.458 |
| Химические и физические данные | |
| Формула | C15ЧАС22О5 |
| Молярная масса | 282.336 г · моль−1 |
| 3D модель (JSmol ) | |
| Плотность | 1,24 ± 0,1 г / см3 |
| Температура плавления | От 152 до 157 ° C (от 306 до 315 ° F) |
| Точка кипения | разлагается |
| |
| |
| | |
Артемизинин (/ˌɑːтɪˈмяsɪпɪп/) и это полусинтетический производные группа наркотики используется против малярия из-за Плазмодий falciparum.[1] Он был открыт в 1972 г. Ту Youyou, который был сореципиентом 2015 г. Нобелевская премия по медицине за ее открытие.[2] Процедуры, содержащие производное артемизинина (артемизинин-комбинированная терапия, АКТ) в настоящее время являются стандартным лечением во всем мире P. falciparum малярия, а также малярия, вызванная другими видами Плазмодий.[3] Артемизинин выделяется из растения Полынь однолетняя, сладкая полынь, трава, используемая в Китайская традиционная медицина. Соединение-предшественник можно получить с использованием генно-инженерный дрожжи, что намного эффективнее, чем использование растения.[4]
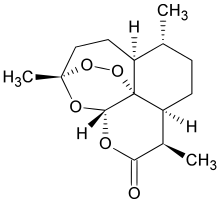
Химически артемизинин представляет собой сесквитерпеновый лактон содержащий необычный перекись мост. Этот эндопероксид 1,2,4-триоксан кольцо отвечает за механизм действия препарата. Известно немного других природных соединений с таким перекисным мостиком.[5]
Артемизинин и его производные использовались для лечения малярии и паразитарный червь (гельминт) инфекции. У них есть преимущество перед другими лекарствами в том, что они способны убивать быстрее и убивать паразитов на всех стадиях жизненного цикла.[6] Но низкий биодоступность, бедные фармакокинетический Свойства и дороговизна препаратов - главные недостатки их применения.[7] Использование самого препарата в качестве монотерапия явно не одобряется Всемирная организация здоровья,[8] поскольку появились признаки того, что малярийные паразиты развиваются сопротивление к препарату. Терапия, сочетающая артемизинин или его производные с некоторыми другими противомалярийными препаратами, является предпочтительным лечением от малярии.[9]
Медицинское использование
Неосложненная малярия
Артемизинины можно использовать отдельно, но это приводит к высокому уровню обострение (возвращение паразитов) и другие препараты необходимы для очистки организма от всех паразитов и предотвращения рецидива. В Всемирная организация здоровья (ВОЗ) оказывает давление на производителей с тем, чтобы они прекратили предоставление несоставных лекарств медицинскому сообществу в целом, осознавая катастрофу, которая может произойти, если малярийный паразит разовьет устойчивость к артемизининам.[10]
ВОЗ рекомендовала комбинированная терапия с артемизинином (ACT) быть терапией первой линии для P. falciparum малярия во всем мире.[11] В качестве препаратов короткого действия соединения артемизинина назначают с одним или двумя препаратами длительного действия, такими как амодиахин, мефлохин, сульфадоксин / пириметамин или люмефантрин.[6] Комбинации эффективны, потому что компонент артемизинина убивает большинство паразитов в начале лечения, в то время как более медленно удаляемое лекарственное средство-партнер устраняет оставшихся паразитов.[12]
В настоящее время доступно несколько фиксированных доз АКТ, содержащих компонент артемизинин и лекарственный препарат-партнер, имеющий длительный период полураспада, Такие как мефлохин (ASMQ),[13] люмефантрин (Coartem ), амодиахин (ASAQ ), пиперахин (Дуо-Котекксин) и пиронаридин (Пирамакс). Все чаще эти комбинации используются для GMP стандарт. Отдельный вопрос касается качества некоторых продуктов, содержащих артемизинин, которые продаются в Африке и Юго-Восточной Азии.[14][15]
Артемизинины не используются для профилактики малярии из-за чрезвычайно короткой активности (период полураспада ) препарата. Чтобы он был эффективным, его нужно вводить несколько раз в день.
Тяжелая малярия
Артесунат управляется внутривенный или же внутримышечный инъекция оказалась лучше хинин в крупных рандомизированных контролируемых исследованиях у обоих взрослых[16] и дети.[17] В совокупности всех исследований, в которых сравнивались эти два препарата, уровень смертности артесуната примерно на 30% ниже, чем у хинина.[17] Причины этой разницы включают снижение заболеваемости гипогликемия, более легкое введение и более быстрые действия против циркулирующих и секвестрированных паразитов. В настоящее время ВОЗ рекомендует артесунат для лечения всех тяжелых форм малярии. Доказано, что эффективное лечение АКТ (комбинированная терапия артемизинином) снижает заболеваемость и смертность от малярии в течение двух лет примерно на 70%.[18]
Гельминтоз
Случайное открытие было сделано в Китае в начале 1980-х годов во время поиска романа. глистогонные средства за шистосомоз что артемизинин был эффективен против шистосомы,[19][20][21] человеческая кровь двуустки, которые являются вторыми по распространенности паразитарными инфекциями после малярии. Артемизинин и его производные являются сильнодействующими глистогонными средствами.[22] Позже было обнаружено, что артемизинины обладают широким спектром активности против широкого спектра трематоды, включая Schistosoma japonicum, S. mansoni, С. haematobium, Clonorchis sinensis, Фасциола гепатика, и Описторхис виверрини. Клинические испытания также были успешно проведены в Африке среди пациентов с шистосомозом.[23]
Рак
Артемизинин и его производные проходят лабораторные исследования на предмет их потенциального противоракового действия.[24] По состоянию на 2018 год только предварительные клинические исследования были проведены с использованием производных артемизининина при различных раковых заболеваниях, без утвержденных клинических применений.[25]
Аутоиммунное заболевание
Производные артемизинина известны своей способностью подавлять иммунные реакции, такие как воспаление. Один производный инструмент, SM934, был одобрен в 2015 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов Китая для клинических испытаний как препарат для системная красная волчанка.[26] Эксперименты на животных моделях дали хорошие результаты. Он может регулировать субпопуляции Т-клеток, ингибировать активацию В-клеток, блокировать выработку воспалительных цитокинов и путь передачи сигнала NF-κB.[27]
Побочные эффекты
Артемизинины обычно хорошо переносятся в дозах, используемых для лечения малярии.[28] Побочные эффекты от препаратов класса артемизинина аналогичны симптомам малярии: тошнота, рвота, потеря аппетита, и головокружение. Также были отмечены легкие отклонения от нормы крови. Редкий, но серьезный побочный эффект: аллергическая реакция.[28][29] Один случай значительного воспаление печени сообщалось в связи с длительным применением относительно высоких доз артемизинина по неясной причине (у пациента не было малярии).[30] Лекарства, используемые в комбинированной терапии, могут способствовать возникновению побочных эффектов у тех, кто проходит лечение. Побочные эффекты у пациентов с острым P. falciparum малярия, леченная производными артемизинина, как правило, выше.[31]
Химия
Необычным компонентом молекул артемизинина является 1,2,4-триоксановое кольцо эндопероксида. Это главный противомалярийный центр молекулы.[32] Модификации в положении углерода 10 (C10) приводят к появлению множества производных, которые более мощны, чем исходное соединение.[33] Поскольку физические свойства самого артемизинина, такие как низкая биодоступность, ограничивают его эффективность, полусинтетический производные артемизинина. Производные дигидроартемизинина производятся с 1976 года. В 1986 году были синтезированы артесунат, артэтер и артеметер. Было произведено множество производных, из которых артелиновая кислота, артемотил, артемизон, SM735, SM905, SM933, SM934 и SM1044 являются одними из самых мощных соединений.[34][35] Также существуют упрощенные аналоги в доклинических исследованиях.[36] Было подготовлено более 120 других производных инструментов, но клиническое тестирование оказалось невозможным из-за отсутствия финансовой поддержки.[32]
Артемизинин относится к классу сесквитерпеновых лактонов. Твердое вещество плохо растворяется в маслах и воде. Поэтому его чаще всего вводят через пищеварительный тракт, перорально или ректально. Некоторые химические модификации подходят для инъекций. Артесунат - единственное соединение артемизинина, доступное для всех типов процедур введения.[37] Синтетическое соединение с аналогичной структурой триоксолана (кольцо, содержащее три атома кислорода), названное RBx-11160[38] показал обещание в in vitro тестирование. Тестирование фазы II у пациентов с малярией было не таким успешным, как ожидалось, но производитель все равно решил начать тестирование фазы III.[39]
Механизм действия
По состоянию на 2018 год точный механизм действия артемизининов полностью не выяснен.[40] Артемизинин сам по себе пролекарство биологически активных дигидроартемизинин. Этот метаболит подвергается расщеплению эндопероксид кольцо внутри эритроциты. Когда молекулы лекарства вступают в контакт с гем (связанный с гемоглобин красных кровяных телец), оксид железа (II) разрывает эндопероксидное кольцо.[41] Этот процесс производит свободные радикалы это, в свою очередь, повреждает восприимчивые белки, что приводит к гибели паразита.[42][43] В 2016 году было показано, что артемизинин связывается с большим количеством мишеней, что позволяет предположить, что он действует беспорядочно. Однако эндопероксидный фрагмент артемизинина менее чувствителен к свободному оксиду железа (II) и, следовательно, более активен на внутриэритроцитарных стадиях Плазмодий falciparum.[44] Напротив, клиническая практика показывает, что в отличие от других противомалярийных средств артемизинин активен на всех стадиях жизненного цикла паразита.[45]
Сопротивление
Клинические данные для артемизинина устойчивость к лекарству в Юго-Восточной Азии впервые было сообщено в 2008 году,[46] и впоследствии было подтверждено подробным исследованием западных Камбоджа.[47][48] Сопротивление в соседних Таиланд было сообщено в 2012 году,[49] и в северной Камбодже, Вьетнам и восточный Мьянма в 2014.[50][51] Сообщалось о появлении сопротивления в южных Лаос, центральная Мьянма и северо-восточная Камбоджа в 2014 году.[50][51] Паразита кельч ген на хромосоме 13, по-видимому, является надежным молекулярным маркером клинической устойчивости в Юго-Восточной Азии.[52]
В апреле 2011 г. ВОЗ заявили, что устойчивость к самому эффективному противомалярийному препарату, артемизинину, может подорвать национальные программы борьбы с малярией в Индии, которые достигли значительного прогресса за последнее десятилетие. ВОЗ выступает за рациональное использование противомалярийных препаратов и признает решающую роль местных медицинских работников в сокращении заболеваемости малярией в регионе.[53]
Два основных механизма сопротивления движению Плазмодий устойчивость к противомалярийным препаратам. Первый - это утечка препарата из места его действия из-за мутаций в различных генах-переносчиках (например, pfcrt в хлорохин резистентность) или увеличенное количество копий гена (например, количество копий pfmdr1 в мефлохин сопротивление). Второй - изменение паразита-мишени из-за мутаций в соответствующих генах (например, на уровне цитозоля, dhfr и dhps в сульфадоксин -пириметамин резистентность или, на уровне митохондрий, цитохром b в атоваквон сопротивление). Сопротивление Плазмодий falciparum к новым соединениям артемизинина включает новый механизм, соответствующий феномену покоя.[54]
Синтез
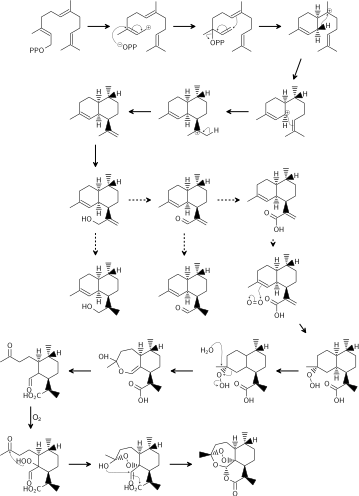
Биосинтез в A. annua
Считается, что в биосинтез артемизинина вовлечены мевалонатный путь (MVA) и циклизация фарнезил дифосфат (СвДП). Неясно, действительно ли немевалонатный путь также могут вносить 5-углеродные предшественники (IPP или же DMAPP ), как и в других биосинтетических системах сесквитерпена. Пути от артемизинового спирта к артемизинину остаются противоречивыми, и они различаются, главным образом, тем, когда происходит стадия восстановления. Оба пути предполагали, что дигидроартемизиновая кислота является конечным предшественником артемизинина. Затем дигидроартемизиновая кислота подвергается фотоокислению с образованием гидропероксида дигидроартемизиновой кислоты. Расширение цикла за счет расщепления гидропероксида и второго опосредованного кислородом гидропероксидации завершают биосинтез артемизинина.
Химический синтез
Полный синтез артемизинина был выполнен из доступных органических исходных материалов с использованием основных органических реагентов много раз. Первые два полных синтеза были «замечательным ... стереоселективным синтезом» Шмида и Хофхайнца в Hoffmann-La Roche в Базеле, начиная с (-) -изопулегол (13 шагов, общий выход ~ 5%) и параллельный синтез Чжоу и его коллег из Шанхайского института органической химии из (р)-(+)-цитронеллаль (20 шагов, общий выход ~ 0,3%).[55] Ключевые шаги подхода Schmid-Hofheinz включали начальное стереоселективное гидроборирование / окисление Орлоффа для установления "внекольцевого" метил стереоцентра на пропеновой боковой цепи; два последовательных алкилирования, опосредованных литиевым реагентом, которые вводили все необходимые атомы углерода и вместе обладали высокой диастереоселективностью; и дальнейшие стадии восстановления, окисления и десилилирования, выполняемые на этом монокарбоциклическом промежуточном продукте, включая конечный синглетный кислород -использование фотооксигенация и ее реакция, который после кислотной обработки замыкал три оставшихся оксациклических кольца желаемого продукта, артемизинина, за одну стадию.[55][56][57](По сути, заключительная операция закрытия окислительного цикла в этих синтезах завершает три завершающих этапа биосинтеза, показанных выше.)
С первых дней до сегодняшнего дня продолжается исследование широкого спектра дальнейших маршрутов, включая маршруты полного синтеза из (р) - (+) - пулегон, изоментен,[55] и даже 2-циклогексен-1-он,[58] а также маршруты, которые лучше описать как частичные или полусинтезы из более обильного биосинтетического предшественника, артемизиновая кислота —В последнем случае, в том числе некоторые очень короткие и очень урожайные биомиметический синтез примеры (Рота и Актона, и Хейнса и др., 3 стадии, выход 30%), которые снова показывают химию синглетного кислорода и ена.[59][55][60][61]
Синтез в созданных организмах
Партнерство по разработке полусинтетического артемизинина проводилось программой PATH по разработке лекарств (через партнерство с OneWorld Health ) при финансировании Фонд Билла и Мелинды Гейтс. Проект начался в 2004 году, и первоначальные партнеры по проекту включали Калифорнийский университет в Беркли (который предоставил технологию, на которой был основан проект - процесс, который генетически изменял дрожжи для производства артемизиновой кислоты)[62] и Amyris (биотехнологическая фирма в Калифорнии, которая усовершенствовала процесс для обеспечения крупномасштабного производства и разработала масштабируемые процессы для передачи промышленному партнеру).
В 2006 году команда из Калифорнийского университета в Беркли сообщила, что они спроектировали Saccharomyces cerevisiae дрожжи для производства небольшого количества предшественника артемизиновой кислоты. Синтезированная артемизиновая кислота затем может быть транспортирована, очищена и химически преобразована в артемизинин, который, как они заявляют, будет стоить примерно 0,25 доллара США за дозу. В этом усилии синтетическая биология модифицированный мевалонатный путь был использован, и дрожжевые клетки были сконструированы для экспрессии фермента аморфадиен-синтаза и цитохром P450 монооксигеназа (CYP71AV1), как из A. annua. Трехступенчатое окисление аморфо-4,11-диен дает образовавшуюся артемизиновую кислоту.[63]
Метод Беркли был дополнен технологиями других организаций. Последняя успешная технология основана на изобретениях, лицензированных Калифорнийским университетом в Беркли и Канадским институтом биотехнологии растений Национального исследовательского совета (NRC).
Коммерческое производство полусинтетического артемизинина в настоящее время ведется на предприятии Sanofi в Гарессио, Италия. Этот второй источник артемизинина призван обеспечить более стабильный поток основных противомалярийных препаратов для тех, кто в них больше всего нуждается.[64] Производственная цель установлена на уровне 35 тонн на 2013 год. Ожидается, что в 2014 году он вырастет до 50–60 тонн в год, что обеспечит примерно одну треть мировой годовой потребности в артемизинине.
8 мая 2013 г. Программа преквалификации лекарственных средств ВОЗ объявила о приемлемости полусинтетического артемизинина для использования в производстве активных фармацевтических ингредиентов, представленных в ВОЗ для преквалификации или уже прошедших квалификацию ВОЗ.[65] Активный фармацевтический ингредиент (API) санофи, полученный из полусинтетического артемизинина (артесунат), также прошел предварительную квалификацию ВОЗ 8 мая 2013 г., что сделало его первым полусинтетическим производным артемизинина, прошедшим предварительную квалификацию.
В 2010 году команда из Университет Вагенингена сообщили, что они создали близкого родственника табака, Nicotiana benthamiana, который также может производить прекурсор артемизиновой кислоты.[66]
Производство и цена
Китай и Вьетнам обеспечивают 70%, а Восточная Африка 20% растительного сырья.[нужна цитата ] Саженцы выращивают в питомниках, а затем пересаживают на поля. Для достижения полного размера им требуется около 8 месяцев. Растения собирают, листья сушат и отправляют на объекты, где артемизинин экстрагируется с использованием растворителя, обычно гексан. Были предложены альтернативные методы экстракции.[67] Рыночная цена на артемизинин колебалась в широких пределах: АМЕРИКАНСКИЙ ДОЛЛАР$ 120 и 1200 долларов за килограмм с 2005 по 2008 год.[68]
Китайская компания Артефарм создали комбинацию артемизинина и пиперахин препарат продается как Artequick. В дополнение к клиническим исследованиям, проведенным в Китае и Юго-Восточной Азии, Artequick использовался в крупномасштабных усилиях по искоренению малярии в Коморские острова. Эти усилия, предпринятые в 2007, 2012 и 2013–2014 годах, привели к сокращению числа случаев малярии на Коморских Островах на 95–97%.[69]
После переговоров с ВОЗ, Новартис и Санофи-Авентис предоставлять препараты для АКТ по себестоимости на некоммерческой основе; однако эти лекарства по-прежнему дороже других средств лечения малярии.[70] Инъекция артесуната для лечения тяжелой малярии производится Guilin Pharmaceutical завод в Китае, продукция которого прошла предварительную квалификацию ВОЗ.[71] Урожайные сорта Полынь производятся Центром новой сельскохозяйственной продукции на Йоркский университет с использованием методов молекулярного разведения.[68]
Используя семена, предоставленные Action for Natural Medicine (ANAMED), Всемирный центр агролесоводства (ICRAF) разработала гибрид, получивший название A3, который может вырастать до 3 метров в высоту и производить в 20 раз больше артемизинина, чем дикие сорта. На северо-западе Мозамбик, ICRAF работает вместе с медицинской организацией, Médecins sans frontières, ANAMED и Министерством сельского хозяйства и развития сельских районов для обучения фермеров тому, как выращивать кусты из черенков, а также собирать урожай и сушить листья для приготовления чая из полыни. Тем не менее Всемирная организация здоровья (ВОЗ) не рекомендует использовать A. annua растительные материалы, включая чай, для профилактики и лечения малярии.[72]
В апреле 2013 г. Санофи объявила о запуске[64] производственного объекта в Garessio, Италия, для крупномасштабного производства антиплазмодийного препарата. Партнерство по созданию нового фармацевтического производственного процесса возглавило программу PATH по разработке лекарств (через сотрудничество с OneWorld Health ) при финансировании Фонд Билла и Мелинды Гейтс и основан на модифицированном процессе биосинтеза артемизиновой кислоты, первоначально разработанном Джей Кислинг на Калифорнийский университет в Беркли и оптимизирован Амирис. За реакцией следует фотохимический процесс создания синглетного кислорода для получения конечного продукта. Санофи рассчитывает произвести 25 тонн артемизинина в 2013 году, увеличив производство до 55–60 тонн в 2014 году. Цена за килограмм составит 350–400 долларов США, что примерно соответствует стоимости растительного источника.[73] Несмотря на опасения, что этот эквивалентный источник приведет к краху компаний, которые производят это вещество традиционным способом путем добычи A. annua биомассы, увеличение предложения этого препарата, вероятно, приведет к снижению цен и, следовательно, повысит доступность лечения АКТ. В августе 2014 года Санофи объявила о выпуске первой партии полусинтетического артемизинина. 1,7 миллиона доз артесуната амодиахина Винтропа (ASAQ Winthrop) компании Sanofi, комбинированного препарата с фиксированной дозой артемизинина, будут отправлены в полдюжины африканских стран в течение следующих нескольких месяцев.[74]
Систематический обзор четырех исследований, проведенных в Восточной Африке в 2016 году, пришел к выводу, что субсидирование комбинации на основе артемизинина (терапия АКТ) в частном секторе розничной торговли в сочетании с обучением и маркетингом привело к увеличению доступности АКТ в магазинах, увеличению использования АКТ у детей до пяти лет с лихорадкой. лет и сокращение использования более старых, менее эффективных противомалярийных средств среди детей в возрасте до пяти лет; основные исследования не определили, были ли дети малярии, и не выяснили, есть ли польза для здоровья.[75]
Метаболизм
В печени артемизинин превращается в различные неактивные метаболиты, такие как дезоксиартемизинин, дезоксидигидроартемизинин, кристалл 7 и 9,10-дигидродезоксиартемизинин. Метаболиты потеряли эндопероксидную группу и стали неэффективными. Реакция катализируется ферментом CYP2B6, а другой фермент CYP3A4 действует как вторичный катализатор. В отсутствие CYP2B6 CYP3A4 становится основным ферментом. Эти ферменты относятся к цитохром P450 группа присутствует в гладкой эндоплазматической сети. Производные артемизинина метаболизируются по-разному. Сначала они конвертируются в дигидроартемизинин (ДГК). Сама DHA представляет собой сильную противомалярийную молекулу и активна в кровообращении в течение двух-трех часов. Противомалярийное действие артесуната на самом деле осуществляется только через DHA. (Артемизинин, артетер, артеметер и т. Д. Являются непосредственно противомалярийными средствами.) Артесунат превращается в DHA в течение минуты после его всасывания. Около 90% общего количества DHA обычно связывается с плазмой крови.[33] В печени ферментная система цитохрома P450 (включая CYP2A6, CYP3A4 и CYP3A5) превращает DHA в неактивные метаболиты. Все метаболиты подвергаются глюкуронизация после чего они выводятся с мочой или фекалиями. UDP-глюкуронозилтрансферазы, в частности UGT1A9 и UGT2B7, отвечают за процесс. DHA также удаляется с желчью в виде второстепенных глюкуронидов, таких как тетрагидрофураноцетат. Из-за быстрого метаболизма артемизинины являются относительно безопасными препаратами.[6]
История
Этимология
Артемизинин - это противомалярийный лактон, полученный из Цинхао (青蒿, Полынь однолетняя или же сладкая полынь ). Лекарственная ценность этого растения известна китайцам не менее 2000 лет. В 1596 г. Ли Шичжэнь рекомендуемый чай из Цинхао специально для лечения симптомов малярии у его Компендиум Материа Медика. Название рода происходит от греческой богини Артемида и, более конкретно, мог быть назван в честь королевы Артемизия II Карии, ботаник и медицинский исследователь в четвертом веке до нашей эры.[76]
Открытие
Полынь однолетняя общий трава найдены во многих частях мира и использовались китайцами травники более 2000 лет занимается лечением малярии. Самая ранняя запись относится к 200 г. до н.э., в Пятьдесят два рецепта раскопанный из Mawangdui.[77] Его противомалярийный приложение было впервые описано в Чжоу Бейджи Фанг (Справочник рецептов на случай чрезвычайных ситуаций, Китайский : 肘 後備 急 方), отредактированный в середине IV века н.э. Ге Хонг; в этой книге было записано 43 метода лечения малярии.[78] Изображения оригинальных научных работ, в которых описывается история открытия, доступны в Интернете с 2006 года.[79]

В 1967 году в рамках секретной военной программы под кодовым названием "Проект 523" была создана программа исследований по отбору растений. Народно-освободительная армия найти адекватное лечение малярии; программа и ранняя клиническая работа были заказаны Мао Зедун по запросу Северный Вьетнам лидеров для оказания помощи своей пораженной малярией армии.[80] В ходе этого исследования в 1972 г. Ту Youyou обнаружил артемизинин в листьях Полынь однолетняя.[81]
Названный Цинхаосу (Китайский : 青蒿素; горит 'соединение зелено-голубой полыни'),[81][82] это был один из многих кандидатов, протестированных в качестве возможных методов лечения малярия китайскими учеными из списка почти 5000 традиционных Китайские лекарства.[нужна цитата ] Ту Youyou также обнаружил, что процесс низкотемпературной экстракции может быть использован для выделения эффективного противомалярийного вещества из растения. Ту говорит, что на нее повлиял традиционная китайская фитотерапия источник Справочник рецептов неотложной помощи написано в 340 г. Ге Хонг говоря, что эту траву нужно замочить в холодной воде.[83] Эта книга содержала полезную ссылку на эту траву: «Горстка Цинхао залить двумя литрами воды, отжать сок и все это выпить ».
Команда Ту впоследствии выделила полезный отрывок.[81] Результаты опубликованы в Китайский медицинский журнал в 1979 г.[81][84][5] Экстрагированное вещество, подвергшееся очистке, оказалось полезной отправной точкой для получения очищенного артемизинина.[81] В обзоре 2012 года сообщается, что терапии на основе артемизинина были наиболее эффективными лекарствами для лечения малярии в то время;[85] также сообщалось, что он избавлялся от малярийных паразитов из тел пациентов быстрее, чем другие лекарства. Помимо артемизинина, в рамках проекта 523 разработан ряд продуктов, которые можно использовать в сочетании с артемизинином, в том числе: люмефантрин, пиперахин, и пиронаридин.[81]
В конце 1990-х гг. Новартис подала новый китайский патент на комбинированное лечение с артеметер и люмефантрин, предлагая первые комбинированные препараты на основе артемизинина (Коартем) по сниженным ценам до Всемирная организация здоровья.[86] В 2006 году, после того как артемизинин стал предпочтительным препаратом для лечения малярии, ВОЗ призвала к немедленному прекращению использования препаратов артемизинина с одним лекарством в пользу комбинаций артемизинина с другим лекарством от малярии, чтобы снизить риск развития резистентности паразитов.[87]
В 2011, Ту Youyou был удостоен престижной Премия Ласкера-Дебейки за клинические медицинские исследования за ее роль в открытии и разработке артемизинина.[81][88] 5 октября 2015 года ей вручили половину 2015 года. Нобелевская премия по физиологии и медицине за открытие артемизинина, «препарата, который значительно снизил уровень смертности пациентов, страдающих малярией».[2] Другая половина премии была вручена совместно Уильям К. Кэмпбелл и Сатоши Омура для открытия авермектин, "производные которых радикально снизили частоту возникновения Речная слепота и Лимфатический филяриатоз, а также демонстрирует эффективность против растущего числа других паразитарных заболеваний ".[2]
Смотрите также
- Artemisia (род), выносливые травянистые растения и кустарники, известные своими мощными химическими составляющими в эфирных маслах
- Артемизин, гидроксилированное производное сантонина
- Сантонин, глистогонный, препарат, изгоняющий паразитарных червей (гельминты ) парализовав их
Рекомендации
Эта статья содержит текст из общественного достояния от CDC, как указано
- ^ Белый Нью-Джерси (июль 1997 г.). «Оценка фармакодинамических свойств противомалярийных препаратов in vivo». Противомикробные препараты и химиотерапия. 41 (7): 1413–22. Дои:10.1128 / AAC.41.7.1413. ЧВК 163932. PMID 9210658.
- ^ а б c «Нобелевская премия по физиологии и медицине 2015 г.». Нобелевский фонд. Получено 2020-10-12.
- ^ ВОЗ (2015). Рекомендации по лечению малярии. Всемирная организация здравоохранения (Третье изд.). Женева. С. 9–11. ISBN 978-92-4-154912-7. OCLC 908628497.
- ^ Арсено П.Р., Воббе К.К., Уэтерз П.Дж. (2008). «Последние достижения в производстве артемизинина за счет гетерологичной экспрессии». Современная лекарственная химия. 15 (27): 2886–96. Дои:10.2174/092986708786242813. ЧВК 2821817. PMID 18991643.
- ^ а б Браун G (июль 2006 г.). «Артемизинин и противомалярийные препараты нового поколения». Образование в области химии. Vol. 43 нет. 4. Королевское химическое общество. стр. 97–99. Получено 2018-03-09.
- ^ а б c Whirl-Carrillo M, McDonagh EM, Hebert JM, Gong L, Sangkuhl K, Thorn CF и др. (Октябрь 2012 г.). «Знания фармакогеномики для персонализированной медицины». Клиническая фармакология и терапия. 92 (4): 414–7. Дои:10.1038 / clpt.2012.96. ЧВК 3660037. PMID 22992668.
- ^ «Разработка новых противомалярийных препаратов». Мир малярии. 6 сентября 2010 г.. Получено 2016-10-22.
- ^ «ВОЗ призывает к немедленному прекращению поставок одноразовых таблеток от малярии с артемизинином». ВОЗ. 19 января 2006 г.
- ^ Пельфрен Э., Пинейро М.Х., Кавалери М. (июль 2015 г.). «Комбинированная терапия на основе артемизинина в лечении неосложненной малярии: обзор недавнего регуляторного опыта Европейского агентства по лекарственным средствам». Международное здравоохранение. 7 (4): 239–46. Дои:10.1093 / inthealth / ihv017. ЧВК 4492341. PMID 25855638.
- ^ Rehwagen C (май 2006 г.). «Ультиматум ВОЗ по монотерапии артемизинином дает результаты». BMJ. 332 (7551): 1176. Дои:10.1136 / bmj.332.7551.1176-б. ЧВК 1463909. PMID 16709988.
- ^ Рекомендации по лечению малярии. Женева: Всемирная организация здравоохранения. 2006 г. ISBN 978-92-4-154694-2.
- ^ Белый Нью-Джерси (апрель 2004 г.). «Устойчивость к противомалярийным препаратам». Журнал клинических исследований. 113 (8): 1084–92. Дои:10.1172 / JCI21682. ЧВК 385418. PMID 15085184.
- ^ Krudsood S, Looareesuwan S, Tangpukdee N, Wilairatana P, Phumratanaprapin W, Leowattana W. и др. (Сентябрь 2010 г.). «Новая композиция артесуната-мефлохина с фиксированной дозой против Plasmodium falciparum с множественной лекарственной устойчивостью у взрослых: сравнительное исследование безопасности и фармакокинетики фазы IIb со стандартной дозой нефиксированного артесуната плюс мефлохин». Противомикробные препараты и химиотерапия. 54 (9): 3730–7. Дои:10.1128 / AAC.01187-09. ЧВК 2935027. PMID 20547795.
- ^ «В Кении отозвали лекарства от малярии». Новости BBC. 17 августа 2007 г.
- ^ Ньютон П., Пру С., Грин М., Смитьюис Ф., Розендаал Дж., Праконгпан С. и др. (Июнь 2001 г.). «Поддельный артесунат в Юго-Восточной Азии». Ланцет. 357 (9272): 1948–50. Дои:10.1016 / S0140-6736 (00) 05085-6. PMID 11425421. S2CID 27929151.
- ^ Дондорп А, Ностен Ф, Степневска К., День N, Белый N (2005). «Артесунат по сравнению с хинином для лечения тяжелой малярии, вызванной falciparum: рандомизированное испытание». Ланцет. 366 (9487): 717–25. Дои:10.1016 / S0140-6736 (05) 67176-0. PMID 16125588. S2CID 173027.
- ^ а б Дондорп А.М., Фанелло К.И., Хендриксен И.К., Гомес Э., Сени А., Чхаганлал К.Д. и др. (Ноябрь 2010 г.). «Артесунат по сравнению с хинином в лечении тяжелой малярии, вызванной falciparum, у африканских детей (АКВАМАТ): открытое рандомизированное исследование». Ланцет. 376 (9753): 1647–57. Дои:10.1016 / S0140-6736 (10) 61924-1. ЧВК 3033534. PMID 21062666.
- ^ Бхаттарай А., Али А.С., Качур С.П., Мартенссон А., Аббас А.К., Хатиб Р. и др. (Ноябрь 2007 г.). «Влияние комбинированной терапии на основе артемизинина и обработанных инсектицидами сеток на бремя малярии на Занзибаре». PLOS Медицина. 4 (11): e309. Дои:10.1371 / journal.pmed.0040309. ЧВК 2062481. PMID 17988171.
- ^ Le WJ, You JQ, Mei JY, Wang GF, Xie RR (август 1981 г.). «[Антишистосомное действие некоторых производных Qing Hao Su на инфицированных мышей (перевод автора)]». Яо Сюэ Сюэ Бао = Acta Pharmaceutica Sinica. 16 (8): 561–3. PMID 7324954.
- ^ Le WJ, You JQ, Yang YQ, Mei JY, Guo HF, Yang HZ, Zhang CW (1982). «[Исследования эффективности артеметера при экспериментальном шистосомозе (авторский перевод)]». Яо Сюэ Сюэ Бао. 17 (3): 187–93. PMID 7115549.CS1 maint: несколько имен: список авторов (связь)
- ^ Le WJ, You JQ, Mei JY (август 1983 г.). «[Химиотерапевтический эффект артесуната при экспериментальном шистосомозе]». Яо Сюэ Сюэ Бао = Acta Pharmaceutica Sinica. 18 (8): 619–21. PMID 6677044.
- ^ Сяо Ш. (2005). «Разработка антишистосомных препаратов в Китае с особым вниманием к празиквантелу и артемизининам». Acta Tropica. 96 (2–3): 153–67. Дои:10.1016 / j.actatropica.2005.07.010. PMID 16112072.
- ^ Кейзер Дж., Утцингер Дж. (Декабрь 2007 г.). «Артемизинины и синтетические триоксоланы в лечении гельминтозов». Современное мнение об инфекционных заболеваниях. 20 (6): 605–12. Дои:10.1097 / QCO.0b013e3282f19ec4. PMID 17975411. S2CID 34591129.
- ^ Konstat-Korzenny E, Ascencio-Aragón JA, Niezen-Lugo S, Vázquez-López R (февраль 2018 г.). «Артемизинин и его синтетические производные как возможное средство лечения рака». медицинские науки. 6 (1): 19. Дои:10.3390 / medsci6010019. ЧВК 5872176. PMID 29495461.
- ^ Raffetin A, Bruneel F, Roussel C, Thellier M, Buffet P, Caumes E, Jauréguiberry S (июнь 2018 г.). «Использование артесуната по немалярийным показаниям» (PDF). Médecine et Maladies Infectieuses. 48 (4): 238–249. Дои:10.1016 / j.medmal.2018.01.004. PMID 29422423.
- ^ Ши К., Ли Х, Ян И, Хоу Л. (2015). «Противовоспалительные и иммунорегуляторные функции артемизинина и его производных». Медиаторы воспаления. 2015: 435713. Дои:10.1155/2015/435713. ЧВК 4415672. PMID 25960615.
- ^ Му Икс, Ван Си (июль 2018 г.). «Артемизинины - новый многообещающий метод лечения системной красной волчанки: описательный обзор». Текущие отчеты ревматологии. 20 (9): 55. Дои:10.1007 / s11926-018-0764-у. PMID 30056574. S2CID 51866562.
- ^ а б Тейлор WR, Белый Нью-Джерси (2004). «Антималярийная токсичность лекарств: обзор». Безопасность лекарств. 27 (1): 25–61. Дои:10.2165/00002018-200427010-00003. PMID 14720085. S2CID 28284347.
- ^ Леонарди Э., Гилвари G, Уайт Нью-Джерси, Ностен Ф. (2001). «Тяжелые аллергические реакции на пероральный артесунат: сообщение о двух случаях». Труды Королевского общества тропической медицины и гигиены. 95 (2): 182–3. Дои:10.1016 / S0035-9203 (01) 90157-9. PMID 11355556.
- ^ «Гепатит, временно связанный с травяными добавками, содержащими артемизинин - Вашингтон, 2008 г.». CDC.
- ^ Прайс Р., ван Вугт М., Фаипун Л., Люксембург С., Симпсон Дж., МакГриди Р. и др. (Апрель 1999 г.). «Побочные эффекты у пациентов с острой малярией falciparum, получавших производные артемизинина». Американский журнал тропической медицины и гигиены. 60 (4): 547–55. Дои:10.4269 / ajtmh.1999.60.547. PMID 10348227.
- ^ а б Роберт А., Бенуа-Викаль Ф, Лю И, Менье Б. (январь 2019 г.). Сигель А., Фрайзингер Э., Сигель Р.К., Карвер П.Л. (ред.). «Малые молекулы: прошлое или будущее в области лекарственных инноваций?». Ионы металлов в науках о жизни. de Gruyter mbH. 19: 17–48. Дои:10.1515/9783110527872-008. ISBN 978-3-11-052691-2. PMID 30855103.
- ^ а б Вудро С.Дж., Хейнс Р.К., Кришна С. (февраль 2005 г.). «Артемизинины». Последипломный медицинский журнал. 81 (952): 71–8. Дои:10.1136 / pgmj.2004.028399. ЧВК 1743191. PMID 15701735.
- ^ Ли И (сентябрь 2012 г.). «Цинхаосу (артемизинин): химия и фармакология». Acta Pharmacologica Sinica. 33 (9): 1141–6. Дои:10.1038 / aps.2012.104. ЧВК 4003104. PMID 22922345.
- ^ Адерибигбе Б.А. (февраль 2017 г.). «Разработка систем доставки лекарств, содержащих артемизинин и его производные». Молекулы. 22 (2): 323. Дои:10.3390 / молекулы22020323. ЧВК 6155641. PMID 28230749.
- ^ Познер Г.Х., Parker MH, Northrop J, Elias JS, Ploypradith P, Xie S, Shapiro TA (январь 1999 г.). «Перорально активные, гидролитически стабильные, полусинтетические противомалярийные триоксаны в семействе артемизининов». Журнал медицинской химии. 42 (2): 300–4. Дои:10.1021 / jm980529v. PMID 9925735.
- ^ Моррис К.А., Дюпарк С., Боргини-фюрер I, Юнг Д., Шин С.С., Флекенштейн Л. (сентябрь 2011 г.). «Обзор клинической фармакокинетики артесуната и его активного метаболита дигидроартемизинина после внутривенного, внутримышечного, перорального или ректального введения». Журнал Малярии. 10 (1): 263. Дои:10.1186/1475-2875-10-263. ЧВК 3180444. PMID 21914160.
- ^ Веннерстром Дж. Л., Арбе-Барнс С., Брун Р., Чарман С. А., Чиу Ф. К., Шолле Дж. И др. (Август 2004 г.). «Идентификация кандидата на разработку противомалярийного синтетического триоксолана». Природа. 430 (7002): 900–4. Bibcode:2004 Натур.430..900В. Дои:10.1038 / природа02779. PMID 15318224. S2CID 4320974.
- ^ Унникришнан СН (21 сентября 2007 г.). "Подорвать планы Ranbaxy по исследованию наркотиков". livemint.com.
- ^ Кригер Дж., Смейлус Т., Кайзер М., Сео Э. Дж., Эфферт Т., Яннис А. (июль 2018 г.). «Полный синтез и биологическое исследование (-) - артемизинина: антималярийная активность артемизинина не является стереоспецифической». Angewandte Chemie. 57 (27): 8293–8296. Дои:10.1002 / anie.201802015. PMID 29723442.
- ^ Тилли Л., Страймер Дж., Гнэдиг Н.Ф., Ральф С.А., Фидок Д.А. (сентябрь 2016 г.). «Действие и устойчивость к артемизинину у Plasmodium falciparum». Тенденции в паразитологии. 32 (9): 682–696. Дои:10.1016 / j.pt.2016.05.010. ЧВК 5007624. PMID 27289273.
- ^ Winzeler EA, Manary MJ (ноябрь 2014 г.). «Геномика лекарственной устойчивости противомалярийного препарата артемизинин». Геномная биология. 15 (11): 544. Дои:10.1186 / s13059-014-0544-6. ЧВК 4283579. PMID 25470531.
- ^ Краво П., Наполитано Х, Каллетон Р. (август 2015 г.). «Как геномика способствует борьбе с устойчивыми к артемизинину малярийными паразитами». Acta Tropica. 148: 1–7. Дои:10.1016 / j.actatropica.2015.04.007. PMID 25910626.
- ^ Ван Дж., Чжан С.Дж., Чиа В.Н., Ло С.К., Ли З., Ли Ю.М. и др. (Декабрь 2015 г.). «Активированное гемом беспорядочное нацеливание артемизинина в Plasmodium falciparum». Nature Communications. 6: 10111. Bibcode:2015 НатКо ... 610111W. Дои:10.1038 / ncomms10111. ЧВК 4703832. PMID 26694030.
- ^ Немецкий ИП, Aweeka FT (2008). «Клиническая фармакология комбинированной терапии на основе артемизинина». Клиническая фармакокинетика. 47 (2): 91–102. Дои:10.2165/00003088-200847020-00002. PMID 18193915. S2CID 24983411.
- ^ Ноэдл Х., Се И, Шехер К., Смит Б.Л., Сохеат Д., Фукуда М.М. (декабрь 2008 г.). «Доказательства устойчивости к артемизинину малярии в западной Камбодже». Медицинский журнал Новой Англии. 359 (24): 2619–20. Дои:10.1056 / NEJMc0805011. PMID 19064625.
- ^ Морелль Р. (20 октября 2015 г.). «Малярия с лекарственной устойчивостью может заразить африканских комаров». Новости BBC. Получено 20 октября 2015.
- ^ Дондорп А.М., Ностен Ф., Йи П., Дас Д., Фио А.П., Тарнинг Дж. И др. (Июль 2009 г.). «Устойчивость к артемизинину при малярии, вызванной Plasmodium falciparum». Медицинский журнал Новой Англии. 361 (5): 455–67. Дои:10.1056 / NEJMoa0808859. ЧВК 3495232. PMID 19641202.
- ^ Phyo AP, Nkhoma S, Stepniewska K, Ashley EA, Nair S, McGready R и др. (Май 2012 г.). «Появление устойчивой к артемизинину малярии на западной границе Таиланда: продольное исследование». Ланцет. 379 (9830): 1960–6. Дои:10.1016 / S0140-6736 (12) 60484-X. ЧВК 3525980. PMID 22484134.
- ^ а б Бриггс Х (30 июля 2014 г.). «Призыв к« радикальным действиям »против лекарственно-устойчивой малярии». Новости BBC. Получено 2013-07-30.
- ^ а б Эшли Э.А., Дорда М., Фэрхерст Р.М., Амаратунга С., Лим П., Суон С. и др. (Июль 2014 г.). «Распространение устойчивости к артемизинину при малярии, вызванной Plasmodium falciparum». Медицинский журнал Новой Англии. 371 (5): 411–23. Дои:10.1056 / NEJMoa1314981. ЧВК 4143591. PMID 25075834.
- ^ Ariey F, Witkowski B, Amaratunga C, Beghain J, Langlois AC, Khim N и др. (Январь 2014). «Молекулярный маркер малярии Plasmodium falciparum, устойчивой к артемизинину». Природа. 505 (7481): 50–5. Bibcode:2014Натура 505 ... 50А. Дои:10.1038 / природа12876. ЧВК 5007947. PMID 24352242.
- ^ «Иммунитет к лекарственным препаратам может« не подвести ». The Jakarta Post. 23 апреля 2011 г. Архивировано с оригинал 4 марта 2016 г.
- ^ Оджи М., Ожеро Дж. М., Палок Л., Бенуа-Викаль Ф (2018). «Устойчивость Plasmodium falciparum к комбинированной терапии на основе артемизинина: дамоклов меч на пути к ликвидации малярии». Паразит. 25: 24. Дои:10.1051 / паразит / 2018021. ЧВК 5909375. PMID 29676250.

- ^ а б c d Пиррунг М.С., Морхед А.Т. младший (1997). "Sesquidecade of Sesquiterpenes, 1980–1994: Part A. Ациклические и моноциклические сесквитерпены, Часть 1". В Goldsmith D (ред.). Полный синтез натуральных продуктов. 10. Нью-Йорк: Джон Вили и сыновья. С. 90–96. ISBN 978-0-470-12962-3.
- ^ Шмид Г., Хофхайнц В. (1983). «Полный синтез цинхаосу». Журнал Американского химического общества. 105 (3): 624–625. Дои:10.1021 / ja00341a054.
- ^ Актон Н., Клейман Д.Л. (октябрь 1985 г.). «Артемизитен, новый эндопероксид сесквитерпенового лактона из Artemisia annua». Planta Medica. 51 (5): 441–2. Дои:10.1055 / с-2007-969543. PMID 17342606.
- ^ Чжу С., Кук С.П. (август 2012 г.). «Краткий синтез (+) - артемизинина». Журнал Американского химического общества. 134 (33): 13577–9. Дои:10.1021 / ja3061479. PMID 22866604.
- ^ «Химические составляющие Artemisia annua». Китайский журнал китайской Materia Medica. 2014-12-15. Дои:10.4268 / cjcmm20142423. ISSN 1001-5302.
- ^ Lévesque F, Seeberger PH (февраль 2012 г.). «Непрерывный синтез противомалярийного препарата артемизинин». Angewandte Chemie. 51 (7): 1706–9. Дои:10.1002 / anie.201107446. PMID 22250044.
- ^ Туркони Дж., Гриолет Ф., Гевель Р., Оддон Дж., Вилла Р., Геатти А. и др. (2014). «Полусинтетический артемизинин - химический путь к промышленному производству». Исследования и разработки в области органических процессов. 18 (3): 417–422. Дои:10.1021 / op4003196.
- ^ Болл П (2016). "Сделано человеком: история синтетической жизни". Дистилляции. 2 (1): 15–23. Получено 20 марта 2018.
- ^ Ро Д.К., Парадайз Е.М., Уэллет М., Фишер К.Дж., Ньюман К.Л., Ндунгу Дж.М. и др. (Апрель 2006 г.). «Производство противомалярийного препарата-предшественника артемизиновой кислоты в модифицированных дрожжах». Природа. 440 (7086): 940–3. Bibcode:2006Натура.440..940р. Дои:10.1038 / природа04640. PMID 16612385. S2CID 3199654.
- ^ а б Пантюшенко Е. «Санофи и PATH объявляют о запуске крупномасштабного производства полусинтетического артемизинина против малярии». ДОРОЖКА.
- ^ Пантюшенко Е. «Полусинтетический артемизинин прошел предварительную квалификацию ВОЗ». ДОРОЖКА. Получено 8 февраля 2014.
- ^ ван Херпен Т.В., Цанкар К., Ногейра М., Бош Д., Бауместер Х.Дж., Биквилдер Дж. (декабрь 2010 г.). Ян Х (ред.). «Nicotiana benthamiana как производственная платформа для прекурсоров артемизинина». PLOS ONE. 5 (12): e14222. Bibcode:2010PLoSO ... 514222V. Дои:10.1371 / journal.pone.0014222. ЧВК 2997059. PMID 21151979.
- ^ Лапкин А.А., Петерс М., Грейнер Л., Chemat S, Леонхард К., Лиау М.А., Лейтнер В. (2010). «Скрининг новых растворителей для процесса экстракции артемизинина с использованием ab initio методология ». Зеленая химия. 12 (2): 241–251. Дои:10.1039 / b922001a. и цитируемая там литература
- ^ а б "Отчет о конференции Artemisinin Enterprise 2008" (PDF). Архивировано из оригинал (PDF) на 2014-06-17. Получено 2011-07-12.
- ^ "Вылечить все?". Экономист. 25 января 2014 г.. Получено 2016-10-22.
- ^ «Комбинированная терапия с артемизинином». Проект CNAP Artemisia. Йоркский университет. Архивировано из оригинал на 2012-10-05. Получено 2011-07-12.
- ^ "Guilin Pharmaceutical ─ Первый в мире производитель преквалифицированного ВОЗ артесуната для инъекций при тяжелой малярии". mmv.org. 2010. Архивировано с оригинал в 2016-10-22. Получено 2016-10-22.
- ^ «Эффективность нефармацевтических форм Artemisia annua L. против малярии». Всемирная организация здоровья. Глобальная программа борьбы с малярией. Заявление о позиции (июнь 2012 г.). Проверено апрель 2020.
- ^ Peplow M (апрель 2013 г.). «Санофи запускает производство лекарств от малярии, чтобы поддерживать стабильную доступность артемизинина». Chemistryworld Интернет. RSC. Получено 2013-04-19.
- ^ Палмер Э. (19 августа 2014 г.). "Санофи поставляет новое лекарство от малярии, изготовленное из полусинтетического артемизинина.'". Жесткое фармацевтическое производство. Получено 2014-09-14.
- ^ Опийо Н., Ями Дж., Гарнер П. (март 2016 г.). «Субсидирование комбинированной терапии на основе артемизинина в частном розничном секторе». Кокрановская база данных систематических обзоров. 3: CD009926. Дои:10.1002 / 14651858.cd009926.pub2. ЧВК 4916935. PMID 26954551.
- ^ Центры по контролю и профилактике заболеваний (CDC) (июль 2014 г.). «Этимология: Артемизинин». Возникающие инфекционные заболевания. 20 (7): 1217. Дои:10.3201 / eid2007.ET2007. ЧВК 4073852.
- ^ «Медицинские рукописи Ма Ван Дуй». Проект Цинхаосу.
- ^ Бернс В. "Чжоу Хоу Бей Джи Фан" [Удобные методы лечения в чрезвычайных ситуациях]. Проект Цинхаосу.
- ^ Бернс В. "Сайт проекта Цинхаосу". Blogspot. Получено 8 августа 2014.
- ^ Цзяньфан З (2006). Подробная хронологическая запись проекта 523 и открытия и развития Цинхаосу (Артемисинин). ISBN 9781622121649.
- ^ а б c d е ж грамм Миллер Л.Х., Вс X (сентябрь 2011 г.). «Артемизинин: открытие из китайского травяного сада». Клетка. 146 (6): 855–8. Дои:10.1016 / j.cell.2011.08.024. ЧВК 3414217. PMID 21907397.
- ^ Китайская Академия Наук, изд. (Ноябрь 1999 г.). Сяндай Ханью Сидиан 现代 汉语 词典 [Словарь современного китайского языка] (на китайском языке) (3-е (исправленное) изд.). Пекин: Коммерческая пресса. п. 1204. ISBN 7-100-01777-7. OCLC 41467509.
素 : ... 5.带有 根本 性质 的 物质 'вещество с фундаментальными свойствами'
- ^ Хао Ц. (29 сентября 2011 г.). «Премия Ласкера возрождает дебаты по поводу открытия Артемизинина». Наука. Получено 2014-01-07.
- ^ Координационная исследовательская группа по антималярии Цинхаосу (декабрь 1979 г.). «Антималярийные исследования на Цинхаосу». Китайский медицинский журнал. 92 (12): 811–6. PMID 117984.
- ^ Fairhurst RM, Nayyar GM, Breman JG, Hallett R, Vennerstrom JL, Duong S и др. (Август 2012 г.). «Малярия, устойчивая к артемизинину: исследовательские задачи, возможности и последствия для общественного здравоохранения». Американский журнал тропической медицины и гигиены. 87 (2): 231–241. Дои:10.4269 / ajtmh.2012.12-0025. ЧВК 3414557. PMID 22855752.
- ^ Нил Д.М. (17 января 2012 г.). «За интриги лекарство от малярии получает премию». Нью-Йорк Таймс. Получено 20 апреля 2013.
- ^ «ВОЗ призывает к немедленному прекращению поставок одноразовых таблеток от малярии с артемизинином» (Пресс-релиз). Всемирная организация здоровья. 19 января 2006 г.
- ^ Weise E (12 сентября 2011 г.). "'Американский ученый получил Нобелевскую премию ". USA Today. Получено 2011-09-12.
дальнейшее чтение
- Дэвис Б. (2005). «Малярия, наука и социальная ответственность: некоммерческое партнерство по разработке лекарств стремится излечить болезни развивающихся стран». Ученый. 19 (6): 42.
внешняя ссылка
- «Победа над проклятием». BBC Horizon.
Артемизинин оказался наиболее эффективным противомалярийным препаратом из когда-либо созданных.
