Агонист PPAR - PPAR agonist
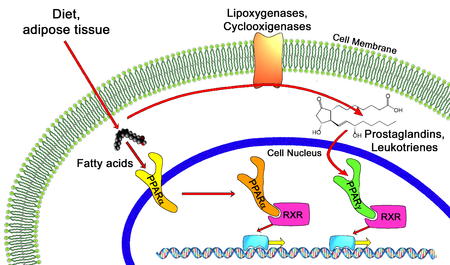
Агонисты PPAR находятся наркотики которые действуют на рецептор, активируемый пролифератором пероксисом. Они используются для лечения симптомов метаболический синдром, в основном для понижения триглицериды и содержание сахара в крови.
Классификация
PPAR-альфа и PPAR-гамма являются молекулярными мишенями для ряда продаваемых на рынке лекарств. Основными классами агонистов PPAR являются:
Агонисты PPAR-альфа
PPARα (альфа) главная цель фибрат наркотики, класс амфипатических карбоновых кислот (клофибрат, гемфиброзил, ципрофибрат, безафибрат, и фенофибрат ). Изначально они были указаны для холестерин расстройства, а в последнее время - расстройства с высоким содержанием триглицеридов.
Агонисты PPAR-гамма
PPARγ (гамма) является основной мишенью класса наркотиков тиазолидиндионы (TZDs), используемые в сахарный диабет и другие заболевания, характерные для резистентность к инсулину. Он также мягко активируется некоторыми НПВП (Такие как ибупрофен ) и индолы, а также из ряда природных соединений. Известные ингибиторы включают экспериментальный агент GW-9662.
Они также используются при лечении гиперлипидемии у атеросклероз. Здесь они действуют, увеличивая выражение ABCA1, который транспортирует внепеченочный холестерин в ЛПВП. Следовательно, увеличивается поглощение и выведение из печени.
Исследования на животных показали их возможную роль в уменьшении воспаления легких, особенно при астме.[1]
Агонисты PPAR-дельта
PPARδ (дельта) является основной целью исследовательского химического вещества под названием GW501516. Было показано, что агонизм PPARδ изменяет предпочтение организмом топлива от глюкозы к липидам.[2]
Двойные и пан-агонисты PPAR
Четвертый класс двойных агонистов PPAR, так называемые глитазары, которые связываются как с изоформами α, так и с γ PPAR, в настоящее время активно исследуются для лечения более широкого набора симптомов метаболического синдрома.[3][4] К ним относятся экспериментальные соединения алеглитазар, мураглитазар и тесаглитазар. В июне 2013 г. сароглитазар был первым глитазаром, одобренным для клинического применения.[5]
Кроме того, продолжаются исследования и разработка новых двойных агонистов α / δ и γ / δ PPAR для дополнительных терапевтический показания, а также «пан» агонисты, действующие на все три изоформы.[6][7]
Исследование
Агонисты PPARα / γ показали свой потенциал при лечении многих воспалительных состояний, включая астму и экзему.[8][9]
Еще одно относительно недавнее направление исследований лекарств для лечения депрессии и наркомании - это PPARα и PPARγ активация.[10] Обе TLR4 -опосредованно и NF-κB -опосредованные сигнальные пути участвуют в развитии зависимости от некоторых наркотиков, таких как опиоиды и кокаин, и поэтому являются привлекательными мишенями для фармакотерапии.[11][12][13] Несмотря на широту доклинических исследований, показывающих потенциал на животных моделях в лечении наркозависимости, включая алкоголь, никотин, кокаин, опиоиды и метамфетамин, данные на людях ограничены, так как количество испытаний, посвященных использованию агонистов PPAR для людей, все еще невелико; и пока (по состоянию на 2020 год) не особо перспективны. Существует несколько гипотез о плохой трансляции данных исследований от животных к человеку, таких как эффективность и селективность лигандов PPAR, изменчивость, связанная с полом, и видовые различия в распределении и передаче сигналов PPAR. [14]
Рекомендации
- ^ Gu, M. X .; Лю, X. C .; Цзян, Л. (2013). «Эффект гамма-рецептора, активируемого пролифератором пероксисом, на пролиферацию гладкомышечных клеток дыхательных путей у мышей с астмой». Чжунго Данг Дай Эр Кэ За Чжи = Китайский журнал современной педиатрии. 15 (7): 583–7. Дои:10.7499 / j.issn.1008-8830.2013.07.018. PMID 23866284.
- ^ Б. Брунмайр; и другие. (2006). «Активация PPAR-δ в изолированных скелетных мышцах крысы переключает предпочтение топлива с глюкозы на жирные кислоты». Диабетология. 49 (11): 2713–22. Дои:10.1007 / s00125-006-0357-6. PMID 16960684. S2CID 31757997.
- ^ Fiévet C, Fruchart JC, Staels B (2006). «Двойные агонисты PPARalpha и PPARgamma для лечения диабета 2 типа и метаболического синдрома». Текущее мнение в фармакологии. 6 (6): 606–14. Дои:10.1016 / j.coph.2006.06.009. PMID 16973418.
- ^ Балакумар П., Роуз М., Ганти С.С., Кришан П., Сингх М. (2007). «Двойные агонисты PPAR: открывают ли они ящик Пандоры?». Pharmacol. Res. 56 (2): 91–8. Дои:10.1016 / j.phrs.2007.03.002. PMID 17428674.
- ^ http://www.wallstreet-online.de/nachricht/6228479-zydus-gelingt-durchbruch-lipaglyn-wirkstoff-indien-markt-gelangt (на немецком)
- ^ Стэлс Б., Фрючарт Дж. К. (2005). «Терапевтическая роль агонистов рецепторов, активируемых пролифератором пероксисом». Сахарный диабет. 54 (8): 2460–70. Дои:10.2337 / диабет.54.8.2460. PMID 16046315.
- ^ Невин Д.К., Фейн Д., Ллойд Д.Г. (2011). «Рациональное нацеливание на подтипы активированных рецепторов пролиферации пероксисом». Современная лекарственная химия. 18 (36): 5598–623. Дои:10.2174/092986711798347243. PMID 22172067.
- ^ Банно А., Редди А.Т., Лакшми С.П. и Редди Р.С. (2018). «PPAR: ключевые регуляторы воспаления дыхательных путей и потенциальные терапевтические цели при астме». Исследование ядерных рецепторов. 5: 101306. Дои:10.11131/2018/101306. ЧВК 5810409. PMID 29450204.CS1 maint: использует параметр авторов (связь)
- ^ Дубрак С, Шмут М (2011). «PPAR-альфа при кожном воспалении». Дермато-эндокринология. 3 (1): 23–26. Дои:10.4161 / derm.3.1.14615. ЧВК 3051849. PMID 21519405.CS1 maint: использует параметр авторов (связь)
- ^ Ле Фолль, Б., Ди Чиано, П., Панлилио, С. Р. Голдберг, и Чичкочоппо, Р. (2013). «Агонисты рецепторов, активируемых пролифератором пероксисом (PPAR), как многообещающие новые лекарства от наркозависимости: доклинические данные». Текущие цели в отношении лекарств. 14 (7): 768–776. Дои:10.2174/1389450111314070006. ЧВК 3826450. PMID 23614675.CS1 maint: использует параметр авторов (связь)
- ^ Батчелл, Р.К., Хатчинсон, М.Р., Ван, X., Райс, К.С., Майер, С.Ф., и Уоткинс, Л. (2015). «Задача борьбы со злоупотреблением наркотиками: трансляционный потенциал толл-подобного рецептора 4». Целевые препараты для лечения заболеваний ЦНС и неврологических расстройств. 14 (6): 692–9. Дои:10.2174/1871527314666150529132503. ЧВК 5548122. PMID 26022268.CS1 maint: использует параметр авторов (связь)
- ^ Найннинг, С. и Шенк, Дж. Р. (2013). «Роль NFkB в наркомании: помимо воспаления». Алкоголь и алкоголизм. 14 (7): 768–776. Дои:10.1093 / alcalc / agw098. ЧВК 6410896. PMID 28043969.CS1 maint: использует параметр авторов (связь)
- ^ Руссо, С.Дж., Уилкинсон, М., Мазей-Робисон, М., Дитц, Д.М., Мейз, И., Кришнан, В., Рента, В., Грэм, А., Бибаум, С.Г., Грин, Т.А., Робисон, Б., Лессельонг, А., Перротти, Л.И., Боланос, Калифорния, Кумар, А., Кларк, М.С., Ноймайер, Дж. Ф., Неве, Р.Л., Бхакар, А.Л., Баркер, П.А. и Нестлер, Э.Дж. (2009). «Передача сигналов NFκB регулирует морфологию нейронов и вознаграждение кокаина». Журнал неврологии. 29 (11): 3529–3537. Дои:10.1523 / jneurosci.6173-08.2009. ЧВК 3826450. PMID 23614675.CS1 maint: использует параметр авторов (связь)
- ^ Мэтисон, Джастин; Ле Фолль, Бернар (май 2020 г.). «Терапевтический потенциал агонистов рецепторов, активируемых пролифератором пероксисом (PPAR), при расстройствах, связанных с употреблением психоактивных веществ: синтез доклинических и человеческих данных». Клетки. 9: 1196. Дои:10.3390 / ячейки905119 (неактивно 13.09.2020). PMID 32408505.CS1 maint: DOI неактивен по состоянию на сентябрь 2020 г. (связь)
