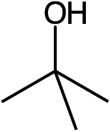
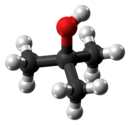
Трет-бутиловый спирт - Tert-Butyl alcohol
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название IUPAC 2-метилпропан-2-ол | |||
Другие имена
| |||
| Идентификаторы | |||
3D модель (JSmol ) | |||
| 906698 | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.809 | ||
| Номер ЕС |
| ||
| 1833 | |||
| MeSH | трет-бутил + спирт | ||
PubChem CID | |||
| Номер RTECS |
| ||
| UNII | |||
| Номер ООН | 1120 | ||
| |||
| |||
| Характеристики | |||
| C4ЧАС10О | |||
| Молярная масса | 74.123 г · моль−1 | ||
| Внешность | Бесцветное твердое вещество | ||
| Запах | Камфор | ||
| Плотность | 0,775 г / мл | ||
| Температура плавления | От 25 до 26 ° С; От 77 до 79 ° F; От 298 до 299 К | ||
| Точка кипения | 82-83 ° С; От 179 до 181 ° F; От 355 до 356 К | ||
| смешивающийся[2] | |||
| бревно п | 0.584 | ||
| Давление газа | 4,1 кПа (при 20 ° C) | ||
| Кислотность (пKа) | 16.54 [3] | ||
| 5.742×10−5 см3/ моль | |||
| 1.387 | |||
| 1,31 D | |||
| Термохимия | |||
Теплоемкость (C) | 215,37 Дж К−1 моль−1 | ||
Стандартный моляр энтропия (S | 189,5 Дж · К−1 моль−1 | ||
Станд. Энтальпия формирование (ΔжЧАС⦵298) | От −360,04 до −358,36 кДж моль−1 | ||
Станд. Энтальпия горение (ΔcЧАС⦵298) | От −2,64479 до −2,64321 МДж моль−1 | ||
| Опасности | |||
| Паспорт безопасности | inchem.org | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| H225, H319, H332, H335 | |||
| P210, P261, P305 + 351 + 338 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | 11 ° С (52 ° F, 284 К) | ||
| 480 ° С (896 ° F, 753 К) | |||
| Пределы взрываемости | 2.4–8.0% | ||
| Смертельная доза или концентрация (LD, LC): | |||
LD50 (средняя доза ) | 3559 мг / кг (кролик, перорально) 3500 мг / кг (крыса, перорально)[4] | ||
| NIOSH (Пределы воздействия на здоровье в США): | |||
PEL (Допустимо) | TWA 100 частей на миллион (300 мг / м3)[1] | ||
REL (Рекомендуемые) | TWA 100 частей на миллион (300 мг / м3) ST 150 частей на миллион (450 мг / м3)[1] | ||
IDLH (Непосредственная опасность) | 1600 частей на миллион[1] | ||
| Родственные соединения | |||
Связанный бутанолы | 2-бутанол | ||
Родственные соединения | 2-метил-2-бутанол Триметилсиланол | ||
Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки на инфобоксы | |||
терт-Бутиловый спирт (TBA), также называемый терт-бутанол или же т-бутанол, самый простой третичный спирт, с формула из (CH3)3COH (иногда представлен в качестве т-BuOH). Это один из четырех изомеры из бутанол.[а] терт-Бутиловый спирт представляет собой бесцветное твердое вещество, которое плавится при комнатной температуре и имеет камфора -подобный запах. Он смешивается с воды, этиловый спирт и диэтиловый эфир.
Естественное явление
терт-Бутиловый спирт был обнаружен в пиво и нут.[5] Он также встречается в маниока,[6] который используется в качестве ингредиента ферментации в некоторых Алкогольные напитки.
Подготовка
терт-Бутиловый спирт коммерчески получают из изобутан как побочный продукт оксид пропилена производство. Он также может быть получен каталитическим гидратация из изобутилен, или Реакция Гриньяра между ацетон и метилмагний хлорид.
Очистка не может быть проведена простой перегонкой из-за образования азеотроп с водой, хотя начальная сушка растворителя, содержащего большое количество воды, выполняется путем добавления бензола с образованием третичного азеотропа и отгонки воды. Меньшее количество воды удаляется сушкой оксид кальция (CaO), карбонат калия (K2CO3), сульфат кальция (CaSO4), или же сульфат магния (MgSO4) с последующей фракционной перегонкой. Безводный терт-бутиловый спирт получают путем дальнейшего кипячения с обратным холодильником и перегонки из магния, активированного йодом, или щелочных металлов, таких как натрий или калий. Другие методы включают использование 4Å молекулярные сита, алюминий терт-бутилат, гидрид кальция (CaH2) или фракционной кристаллизацией в инертной атмосфере.[7]
Приложения
терт-Бутиловый спирт используется как растворитель, этанол денатурирующий агент, средство для удаления краски ингредиент и бензин октан бустер и насыщать кислородом. Это промежуточный химический продукт, используемый для производства метил терт-бутиловый эфир (МТБЭ) и этил терт-бутиловый эфир (ETBE) путем реакции с метанол и этиловый спирт соответственно и терт-бутилгидропероксид (TBHP) путем реакции с пероксид водорода.
Реакции
Как третичный спирт, терт-бутиловый спирт более устойчив к окислению, чем другие изомеры бутанола.
терт-Бутиловый спирт депротонируется с сильным основание дать алкоксид. Особенно часто встречается калий терт-бутоксид, который готовится путем обработки терт-бутанол с калий металл.[8]
- K + т-BuOH → т-BuO−K+ + 1/2 ЧАС2
В терт-бутоксид - сильный, не-нуклеофильный база в органической химии. Он легко отделяет кислотные протоны от субстратов, но его стерическая масса препятствует участию группы в нуклеофильное замещение, например, в Синтез эфира Вильямсона или SN2 реакция.
терт-Бутиловый спирт реагирует с хлористый водород формировать терт-бутилхлорид.
О-хлорирование трет-бутилового спирта хлорноватистой кислотой с получением трет-бутилгипохлорит:[9]
- (CH3)3COH + HOCl → (CH3)3COCl + H2О
Фармакология и токсикология
Данные о фармакологии и токсикологии трет-бутанола у людей и других животных ограничены.[10] Воздействие на человека может происходить из-за метаболизма кислородсодержащих веществ. Трет-бутанол плохо всасывается через кожу, но быстро всасывается при вдыхании или проглатывании. Трет-бутанол раздражает кожу и глаза. Токсичность однократных доз обычно невысока, но высокие дозы могут вызывать седативный или анестезирующий эффект.
Примечания
- ^ Остальные изомеры терт-Бутиловый спирт, (CH3)3COH, являются Изобутанол, (CH3)2CHCH2ОЙ, 2-бутанол, CH3CH2СН (ОН) СН3, и н-бутанол, CH3CH2CH2CH2ОЙ. Все эти соединения имеют одну и ту же общую химическую формулу C4ЧАС10O, и как таковые они считаются изомерами.
Рекомендации
- ^ а б c d Карманный справочник NIOSH по химической опасности. "#0078". Национальный институт охраны труда и здоровья (NIOSH).
- ^ «ICSC 0114 - терт-Бутанол ». Inchem.org. Получено 29 марта 2018.
- ^ Рив, В .; Erikson, C.M .; Алуотто, П. Ф. (1979). «трет-бутиловый спирт». Может. J. Chem. 57: 2747. Дои:10.1139 / v79-444.
- ^ «трет-бутиловый спирт». Немедленно опасные для жизни и здоровья концентрации (IDLH). Национальный институт охраны труда и здоровья (NIOSH).
- ^ "т-Бутиловый спирт ». База данных HSDB Национальной медицинской библиотеки. Национальный институт здоровья. Получено 29 марта 2018.
- ^ «Архивная копия» (PDF). Архивировано из оригинал (PDF) на 2016-03-04. Получено 2013-03-05.CS1 maint: заархивированная копия как заголовок (связь)
- ^ Perrin, D. D .; Армарего, В. Л. Ф. (1988). Очистка лабораторных химикатов (3-е изд.). Pergamon Press.
- ^ Johnson, W. S .; Шнайдер, В. П. (1950). «β-Карбетокси-γ, γ-дифенилвинилуксусная кислота». Органический синтез. 30: 18. Дои:10.15227 / orgsyn.030.0018.
- ^ Mintz, H.M .; Уоллинг, К. (1969). «трет-Бутилгипохлорит». Орг. Синтезатор. 49: 9. Дои:10.15227 / orgsyn.049.0009.
- ^ Дуглас МакГрегор (2010). «Третичный бутанол: токсикологический обзор». Критические обзоры в токсикологии. 40 (8): 697–727. Дои:10.3109/10408444.2010.494249. PMID 20722584. S2CID 26041562.
внешняя ссылка
- Международная карта химической безопасности 0114
- Карманный справочник NIOSH по химической опасности. "#0078". Национальный институт охраны труда и здоровья (NIOSH).
- IPCS Критерии гигиены окружающей среды 65: Бутанолы: четыре изомера
- IPCS Руководство по охране труда и технике безопасности 7: терт-Бутанол