Углерод - Carbon
 Графит (слева) и алмаз (справа), два аллотропа углерода | ||||||||||||||||||||||||||
| Углерод | ||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Аллотропы | графит, алмаз, другие | |||||||||||||||||||||||||
| Внешность |
| |||||||||||||||||||||||||
| Стандартный атомный вес Аr, std(С) | [12.0096, 12.0116] общепринятый:12.011 | |||||||||||||||||||||||||
| Углерод в периодическая таблица | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
| Атомный номер (Z) | 6 | |||||||||||||||||||||||||
| Группа | группа 14 (углеродная группа) | |||||||||||||||||||||||||
| Период | период 2 | |||||||||||||||||||||||||
| Блокировать | p-блок | |||||||||||||||||||||||||
| Категория элемента | Реактивный неметалл, иногда считается металлоид | |||||||||||||||||||||||||
| Электронная конфигурация | [Он ] 2 с2 2p2 | |||||||||||||||||||||||||
| Электронов на оболочку | 2, 4 | |||||||||||||||||||||||||
| Физические свойства | ||||||||||||||||||||||||||
| Фаза вSTP | твердый | |||||||||||||||||||||||||
| Точка сублимации | 3915 К (3642 ° С, 6588 ° F) | |||||||||||||||||||||||||
| Плотность (возлеr.t.) | аморфный: 1,8–2,1 г / см3[1] графит: 2,267 г / см3 алмаз: 3,515 г / см3 | |||||||||||||||||||||||||
| Тройная точка | 4600 К, 10 800 кПа[2][3] | |||||||||||||||||||||||||
| Теплота плавления | графит: 117кДж / моль | |||||||||||||||||||||||||
| Молярная теплоемкость | графит: 8,517 Дж / (моль · К) алмаз: 6,155 Дж / (моль · К) | |||||||||||||||||||||||||
| Атомные свойства | ||||||||||||||||||||||||||
| Состояния окисления | −4, −3, −2, −1, 0, +1,[4] +2, +3,[5] +4[6] (мягко кислый окись) | |||||||||||||||||||||||||
| Электроотрицательность | Шкала Полинга: 2,55 | |||||||||||||||||||||||||
| Энергии ионизации |
| |||||||||||||||||||||||||
| Ковалентный радиус | зр3: 77 вечера зр2: 73 вечера sp: 69вечера | |||||||||||||||||||||||||
| Радиус Ван-дер-Ваальса | 170 вечера | |||||||||||||||||||||||||
| Другие свойства | ||||||||||||||||||||||||||
| Естественное явление | изначальный | |||||||||||||||||||||||||
| Кристальная структура | графит:простой шестиугольник (чернить) | |||||||||||||||||||||||||
| Кристальная структура | алмаз:гранецентрированный алмазно-кубический (Чисто) | |||||||||||||||||||||||||
| Скорость звука тонкий стержень | алмаз: 18 350 м / с (при 20 ° C) | |||||||||||||||||||||||||
| Тепловое расширение | алмаз: 0,8 мкм / (м · К) (при 25 ° C)[7] | |||||||||||||||||||||||||
| Теплопроводность | графит: 119–165 Вт / (м · К) алмаз: 900–2300 Вт / (м · К) | |||||||||||||||||||||||||
| Удельное электрическое сопротивление | графит: 7,837 мкОм · м[8] | |||||||||||||||||||||||||
| Магнитный заказ | диамагнитный[9] | |||||||||||||||||||||||||
| Магнитная восприимчивость | −5.9·10−6 (график) см3/ моль[10] | |||||||||||||||||||||||||
| Модуль для младших | алмаз: 1050 ГПа[7] | |||||||||||||||||||||||||
| Модуль сдвига | алмаз: 478 ГПа[7] | |||||||||||||||||||||||||
| Объемный модуль | алмаз: 442 ГПа[7] | |||||||||||||||||||||||||
| коэффициент Пуассона | алмаз: 0,1[7] | |||||||||||||||||||||||||
| Твердость по Моосу | графит: 1–2 алмаз: 10 | |||||||||||||||||||||||||
| Количество CAS |
| |||||||||||||||||||||||||
| История | ||||||||||||||||||||||||||
| Открытие | Египтяне и Шумеры[11] (3750 г. до н.э.) | |||||||||||||||||||||||||
| Признан как элемент | Антуан Лавуазье[12] (1789) | |||||||||||||||||||||||||
| Главный изотопы углерода | ||||||||||||||||||||||||||
| ||||||||||||||||||||||||||
Углерод (из латинский: карбо «уголь») является химический элемент с символ C и атомный номер 6. Это неметаллических и четырехвалентный —Сделать четыре электроны доступны для формирования ковалентный химические связи. Он принадлежит к 14 группе таблицы Менделеева.[13] Углерод составляет всего около 0,025 процента земной коры.[14] Три изотопы происходят естественно, 12C и 13C быть стабильным, в то время как 14C это радионуклид, распадаясь с период полураспада около 5730 лет.[15] Углерод является одним из несколько элементов, известных с древности.[16]
Углерод 15-й самый распространенный элемент в земной коре, а четвертый самый распространенный элемент во Вселенной по массе после водород, гелий, и кислород. Обилие углерода, его уникальное разнообразие органические соединения, и его необычная способность образовывать полимеры при температурах, обычно встречающихся на земной шар позволяет этому элементу служить общим элементом всем известная жизнь. Это второй по распространенности элемент в тело человека по массе (около 18,5%) после кислорода.[17]
Атомы углерода могут связываться друг с другом различными способами, что приводит к различным аллотропы углерода. Самые известные аллотропы: графит, алмаз, и бакминстерфуллерен.[18] В физические свойства углерода широко варьируются в зависимости от аллотропной формы. Например, графит - это непрозрачный и черный, в то время как алмаз высоко прозрачный. Графит достаточно мягкий, чтобы образовать полосу на бумаге (отсюда и название, от Греческий глагол «γράφειν», что означает «писать»), а алмаз - тяжелейший известный природный материал. Графит хороший электрический проводник в то время как у алмаза низкий электрическая проводимость. В нормальных условиях алмаз, углеродные нанотрубки, и графен иметь самый высокий теплопроводность из все известные материалы. Все аллотропы углерода в нормальных условиях являются твердыми телами, причем графит является наиболее термодинамически стабильный форма при стандартной температуре и давлении. Они химически устойчивы и требуют высокой температуры для реакции даже с кислородом.
Самый распространенный степень окисления углерода в неорганические соединения +4, а +2 находится в монооксид углерода и переходный металл карбонил комплексы. Крупнейшие источники неорганического углерода: известняки, доломиты и углекислый газ, но значительные количества встречаются в органических отложениях каменный уголь, торф, масло, и клатраты метана. Углерод образует огромное количество соединения, больше, чем любой другой элемент, на сегодняшний день описано почти десять миллионов соединений,[19] и тем не менее это число - лишь часть числа теоретически возможных соединений при стандартных условиях. По этой причине углерод часто называют «королем элементов».[20]
Характеристики
В аллотропы углерода включают графит, одно из самых мягких известных веществ, и алмаз, самое твердое вещество природного происхождения. Это облигации охотно с другими маленькими атомы, включая другие атомы углерода, и способен образовывать несколько стабильных ковалентный связи с подходящими многовалентными атомами. Известно, что углерод образует почти десять миллионов соединений, подавляющее большинство из которых химические соединения.[19] Углерод также имеет самый высокий сублимация точка всех элементов. В атмосферное давление не имеет точки плавления, так как его тройная точка я сидела 10.8±0,2 МПа и 4600 ± 300 К (4330 ± 300 ° C; 7820 ± 540 ° F),[2][3] поэтому он сублимируется при температуре около 3900 К (3630 ° C; 6560 ° F).[21][22] Графит намного более реакционноспособен, чем алмаз при стандартных условиях, несмотря на то, что он более термодинамически стабилен, поскольку его делокализованный система пи гораздо более уязвим для атак. Например, графит можно окислить горячим концентрированным азотная кислота при стандартных условиях меллитовая кислота, С6(CO2ЧАС)6, который сохраняет гексагональные единицы графита, разрушая более крупную структуру.[23]
Углерод возгоняется в угольной дуге, температура которой составляет около 5800 К (5 530 ° C или 9 980 ° F). Таким образом, независимо от своей аллотропной формы, углерод остается твердым при более высоких температурах, чем металлы с самой высокой температурой плавления, такие как вольфрам или же рений. Хотя термодинамически склонен к окисление, углерод сопротивляется окислению более эффективно, чем такие элементы, как утюг и медь, которые при комнатной температуре являются более слабыми восстановителями.
Углерод - шестой элемент с основным состоянием электронная конфигурация из 1 с22 с22p2, из которых четыре внешних электрона валентные электроны. Его первые четыре энергии ионизации, 1086,5, 2352,6, 4620,5 и 6222,7 кДж / моль, намного выше, чем у более тяжелых элементов группы 14. Электроотрицательность углерода составляет 2,5, что значительно выше, чем у более тяжелых элементов группы 14 (1,8–1,9), но близко к большинству ближайших неметаллов, а также к некоторым элементам второго и третьего ряда. переходные металлы. Углерода ковалентные радиусы обычно принимаются равными 77,2 пм (C-C), 66,7 пм (C = C) и 60,3 пм (C≡C), хотя они могут варьироваться в зависимости от координационного числа и того, с чем связан углерод. Как правило, ковалентный радиус уменьшается с меньшим координационным числом и более высоким порядком связи.[24]
Соединения углерода составляют основу всей известной жизни на земной шар, а углеродно-азотный цикл обеспечивает часть энергии, производимой солнце и другие звезды. Хотя он образует необычайное разнообразие соединений, большинство форм углерода в обычных условиях сравнительно неактивны. При стандартной температуре и давлении он сопротивляется всем, кроме самых сильных окислителей. Не реагирует с серная кислота, соляная кислота, хлор или любой щелочи. При повышенных температурах углерод реагирует с кислород формировать оксиды углерода и будет отнимать кислород у оксидов металлов, чтобы оставить элементарный металл. Этот экзотермическая реакция используется в черной металлургии для нюхать железо и контролировать содержание углерода в стали:
- Fe
3О
4 + 4 С(s) → 3 Fe(s) + 4 СО(грамм)
Окись углерода можно переработать, чтобы выплавить еще больше железа:
- Fe
3О
4 + 4 СО(грамм) → 3 Fe(s) + 4 CO
2(грамм)
с сера формировать сероуглерод и с паром в реакции уголь-газ:
- C(s) + H2О(грамм) → CO(грамм) + H2 (г).
Углерод соединяется с некоторыми металлами при высоких температурах с образованием карбидов металлов, таких как карбид железа. цементит в стали и карбид вольфрама, широко используется как абразивный и для изготовления твердых наконечников для режущих инструментов.
Система углеродных аллотропов охватывает целый ряд крайностей:
| Графит - один из самых мягких известных материалов. | Синтетический нанокристаллический алмаз это самый твердый из известных материалов.[25] |
| Графит очень хороший смазка, отображение сверхсмазочность.[26] | Алмаз - это самое лучшее абразивный. |
| Графит - это дирижер электричества.[27] | Diamond - отличный электрик изолятор,[28] и имеет самое высокое электрическое поле пробоя среди всех известных материалов. |
| Некоторые формы графита используются для теплоизоляция (например, противопожарные щиты и тепловые экраны), но некоторые другие формы являются хорошими проводниками тепла. | Алмаз - самый известный из встречающихся в природе проводник тепла |
| Графит непрозрачный. | Алмаз очень прозрачен. |
| Графит кристаллизуется в шестиугольная система.[29] | Алмаз кристаллизуется в кубическая система. |
| Аморфный углерод полностью изотропный. | Углеродные нанотрубки являются одними из самых анизотропный материалы известны. |
Аллотропы
Атомарный углерод является очень короткоживущим веществом, поэтому углерод стабилизирован в различных многоатомных структурах с различными молекулярными конфигурациями, называемыми аллотропы. Три относительно хорошо известных аллотропа углерода: аморфный углерод, графит, и алмаз. Когда-то считалось экзотическим, фуллерены в настоящее время обычно синтезируются и используются в исследованиях; они включают Bukyballs,[30][31] углеродные нанотрубки,[32] углеродные нанопочки[33] и нановолокна.[34][35] Также было обнаружено несколько других экзотических аллотропов, таких как лонсдейлит,[36] стеклоуглерод,[37] углеродная нано пена[38] и линейный ацетиленовый углерод (карбин).[39]
Графен представляет собой двумерный лист углерода с атомами, расположенными в гексагональной решетке. По состоянию на 2009 год графен оказался самым прочным материалом из когда-либо протестированных.[40] Процесс отделения его от графит потребует дальнейшего технологического развития, прежде чем он станет экономичным для промышленных процессов.[41] В случае успеха графен можно было бы использовать в конструкции космический лифт. Его также можно использовать для безопасного хранения водорода для использования в водородном двигателе автомобилей.[42]

В аморфный Форма представляет собой набор атомов углерода в некристаллическом, нерегулярном, стеклообразном состоянии, не удерживаемых в кристаллической макроструктуре. Он присутствует в виде порошка и является основным компонентом таких веществ, как уголь, черная лампа (сажа ) и Активированный уголь. При нормальном давлении углерод принимает форму графита, в котором каждый атом тригонально связан с тремя другими атомами в плоскости, состоящей из сплавленных шестиугольник кольца, как и в ароматические углеводороды.[43] Полученная сеть является двумерной, а полученные плоские листы уложены друг на друга и неплотно скреплены посредством слабых силы Ван дер Ваальса. Это придает графиту мягкость и раскалывание свойства (листы легко скользят друг по другу). Из-за делокализации одного из внешних электронов каждого атома с образованием π-облако, графит проводит электричество, но только в плоскости каждого ковалентно связанный простынь. Это приводит к меньшему объему электрическая проводимость для углерода, чем для большинства металлы. Делокализация также объясняет энергетическую стабильность графита над алмазом при комнатной температуре.

При очень высоких давлениях углерод образует более компактный аллотроп, алмаз, имеющий почти вдвое большую плотность графита. Здесь каждый атом связан тетраэдрически с четырьмя другими, образуя 3-мерную сеть сморщенных шестичленных атомов. У алмаза то же самое кубическая структура в качестве кремний и германий, и из-за прочности углерод-углерод облигации, это самое твердое вещество, встречающееся в природе. устойчивость к царапинам. Вопреки распространенному мнению, что "бриллианты вечны", они термодинамически неустойчивы (Δжграмм° (алмаз, 298 К) = 2,9 кДж / моль[44]) в нормальных условиях (298 К, 105 Па) и преобразовать в графит.[18] Из-за высокого энергетического барьера активации переход в графит при нормальной температуре настолько медленный, что незаметен. Левый нижний угол фазовой диаграммы углерода экспериментально не исследовался. Однако недавнее вычислительное исследование с использованием теория функционала плотности методы пришли к выводу, что как Т → 0 К и п → 0 Па, алмаз становится более стабильный чем графит примерно на 1,1 кДж / моль.[45] В некоторых условиях углерод кристаллизуется в виде лонсдейлит, а шестиугольник кристалл решетка со всеми ковалентно связанными атомами и свойствами, аналогичными свойствам алмаза.[36]
Фуллерены представляют собой синтетические кристаллические образования с графитоподобной структурой, но вместо плоских гексагональные ячейки только некоторые из ячеек, из которых образуются фуллерены, могут быть пятиугольниками, неплоскими шестиугольниками или даже семиугольниками атомов углерода. Таким образом, листы деформируются в сферы, эллипсы или цилиндры. Свойства фуллеренов (разделенных на бакиболлы, бакитрубки и нанопочки) еще не полностью проанализированы и представляют собой интенсивную область исследований в наноматериалы. Имена фуллерен и Buckyball даются после Ричард Бакминстер Фуллер, популяризатор геодезические купола, напоминающие структуру фуллеренов. Букиболлы - это довольно большие молекулы, полностью состоящие из углерода, связанного тригонально, образуя сфероиды (самый известный и простой - футбольный мяч C60 бакминстерфуллерен ).[30] Углеродные нанотрубки (бакитрубки) структурно похожи на бакиболлы, за исключением того, что каждый атом тригонально связан в изогнутом листе, который образует полость. цилиндр.[31][32] Впервые о нанопочках было сообщено в 2007 году, и они представляют собой гибридные материалы Buckytube / Bukyball (Buckyballs ковалентно связаны с внешней стенкой нанотрубки), которые сочетают в себе свойства обоих в единой структуре.[33]

Из других обнаруженных аллотропов углеродная нано пена это ферромагнитный аллотроп, открытый в 1997 году. Он состоит из кластера с низкой плотностью, состоящего из атомов углерода, связанных вместе в рыхлой трехмерной паутине, в которой атомы тригонально связаны в шестичленные и семичленные кольца. Это один из самых легких известных твердых веществ с плотностью около 2 кг / м3.3.[46] По аналогии, стеклоуглерод содержит высокую долю закрытых пористость,[37] но, в отличие от обычного графита, графитовые слои не сложены, как страницы в книге, а имеют более случайное расположение. Линейный ацетиленовый углерод[39] имеет химическую структуру[39] - (C ::: C)п-. Углерод в этой модификации линейен с зр орбитальная гибридизация, и является полимер с чередованием одинарных и тройных связей. Этот карбин представляет значительный интерес для нанотехнологии как его Модуль для младших в 40 раз больше, чем самый твердый из известных материалов - алмаз.[47]
В 2015 году команда Университет штата Северная Каролина объявили о разработке еще одного аллотропа, которого они назвали Q-углерод, создаваемый высокоэнергетическим лазерным импульсом малой длительности на аморфной углеродной пыли. Сообщается, что Q-углерод проявляет ферромагнетизм, флуоресценция и твердость превосходит алмазы.[48]
В паровой фазе часть углерода находится в виде дикарбон (C
2). В возбужденном состоянии этот газ светится зеленым.
Вхождение


Углерод - это четвертый по распространенности химический элемент в наблюдаемая вселенная по массе после водорода, гелия и кислорода. В июле 2020 года астрономы сообщили о том, что углерод образовался в основном в белые карликовые звезды, особенно те, которые больше двух солнечных масс.[49][50] Углерод в большом количестве солнце, звезды, кометы, а в атмосферы из большинства планеты.[51] Немного метеориты содержат микроскопические алмазы, которые образовались, когда Солнечная система все еще был протопланетный диск.[52] Микроскопические алмазы также могут образовываться под действием сильного давления и высокой температуры в местах падения метеоритов.[53]
В 2014 НАСА объявил значительно обновленная база данных для отслеживания полициклические ароматические углеводороды (ПАУ) в вселенная. Более 20% углерода во Вселенной может быть связано с ПАУ, сложными соединениями углерода и водорода без кислорода.[54] Эти соединения фигурируют в Гипотеза мира ПАУ где предполагается, что они играют роль в абиогенез и формирование жизнь. Кажется, что ПАУ образовались «через пару миллиардов лет» после Большой взрыв, широко распространены во Вселенной и связаны с новые звезды и экзопланеты.[51]
Было подсчитано, что в твердой Земле в целом содержится 730 промилле углерода, с 2000 ppm в ядре и 120 ppm в объединенной мантии и коре.[55] Поскольку масса Земли равна 5.972×1024 кг, это будет означать 4360 миллионов гигатонны углерода. Это намного больше, чем количество углерода в океанах или атмосфере (см. Ниже).
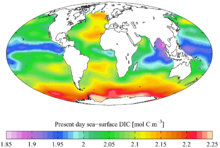
В комбинации с кислород в углекислый газ, углерод содержится в атмосфере Земли (примерно 900 гигатонн углерода - каждая ppm соответствует 2,13 Гт) и растворен во всех водоемах (примерно 36 000 гигатонн углерода). Углерод в биосфера оценивается в 550 гигатонн, но с большой неопределенностью, в основном из-за огромной неопределенности в количестве глубинных земных подповерхностные бактерии.[56] Углеводороды (Такие как каменный уголь, нефть, и натуральный газ ) также содержат углерод. Каменный уголь «резервы» (не «ресурсы») составляют около 900 гигатонн при примерно 18 000 Гт ресурсов.[57] Запасы нефти составляют около 150 гигатонн. Проверенные источники природного газа примерно 175×1012 кубометры (содержащий около 105 гигатонн углерода), но исследования оценивают другое 900×1012 кубометры «нетрадиционных» месторождений, таких как сланцевый газ, что составляет около 540 гигатонн углерода.[58]
Углерод также содержится в гидраты метана в полярных регионах и под морями. По разным оценкам, это количество углерода от 500 до 2500. Gt,[59] или 3000 Гт.[60]
Раньше углеводородов было больше. Согласно одному источнику, в период с 1751 по 2008 год около 347 гигатонн углерода было выброшено в атмосферу в виде двуокиси углерода в результате сжигания ископаемого топлива.[61] Другой источник оценивает количество, добавленное в атмосферу за период с 1750 г., на уровне 879 Гт, а общее количество, поступающее в атмосферу, море и сушу (например, торфяные болота ) почти на 2000 Гт.[62]
Углерод является составной частью (около 12% по массе) очень больших масс карбонат камень (известняк, доломит, мрамор и так далее). Каменный уголь очень богат углеродом (антрацит содержит 92–98%)[63] и является крупнейшим коммерческим источником минерального углерода, составляющим 4 000 гигатонн или 80% ископаемое топливо.[64]
Что касается отдельных углеродных аллотропов, то графит в больших количествах встречается в Соединенные Штаты (в основном в Нью-Йорк и Техас ), Россия, Мексика, Гренландия, и Индия. Природные алмазы встречаются в скале кимберлит, найденный в древних вулканический «шеи» или «трубы». Большинство месторождений алмазов находится в Африка, особенно в Южная Африка, Намибия, Ботсвана, то Республика Конго, и Сьерра-Леоне. Месторождения алмазов также обнаружены в Арканзас, Канада, российский Арктический, Бразилия, а в Северной и Западной Австралия. Сейчас алмазы также добывают со дна океана у мыс Доброй надежды. Алмазы встречаются естественным образом, но в настоящее время производится около 30% всех промышленных алмазов, используемых в США.
Углерод-14 образуется в верхних слоях тропосферы и стратосферы на высотах 9–15 км в результате реакции, вызываемой космические лучи.[65] Тепловые нейтроны образуются, которые сталкиваются с ядрами азота-14, образуя углерод-14 и протон. В качестве таких, 1.5%×10−10 атмосферного углекислого газа содержит углерод-14.[66]
Астероиды, богатые углеродом, относительно преобладают во внешних частях Земли. пояс астероидов в нашем Солнечная система. Ученые еще не исследовали образцы этих астероидов. Астероиды можно использовать в гипотетических космическая добыча углерода, что может быть возможно в будущем, но в настоящее время технологически невозможно.[67]
Изотопы
Изотопы углерода атомные ядра которые содержат шесть протоны плюс ряд нейтроны (варьируется от 2 до 16). Углерод имеет два стабильных, встречающихся в природе изотопы.[15] Изотоп углерод-12 (12C) образует 98,93% углерода на Земле, а углерод-13 (13C) составляет оставшиеся 1,07%.[15] Концентрация 12C дополнительно увеличивается в биологических материалах, потому что биохимические реакции дискриминируют 13С.[68] В 1961 г. Международный союз теоретической и прикладной химии (ИЮПАК) принял изотоп углерод-12 в качестве основы для атомные веса.[69] Идентификация углерода в ядерный магнитный резонанс (ЯМР) эксперименты проводятся с изотопом 13С.
Углерод-14 (14C) является естественным радиоизотоп, созданный в верхняя атмосфера (ниже стратосфера и верхний тропосфера ) путем взаимодействия азот с космические лучи.[70] На Земле он содержится в следовых количествах - 1 часть на триллион (0,0000000001%) или более, в основном ограниченные атмосферой и поверхностными отложениями, особенно торф и другие органические материалы.[71] Этот изотоп распадается на 0,158 МэВ. β− выброс. Из-за относительно короткого период полураспада 5730 лет, 14C в древних породах практически отсутствует. Количество 14C в атмосфера и у живых организмов почти постоянна, но предсказуемо уменьшается в их телах после смерти. Этот принцип используется в радиоуглеродное датирование, изобретенный в 1949 году, который широко использовался для определения возраста углеродистых материалов с возрастом примерно до 40 000 лет.[72][73]
Известно 15 изотопов углерода, и самый короткоживущий из них - 8C, который распадается на испускание протона и альфа-распад и имеет период полураспада 1,98739 × 10−21 с.[74] Экзотика 19C демонстрирует ядерный ореол, что означает его радиус заметно больше, чем можно было бы ожидать, если бы ядро были сфера постоянного плотность.[75]
Формирование в звездах
Формирование атомного ядра углерода происходит в пределах гигант или же сверхгигант звезда через тройной альфа-процесс. Это требует почти одновременного столкновения трех альфа-частицы (гелий ядер), как продукты дальнейшего термоядерная реакция реакции гелия с водородом или другим ядром гелия производят литий-5 и бериллий-8 соответственно, оба очень нестабильны и почти мгновенно распадаются обратно на более мелкие ядра.[76] Тройной альфа-процесс происходит в условиях температур выше 100 мегакельвинов и концентрации гелия, которые запрещались быстрым расширением и охлаждением ранней Вселенной, и поэтому во время существования не образовывалось никакого значительного углерода. Большой взрыв.
Согласно современной теории физической космологии, углерод образуется внутри звезд на горизонтальная ветвь.[77] Когда массивные звезды умирают как сверхновые, углерод рассеивается в космос в виде пыли. Эта пыль становится составным материалом для образования звезда следующего поколения системы с аккрецированными планетами.[51][78] В Солнечная система это одна из таких звездных систем с изобилием углерода, обеспечивающая существование жизни в том виде, в каком мы ее знаем.
В Цикл CNO является дополнительным механизмом синтеза водорода, который приводит в действие звезды, в котором углерод действует как катализатор.
Вращательные переходы различных изотопных форм оксида углерода (например, 12CO, 13CO и 18CO) обнаруживаются в субмиллиметр диапазон длин волн, и используются при изучении новые звезды в молекулярные облака.[79]
Цикл углерода
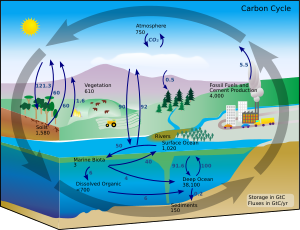
В земных условиях превращение одного элемента в другой происходит очень редко. Следовательно, количество углерода на Земле практически постоянно. Таким образом, процессы, в которых используется углерод, должны получать его откуда-то и где-то утилизировать. Пути углерода в окружающей среде образуют цикл углерода. Например, фотосинтетический растения рисуют углекислый газ из атмосферы (или морской воды) и превратить его в биомассу, как в Цикл Кальвина, процесс фиксация углерода. Часть этой биомассы поедается животными, а часть углерода выделяется животными в виде двуокиси углерода. Углеродный цикл значительно сложнее, чем этот короткий цикл; например, углекислый газ растворяется в океанах; если бактерии не потребляют его, мертвые растения или животные могут стать нефть или же каменный уголь, который выделяет углерод при горении.[80][81]
Соединения
Органические соединения


Углерод может образовывать очень длинные цепочки взаимосвязанных углерод-углеродные связи, свойство, которое называется цепочка. Связи углерод-углерод прочные и стабильные. За счет катенации углерод образует бесчисленное множество соединений. Подсчет уникальных соединений показывает, что углерод содержат больше, чем не содержат.[82] То же самое можно сказать и о водороде, поскольку большинство органических соединений содержат водород, химически связанный с углеродом или другим обычным элементом, таким как кислород или азот.
Простейшая форма органической молекулы - это углеводород - большая семья Органические молекулы которые состоят из водород атомы, связанные с цепочкой атомов углерода. Углеводородный каркас может быть замещен другими атомами, известными как гетероатомы. Обычные гетероатомы, которые встречаются в органических соединениях, включают кислород, азот, серу, фосфор и нерадиоактивные галогены, а также металлы литий и магний. Органические соединения, содержащие связи с металлом, известны как металлоорганические соединения (Смотри ниже). Определенные группы атомов, часто включающие гетероатомы, повторяются в большом количестве органических соединений. Эти коллекции, известные как функциональные группы, дают общие образцы реакционной способности и позволяют систематическое изучение и категоризацию органических соединений. Длина цепи, форма и функциональные группы влияют на свойства органических молекул.
В большинстве стабильных соединений углерода (и почти во всех стабильных органический соединений) углерод подчиняется Правило октета и является четырехвалентный, что означает, что атом углерода образует в общей сложности четыре ковалентных связи (которые могут включать двойные и тройные связи). Исключения составляют небольшое количество стабилизированных карбокатионы (три связи, положительный заряд), радикалы (три облигации, нейтральный), карбанионы (три связи, отрицательный заряд) и карбены (две связи, нейтральный), хотя эти виды гораздо чаще встречаются как нестабильные реакционноспособные промежуточные соединения.
Углерод встречается во всех известных органический жизнь и это основа органическая химия. При объединении с водород, он образует различные углеводороды, которые важны для промышленности, так как хладагенты, смазочные материалы, растворители, как химическое сырье для производства пластмассы и нефтехимия, и, как ископаемое топливо.
В сочетании с кислородом и водородом углерод может образовывать множество групп важных биологических соединений, включая сахара, лигнаны, хитины, спирты, жиры и ароматный сложные эфиры, каротиноиды и терпены. С азот это формирует алкалоиды, а с добавлением серы также образует антибиотики, аминокислоты, и резинка товары. С добавлением фосфора к этим другим элементам он образует ДНК и РНК, носители химического кода жизни, и аденозинтрифосфат (АТФ), важнейшая молекула-переносчик энергии во всех живых клетках.
Неорганические соединения
Обычно углеродсодержащие соединения, которые связаны с минералами или которые не содержат связей с другими атомами углерода, галогенами или водородом, рассматриваются отдельно от классических органические соединения; определение не является жестким, и классификация некоторых соединений может варьироваться от автора к автору (см. справочные статьи выше). Среди них простые оксиды углерода. Наиболее заметный оксид - это углекислый газ (CO
2). Когда-то это была основная составляющая палеоатмосфера, но является второстепенным компонентом Атмосфера Земли сегодня.[83] Растворено в воды, это образует угольная кислота (ЧАС
2CO
3), но, как и большинство соединений с несколькими атомами кислорода с одинарными связями на одном атоме углерода, он нестабилен.[84] Однако через этот промежуточный стабилизированный резонанс карбонат ионы производятся. Некоторые важные минералы - карбонаты, особенно кальцит. Сероуглерод (CS
2) похож.[23] Тем не менее, из-за своих физических свойств и связи с органическим синтезом сероуглерод иногда классифицируется как органический растворитель.
Другой распространенный оксид - это монооксид углерода (CO). Он образуется при неполном сгорании и представляет собой бесцветный газ без запаха. Каждая молекула содержит тройную связь и достаточно полярный, что приводит к тенденции к постоянному связыванию с молекулами гемоглобина, вытесняя кислород, который имеет более низкое сродство связывания.[85][86] Цианид (CN−), имеет аналогичную структуру, но ведет себя как галогенид ион (псевдогалоген ). Например, он может образовывать нитрид циан молекула ((CN)2), аналогично двухатомным галогенидам. Аналогично, более тяжелый аналог цианида, циафид (CP−), также считается неорганическим, хотя большинство простых производных крайне нестабильны. Другие необычные оксиды: недокись углерода (C
3О
2),[87] нестабильный монооксид дикарбона (C2O),[88][89] триоксид углерода (CO3),[90][91] циклопентанепентон (C5О5),[92] циклогексангексон (C6О6),[92] и меллитовый ангидрид (C12О9). Однако ангидрид меллитовой кислоты представляет собой тройной ацильный ангидрид меллитовой кислоты; кроме того, он содержит бензольное кольцо. Таким образом, многие химики считают его органическим.
С реактивным металлы, Такие как вольфрам, углерод образует либо карбиды (C4−) или же ацетилиды (C2−
2) с образованием сплавов с высокими температурами плавления. Эти анионы также связаны с метан и ацетилен, оба очень слабые кислоты. При электроотрицательности 2,5[93] углерод предпочитает образовывать ковалентные связи. Некоторые карбиды представляют собой ковалентные решетки, например карборунд (SiC), напоминающий алмаз. Тем не менее даже самые полярные и солеподобные карбиды не являются полностью ионными соединениями.[94]
Металлоорганические соединения
Металлоорганические соединения по определению содержат по крайней мере одну ковалентную связь углерод-металл. Существует широкий спектр таких соединений; основные классы включают простые соединения алкил-металлов (например, тетраэтилсвинец ), η2-алкеновые соединения (например, Соль Цейзе ) и η3-аллильные соединения (например, димер хлорида аллилпалладия ); металлоцены содержащие циклопентадиенильные лиганды (например, ферроцен ); и карбеновые комплексы переходных металлов. Много карбонилы металлов и цианиды металлов существуют (например, тетракарбонилникель и феррицианид калия ); Некоторые исследователи считают карбонильные и цианидные комплексы металлов без других углеродных лигандов чисто неорганическими, а не металлоорганическими. Однако большинство металлоорганических химиков считают, что комплексы металлов с любым углеродным лигандом, даже с «неорганическим углеродом» (например, карбонилы, цианиды и определенные типы карбидов и ацетилидов), имеют металлоорганическую природу. Комплексы металлов, содержащие органические лиганды без ковалентной связи углерод-металл (например, карбоксилаты металлов), называются металлоорганический соединения.
Хотя понятно, что углерод сильно предпочитает образование четырех ковалентных связей, известны и другие экзотические схемы связывания. Карбораны являются высокостабильными додекаэдрическими производными [B12ЧАС12]2- блок, с заменой одной BH на CH+. Таким образом, углерод связан с пятью атомами бора и одним атомом водорода. Катион [(Ph3PAu)6C]2+ содержит октаэдрический углерод, связанный с шестью фосфин-золотыми фрагментами. Это явление было объяснено аурофильность золотых лигандов, которые обеспечивают дополнительную стабилизацию в остальном лабильных видов.[95] В природе кофактор железо-молибден (FeMoco ) отвечает за микробный азотфиксация аналогично имеет октаэдрический углеродный центр (формально карбид C (-IV)), связанный с шестью атомами железа. В 2016 году было подтверждено, что в соответствии с более ранними теоретическими прогнозами гексаметилбензол дикатион содержит атом углерода с шестью связями. Более конкретно, дикатион можно описать структурно формулой [MeC (η5-C5Мне5)]2+, что делает его "органическим металлоцен "в котором MeC3+ фрагмент связан с η5-C5Мне5− фрагмент через все пять атомов углерода кольца.[96]
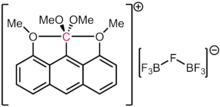
Важно отметить, что в описанных выше случаях каждая из связей с углеродом содержит менее двух формальных электронных пар. Таким образом, формальное число электронов этих разновидностей не превышает октета. Это делает их гиперкоординированными, но не гипервалентными. Даже в случаях предполагаемых разновидностей 10-C-5 (то есть углерода с пятью лигандами и формальным числом электронов десять), как сообщили Акиба и его сотрудники,[97] расчеты электронной структуры показывают, что электронная популяция вокруг углерода все еще меньше восьми, как и в других соединениях, содержащих четыре электрона. трехцентровое соединение.
История и этимология

В английский имя углерод исходит из латинский карбо для угля и древесного угля,[98] откуда также приходит Французский Charbon, что означает уголь. В Немецкий, нидерландский язык и Датский, названия углерода Коленстофф, Koolstof и Кульстоф соответственно все буквально означают каменный уголь -вещество.
Углерод был открыт в доисторические времена и был известен в форме сажа и уголь к самому раннему человек цивилизации. Алмазы были известны, вероятно, еще в 2500 г. до н.э. в Китае, а углерод в виде уголь был сделан во времена Римской империи той же химией, что и сегодня, путем нагрева древесины в пирамида покрыт глина исключить воздух.[99][100]
В 1722 г. Рене Антуан Фершо де Реомюр продемонстрировали, что железо превратилось в сталь в результате поглощения некоторого вещества, теперь известного как углерод.[101] В 1772 г. Антуан Лавуазье показал, что алмазы представляют собой форму углерода; когда он сжег образцы древесного угля и алмаза и обнаружил, что ни один из них не дает воды, и что оба выделяют одинаковое количество углекислый газ на грамм В 1779 г.[102] Карл Вильгельм Шееле показал, что графит, который считался формой вести, вместо этого был идентичен древесному углю, но с небольшой примесью железа, и что он давал «воздушную кислоту» (его название диоксида углерода) при окислении азотной кислотой.[103] В 1786 году французские ученые Клод Луи Бертолле, Гаспар Монж и К.А. Вандермонде подтвердили, что графит в основном состоит из углерода, окислив его кислородом почти так же, как Лавуазье поступил с алмазом.[104] Снова осталось немного железа, которое, по мнению французских ученых, было необходимо для структуры графита. В своей публикации они предложили название карбона (Латинский карбонум) для элемента в графите, который выделялся в виде газа при горении графита. Затем Антуан Лавуазье назвал углерод элемент в его учебнике 1789 г.[105]
Новый аллотроп углерода, фуллерен, который был открыт в 1985 г.[106] включает наноструктурированный формы, такие как Bukyballs и нанотрубки.[30] Их первооткрыватели - Роберт Керл, Гарольд Крото и Ричард Смолли - получил Нобелевская премия по химии в 1996 году.[107] Возобновившийся интерес к новым формам привел к открытию новых экзотических аллотропов, в том числе стеклоуглерод, и осознание того, что "аморфный углерод "не совсем аморфный.[37]
Производство
Графитовый
Коммерчески жизнеспособные природные месторождения графита встречаются во многих частях мира, но наиболее важные с экономической точки зрения источники находятся в Китай, Индия, Бразилия и Северная Корея. Графитовые месторождения имеют метаморфический происхождение, найдено в связи с кварц, слюда и полевые шпаты в сланцах, гнейсы и метаморфизируется песчаники и известняк в качестве линзы или же вены, иногда толщиной в метр и более. Месторождения графита в Borrowdale, Камберленд, Англия поначалу были достаточно большими и чистыми, чтобы до 19 века карандаши были сделаны просто путем распиливания блоков натурального графита на полосы перед тем, как обернуть полосы деревом. Сегодня меньшие месторождения графита получают путем дробления материнской породы и плавания более легкого графита на воде.[108]
Существует три типа природного графита: аморфный, чешуйчатый или кристаллический, а также жильный или комковый. Аморфный графит самого низкого качества и наиболее распространен. Вопреки науке, в промышленности термин «аморфный» относится к кристаллам очень маленького размера, а не к полному отсутствию кристаллической структуры. Аморфный графит используется для изделий из более дешевого графита, и это графит с самой низкой ценой. Крупные месторождения аморфного графита находятся в Китае, Европе, Мексике и США. Чешуйчатый графит встречается реже и более высокого качества, чем аморфный; это происходит в виде отдельных пластин, кристаллизовавшихся в метаморфической породе. Чешуйчатый графит может быть в четыре раза дороже аморфного. Хлопья хорошего качества можно переработать в расширяемый графит для многих целей, таких как антипирены. Самые передовые месторождения находятся в Австрии, Бразилии, Канаде, Китае, Германии и Мадагаскаре. Жилковый или кусковой графит - самый редкий, самый ценный и высококачественный вид природного графита. Он встречается в жилах вдоль интрузивных контактов в твердых глыбах, и его промышленная добыча ведется только в Шри-Ланке.[108]
Согласно USGS мировое производство природного графита в 2010 году составило 1,1 миллиона тонн, из которых Китай дал 800 000 тонн, Индия - 130 000 тонн, Бразилия - 76 000 тонн, Северная Корея - 30 000 тонн и Канада - 25 000 тонн. В Соединенных Штатах не сообщалось о добыче природного графита, но в 2009 году было произведено 118 000 т синтетического графита с оценочной стоимостью 998 миллионов долларов.[108]
Алмаз

Цепочка поставок алмазов контролируется ограниченным числом влиятельных предприятий, а также очень сконцентрирована в небольшом количестве мест по всему миру (см. Рисунок).
Только очень небольшая часть алмазной руды состоит из настоящих алмазов. Руда дробится, при этом необходимо соблюдать осторожность, чтобы предотвратить разрушение более крупных алмазов в этом процессе, а затем частицы сортируются по плотности. Сегодня алмазы располагаются в богатой алмазами фракции плотности с помощью Рентгеновская флуоресценция, после чего вручную выполняются заключительные этапы сортировки. Перед использованием Рентгеновские лучи стало обычным явлением, разделение производилось при помощи смазочных лент; алмазы имеют более сильную тенденцию к прилипанию жира, чем другие минералы в руде.[109]
Исторически известно, что алмазы находили только в аллювиальных отложениях в южная Индия.[110] Индия стала мировым лидером в производстве алмазов с момента их открытия примерно в 9 веке до нашей эры.[111] до середины 18 века нашей эры, но коммерческий потенциал этих источников был исчерпан к концу 18 века, и тогда Индию затмила Бразилия, где в 1725 году были обнаружены первые неиндийские алмазы.[112]
Добыча алмазов на первичных месторождениях (кимберлиты и лампроиты) началась только в 1870-х годах после открытия алмазных полей в Южной Африке. С течением времени добыча росла, и с тех пор было добыто в общей сложности 4,5 миллиарда каратов.[113] Около 20% от этого количества было добыто только за последние 5 лет, а за последние десять лет 9 новых рудников начали добычу, а еще 4 ждут своего открытия в ближайшее время. Большинство из этих шахт расположены в Канаде, Зимбабве, Анголе и одна в России.[113]
В Соединенных Штатах алмазы были найдены в Арканзас, Колорадо и Монтана.[114][115] В 2004 году в США было обнаружено поразительное открытие микроскопического алмаза.[116] привело к оптовой выборке в январе 2008 г. кимберлитовые трубки в отдаленной части Монтана.[117]
Сегодня наиболее коммерчески рентабельные месторождения алмазов находятся в Россия, Ботсвана, Австралия и Демократическая Республика Конго.[118] В 2005 году Россия произвела почти пятую часть мировой добычи алмазов, сообщает Британская геологическая служба. В Австралии самая богатая диамантифицированная труба, пиковая добыча которой достигла 42 метрических тонн (41 длинная тонна; 46 коротких тонн) в год в 1990-х годах.[114] Также в районе активно ведется разработка коммерческих месторождений. Северо-западные территории из Канада, Сибирь (в основном в Территория Якутии; Например, Трубка Мир и Трубка Удачная ), Бразилии, а также в Северной и Западной Австралия.
Приложения




Углерод необходим для всех известных живых систем, и без него жизнь, как мы ее знаем, не могла бы существовать (см. альтернативная биохимия ). Основное экономическое использование углерода, помимо продуктов питания и древесины, находится в форме углеводородов, в первую очередь ископаемое топливо метан газ и сырая нефть (нефть). Сырая нефть является дистиллированный в нефтеперерабатывающие заводы посредством нефтехимическая промышленность производить бензин, керосин, и другие продукты. Целлюлоза представляет собой природный углеродсодержащий полимер, производимый растениями в виде дерево, хлопок, шерсть, и конопля. Целлюлоза используется в основном для поддержания структуры растений. Коммерчески ценные углеродные полимеры животного происхождения включают: шерсть, кашемир и шелк. Пластмассы сделаны из синтетических углеродных полимеров, часто с атомами кислорода и азота, включенными через равные промежутки в основную полимерную цепь. Сырьем для многих из этих синтетических веществ является сырая нефть.
Использование углерода и его соединений чрезвычайно разнообразно. Он может образовывать сплавы с утюг, из которых наиболее распространенным является углеродистая сталь. Графитовый сочетается с глины чтобы сформировать «свинец», используемый в карандаши используется для письмо и Рисование. Он также используется как смазка и пигмент, как формовочный материал в стекло производство, в электроды для сухой батареи И в гальваника и гальванопластика, в кисти за электродвигатели и как замедлитель нейтронов в ядерные реакторы.
Уголь используется как материал для рисования в произведение искусства, барбекю гриль, выплавка чугуна, и во многих других приложениях. Древесина, уголь и нефть используются как топливо для производства энергии и обогрев. Качество драгоценных камней алмаз используется в ювелирных изделиях, и промышленные алмазы используются в сверлильных, режущих и полировальных инструментах для обработки металлов и камня. Пластмассы сделаны из ископаемых углеводородов, и углеродное волокно, сделан пиролиз синтетических полиэстер волокна используется для армирования пластмасс, чтобы сформировать современные, легкие композитные материалы.
Углеродное волокно производится пиролизом экструдированных и вытянутых нитей полиакрилонитрил (ПАН) и другие органические вещества. Кристаллографическая структура и механические свойства волокна зависят от типа исходного материала и от последующей обработки. Углеродные волокна, изготовленные из ПАН, имеют структуру, напоминающую узкие нити графита, но термическая обработка может переупорядочить структуру в непрерывный прокатанный лист. Результат - волокна с более высокой удельная прочность на разрыв чем сталь.[119]
Черный карбон используется как черный пигмент в печать чернила, масляные краски художника и акварель, копировальная бумага, автомобильная отделка, Тушь и лазерный принтер тонер. Черный карбон также используется как наполнитель в резинка такие продукты, как шины и в пластик соединения. Активированный уголь используется как абсорбент и адсорбент в фильтр материал в таких разнообразных приложениях, как противогазы, очистка воды, и кухня вытяжки, а в медицине - впитывать токсины, яды или газы из пищеварительная система. Углерод используется в химическое восстановление при высоких температурах. Кокс используется для восстановления железной руды в железо (плавка). Поверхностное упрочнение из стали достигается нагревом готовых стальных деталей в углеродном порошке. Карбиды из кремний, вольфрам, бор и титан, являются одними из самых твердых известных материалов и используются в качестве абразивы в режущих и шлифовальных инструментах. Углеродные соединения составляют большинство материалов, используемых в одежде, таких как натуральные и синтетические. текстиль и натуральная кожа, и почти все внутренние поверхности в застроенная среда кроме стекла, камня и металла.
Бриллианты
В алмаз промышленность делится на две категории: одна связана с бриллиантами ювелирного качества, а другая - с алмазами промышленного качества. Хотя существует большая торговля обоими типами алмазов, эти два рынка функционируют совершенно по-разному.
В отличие от драгоценные металлы Такие как золото или же платина, драгоценные бриллианты не торгуются как товар: при продаже алмазов существует значительная наценка, а рынок перепродажи алмазов не очень активен.
Промышленные алмазы ценятся в основном за их твердость и теплопроводность, при этом геммологические качества чистоты и цвета в основном не имеют значения. Около 80% добываемых алмазов (около 100 миллионов каратов или 20 тонн в год) непригодны для использования, поскольку драгоценные камни предназначены для промышленного использования (известные как борт ).[120] синтетические бриллианты изобретенный в 1950-х годах, практически сразу нашел промышленное применение; 3 миллиарда карат (600тонны ) синтетического алмаза производится ежегодно.[121]
Доминирующее промышленное использование алмаза - это резка, сверление, шлифовка и полировка. Большинство этих приложений не требуют больших алмазов; Фактически, большинство алмазов ювелирного качества, за исключением их небольшого размера, могут использоваться в промышленных масштабах. Алмазы встраивают в наконечники сверл или пильные диски или измельчают в порошок для использования при шлифовании и полировке.[122] Специализированные применения включают использование в лабораториях в качестве локализации для эксперименты под высоким давлением (видеть ячейка с алмазной наковальней ), высокая производительность подшипники, и ограниченное использование в специализированных окна.[123][124] С постоянным прогрессом в производстве синтетических алмазов становятся возможными новые применения. Большой интерес вызывает возможное использование алмаза в качестве полупроводник подходит для микрочипы, и из-за его исключительной теплопроводности, как радиатор в электроника.[125]
Меры предосторожности

Чистый углерод имеет чрезвычайно низкий токсичность людям, и с ними можно безопасно обращаться в виде графита или древесного угля. Он устойчив к растворению или химическому воздействию, даже в кислой среде пищеварительного тракта. Следовательно, как только он попадает в ткани тела, он может оставаться там неопределенно долго. Черный карбон вероятно был одним из первых пигментов, которые использовались для татуировка, и Эци-ледяной человек Было обнаружено, что у него были углеродные татуировки, которые сохранились при его жизни и в течение 5200 лет после его смерти.[126] Вдыхание угольной пыли или сажи (технического углерода) в больших количествах может быть опасным, поскольку раздражает ткани легких и вызывает застойные явления. легкое болезнь, пневмокониоз угольщиков. Алмазная пыль, используемая в качестве абразива, может причинить вред при проглатывании или вдыхании. Микрочастицы углерода образуются в выхлопных газах дизельных двигателей и могут накапливаться в легких.[127] В этих примерах вред может быть вызван загрязнителями (например, органическими химическими веществами, тяжелыми металлами), а не самим углеродом.
Углерод обычно имеет низкую токсичность для жизнь на Земле; но наночастицы углерода смертельны для Дрозофила.[128]
Углерод может сильно и ярко гореть в присутствии воздуха при высоких температурах. Большие скопления угля, которые оставались инертными в течение сотен миллионов лет в отсутствие кислорода, могут самовозгорание при контакте с воздухом в свалках угольных шахт, грузовых трюмах судов и угольных бункерах,[129][130] и свалки хранилищ.
В ядерные приложения где графит используется как замедлитель нейтронов, накопление Энергия Вигнера с последующим внезапным самопроизвольным высвобождением. Отжиг до 250 ° C может безопасно выделять энергию, хотя в Уиндскейл огонь процедура пошла не так, что привело к возгоранию других материалов реактора.
Большое разнообразие углеродных соединений включает такие смертельные яды, как тетродотоксин, то лектин рицин из семян касторовое масло Ricinus communis, цианид (CN−), и монооксид углерода; и такие необходимые для жизни, как глюкоза и белок.
Смотрите также
Рекомендации
- ^ Лиде, Д. Р., изд. (2005). CRC Справочник по химии и физике (86-е изд.). Бока-Ратон (Флорида): CRC Press. ISBN 0-8493-0486-5.
- ^ а б Хааланд, Д. (1976). «Давление тройной точки графит-жидкость-пар и плотность жидкого углерода». Углерод. 14 (6): 357–361. Дои:10.1016/0008-6223(76)90010-5.
- ^ а б Савватимский А (2005). «Измерения температуры плавления графита и свойств жидкого углерода (обзор за 1963–2003 гг.)». Углерод. 43 (6): 1115–1142. Дои:10.1016 / j.carbon.2004.12.027.
- ^ "Спектроскопия преобразования Фурье электронного перехода свободнорадикала CCI, охлаждаемого струей" (PDF). Получено 2007-12-06.
- ^ "Спектроскопия с преобразованием Фурье системы КП" (PDF). Получено 2007-12-06.
- ^ «Углерод: бинарные соединения». Получено 2007-12-06.
- ^ а б c d е Свойства алмаза, База данных Института Иоффе
- ^ «Свойства материалов - разные материалы». www.nde-ed.org. Получено 12 ноября 2016.
- ^ Магнитная восприимчивость элементов и неорганических соединений, в Справочнике по химии и физике, 81-е издание, CRC press.
- ^ Weast, Роберт (1984). CRC, Справочник по химии и физике. Бока-Ратон, Флорида: Издательство Chemical Rubber Company. стр. E110. ISBN 978-0-8493-0464-4.
- ^ «История углерода и углеродных материалов - Центр прикладных исследований в области энергетики - Университет Кентукки». Caer.uky.edu. Получено 2008-09-12.
- ^ Сенез, Фред (9 сентября 2000 г.). "Кто открыл углерод?". Государственный университет Фростбурга. Получено 2007-11-24.
- ^ «Углерод | Факты, использование и свойства». Энциклопедия Британника. В архиве из оригинала от 24.10.2017.
- ^ "углерод". Энциклопедия Британика.
- ^ а б c «Углерод - изотопы природного происхождения». Периодическая таблица WebElements. В архиве из оригинала 2008-09-08. Получено 2008-10-09.
- ^ «История углерода». Архивировано из оригинал на 2012-11-01. Получено 2013-01-10.
- ^ Рис, Джейн Б. (31 октября 2013 г.). Кэмпбелл Биология (10-е изд.). Пирсон. ISBN 9780321775658.
- ^ а б «Мир углерода - интерактивная нановизулизация в науке и инженерном образовании (IN-VSEE)». Архивировано из оригинал на 2001-05-31. Получено 2008-10-09.
- ^ а б Химические операции (15 декабря 2003 г.). «Карбон». Лос-Аламосская национальная лаборатория. Архивировано из оригинал на 2008-09-13. Получено 2008-10-09.
- ^ Деминг, Анна (2010). "Король стихий?". Нанотехнологии. 21 (30): 300201. Bibcode:2010Нанот..21D0201D. Дои:10.1088/0957-4484/21/30/300201. PMID 20664156.
- ^ Гринвилл Уиттакер, А. (1978). «Спорная тройная точка углерода твердое тело-жидкость-пар». Природа. 276 (5689): 695–696. Bibcode:1978Натура 276..695Вт. Дои:10.1038 / 276695a0. S2CID 4362313.
- ^ Зазула, Дж. М. (1997). «О превращениях графита при высоких температурах и давлении, вызванных поглощением пучка LHC» (PDF). ЦЕРН. В архиве (PDF) из оригинала от 25.03.2009. Получено 2009-06-06.
- ^ а б Гринвуд и Эрншоу, стр. 289–292.
- ^ Гринвуд и Эрншоу, стр. 276–8.
- ^ Ирифуне, Тецуо; Курио, Аяко; Сакамото, Сидзуэ; Иноуэ, Тору; Сумия, Хитоши (2003). «Материалы: сверхтвердый поликристаллический алмаз из графита». Природа. 421 (6923): 599–600. Bibcode:2003Натура.421..599I. Дои:10.1038 / 421599b. PMID 12571587. S2CID 52856300.
- ^ Динвибель, Мартин; Верховен, Гертян; Прадип, Намбудири; Френкен, Йост; Хаймберг, Дженнифер; Зандберген, Хенни (2004). «Сверхсмазывающая способность графита» (PDF). Письма с физическими проверками. 92 (12): 126101. Bibcode:2004ПхРвЛ..92л6101Д. Дои:10.1103 / PhysRevLett.92.126101. PMID 15089689. В архиве (PDF) из оригинала от 17.09.2011.
- ^ Deprez, N .; Маклахан, Д. С. (1988). «Анализ электропроводности графита, электропроводность графитовых порошков при прессовании». Журнал физики D: Прикладная физика. 21 (1): 101–107. Bibcode:1988JPhD ... 21..101D. Дои:10.1088/0022-3727/21/1/015.
- ^ Коллинз, А. Т. (1993). «Оптические и электронные свойства полупроводникового алмаза». Философские труды Королевского общества A. 342 (1664): 233–244. Bibcode:1993RSPTA.342..233C. Дои:10.1098 / Рста.1993.0017. S2CID 202574625.
- ^ Делэйс, П. (2001). Графит и прекурсоры. CRC Press. ISBN 978-90-5699-228-6.
- ^ а б c Анвин, Питер. «Фуллерены (обзор)». В архиве из оригинала 2007-12-01. Получено 2007-12-08.
- ^ а б Ebbesen, T. W., ed. (1997). Углеродные нанотрубки - получение и свойства. Бока-Ратон, Флорида: CRC Press. ISBN 978-0-8493-9602-1.
- ^ а б Dresselhaus, M. S .; Dresselhaus, G .; Avouris, Ph., Eds. (2001). Углеродные нанотрубки: синтез, структуры, свойства и применение. Темы прикладной физики. 80. Берлин. ISBN 978-3-540-41086-7.
- ^ а б Насибулин, Альберт Г .; Пихица, П. В .; Jiang, H .; Браун, Д. П .; Крашенинников, А. В .; Анисимов, А. С .; Queipo, P .; Moisala, A .; и другие. (2007). «Новый гибридный углеродный материал». Природа Нанотехнологии. 2 (3): 156–161. Bibcode:2007НатНа ... 2..156Н. Дои:10.1038 / nnano.2007.37. PMID 18654245. S2CID 6447122.
- ^ Насибулин, А .; Анисимов, Антон С .; Пихица, Петр В .; Цзян, Хуа; Браун, Дэвид П .; Чой, Мансу; Кауппинен, Эско И. (2007). «Исследования формирования NanoBud». Письма по химической физике. 446 (1): 109–114. Bibcode:2007CPL ... 446..109N. Дои:10.1016 / j.cplett.2007.08.050.
- ^ Vieira, R; Леду, Марк-Жак; Фам-Хуу, Куонг (2004). «Синтез и характеристика углеродных нановолокон с макроскопической формой, образованных каталитическим разложением C2ЧАС6/ЧАС2 над никелевым катализатором ». Прикладной катализ A: Общие. 274 (1–2): 1–8. Дои:10.1016 / j.apcata.2004.04.008.
- ^ а б Клиффорд, Фрондел; Марвин, Урсула Б. (1967). «Лонсдейлит, новый гексагональный полиморф алмаза». Природа. 214 (5088): 587–589. Bibcode:1967Натура.214..587F. Дои:10.1038 / 214587a0. S2CID 4184812.
- ^ а б c Харрис, PJF (2004). «Фуллереновая структура товарных стеклоуглеродов» (PDF). Философский журнал. 84 (29): 3159–3167. Bibcode:2004PMag ... 84.3159H. CiteSeerX 10.1.1.359.5715. Дои:10.1080/14786430410001720363. Архивировано из оригинал (PDF) на 2012-03-19. Получено 2011-07-06.
- ^ Роде, А. В .; Hyde, S.T .; Gamaly, E. G .; Elliman, R.G .; McKenzie, D. R .; Балкок, С. (1999). «Структурный анализ углеродной пены, образованной лазерной абляцией с высокой частотой импульсов». Прикладная физика A: Материаловедение и обработка материалов. 69 (7): S755 – S758. Bibcode:1999АпФА..69С.755Р. Дои:10.1007 / s003390051522. S2CID 96050247.
- ^ а б c Хайманн, Роберт Бертрам; Евсюков, Сергей Э. и Каван, Ладислав (28 февраля 1999 г.). Карбиновые и карбиноидные структуры. Springer. стр. 1–. ISBN 978-0-7923-5323-2. В архиве из оригинала 23 ноября 2012 г.. Получено 2011-06-06.
- ^ Lee, C .; Wei, X .; Kysar, J. W .; Хоун, Дж. (2008). «Измерение упругих свойств и внутренней прочности однослойного графена». Наука. 321 (5887): 385–8. Bibcode:2008Sci ... 321..385L. Дои:10.1126 / science.1157996. PMID 18635798. S2CID 206512830. Сложить резюме.
- ^ Сандерсон, Билл (25 августа 2008 г.). «Самое сложное, что известно человеку: открытие открывает дверь в космический лифт». nypost.com. В архиве из оригинала от 06.09.2008. Получено 2008-10-09.
- ^ Цзинь, Чжун; Лу, Вэй; О'Нил, Кевин Дж .; Parilla, Philip A .; Симпсон, Лин Дж .; Киттрелл, Картер; Тур, Джеймс М. (22 февраля 2011 г.). «Наноинженерное пространство в графеновых листах для хранения водорода». Химия материалов. 23 (4): 923–925. Дои:10,1021 / см 10 25 188. ISSN 0897-4756.
- ^ Дженкинс, Эдгар (1973). Полиморфизм элементов и соединений. Тейлор и Фрэнсис. п. 30. ISBN 978-0-423-87500-3. В архиве из оригинала от 23.11.2012. Получено 2011-05-01.
- ^ Россини, Ф. Д .; Джессап, Р. С. (1938). «Тепло и свободная энергия образования диоксида углерода и перехода между графитом и алмазом». Журнал исследований Национального бюро стандартов. 21 (4): 491. Дои:10.6028 / jres.021.028.
- ^ Грохала, Войцех (01.04.2014). «Алмаз: основное электронное состояние углерода при температурах, приближающихся к 0 К». Angewandte Chemie International Edition. 53 (14): 3680–3683. Дои:10.1002 / anie.201400131. ISSN 1521-3773. PMID 24615828. S2CID 13359849.
- ^ Шеве, Фил и Штейн, Бен (26 марта 2004 г.). «Углеродная нано-пена - первый в мире чистый углеродный магнит». Новости физики. 678 (1). В архиве из оригинала 7 марта 2012 г.
- ^ Ицхаки, Лиор; Альтус, Эли; Баш, Гарольд; Хоз, Шмарьяху (2005). «Тверже, чем алмаз: определение площади поперечного сечения и модуля Юнга молекулярных стержней». Энгью. Chem. Int. Эд. 44 (45): 7432–5. Дои:10.1002 / anie.200502448. PMID 16240306.
- ^ «Исследователи открывают новую фазу углерода, делают алмаз при комнатной температуре». news.ncsu.edu. 2015-11-30. В архиве из оригинала на 2016-04-06. Получено 2016-04-06.
- ^ Раби, Пассан (6 июля 2020 г.). «Астрономы нашли источник жизни во Вселенной». Обратный. Получено 7 июля 2020.
- ^ Мариго, Паола; и другие. (6 июля 2020 г.). «Формирование углеродных звезд через немонотонное соотношение начальной и конечной масс». Природа Астрономия. 152. arXiv:2007.04163. Дои:10.1038 / с41550-020-1132-1. S2CID 220403402. Получено 7 июля 2020.
- ^ а б c Гувер, Рэйчел (21 февраля 2014 г.). «Нужно отслеживать органические наночастицы по всей Вселенной? У НАСА есть для этого приложение». НАСА. В архиве из оригинала 6 сентября 2015 г.. Получено 2014-02-22.
- ^ Lauretta, D.S .; Максуин, Х. (2006). Метеориты и ранняя солнечная система II. Серия космической науки. Университет Аризоны Press. п. 199. ISBN 978-0-8165-2562-1. В архиве из оригинала от 22.11.2017. Получено 2017-05-07.
- ^ Марк, Кэтлин (1987). Метеоритные кратеры. Университет Аризоны Press. ISBN 978-0-8165-0902-7.
- ^ «Онлайн-база данных отслеживает наличие органических наночастиц по всей Вселенной». Sci Tech Daily. 24 февраля 2014 г. В архиве с оригинала 18 марта 2015 г.. Получено 2015-03-10.
- ^ Уильям Ф. Макдонаф Состав Земли В архиве 2011-09-28 на Wayback Machine в Маевский, Евгениуш (2000). Термодинамика землетрясений и фазовые превращения в недрах Земли. ISBN 978-0126851854.
- ^ Йинон Бар-Он; и другие. (19 июня 2018 г.). «Распределение биомассы на Земле». PNAS. 115 (25): 6506–6511. Дои:10.1073 / pnas.1711842115. ЧВК 6016768. PMID 29784790.
- ^ Фред Пирс (2014-02-15). «Пожар в яме: после гидроразрыва идет уголь». Новый ученый. 221 (2956): 36–41. Bibcode:2014NewSc.221 ... 36P. Дои:10.1016 / S0262-4079 (14) 60331-6. В архиве из оригинала от 16.03.2015.
- ^ "Wonderfuel: Добро пожаловать в эпоху нетрадиционного газа" В архиве 2014-12-09 в Wayback Machine Хелен Найт, Новый ученый, 12 июня 2010 г., стр. 44–7.
- ^ Запасы метана в океане `` завышены '' В архиве 2013-04-25 в Wayback Machine, BBC, 17 февраля 2004 г.
- ^ «Лед в огне: следующее ископаемое топливо» В архиве 2015-02-22 в Wayback Machine к Фред Пирс, Новый ученый, 27 июня 2009 г., стр. 30–33.
- ^ Рассчитано из файла global.1751_2008.csv в "Индекс / ftp / ndp030 / CSV-FILES". Архивировано из оригинал на 2011-10-22. Получено 2011-11-06. от Информационно-аналитический центр по двуокиси углерода.
- ^ Рэйчел Гросс (21 сентября 2013 г.). "Глубокий и сырой таинственный". Новый ученый: 40–43. В архиве из оригинала от 21.09.2013.
- ^ Стефаненко, Р. (1983). Технология добычи угля: теория и практика. Общество горной металлургии. ISBN 978-0-89520-404-2.
- ^ Кастинг, Джеймс (1998). «Углеродный цикл, климат и долгосрочные последствия сжигания ископаемого топлива». Последствия: природа и последствия изменения окружающей среды. 4 (1). В архиве из оригинала от 24.10.2008.
- ^ «Пласт Углерод-14». В архиве с оригинала на 1 августа 2015 г.. Получено 13 октября 2014.
- ^ Эйткен, М.Дж. (1990). Научные знакомства в археологии. С. 56–58. ISBN 978-0-582-49309-4.
- ^ Николс, Чарльз Р. «Летучие продукты из углеродистых астероидов» (PDF). UAPress.Arizona.edu. Архивировано из оригинал (PDF) 2 июля 2016 г.. Получено 12 ноября 2016.
- ^ Ганнес, Леонард З .; Дель Рио, Карлос Мартинес; Кох, Пол (1998). «Естественные изменения численности стабильных изотопов и их потенциальное использование в физиологической экологии животных». Сравнительная биохимия и физиология - Часть A: Молекулярная и интегративная физиология. 119 (3): 725–737. Дои:10.1016 / S1095-6433 (98) 01016-2. PMID 9683412.
- ^ «Официальные определения единиц СИ». В архиве из оригинала от 14.10.2007. Получено 2007-12-21.
- ^ Боуман, С. (1990). Интерпретация прошлого: радиоуглеродное датирование. Британский музей прессы. ISBN 978-0-7141-2047-8.
- ^ Браун, Том (1 марта 2006 г.). «Углерод на Амазонке делает полный круг». Ливерморская национальная лаборатория Лоуренса. В архиве из оригинала 22 сентября 2008 г.. Получено 2007-11-25.
- ^ Либби, У. Ф. (1952). Радиоуглеродное датирование. Издательство Чикагского университета и ссылки в нем.
- ^ Вестгрен, А. (1960). "Нобелевская премия по химии 1960 г.". Нобелевский фонд. В архиве из оригинала от 25.10.2007. Получено 2007-11-25.
- ^ "Использовать запрос для углерода-8". barwinski.net. В архиве из оригинала от 07.02.2005. Получено 2007-12-21.
- ^ Уотсон, А. (1999). «Сияние в темных углах ядерной кухни». Наука. 286 (5437): 28–31. Дои:10.1126 / science.286.5437.28. S2CID 117737493.
- ^ Ауди, Жорж; Берсильон, Оливье; Blachot, Жан; Вапстра, Алдерт Хендрик (1997). "ТогдаUBASE оценка ядерных и распадных свойств » (PDF). Ядерная физика A. 624 (1): 1–124. Bibcode:1997НуФА.624 .... 1А. Дои:10.1016 / S0375-9474 (97) 00482-X. Архивировано из оригинал (PDF) на 2008-09-23.
- ^ Остли, Дейл А. и Кэрролл, Брэдли В. (2007). Введение в современную звездную астрофизику. Сан-Франциско (Калифорния): Эддисон Уэсли. ISBN 978-0-8053-0348-3.
- ^ Уиттет, Дуглас К. Б. (2003). Пыль в галактическом окружении. CRC Press. С. 45–46. ISBN 978-0-7503-0624-9.
- ^ Пикельнер, Соломон Борисович (1977). Звездообразование. Springer. п. 38. ISBN 978-90-277-0796-3. В архиве из оригинала от 23.11.2012. Получено 2011-06-06.
- ^ Falkowski, P .; Scholes, R.J .; Boyle, E .; Canadell, J .; Canfield, D .; Elser, J .; Gruber, N .; Hibbard, K .; и другие. (2000). «Глобальный углеродный цикл: проверка наших знаний о Земле как системе». Наука. 290 (5490): 291–296. Bibcode:2000Sci ... 290..291F. Дои:10.1126 / science.290.5490.291. PMID 11030643. S2CID 1779934.
- ^ Smith, T. M .; Cramer, W. P .; Dixon, R.K .; Leemans, R .; Neilson, R.P .; Соломон, А. М. (1993). «Глобальный земной углеродный цикл». Загрязнение воды, воздуха и почвы. 70 (1–4): 19–37. Bibcode:1993WASP ... 70 ... 19S. Дои:10.1007 / BF01104986. S2CID 97265068.
- ^ Берроуз, А .; Holman, J .; Parsons, A .; Пиллинг, G .; Прайс, Г. (2017). Chemistry3: Введение в неорганическую, органическую и физическую химию. Издательство Оксфордского университета. п. 70. ISBN 978-0-19-873380-5. В архиве из оригинала от 22.11.2017. Получено 2017-05-07.
- ^ Левин, Джоэл С .; Augustsson, Tommy R .; Натараджан, Мурали (1982). «Пребиологическая палеоатмосфера: стабильность и состав». Истоки жизни и эволюция биосфер. 12 (3): 245–259. Bibcode:1982 ОрЛи ... 12..245л. Дои:10.1007 / BF00926894. PMID 7162799. S2CID 20097153.
- ^ Loerting, T .; и другие. (2001). «Об удивительной кинетической стабильности угольной кислоты». Энгью. Chem. Int. Эд. 39 (5): 891–895. Дои:10.1002 / (SICI) 1521-3773 (20000303) 39: 5 <891 :: AID-ANIE891> 3.0.CO; 2-E. PMID 10760883.
- ^ Холдейн Дж. (1895). «Действие оксида углерода на человека». Журнал физиологии. 18 (5–6): 430–462. Дои:10.1113 / jphysiol.1895.sp000578. ЧВК 1514663. PMID 16992272.
- ^ Горман, Д .; Drewry, A .; Huang, Y. L .; Самес, К. (2003). «Клиническая токсикология окиси углерода». Токсикология. 187 (1): 25–38. Дои:10.1016 / S0300-483X (03) 00005-2. PMID 12679050.
- ^ «Соединения углерода: недокись углерода». В архиве из оригинала 07.12.2007. Получено 2007-12-03.
- ^ Байес, К. (1961). «Фотолиз недооксида углерода». Журнал Американского химического общества. 83 (17): 3712–3713. Дои:10.1021 / ja01478a033.
- ^ Андерсон Д. Дж .; Розенфельд, Р. Н. (1991). «Фотодиссоциация недооксида углерода». Журнал химической физики. 94 (12): 7852–7867. Bibcode:1991ЖЧФ..94.7857А. Дои:10.1063/1.460121.
- ^ Sabin, J. R .; Ким, Х. (1971). «Теоретическое исследование структуры и свойств триоксида углерода». Письма по химической физике. 11 (5): 593–597. Bibcode:1971CPL .... 11..593S. Дои:10.1016/0009-2614(71)87010-0.
- ^ Moll N. G .; Clutter D. R .; Томпсон В. Э. (1966). «Триоксид углерода: его производство, инфракрасный спектр и структура, изученные в матрице твердого CO.2". Журнал химической физики. 45 (12): 4469–4481. Bibcode:1966ЖЧФ..45.4469М. Дои:10.1063/1.1727526.
- ^ а б Фатиади, Александр Дж .; Isbell, Horace S .; Сагер, Уильям Ф. (1963). «Циклические полигидроксикетоны. I. Продукты окисления гексагидроксибензола (бензолгексола)» (PDF). Журнал исследований Национального бюро стандартов Раздел A. 67A (2): 153–162. Дои:10.6028 / jres.067A.015. ЧВК 6640573. PMID 31580622. Архивировано из оригинал (PDF) на 2009-03-25. Получено 2009-03-21.
- ^ Полинг, Л. (1960). Природа химической связи (3-е изд.). Итака, Нью-Йорк: Издательство Корнельского университета. п.93. ISBN 978-0-8014-0333-0.
- ^ Гринвуд и Эрншоу, стр. 297–301.
- ^ Шербаум, Франц; и другие. (1988). ""Аурофильность »как следствие релятивистских эффектов: Дикация метана Hexakis (трифенилфосфанаурио) [(Ph3PAu)6C]2+". Энгью. Chem. Int. Эд. Англ. 27 (11): 1544–1546. Дои:10.1002 / anie.198815441.
- ^ Риттер, Стивен К. «Шесть связей с углеродом: подтверждено». Новости химии и машиностроения. В архиве из оригинала от 09.01.2017.
- ^ Ямасита, Макото; Ямамото, Ёсукэ; Акиба, Кин-я; Хашизуме, Дайсуке; Ивасаки, Фудзико; Такаги, Нозоми; Нагасе, Сигэру (01.03.2005). «Синтезы и структуры гипервалентных пятикоординированных соединений углерода и бора, несущих антраценовый скелет - выяснение гипервалентного взаимодействия на основе рентгеноструктурного анализа и расчета методом DFT». Журнал Американского химического общества. 127 (12): 4354–4371. Дои:10.1021 / ja0438011. ISSN 0002-7863. PMID 15783218.
- ^ Краткий оксфордский словарь английского языка, Oxford University Press
- ^ «Китайцы впервые применили алмаз». Новости BBC. 17 мая 2005 г. В архиве из оригинала 20 марта 2007 г.. Получено 2007-03-21.
- ^ ван дер Крогт, Питер. «Карбоний / Углерод в Elementymology & Elements Multidict». В архиве из оригинала от 23.01.2010. Получено 2010-01-06.
- ^ Фершо де Реомюр, Р.-А. (1722). L'art de convertir le fer forgé en acier, et l'art d'adoucir le fer fondu, ou de faire des ouvrages de fer fondu aussi finis que le fer forgé (английский перевод с 1956 г.). Париж, Чикаго.
- ^ «Карбон». Канада соединяется. Архивировано из оригинал на 2010-10-27. Получено 2010-12-07.
- ^ Сенезе, Фред. "Кто открыл углерод?". Фростбургский государственный университет. В архиве из оригинала 2007-12-07. Получено 2007-11-24.
- ^ Джолитти, Федерико (1914). Цементирование железа и стали. McGraw-Hill Book Company, inc.
- ^ Сенез, Фред (9 сентября 2000). «Кто открыл углерод». Фростбургский государственный университет. В архиве из оригинала 2007-12-07. Получено 2007-11-24.
- ^ Kroto, H.W .; Heath, J. R .; O'Brien, S.C .; Curl, R. F .; Смолли Р. Э. (1985). "C60: Бакминстерфуллерен ". Природа. 318 (6042): 162–163. Bibcode:1985Натура.318..162K. Дои:10.1038 / 318162a0. S2CID 4314237.
- ^ "Нобелевская премия по химии 1996 г." за открытие фуллеренов."". В архиве из оригинала от 11.10.2007. Получено 2007-12-21.
- ^ а б c Ежегодник USGS Minerals: Графит, 2009 г. В архиве 2008-09-16 на Wayback Machine и графит: обзор минерального сырья, 2011 г.
- ^ Харлоу, Г. Э. (1998). Природа алмазов. Издательство Кембриджского университета. п. 223. ISBN 978-0-521-62935-5.
- ^ Кателл, В. Р. (1911). Бриллиант. Компания John Lane. п. 159. обсуждение аллювиальных алмазов в Индии и других странах, а также самые ранние находки
- ^ Болл, В. (1881). Бриллианты, золото и уголь Индии. Лондон, Трубнер и Ко. Болл был геологом на британской службе. Глава I, Страница 1
- ^ Херши, Дж. У. (1940). Книга алмазов: их любопытные знания, свойства, тесты и синтетическое производство. Kessinger Pub Co., стр. 28. ISBN 978-1-4179-7715-4.
- ^ а б Янсе, А. Дж. А. (2007). «Мировое производство алмазов с 1870 года». Драгоценные камни и геммология. XLIII (Лето 2007 г.): 98–119. Дои:10.5741 / GEMS.43.2.98.
- ^ а б Лоренц, В. (2007). «Аргайл в Западной Австралии: самая богатая алмазная трубка в мире; ее прошлое и будущее». Gemmologie, Zeitschrift der Deutschen Gemmologischen Gesellschaft. 56 (1/2): 35–40.
- ^ «Микроскопический алмаз найден в Монтане». Стандарт Монтаны. 2004-10-17. Архивировано из оригинал 21 января 2005 г.. Получено 2008-10-10.
- ^ Кук, Сара (2004-10-19). "Микроскопический алмаз найден в Монтане". Livescience.com. Архивировано из оригинал на 2008-07-05. Получено 2008-09-12.
- ^ "Delta News / Пресс-релизы / Публикации". Deltamine.com. Архивировано из оригинал на 2008-05-26. Получено 2008-09-12.
- ^ Маршалл, Стивен; Шор, Джош (2004-10-22). "Бриллиантовая жизнь". Сеть партизанских новостей. Архивировано из оригинал на 2008-06-09. Получено 2008-10-10.
- ^ Cantwell, W. J .; Мортон, Дж. (1991). «Ударопрочность композитных материалов - обзор». Композиты. 22 (5): 347–62. Дои:10.1016 / 0010-4361 (91) 90549-В.
- ^ Holtzapffel, Ch. (1856 г.). Токарная обработка и механические манипуляции. Чарльз Хольцапффель. Интернет-архив В архиве 2016-03-26 в Wayback Machine
- ^ «Статистика и информация промышленных алмазов». Геологическая служба США. В архиве из оригинала от 06.05.2009. Получено 2009-05-05.
- ^ Коэльо, Р. Т .; Yamada, S .; Aspinwall, D. K .; Мудрый, М. Л. Х. (1995). «Применение инструментальных материалов из поликристаллического алмаза (PCD) при сверлении и расширении сплавов на основе алюминия, включая MMC». Международный журнал станков и производства. 35 (5): 761–774. Дои:10.1016/0890-6955(95)93044-7.
- ^ Харрис, Д. К. (1999). Материалы для инфракрасных окон и куполов: свойства и характеристики. SPIE Press. С. 303–334. ISBN 978-0-8194-3482-1.
- ^ Нусинович, Г. С. (2004). Введение в физику гиротронов. JHU Press. п. 229. ISBN 978-0-8018-7921-0.
- ^ Сакамото, М .; Endriz, J. G .; Сцифрес, Д. Р. (1992). «Выходная мощность 120 Вт в непрерывном режиме от монолитной диодной матрицы AlGaAs (800 нм), установленной на алмазном радиаторе». Письма об электронике. 28 (2): 197–199. Bibcode:1992ElL .... 28..197S. Дои:10.1049 / el: 19920123.
- ^ Дорфер, Леопольд; Moser, M .; Шпиндлер, К .; Bahr, F .; Egarter-Vigl, E .; Дор, Г. (1998). «5200-летняя акупунктура в Центральной Европе?». Наука. 282 (5387): 242–243. Bibcode:1998Sci ... 282..239D. Дои:10.1126 / science.282.5387.239f. PMID 9841386. S2CID 42284618.
- ^ Donaldson, K .; Stone, V .; Clouter, A .; Renwick, L .; Макни, В. (2001). «Сверхмелкие частицы». Медицина труда и окружающей среды. 58 (3): 211–216. Дои:10.1136 / oem.58.3.211. ЧВК 1740105. PMID 11171936.
- ^ Углеродные наночастицы токсичны для взрослых плодовых мух, но благоприятны для молодых В архиве 2011-11-02 в Wayback Machine ScienceDaily (17 августа 2009 г.)
- ^ "Пресс-релиз - Титаническая катастрофа: новая теория угольного огня". www.geosociety.org. В архиве из оригинала на 2016-04-14. Получено 2016-04-06.
- ^ Макшерри, Патрик. «Угольный бункер Fire». www.spanamwar.com. В архиве из оригинала от 23.03.2016. Получено 2016-04-06.
Библиография
- Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн. ISBN 978-0-08-037941-8.



