Слабоумие - Dementia - Wikipedia
| Слабоумие | |
|---|---|
| Другие имена | Старость,[1] старческое слабоумие |
 | |
| Изображение мужчины с диагнозом деменция в 1800-х годах | |
| Специальность | Неврология, психиатрия |
| Симптомы | Сниженная способность считать и помните, эмоциональные проблемы, проблемы с язык, уменьшилось мотивация[2][3] |
| Обычное начало | Постепенный[2] |
| Продолжительность | Долгосрочный[2] |
| Причины | Болезнь Альцгеймера, сосудистая деменция, Деменция с тельцами Леви, лобно-височная деменция[2][3] |
| Диагностический метод | Когнитивное тестирование (мини-обследование психического состояния )[3][4] |
| Дифференциальная диагностика | Бред[5] |
| Профилактика | Раннее образование, предотвратить высокое кровяное давление, предотвратить ожирение, не курить, социальная активность[6] |
| Уход | Поддерживающая терапия[2] |
| Медикамент | Ингибиторы холинэстеразы (небольшое преимущество)[7][8] |
| Частота | 50 миллионов (2020)[9] |
| Летальные исходы | 1,9 миллиона (2015)[10] |
Слабоумие происходит как набор связанных симптомов когда мозг поражен болезнью.[11] Симптомы включают прогрессирующие нарушения памяти, мышления и поведения, которые влияют на способность выполнять повседневную деятельность.[9] Другие общие симптомы включают эмоциональные проблемы, трудности с языком и снижение мотивация.[2][3] Деменция - это не расстройство сознания, и сознание обычно не влияет.[9][а] Диагноз деменции требует изменения обычного психического функционирования человека и большего познавательный снижение, чем это из-за нормального старение.[9][13] Некоторые заболевания и травмы головного мозга, такие как Инсульт может привести к слабоумию, которое оказывает значительное влияние на отношения и сиделки.[9] В DSM-5, деменция была реклассифицирована как основное нейрокогнитивное расстройство, с разной степенью серьезности, и многие причинный подтипы.[14]
Причинные подтипы деменции могут быть основаны на известной потенциальной причине, например: болезнь Паркинсона, за Деменция при болезни Паркинсона; болезнь Хантингтона деменции при болезни Хантингтона; сосудистое заболевание за сосудистая деменция; травмы головного мозга, включая инсульт, часто приводят к сосудистой деменции; или многие другие медицинские условия, включая ВИЧ-инфекция за Деменция ВИЧ; и прионные болезни. Подтипы могут быть основаны на различных симптомах, которые могут быть вызваны нейродегенеративное расстройство Такие как Болезнь Альцгеймера; лобно-височная долевая дегенерация за лобно-височная деменция; или же Болезнь телец Леви за деменция с тельцами Леви.[9][14] У одного и того же человека может быть более одного типа деменции.[9] Диагноз обычно ставится на основании: история болезни и когнитивное тестирование с медицинская визуализация, и анализы крови чтобы исключить другие возможные причины,[4] и определить конкретный подтип.[15] В мини-обследование психического состояния один из широко используемых когнитивный тест.[3]Факторы риска слабоумие, которое можно уменьшить, связаны с сосудистыми заболеваниями и включают высокое кровяное давление, курение, сахарный диабет, и ожирение.[2] Скрининг всего населения на наличие расстройства не рекомендуется.[16]
Нет никаких известных излечивать при слабоумие.[2] Ингибиторы холинэстеразы Такие как донепезил часто используются и могут быть полезны при легких и умеренных расстройствах.[7][17][18] Однако общая польза может быть незначительной.[7][8] Существует множество мер, которые могут улучшить качество жизни людей с деменцией и их сиделки.[2] Когнитивные и поведенческие вмешательства может быть уместным.[2] Просвещение и эмоциональная поддержка воспитателя очень важны.[2] Программы упражнений могут быть полезны в отношении ежедневные занятия и потенциально улучшить результаты.[19] Лечение поведенческих проблем с помощью нейролептики является обычным, но обычно не рекомендуется из-за ограниченной пользы и побочных эффектов, включая повышенный риск смерти.[20][21]
По оценкам, в 2020 году деменцией страдают около 50 миллионов человек во всем мире.[9] Это больше оценки 2015 года в 46 миллионов.[22] Около 10% людей в какой-то момент своей жизни заболевают этим заболеванием.[23] обычно в результате старение.[24] Примерно 3% людей в возрасте 65–74 лет страдают деменцией, 19% - между 75 и 84 годами и почти половина людей старше 85 лет.[25] В 2015 году деменция стала причиной смерти около 1,9 миллиона человек по сравнению с 0,8 миллиона в 1990 году.[10] По мере того, как все больше людей живут дольше, деменция становится все более распространенным явлением.[24] Однако для людей определенного возраста это может стать менее частым, по крайней мере, в развитом мире, из-за уменьшения факторов риска.[24] Это одна из наиболее частых причин инвалидность среди старых.[3] Во всем мире стоимость деменции в 2015 году оценивалась как 818 миллиардов долларов США.[9] Люди с деменцией часто физически или химически сдержанный в большей степени, чем необходимо, поднимая вопросы права человека.[2] Социальное клеймо против пострадавших - обычное дело.[3]
Признаки и симптомы


Симптомы деменции и скорость прогрессирования варьируются в зависимости от подтипа заболевания.[26] Наиболее часто поражаемые области включают: объем памяти, зрительно-пространственная функция влияющие на восприятие и ориентацию, язык, внимание и решение проблем. Большинство типов деменции протекают медленно и прогрессируют с некоторым ухудшением состояния головного мозга, установленным до того, как признаки расстройства станут очевидными. Часто у людей с деменцией присутствуют и другие состояния, типы которых также различаются в зависимости от подтипов деменции. Высокое кровяное давление, и сахарный диабет являются общими сопутствующими заболеваниями, и может быть три или более связанных сопутствующих состояния.[27]
Симптомы деменции имеют как поведенческий, так и психологический характер и называются поведенческие и психологические симптомы деменции (БПСД).[28] Вариации BPSD встречаются у разных подтипов деменции.[29][30]
Поведенческие симптомы могут включать возбуждение, беспокойство, несоответствующее поведение, сексуальную расторможенность и агрессию, которая может быть вербальной или физической.[28]
Психологические симптомы могут включать депрессию, психотические галлюцинации и бред, апатию и тревогу.[28][31]
Когда люди с деменцией попадают в обстоятельства, выходящие за рамки их возможностей, они могут внезапно перерасти в плач или гнев, известный как катастрофическая реакция.[32]
Этапы
Легкие когнитивные нарушения
На первых стадиях деменции признаки и симптомы могут быть незаметными. Часто первые признаки становятся очевидными, если оглянуться назад во времени. Самая ранняя стадия деменции называется легкие когнитивные нарушения (MCI). 70% из тех, кому поставлен диагноз MCI, позже прогрессируют до деменции.[13] При MCI изменения в мозге человека происходят уже давно, но симптомы только начинают появляться. Однако эти проблемы недостаточно серьезны, чтобы повлиять на повседневное функционирование. Если / однажды они это сделают, диагноз станет деменцией. Человек с MCI набирает от 27 до 30 баллов по шкале Краткий экзамен на психическое состояние (MMSE), что является нормальной оценкой. У них могут быть проблемы с памятью и трудности с поиском слов, но они решают повседневные проблемы и грамотно справляются со своими жизненными делами.[33]
Легкие когнитивные нарушения были зарегистрированы в обоих случаях. DSM-5, и МКБ-11, так как легкие нейрокогнитивные расстройства, - более легкие формы подтипов основного нейрокогнитивного расстройства (деменции).[14]
Ранние стадии
На ранней стадии деменции симптомы становятся заметными для окружающих. Кроме того, симптомы начинают мешать повседневной деятельности. MMSE оценка составляет от 20 до 25. Симптомы зависят от типа деменции. Более сложные дела по дому или на работе становятся все труднее. Обычно человек все еще может позаботиться о себе, но может забыть о таких вещах, как прием таблеток или стирка, и ему могут потребоваться подсказки или напоминания.[34]
Симптомы ранней деменции обычно включают проблемы с памятью, но могут также включать некоторые проблемы с поиском слов, а также проблемы с планированием и организационными навыками (исполнительная функция ).[35] Один очень хороший способ оценить состояние человека - это спросить, могут ли он по-прежнему самостоятельно управлять своими финансами. Часто это становится проблемой в первую очередь. Другие признаки могут быть потеряны в новых местах, повторяющиеся вещи, изменения личности,[36] социальная изоляция и трудности на работе.
При оценке деменции важно учитывать, как человек функционировал пять или десять лет назад. При оценке функции также важно учитывать уровень образования. Например, бухгалтер, который больше не может балансировать в чековой книжке, будет беспокоить больше, чем человек, который не закончил среднюю школу или никогда не заботился о своих финансах.[13]
При деменции Альцгеймера наиболее заметным ранним признаком является нарушение памяти. К другим относятся проблемы с поиском слов и заблуждение. При других типах деменции, таких как деменция с тельцами Леви и лобно-височная деменция, первыми признаками могут быть изменения личности и трудности с организацией и планированием.[37][38]
Средние стадии
По мере прогрессирования деменции начальные симптомы обычно ухудшаются. Скорость снижения у каждого человека разная. Показатели MMSE от 6 до 17 указывают на умеренную деменцию. Например, люди с умеренной деменцией Альцгеймера теряют почти всю новую информацию. Люди с деменцией могут быть серьезно затруднены в решении проблем, и их социальное суждение обычно также ухудшается. Обычно они не могут функционировать вне своего дома, и, как правило, их не следует оставлять в покое. Они могут выполнять простые дела по дому, но не более того, и им начинает требоваться помощь в вопросах личной гигиены и ухода, помимо простых напоминаний.[13] А отсутствие понимания состояние станет очевидным.[39][40]
Поздние стадии
Люди с деменцией на поздней стадии обычно все больше и больше обращаются внутрь себя и нуждаются в большей или большей части личной помощи. Людям с деменцией на поздних стадиях обычно требуется круглосуточное наблюдение для обеспечения их личной безопасности и удовлетворения основных потребностей. Если их оставить без присмотра, они могут блуждать или упасть; может не распознавать общие опасности, такие как горячая плита; или могут не осознавать, что им нужно пользоваться ванной и стать недержание мочи.[33]
Часто происходят изменения в питании. Люди с поздней стадией деменции часто едят протертые диеты, загустевшие жидкости и нуждаются в помощи в приеме пищи, чтобы продлить их жизнь, сохранить вес, снизить риск удушья и облегчить прием пищи.[41] Аппетит у человека может снизиться до такой степени, что он вообще не захочет есть. Они могут не захотеть вставать с постели или им может потребоваться помощь. Обычно человек больше не узнает знакомые лица. У них могут быть значительные изменения в привычках сна или вообще проблемы со сном.[13]
Подтипы
Эта секция нужны дополнительные цитаты для проверка. (Ноябрь 2015) (Узнайте, как и когда удалить этот шаблон сообщения) |
Болезнь Альцгеймера

Болезнь Альцгеймера на него приходится более 80% случаев деменции во всем мире.[42] Наиболее частые симптомы болезни Альцгеймера: кратковременная потеря памяти и трудности с поиском слов. Проблемы с зрительно-пространственное функционирование (часто заблудиться), рассуждения, суждения и проницательность терпят неудачу. Проницательность относится к тому, осознает ли человек, что у него проблемы с памятью.
Общие ранние симптомы болезни Альцгеймера включают повторение, заблуждение, трудности с отслеживанием счетов, проблемы с приготовлением блюд, особенно новых или сложных блюд, забывание приема лекарств и проблемы с поиском слов.
Часть мозга, наиболее пораженная болезнью Альцгеймера, - это гиппокамп.[43] Другие части, которые показывают атрофия (усадка) включает временный и теменные доли.[13] Хотя такая модель сокращения мозга предполагает болезнь Альцгеймера, она вариабельна, и сканирование мозга не позволяет поставить диагноз. Отношения между анестезия и AD неясно.[44]
Течение болезни Альцгеймера часто описывается четырьмя стадиями, которые показывают картину прогрессирующих когнитивных и функциональных нарушений. Более подробный курс описан в семи этапах, два из которых разбиты на пять и шесть ступеней. Это в соответствии с Глобальная шкала ухудшения состояния который более точно определяет каждую стадию прогрессирования заболевания. Этап 7 (f) - заключительный этап.[45][46] Другой используемый масштаб - это Тест функциональной оценки.[45]
Сосудистая деменция
Сосудистая деменция составляет не менее 20% случаев деменции, что делает ее вторым по распространенности типом.[47] Это вызвано болезнью или травмой, поражающей кровоснабжение мозга, обычно включающий серию мини-штрихи. Симптомы этой деменции зависят от того, где в головном мозге произошел инсульт и были ли пораженные кровеносные сосуды большими или маленькими.[13] Множественные травмы со временем могут вызвать прогрессирующее слабоумие, в то время как одиночная травма, расположенная в области, критической для познания, такой как гиппокамп или таламус, может привести к внезапному снижению когнитивных функций.[47]
Сканирование мозга может свидетельствовать о множественных мазках разного размера в разных местах. Люди с сосудистой деменцией, как правило, имеют факторы риска заболевание кровеносных сосудов, Такие как употребление табака, высокое кровяное давление, мерцательная аритмия, высокое содержание холестерина, сахарный диабет или другие признаки сосудистого заболевания, такие как предыдущий острое сердечно-сосудистое заболевание или же стенокардия.
Деменция с тельцами Леви
Симптомы деменция с тельцами Леви (DLB) встречаются чаще, тяжелее и раньше, чем при других подтипах деменции.[48]Деменция с тельцами Леви имеет основные симптомы нестабильности познания, бдительности или внимания; Расстройство быстрого сна (RBD); одна или несколько основных характеристик паркинсонизм не из-за лекарств или инсульта; и повторяющиеся зрительные галлюцинации.[49] Визуальные галлюцинации в DLB обычно представляют собой яркие галлюцинации людей или животных, и они часто возникают, когда кто-то собирается заснуть или проснуться. Другие заметные симптомы включают проблемы с планированием (исполнительная функция) и трудности с зрительно-пространственной функцией.[13] и нарушение автономные функции организма.[50] Аномальное поведение во сне может начаться до того, как наблюдается снижение когнитивных функций, и является основной характеристикой DLB.[49] RBD диагностируется либо путем записи исследования сна, либо, если исследования сна невозможно провести, на основании истории болезни и утвержденных анкет.[49]
Лобно-височная деменция
Лобно-височная деменция (FTD) характеризуются резкими изменениями личности и языковыми трудностями. При всех ЛТД у человека относительно ранняя социальная изоляция и раннее отсутствие понимания. Проблемы с памятью не являются главной особенностью.[13][51]
Существует шесть основных типов FTD. Первый имеет серьезные симптомы в личности и поведении. Это называется поведенческим вариантом FTD (bv-FTD) и является наиболее распространенным. При bv-FTD человек демонстрирует изменение личной гигиены, становится негибким в своем мышлении и редко признает проблемы; они социально замкнуты, и у них часто резко повышается аппетит. Они могут стать социально неприемлемыми. Например, они могут сделать неуместные сексуальные комментарии, или могут начать использовать порнографию открыто. Один из самых распространенных признаков - апатия или безразличие. Однако апатия - частый симптом многих деменций.[13]
Два типа функции FTD афазия (языковые проблемы) в качестве основного симптома. Один тип называется семантическим вариантом первичной прогрессирующей афазии (SV-PPA). Главная особенность этого - потеря смысла слов. Это может начаться с трудностей в назывании вещей. Со временем человек может потерять и значение предметов. Например, изображение птицы, собаки и самолета у человека с ЛТД может показаться почти одинаковым.[13] В классическом тесте на это пациенту показывают изображение пирамиды, а под ним - изображение пальмы и сосны. Человека просят сказать, какой из них лучше всего подходит для пирамиды. В SV-PPA человек не может ответить на этот вопрос. Другой тип называется аграмматическим вариантом первично-прогрессирующей афазии (NFA-PPA). В основном это проблема с воспроизведением речи. Им сложно подобрать нужные слова, но в основном им сложно координировать работу мышц, которые им нужны, чтобы говорить. В конце концов, кто-то с NFA-PPA использует только односложные слова или может полностью стать немым.
Прогрессирующий надъядерный паралич (PSP) - это форма FTD, которая характеризуется проблемами с движениями глаз.[нужна цитата ] Обычно проблемы начинаются с затруднения движения глаз вверх или вниз (паралич вертикального взгляда). Поскольку при нормальном старении иногда возникают трудности с движением глаз вверх, проблемы с движением глаз вниз являются ключевыми в PSP. Другие ключевые симптомы включают падение назад, проблемы с равновесием, медленные движения, жесткие мышцы, раздражительность, апатию, социальную изоляцию и депрессию. У человека могут быть определенные признаки лобной доли, такие как персеверация, хватательный рефлекс и поведение использования (необходимость использовать объект, когда вы его видите). Люди с PSP часто испытывают прогрессирующие трудности с едой и глотанием, а в конечном итоге и с разговором. Из-за жесткости и медленных движений PSP иногда ошибочно принимают за болезнь Паркинсона. При сканировании средний мозг людей с PSP, как правило, сморщены (атрофированы), но других общих аномалий мозга не наблюдается.
Кортикобазальная дегенерация (CBD) - редкая форма FTD, которая характеризуется множеством различных типов неврологических проблем, которые постепенно ухудшаются. Это связано с тем, что заболевание поражает мозг во многих разных местах, но с разной скоростью. Один общий признак - трудности с использованием только одной конечности. Симптом, который редко встречается при любом другом состоянии, - это «чужеродная конечность». Инопланетная конечность - это конечность, которая, кажется, имеет собственный разум, она движется без сознательного контроля над мозгом человека. Другие общие симптомы включают резкие движения одной или нескольких конечностей (миоклонус ), симптомы, которые различаются в разных конечностях (асимметричные), трудности с речью из-за неспособности скоординированно двигать мышцами рта, онемения и покалывания в конечностях и игнорирования одной стороны зрения или чувств. В пренебрежении человек игнорирует сторону тела, противоположную той, на которой возникла проблема. Например, человек может не чувствовать боли с одной стороны или может нарисовать только половину изображения, когда его попросят. Кроме того, пораженные конечности могут быть жесткими или иметь мышечные сокращения, вызывающие дистония (странные повторяющиеся движения).[13] Область мозга, наиболее часто поражаемая кортикобазальной дегенерацией, - это задняя часть мозга. лобная доля и теменная доля, хотя могут быть затронуты многие другие части.[13]
Наконец, деменция при FT, связанная с ALS (FTD-ALS), включает в себя симптомы FTD (проблемы с поведением, речью и движением), сопутствующие боковой амиотрофический склероз (гибель мотонейронов).
Быстро прогрессирующий
болезнь Крейтцфельдта-Якоба обычно вызывает деменцию, которая ухудшается в течение недель или месяцев, и вызвана: прионы. Общие причины медленно прогрессирующей деменции также иногда проявляются быстрым прогрессированием: Болезнь Альцгеймера, деменция с тельцами Леви, лобно-височная долевая дегенерация (включая кортикобазальная дегенерация и прогрессирующий надъядерный паралич ).
Энцефалопатия или же бред может развиваться относительно медленно и напоминать слабоумие. Возможные причины включают инфекцию головного мозга (вирусный энцефалит, подострый склерозирующий панэнцефалит, Болезнь Уиппла ) или воспаление (лимбический энцефалит, Энцефалопатия Хашимото, церебральный васкулит ); опухоли, такие как лимфома или же глиома; токсичность препарата (например, противосудорожное средство наркотики[уточнить ]); метаболические причины, такие как отказ печени или же почечная недостаточность; хронический субдуральная гематома; и повторные травмы головного мозга (хроническая травматическая энцефалопатия, состояние, связанное с контактными видами спорта).
Иммунологически опосредованный
Хронические воспалительные состояния, которые могут повлиять на мозг и познание, включают: Болезнь Бехчета, рассеянный склероз, саркоидоз, Синдром Шегрена, системная красная волчанка, глютеновая болезнь, и не глютеновая чувствительность.[52][53] Эти типы деменции могут быстро прогрессировать, но обычно хорошо поддаются раннему лечению. Это состоит из иммуномодуляторы или же стероидный препарат введение или в некоторых случаях устранение возбудителя.[53] Обзор 2019 года не обнаружил связи между целиакией и деменцией в целом, но потенциальную связь с сосудистая деменция.[54] Обзор 2018 года обнаружил связь между глютеновой болезнью или чувствительностью к глютену, отличной от целиакии, и когнитивными нарушениями, и что глютеновая болезнь может быть связана с Болезнь Альцгеймера, сосудистая деменция и лобно-височная деменция.[55] А строгая безглютеновая диета раннее начало может защитить от деменции, связанной с расстройства, связанные с глютеном.[54][55]
Обратимые случаи
Случаи легко обратимая деменция включают гипотиреоз, дефицит витамина B12, Болезнь Лайма, и нейросифилис. Все люди с нарушением памяти должны быть проверены на гипотиреоз и дефицит B12. При болезни Лайма и нейросифилисе необходимо провести тестирование при наличии факторов риска. Потому что факторы риска[56] часто бывает трудно определить, тестирование на нейросифилис и болезнь Лайма, а также на другие упомянутые факторы, само собой разумеется, может быть проведено при подозрении на деменцию.[13]:31–32 Потеря слуха также может быть связано с деменцией у пожилых людей. Одна из гипотез состоит в том, что по мере увеличения потери слуха когнитивные ресурсы перераспределяются между слуховое восприятие, в их ущерб. Потеря слуха может привести к социальная изоляция что отрицательно сказывается на познании.[57]
Другие условия
Многие другие медицинские и неврологические состояния включают слабоумие только на поздних стадиях болезни. Например, доля пациентов с болезнь Паркинсона развиваются слабоумие, хотя для этой доли приводятся самые разные цифры.[58] Когда деменция возникает при болезни Паркинсона, основной причиной может быть: деменция с тельцами Леви или же Болезнь Альцгеймера, или оба.[59] Когнитивные нарушения также возникают при синдромах Паркинсона плюс прогрессирующий надъядерный паралич и кортикобазальная дегенерация (и та же самая основная патология может вызывать клинические синдромы лобно-височная долевая дегенерация ). Хотя острый порфирии может вызывать приступы спутанности сознания и психических расстройств, слабоумие - редкая черта этих редких заболеваний. Лимбическая преобладающая возрастная энцефалопатия TDP-43 (ПОЗДНЕЕ) - это тип слабоумия, который в первую очередь поражает людей в возрасте от 80 до 90 лет и при котором ТДП-43 белковые отложения в лимбический часть мозга.[60]
Помимо упомянутых выше, наследственные состояния, которые могут вызвать деменцию (наряду с другими симптомами), включают:[61]
- Болезнь Александра
- Болезнь Канавана
- Церебротехнический ксантоматоз
- Дентаторубрально-паллидолуйзийская атрофия
- Эпилепсия
- Смертельная семейная бессонница
- Синдром хрупкого Х-ассоциированного тремора / атаксии
- Глутаровая ацидурия 1 типа
- Болезнь Краббе
- Заболевание мочи кленовым сиропом
- Болезнь Ниманна – Пика тип C
- Цероидный липофусциноз нейронов
- Нейроакантоцитоз
- Органические ацидемии
- Болезнь Пелицея-Мерцбахера
- Синдром Санфилиппо тип B
- Спиноцеребеллярная атаксия тип 2
- Нарушения цикла мочевины
Легкие когнитивные нарушения
Легкие когнитивные нарушения означает, что у человека наблюдаются проблемы с памятью или мышлением, но эти трудности недостаточно серьезны для диагностики деменции.[62] Они должны набрать от 25 до 30 баллов по MMSE.[13] Примерно у 70% людей с MCI развивается какая-либо форма деменции.[13] MCI обычно делится на две категории. Первый - это прежде всего потеря памяти (амнезиальная MCI). Второй - это что-нибудь еще (неамнестический MCI). Болезнь Альцгеймера обычно развивается у людей с преимущественно проблемами памяти. У людей с другим типом MCI могут развиться другие типы деменции.
Диагностика MCI часто затруднена, так как когнитивные тесты могут быть нормальными. Часто более подробный нейропсихологический для постановки диагноза необходимо тестирование. Наиболее часто используемые критерии называются критериями Петерсона и включают:
- Жалобы на память или другие когнитивные (связанные с обработкой мыслей) жалобы человека или человека, хорошо знающего пациента.
- Проблемы с памятью или другие когнитивные проблемы по сравнению с человеком того же возраста и уровня образования.
- Симптомы недостаточно серьезны, чтобы повлиять на повседневную жизнь.
- Отсутствие деменции.
Фиксированные когнитивные нарушения
Различные типы травм головного мозга могут вызывать необратимые когнитивные нарушения, которые остаются стабильными с течением времени. Травматическое повреждение мозга может вызвать общее повреждение белого вещества головного мозга (диффузное повреждение аксонов ) или более локализованное повреждение (которое также может сопровождать нейрохирургия ). Временное снижение притока крови или кислорода в мозг может привести к гипоксически-ишемическое повреждение. Штрихи (ишемический инсульт или внутримозговое, субарахноидальное, субдуральное или экстрадуральное кровоизлияние) или инфекции (менингит или же энцефалит ) поражающие головной мозг, затяжной эпилептический припадки, и острый гидроцефалия также может иметь долгосрочное влияние на познавательные способности. Чрезмерное употребление алкоголя может вызвать алкогольная деменция, Энцефалопатия Вернике, или же Корсаковский психоз.
Медленно прогрессивный
Деменция, которая начинается постепенно и ухудшается в течение нескольких лет, обычно вызвана: нейродегенеративное заболевание - то есть состояниями, которые влияют только или преимущественно на нейроны мозга и вызывают постепенную, но необратимую потерю функции. Реже недегенеративное состояние может оказывать вторичное воздействие на клетки мозга, которое может быть или не быть обратимым при лечении.
Причины деменции зависят от возраста появления симптомов. Среди пожилых людей подавляющее большинство случаев деменции вызвано: Болезнь Альцгеймера, сосудистая деменция, или же деменция с тельцами Леви.[63][64][65] Гипотиреоз иногда вызывает медленно прогрессирующие когнитивные нарушения в качестве основного симптома, которые могут быть полностью обратимы при лечении. Гидроцефалия нормального давления хотя и относительно редко, но важно распознать, поскольку лечение может предотвратить прогрессирование и улучшить другие симптомы заболевания. Однако значительное улучшение когнитивных функций встречается редко.
Деменция гораздо реже встречается в возрасте до 65 лет. Болезнь Альцгеймера по-прежнему является наиболее частой причиной, но унаследованные формы расстройства составляют более высокую долю случаев в этой возрастной группе. Лобно-височная долевая дегенерация и болезнь Хантингтона приходится большинство оставшихся случаев.[66] Сосудистая деменция также происходит, но это, в свою очередь, может быть связано с основными условиями (включая антифосфолипидный синдром, КАДАСИЛ, МЕЛАС, гомоцистинурия, Моямоя, и Болезнь Бинсвангера ). Люди, которые часто получают травмы головы, например боксеры или футболисты, подвержены риску хроническая травматическая энцефалопатия[67] (также называемый пугилистическое слабоумие в боксерах).
У молодых людей (до 40 лет), которые ранее имели нормальный интеллект, очень редко развивается деменция без других признаков неврологического заболевания или без признаков болезни в других частях тела. Большинство случаев прогрессирующего когнитивного нарушения в этой возрастной группе вызвано психическим заболеванием, употреблением алкоголя или других наркотиков или нарушением обмена веществ. Однако определенные генетические нарушения могут вызвать истинную нейродегенеративную деменцию в этом возрасте. К ним относятся семейная болезнь Альцгеймера, SCA17 (доминирующий наследование); адренолейкодистрофия (Х-связанный ); Болезнь Гоше тип 3, метахроматическая лейкодистрофия, Болезнь Ниманна-Пика тип C, нейродегенерация, связанная с пантотенаткиназой, Болезнь Тея – Сакса, и Болезнь Вильсона (все рецессивный ). Болезнь Вильсона особенно важна, поскольку когнитивные способности могут улучшиться при лечении.
В любом возрасте у значительной части пациентов, которые жалуются на проблемы с памятью или другие когнитивные симптомы, депрессия а не нейродегенеративное заболевание. Дефицит витаминов и хронические инфекции также могут возникать в любом возрасте; они обычно вызывают другие симптомы до появления деменции, но иногда имитируют дегенеративную деменцию. К ним относятся недостатки витамин B12, фолиевая кислота, или же ниацин, и инфекционные причины, включая криптококковый менингит, СПИД, Болезнь Лайма, прогрессирующая мультифокальная лейкоэнцефалопатия, подострый склерозирующий панэнцефалит, сифилис, и Болезнь Уиппла.
Лимбическая преобладающая возрастная энцефалопатия TDP-43 (ПОЗДНЕЕ) - это тип деменции, похожий на болезнь Альцгеймера, предложенную в 2019 году.[68] Обычно страдают пожилые люди.[68]
Смешанная деменция
Около 10% людей с деменцией страдают так называемым смешанная деменция, который обычно представляет собой комбинацию болезни Альцгеймера и другого типа деменции, такого как лобно-височная деменция или же сосудистая деменция.[69][70] Наиболее распространенным типом смешанной деменции является болезнь Альцгеймера и сосудистая деменция.[71] Основными проявлениями этого особого типа смешанного слабоумия являются старость, высокое кровяное давление и повреждение кровеносных сосудов головного мозга.[72]
Диагностика смешанной деменции может быть сложной задачей для врача, в большинстве случаев они ошибочно диагностируют пациента как имеющего только один тип деменции. Это делает лечение людей со смешанной деменцией редкостью, и большинство людей с деменцией обходятся без лечения, которое могло бы принести пользу их жизни из-за неправильного диагноза. Ошибочный диагноз является обычным явлением, потому что набор симптомов смешанной деменции варьируется в зависимости от поврежденных или пораженных частей мозга. Когда существует более одного типа деменции, симптомы возникают и быстро ухудшаются, потому что повреждение мозга происходит быстрее, чем при наличии только одного типа деменции.[72]
Диагностика
Симптомы схожи для разных типов деменции, и их трудно диагностировать только по симптомам. В диагностике может помочь: сканирование мозга техники. Во многих случаях для диагностики требуется биопсия головного мозга стать окончательным, но это редко рекомендуется (хотя это может быть выполнено на вскрытие ). У тех, кто стареет, общий скрининг на когнитивные нарушения Использование когнитивного тестирования или ранней диагностики деменции не улучшило исходы.[73] Однако скрининговые экзамены полезны для более чем 65 человек с жалобами на память.[13]
Обычно симптомы должны присутствовать не менее шести месяцев, чтобы подтвердить диагноз.[74] Когнитивная дисфункция меньшей продолжительности называется бред. Делирий можно легко спутать с деменцией из-за схожих симптомов. Делирий характеризуется внезапным началом, неустойчивым течением, короткой продолжительностью (часто от нескольких часов до недель) и в первую очередь связан с соматическим (или медицинским) нарушением. Для сравнения, деменция обычно имеет долгое, медленное начало (за исключением случаев инсульта или травмы), медленное снижение умственной деятельности, а также более длительную траекторию (от месяцев до лет).[75]
Немного психические заболевания, включая депрессия и психоз, может вызывать симптомы, которые необходимо дифференцировать как от делирия, так и от деменции.[76] Следовательно, любая оценка деменции должна включать в себя обследование депрессии, такое как нейропсихиатрический опросник или Гериатрическая шкала депрессии.[13] Раньше врачи считали, что люди с нарушениями памяти страдают депрессией, а не слабоумием (потому что они думали, что люди с деменцией обычно не знают о своих проблемах с памятью). Это называется псевдодеменция. Однако в последние годы исследователи поняли, что многие пожилые люди с нарушениями памяти на самом деле имеют MCI, самую раннюю стадию деменции. Однако депрессия всегда должна оставаться в списке возможностей для пожилого человека с проблемами памяти.
Изменения мышления, слуха и зрения связаны с нормальным старением и могут вызывать проблемы при диагностике деменции из-за сходства.[77]
Когнитивное тестирование
| Тест | Чувствительность | Специфика | Ссылка |
| MMSE | 71%–92% | 56%–96% | [78] |
| 3МС | 83%–93.5% | 85%–90% | [79] |
| AMTS | 73%–100% | 71%–100% | [79] |
Различные краткие тесты (5–15 минут) достаточно надежны для выявления деменции. Хотя многие тесты были изучены,[80][81][82] в настоящее время мини-обследование психического состояния (MMSE) является наиболее изученным и наиболее часто используемым. MMSE - полезный инструмент, помогающий диагностировать деменцию, если результаты интерпретируются вместе с оценкой личности человека, его способности выполнять повседневную деятельность и его поведения.[83] Другие когнитивные тесты включают сокращенный результат интеллектуального тестирования (AMTS), Модифицированный краткий экзамен по психическому состоянию (3МС),[84] то Инструмент для проверки когнитивных способностей (CASI),[85] то Испытание на прокладку маршрута,[86] и тест рисования часов.[87] MoCA (Монреальский когнитивный тест ) - надежный скрининговый тест, доступный в Интернете бесплатно на 35 различных языках.[13] Также было показано, что MoCA несколько лучше выявляет легкие когнитивные нарушения, чем MMSE.[88][89] AD-8 - скрининговая анкета, используемая для оценки функциональных изменений, связанных с когнитивным снижением, - потенциально полезна, но не является диагностической, вариативной и имеет риск систематической ошибки.[90] Краткие когнитивные тесты могут зависеть от таких факторов, как возраст, образование и этническая принадлежность.[91]
Другой подход к скринингу на деменцию - попросить информатора (родственника или другого помощника) заполнить анкету о повседневном когнитивном функционировании человека. Анкеты информаторов предоставляют дополнительную информацию для кратких когнитивных тестов. Вероятно, самый известный вопросник такого рода - это Анкета информатора о когнитивном снижении у пожилых людей (IQCODE).[92] Доказательств недостаточно, чтобы определить, насколько точен IQCODE для диагностики или прогнозирования деменции.[93] Анкета для лиц, осуществляющих уход за больными болезнью Альцгеймера, - еще один инструмент. Точность при болезни Альцгеймера составляет около 90% при использовании опекуном.[13] В Оценка познания врачом общей практики сочетает в себе оценку пациента и интервью с информатором. Он был специально разработан для использования в учреждениях первичной медико-санитарной помощи.
Клинические нейропсихологи проводят диагностические консультации после проведения полного набора когнитивных тестов, часто продолжающихся несколько часов, для определения функциональных паттернов снижения, связанных с различными типами деменции. Актуальны тесты памяти, исполнительной функции, скорости обработки информации, внимания и языковых навыков, а также тесты эмоциональной и психологической адаптации. Эти тесты помогают исключить другие этиологии и определить относительное снижение когнитивных функций с течением времени или исходя из оценок предшествующих когнитивных способностей.
Вместо того, чтобы использовать в качестве дескрипторов «легкую или раннюю стадию», «среднюю стадию» и «позднюю стадию» деменции, числовые шкалы позволяют более детальное описание. Эти шкалы включают: Глобальную шкалу ухудшения состояния для оценки первичной дегенеративной деменции (GDS или шкалу Рейсберга),[94] Функциональный оценочный тест (FAST),[95] и Рейтинг клинической деменции (CDR).
Лабораторные тесты
Рутина анализы крови обычно выполняются для исключения излечимых причин. Эти тесты включают витамин B12, фолиевая кислота, тиреотропный гормон (ТТГ), С-реактивный белок, полный анализ крови, электролиты, кальций, функция почек, и ферменты печени. Аномалии могут указывать на авитаминоз, инфекционное заболевание или другие проблемы, которые обычно вызывают замешательство или дезориентацию у пожилых людей.[нужна цитата ]
Изображения
А компьютерная томография или же магнитно-резонансная томография (МРТ) обычно выполняется, хотя эти тесты не выявляют диффузных метаболических изменений, связанных с деменцией, у человека, который не показывает серьезных неврологических проблем (таких как паралич или слабость) при неврологическом обследовании.[нужна цитата ] КТ или МРТ могут предложить гидроцефалия нормального давления, потенциально обратимая причина деменции, и может дать информацию, относящуюся к другим типам деменции, таким как инфаркт (Инсульт ), что указывает на сосудистый тип деменции.
В функциональная нейровизуализация условия ОФЭКТ и ДОМАШНИЙ ПИТОМЕЦ более полезны для оценки давней когнитивной дисфункции, поскольку они показали такую же способность диагностировать деменцию, как клиническое обследование и когнитивное тестирование.[96] Способность ОФЭКТ дифференцировать сосудистую причину (т. Е. мультиинфарктная деменция ) от деменции, вызванной болезнью Альцгеймера, по-видимому, лучше дифференцировать при клиническом обследовании.[97]
Недавние исследования установили ценность ПЭТ-визуализации с использованием углерод-11 Питтсбургский комплекс B как радиоактивный индикатор (PIB-PET) в прогностической диагностике, особенно Болезнь Альцгеймера. Исследования показали, что PIB-PET с точностью 86% предсказывал, у каких пациентов с легкими когнитивными нарушениями разовьется болезнь Альцгеймера в течение двух лет. В другом исследовании, проведенном с участием 66 пациентов, ПЭТ-исследования с использованием либо PIB, либо другого радиоактивного индикатора, углерода-11. дигидротетрабеназин (DTBZ), позволили поставить более точный диагноз более чем у четверти пациентов с легкими когнитивными нарушениями или легкой деменцией.[98]
Профилактика
Различные факторы могут снизить риск деменции.[6] Группой они могут предотвратить треть случаев. В группу входит раннее воспитание, лечение высокое кровяное давление, предотвращение ожирения, предотвращение потеря слуха, лечение депрессии, физическая активность, профилактика диабета, отказ от курения и социальные связи.[6][99] Снижение риска при здоровом образе жизни наблюдается даже у людей с высоким генетическим риском.[100] Однако обзор 2018 года пришел к выводу, что ни одно лекарство не имеет убедительных доказательств профилактического эффекта, включая лекарства от артериального давления.[101] Обзор 2020 года показал снижение риска деменции или когнитивных проблем с 7,5% до 7,0% при приеме препаратов, снижающих артериальное давление.[102]
Среди в остальном здоровых пожилых людей компьютеризированные когнитивная тренировка может на время улучшить память.[103] Однако неизвестно, предотвращает ли он деменцию.[104][105] Физические упражнения не имеют достаточных доказательств предотвращения деменции.[106][107] Доказательства приема лекарств у людей с нормальной психической функцией недостаточны.[108] То же самое касается добавки.[109]
Раннее внедрение строгая безглютеновая диета в людях с глютеновая болезнь или же не глютеновая чувствительность до начала когнитивных нарушений потенциально имеет защитный эффект.[54]
Управление
За исключением обратимых типов, никаких лекарств не разработано. Ингибиторы холинэстеразы часто используются на ранних стадиях заболевания; однако выгода обычно невелика.[8][110] Другие виды лечения, помимо лекарств, кажутся более эффективными при возбуждении и агрессии, чем лекарства.[111] Могут быть уместными когнитивные и поведенческие вмешательства. Некоторые данные свидетельствуют о том, что образование и поддержка человека с деменцией, а также лиц, осуществляющих уход, и членов семьи улучшают результаты.[112] Программы упражнений полезны для повседневной жизни и потенциально улучшают деменцию.[19]
Эффект лечения можно оценить, например, путем оценки возбуждения (Cohen-Mansfield Agitation Inventory, CMAI); путем оценки настроения и вовлеченности (Шкала вовлеченности Menorah Park, MPES;[113] Шкала наблюдаемых эмоций, OERS[114]) или путем оценки показателей депрессии (Корнеллская шкала депрессии при деменции, CSDD[115][116] или его упрощенная версия[117]).
Психологическая и психосоциальная терапия
Психологические методы лечения деменции включают некоторые ограниченные доказательства воспоминания терапия (а именно, некоторые положительные эффекты в области качества жизни, познания, общения и настроения - первые три, особенно в домашних условиях),[118] некоторая выгода для когнитивный рефрейминг для смотрителей,[119] неясные доказательства для валидационная терапия[120] и предварительные доказательства для умственные упражнения, например, программы когнитивной стимуляции для людей с слабоумием легкой и средней степени тяжести.[121]
Детский сад для взрослых центры, а также специализированные отделения в домах престарелых часто оказывают специализированную помощь пациентам с деменцией. Центры дневного ухода за детьми предлагают участникам присмотр, отдых, питание и ограниченную медицинскую помощь, а также предоставляют передышку лицам, осуществляющим уход. Кроме того, домашний уход может оказывать индивидуальную поддержку и уход на дому, позволяя уделять больше индивидуального внимания, которое требуется по мере прогрессирования заболевания. Психиатрические медсестры могут внести заметный вклад в психическое здоровье людей.[122]
Поскольку деменция нарушает нормальное общение из-за изменений восприимчивого и выразительного языка, а также способности планировать и решать проблемы, возбужденное поведение часто является формой общения для человека с деменцией. Активный поиск потенциальной причины, такой как боль, физическое заболевание или чрезмерная стимуляция, может помочь уменьшить возбуждение.[123] Кроме того, использование «ABC-анализа поведения» может быть полезным инструментом для понимания поведения людей с деменцией. Он включает рассмотрение антецедентов (A), поведения (B) и последствий (C), связанных с событием, чтобы помочь определить проблему и предотвратить дальнейшие инциденты, которые могут возникнуть, если потребности человека будут неправильно поняты.[124] Наиболее убедительными доказательствами в пользу немедикаментозной терапии измененного поведения при деменции являются использование таких подходов.[125] Доказательства низкого качества свидетельствуют о том, что регулярные (не менее пяти сеансов) музыкальная терапия может помочь проживающим в учреждениях. Это может уменьшить симптомы депрессии и улучшить общее поведение. Он также может оказать благотворное влияние на эмоциональное благополучие и качество жизни, а также уменьшить беспокойство.[126] В 2003 г. Общество Альцгеймера учредил проект «Пение для мозга» (SftB), основанный на пилотных исследованиях, которые показали, что это мероприятие поощряет участие и способствует разучиванию новых песен. Сеансы сочетают в себе аспекты терапии воспоминаниями и музыку.[127] Музыкальные и межличностные связи могут подчеркнуть ценность человека и улучшить качество жизни.[128]
Некоторые лондонские больницы обнаружили, что использование цвета, рисунков, изображений и света помогает людям с деменцией приспособиться к пребыванию в больнице. Эти изменения в расположении крыльев деменции в этих больницах помогли пациентам избежать путаницы.[129]
История жизни работа и видеобиографии были найдены для удовлетворения потребностей клиентов и их опекунов различными способами, предлагая клиенту возможность оставить наследство и повысить свою индивидуальность, а также принести пользу молодежи, которая участвует в такой работе. Такие вмешательства будут более эффективными, если они будут предприняты на относительно ранней стадии деменции. Они также могут вызывать проблемы у тех, кто испытывает трудности с обработкой прошлого опыта.[128] (смотрите также: Воспоминания о терапии # Деменция ).
Терапия с использованием животных оказался полезным. Недостатки могут заключаться в том, что домашние животные не всегда приветствуются в общественном месте в учреждении по уходу. Животное может представлять опасность для жителей или может считаться опасным. Некоторые культурные группы также могут считать некоторых животных «нечистыми» или «опасными».[128]
Лекарства

Не было показано никаких лекарств для предотвращения или лечения деменции.[130] Лекарства можно использовать для лечения поведенческих и когнитивных симптомов, но они не влияют на процесс основного заболевания.[13][131]
Ингибиторы ацетилхолинэстеразы, Такие как донепезил, может быть полезно при болезни Альцгеймера[132] и деменция при болезни Паркинсона, DLB или сосудистой деменции.[131] Качество доказательств низкое[133] а польза небольшая.[8] Никаких различий между агентами в этом семействе не выявлено.[17] У меньшинства людей побочные эффекты включают: медленный пульс и обморок.[134] Ривастигмин рекомендуется для лечения симптомов деменции при болезни Паркинсона.[135]
Перед тем, как назначать антипсихотические препараты пожилым людям, необходимо выяснить первопричину поведения.[136] Тяжелые и опасные для жизни реакции возникают почти у половины людей с ДЛБ,[50][137] и может быть смертельным после однократного приема.[138] Люди с деменцией с тельцами Леви, принимающие нейролептики, подвержены риску развития злокачественного нейролептического синдрома, опасного для жизни заболевания.[139] Необходимо соблюдать особую осторожность при использовании антипсихотических препаратов у людей с DLB из-за их чувствительности к этим агентам.[49] Антипсихотические препараты используются для лечения деменции только в том случае, если немедикаментозные методы лечения не помогли, а действия человека угрожают ему самому или другим.[140][141][15][142] Агрессивные изменения поведения иногда являются результатом других решаемых проблем, которые могут сделать ненужным лечение антипсихотиками.[140] Поскольку люди с деменцией могут быть агрессивными, резистентными к их лечению и в других отношениях разрушительными, иногда антипсихотические препараты рассматриваются как ответная терапия.[140] Эти препараты имеют опасные побочные эффекты, в том числе повышают вероятность инсульта и смерти.[140] Принимая во внимание эти побочные эффекты и небольшие преимущества, по возможности следует избегать приема антипсихотиков.[125] Как правило, прекращение приема антипсихотиков у людей с деменцией не вызывает проблем, даже у тех, кто принимал их долгое время.[143]
Рецептор N-метил-D-аспартата (NMDA) блокираторы, такие как мемантин может быть полезным, но доказательства менее убедительны, чем для AChEI.[144] Из-за различий в механизмах действия ингибиторы мемантина и ацетилхолинэстеразы можно использовать в комбинации, однако польза от них незначительна.[145][146]
Пока депрессия часто ассоциируется с деменцией, селективные ингибиторы обратного захвата серотонина (СИОЗС) не влияют на результаты.[147][148] Было продемонстрировано, что СИОЗС сертралин и циталопрам уменьшают симптомы возбуждения по сравнению с плацебо.[149]
Использование лекарств для облегчения нарушений сна, с которыми часто сталкиваются люди с деменцией, не было хорошо изучено, даже в отношении обычно назначаемых лекарств.[150] В 2012 г. Американское гериатрическое общество рекомендовал бензодиазепины Такие как диазепам, и небензодиазепины снотворные, следует избегать людям с деменцией из-за риска увеличения когнитивных нарушений и падений.[151] Кроме того, мало доказательств, подтверждающих эффективность бензодиазепинов в этой популяции.[150][152] Нет четких доказательств того, что мелатонин или же Рамелтеон улучшает сон людей с деменцией из-за болезни Альцгеймера,[150] но он используется для лечения Расстройство быстрого сна при деменции с тельцами Леви.[50] Ограниченные данные свидетельствуют о том, что низкая доза тразодон может улучшить сон, однако необходимы дополнительные исследования.[150]
Нет убедительных доказательств того, что фолиевая кислота или же витамин B12 улучшает результаты у людей с когнитивными проблемами.[153] Статины не имеют пользы при деменции.[154] Для человека с диагнозом деменция может потребоваться другой прием лекарств для лечения других заболеваний. Неясно, связаны ли лекарства от кровяного давления и деменция. Если отменить эти лекарства, у людей может наблюдаться учащение сердечно-сосудистых событий.[155]
В Инструмент подбора лекарств при коморбидных состояниях здоровья при деменции Критерии (MATCH-D) могут помочь определить способы, которыми диагноз деменции изменяет схему приема лекарств при других состояниях здоровья.[156] Эти критерии были разработаны, потому что люди с деменцией живут в среднем с пятью другими хроническими заболеваниями, которые часто лечатся с помощью лекарств.
Боль
С возрастом у людей возникает больше проблем со здоровьем, и большинство проблем со здоровьем, связанных со старением, несут в себе существенное бремя боли; поэтому от 25% до 50% пожилых людей испытывают постоянную боль. Пожилые люди с деменцией сталкиваются с такими же состояниями, которые могут вызвать боль, как и пожилые люди без деменции.[157] У пожилых людей боль часто упускается из виду и при обследовании часто плохо оценивается, особенно среди людей с деменцией, поскольку они становятся неспособными сообщать другим о своей боли.[157][158] Помимо вопросов гуманного ухода, неотвратимая боль имеет функциональные последствия. Постоянная боль может привести к ухудшению передвижения, депрессивному настроению, нарушениям сна, ухудшению аппетита и обострению когнитивных нарушений.[158] и связанное с болью вмешательство в деятельность является фактором, способствующим падению у пожилых людей.[157][159]
Хотя стойкую боль у людей с деменцией сложно выявить, диагностировать и лечить, неспособность устранить постоянную боль имеет глубокие функциональные, психосоциальный и качество жизни последствия для этой уязвимой группы населения. Медицинским работникам часто не хватает навыков и времени, необходимого для распознавания, точной оценки и адекватного мониторинга боли у людей с деменцией.[157][160] Члены семьи и друзья могут внести ценный вклад в уход за больным деменцией, научившись распознавать и оценивать свою боль. Образовательные ресурсы (например, Понять боль и деменцию учебное пособие) и инструменты оценки на основе наблюдений.[157][161][162]
Проблемы с приемом пищи
Люди с деменцией могут испытывать трудности с приемом пищи. Если это доступно в качестве опции, рекомендуемым ответом на проблемы с питанием является присутствие опекуна. помочь им.[140] Второстепенным вариантом для людей, которые не могут эффективно глотать, является рассмотрение: гастростомия питательная трубка размещение как способ дать питание. Однако для обеспечения комфорта и поддержания функционального состояния при одновременном снижении риска аспирационная пневмония и смерть, помощь при пероральном кормлении не хуже, чем через зонд.[140][163] Питание через зонд связано с возбуждением, более частым применением физических и химических средств сдерживания и обострением пролежней. Питание через зонд может вызвать перегрузку жидкостью, диарею, боль в животе, местные осложнения, меньшее взаимодействие с человеком и может увеличить риск аспирации.[164][165]
Польза для людей с запущенной деменцией не показана.[166] Риски использования зондового питания включают возбуждение, отторжение человеком (выдергивание зонда или иное физическое или химическое обездвиживание для предотвращения этого) или развитие пролежни.[140] Эта процедура напрямую связана со смертельным исходом в 1%.[167] с частотой серьезных осложнений 3%.[168] Процент людей с деменцией в конце жизни, пользующихся зондом для кормления, в США упал с 12% в 2000 году до 6% в 2014 году.[169][170]
Рацион питания
Доказано, что диета играет важную роль при заболеваниях памяти и памяти. Доказано, что диеты, которые помогают отсрочить наступление болезни Альцгеймера, улучшают память. Эти диеты, как правило, содержат мало насыщенных жиров, но являются хорошим источником углеводов, в основном тех, которые помогают стабилизировать уровень сахара в крови и инсулина.[171] Уровень сахара в крови может повредить нервы и вызвать проблемы с памятью, если с ними не справиться и не поддерживать их в нормальном состоянии, и самый непоправимый ущерб случается, когда недостаток обслуживания сохраняется в течение многих лет.[172]
В тех, у кого глютеновая болезнь или же не глютеновая чувствительность, а строгая безглютеновая диета может облегчить симптомы при легких когнитивных нарушениях.[54][55] Когда деменция прогрессирует, нет доказательств того, что безглютеновая диета полезна.[54]
Исследования, опубликованные в 2010-х годах, подчеркнули роль факторов питания в предотвращении и снижении риска ювенильных и старческих форм деменции. Пищевые факторы, такие как средиземноморская диета, ненасыщенные жирные кислоты, антиоксиданты (витамин Е, Витамин С, флавоноиды, витамин B ) являются важными компонентами для снижения риска деменции. Точно так же дефицит Витамин Д был статистически связан с увеличением частоты деменции.[173][174]
Упражнение
Программы упражнений могут улучшить способность людей с деменцией выполнять повседневные действия, но лучший тип упражнений все еще неясен.[175] Положительного воздействия на когнитивные способности, психологические симптомы и депрессию не обнаружено.[175] Больше физических упражнений может замедлить развитие когнитивных проблем, таких как деменция, что снижает риск болезни Альцгеймера примерно на 50%. Баланс силовых упражнений, чтобы помочь мышцам перекачивать кровь к мозгу, и упражнения на равновесие рекомендуются для стареющих людей; рекомендуемое количество примерно 2 с половиной часов в неделю может снизить риск когнитивного распада, а также другие риски для здоровья, такие как падение.[176]
Альтернативная медицина
Ароматерапия и массаж есть неясные доказательства.[177][178] Исследования подтверждают эффективность и безопасность каннабиноиды в облегчении поведенческих и психологических симптомов деменции.[179]
Омега-3 жирные кислоты Добавки из растений или рыбы не приносят пользы или вреда людям с болезнью Альцгеймера от легкой до умеренной. Неясно, может ли прием добавок омега-3 жирных кислот улучшить другие типы деменции.[180]
Паллиативная помощь
Учитывая прогрессирующий и неизлечимый характер деменции, паллиативная помощь могут быть полезны пациентам и их опекунам, помогая людям с расстройством и их опекунам понять, чего ожидать, справиться с потерей физических и умственных способностей, поддержать желания и цели человека, включая принятие суррогатных решений, и обсудить пожелания за или против CPR и жизненная поддержка.[181][182] Поскольку спад может быть быстрым, и поскольку большинство людей предпочитают позволить человеку с деменцией принимать собственные решения, рекомендуется участие в паллиативной помощи до поздних стадий деменции.[183][184] Требуются дальнейшие исследования, чтобы определить соответствующие вмешательства паллиативной помощи и насколько хорошо они помогают людям с запущенной деменцией.[185]
Личностно-ориентированная помощь помогает поддерживать достоинство людей с деменцией.[186]
Эпидемиология
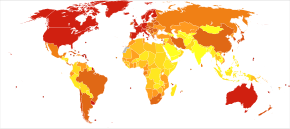

<100 100–120 120–140 140–160 160–180 180–200 | 200–220 220–240 240–260 260–280 280–300 >300 |
Самый распространенный тип деменции - болезнь Альцгеймера.[2] Другие распространенные типы включают сосудистую деменцию, деменцию с тельцами Леви и лобно-височную деменцию.[2][b] Менее распространенные причины включают: гидроцефалия нормального давления, Деменция при болезни Паркинсона, сифилис, ВИЧ, и Болезнь Крейтцфельдта-Якоба.[190]Число случаев деменции во всем мире в 2010 году оценивалось в 35,6 миллиона.[191] В 2015 году 46,8 миллиона человек страдали деменцией, из них 58% - в странах с низким и средним уровнем доходов.[192] Распространенность деменции различается в разных регионах мира: от 4,7% в Центральной Европе до 8,7% в Северной Африке / на Ближнем Востоке; распространенность в других регионах оценивается от 5,6 до 7,6%.[192] По оценкам, количество людей, живущих с деменцией, удваивается каждые 20 лет. В 2013 году деменция стала причиной смерти около 1,9 миллиона человек по сравнению с 0,8 миллиона в 1990 году.[10] Около двух третей людей с деменцией живут в странах с низким и средним уровнем доходов, где в исследовании 2009 года прогнозировалось резкое увеличение численности.[191]
Ежегодная заболеваемость деменцией во всем мире составляет более 9,9 миллиона человек. Почти половина новых случаев деменции происходит в Азии, за которой следуют Европа (25%), Америка (18%) и Африка (8%). Заболеваемость деменцией экспоненциально увеличивается с возрастом, удваиваясь каждые 6,3 года с возрастом.[192] Деменция поражает 5% населения старше 65 лет и 20–40% людей старше 85 лет.[193] Показатели немного выше у женщин, чем у мужчин в возрасте 65 лет и старше.[193]
Деменция поражает не только людей, страдающих деменцией, но и тех, кто за ними ухаживает, и общество в целом. Среди людей в возрасте 60 лет и старше деменция занимает 9-е место среди наиболее обременительных состояний по данным 2010 г. Глобальное бремя болезней (ГББ) оценки. Глобальные затраты на деменцию составили около 818 миллиардов долларов США в 2015 году, что на 35,4% больше, чем 604 миллиарда долларов США в 2010 году.[192]
История
Эта секция нужны дополнительные цитаты для проверка. (Ноябрь 2015) (Узнайте, как и когда удалить этот шаблон сообщения) |
До конца XIX века деменция была гораздо более широким клиническим понятием. Сюда входили психические заболевания и любой тип психосоциальной неспособности, включая обратимые состояния.[194] Слабоумие в то время просто относился к любому, кто потерял способность рассуждать, и в равной степени относился к психозам, «органическим» заболеваниям, таким как сифилис которые разрушают мозг, и к слабоумию, связанному со старостью, которое было приписано "затвердение артерий ".
Деменция упоминается в медицинских текстах с тех пор, как древность. Один из самых ранних намеков на деменцию относится к 7 веку до нашей эры. Греческий философ Пифагор, которые разделили продолжительность жизни человека на шесть отдельных фаз: 0–6 (младенчество), 7–21 (юность), 22–49 (юная взрослая жизнь), 50–62 (средний возраст), 63–79 (старость) и 80 - смерть (пожилой возраст). Последние два он описал как «сениум», период умственного и физического упадка, и что заключительная фаза наступила, когда «сцена смертного существования закрывается по прошествии длительного периода времени, к которому, к счастью, немногие из человеческих видов прибывают. , где ум сведен к слабоумию первой эпохи младенчества ».[195] В 550 г. до н.э. афинский государственный деятель и поэт Солон утверждал, что условия завещания мужчины могут быть признаны недействительными, если он демонстрирует потерю рассудительности из-за преклонного возраста. Китайская медицина тексты также ссылаются на это состояние, а символы «слабоумие» буквально переводятся как «глупый старик».[196]
Афиняне Аристотель и Платон говорил о умственном разложении пожилого возраста, очевидно рассматривая его как неизбежный процесс, который затрагивает всех стариков и которому ничто не может предотвратить. Платон утверждал, что пожилые люди не подходят для какой-либо ответственной должности, потому что «не так много сообразительности, которая когда-то несла их в молодости, - те характеристики, которые можно было бы назвать суждением, воображением, силой рассуждения и памятью. Они видят их. постепенно притупляются из-за ухудшения и с трудом могут выполнять свою функцию ».[нужна цитата ]
Для сравнения, римский государственный деятель Цицерон придерживался точки зрения, которая в большей степени соответствовала современной медицинской мудрости, согласно которой потеря умственной функции не была неизбежной для пожилых людей и «затрагивала только тех стариков, которые были безвольными». Он говорил о том, как те, кто остается умственно активным и стремится узнавать новое, могут предотвратить деменцию. Однако взгляды Цицерона на старение, хотя и прогрессивные, в значительной степени игнорировались в мире, в котором на протяжении столетий доминировали медицинские труды Аристотеля. Врачи времен Римской империи, такие как Гален и Цельс, просто повторил убеждения Аристотеля, добавив при этом несколько новых вкладов в медицинские знания.
византийский врачи иногда писали о деменции. Зарегистрировано, что по крайней мере семь императоров, чья продолжительность жизни превышала 70 лет, демонстрировали признаки снижения умственных способностей. В Константинополь в специальных больницах размещались люди с диагнозом слабоумие или безумие, но это не относилось к императорам, которые стояли выше закона и состояние здоровья которых не могло быть публично признано.
В остальном, в западных медицинских текстах почти 1700 лет мало говорится о деменции. Одним из немногих упоминаний был монах XIII века. Роджер Бэкон, которые считали старость божественным наказанием за первородный грех. Хотя он повторил существующие аристотелевские убеждения о неизбежности деменции, он все же сделал прогрессивное утверждение, что мозг является центром памяти и мысли, а не сердце.
Поэты, драматурги и другие писатели часто упоминали о потере умственных способностей в старости. Уильям Шекспир особенно упоминает это в пьесах, таких как Гамлет и Король Лир.
В 19 веке врачи в основном полагали, что старческое слабоумие является результатом церебральный атеросклероз, хотя мнения колебались между идеей, что это произошло из-за закупорки крупных артерий, снабжающих мозг, или небольших ударов в сосудах головного мозга. кора головного мозга.
В 1907 г. Болезнь Альцгеймера был описан. Это было связано с особыми микроскопическими изменениями в головном мозге, но считалось редким заболеванием среднего возраста, потому что первым диагнозом этого заболевания был 50-летняя женщина. К 1913–20 гг. шизофрения был четко определен, как и в более поздние времена.
Эта точка зрения оставалась традиционной медицинской мудростью в течение первой половины 20-го века, но к 1960-м годам ее все больше оспаривали как связь между нейродегенеративные заболевания установлено возрастное когнитивное снижение. К 1970-м годам медицинское сообщество утверждало, что сосудистая деменция встречается реже, чем считалось ранее, а болезнь Альцгеймера является причиной подавляющего большинства умственных нарушений в пожилом возрасте. Однако в последнее время считается, что деменция часто представляет собой смесь состояний.
В 1976 г. невролог Роберт Кацманн предположил связь между старческим слабоумием и болезнью Альцгеймера.[197] Кацманн предположил, что большая часть старческого слабоумия, возникающего (по определению) после 65 лет, патологически идентична болезни Альцгеймера, возникающей у людей в возрасте до 65 лет, и поэтому не следует лечить иначе.[198] Таким образом, Кацманн предположил, что болезнь Альцгеймера, если она возникает в возрасте старше 65 лет, на самом деле встречается часто, а не редко, и была четвертой или пятой по значимости причиной смерти, хотя в 1976 году она редко указывалась в свидетельствах о смерти.
Полезным открытием было то, что, хотя заболеваемость болезнью Альцгеймера увеличивалась с возрастом (с 5–10% среди 75-летних до 40–50% среди 90-летних), не было найдено порогового значения, к которому возраст всех человек разработал это. Об этом свидетельствуют документально подтвержденные сверх долгожители (люди, дожившие до 110 лет и более), у которых не было существенных когнитивных нарушений. Некоторые данные свидетельствуют о том, что деменция с наибольшей вероятностью разовьется в возрасте от 80 до 84 лет, а у людей, которые прошли эту точку без какого-либо воздействия, вероятность ее развития ниже. На долю женщин приходится больший процент случаев деменции, чем на мужчин, хотя это можно объяснить более длительной общей продолжительностью их жизни и более высокими шансами достичь возраста, в котором это состояние может возникнуть.[нужна цитата ]
Как и другие болезни, связанные со старением, деменция была сравнительно редкой до 20 века, потому что немногие люди доживали до 80 лет. И наоборот, сифилитическая деменция была широко распространена в развитых странах, пока ее не искоренили с помощью пенициллин после Вторая Мировая Война. После значительного увеличения продолжительности жизни число людей старше 65 лет начало быстро расти. Хотя до 1945 года пожилые люди составляли в среднем 3-5% населения, к 2010 году во многих странах этот показатель достиг 10-14%, а в Германии и Японии этот показатель превысил 20%. Осведомленность общественности о болезни Альцгеймера значительно возросла в 1994 году, когда бывший президент США Рональд Рейган объявил, что ему поставили диагноз.
В 21 веке другие виды деменции были дифференцированы от болезни Альцгеймера и сосудистой деменции (наиболее распространенные типы). Эта дифференциация основана на патологическом исследовании тканей мозга, по симптоматике и по различным моделям метаболической активности мозга в тестах ядерной медицинской визуализации, таких как ОФЭКТ и ПЭТ-сканирование мозга. Различные формы имеют разные прогнозы и разные эпидемиологические факторы риска. Причинная этиология, то есть причина или происхождение многих из них, включая болезнь Альцгеймера, остается неясной.[нужна цитата ]
Терминология
Деменцию у пожилых людей когда-то называли старческое слабоумие или же старость, и рассматривается как нормальный и несколько неизбежный аспект старения. Эта терминология больше не является стандартной.[199][200]
К 1913–20 гг. Срок раннее слабоумие был введен, чтобы предположить развитие деменции старческого типа в более молодом возрасте. В конце концов эти два термина соединились, так что до 1952 года врачи использовали термины раннее слабоумие (преждевременная деменция) и шизофрения взаимозаменяемо. С тех пор наука определила, что деменция и шизофрения - два разных заболевания, хотя у них есть некоторые общие черты.[201] Период, термин преждевременное слабоумие для психического заболевания предполагал, что такой тип психического заболевания, как шизофрения (включая паранойя и снижение когнитивных способностей) можно ожидать нормально у всех людей старшего возраста (см. парафрения ). Примерно после 1920 года начало использования слабоумие поскольку то, что сейчас понимается как шизофрения и старческое слабоумие, помогло ограничить значение этого слова до «постоянного, необратимого умственного ухудшения». С этого началось изменение более позднего использования термина. В недавних исследованиях исследователи обнаружили связь между теми, у кого диагностирована шизофрения, и пациентами, у которых диагностирована деменция, и обнаружили положительную корреляцию между этими двумя заболеваниями.[202]
Мнение о том, что деменция всегда должна быть результатом определенного болезненного процесса, на какое-то время привело к предложению диагноза «старческое слабоумие типа Альцгеймера» (SDAT) у лиц старше 65 лет, с диагнозом «болезнь Альцгеймера» у людей. моложе 65 лет с такой же патологией. В конце концов, однако, было решено, что возрастное ограничение было искусственным и что Болезнь Альцгеймера был подходящим термином для людей с данной патологией головного мозга, независимо от возраста.
После 1952 года психические заболевания, в том числе шизофрения, были исключены из категории органические мозговые синдромы, и таким образом (по определению) исключены из возможных причин «безумных болезней» (деменции). В то же время, однако, традиционная причина старческого слабоумия - «уплотнение артерий» - теперь вернулась в виде набора деменций сосудистого происхождения (небольшие инсульты). Теперь они были названы мультиинфарктная деменция или же сосудистая деменция.
Общество и культура

Социальные издержки деменции высоки, особенно для членов семьи.[203]
Многие страны считают заботу о людях, страдающих деменцией, национальным приоритетом и вкладывают средства в ресурсы и образование, чтобы лучше информировать медицинских и социальных работников, лиц, осуществляющих неоплачиваемый уход, родственников и членов более широкого сообщества. Несколько стран разработали национальные планы или стратегии.[204][205] В этих планах признается, что люди могут разумно жить с деменцией в течение многих лет при условии наличия необходимой поддержки и своевременного доступа к диагностике. Премьер-министр Великобритании Дэвид Кэмерон описал деменцию как «национальный кризис», от которого страдают 800 000 человек в Соединенном Королевстве.[206]
Там, как и при всех психических расстройствах, люди с деменцией потенциально могут представлять опасность для себя или других, они могут содержаться под стражей в Закон о психическом здоровье 1983 г. для оценки, ухода и лечения. Это последнее средство, и обычно его избегают люди с семьей или друзьями, которые могут обеспечить уход.
Некоторые больницы в Британии работают над тем, чтобы обеспечить более качественную и дружелюбную помощь. Чтобы сделать палаты более спокойными и менее перегруженными для жителей, персонал заменил обычное место медсестер на несколько столов меньшего размера, похожих на приемную. Яркое освещение помогает улучшить настроение и позволяет жителям лучше видеть.[207]
Вождение при деменции может привести к травмам или смерти. Врачи должны посоветовать провести соответствующее обследование, когда следует отказаться от вождения.[208] Объединенное королевство DVLA (Агентство по лицензированию водителей и транспортных средств) заявляет, что людям с деменцией, у которых особенно плохая кратковременная память, дезориентация или отсутствие понимания или суждения, не разрешается водить машину, и в этих случаях необходимо проинформировать DVLA, чтобы водительские права могли быть отозванным. Они признают, что в случаях легкой степени тяжести и при ранней диагностике водителям может быть разрешено продолжить движение.
Для людей с деменцией, их семей и лиц, осуществляющих уход, доступно множество сетей поддержки. Благотворительные организации нацелены на повышение осведомленности и кампании за права людей, живущих с деменцией. Доступны поддержка и рекомендации по оценке способности завещания у людей с деменцией.[209]
В 2015 году Atlantic Philanthropies объявила о подарке в размере 177 миллионов долларов, направленном на понимание и уменьшение деменции. Получателем был Глобальный институт здоровья мозга, программа, возглавляемая Калифорнийский университет в Сан-Франциско и Тринити-колледж Дублина. Это пожертвование является самым крупным грантом, не связанным с капиталом, который когда-либо делала Atlantic, и самым крупным благотворительным пожертвованием в истории Ирландии.[210]
2 ноября 2020 года шотландский миллиардер сэр Том Хантер пожертвовал 1 миллион фунтов стерлингов благотворительным организациям, работающим с деменцией, после того, как увидел, как бывший учитель музыки с деменцией Пол Харви играет на пианино, используя всего четыре ноты в вирусном видео. Было объявлено, что пожертвование будет разделено между Обществом Альцгеймера и Music for Dementia.[211]
Здоровье зубов
Ограниченные данные связывают плохое здоровье полости рта с когнитивным снижением. Однако невыполнение чистки зубов и воспаление десен могут использоваться в качестве предикторов риска деменции.[212]
Оральные бактерии
Связь между болезнью Альцгеймера и заболевания десен является бактерии полости рта.[213] В полости рта к видам бактерий относятся: P. gingivalis, F. nucleatum, P. intermedia, и T. forsythia. Шесть оральных трепоменов спирохеты были исследованы в мозге пациентов с болезнью Альцгеймера.[214] Спирохеты по своей природе нейротропны, то есть они разрушают нервную ткань и вызывают воспаление. Воспалительные патогены являются индикатором болезни Альцгеймера, а бактерии, связанные с заболеванием десен, были обнаружены в мозге людей, страдающих болезнью Альцгеймера.[214] Бактерии проникают в нервную ткань головного мозга, увеличивая проницаемость гематоэнцефалический барьер и способствуя возникновению болезни Альцгеймера. Люди с множеством зубных отложений рискуют снизить когнитивные способности.[215] Плохая гигиена полости рта может отрицательно сказаться на речи и питании, вызывая ухудшение общего и когнитивного здоровья.
Оральные вирусы
Вирус простого герпеса (HSV) был обнаружен более чем у 70% людей в возрасте старше 50 лет. HSV сохраняется в периферической нервной системе и может быть вызван стрессом, болезнью или усталостью.[214] Высокие доли ассоциированных с вирусами белков в амилоидсодержащих бляшках или нейрофибриллярные сплетения (NFT) подтверждают участие HSV-1 в патологии болезни Альцгеймера. NFT известны как первичный маркер болезни Альцгеймера. HSV-1 производит основные компоненты NFT.[216]
Примечания
- ^ Продромальный подтипы делирия с началом деменция с тельцами Леви были предложены по состоянию на 2020 год.[12]
- ^ Косака (2017) пишет: «Деменция с тельцами Леви (DLB) сейчас хорошо известна как вторая по частоте деменция после болезни Альцгеймера (AD). Известно, что из всех типов деменции на AD приходится около 50%, DLB - около 50%. 20% и сосудистая деменция (VD) около 15%. Таким образом, AD, DLB и VD теперь считаются тремя основными видами деменции ».[187] В NINDS (2020) говорится, что деменция с тельцами Леви «является одной из наиболее частых причин деменции после болезни Альцгеймера и сосудистых заболеваний».[188] Херши (2019) говорит: «ДЛБ занимает третье место среди всех нейродегенеративных заболеваний после болезни Альцгеймера и болезни Паркинсона».[189]
Рекомендации
- ^ «Деменция». MedlinePlus. Национальная медицинская библиотека США. 14 мая 2015. В архиве из оригинала 12 мая 2015 г.. Получено 6 августа 2018.
Деменция Также называется: старость.
- ^ а б c d е ж грамм час я j k л м п «Информационный бюллетень № 362 о деменции». who.int. Апрель 2012. Архивировано с оригинал 18 марта 2015 г.. Получено 28 ноября 2014.
- ^ а б c d е ж грамм Бернс А., Илифф С. (февраль 2009 г.). «Деменция». BMJ. 338: b75. Дои:10.1136 / bmj.b75. PMID 19196746. S2CID 220101432.
- ^ а б «Диагностика и оценка деменции» (PDF). pathways.nice.org.uk. Архивировано из оригинал (PDF) 5 декабря 2014 г.. Получено 30 ноября 2014.
- ^ Хейлз, Роберт Э. (2008). Американский учебник психиатрии по психиатрии. Американский психиатрический паб. п. 311. ISBN 978-1-58562-257-3. В архиве из оригинала от 08.09.2017.
- ^ а б c Ливингстон Дж., Соммерлад А., Оргета В., Костафреда С. Г., Хантли Дж., Эймс Д. и др. (Декабрь 2017 г.). «Профилактика деменции, вмешательство и уход». Ланцет (Представлена рукопись). 390 (10113): 2673–2734. Дои:10.1016 / S0140-6736 (17) 31363-6. PMID 28735855. S2CID 27466779.
- ^ а б c Кавираджан Х., Шнайдер Л.С. (сентябрь 2007 г.). «Эффективность и побочные эффекты ингибиторов холинэстеразы и мемантина при сосудистой деменции: метаанализ рандомизированных контролируемых исследований». Ланцет. Неврология. 6 (9): 782–92. Дои:10.1016 / с1474-4422 (07) 70195-3. PMID 17689146. S2CID 1291571.
- ^ а б c d Комиссия по прозрачности (июнь 2012 г.). «Лекарства от болезни Альцгеймера: лучше избегать. Нет терапевтических преимуществ» [Лекарства от болезни Альцгеймера: лучше избегать. Нет терапевтического преимущества. Prescrire International. 21 (128): 150. PMID 22822592.
- ^ а б c d е ж грамм час я «Деменция». www.who.int. Получено 7 ноября 2020.
- ^ а б c ГББ 2015 «Смертность и причины смерти соавторов» (октябрь 2016 г.). «Ожидаемая продолжительность жизни на глобальном, региональном и национальном уровнях, смертность от всех причин и смертность от конкретных причин для 249 причин смерти, 1980–2015 гг .: систематический анализ для исследования глобального бремени болезней 2015 г.». Ланцет. 388 (10053): 1459–1544. Дои:10.1016 / с0140-6736 (16) 31012-1. ЧВК 5388903. PMID 27733281.
- ^ «Нормальное старение против деменции». Общество Альцгеймера. Получено 22 ноября 2020.
- ^ МакКейт И.Г., Ферман Т.Дж., Томас А.Дж. и др. (Апрель 2020 г.). «Критерии исследования для диагностики продромальной деменции с тельцами Леви». Неврология (Рассмотрение). 94 (17): 743–55. Дои:10.1212 / WNL.0000000000009323. ЧВК 7274845. PMID 32241955.
- ^ а б c d е ж грамм час я j k л м п о п q р s т ты Будсон А., Соломон П. (2011). Потеря памяти: практическое руководство для врачей. [Эдинбург?]: Эльзевьер Сондерс. ISBN 978-1-4160-3597-8.
- ^ а б c Американская психиатрическая ассоциация (2013 г.). Диагностическое и статистическое руководство психических расстройств: DSM-5 (5-е изд.). Вашингтон, округ Колумбия: Американская психиатрическая ассоциация. стр.591–603. ISBN 978-0-89042-554-1.
- ^ а б «Деменция: оценка, лечение и поддержка людей, живущих с деменцией, и лиц, осуществляющих уход за ними | Рекомендации и рекомендации | NICE». ОТЛИЧНО. Получено 18 декабря 2018.
- ^ «Обзор деменции» (PDF). pathways.nice.org.uk. В архиве (PDF) из оригинала 5 декабря 2014 г.. Получено 30 ноября 2014.
- ^ а б Биркс Дж (январь 2006 г.). Биркс Дж.С. (ред.). «Ингибиторы холинэстеразы при болезни Альцгеймера». Кокрановская база данных систематических обзоров (1): CD005593. Дои:10.1002 / 14651858.CD005593. PMID 16437532.
- ^ Ролински М., Фокс С., Мейдмент I, МакШейн Р. (март 2012 г.). «Ингибиторы холинэстеразы при деменции с тельцами Леви, деменции при болезни Паркинсона и когнитивных нарушениях при болезни Паркинсона» (PDF). Кокрановская база данных систематических обзоров. 3 (3): CD006504. Дои:10.1002 / 14651858.CD006504.pub2. PMID 22419314.
- ^ а б Forbes D, Forbes SC, Блейк CM, Thiessen EJ, Forbes S (апрель 2015 г.). «Программы упражнений для людей с деменцией». Кокрановская база данных систематических обзоров (Представлена рукопись). 132 (4): 195–96. Дои:10.1002 / 14651858.CD006489.pub4. PMID 25874613.
- ^ Национальный институт здоровья и клинического совершенства. «Низкие дозы нейролептиков у людей с деменцией». nice.org.uk. Архивировано из оригинал 5 декабря 2014 г.. Получено 29 ноябрь 2014.
- ^ «Информация для медицинских работников: традиционные нейролептики». fda.gov. 2008-06-16. В архиве из оригинала 29 ноября 2014 г.. Получено 29 ноябрь 2014.
- ^ Соавторы исследования ГББ 2015 по заболеваемости и распространенности заболеваний и травм (октябрь 2016 г.). «Глобальная, региональная и национальная заболеваемость, распространенность и годы, прожитые с инвалидностью для 310 заболеваний и травм, 1990–2015 годы: систематический анализ для исследования глобального бремени болезней 2015». Ланцет. 388 (10053): 1545–1602. Дои:10.1016 / S0140-6736 (16) 31678-6. ЧВК 5055577. PMID 27733282.
- ^ Лой CT, Schofield PR, Turner AM, Kwok JB (март 2014 г.). «Генетика деменции». Ланцет. 383 (9919): 828–40. Дои:10.1016 / с0140-6736 (13) 60630-3. PMID 23927914. S2CID 2525888.
- ^ а б c Ларсон Э.Б., Яффе К., Ланга К.М. (декабрь 2013 г.). «Новые взгляды на эпидемию деменции». Медицинский журнал Новой Англии. 369 (24): 2275–77. Дои:10.1056 / nejmp1311405. ЧВК 4130738. PMID 24283198.
- ^ Умфред, Дарси (2012). Неврологическая реабилитация (6-е изд.). Сент-Луис, Миссури: Эльзевьер Мосби. п. 838. ISBN 978-0-323-07586-2. В архиве из оригинала от 22 апреля 2016 г.
- ^ «Деменция - признаки и симптомы». Американская ассоциация слуха на языке речи.
- ^ «Деменция: сопутствующие заболевания у пациентов - информация». GOV.UK. Получено 22 ноября 2020.
- ^ а б c Шахин Джанкуртаран, Э (декабрь 2014 г.). «Управление поведенческими и психологическими симптомами деменции». Норо Псикиятри Арсиви. 51 (4): 303–12. Дои:10.5152 / нпа.2014.7405. ЧВК 5353163. PMID 28360647.
- ^ Сережейра Дж., Лагарто Л., Мукаетова-Ладинская Е.Б. (2012). «Поведенческие и психологические симптомы деменции». Границы неврологии. 3: 73. Дои:10.3389 / fneur.2012.00073. ЧВК 3345875. PMID 22586419.
- ^ Каллео Дж, Стэнли М (2008). «Тревожные расстройства в дифференцированной диагностике и стратегиях лечения в более позднем возрасте». Психиатрические времена. 25 (8). В архиве из оригинала от 04.09.2009.
- ^ Шуб Д., Куник М.Е. (16 апреля 2009 г.). «Коморбидность психических заболеваний у лиц с деменцией: оценка и стратегии лечения». Психиатрические времена. 26 (4). В архиве с оригинала от 27 апреля 2009 г.
- ^ "Психологический словарь АПА". Dictionary.apa.org. Получено 15 декабря 2020.
- ^ а б Хьюго Дж., Гангули М. (август 2014 г.). «Деменция и когнитивные нарушения: эпидемиология, диагностика и лечение». Клиники гериатрической медицины. 30 (3): 421–42. Дои:10.1016 / j.cger.2014.04.001. ЧВК 4104432. PMID 25037289.
- ^ Дженкинс, Кэтрин (26 января 2016). Краткий обзор помощи при деменции. Гинези, Лаура; Кинан, Берни. Чичестер, Западный Сассекс. ISBN 978-1-118-85998-8. OCLC 905089525.
- ^ Рорер Дж. Д., Найт В. Д., Уоррен Дж. Э., Фокс Северная Каролина, Россор Миннесота, Уоррен Дж. Д. (январь 2008 г.). «Трудность с поиском слов: клинический анализ прогрессирующих афазий». Мозг. 131 (Pt 1): 8–38. Дои:10.1093 / мозг / awm251. ЧВК 2373641. PMID 17947337.
- ^ Ислам, Махин; Мазумдер, Мридул; Швабе-Варф, Дерек; Стефан, Янник; Сутин, Ангелина Р .; Терраччано, Антонио (февраль 2019 г.). «Изменения личности при деменции с точки зрения информатора: новые данные и метаанализ». Журнал Американской ассоциации медицинских директоров. 20 (2): 131–137. Дои:10.1016 / j.jamda.2018.11.004. ЧВК 6432780. PMID 30630729.
- ^ «Диагностика деменции с тельцами Леви». Национальный институт старения. Получено 10 мая 2020.
- ^ Lindau, M .; Альмквист, О .; Kushi, J .; Бун, К .; Johansson, S.E .; Wahlund, L.O .; Cummings, J.L .; Миллер, Б. (2000). «Первые симптомы - лобно-височная деменция против болезни Альцгеймера». Деменция и гериатрические когнитивные расстройства. 11 (5): 286–293. Дои:10.1159/000017251. ISSN 1420-8008. PMID 10940680. S2CID 22599923.
- ^ Уилсон Р.С., Сыцма Дж., Барнс Л.Л., Бойл П.А. (сентябрь 2016 г.). «Анозогнозия при деменции». Текущие отчеты по неврологии и неврологии. 16 (9): 77. Дои:10.1007 / s11910-016-0684-z. PMID 27438597. S2CID 3331009.
- ^ Сундерараман П., Косентино С. (март 2017 г.). «Интеграция конструкций анозогнозии и метапознания: обзор последних результатов в области деменции». Текущие отчеты по неврологии и неврологии. 17 (3): 27. Дои:10.1007 / s11910-017-0734-1. ЧВК 5650061. PMID 28283961.
- ^ Эриксон К. (27.09.2013). Как мы умираем сейчас: близость и работа по умиранию. Издательство Темплского университета. С. 109–11. ISBN 978-1-4399-0823-5. В архиве из оригинала от 23 декабря 2016 г.
- ^ Виджаян М., Редди PH (6 сентября 2016 г.). «Инсульт, сосудистая деменция и болезнь Альцгеймера: молекулярные связи». Журнал болезни Альцгеймера: JAD. 54 (2): 427–43. Дои:10.3233 / JAD-160527. ЧВК 5793908. PMID 27567871.
- ^ Дюбуа Б., Хэмпел Х., Фельдман Х. Х. и др. (Март 2016 г.). «Доклиническая болезнь Альцгеймера: определение, естественное течение и диагностические критерии». Демент Альцгеймера. 12 (3): 292–323. Дои:10.1016 / j.jalz.2016.02.002. ЧВК 6417794. PMID 27012484.
- ^ Хуссейн М., Бергер М., Экенхофф Р.Г., Зейтц Д.П. (2014). «Общая анестезия и риск деменции у пожилых пациентов: текущие выводы». Клинические вмешательства при старении. 9: 1619–28. Дои:10.2147 / CIA.S49680. ЧВК 4181446. PMID 25284995.
- ^ а б «Семь стадий деменции | Симптомы, прогрессирование и продолжительность». Получено 19 декабря 2020.
- ^ «Клинические стадии болезни Альцгеймера». Центр Фишера Фонда исследований болезни Альцгеймера. 29 января 2014 г.. Получено 19 декабря 2020.
- ^ а б Iadecola C (ноябрь 2013 г.). «Патобиология сосудистой деменции». Нейрон. 80 (4): 844–66. Дои:10.1016 / j.neuron.2013.10.008. ЧВК 3842016. PMID 24267647.
- ^ Юрек Л., Херрманн М., Бонзе М. и др. (1 марта 2018 г.). «Поведенческие и психологические симптомы при болезни тельцов Леви: обзор». Geriatrie et Psychologie Neuropsychiatrie du Vieillissement. 16 (1): 87–95. Дои:10.1684 / pnv.2018.0723. PMID 29569570.
- ^ а б c d МакКейт И.Г., Боев Б.Ф., Диксон Д.В. и др. (Июль 2017 г.). «Диагностика и лечение деменции с тельцами Леви: Четвертый консенсусный отчет Консорциума DLB». Неврология (Рассмотрение). 89 (1): 88–100. Дои:10.1212 / WNL.0000000000004058. ЧВК 5496518. PMID 28592453.
- ^ а б c Тейлор Дж. П., МакКейт И. Г., Бёрн Д. Д. и др. (Февраль 2020 г.). «Новые данные о лечении деменции с тельцами Леви». Ланцет Нейрол (Рассмотрение). 19 (2): 157–69. Дои:10.1016 / С1474-4422 (19) 30153-Х. ЧВК 7017451. PMID 31519472. Доступна любезная ссылка здесь.
- ^ Фингер, Элизабет К. (апрель 2016 г.). «Лобно-височное слабоумие». Continuum (Миннеаполис, Миннесота). 22 (2 Деменция): 464–489. Дои:10.1212 / CON.0000000000000300. ISSN 1538-6899. ЧВК 5390934. PMID 27042904.
- ^ Шофилд П. (2005). «Деменция, связанная с токсическими причинами и аутоиммунным заболеванием». Международная психогериатрия (Рассмотрение). 17 Дополнение 1: S129–47. Дои:10,1017 / с1041610205001997. HDL:1959.13/24647. PMID 16240488.
- ^ а б Розенблум М. Х., Смит С., Акдал Г., Гешвинд М. Д. (сентябрь 2009 г.). «Иммунологически опосредованные деменции». Текущие отчеты по неврологии и неврологии (Рассмотрение). 9 (5): 359–67. Дои:10.1007 / s11910-009-0053-2. ЧВК 2832614. PMID 19664365.
- ^ а б c d е Зис П., Хадживассилёв М. (26 февраля 2019 г.). «Лечение неврологических проявлений чувствительности к глютену и целиакии». Варианты лечения Curr Neurol (Рассмотрение). 21 (3): 10. Дои:10.1007 / s11940-019-0552-7. PMID 30806821.
- ^ а б c Махлуф С., Мессельмани М., Зауали Дж., Мрисса Р. (2018). «Когнитивные нарушения при глютеновой болезни и не глютеновой чувствительности: обзор литературы по основным когнитивным нарушениям, визуализации и влиянию безглютеновой диеты». Acta Neurol Belg (Рассмотрение). 118 (1): 21–27. Дои:10.1007 / s13760-017-0870-z. PMID 29247390. S2CID 3943047.
- ^ Дауэс, П. (март 2019 г.). «Слуховые вмешательства для предотвращения деменции». HNO. 67 (3): 165–171. Дои:10.1007 / s00106-019-0617-7. ЧВК 6399173. PMID 30767054.
- ^ Томсон, РС; Auduong, P; Миллер, AT; Гургель, РК (апрель 2017 г.). «Потеря слуха как фактор риска деменции: систематический обзор». Ларингоскоп Исследовательская отоларингология. 2 (2): 69–79. Дои:10.1002 / lio2.65. ЧВК 5527366. PMID 28894825.
- ^ Арсланд Д., Курц М.В. (февраль 2010 г.). «Эпидемиология деменции, связанной с болезнью Паркинсона». Журнал неврологических наук (Рассмотрение). 289 (1–2): 18–22. Дои:10.1016 / j.jns.2009.08.034. PMID 19733364. S2CID 24541533.
- ^ Гэлвин Дж., Поллак Дж., Моррис Дж. К. (ноябрь 2006 г.). «Клинический фенотип деменции при болезни Паркинсона». Неврология. 67 (9): 1605–11. Дои:10.1212 / 01.wnl.0000242630.52203.8f. PMID 17101891. S2CID 25023606.
- ^ Аббаси, Дженнифер (21 августа 2019 г.). «Споры разгорелись ПОЗДНЕЕ, недавно выявленное слабоумие». JAMA. 322 (10): 914. Дои:10.1001 / jama.2019.12232. PMID 31433447.
- ^ Ламонт П. (2004). «Когнитивный спад у молодого взрослого с предсуществующей задержкой развития - что должен знать взрослый невролог». Практическая неврология. 4 (2): 70–87. Дои:10.1111 / j.1474-7766.2004.02-206.x. Архивировано из оригинал на 2008-10-07. Получено 2009-10-12.
- ^ Ланга К.М., Левин Д.А. (декабрь 2014 г.). «Диагностика и лечение легких когнитивных нарушений: клинический обзор». JAMA. 312 (23): 2551–61. Дои:10.1001 / jama.2014.13806. ЧВК 4269302. PMID 25514304.
- ^ Группа невропатологии. Исследование когнитивных функций и старения Совета по медицинским исследованиям (январь 2001 г.). «Патологические корреляты слабоумия с поздним началом в многоцентровом населении в Англии и Уэльсе. Группа невропатологии Совета медицинских исследований по исследованию когнитивных функций и старения (MRC CFAS)». Ланцет. 357 (9251): 169–75. Дои:10.1016 / S0140-6736 (00) 03589-3. PMID 11213093. S2CID 22754910.
- ^ Вакисака Ю., Фурута А., Танидзаки Ю., Киёхара Ю., Иида М., Иваки Т. (октябрь 2003 г.). «Возрастная распространенность и факторы риска патологии с тельцами Леви в общей популяции: исследование Хисаямы». Acta Neuropathologica. 106 (4): 374–82. Дои:10.1007 / s00401-003-0750-х. PMID 12904992. S2CID 19426443.
- ^ Уайт Л., Петрович Х., Хардман Дж., Нельсон Дж., Дэвис Д.Г., Росс Г.В. и др. (Ноябрь 2002 г.). «Цереброваскулярная патология и деменция у вскрытых участников исследования старения в Гонолулу-Азии». Летопись Нью-Йоркской академии наук. 977 (9): 9–23. Bibcode:2002НЯСА.977 .... 9Вт. Дои:10.1111 / j.1749-6632.2002.tb04794.x. PMID 12480729. S2CID 40768144.
- ^ Ратнавалли Е., Брейн С., Доусон К., Ходжес-младший (июнь 2002 г.). «Распространенность лобно-височной деменции». Неврология. 58 (11): 1615–21. Дои:10.1212 / WNL.58.11.1615. PMID 12058088. S2CID 45904851.
- ^ McKee AC, Cantu RC, Nowinski CJ, Hedley-Whyte ET, Gavett BE, Budson AE, Santini VE, Lee HS, Kubilus CA, Stern RA (июль 2009 г.). «Хроническая травматическая энцефалопатия у спортсменов: прогрессирующая таупатия после повторяющейся травмы головы». Журнал невропатологии и экспериментальной неврологии. 68 (7): 709–35. Дои:10.1097 / NEN.0b013e3181a9d503. ЧВК 2945234. PMID 19535999.
- ^ а б Nelson PT, Dickson DW, Trojanowski JQ, Jack CR, Boyle PA, Arfanakis K и др. (Апрель 2019). «Лимбическая преобладающая возрастная энцефалопатия TDP-43 (ПОЗДНЕЕ): консенсусный отчет рабочей группы». Мозг. 142 (6): 1503–1527. Дои:10.1093 / мозг / awz099. ЧВК 6536849. PMID 31039256.
- ^ Что такое сосудистая деменция? В архиве 2013-10-19 в Wayback Machine Общество Альцгеймера.
- ^ Ли А.Ю. (август 2011 г.). «Сосудистая деменция». Медицинский журнал Чоннам. 47 (2): 66–71. Дои:10.4068 / cmj.2011.47.2.66. ЧВК 3214877. PMID 22111063.
- ^ «Что такое смешанная деменция?». Общество Альцгеймера. Получено 2020-12-13.
- ^ а б «Что такое смешанная деменция». Деменция Великобритания. Получено 2020-12-13.
- ^ Лин Дж. С., О'Коннор Е., Россом Р. К., Пердью Л. А., Экстрем Е. (ноябрь 2013 г.). «Скрининг когнитивных нарушений у пожилых людей: систематический обзор для Целевой группы США по профилактическим услугам». Анналы внутренней медицины. 159 (9): 601–12. Дои:10.7326/0003-4819-159-9-201311050-00730. PMID 24145578.
- ^ «Определение деменции». Руководящие принципы ЦРТ. Рид Групп. В архиве из оригинала 2009-06-29. Получено 2009-06-04.
- ^ Каплан Дж. П., Рабинович Т. (ноябрь 2010 г.). «Подход к пациенту с когнитивными нарушениями: делирий и деменция». Медицинские клиники Северной Америки. 94 (6): 1103–16, ix. Дои:10.1016 / j.mcna.2010.08.004. PMID 20951272.
- ^ Глисон О.К. (март 2003 г.). "Бред". Американский семейный врач. 67 (5): 1027–34. PMID 12643363. В архиве из оригинала от 29.09.2007.
- ^ Уорролл Л., Хиксон Л. М. (2003). «Значение для теории, практики и политики». В Worrall LE, Hickson LM (ред.). Коммуникативная неспособность в старении: от профилактики к вмешательству. Клифтон-Парк, штат Нью-Йорк: обучение Делмара. С. 297–98. ISBN 978-0-7693-0015-3.
- ^ Бустани М., Петерсон Б., Хэнсон Л., Харрис Р., Лор К. Н. (июнь 2003 г.). «Скрининг деменции в первичной медико-санитарной помощи: краткое изложение данных для Целевой группы США по профилактическим услугам». Анналы внутренней медицины. 138 (11): 927–37. Дои:10.7326/0003-4819-138-11-200306030-00015. PMID 12779304. S2CID 20779164.
- ^ а б Каллен Б., О'Нил Б., Эванс Дж. Дж., Коэн РФ, Лолор Б.А. (август 2007 г.). «Обзор скрининговых тестов на когнитивные нарушения». Журнал неврологии, нейрохирургии и психиатрии. 78 (8): 790–99. Дои:10.1136 / jnnp.2006.095414. ЧВК 2117747. PMID 17178826.
- ^ Сагер М.А., Херманн Б.П., Ла Рю А, Вудард Дж. Л. (октябрь 2006 г.). «Скрининг на деменцию в местных клиниках памяти» (PDF). WMJ. 105 (7): 25–29. PMID 17163083. Архивировано из оригинал (PDF) на 26.06.2010.
- ^ Fleisher AS, Sowell BB, Taylor C, Gamst AC, Petersen RC, Thal LJ (май 2007 г.). «Клинические предикторы прогрессирования болезни Альцгеймера при амнестических легких когнитивных нарушениях». Неврология. 68 (19): 1588–95. Дои:10.1212 / 01.wnl.0000258542.58725.4c. PMID 17287448. S2CID 9129604.
- ^ Карлавиш Дж. Х., Кларк С. М. (март 2003 г.). «Диагностическая оценка пожилых пациентов с легкими проблемами памяти». Анналы внутренней медицины. 138 (5): 411–19. Дои:10.7326/0003-4819-138-5-200303040-00011. PMID 12614094. S2CID 43798118.
- ^ Кревин С.Т., Вишневски С., Ноэль-Сторр А.Х., Тревельян С.М., Хэмптон Т., Реймент Д. и др. (Январь 2016 г.). «Краткое обследование психического состояния (MMSE) для выявления деменции у людей в возрасте 65 лет и старше, не прошедших клиническую оценку, в группах населения и первичной медико-санитарной помощи» (PDF). Кокрановская база данных систематических обзоров (1): CD011145. Дои:10.1002 / 14651858.CD011145.pub2. HDL:1983 / 00876aeb-2061-43f5-b7e1-938c666030ab. PMID 26760674.
- ^ Teng EL, Chui HC (август 1987 г.). «Экзамен по модифицированному мини-психическому состоянию (3MS)». Журнал клинической психиатрии. 48 (8): 314–8. PMID 3611032.
- ^ Teng EL, Hasegawa K, Homma A, Imai Y, Larson E, Graves A и др. (1994). «Инструмент скрининга когнитивных способностей (CASI): практический тест для межкультурных эпидемиологических исследований деменции». Международная психогериатрия. 6 (1): 45–58, обсуждение 62. Дои:10.1017 / S1041610294001602. PMID 8054493.
- ^ Томбо TN (март 2004 г.). «Тест A и B для создания следов: нормативные данные с разбивкой по возрасту и образованию». Архив клинической нейропсихологии. 19 (2): 203–14. Дои:10.1016 / S0887-6177 (03) 00039-8. PMID 15010086.
- ^ Ройалл Д. Р., Кордес Дж. А., Полк М. (май 1998 г.). "CLOX: задача рисования исполнительных часов". Журнал неврологии, нейрохирургии и психиатрии. 64 (5): 588–94. Дои:10.1136 / jnnp.64.5.588. ЧВК 2170069. PMID 9598672.
- ^ Насреддин З.С., Филлипс Н.А., Бедириан В., Шарбонно С., Уайтхед В., Коллин И., Каммингс Дж. Л., Чертков Х. (апрель 2005 г.). «Монреальская когнитивная оценка, MoCA: краткий инструмент для выявления легких когнитивных нарушений». Журнал Американского гериатрического общества. 53 (4): 695–99. Дои:10.1111 / j.1532-5415.2005.53221.x. PMID 15817019. S2CID 9014589.
- ^ Бретон, Александр; Кейси, Дэниел; Арнаутоглоу, Никитас А. (2019). «Когнитивные тесты для выявления легких когнитивных нарушений (MCI), продромальной стадии деменции: метаанализ исследований диагностической точности». Международный журнал гериатрической психиатрии. 34 (2): 233–242. Дои:10.1002 / GPS.5016. ISSN 1099-1166. PMID 30370616. S2CID 53097138.
- ^ К. Хендри; C, зеленый; Р, МакШейн; Ах, Ноэль-Сторр; DJ, Стотт; S, Anwer; Эй Джей, Саттон; Дж. К., Бертон; Тиджей, Куинн (2019-03-04). «AD-8 для обнаружения деменции в различных медицинских учреждениях». Кокрановская база данных систематических обзоров. 3: CD011121. Дои:10.1002 / 14651858.CD011121.pub2. ЧВК 6398085. PMID 30828783.
- ^ Рэнсон Дж. М., Куйма Е., Гамильтон В., Мунис-Террера Дж., Ланга К. М., Ллевеллин Д. (2018-11-28). «Предикторы ошибочной классификации деменции при использовании кратких когнитивных оценок». Неврология: Клиническая практика. 9 (2): 109–117. Дои:10.1212 / CPJ.0000000000000566. ЧВК 6461420. PMID 31041124.
- ^ Йорм А.Ф. (сентябрь 2004 г.). «Анкета информатора по снижению когнитивных функций у пожилых людей (IQCODE): обзор». Международная психогериатрия. 16 (3): 275–93. Дои:10.1017 / S1041610204000390. PMID 15559753.
- ^ Харрисон Дж. К., Стотт Д. Д., МакШейн Р., Ноэль-Сторр А. Х., Суонн-Прайс Р. С., Куинн Т. Дж. (Ноябрь 2016 г.). «Анкета информатора по снижению когнитивных функций у пожилых людей (IQCODE) для ранней диагностики деменции в различных медицинских учреждениях». Кокрановская база данных систематических обзоров. 11: CD011333. Дои:10.1002 / 14651858.cd011333.pub2. ЧВК 6477966. PMID 27869298.
- ^ Рейсберг Б., Феррис С.Х., де Леон М.Дж., Крук Т. (сентябрь 1982 г.). «Глобальная шкала ухудшения состояния для оценки первичной дегенеративной деменции» (PDF). Am J Psychiatry. 139 (9): 1136–9. Дои:10.1176 / ajp.139.9.1136. PMID 7114305. S2CID 45218227.CS1 maint: несколько имен: список авторов (связь)
- ^ Склан С.Г., Райсберг Б. (1992). «Функциональная оценка стадии (FAST) при болезни Альцгеймера: надежность, достоверность и порядочность». Int Psychogeriatr. 4 (Дополнение 1): 55–69. Дои:10,1017 / с1041610292001157. PMID 1504288.
- ^ Бонте Ф.Дж., Харрис Т.С., Хайнан Л.С., Бигио Э.Х., Белый CL (июль 2006 г.). «Tc-99m HMPAO SPECT в дифференциальной диагностике деменции с гистопатологическим подтверждением». Клиническая ядерная медицина. 31 (7): 376–78. Дои:10.1097 / 01.rlu.0000222736.81365.63. PMID 16785801. S2CID 39518497.
- ^ Дугалл Нью-Джерси, Брюггинк С., Эбмайер КП (2004). «Систематический обзор диагностической точности 99mTc-HMPAO-SPECT при деменции» (PDF). Американский журнал гериатрической психиатрии. 12 (6): 554–70. Дои:10.1176 / appi.ajgp.12.6.554. PMID 15545324. S2CID 12375536.
- ^ Абелла Х.А. (16 июня 2009 г.). «Отчет SNM: ПЭТ-визуализация химического состава мозга позволяет лучше охарактеризовать деменции». Диагностическая визуализация.[постоянная мертвая ссылка ]
- ^ Дин, Джи; Дэвис-Плурд, Кендра Л.; Седагхат, Саназ; Талли, Филлип Дж; Ван, Ванмей; Филлипс, Кэролайн; Пасе, Мэтью П.; Гимали, Джаяндра Дж; Гвен Виндхэм, B; Грисволд, Майкл; Готтесман, Ребекка; Мосли, Томас H; Белый, Лон; Гунасон, Вильмундур; Дебетт, Стефани; Байзер, Алекса S; Сешадри, Судха; Арфан Икрам, М; Мейреллес, Осорио; Цурио, Кристоф; Лаунер, Ленор Дж (ноябрь 2019 г.). «Антигипертензивные препараты и риск развития деменции и болезни Альцгеймера: метаанализ данных отдельных участников проспективных когортных исследований». Ланцетная неврология. 19 (1): 61–70. Дои:10.1016 / S1474-4422 (19) 30393-X. ЧВК 7391421. PMID 31706889.
- ^ Ллевеллин, Дэвид Дж .; Kuźma, Elżbieta; Hyppönen, Элина; Langa, Kenneth M .; Littlejohns, Thomas J .; Хэннон, Эйлиш; Лурида, Илианна (14.07.2019). «Ассоциация образа жизни и генетического риска с заболеваемостью деменцией». JAMA. 322 (5): 430. Дои:10.1001 / jama.2019.9879. ЧВК 6628594. PMID 31302669.
- ^ Финк HA, Jutkowitz E, McCarten JR, Hemmy LS, Butler M, Davila H и др. (Январь 2018). «Фармакологические вмешательства для предотвращения снижения когнитивных функций, умеренных когнитивных нарушений и клинической деменции альцгеймеровского типа: систематический обзор». Анналы внутренней медицины. 168 (1): 39–51. Дои:10.7326 / M17-1529. PMID 29255847. S2CID 24193907.
- ^ Хьюз, Диармайд; Судья, Конор; Мерфи, Роберт; Лафлин, Элейн; Костелло, Мария; Уайтли, Уильям; Босх, Джеки; О’Доннелл, Мартин Дж .; Канаван, Мишель (19 мая 2020 г.). «Связь снижения артериального давления с деменцией или когнитивными нарушениями». JAMA. 323 (19): 1934–1944. Дои:10.1001 / jama.2020.4249. ЧВК 7237983. PMID 32427305.
- ^ Гейтс, Никола Дж .; Rutjes, Anne Ws; Ди Нисио, Марчелло; Карим, Салман; Чонг, Ли-Йи; Марш, Эврим; Мартинес, Габриэль; Верноой, Робин В.М. (27 февраля 2020 г.). «Компьютеризированная когнитивная тренировка в течение 12 или более недель для поддержания когнитивной функции у когнитивно здоровых людей в пожилом возрасте». Кокрановская база данных систематических обзоров. 2: CD012277. Дои:10.1002 / 14651858.CD012277.pub3. ISSN 1469-493X. ЧВК 7045394. PMID 32104914.
- ^ Батлер М., МакКриди Э., Нельсон В.А., Десаи П., Ратнер Э., Финк А.А., Хемми Л.С., МакКартен Дж.Р., Барклай Т.Р., Брасур М., Давила Х., Кейн Р.Л. (январь 2018 г.). «Предотвращает ли когнитивное обучение снижение когнитивных функций ?: Систематический обзор». Анналы внутренней медицины. 168 (1): 63–68. Дои:10.7326 / M17-1531. PMID 29255842. S2CID 1919144.
- ^ Лампит А, Хэллок Х, Валенсуэла М (ноябрь 2014 г.). «Компьютеризированная когнитивная тренировка когнитивно здоровых пожилых людей: систематический обзор и метаанализ модификаторов эффекта». PLOS Медицина. 11 (11): e1001756. Дои:10.1371 / journal.pmed.1001756. ЧВК 4236015. PMID 25405755.
- ^ Brasure M, Desai P, Davila H, Nelson VA, Calvert C, Jutkowitz E, Butler M, Fink HA, Ratner E, Hemmy LS, McCarten JR, Barclay TR, Kane RL (январь 2018 г.). «Вмешательства в области физической активности в предотвращении когнитивного спада и деменции альцгеймеровского типа: систематический обзор». Анналы внутренней медицины. 168 (1): 30–38. Дои:10.7326 / M17-1528. PMID 29255839. S2CID 10032767.
- ^ Кивимяки М., Сингх-Ману А., Пентти Дж., Сабиа С., Нюберг С.Т., Альфредссон Л. и др. (Апрель 2019). «Отсутствие физической активности, кардиометаболическое заболевание и риск деменции: метаанализ индивидуального участника». BMJ. 365: l1495. Дои:10.1136 / bmj.l1495. ЧВК 6468884. PMID 30995986.
- ^ Финк Х.А., Ютковиц Э., МакКартен-младший, Хемми Л.С., Батлер М., Давила Х, Ратнер Э., Калверт С., Барклай Т.Р., Брасюр М., Нельсон В.А., Кейн Р.Л. (январь 2018 г.). «Фармакологические вмешательства для предотвращения когнитивного спада, легкого когнитивного нарушения и клинической деменции альцгеймеровского типа: систематический обзор». Анналы внутренней медицины. 168 (1): 39–51. Дои:10.7326 / M17-1529. PMID 29255847. S2CID 24193907.
- ^ Батлер М., Нельсон В.А., Давила Х., Ратнер Э., Финк Х.А., Хемми Л.С., МакКартен Дж.Р., Барклай Т.Р., Brasure M, Кейн Р.Л. (январь 2018 г.). «Вмешательства, отпускаемые без рецепта, для предотвращения когнитивного спада, умеренного когнитивного нарушения и клинической деменции альцгеймеровского типа: систематический обзор». Анналы внутренней медицины. 168 (1): 52–62. Дои:10.7326 / M17-1530. PMID 29255909. S2CID 11318942.
- ^ Schneider LS, Mangialasche F, Andreasen N, Feldman H, Giacobini E, Jones R, Mantua V, Mecocci P, Pani L, Winblad B, Kivipelto M (март 2014 г.). «Клинические испытания и разработка лекарств на поздних стадиях болезни Альцгеймера: оценка с 1984 по 2014 год». Журнал внутренней медицины. 275 (3): 251–83. Дои:10.1111 / joim.12191. ЧВК 3956752. PMID 24605808.
- ^ Ватт, Дженнифер А .; Гударзи, Захра; Вероники, Арети Ангелики; Нинчич, Вера; Хан, Пол А .; Гассеми, Марко; Томпсон, Юань; Tricco, Andrea C .; Штраус, Шэрон Э. (15 октября 2019 г.). «Сравнительная эффективность вмешательств для агрессивного и возбужденного поведения при деменции». Анналы внутренней медицины. 171 (9): 633–642. Дои:10.7326 / M19-0993. PMID 31610547. S2CID 204699972.
- ^ Vandepitte S, Van Den Noortgate N, Putman K, Verhaeghe S, Verdonck C, Annemans L (декабрь 2016 г.). «Эффективность временного ухода в поддержке неформальных лиц, обеспечивающих уход за людьми с деменцией: систематический обзор». Международный журнал гериатрической психиатрии. 31 (12): 1277–88. Дои:10.1002 / GPS.4504. PMID 27245986. S2CID 3464912.
- ^ Лагерь CJ (2010). «Истоки Монтессори-программирования при деменции». Немедикаментозные методы лечения деменции. 1 (2): 163–174. ЧВК 3600589. PMID 23515663.
- ^ Cheong CY, Tan JA, Foong YL, Koh HM, Chen DZ, Tan JJ, Ng CJ, Yap P (2016). «Креативная музыкальная терапия в условиях интенсивной терапии для пожилых пациентов с делирием и деменцией». Деменция и гериатрические когнитивные расстройства Extra. 6 (2): 268–75. Дои:10.1159/000445883. ЧВК 4959431. PMID 27489560.
- ^ Alexopoulos GS, Abrams RC, Young RC, Shamoian CA (февраль 1988 г.). «Шкала Корнелла для депрессии при деменции». Биологическая психиатрия. 23 (3): 271–84. CiteSeerX 10.1.1.461.315. Дои:10.1016/0006-3223(88)90038-8. PMID 3337862. S2CID 44280392.
- ^ Jeon YH, Li Z, Low LF, Chenoweth L, O'Connor D, Beattie E, Liu Z, Brodaty H (август 2015 г.). «Клиническая полезность Корнельской шкалы депрессии при деменции в качестве рутинной оценки в домах престарелых». Американский журнал гериатрической психиатрии. 23 (8): 784–93. Дои:10.1016 / j.jagp.2014.08.013. PMID 25256214.
- ^ Jeon YH, Liu Z, Li Z, Low LF, Chenoweth L, O'Connor D, Beattie E, Davison TE, Brodaty H (ноябрь 2016 г.). «Разработка и проверка краткой версии Корнелльской шкалы депрессии при деменции для обследований пациентов в домах престарелых». Американский журнал гериатрической психиатрии. 24 (11): 1007–1016. Дои:10.1016 / j.jagp.2016.05.012. PMID 27538349.
- ^ Вудс Б., О'Филбин Л., Фаррелл Е.М., Спектор А.Э., Оррелл М. (март 2018 г.). «Воспоминания о терапии деменции». Кокрановская база данных систематических обзоров. 3: CD001120. Дои:10.1002 / 14651858.CD001120.pub3. ЧВК 6494367. PMID 29493789.
- ^ Верноой-Дассен М., Драшкович И., Макклири Дж., Даунс М. (ноябрь 2011 г.). «Когнитивный рефрейминг для лиц, осуществляющих уход за людьми с деменцией». Кокрановская база данных систематических обзоров (11): CD005318. arXiv:0706.4406. Дои:10.1002 / 14651858.CD005318.pub2. HDL:2066/97731. PMID 22071821.
- ^ Нил М., Бартон Райт П. (2003). «Валидационная терапия деменции». Кокрановская база данных систематических обзоров (3): CD001394. Дои:10.1002 / 14651858.CD001394. PMID 12917907.
- ^ Вудс Б., Агирре Е., Спектор А. Е., Оррелл М. (февраль 2012 г.). «Когнитивная стимуляция для улучшения когнитивных функций у людей с деменцией». Кокрановская база данных систематических обзоров. 2 (2): CD005562. Дои:10.1002 / 14651858.CD005562.pub2. PMID 22336813.
- ^ Баркер П. (2003). Психиатрическая и психиатрическая помощь: искусство заботы. Лондон: Арнольд. ISBN 978-0-340-81026-2. OCLC 53373798.
- ^ Weitzel T, Robinson S, Barnes MR, Berry TA, Holmes JM, Mercer S и др. (2011). «Особые потребности госпитализированного пациента с деменцией». Медсург Медсестра. 20 (1): 13–18, тест 19. PMID 21446290.
- ^ Каннингем С (2006). «Понимание сложного поведения у пациентов с деменцией». Стандарт сестринского дела. 20 (47): 42–45. Дои:10.7748 / нс2006.08.20.47.42.c4477. PMID 16913375.
- ^ а б Дайер С.М., Харрисон С.Л., Лейвер К., Уайтхед С., Кротти М. (март 2018 г.). «Обзор систематических обзоров фармакологических и нефармакологических вмешательств для лечения поведенческих и психологических симптомов деменции». Международная психогериатрия. 30 (3): 295–309. Дои:10.1017 / S1041610217002344. PMID 29143695.
- ^ van der Steen JT, Smaling HJ, van der Wouden JC, Bruinsma MS, Scholten RJ, Vink AC (июль 2018 г.). «Музыкальные терапевтические вмешательства для людей с деменцией». Кокрановская база данных систематических обзоров. 7: CD003477. Дои:10.1002 / 14651858.CD003477.pub4. HDL:1874/350441. ЧВК 6513122. PMID 30033623.
- ^ Элдирдири Осман, Сара; Тишлер, Виктория; Шнайдер, Жюстин (24 ноября 2014 г.). "'Пение для мозга »: качественное исследование, изучающее пользу пения для здоровья и благополучия людей с деменцией и лиц, осуществляющих за ними уход». Слабоумие. 15 (6): 1328. Дои:10.1177/1471301214556291. ЧВК 5089222. PMID 25425445.
- ^ а б c Джонстон Б., Нараянасами М. (апрель 2016 г.). «Изучение психосоциальных вмешательств для людей с деменцией, которые усиливают индивидуальность и связаны с наследием - комплексный обзор». BMC Гериатрия. 16: 77. Дои:10.1186 / s12877-016-0250-1. ЧВК 4820853. PMID 27044417.
- ^ «Британские больницы перестраиваются с учетом деменции». Экономист. Получено 2018-09-19.
- ^ Рафии М.С., Айсен П.С. (февраль 2009 г.). «Последние разработки в области лечения болезни Альцгеймера». BMC Медицина. 7: 7. Дои:10.1186/1741-7015-7-7. ЧВК 2649159. PMID 19228370.
- ^ а б Ллео А, Гринберг С.М., Growdon JH (2006). «Современная фармакотерапия болезни Альцгеймера». Ежегодный обзор медицины. 57 (1): 513–33. Дои:10.1146 / annurev.med.57.121304.131442. PMID 16409164.
- ^ Бонд М., Роджерс Дж., Питерс Дж., Андерсон Р., Хойл М., Майнерс А., Моксхэм Т., Дэвис С., Тхокала П., Вайло А., Джеффрис М., Хайд С. (2012). «Эффективность и рентабельность донепезила, галантамина, ривастигмина и мемантина для лечения болезни Альцгеймера (обзор Технологической оценки № 111): систематический обзор и экономическая модель». Оценка медицинских технологий. 16 (21): 1–470. Дои:10,3310 / hta16210. ЧВК 4780923. PMID 22541366.
- ^ Родда Дж., Морган С., Уокер З. (октябрь 2009 г.). «Эффективны ли ингибиторы холинэстеразы при лечении поведенческих и психологических симптомов деменции при болезни Альцгеймера? Систематический обзор рандомизированных плацебо-контролируемых исследований донепезила, ривастигмина и галантамина». Международная психогериатрия. 21 (5): 813–24. Дои:10.1017 / S1041610209990354. PMID 19538824.
- ^ Gill SS, Anderson GM, Fischer HD, Bell CM, Li P, Normand SL, Rochon PA (май 2009 г.). «Обморок и его последствия у пациентов с деменцией, получающих ингибиторы холинэстеразы: популяционное когортное исследование». Архивы внутренней медицины. 169 (9): 867–73. Дои:10.1001 / archinternmed.2009.43. PMID 19433698.
- ^ Арванитакис З., Шах Р.К., Беннетт Д.А. (22 октября 2019 г.). «Диагностика и лечение деменции: обзор». JAMA. 322 (16): 1589–1599. Дои:10.1001 / jama.2019.4782. ЧВК 7462122. PMID 31638686.
- ^ AMDA - Общество по медицине послеострого и длительного лечения (Февраль 2014), «Десять вещей, о которых должны спрашивать врачи и пациенты», Мудрый выбор: инициатива Фонд ABIM, AMDA - Общество по медицине послеострого и длительного лечения, в архиве из оригинала 12 апреля 2015 г., получено 20 апреля 2015
- ^ Walker Z, Possin KL, Boeve BF, Aarsland D (октябрь 2015 г.). «Деменции с тельцами Леви». Ланцет (Рассмотрение). 386 (10004): 1683–97. Дои:10.1016 / S0140-6736 (15) 00462-6. ЧВК 5792067. PMID 26595642.
- ^ Загрузочный БП (2015). «Комплексное лечение деменции с тельцами Леви». Alzheimers Res Ther (Рассмотрение). 7 (1): 45. Дои:10.1186 / s13195-015-0128-z. ЧВК 4448151. PMID 26029267.
- ^ Гомперт С.Н. (апрель 2016 г.). «Деменции с тельцами Леви: деменция с тельцами Леви и деменция при болезни Паркинсона». Continuum (Миннеап Минн) (Рассмотрение). 22 (2 Деменция): 435–63. Дои:10.1212 / CON.0000000000000309. ЧВК 5390937. PMID 27042903.
- ^ а б c d е ж грамм Американское гериатрическое общество. «Пять вещей, которые должны задать вопросы врачам и пациентам». Мудрый выбор: инициатива ABIM Foundation. В архиве из оригинала 1 сентября 2013 г.. Получено 1 августа, 2013.
- ^ Американская психиатрическая ассоциация (Сентябрь 2013), «Пять вещей, которые должны задать вопросы врачам и пациентам», Мудрый выбор: инициатива Фонд ABIM, Американская психиатрическая ассоциация, в архиве из оригинала от 3 декабря 2013 г., получено 30 декабря 2013
- ^ Дайер С.М., Лейвер К., Pond CD, Камминг Р.Г., Уайтхед С., Кротти М. (декабрь 2016 г.). «Рекомендации по клинической практике и принципы ухода за людьми с деменцией в Австралии». Австралийский семейный врач. 45 (12): 884–889. PMID 27903038.
- ^ Declercq T, Petrovic M, Azermai M, Vander Stichele R, De Sutter AI, van Driel ML, Christiaens T (март 2013 г.). «Прекращение приема против продолжения приема антипсихотических препаратов для лечения поведенческих и психологических симптомов у пожилых людей с деменцией» (PDF). Кокрановская база данных систематических обзоров. 3 (3): CD007726. Дои:10.1002 / 14651858.CD007726.pub2. HDL:1854 / LU-3109108. PMID 23543555.
- ^ Бонд М., Роджерс Дж., Питерс Дж., Андерсон Р., Хойл М., Майнерс А., Моксхэм Т., Дэвис С., Тхокала П., Вайло А., Джеффрис М., Хайд С. (2012). «Эффективность и рентабельность донепезила, галантамина, ривастигмина и мемантина для лечения болезни Альцгеймера (обзор оценки технологии № 111): систематический обзор и экономическая модель». Оценка медицинских технологий. 16 (21): 1–470. Дои:10,3310 / hta16210. ЧВК 4780923. PMID 22541366.
- ^ Райна П., Сантагуида П., Исмаила А., Паттерсон С., Коуэн Д., Левин М. и др. (Март 2008 г.). «Эффективность ингибиторов холинэстеразы и мемантина для лечения деменции: обзор данных для руководства по клинической практике». Анналы внутренней медицины. 148 (5): 379–97. Дои:10.7326/0003-4819-148-5-200803040-00009. PMID 18316756.
- ^ Атри А., Шонесси Л. В., Локасио Дж. Дж., Гроудон Дж. Х. (2008). «Длительный курс и эффективность комбинированной терапии при болезни Альцгеймера». Болезнь Альцгеймера и связанные с ней заболевания. 22 (3): 209–21. Дои:10.1097 / WAD.0b013e31816653bc. ЧВК 2718545. PMID 18580597.
- ^ Джонс Х.Э., Джоши А., Шенкин С., Мид Г.Э. (июль 2016 г.). «Эффект лечения селективными ингибиторами обратного захвата серотонина по сравнению с плацебо при прогрессировании деменции: систематический обзор и метаанализ». Возраст и старение. 45 (4): 448–56. Дои:10.1093 / старение / afw053. PMID 27055878.
- ^ Дудас, Роберт; Малуф, Рим; Макклири, Дженни; Денинг, Том (2018-08-31). Кокрановская группа по деменции и когнитивным улучшениям (ред.). «Антидепрессанты для лечения депрессии при деменции». Кокрановская база данных систематических обзоров. 8: CD003944. Дои:10.1002 / 14651858.CD003944.pub2. ЧВК 6513376. PMID 30168578.
- ^ Зейтц Д.П., Адунури Н., Гилл С.С., Грунейр А., Херрманн Н., Рочон П. (февраль 2011 г.). «Антидепрессанты от возбуждения и психоза при деменции». Кокрановская база данных систематических обзоров (2): CD008191. Дои:10.1002 / 14651858.CD008191.pub2. PMID 21328305.
- ^ а б c d Макклири, Дженни; Шарпли, Энн Л. (15 ноября 2020 г.). «Фармакотерапия нарушений сна при деменции». Кокрановская база данных систематических обзоров. 11: CD009178. Дои:10.1002 / 14651858.CD009178.pub4. ISSN 1469-493X. PMID 33189083.
- ^ Группа экспертов по обновлению критериев пива Американского гериатрического общества, 2012 г. (апрель 2012 г.). «Американское гериатрическое общество обновило критерии Бирса для потенциально несоответствующего использования лекарств пожилыми людьми». Журнал Американского гериатрического общества. 60 (4): 616–31. Дои:10.1111 / j.1532-5415.2012.03923.x. ЧВК 3571677. PMID 22376048.
- ^ Лолк А., Гульманн NC (октябрь 2006 г.). «[Психофармакологическое лечение поведенческих и психологических симптомов при деменции]». Ugeskrift для Laeger (на датском). 168 (40): 3429–32. PMID 17032610.
- ^ Malouf R, Гримли Эванс Дж. (Октябрь 2008 г.). «Фолиевая кислота с витамином B12 или без него для профилактики и лечения здоровых пожилых людей и людей с деменцией». Кокрановская база данных систематических обзоров (4): CD004514. Дои:10.1002 / 14651858.CD004514.pub2. PMID 18843658.
- ^ МакГиннесс Б., Крейг Д., Баллок Р., Малуф Р., Пассмор П. (июль 2014 г.). «Статины для лечения деменции» (PDF). Кокрановская база данных систематических обзоров. 7 (7): CD007514. Дои:10.1002 / 14651858.CD007514.pub3. PMID 25004278. Архивировано из оригинал (PDF) на 2019-09-03. Получено 2019-09-03.
- ^ Jongstra S, Harrison JK, Quinn TJ, Richard E (ноябрь 2016 г.). «Антигипертензивная отмена для предотвращения снижения когнитивных функций». Кокрановская база данных систематических обзоров. 11: CD011971. Дои:10.1002 / 14651858.CD011971.pub2. ЧВК 6465000. PMID 27802359.
- ^ Пейдж А.Т., Поттер К., Клиффорд Р., Маклахлан А.Дж., Этертон-Бир С. (октябрь 2016 г.). «Инструмент адекватности лекарств для сопутствующих заболеваний при деменции: согласованные рекомендации многопрофильной группы экспертов». Журнал внутренней медицины. 46 (10): 1189–1197. Дои:10.1111 / imj.13215. ЧВК 5129475. PMID 27527376.
- ^ а б c d е Hadjistavropoulos T, Herr K, Turk DC, Fine PG, Dworkin RH, Helme R, Jackson K, Parmelee PA, Rudy TE, Lynn Beattie B, Chibnall JT, Craig KD, Ferrell B, Ferrell B, Fillingim RB, Gagliese L, Gallagher Р., Гибсон С.Дж., Харрисон Е.Л., Кац Б., Киф Ф.Дж., Либер С.Дж., Люсье Д., Шмадер К.Э., Тейт Р.С., Вайнер Д.К., Уильямс Дж. (Январь 2007 г.). «Междисциплинарное консенсусное заявление экспертов по оценке боли у пожилых людей». Клинический журнал боли. 23 (1 приложение): S1–43. Дои:10.1097 / AJP.0b013e31802be869. PMID 17179836. S2CID 43777445.
- ^ а б Шега Дж., Эмануэль Л., Варгиш Л., Левин С.К., Бурш Х., Герр К., Карп Дж.Ф., Вайнер Д.К. (май 2007 г.). «Боль у людей с деменцией: сложные, частые и сложные». Журнал боли. 8 (5): 373–78. Дои:10.1016 / j.jpain.2007.03.003. PMID 17485039.
- ^ Блит FM, Камминг Р., Митчелл П., Ван Дж. Дж. (Июль 2007 г.). «Боль и падения у пожилых людей». Европейский журнал боли. 11 (5): 564–71. Дои:10.1016 / j.ejpain.2006.08.001. PMID 17015026. S2CID 27460864.
- ^ Браун, К. (2009). «Боль, старение и слабоумие: кризис надвигается, но готовы ли мы?». Британский журнал профессиональной терапии. 72 (8): 371–75. Дои:10.1177/030802260907200808. S2CID 73245194.
- ^ Герр К., Бьоро К., Декер С. (февраль 2006 г.). «Инструменты для оценки боли у невербальных пожилых людей с деменцией: обзор современного состояния». Журнал по лечению боли и симптомов. 31 (2): 170–92. Дои:10.1016 / j.jpainsymman.2005.07.001. PMID 16488350.
- ^ Столи П., Хиллиер Л. М., Эсбо Дж., Бол Н., Маккеллар Л., Готье Н. (февраль 2005 г.). «Инструменты для оценки боли у пожилых людей с когнитивными нарушениями». Журнал Американского гериатрического общества. 53 (2): 319–26. Дои:10.1111 / j.1532-5415.2005.53121.x. PMID 15673359. S2CID 21006144.
- ^ AMDA - Общество по медицине послеострого и длительного лечения (Февраль 2014), «Пять вещей, которые должны задать вопросы врачам и пациентам», Мудрый выбор: инициатива Фонд ABIM, AMDA - Общество по медицине послеострого и длительного лечения, в архиве из оригинала 13 сентября 2014 г., получено 10 февраля 2013
- ^ AMDA - Общество по медицине послеострого и длительного лечения (Февраль 2014), «Пять вещей, которые должны задать вопросы врачам и пациентам», Мудрый выбор: инициатива Фонд ABIM, AMDA - Общество по медицине послеострого и длительного лечения, в архиве из оригинала 13 сентября 2014 г., получено 10 февраля 2013, который цитирует:
- Тено Дж. М., Гозало П. Л., Митчелл С. Л., Куо С., Родос Р. Л., Байнум Дж. П., Мор В. (октябрь 2012 г.). «Улучшает ли выживание введение зонда для кормления и время его проведения?». Журнал Американского гериатрического общества. 60 (10): 1918–21. Дои:10.1111 / j.1532-5415.2012.04148.x. ЧВК 3470758. PMID 23002947.
- Палецек Э.Дж., Тено Дж. М., Касаретт Д. Д., Hanson LC, Rhodes RL, Mitchell SL (март 2010 г.). «Только комфортное кормление: предложение внести ясность в процесс принятия решений относительно трудностей с приемом пищи для людей с запущенной деменцией». Журнал Американского гериатрического общества. 58 (3): 580–84. Дои:10.1111 / j.1532-5415.2010.02740.x. ЧВК 2872797. PMID 20398123.
- Гиллик М.Р., Воландес А.Е. (июнь 2008 г.). «Стандарт ухода: почему мы до сих пор используем зонд для питания пациентов с запущенной деменцией?». Журнал Американской ассоциации медицинских директоров. 9 (5): 364–67. Дои:10.1016 / j.jamda.2008.03.011. PMID 18519120.
- ^ Mitchell SL, Kiely DK, Lipsitz LA (февраль 1997 г.). «Факторы риска и влияние на выживаемость размещения зонда для кормления в домах престарелых с тяжелыми когнитивными нарушениями». Архивы внутренней медицины. 157 (3): 327–32. Дои:10.1001 / archinte.1997.00440240091014. PMID 9040301.
- ^ Сэмпсон Е.Л., Кэнди Б., Джонс Л. (апрель 2009 г.). «Энтеральное зондовое питание для пожилых людей с запущенной деменцией». Кокрановская база данных систематических обзоров (2): CD007209. Дои:10.1002 / 14651858.CD007209.pub2. ЧВК 7182132. PMID 19370678.
- ^ Локетт М.А., Темплтон М.Л., Бирн Т.К., Норкросс ED (февраль 2002 г.). «Осложнения чрескожной эндоскопической гастростомии в поликлинике». Американский хирург. 68 (2): 117–20. PMID 11842953.
- ^ Finocchiaro C, Galletti R, Rovera G, Ferrari A, Todros L, Vuolo A, Balzola F (июнь 1997 г.). «Чрескожная эндоскопическая гастростомия: отдаленное наблюдение». Питание. 13 (6): 520–3. Дои:10.1016 / S0899-9007 (97) 00030-0. PMID 9263232.
- ^ Митчелл С.Л., Мор В., Гозало П.Л., Сервадио Дж. Л., Тено Дж. М. (август 2016 г.). "Питание через зонд в домах престарелых в США с запущенной деменцией, 2000–2014 гг." (PDF). JAMA. 316 (7): 769–70. Дои:10.1001 / jama.2016.9374. ЧВК 4991625. PMID 27533163. В архиве (PDF) из оригинала от 21.09.2017.
- ^ Span P (29 августа 2016 г.). «Снижение использования зондового питания для пациентов с деменцией». Нью-Йорк Таймс. В архиве из оригинала 3 сентября 2016 г.. Получено 31 августа 2016.
- ^ Гудман, Бренда; MA. «Диета влияет на маркеры болезни Альцгеймера». WebMD. Получено 2020-12-13.
- ^ Редактор (2019-01-15). «Потеря памяти может быть вызвана рядом факторов, от краткосрочных причин, таких как низкий уровень сахара в крови или побочные эффекты лекарств, до долгосрочных проблем со здоровьем, таких как деменция». Сахарный диабет. Получено 2020-12-13.CS1 maint: дополнительный текст: список авторов (связь)
- ^ Cao, L .; Tan, L .; Wang, H.-F .; Jiang, T .; Чжу, X.-C .; Lu, H .; Tan, M.S .; Ту, J.T. (Ноябрь 2016 г.). Модели питания и риск деменции: систематический обзор и метаанализ когортных исследований. Мол. Neurobiol. 53. С. 6144–6154. Дои:10.1007 / s12035-015-9516-4. ISSN 0893-7648. OCLC 6947867710. PMID 26553347. S2CID 8188716.CS1 maint: использует параметр авторов (связь)
- ^ PMID 26553347 цитируется Марко Каневелли; Flaminia Lucchini; Федерика Куарата; Джузеппе Бруно; Маттео Чезари (2016). Питание и деменция: доказательства профилактических подходов?. Питательные вещества. 8. MDPI. п. 144. Дои:10.3390 / nu8030144. ISSN 2072-6643. OCLC 8147564576. ЧВК 4808873. PMID 26959055. В архиве из оригинала 26 мая 2016 г. - через DOAJ.
- ^ а б Форбс, Дороти; Forbes, Scott C .; Блейк, Кэтрин М .; Тиссен, Эмили Дж .; Форбс, Шон (2015-04-15). «Программы упражнений для людей с деменцией». Кокрановская база данных систематических обзоров (4): CD006489. Дои:10.1002 / 14651858.CD006489.pub4. ISSN 1469-493X. PMID 25874613.
- ^ Мелинда. «Предотвращение болезни Альцгеймера - HelpGuide.org». HelpGuide.org. Получено 2020-12-13.
- ^ Вигго Хансен Н., Йоргенсен Т., Ортенблад Л. (октябрь 2006 г.). «Массаж и прикосновения при деменции». Кокрановская база данных систематических обзоров (4): CD004989. Дои:10.1002 / 14651858.CD004989.pub2. ЧВК 6823223. PMID 17054228.
- ^ Болл, Эмили Л .; Оуэн-Бут, Бетан; Грей, Эми; Шенкин, Сьюзан Д .; Хьюитт, Джонатан; Макклири, Дженни (19 августа 2020 г.). «Ароматерапия при деменции». Кокрановская база данных систематических обзоров. 8: CD003150. Дои:10.1002 / 14651858.CD003150.pub3. ISSN 1469-493X. ЧВК 7437395. PMID 32813272.
- ^ ван ден Эльсен Г.А., Ахмед А.И., Ламмерс М., Крамерс С., Веркес Р.Дж., ван дер Марк М.А., Риккерт М.Г. (март 2014 г.). «Эффективность и безопасность медицинских каннабиноидов у пожилых людей: систематический обзор». Обзоры исследований старения. 14: 56–64. Дои:10.1016 / j.arr.2014.01.007. PMID 24509411. S2CID 20498524.
- ^ Буркхардт М., Херке М., Вустманн Т., Ватцке С., Лангер Г., Финк А. (апрель 2016 г.). «Омега-3 жирные кислоты для лечения деменции». Кокрановская база данных систематических обзоров. 4: CD009002. Дои:10.1002 / 14651858.CD009002.pub3. ЧВК 7117565. PMID 27063583.
- ^ Сэмпсон Э.Л., Ричи С.В., Лай Р., Рэйвен П.В., Бланшар М.Р. (март 2005 г.). «Систематический обзор научных данных об эффективности паллиативной помощи при запущенной деменции» (PDF). Международная психогериатрия. 17 (1): 31–40. Дои:10.1017 / S1041610205001018. PMID 15945590. S2CID 7861568.
- ^ Ван ден Блок L (октябрь 2014 г.). «Необходимость интеграции паллиативной помощи в политику в отношении старения и деменции». Европейский журнал общественного здравоохранения. 24 (5): 705–06. Дои:10.1093 / eurpub / cku084. PMID 24997202.
- ^ Ван дер Стин, Дженни Т .; Радбрух, Лукас; Hertogh, Cees MPM; Де Бур, Марике Э .; Хьюз, Джулиан С .; Ларкин, Филипп; Francke, Anneke L .; Юнгер, Саския; Гоув, Дайанна; Ферт, Пэм; Купманс, Раймонд ТКМ; Волицер, Ладислав; Европейская ассоциация паллиативной помощи (EAPC) (11 марта 2014 г.). «Белая книга, определяющая оптимальную паллиативную помощь пожилым людям с деменцией: исследование Delphi и рекомендации Европейской ассоциации паллиативной помощи». Паллиативная медицина. 28 (3): 197–209. Дои:10.1177/0269216313493685. PMID 23828874.
- ^ Берч Д., Дрейпер Дж. (Май 2008 г.). «Критический обзор литературы, посвященный проблемам оказания эффективной паллиативной помощи пожилым людям с деменцией» (PDF). Журнал клинического сестринского дела. 17 (9): 1144–63. Дои:10.1111 / j.1365-2702.2007.02220.x. PMID 18416791.
- ^ Мерфи Э., Фроггатт К., Коннолли С., О'Ши Э, Сэмпсон Э.Л., Кейси Д., Девейн Д. (декабрь 2016 г.). «Вмешательства по паллиативной помощи при запущенной деменции». Кокрановская база данных систематических обзоров. 12: CD011513. Дои:10.1002 / 14651858.CD011513.pub2. ЧВК 6463843. PMID 27911489.
- ^ Митчелл Дж., Аньелли Дж. (Октябрь 2015 г.). «Личностно-ориентированная помощь людям с деменцией: пересмотр Китвуда». Стандарт сестринского дела. 30 (7): 46–50. Дои:10.7748 / нс.30.7.46.s47. PMID 26463810.
- ^ Косака К, изд. (2017). Деменция с тельцами Леви: клинические и биологические аспекты (1-е изд.). Спрингер: Япония. Дои:10.1007/978-4-431-55948-1. ISBN 978-4-431-55948-1.
- ^ «Деменция с тельцами Леви: надежда через исследования». Национальный институт неврологических расстройств и инсульта. Национальные институты здоровья США. 10 января 2020 г.. Получено 18 марта, 2020.
- ^ Херши Л.А., Коулман-Джексон Р. (апрель 2019 г.). «Фармакологическое лечение деменции с помощью доделий Леви». Наркотики старения (Рассмотрение). 36 (4): 309–19. Дои:10.1007 / s40266-018-00636-7. ЧВК 6435621. PMID 30680679.
- ^ Готье С (2006). Клиническая диагностика и лечение болезни Альцгеймера (3-е изд.). Абингдон, Oxon: Informa Healthcare. С. 53–54. ISBN 978-0-203-93171-4. В архиве из оригинала от 03.05.2016.
- ^ а б Принц М., Джексон Дж. (2009). «Всемирный отчет о болезни Альцгеймера 2009». Международная ассоциация болезни Альцгеймера: 38. Архивировано с оригинал 11 марта 2012 г.. Получено 11 марта 2012.
- ^ а б c d Международная организация по болезни Альцгеймера (сентябрь 2015 г.). «Всемирный доклад о болезни Альцгеймера, 2015 г.» (PDF). Получено 30 октября 2018.
- ^ а б Садок Б.Дж., Садок В.А. (2008). «Делирий, слабоумие, амнезиальные и другие расстройства половой жизни и психические расстройства, вызванные общим заболеванием». Краткий учебник по клинической психиатрии Каплана и Садока (3-е изд.). Филадельфия: Уолтерс Клувер / Липпинкотт Уильямс и Уилкинс. п. 52. ISBN 978-0-7817-8746-8.
- ^ Berrios GE (ноябрь 1987 г.). «Деменция в семнадцатом и восемнадцатом веках: концептуальная история». Психологическая медицина. 17 (4): 829–37. Дои:10.1017 / S0033291700000623. PMID 3324141.
- ^ Берхтольд NC, Котман CW (1998). «Эволюция концептуализации деменции и болезни Альцгеймера: греко-римский период до 1960-х годов». Нейробиол старения. 19 (3): 173–89. Дои:10.1016 / s0197-4580 (98) 00052-9. PMID 9661992. S2CID 24808582.
- ^ Диагностика и лечение старческой деменции. Бергенер, Манфред., Райсберг, Барри. Берлин: Springer-Verlag. 1989 г. ISBN 0-387-50800-7. OCLC 19455117.CS1 maint: другие (связь)
- ^ Колата Г (17 июня 2010 г.). «Смелый план испытаний лекарств по замедлению болезни Альцгеймера». Нью-Йорк Таймс. В архиве из оригинала от 9 апреля 2012 г.. Получено 17 июня, 2010.
- ^ Кацман Р. (апрель 1976 г.). «От редакции: распространенность и злокачественность болезни Альцгеймера. Главный убийца». Архив неврологии. 33 (4): 217–18. Дои:10.1001 / archneur.1976.00500040001001. PMID 1259639.
- ^ "Что такое деменция?". Ассоциация Альцгеймера. Получено 6 августа 2018.
Деменцию часто неправильно называют «дряхлостью» или «старческим слабоумием», что отражает ранее широко распространенное, но ошибочное мнение о том, что серьезное снижение умственного развития является нормальным явлением старения.
- ^ Тейлор, Данетт С. «Деменция». MedicineNet. Получено 6 августа 2018.
Старческое слабоумие («старческое слабоумие») - это термин, который когда-то использовался для описания всех видов деменции; этот термин больше не используется в качестве диагноза.
- ^ "Здорово". Здорово. Получено 2020-12-13.
- ^ «Взаимосвязь между шизофренией и деменцией». Психология сегодня. Получено 2020-12-13.
- ^ Бродатый Н., Донкин М. (29 апреля 2017 г.). «Семейные опекуны людей с деменцией». Диалоги в клинической неврологии. 11 (2): 217–28. ЧВК 3181916. PMID 19585957.
- ^ "Национальные планы действий по борьбе с болезнью Альцгеймера и деменции, планируемые меры и действия (PDF)" (PDF). Лондон: Международная болезнь Альцгеймера. Апрель 2012. Архивировано с оригинал (PDF) на 2012-05-18. Получено 2012-12-03.
- ^ «Борьба с болезнью Альцгеймера и другими типами деменции: сводный документ по национальной стратегии Израиля, подготовленный междисциплинарной межорганизационной группой экспертов» Brookdale ». Brookdale. Получено 2018-06-04.
- ^ Boseley S (26 марта 2012 г.). «Финансирование исследований деменции к 2015 году увеличится более чем вдвое, до 66 миллионов фунтов стерлингов». Хранитель. Лондон. ISSN 0261-3077. OCLC 60623878. В архиве из оригинала 20 октября 2013 г.. Получено 27 апреля 2012.
- ^ «Британские больницы перестраиваются с учетом деменции». Экономист. Получено 2018-09-17.
- ^ «Драйверы с деменцией - растущая проблема, - предупреждают доктора». CBC News, Канада. 19 сентября 2007 г. В архиве из оригинала от 2 октября 2007 г.
- ^ Томпсон С.Б. (2009). «Способность к завещанию и когнитивная реабилитация: последствия для людей с травмами головы и неврологическими нарушениями». Журнал когнитивной реабилитации. 27: 11–13.
- ^ «Борьба с деменцией». Журнал Филантропия. Зима 2016. В архиве из оригинала от 11.02.2016.
- ^ «Пол Харви: композитор с деменцией вдохновляет пожертвовать 1 миллион фунтов стерлингов». Новости BBC. Получено 2 ноября 2020.
- ^ Дейли Б., Томпселл А., Шарплинг Дж., Руни Ю.М., Хиллман Л., Ванони К.Л., Уайт С., Галлахер Дж. Э. (январь 2018 г.). «Резюме данных: взаимосвязь между здоровьем полости рта и деменцией» (PDF). Британский стоматологический журнал. 223 (11): 846–53. Дои:10.1038 / sj.bdj.2017.992. PMID 29192686. S2CID 19633523.
- ^ Миклосси, Дж (2015). «Исторические данные, подтверждающие причинно-следственную связь между спирохетальными инфекциями и болезнью Альцгеймера». Границы старения нейронауки. 7: 46. Дои:10.3389 / fnagi.2015.00046. ЧВК 4399390. PMID 25932012.
- ^ а б c Олсен И., Сингхрао СК (2015-09-17). «Может ли оральная инфекция быть фактором риска болезни Альцгеймера?». Журнал оральной микробиологии. 7: 29143. Дои:10.3402 / jom.v7.29143. ЧВК 4575419. PMID 26385886.
- ^ «Может ли плохое состояние полости рта привести к слабоумию?». Британский стоматологический журнал. 223 (11): 840. Декабрь 2017. Дои:10.1038 / sj.bdj.2017.1064. PMID 29243693. S2CID 25898592.
- ^ Картер CJ (февраль 2011 г.). «Бляшки и клубки болезни Альцгеймера: кладбище пирровой победы сети иммунной защиты против инфекции простого герпеса за счет разрушения нейронов, опосредованного комплементом и воспалением». Международная нейрохимия. 58 (3): 301–20. Дои:10.1016 / j.neuint.2010.12.003. PMID 21167244. S2CID 715832.
внешняя ссылка
| Классификация | |
|---|---|
| Внешние ресурсы |
![]() СМИ, связанные с Слабоумие в Wikimedia Commons
СМИ, связанные с Слабоумие в Wikimedia Commons
