Бета-ситостерин - Beta-Sitosterol
 | |
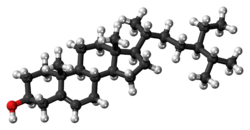 | |
| Имена | |
|---|---|
| Название ИЮПАК 17- (5-Этил-6-метилгептан-2-ил) -10,13-диметил-2,3,4,7,8,9,11,12,14,15,16,17-додекагидро-1ЧАС-циклопента [а] фенантрен-3-ол | |
| Другие имена 22,23-Дигидростигмастерол, Стигмаст-5-ен-3-ол, β-Ситостерин | |
| Идентификаторы | |
3D модель (JSmol ) | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.001.346 |
PubChem CID | |
| UNII | |
| |
| |
| Характеристики | |
| C29ЧАС50О | |
| Молярная масса | 414.718 г · моль−1 |
| Температура плавления | От 136 до 140 ° C (от 277 до 284 ° F, от 409 до 413 K)[1] |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
β-ситостерин (бета-ситостерин) является одним из нескольких фитостерины (растительные стерины) с химические структуры похожий на холестерин. Это белый воскообразный порошок с характерным запахом, входящий в состав пищевой добавки. E499. Фитостерины гидрофобны и растворимы в спиртах.
Природные явления и еда
Бета-ситостерин широко распространен в царство растений и найдено в растительное масло, орехи, авокадо и готовые продукты, такие как заправки для салатов.[2]
Человеческие исследования
β-ситостерин изучается на предмет его способности снижать доброкачественная гиперплазия предстательной железы (ДГПЖ)[3][4] и кровь холестерин уровни.[5]
Генетическое расстройство
Хотя растительные стерины обычно полезны, существует редкое аутосомно-рецессивное генетическое заболевание. фитостеринемия что вызывает чрезмерное всасывание фитостеринов.[6]
Предшественник анаболического стероида болденона
Будучи стероидом, β-ситостерин является предшественником анаболического стероида. Болденон. Болденона ундециленат обычно используется в ветеринарии для стимуляции роста крупного рогатого скота, но он также является одним из наиболее часто используемых анаболических стероидов в спорте. Это привело к подозрению, что некоторые спортсмены с положительным результатом на ундециленат болденона на самом деле не злоупотребляли самим гормоном, а употребляли пищу, богатую β-ситостерином.[7][8][9]
Химия
Химическая инженерия
Использование ситостерина в качестве промежуточного химического соединения в течение многих лет было ограничено из-за отсутствия химической точки атаки на боковой цепи, которая позволила бы его удалить. Активные усилия многих лабораторий в конечном итоге привели к открытию псевдомонады микроб это эффективно осуществило эту трансформацию. Ферментация переваривает всю алифатическую боковую цепь на углероде 17 с получением смеси 17-кето-продуктов, включая дегидроэпиандростерон.[10]
Синтез
Полный синтез β-ситостерина не достигнут. Однако β-ситостерин был синтезирован из стигмастерина. 1, который включает специфическое гидрирование боковой цепи стигмастерина.
На первом этапе синтеза образуется тозилат стигмастерола. 2 от стигмастерина 1 (Чистота 95%) с использованием p-TsCl, DMAP и пиридина (выход 90%). Тозилат 2 затем подвергается сольволизу при обработке пиридином и безводным МеОН с получением метилового эфира изо-стигмастерола в соотношении 5: 1 3 (Выход 74%) в метиловый эфир стигмастерина 4, который впоследствии удаляется хроматографией. На стадии гидрирования ранее предложенного синтеза использовались катализатор Pd / C и растворитель этилацетат. Однако из-за изомеризации во время гидролиза были протестированы другие катализаторы, такие как PtO2, и растворители, такие как этанол. С использованием другого катализатора мало что изменилось. Этанол, однако, предотвращал изомеризацию и образование неидентифицированной примеси с образованием соединения 5. Последней стадией синтеза является снятие защиты с двойной связи β-кольца 5 с p-TsOH, водным диоксаном и нагреванием (80 ° C) с получением β-ситостерина 6. Совокупный выход на последних двух стадиях составлял 55%, а общий выход синтеза составлял 37%.[11]

Биосинтез

Регуляция биосинтеза как стеринов, так и некоторых специфических липидов происходит во время биогенеза мембран.[12] С помощью паттернов мечения 13C было определено, что пути как мевалоната, так и дезоксиксилулозы участвуют в образовании β-ситостерина.[13] Точный механизм образования β-ситостерина варьируется в зависимости от организма, но, как правило, он происходит из циклоартенол.[14]
Биосинтез циклоартенола начинается с образования одной молекулы изопентенилдифосфата (IPP) и двух молекул диметилаллилдифосфата (DMAPP). фарнезил дифосфат (FPP). Затем две молекулы FPP соединяют хвост к хвосту, чтобы получить сквален, тритерпен. Сквален в результате реакции циклизации с 2,3-оксидоскваленом 6 в качестве промежуточного соединения образует циклоартенол.
Двойная связь циклоартенола (соединение 7 на схеме) метилируется SAM с образованием карбокатиона, который претерпевает гидридный сдвиг и теряет протон, давая соединение с метиленовой боковой цепью. Обе эти стадии катализируются метилтрансферазой стерол C-24 (стадия E1 на схеме). Затем соединение 8 катализируется стерол-C-4-деметилазой (E2) и теряет метильную группу с образованием циклоэукаленола. После этого циклопропановое кольцо открывается циклоэукаленолциклоизомеразой (E3) с образованием 10. Сложный 10 теряет метильную группу и подвергается аллильной изомеризации с образованием грамистерола 11. Эта стадия катализируется стерол-C-14-деметилазой (E4), стерин-Δ14-редуктазой (E5) и стерол-Δ8-Δ7-изомеразой (E6). Последняя метильная группа удаляется стеролдеметилазой (E7) с образованием эпистерола. 12. Эпистерол 12 метилируется SAM с образованием второго карбокатиона, который теряет протон с образованием 13. Эта стадия катализируется 24-метиленэстерол-C-метилтрансферазой (E8). Сложный 13 теперь подвергается восстановлению под действием НАДФН и модификациям β-кольца с образованием β-ситостерина.
Смотрите также
- Charantin, β-ситостерил глюкозид, обнаруженный в Горький лимон растение.
Рекомендации
- ^ Оджа, Вахур; Чен, Сюй; Hajaligol, Mohammad R .; Чан, В. Джеффри (2009). «Термодинамические параметры сублимации холестерина, эргостерола, β-ситостерина и стигмастерола». Журнал химических и технических данных. 54 (3): 730–734. Дои:10.1021 / je800395m.
- ^ «Данные о питании: продукты с самым высоким содержанием бета-ситостерина на порцию 200 калорий». Conde Nast, Национальная база данных по питательным веществам Министерства сельского хозяйства США, версия SR-21. 2014 г.. Получено 25 сентября 2015.
- ^ Уилт, Т; Ишани, А; Макдональд, Р. Старк, G; Mulrow, C; Лау, Дж (2000). «Бета-ситостерины при доброкачественной гиперплазии простаты». Кокрановская база данных систематических обзоров (2): CD001043. Дои:10.1002 / 14651858.CD001043. PMID 10796740.
- ^ Kim, T. H .; Lim, H.J .; Kim, M. S .; Ли, М. С. (2012). «Биологически активные добавки при доброкачественной гиперплазии простаты: обзор систематических обзоров». Maturitas. 73 (3): 180–5. Дои:10.1016 / j.maturitas.2012.07.007. PMID 22883375.
- ^ Рудковска И., Абу-Мвейс С.С., Николь С., Джонс П.Дж. (2008). «Эффективность растительных стеролов в снижении холестерина в обезжиренном йогурте, потребляемом в качестве закуски или во время еды». J Am Coll Nutr. 27 (5): 588–95. Дои:10.1080/07315724.2008.10719742. PMID 18845709.
- ^ Patel Manoj D .; Томпсон Пол Д. (2006). «Фитостерины и сосудистые заболевания». Атеросклероз. 186 (1): 12–19. Дои:10.1016 / j.atherosclerosis.2005.10.026. PMID 16325823.
- ^ Г. Галлина; Г. Ферретти; Р. Мерланти; C. Civitareale; Ф. Каполонго; Р. Драйши; К. Монтесисса (2007). «Болденон, Болдион и заменители молока в рационе телят: влияние содержания фитостерола на выведение метаболитов болденона с мочой». J. Agric. Food Chem. 55 (20): 8275–8283. Дои:10.1021 / jf071097c. PMID 17844992.
- ^ Рос М.М., Стерк С.С., Верхаген Х., Сталенхоф А.Ф., де Йонг Н. (2007). «Потребление фитостерола и анаболический стероид болденон у людей: экспериментальная гипотеза» (PDF). Пищевая добавка. Contam. 24 (7): 679–84. Дои:10.1080/02652030701216727. PMID 17613052.
- ^ Р. Драйши; Р. Мерланти; Г. Ферретти; Л. Фантоцци; К. Ферранти; Ф. Каполонго; С. Сегато; К. Монтесисса (2007). «Профиль экскреции болденона с мочой телят, получавших два разных заменителя молока». Analytica Chimica Acta. 586 (1–2): 171–176. Дои:10.1016 / j.aca.2007.01.026. PMID 17386709.
- ^ Lenz, G.R .; Энциклопедия химической технологии Кирка-Отмера, 3-е изд., Wiley Interscience, Лондон, 1983, Vol. 21, 645.
- ^ Маккарти, ФО; Чопра, Дж; Форд, А; Hogan, SA; Керри, JP; О'Брайен, Нью-Мексико; Райан, Э; Магуайр, АР (2005). «Синтез, выделение и характеристика производных бета-ситостерина и бета-ситостерина оксида». Органическая и биомолекулярная химия. 3 (16): 3059–65. Дои:10.1039 / b505069c. PMID 16186940.
- ^ Хартманн, Мари-Андре (2003). «Метаболизм и функции 5 стеролов у высших растений». Липидный метаболизм и мембранный биогенез. Темы современной генетики. 6. С. 183–211. Дои:10.1007/978-3-540-40999-1_6. ISBN 978-3-540-20752-8.
- ^ Де-Экнамкул В .; Потдуанг Б. (2003). «Биосинтез β-ситостерола и стигмастерина в Croton sublyratus происходит через смешанное происхождение единиц изопрена». Фитохимия. 62 (3): 389–398. Дои:10.1016 / S0031-9422 (02) 00555-1. PMID 12620352.
- ^ Дьюик, П. М. Лекарственные натуральные продукты: биосинтетический подход. 3-е изд .; John Wiley & Sons Ltd.: Циклизация Соединенного Королевства, 2009 г .; С. 539.
