Норметандрон - Normethandrone - Wikipedia
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Металютин и др. |
| Другие имена | Норметандрон; Метилэстренолон; Метилоэстренолон; Метилнортестостерон; Норметилтестостерон; Норметандролон; Норметистерон; Метилнандролон; NMT; 17α-метил-19-нортестостерон; 17α-метилэстр-4-ен-17β-ол-3-он; Р-6051; RU-598; NSC-10039 |
| Маршруты администрация | Устно |
| Класс препарата | Прогестаген; Прогестин; Андроген; Анаболический стероид |
| Код УВД | |
| Идентификаторы | |
| |
| Количество CAS | |
| PubChem CID | |
| ChemSpider | |
| UNII | |
| ЧЭМБЛ | |
| Панель управления CompTox (EPA) | |
| ECHA InfoCard | 100.007.440 |
| Химические и физические данные | |
| Формула | C19ЧАС28О2 |
| Молярная масса | 288.431 г · моль−1 |
| 3D модель (JSmol ) | |
| |
| |
Норметандрон, также известный как метилэстренолон или же метилнортестостерон и продается под торговой маркой Металютин среди прочего, это прогестин и андроген /анаболический стероид (AAS) лекарство, которое используется в сочетании с эстроген в лечении аменорея и менопаузальный симптомы у женщин.[1][2][3][4] Принято устно.[5]
Побочные эффекты Норметандрон включают симптомы из маскулинизация подобно угревая сыпь, усиленный рост волос, голос меняется, и увеличил сексуальное желание.[6] Это также может вызвать повреждение печени.[7] Норметандрон - это прогестин или синтетический прогестаген, и, следовательно, является агонист из рецептор прогестерона, то биологическая мишень прогестагенов, таких как прогестерон.[5] Это также синтетический AAS и, следовательно, является агонист из рецептор андрогенов, то биологическая мишень андрогенов как тестостерон и дигидротестостерон (DHT).[4][8] В нем есть эстрогенный активность, а не другие важные гормональный Мероприятия.[9][1][3]
Норметандрон был введен для использования в медицине в 1957 году.[10] Он доступен только в нескольких странах, в том числе Бразилия, Индонезия, и Венесуэла, и доступен только в сочетании с метилэстрадиол или же эстрадиола валерат.[2][1]
Медицинское использование
Норметандрон используется в сочетании с эстроген, либо метилэстрадиол или же эстрадиола валерат, при лечении аменорея и менопаузальный симптомы у женщин.[1][2][11] Он также использовался для лечения дисменорея у женщин.[12] Норметандрон успешно применялся для подавления либидо у мужчин с сексуальные отклонения.[13] Хотя норметандрон может быть классифицирован как ААС и обладает сильным подобным действием при достаточно высоких дозах, он обычно не используется как таковой, а вместо этого используется в медицине только как прогестин.[3][1][4] Это потому, что по сравнению с ним он очень прогестаген.[4]
| Маршрут | Медикамент | Основные торговые марки | Форма | Дозировка |
|---|---|---|---|---|
| Устный | Ундеканоат тестостерона | Андриол, Джатензо | Капсула | 40–80 мг 1 раз в 1-2 дня |
| Метилтестостерон | Метандрен, Estratest | Планшет | 0,5–10 мг / день | |
| Флуоксиместерон | Халотестин | Планшет | 1–2,5 мг 1 раз / 1–2 дня | |
| Норметандрона | Гинекозид | Планшет | 5 мг / день | |
| Тиболон | Ливиал | Планшет | 1,25–2,5 мг / день | |
| Прастерон (DHEA)б | – | Планшет | 10–100 мг / день | |
| Сублингвальный | Метилтестостерон | Метандрен | Планшет | 0,25 мг / день |
| Трансдермальный | Тестостерон | Intrinsa | Пластырь | 150–300 мкг / день |
| АндроГель | Гель, крем | 1–10 мг / день | ||
| Вагинальный | Прастерон (DHEA) | Intrarosa | Вставлять | 6,5 мг / день |
| Инъекция | Тестостерона пропионата | Тестовирон | Масляный раствор | 25 мг 1 раз в 1-2 недели |
| Тестостерон энантат | Делатестрил, Primodian Depot | Масляный раствор | 25–100 мг 1 раз в 4–6 недель | |
| Ципионат тестостерона | Депо-тестостерон, депо-тестадиол | Масляный раствор | 25–100 мг 1 раз в 4–6 недель | |
| Изобутират тестостеронаа | Фемандрен М, Фоливирин | Водная суспензия | 25-50 мг 1x / 4-6 недель | |
| Смешанные эфиры тестостерона | Климактерона | Масляный раствор | 150 мг 1x / 4-8 недель | |
| Омнадрен, Сустанон | Масляный раствор | 50–100 мг 1 раз / 4–6 недель | ||
| Деканоат нандролона | Дека-дураболин | Масляный раствор | 25-50 мг 1 раз / 6-12 недель | |
| Прастерон энантата | Гинодиан Депо | Масляный раствор | 200 мг 1 раз / 4–6 недель | |
| Имплант | Тестостерон | Testopel | Пеллет | 50–100 мг 1 раз в 3–6 месяцев |
| Примечания: Пременопаузальный женщины производят около 230 ± 70 мкг тестостерон в день (6,4 ± 2,0 мг тестостерона за 4 недели) с диапазоном от 130 до 330 мкг в день (3,6–9,2 мг за 4 недели). Сноски: а = В основном снято с производства или недоступно. б = Без рецепта. Источники: См. Шаблон. | ||||
| Маршрут | Медикамент | Форма | Дозировка | |
|---|---|---|---|---|
| Устный | Метилтестостерон | Планшет | 30–200 мг / день | |
| Флуоксиместерон | Планшет | 10-40 мг 3 раза в день | ||
| Калустероне | Планшет | 40–80 мг 4 раза в день | ||
| Норметандрон | Планшет | 40 мг / день | ||
| Буккальный | Метилтестостерон | Планшет | 25–100 мг / день | |
| Инъекция (Я или же SC ) | Тестостерона пропионат | Масляный раствор | 50–100 мг 3 раза в неделю | |
| Тестостерон энантат | Масляный раствор | 200–400 мг 1 раз в 2–4 недели | ||
| Ципионат тестостерона | Масляный раствор | 200–400 мг 1 раз в 2–4 недели | ||
| Смешанные эфиры тестостерона | Масляный раствор | 250 мг 1 раз в неделю | ||
| Метандриол | Водная суспензия | 100 мг 3 раза в неделю | ||
| Андростанолон (DHT) | Водная суспензия | 300 мг 3 раза в неделю | ||
| Дростанолона пропионат | Масляный раствор | 100 мг 1–3 раза в неделю | ||
| Метенолона энантат | Масляный раствор | 400 мг 3 раза в неделю | ||
| Деканоат нандролона | Масляный раствор | 50–100 мг 1 раз в 1–3 недели | ||
| Фенилпропионат нандролона | Масляный раствор | 50–100 мг / неделя | ||
| Примечание: Дозировки не обязательно эквивалентны. Источники: См. Шаблон. | ||||
Доступные формы
Норметандрон продается в сочетании с метилэстрадиол в виде устный таблетки содержащий 5 мг норметандрона и 0,3 мг метилэстрадиола.[11][14]
Побочные эффекты
Норметандрон был связан с симптомы из маскулинизация и гепатотоксичность.[6][7][15]
Фармакология
Фармакодинамика
Норметандрон показывает высокий уровень прогестагенный Мероприятия.[5] С сублингвальное введение у женщин он как минимум в 150 раз больше потенция сублингвальных прогестерон и в 50 раз эффективнее сублингвального этистерон.[5] Он также в 10 раз эффективнее вводимого этим путем прогестерона.[5] Оральная эффективность норметандрона с точки зрения трансформация эндометрия похож на норэтистерон.[16][17] Сообщалось, что он подавляет овуляция у женщин.[18]
Помимо прогестагенной активности, норметандрон обладает анаболический и андрогенный активности и может вызывать эффекты, связанные с этой деятельностью.[1][4] Он имеет высокое соотношение анаболической и андрогенной активности.[19] Анаболический потенция Норметандрон похож на норетандролон и намного больше, чем у нандролон или же метандиенон.[8] Это также больше, чем у этилэстренол.[8] Было обнаружено, что норметандрон увеличивает задержка азота, мера анаболического эффекта, при дозировке 30 мг / день.[20] Аналогично нандролону и норетандролон, 5α-дигидронорметандрон, то 5α-восстановленный метаболит норметандрона, показывает снижение близость для рецептор андрогенов относительно норметандрона.[21][22] Его сродство к рецептору андрогенов составляет примерно от 33 до 60% от сродства норметандрона.[21]
Норметандрон имеет эстрогенный активность через ароматизация в метилэстрадиол.[3]
| Сложный | PR | AR | ER | GR | МИСТЕР | SHBG | CBG |
|---|---|---|---|---|---|---|---|
| Норметандрон | 75–125 | 125–150 | <1 | 1–5 | <1 | ? | ? |
| 5α-дигидронорметандрон | 15–25 | 50–75 | ? | <1 | ? | ? | ? |
| Примечания: Значения указаны в процентах (%). Ссылка лиганды (100%) были прогестерон для PR, тестостерон для AR, эстрадиол для ER, дексаметазон для GR, и альдостерон для МИСТЕР. Источники: См. Шаблон. | |||||||
Фармакокинетика
Норметандрон - это метаболизируется к ароматаза в метилэстрадиол в небольших количествах, аналогично метилтестостерон и метандиенон.[3][23][24] Метаболиты норметандрона изучены недостаточно, но 5α-дигидронорметандрон вероятный метаболит, образованный 5α-редуктаза.[25][26]
В фармакокинетика Норметандрона были рассмотрены.[27]
Химия
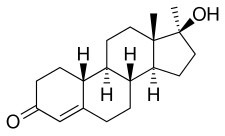
Норметандрон, также известный как 17α-метил-19-нортестостерон или 17α-метилэстр-4-ен-17β-ол-3-он, представляет собой синтетический эстран стероидный препарат и 17α-алкилированный производная из нандролон (19-нортестостерон; 19-NT). В частности, это 17α-метил производное нандролона, а также 17α-метиловый вариант норетандролон (17α-этил-19-NT) и норэтистерон (17α-этинил-19-NT).[28]
Синтез
Химический синтез норметандрона были опубликованы.[27]
История
Норметандрон продается для медицинского применения с 1957 года.[10] Комбинация норметандрона и метилэстрадиола была введена как минимум к 1966 году.[14]
Общество и культура
Родовые имена
Норметандрону не назначали ГОСТИНИЦА или другие официальные названия.[28][29][2] Он также известен как метилэстренолон, метилнортестостерон, норметандролон, и норметистерон.[28][29][2]
Фирменные наименования
Торговые марки норметандрона включают Батынид, Гинекозид, Гинекозид, Гиномин, Лутенин, Матронал, Медиол, Металутин, Металутин, Оргастерон, Оростерон и Ренодиол.[28][29][2][1][30][11]
Доступность
Норметандрон продается в Бразилия, Индонезия, и Венесуэла в комбинации с метилэстрадиол или же эстрадиола валерат.[2][1]
Рекомендации
- ^ а б c d е ж грамм час https://www.medicinescomplete.com/about/
- ^ а б c d е ж грамм https://www.drugs.com/international/normethandrone.html
- ^ а б c d е Фридл К.Э. (1990). «Переоценка рисков для здоровья, связанных с использованием высоких доз пероральных и инъекционных андрогенных стероидов». NIDA Res. Monogr. 102: 142–77. PMID 1964199.
- ^ а б c d е Х.-Л. Крюскемпер (22 октября 2013 г.). Анаболические стероиды. Эльзевир. С. 10–. ISBN 978-1-4832-6504-9.
- ^ а б c d е Ферин Дж (1956). «Новое вещество с прогестагенной активностью; сравнительные исследования у женщин с удаленными яичниками; клинические результаты». Акта Эндокринол. 22 (4): 303–17. Дои:10.1530 / acta.0.0220303. PMID 13354223.
- ^ а б Лундберг, П.О. (1962). «Профилактика мигрени с помощью гестагенов». Европейский журнал эндокринологии. 40 (4 Прил.): S5 – S22. Дои:10.1530 / acta.0.040S0005. ISSN 0804-4643.
- ^ а б Делоримье А.А., Гордан Г.С., Лоу Р.С., Карбон СП (1965). «Метилтестостерон, родственные стероиды и функция печени». Arch. Междунар. Med. 116 (2): 289–94. Дои:10.1001 / archinte.1965.03870020129023. PMID 14315662.
- ^ а б c Брюггемайер, Роберт В. (2006). «Половые гормоны (мужские): аналоги и антагонисты». Энциклопедия молекулярной клеточной биологии и молекулярной медицины. п. 42. Дои:10.1002 / 3527600906.mcb.200500066. ISBN 3527600906.
- ^ Эрих Хефтманн (1970). Стероидная биохимия. Академическая пресса. п. 72. ISBN 9780123366504.
Норметандрон (рис. 49) представляет собой производное 19-нортестостерона, обладающее прогестационной, а также андрогенной и анаболической активностью.
- ^ а б Соединенные Штаты. Патентное ведомство (1957 г.). Официальный вестник Патентного ведомства США. Патентное ведомство США.
- ^ а б c Не включенные в перечень лекарственные препараты. Фармацевтическая секция, Ассоциация специальных библиотек. 1982 г.
Батынид. C. Каждое драже содержит: норметандрон, 5 мг; и метилэстрадиол 0,3 мг. E. (Ранее) Gynaekosid. М. Берингер Биохимия, Флоренция. А. Эстрогенный; Риск вторичной аменореи. Р. Нотиз Мед Фарм 32; 295, ноябрь-декабрь 81.
- ^ Беньи-Кальвет, Д. (1959). «Два свойства метилэстренолона (17-альфа-метил-19-нортестостерон): его эффективность в лечении дисменореи, его анаболическое действие». Gynécologie Pratique. 10: 261–272. PMID 13798272.
- ^ Серве Дж. (1973). «Клиническое исследование случаев психосексуальных нарушений у мужчин, получавших лечение ингибитором либидо: метилэстренолоном». Архивы сексуального поведения. 2 (4): 387–390. Дои:10.1007 / BF01541012. ISSN 0004-0002. S2CID 145090184.
- ^ а б Akingba JB, Ayodeji EA (февраль 1966 г.). «Аменорея как ведущий симптом хориокарциномы». J Obstet Gynaecol Br Commonw. 73 (1): 153–5. Дои:10.1111 / j.1471-0528.1966.tb05137.x. PMID 5948541. S2CID 38008851.
- ^ Фельдман, Элейн Босак; Картер, Энн С.; Kossa, Jane L .; Маккаррик, Джеймс Ф .; Шварц, Гарольд Л. (1960). «Эндокринологические и метаболические эффекты 17α-метил-19-нортестостерона у женщин». Журнал клинической эндокринологии и метаболизма. 20 (6): 842–857. Дои:10.1210 / jcem-20-6-842. ISSN 0021-972X. PMID 13822027.
- ^ Горски, Ян; Пресл, Иржи (1981). «Гормональное лечение нарушений менструального цикла». В J. Horsky; J. Presl (ред.). Функция яичников и ее нарушения: диагностика и лечение. Springer Science & Business Media. С. 309–332. Дои:10.1007/978-94-009-8195-9_11. ISBN 978-94-009-8195-9.
- ^ Boschann HW (июль 1958 г.). «Наблюдения за ролью прогестагентов в гинекологических заболеваниях человека и осложнениях беременности». Анна. Акад. Наука. 71 (5): 727–52. Дои:10.1111 / j.1749-6632.1958.tb46803.x. PMID 13583829.
- ^ Camerino, B .; Сала, Г. (1960). "Анаболические стероиды". Fortschritte der Arzneimittelforschung / Прогресс в исследованиях лекарственных средств / Progrès des recherches Pharmaceutiques. Fortschritte der Arzneimittelforschung. Прогресс в исследованиях лекарств. Progres des Recherches Pharmaceutiques. 2. С. 71–134. Дои:10.1007/978-3-0348-7038-2_2. ISBN 978-3-0348-7040-5. PMID 14448579.
- ^ Чарльз Д. Кочакян (6 декабря 2012 г.). Анаболически-андрогенные стероиды. Springer Science & Business Media. С. 379–. ISBN 978-3-642-66353-6.
- ^ Ральф И. Дорфман (5 декабря 2016 г.). Стероидная активность у экспериментальных животных и человека. Elsevier Science. С. 68–. ISBN 978-1-4832-7300-6.
- ^ а б Охасу Т., Делеттре Дж., Морнон Дж. П., Турпин-Ван-Дайк С., Рейно Дж. П. (1987). «К картированию рецепторов прогестерона и андрогенов». J. Стероид Биохим. 27 (1–3): 255–69. Дои:10.1016/0022-4731(87)90317-7. PMID 3695484.
- ^ Behre HM, Kliesch S, Lemcke B, von Eckardstein S, Nieschlag E (декабрь 2001 г.). «Подавление сперматогенеза до азооспермии путем комбинированного введения антагониста GnRH и 19-нортестостерона не может поддерживаться одним этим неароматизируемым андрогеном». Гм. Репрод. 16 (12): 2570–7. Дои:10.1093 / humrep / 16.12.2570. PMID 11726576.
- ^ Детлеф Тиме; Петер Хеммерсбах (18 декабря 2009 г.). Допинг в спорте. Springer Science & Business Media. С. 470–. ISBN 978-3-540-79088-4.
- ^ Уильям Ллевеллин (2011). Анаболики. Molecular Nutrition Llc. С. 444–454, 533. ISBN 978-0-9828280-1-4.
- ^ Fragkaki AG, Angelis YS, Tsantili-Kakoulidou A, Koupparis M, Georgakopoulos C (май 2009 г.). «Схемы метаболических паттернов анаболических андрогенных стероидов для оценки метаболитов дизайнерских стероидов в моче человека». J. Steroid Biochem. Мол. Биол. 115 (1–2): 44–61. Дои:10.1016 / j.jsbmb.2009.02.016. PMID 19429460. S2CID 10051396.
- ^ Шьёльберг, Т. Х. (2013). Синтез in vitro метаболитов трех анаболических андрогенных стероидов микросомами печени человека (Магистерская диссертация, Институт биотехнологий). https://brage.bibsys.no/xmlui/handle/11250/246018
- ^ а б Die Gestagene. Springer-Verlag. 27 ноября 2013. С. 12–13, 282. ISBN 978-3-642-99941-3.
- ^ а б c d Дж. Элкс (14 ноября 2014 г.). Словарь лекарственных средств: химические данные: химические данные, структуры и библиографии. Springer. С. 888–. ISBN 978-1-4757-2085-3.
- ^ а б c И.К. Мортон; Джудит М. Холл (6 декабря 2012 г.). Краткий словарь фармакологических агентов: свойства и синонимы. Springer Science & Business Media. С. 202–. ISBN 978-94-011-4439-1.
- ^ Мартин Негвер; Ханс-Георг Шарнов (2001). Органико-химические препараты и их синонимы: (международное исследование). Wiley-VCH. п. 1831 г. ISBN 978-3-527-30247-5.
