Фармакокинетика прогестерона - Pharmacokinetics of progesterone
В фармакокинетика прогестерона, касается фармакодинамика, фармакокинетика, и различные пути введения из прогестерон.[16][17]
Прогестерон - это встречающиеся в природе и биоидентичный прогестаген, или агонист из рецептор прогестерона, то биологическая мишень из прогестагены любить эндогенный прогестерон.[16] Прогестерон также имеет антиминералокортикоид и тормозящий нейростероид активности, в то время как она, похоже, практически не имеет глюкокортикоид или антиандрогенный активности и не имеет андрогенный Мероприятия.[16] Прогестерон обладает прогестагенной активностью. антиэстрогенный эффекты в некоторых ткани такой как матка, шейка матки, и влагалище.[16] Кроме того, прогестерон имеет антигонадотропный эффекты из-за его прогестагенной активности и могут подавлять плодородие и подавить половой гормон производство.[16] Прогестерон отличается от прогестины (синтетический прогестагены ) любить медроксипрогестерона ацетат и норэтистерон, с последствиями для фармакодинамика и фармакокинетика а также эффективность, переносимость, и безопасность.[16]
Прогестерон можно принимать устно, через влагалище, и по инъекция в мышца или жир, среди других маршрутов.[16] А вагинальное кольцо с прогестероном и прогестерон внутриматочная спираль также доступны в виде фармацевтических продуктов.[18][19]
Нормальные уровни
Прогестерон используется как часть заместительной гормональной терапии у людей с низким уровнем прогестерона и по другим причинам. Для сравнения с нормальными физиологическими условиями, уровни прогестерона в лютеиновой фазе составляют от 4 до 30 нг / мл, в то время как уровни прогестерона в фолликулярной фазе составляют от 0,02 до 0,9 нг / мл, уровни в менопаузе составляют от 0,03 до 0,3 нг / мл и уровни прогестерона. у мужчин от 0,12 до 0,3 нг / мл.[20][21] Во время беременности уровень прогестерона в первые 4–8 недель составляет от 25 до 75 нг / мл, а при доношенных сроках - от 140 до 200 нг / мл.[22][20] Производство прогестерона в организме на поздних сроках беременности составляет примерно 250 мг в день, 90% которого попадает в кровоток матери.[23]
- Нормальный уровень прогестерона у женщин

Уровни прогестерона в менструальный цикл при нормальной езде на велосипеде, овуляторный женщины.[24] Пунктирные горизонтальные линии представляют собой средние интегрированные уровни для каждой кривой, а пунктирная вертикальная линия - середина цикла (примерно при овуляции).

Уровни эстрогена и прогестерона в детском и подростковом возрасте, в том числе: половое созревание, у девочек.[25][26][27] Пунктирная вертикальная линия - средний возраст менархе (первый менструация и наступление менструальные циклы ).

Эстроген, прогестерон и 17α-гидроксипрогестерон (17α-OHP) уровни во время беременность у женщин.[28] Пунктирные вертикальные линии разделяют триместры.
Пути администрирования
| Маршрут | Форма | Доза | CМаксимум (нг / мл) | ТМаксимум (часы) | т1/2 (часы) | ||
|---|---|---|---|---|---|---|---|
| Устный | Капсула | 200 мг | 4.3–11.7 | 2–2.5 | ? | ||
| Сублингвальный | Планшет[а] | 100 мг | 13.5 | 1–4 | ~6–7 | ||
| Подвеска | 100 мг | 17.6 | 0.5–1 | ? | |||
| Вагинальный | Планшет[а] | 100 мг | 10.9 | 6–7 | 13.7 | ||
| Капсула | 100 мг | 9.7 | 1–3 | ? | |||
| Внутримышечный инъекция | Масляный раствор | 50 мг | 14.3 | 8.7 | ? | ||
| 100 мг | 113 | 6.7 | 22.3 | ||||
| Aq. решение[b] | 100 мг | 440 | 0.88 | 14.3 | |||
| Подкожный инъекция | Aq. решение[b] | 25 мг | 57.8 | 0.92 | 13.1 | ||
| 50 мг | 103 | 0.92 | 17.2 | ||||
| 100 мг | 235–300 | 0.92 | 17.2–17.6 | ||||
| |||||||
| Маршрут | Форма | Доза | Название бренда | Доступность[b] |
|---|---|---|---|---|
| Устный | Капсула | 100, 200, 300 мг | Прометриум[c] | Широко распространенный |
| Таблетка (SR) | 200, 300, 400 мг | Dubagest SR[c] | Индия | |
| Сублингвальный | Планшет | 10, 25, 50, 100 мг | Лютеина[c] | Европа[d] |
| Трансдермальный | Гель[e] | 1% (25 мг) | Прожестожель | Европа |
| Вагинальный | Капсула | 100, 200 мг | Утрожестан | Широко распространенный |
| Планшет | 100 мг | Эндометрин[c] | Широко распространенный | |
| Гель | 4,8% (45, 90 мг) | Crinone[c] | Широко распространенный | |
| Суппозиторий | 200, 400 мг | Циклогест | Европа | |
| Кольцо | 10 мг / день[f] | Фертиринг[c] | Южная Америка[г] | |
| Ректальный | Суппозиторий | 200, 400 мг | Циклогест | Европа |
| Матка | ВМС | 38 мг | Прогестасерт | Снято с производства |
| Внутримышечный инъекция | Масляный раствор | 2, 5, 10, 20, 25, 50, 100 мг / мл | Пролутон[c] | Широко распространенный |
| Aq. Susp. | 12,5, 30, 100 мг / мл | Аголютин[c] | Европа[час] | |
| Эмульсия | 5, 10, 25 мг / мл | Ди-про-эмульсия | Снято с производства | |
| Микросф. | 20, 100 мг / мл | ProSphere[c] | Мексика | |
| Подкожный | Aq. soln. (травма) | 25 мг / флакон | Пролутекс | Европа |
| Имплант | 50, 100 мг | Пролутон[c] | Снято с производства | |
| Внутривенно | Aq. soln. (травма) | 20 мг / мл | Примолют | Снято с производства |
Источники и сноски:
| ||||
В фармакокинетика прогестерона зависят от его путь введения. Медикамент одобрен в виде масло -заполненный капсулы содержащие микронизированный прогестерон для пероральное введение, называемый «микронизированный прогестерон для перорального применения» («OMP») или просто «прогестерон для перорального приема».[40] Он также доступен в виде вагинальный или ректальный суппозитории, вагинальный гели, масляные растворы для внутримышечная инъекция, и водные растворы для подкожная инъекция, среди прочего.[40][12][41]
Пути администрирования что прогестерон использовался, включая устный, интраназальный, трансдермальный, вагинальный, ректальный, внутримышечный, подкожный, и внутривенная инъекция.[12] Было обнаружено, что пероральный прогестерон уступает вагинальному и внутримышечному прогестерону с точки зрения поглощение (низкий) и скорость оформления (быстрый).[12] Вагинальный прогестерон доступен в форме прогестерона. гель, кольца, и суппозитории или пессарии.[12] Преимущества интравагинального введения прогестерона перед пероральным включают высокий биодоступность, быстрый поглощение, избегание метаболизм первого прохождения, устойчивые концентрации в плазме и местное эндометрий эффект, в то время как преимущества интравагинального прогестерона по сравнению с внутримышечной инъекцией включают большее удобство и отсутствие боли в месте инъекции.[12]
Прогестерон интраназально как назальный спрей было обнаружено, что он эффективен для достижения терапевтических уровней и не был связан с раздражением носа, но был связан с неприятным вкусом спрея.[12] Ректальный, внутримышечный и внутривенный пути введения могут быть неудобными, особенно при длительном лечении.[12] Уровни прогестерона в плазме одинаковы после вагинального и ректального введения, несмотря на разные пути введения, и ректальное введение является альтернативой вагинальному прогестерону в условиях вагинальная инфекция, цистит, недавний роды, или когда барьерные методы контрацепции используются.[12] Внутримышечная инъекция прогестерона может привести к гораздо более высоким уровням прогестерона, чем нормальные концентрации лютеиновой фазы и уровни, достигаемые другими путями.[12]
Пероральное введение
Методологические вопросы в исследованиях
Знания о фармакокинетика перорального приема прогестерона осложняется использованием некорректных аналитические методы.[42][43][44] Когда прогестерон принимают внутрь, из-за метаболизм первого прохождения, очень высокий уровень его метаболиты происходят.[42][43][44] В большинстве предыдущих исследований использовался метод, известный как иммуноанализ (IA) для измерения уровня прогестерона.[42][43][44] Однако ИА без хроматографическое разделение (CS) имеет высокий перекрестная реактивность и не может отличить прогестерон от метаболитов, таких как аллопрегнанолон и прегнанолон.[42][43][44] В результате исследования, в которых оценивалась фармакокинетика перорального прогестерона с использованием IA, сообщили о ложно высоких уровнях прогестерона и неточных зависимых фармакокинетических параметрах.[42][43][44]
Сравнительные исследования с использованием надежных и точных методов, таких как жидкостная хроматография – масс-спектрометрия (ЖХ – МС) и IA в сочетании с адекватным CS обнаружили, что IA без CS переоценивает уровни прогестерона в 5-8 раз.[42][43][44] По этой причине использование надежных анализов обязательно при изучении фармакокинетики перорального прогестерона, и знание этих методологических вопросов также важно для точного понимания фармакокинетики перорального прогестерона.[42][43][44] И наоборот, те же проблемы не применимы к парентеральным путям введения прогестерона, таким как вагинальное введение и внутримышечная инъекция, потому что эти пути не подлежат первому прохождению и образуются относительно низкие уровни метаболитов прогестерона.[42][43][44]
Абсорбция, биодоступность и уровни
В устный биодоступность прогестерона очень мало.[45] В исследованиях с использованием ИА биодоступность прогестерона при пероральном приеме обычно составляла менее 10%.[45] в одном исследовании сообщалось о значениях от 6,2 до 8,6%.[46][11] Однако эти значения являются завышенными; исследование с использованием ЖХ-МС показало, что биодоступность прогестерона при пероральном приеме составляет всего 2,4% по сравнению с вагинальным гелем прогестерона.[1] Более того, это не относилось к стандарту прогестерона для внутримышечной инъекции, который имеет гораздо более высокую биодоступность, чем вагинальный прогестерон.[47][4] Очень низкая биодоступность прогестерона при пероральном приеме связана с тем, что он плохо поглощен от желудочно-кишечный тракт и претерпевает массовые метаболизм, что приводит к почти полной инактивации при первом проходе через печень.[45][48] Из-за его низкой пероральной биодоступности очень высокие дозы прогестерона должны использоваться перорально для достижения значительных уровней циркулирующего прогестерона.[45] Кроме того, прогестерон для перорального приема сегодня всегда микронизирован и взвешен в масле.[45][40][47][49] Это значительно улучшает биодоступность перорального прогестерона по сравнению с простым измельченным прогестероном и позволяет использовать его в практических дозах.[45] Когда используется термин «пероральный прогестерон», то, что используется в клинической практике и что почти всегда упоминается, если не указано иное, является микронизированный прогестерон приостановлено в масло.[45][16][42]
Микронизация - это процесс уменьшения среднего диаметра частицы из твердый материал.[32] За счет микронизации прогестерона его частицы становятся меньше (в основном <10 мкМ), а его площадь поверхности увеличивается, тем самым увеличивая абсорбцию из кишечник.[45][32] Приостановка и частичная солюбилизация[50] прогестерона в масле, содержащем Средняя- к Длинная цепочка жирные кислоты аналогичным образом улучшает биодоступность прогестерона при пероральном приеме.[16][51][52] Прогестерон - это липофильный соединение, и было предположено, что суспензия прогестерона в масле может улучшить его абсорбцию лимфатическая система, тем самым позволяя части перорального прогестерона обходить первое прохождение через печень и, следовательно, повышая его биодоступность.[45][53][54][55] По сравнению с простым измельченным прогестероном пиковые уровни прогестерона после однократной пероральной дозы 200 мг были увеличены в 1,4 раза при микронизации, в 1,2 раза при суспендировании в масле и в 3,2 раза при сочетании микронизации и суспендирования в масле.[55] Пероральный микронизированный прогестерон, суспендированный в масле, быстро и почти полностью всасывается из кишечника.[13] Есть широкий межиндивидуальная изменчивость в биодоступности прогестерона при приеме внутрь.[16][11] Поскольку прогестерон не применялся перорально в течение многих десятилетий из-за его плохой биодоступности (до введения микронизированного прогестерона перорально в масляных желатиновых капсулах в 1980 г.),[47] оральные прогестины (синтетический прогестагены) с улучшенными метаболическая стабильность и высокая пероральная биодоступность были разработаны и использовались вместо этого в клинических условиях.[56]
При пероральном применении прогестерона в типичных клинических дозах надежными методами измеряются только очень низкие уровни прогестерона.[42][43][44] После однократных доз прогестерона перорально с помощью ЖХ-МС были измерены пиковые уровни прогестерона от 1,5 до 2,4 нг / мл при дозе 100 мг и от 2,8 до 4,7 нг / мл при дозе 200 мг. жидкостная хроматография – тандемная масс-спектрометрия (ЖХ – МС / МС) и ИА с адекватным CS.[42][57][1] В одном из таких исследований, хотя пиковые уровни прогестерона составляли 2,2 нг / мл после однократного приема 100 мг перорального прогестерона, уровни прогестерона оставались значительно повышенными менее чем примерно на 4 часа, а средние уровни прогестерона в течение 24 часов были всего 0,14 нг / мл.[44][1] Для сравнения нормальный уровень прогестерона во время лютеиновой фазы из менструальный цикл при ЖХ-МС / МС от 6,7 до 22,2 нг / мл.[58] Когда один ИА использовался для измерения уровней прогестерона при пероральном приеме прогестерона, наблюдались гораздо более высокие пиковые уровни от 6,5 до 10,2 нг / мл, от 13,8 до 19,9 нг / мл и от 32,3 до 49,8 нг / мл после однократного приема 100, 200 и Дозы 300 мг соответственно.[46][11] Одно исследование на основе IA даже сообщило о максимальных уровнях прогестерона от 16 до 626 нг / мл (в среднем 247 нг / мл) при однократной дозе 300 мг прогестерона перорально.[59][60]
Когда прогестерон перорально принимают во время еды, а не натощак, пиковые и общие уровни прогестерона значительно выше.[61][11][7] Исследование с использованием ЖХ-МС / МС показало, что при пероральном приеме 100 мг прогестерона в течение 30 минут после начала приема пищи с высоким содержанием жиров пиковые уровни прогестерона были в 2,6 раза выше и площадь под кривой уровни были в 1,8 раза выше по сравнению с приемом натощак.[61] В другом исследовании пиковые уровни прогестерона были увеличены в 5 раз, а уровни площади под кривой - в 2 раза, когда 200 мг прогестерона перорально принимались с пищей.[11] Однако в этом исследовании использовался ненадежный метод ИА для количественного определения уровня прогестерона.[11] Хотя биодоступность прогестерона при пероральном приеме увеличивается, если его принимать с пищей, его общая биодоступность все еще низкая, даже если измерять с использованием ИА.[17] Было высказано предположение, что улучшение уровня прогестерона при пероральном приеме прогестерона с пищей может быть связано с усилением лимфатической абсорбции, что позволяет пероральному прогестерону частично обходить метаболизм первого прохождения.[11][45][53][54]
Устранение и продолжительность
Уровни прогестерона при пероральном приеме прогестерона были определены ненадежным методом ИА и оставались повышенными в течение 12–24 часов.[1][40] Независимо от метода анализа пиковые уровни прогестерона после перорального приема прогестерона возникают примерно через 1–3 часа.[43] В период полувыведения прогестерона в обращение очень короткое в диапазоне от 3 до 90 минут.[13] Предыдущие исследования с использованием ИА сообщили о завышенном периоде полувыведения прогестерона при пероральном приеме, составляющем от 16 до 18 часов.[40] Последующее надежное исследование с использованием высокоэффективная жидкостная хроматография –тандемная масс-спектрометрия (ВЭЖХ – МС / МС) сообщил, что период полувыведения прогестерона орально при приеме с пищей составляет от 4,6 до 5,2 часа.[7] Из-за короткого периода полураспада и продолжительность действия перорального прогестерона его можно принимать в разделенных дозах два или три раза в день.[40][62][63]
Эффект первого прохождения и нейростероиды

Прогестерон метаболизируется в аллопрегнанолон и прегнанолон, которые являются нейростероидами и мощными потенциаторами ГАМКА рецептор.[65][66] Превращение прогестерона в эти метаболиты катализированный посредством ферменты 5α- и 5β-редуктаза и 3α-гидроксистероид дегидрогеназа, и встречается в основном в печень, но также встречается в репродуктивный эндокринный ткани, то кожа, то мозг, и другие ткани.[67] Из-за обширного метаболизм первого прохождения при пероральном приеме прогестерона от 80 до 90% или более прогестерона быстро превращается в эти метаболиты, в результате чего образуются огромные количества этих нейростероидов, которые циркулируют по телу и мозгу.[68][69][70][71] Именно по этой причине обычно сообщается побочные эффекты перорального прогестерона включают головокружение, сонливость, седация, сонливость, и усталость.[65][66] Эти седативные эффекты могут вызывать как пероральные, так и достаточно высокие внутримышечные дозы прогестерона.[72][73][74] Однако, по сравнению с пероральным прогестероном, уровни этих нейростероидов оказались очень низкими при парентеральном введении, например, при вагинальном и внутримышечном введении прогестерона.[64][75] Как и в случае с биодоступностью прогестерона при пероральном приеме, существует высокая индивидуальная вариабельность образования и уровней аллопрегнанолона и прегнанолона при приеме прогестерона перорально.[16] В результате некоторые люди могут испытывать значительные центральный депрессант эффекты прогестерона перорально, тогда как другие могут испытывать минимальные такие эффекты.[16]
При пероральном приеме прогестерона аллопрегнанолон и прегнанолон циркулируют в более высоких концентрациях, чем прогестерон.[16][64] Эти нейростероидные метаболиты прогестерона имеют относительно короткие биологический период полураспада в обращение.[76][77] Из-за этого наблюдаются резкие и в высшей степени супрафизиологические всплески концентраций аллопрегнанолона и прегнанолона, за которыми следует резкое снижение с каждым пероральным приемом прогестерона.[69][70][64] Таким образом, уровни нейростероидов существенно колеблются (например, в 15 раз в случае аллопрегнанолона) и нефизиологическим образом при пероральной терапии прогестероном.[69][71] Кроме того, потребление пищи с пероральным прогестероном увеличивает его всасывание в 2 раза, и это также может еще больше усилить колебания уровней нейростероидов, особенно если прием пищи с прогестероном не соответствует дозе.[11]
В отличие от перорального приема, парентеральный прогестерон, например, при вагинальном введении, позволяет избежать эффекта первого прохождения и не связан с супрафизиологическими уровнями метаболитов нейростероидов, а также с пиками или заметными колебаниями уровней нейростероидов.[69] Парентеральные пути введения можно использовать вместо перорального, чтобы избежать побочных эффектов, связанных с колебаниями нейростероидов, если они окажутся проблематичными.[71][16] Более низкие дозы прогестерона перорально (например, 100 мг / день) также связаны с относительно сниженным образованием метаболитов нейростероидов и могут также помочь облегчить такие побочные эффекты.[16] В дополнение Ингибитор 5α-редуктазы дутастерид, который блокирует выработку аллопрегнанолона (но не прегнанолона) из прогестерона, как было обнаружено, уменьшает симптомы предменструального синдрома.[78]
Прегненолон, без рецепта дополнение и близко аналог прогестерона, при пероральном приеме так же, как и прогестерон, при пероральном применении широко превращается в нейростероиды, такие как аллопрегнанолон и прегнанолон.[79][80][81][82] И наоборот, этого не наблюдалось с трансдермальное введение прегненолона.[82]
Клиническая прогестагенная активность и эффекты
Из-за исследований, в которых использовалась ИА, в течение многих лет ошибочно считалось, что пероральный прогестерон может легко достичь уровней прогестерона в лютеиновой фазе или выше и может вызывать значительные прогестагенные эффекты.[42][43][44] На самом деле, очень низкие уровни прогестерона при пероральном приеме, измеренные с помощью надежных методов, таких как ЖХ-МС, кажутся недостаточными для устойчивых прогестагенных эффектов.[44][1] Об этом свидетельствует тот факт, что, в отличие от почти всех прогестинов, повышенный риск рак эндометрия Наблюдается, когда пероральный прогестерон сочетается с эстрогеном при менопаузальной гормональной терапии.[44][1] Это открытие предполагает, что типичных клинических доз прогестерона перорально может быть недостаточно для полной защиты эндометрия.[44][1] Однако, несмотря на очень низкие достигнутые уровни прогестерона, типичные клинические дозы прогестерона перорально эффективны для предотвращения эстроген-индуцированного гиперплазия эндометрия.[42][43] С другой стороны, пероральный прогестерон не вызывает полной секреторной трансформации эндометрия и считается неприемлемым для использования в вспомогательная репродукция, тогда как вагинальный и внутримышечный прогестерон эффективны.[83][68] Даже 600 мг прогестерона перорально в день, что является очень высокой дозой, не вызывает полных изменений эндометрия в лютеиновой фазе.[71] хотя, как сообщается, пероральные дозы прогестерона от 300 до 600 мг / день использовались для лютеиновая поддержка при вспомогательной репродукции.[68] Исследование того, есть ли у перорального немикронизированного прогестерона термогенный Эффект показал противоречивые результаты в различных исследованиях.[84]
Низкий уровень прогестерона при пероральном приеме прогестерона также может объяснить различия в риске рак молочной железы и Венозная тромбоэмболия относительно прогестагенов при добавлении к терапии эстрогенами у женщин в постменопаузе.[44] Такие риски увеличиваются прогестинами, которые, как и прогестерон, являются агонистами PR, но было обнаружено, что прогестерон перорально увеличивает их меньше или совсем не увеличивает.[43][44] Поскольку типичные клинические дозы прогестерона перорально достигают очень низких уровней прогестерона, а терапия прогестероном с уровнями прогестерона лютеиновой фазы никогда должным образом не оценивалась в достаточно крупных клинических исследованиях, было сказано, что представление о том, что прогестерон каким-то образом отличается от прогестинов и не увеличивает риск рака груди или венозной тромбоэмболии не подтвержден.[43][44][57] Более того, при отсутствии адекватных данных об обратном, было бы разумно рассматривать прогестерон, по крайней мере, эквивалентный прогестинам, как потенциальный фактор риска таких осложнений.[43][44][57] Действительно, доклинические исследования предлагает канцерогенный роль прогестерона в грудь,[85] а французское исследование E3N выявило значительно более высокий риск рака груди при терапии эстрогеном и пероральным прогестероном у женщин в постменопаузе после длительного (> 5 лет) приема.[43][44] Это потенциально соответствует слабому пролиферативный воздействие прогестерона перорально на грудь, так что для увеличения риска рака груди может потребоваться более длительное воздействие.[43][44]
Состав с замедленным высвобождением
А с замедленным выпуском планшет состав микронизированного прогестерона для перорального применения (также известный как «пероральный натуральный микронизированный прогестерон с замедленным высвобождением» или «пероральный NMP SR») продается в Индия под торговыми марками Dubagest SR, Gestofit SR и Susten SR среди других.[86][87][88][89][90][91][92][93][94] Он показывает медленный и плавный профиль высвобождения прогестерона в течение 24 часов и имеет период полувыведения 18 часов.[86][93] Это приводит к более стабильному и устойчивому уровню прогестерона, а также к минимизации связанных с нейростероидами побочных эффектов перорального прогестерона, таких как седативный эффект.[86][93]
Буккальное управление
Прогестерон был изучен для использования буккальное введение.[16][95][96][97][98][99][100] Препарат продается в форме буккального таблетки под торговыми марками Progesterone Lingusorbs, Lutocylol, Membrettes и Syngestrets.[101][102] Клиническая дозировка буккального прогестерона составляет от 10 до 50 мг / день по сравнению с 5-60 мг / день в случае внутримышечная инъекция.[101]
Сублингвальное введение
Состав микронизированных таблеток прогестерона, продаваемых под торговой маркой Luteina, рекомендован для использования сублингвальное введение в дополнение к вагинальному введению и одобрен для использования в Польша и Украина.[105] Он используется сублингвально в дозировках от 50 до 150 мг три-четыре раза в день.[105][8] Было обнаружено, что однократная сублингвальная доза лютеина в дозе 100 мг достигает средних пиковых уровней прогестерона 13,5 нг / мл через 1–4 часа с периодом полувыведения примерно от 6 до 7 часов.[105][8]
В ряде других исследований также изучалось использование прогестерона сублингвальное введение.[106][107][108][104] В более ранних исследованиях также изучались сублингвальные приемы прогестерона.[109][110][111][112] Исследование сублингвального прогестерона для лютеиновая поддержка у пациентов, проходящих перенос эмбриона обнаружили, что после сублингвального введения 50 или 100 мг прогестерона, растворенного в суспензии 1 мл, пиковые уровни прогестерона были достигнуты через 30-60 минут и составили в среднем 17,61 ± 3,78 нг / мл при дозе 100 мг.[106][107] Однако продолжительность был коротким, с уровнями менее 5 нг / мл через 6 часов, и повторное введение нужно было проводить два или три раза в день для поддержания адекватных уровней прогестерона в кровотоке в течение дня.[106][107] Другое исследование показало, что прогестерон необходимо вводить сублингвально в дозе 400 мг каждые 8 часов, чтобы достичь уровней циркуляции, аналогичных тем, которые вырабатываются при внутримышечном введении 100 мг / день прогестерона.[106] Одно исследование вводило 400 мг прогестерона сублингвально три раза в день и достигло средних уровней прогестерона 57,8 ± 37,4 нг / мл, которые были аналогичны уровням прогестерона в дозе 50 мг / день внутримышечно.[107]
Интраназальное введение
Прогестерон был оценен интраназальный маршрут, в виде назальный спрей, в одном исследовании.[106][16][113][114] Уровень прогестерона был низким и недостаточным с точки зрения изменений эндометрия.[71]
Трансдермальное введение
Прогестерон для трансдермальное введение не одобрен FDA в США.[115][116][57] Множественный Фармацевтические компании занимались разработкой системных трансдермальных препаратов прогестерона, но в конечном итоге ни один из них не был успешно разработан и внедрен для клинического использования.[117] Несмотря на то, что ни один из составов трансдермального прогестерона не одобрен для системного использования, 1% гелевый состав прогестерона для местного применения для местного применения на грудь одобрен для лечения боль в груди под торговой маркой Progestogel в разных странах.[118][47][119]
Хотя ни один из составов трансдермального прогестерона не одобрен для системного применения, трансдермальный прогестерон доступен в форме кремы и гели из обычай рецептура аптек в некоторых странах, а также доступно без рецепта без рецепт В Соединенных Штатах.[115][116][57] Трансдермальный прогестерон использовался тысячами женщин в качестве компонента гормональной терапии в период менопаузы в США и Европе.[115] Однако эти продукты не регулируются и не клинически протестирован, зачастую об их фармакокинетике мало что известно.[115] В дополнение поглощение трансдермального прогестерона может значительно отличаться от препарата к препарату из-за широкого разнообразия ингредиентов.[116] Более того, системная эффективность трансдермального прогестерона в отношении терапевтического прогестагенного действия, наиболее важно адекватная эндометрий защита от эстрогены, является спорным.[115][116]
Некоторые нерегулируемые трансдермальные препараты прогестерона содержат «экстракт дикого ямса», полученный из Dioscorea villosa, но нет никаких доказательств того, что человеческий организм может преобразовывать свой активный ингредиент (диосгенин, растительный стероид, который химически превращается в промышленное производство прогестерона)[120] в прогестерон.[121][122]
Поглощение и распределение

Кожа проницаемость соединения основано на его физико-химический свойства, особенно липофильность и гидрофильность.[16][123] В общем, чем больше полярный группы, например гидроксильные группы, которые присутствуют в стероиде, и, следовательно, чем он более гидрофильный и менее липофильный, тем ниже проницаемость для кожи.[16][123] По этой причине прогестерон и эстрон имеют более высокую проницаемость кожи, эстрадиол имеет умеренную проницаемость кожи, и эстриол и кортизол имеют меньшую проницаемость кожи.[16] Трансдермальный биодоступность прогестерона применяется к грудь составляет примерно 10%.[117][124][125][126] Это примерно то же самое, что и при общей трансдермальной абсорбции эстрадиола и тестостерона, хотя применяется к другим участкам кожи.[117][127][128][129] Место нанесения трансдермального прогестерона может влиять на его абсорбцию.[116] В исследовании наблюдалось значительное увеличение циркулирующих уровней прогестерона вскоре после приема, когда он применялся как трансдермальный. мазь на грудь, но не на другие области, такие как бедро или брюшная полость.[116]
В то время как эстрадиол циркулирует на уровнях в пикомолярный диапазон (пг / мл), прогестерон циркулирует в концентрациях в наномолярный диапазон (нг / мл), и для получения этих уровней требуется относительно большая доза.[130][71] В лютеиновой фазе организм синтезирует в среднем около 25 мг прогестерона в день.[17][106][71] Было заявлено, что это относительно большое количество по массе требует, чтобы около 50% тела использовалось в качестве поверхности для абсорбции для доставки аналогичного количества прогестерона на основе его механики абсорбции.[17][106] Таким образом, трансдермальный путь не может легко достичь адекватных уровней циркулирующего прогестерона, и это делает трансдермальный прогестерон непрактичным для системной терапии.[17][106][130][71] Клинические исследования показали только очень низкие уровни циркулирующего прогестерона при использовании трансдермального прогестерона, и эти уровни считаются недостаточными для обеспечения защиты эндометрия от эстрогенов.[115][116] Диапазон циркулирующих уровней прогестерона, который наблюдался в клинических исследованиях с различными формами и дозами трансдермального прогестерона, составляет от 0,38 до 3,5 нг / мл.[47][115]
Хотя очень низкие уровни прогестерона наблюдались в венозной крови с трансдермальным прогестероном, очень высокие и на самом деле очень высокие. супрафизиологический уровни прогестерона неожиданно были обнаружены в слюна и капиллярная кровь.[115][116][131] В одном исследовании уровни прогестерона в слюне и капиллярной крови были в 10 и 100 раз выше, чем уровни в венозной крови, соответственно.[115][116][131] Наблюдаемые уровни прогестерона в слюне колеблются от 2,9 до 2840 нг / мл.[47] Высокие уровни прогестерона в слюне и капиллярной крови предполагают, что, несмотря на низкие уровни прогестерона в крови, системное распределение прогестерона и значительное воздействие этого гормона на некоторые ткани могут каким-то образом происходить с трансдермальным прогестероном.[115][116][131] Однако несколько клинических исследований, в которых оценивалось влияние трансдермального прогестерона на эндометрий, дали неоднозначные результаты, и необходимы дальнейшие исследования, чтобы определить, может ли он обеспечить адекватную защиту эндометрия в качестве компонента гормональной терапии менопаузы.[115][116]
Трансдермальный прогестерон обычно поставляется в форме кремов и гелей на водной основе, и исследования, в которых наблюдались очень низкие уровни прогестерона в циркуляции с трансдермальным прогестероном, использовали эти составы.[115][116] Одно исследование трансдермального прогестерона 100 мг / день в форме алкоголь гель на основе геля обнаружил относительно высокие концентрации прогестерона в кровотоке, что соответствовало лютеиновой фазы уровни.[115][116] В пиковые уровни прогестерона составляли 8 нг / мл и теоретически были достаточными для защиты эндометрия.[115][116] Эти результаты, хотя и основаны на единственном исследовании, предполагают, что гели с прогестероном на спиртовой основе могут давать относительно высокие уровни циркулирующего прогестерона.[115][116] Одно из возможных объяснений разницы в том, что кремы с прогестероном более эффективны. липофильный и может иметь предпочтение в отношении поглощения жирный слой под кожей.[116] И наоборот, гели на спиртовой основе более вода и может быстро распространиться в микроциркуляция кожи, а затем в общий кровоток.[116] Однако в другом исследовании, в котором изучалась фармакокинетика трансдермального прогестерона с использованием либо гидрофильный -, липофильный -, или эмульсия -типа базы было установлено, что во всех трех случаях время до пиковых концентраций было около 4 часов, и венозная кровь наблюдаемые уровни были очень низкими.[10]
Высокий уровень в слюне и капиллярной крови
На основании очень низких уровней прогестерона, наблюдаемых в венозной крови с трансдермальным прогестероном, некоторые исследователи пришли к выводу, что трансдермальный прогестерон плохо всасывается и не обеспечивает адекватную защиту эндометрия.[131][116] Однако, несмотря на очень низкий уровень прогестерона в кровотоке, исследования, в которых измеряли уровень прогестерона в слюна и / или капиллярная кровь с трансдермальным прогестероном обнаружили, что они значительно повышены и на самом деле значительно супрафизиологический.[115][116][131] В одном исследовании, в котором использовался масло в креме или геле на водной основе, уровни прогестерона в слюне и капиллярной крови из кончиков пальцев были примерно в 10 и 100 раз выше, чем уровни в венозной крови, соответственно.[115][131] Точные уровни прогестерона составляли от 4 до 12 нг / мл в слюне и от 62 до 96 нг / мл в капиллярной крови; то эталонные диапазоны прогестерона в слюне и капиллярной крови из указанной лаборатории составляли от 0,75 до 2,5 нг / мл и от 3,3 до 22,5 нг / мл для женщин в пременопаузе в лютеиновой фазы и от 0,12 до 1,0 нг / мл и от 0,1 до 0,8 нг / мл у женщин в постменопаузе, соответственно.[115][131] Таким образом, эти данные подтверждают распространение прогестерона по крайней мере до определенного ткани с трансдермальным прогестероном, несмотря на очень низкие уровни прогестерона в кровотоке, и указывают на то, что уровни прогестерона в венозной крови не обязательно могут использоваться в качестве показателя воздействия прогестерона на ткани при этом пути введения.[115][116] Эти результаты дают возможное объяснение того, как некоторые исследования обнаружили антипролиферативные и атрофические изменения в эндометрии с трансдермальным прогестероном.[131][116] Однако повышение уровня прогестерона в эндометрии при трансдермальном прогестероне еще предстоит продемонстрировать.[116]
В отношении трансдермального прогестерона высказывалась озабоченность в связи с тем, что эффекты таких супрафизиологических уровней прогестерона в тканях неизвестны, и, следовательно, не исключена возможность побочных эффектов.[115] Слюна мониторинг Уровни прогестерона у женщин, принимающих трансдермальный прогестерон, и корректировка дозировки по мере необходимости были предложены в качестве возможных средств предотвращения потенциальных побочных эффектов.[115]
Механизм, с помощью которого трансдермальный прогестерон в креме и геле на водной основе производит очень высокие уровни в слюнной и капиллярной крови, несмотря на низкие уровни циркулирующей крови, недостаточно изучен.[115] Однако было предложено как минимум две гипотезы.[116][132] Стероидные гормоны в том числе прогестерон переносится красные кровяные клетки в дополнение к сыворотка белки-носители любить альбумин, глобулин, связывающий половые гормоны, и кортикостероид-связывающий глобулин, и от 15 до 35% общего содержания стероидных гормонов в цельной крови может быть ограничено эритроцитами.[116] Согласно этой гипотезе, очень высокие локальные концентрации прогестерона возникают в капиллярах кожи после трансдермального применения и поглощаются эритроцитами.[116] Время прохождения эритроцитов из капилляров и высвобождение стероидных гормонов из красных кровяных телец очень быстрое, поэтому предполагается, что прогестерон доставляется через циркуляцию к тканям через красные кровяные тельца, не успевая уравновеситься с системной кровью.[116] Это потенциально может объяснить низкие уровни прогестерона в венозной крови, несмотря на очень высокие уровни в капиллярной крови и слюне.[116] Однако в одном исследовании оценивали уровни прогестерона в красных кровяных тельцах с трансдермальным прогестероном и обнаружили, что они были значительно повышены, но все еще очень низки.[116] Тем не менее, по мнению других авторов, «[а] хотя исследователи этого исследования пришли к выводу, что уровни прогестерона в эритроцитах были слишком низкими, чтобы играть важную роль в доставке прогестерона к тканям-мишеням, следует понимать, что даже небольшие количества прогестерон, поглощаемый эритроцитами, может иметь важное значение, поскольку время прохождения эритроцитов из капилляров очень короткое. [...] Однако роль эритроцитов в транспорте стероидных гормонов тщательно не изучена, и такие исследования гарантированы ".[116]
An in vitro учиться с использованием свинья кожа и несколько составов трансдермального прогестерона обнаружили, что через кожу проникают лишь незначительные количества прогестерона, но наблюдается значительное распределение прогестерона в тканях кожи.[132] По словам исследователей, результаты показали, что лимфатическая циркуляция в коже может быть причиной системного распределения трансдермального прогестерона.[132]
Метаболизм и устранение
5α-редуктаза является основным фермент участвует в метаболизм прогестерона и, как известно, в больших количествах экспрессируется в коже.[133][116] По этой причине было высказано предположение, что быстрый метаболизм прогестерона 5α-редуктазой может объяснить низкие уровни циркулирующего прогестерона, продуцируемого трансдермальным введением.[116] Исследования прогестерона показали, что при трансдермальном введении прогестерона 80% метаболизируется в коже и только 20% могут пройти через кожный барьер.[134][135] В этом направлении исследование радиоактивно меченый прогестерон обнаружил, что 5β-восстановленный прегнандиол экскреция была в 8 раз выше, чем 5α-восстановленная аллопрегнандиол выделение с внутривенный прогестерон, однако экскреция аллопрегнандиола была немного выше, чем экскреция прегнандиола с трансдермальным прогестероном.[136] Метаболиты прогестерона в коже не обладают гормональной активностью.[134] Помимо 5α-редуктазы, другие ферменты, такие как 20α-гидроксистероид дегидрогеназа, метаболизируют прогестерон в коже.[133] Прогестерон и / или его метаболиты, такие как 5α-дигидропрогестерон вести себя как Ингибиторы 5α-редуктазы и ингибиторы из 3α- и 3β-гидроксистероид дегидрогеназы в коже.[133]
С другой стороны, другие исследования поставили под сомнение идею о том, что прогестерон активно метаболизируется в коже.[116] Одно исследование показало, что трансдермальный прогестерон в геле на спиртовой основе продуцирует высокий уровень циркулирующего прогестерона.[116] Это предполагает, что состав, а не метаболизм, может быть решающим ограничивающим фактором биодоступности трансдермального прогестерона.[116] Оценка исследования мочевой уровни прегнандиол глюкуронид, основного метаболита прогестерона в моче, и обнаружили, что, хотя уровни циркулирующего прогестерона и уровни глюкуронида прегнандиола в моче увеличивались после лечения трансдермальным прогестероном, уровни обоих, тем не менее, оставались в диапазоне фолликулярная фаза и, следовательно, были очень низкими.[116] А история болезни обнаружил, что Ингибитор 5α-редуктазы финастерид не увеличивал уровни циркулирующего прогестерона или уровни глюкуронида прегнандиола в моче, продуцируемого трансдермальным прогестероном.[116] Аналогичным образом, исследование показало, что ингибитор 5α-редуктазы дутастерид в результате трансдермального прогестерона лишь немного повысился уровень прогестерона.[137][138][139][47] Наконец, 5α-редуктаза также является основным ферментом, участвующим в метаболизме тестостерон, но трансдермальный тестостерон одобрен для заместительная андрогенная терапия и очень эффективен в повышении уровня тестостерона.[140]
С точки зрения устранение, исследование, в котором изучалась фармакокинетика трансдермального прогестерона с использованием либо гидрофильный -, липофильный -, или эмульсия -типа основания обнаружил, что во всех трех случаях период полувыведения находился в диапазоне от 30 до 40 часов.[10]
Системная клиническая эффективность
По крайней мере, семь исследований оценивали трансдермальный прогестерон.[115][116] В этих исследованиях использовались различные составы трансдермального прогестерона, включая кремы и гели на водной основе (торговые марки Pro-Gest, Progestelle и Pro-Femme, а также составные части), с разными размеры выборки (от n = 6 до n = 40), при разных дозировки (От 15 до 80 мг в день) и для различной продолжительности лечения (от 1,4 до 24 недель).[115][116] Венозная кровь Уровни прогестерона оценивались и сообщались в пяти исследованиях, и во всех случаях были низкими и не превышали 3,5 нг / мл.[115][116] Принято считать, что уровни прогестерона 5 нг / мл необходимы для подавления митоз и побудить секреторные изменения в эндометрии,[115] хотя некоторые исследователи оспаривают это утверждение.[116] Влияние трансдермального прогестерона на эндометрий оценивалось в трех исследованиях через эндометрий. биопсия и результаты были неоднозначными.[115][116] В одном исследовании эффекта не было; в другой, антипролиферативный наблюдались эффекты; и в последнем исследовании атрофический состояние наблюдалось, но только у 28 из 40 (70%) женщин.[115][116] Уровни циркулирующего прогестерона были ниже 3,5 нг / мл в первом исследовании, низкие и широко варьирующие во втором исследовании, и не были указаны в третьем исследовании.[115][116] Более того, продолжительность исследования, в котором не наблюдалось никакого эффекта, была короткой - всего 2 недели, а для изменения эндометрия необходим более длительный период лечения от 4 до 6 недель.[115][116] Также было высказано предположение, что используемая доза эстрогена могла быть недостаточной, чтобы обеспечить надлежащую подготовку эндометрия к действию прогестерона.[116] Вместе взятые, необходимы дальнейшие исследования, чтобы адекватно установить защитный эффект трансдермального прогестерона на эндометрий.[115]
Местное нанесение на грудь
Трансдермальное применение прогестерона с целью системной терапии не следует приравнивать к местному лечению.[47] Было обнаружено, что место нанесения трансдермального прогестерона значительно влияет на его поглощение.[116] Когда трансдермальный прогестерон наносится на грудь наблюдались высокие концентрации в тканях груди.[117] В одном исследовании наблюдалось 3-5-кратное увеличение локальных уровней прогестерона в груди при применении 50 мг трансдермального прогестерона в геле на спиртовой / водной основе, нанесенного на каждую грудь у женщин в пременопаузе.[117][124][141] В другом исследовании при нанесении водно-спиртового геля на грудь у женщин в пременопаузе было измерено увеличение локальной концентрации прогестерона в груди в 70–110 раз.[142][143] В исследовании наблюдалось значительное увеличение циркулирующих уровней прогестерона при его применении в качестве местного средства. мазь на грудь, но не тогда, когда его наносили на другие области, такие как бедро или брюшная полость.[116] Однако в двух других исследованиях не было обнаружено явного увеличения циркулирующих уровней прогестерона при трансдермальном нанесении прогестерона на грудь.[142][124] На основании его 10% трансдермальной биодоступности при нанесении на грудь, доза прогестерона 50 мг, применяемая трансдермально, может привести к локальной концентрации прогестерона в груди, эквивалентной 5 мг.[117][141]
Хотя трансдермальный прогестерон не одобрен для использования в гормональной терапии менопаузы или в качестве системного лекарства, он зарегистрирован в некоторых странах под торговой маркой Progestogel в виде 1% геля (10 мг / г) для прямого местного применения в грудь лечить предменструальный боль в груди.[118][47][126] В клинических исследованиях было обнаружено, что лекарство ингибирует эстроген-индуцированный распространение груди эпителиальные клетки, чтобы быть высокоэффективным при лечении доброкачественная болезнь груди, чтобы значительно уменьшить грудь узловатость, и почти полностью облегчить боль и нежность груди у женщин с этим заболеванием.[47][117][124][126] Напротив, трансдермальный прогестерон оказался почти полностью неэффективным при фиброзно-кистозная болезнь груди, кисты груди, и фиброаденомы груди, в то время как оральные прогестины оказались значительно эффективными.[117] Эффективность прогестерона и других прогестагенов при лечении заболевания груди может быть связано с их функциональностью антиэстрогенный эффекты в груди.[117][124]
Вагинальное введение

Прогестерон доступен для вагинальное введение в виде капсулы (Утрожестан), гели (Crinone, Prochieve), суппозитории (Циклогест), вставки /таблетки (Эндометрин, Lutinus) и кольца (Фертиринг, Прогеринг).[145][146][147] Кроме того, пероральные микронизированные капсулы с прогестероном успешно применялись вагинально.[148]
В биодоступность вагинального микронизированного прогестерона составляет от 4 до 8%.[2][3][4] Вагинальная абсорбция прогестерона ниже у женщин в постменопаузе с вагинальная атрофия.[144] Биодоступность вагинального прогестерона примерно в 40 раз выше, чем у перорального прогестерона.[149][1] После введения одного вагинального суппозитория с прогестероном 25, 50 или 100 мг женщинам максимальные уровни прогестерона в кровотоке наблюдались в течение 2-3 часов и составили 7,27 ± 2,8 нг / мл, 8,84 ± 3,14 нг / мл и 9,82 ± 9,8 нг. / мл соответственно.[144] После пикового уровня уровень прогестерона постепенно снижался с период полувыведения от 6 до 12 часов.[144] Уровни прогестерона были менее 3 нг / мл для всех трех доз через 24 часа.[144] Исследователи пришли к выводу, что дозы 25 и 50 мг будут подходящими для приема дважды в день, а доза 100 мг будет подходящей для приема три раза в день.[144]
Существует эффект первого прохождения через матку с вагинальным прогестероном, так что уровни прогестерона намного выше в матка чем в тираже.[47] Полная секреторная трансформация эндометрия вызывалась вагинальным введением прогестерона, что приводило к уровню циркулирующего прогестерона от 1 до 3 нг / мл, тогда как другие парентеральные пути (внутримышечный и интраназальный) были менее эффективными по сравнению с этим.[144] Разница может быть связана с эффектом первого прохождения эндометрия вагинальным прогестероном.[144]
Ректальное введение

Прогестерон можно принимать ректальное введение.[150][17][21] А суппозиторий продаваемый под торговой маркой Cyclogest, показан для ректального применения в дополнение к вагинальному введению.[32][151][152] Ежедневное ректальное введение прогестерона неудобно и плохо подходит для длительной терапии.[46][150] Тем не менее, ректальный прогестерон может быть полезной альтернативой вагинальному введению в контексте вагинальная инфекция, цистит, недавний роды, или когда барьерная контрацепция используются методы.[150]
В ряде исследований оценивали прогестерон ректальным путем.[153][154][155][156][157][113][158][159] Было обнаружено, что уровни прогестерона после ректального введения составляют 6,4 нг / мл после приема одного суппозитория 25 мг, 22,5 нг / мл после приема одного суппозитория 100 мг и 20,0 нг / мл после приема одного суппозитория 200 мг.нужна цитата] Абсорбция ректального пути варьирует, с широким диапазоном максимальных концентраций прогестерона от 15 до 52 нг / мл после однократного ректального введения прогестерона в дозе 100 мг.[17][155] Уровень прогестерона достигает максимума через 6-8 часов, а затем постепенно снижается.[17][150] В нескольких исследованиях было обнаружено, что уровни прогестерона схожи и незначительно отличаются после введения ректальных и вагинальных суппозиториев.[150]
Прогестерон попадает прямо в кровоток, когда он всасывается нижней частью прямая кишка и транспортируется низший и средние ректальные вены.[17] И наоборот, если он всасывается в верхней части прямой кишки, прогестерон подвергается печеночному метаболизм первого прохождения в связи с вступлением в печеночная портальная система через верхняя ректальная вена.[17] Таким образом, хотя ректальное введение является парентеральный путь, он все еще может подвергаться некоторому метаболизму первого прохождения, подобно пероральному прогестерону.[17]
Внутримышечная инъекция
| Соединение | Форма | Доза для конкретного использования (мг)[c] | DOA[d] | |||
|---|---|---|---|---|---|---|
| TFD[e] | POICD[f] | CICD[г] | ||||
| Алгестон ацетофенид | Масло солн. | - | – | 75–150 | 14–32 дней | |
| Гестонорон капроат | Масло солн. | 25–50 | – | – | 8–13 дней | |
| Гидроксипрогест. ацетат[час] | Aq. Susp. | 350 | – | – | 9–16 дней | |
| Гидроксипрогест. капроат | Масло солн. | 250–500[я] | – | 250–500 | 5–21 дн. | |
| Medroxyprog. ацетат | Aq. Susp. | 50–100 | 150 | 25 | 14–50 + д | |
| Мегестрола ацетат | Aq. Susp. | - | – | 25 | > 14 дней | |
| Норэтистерона энантат | Масло солн. | 100–200 | 200 | 50 | 11–52 дня | |
| Прогестерон | Масло солн. | 200[я] | – | – | 2–6 дней | |
| Aq. soln. | ? | – | – | 1–2 дня | ||
| Aq. Susp. | 50–200 | – | – | 7–14 дней | ||
Примечания и источники:
| ||||||
Масляные растворы
Когда используется внутримышечная инъекция прогестерон обходит метаболизм первого прохождения в кишечнике и печени и обеспечивает очень высокий уровень циркулирующего прогестерона.[16][47] Уровни прогестерона при внутримышечном введении 100 мг / день прогестерона были значительно выше, чем при вагинальном прогестероне 800 мг / день (около 70 нг / мл и 12 нг / мл соответственно), хотя локальные уровни прогестерона в матка были в 10 раз выше при вагинальном введении из-за эффекта первого прохождения через матку (около 1,5 нг / мл и почти 12 нг / мл соответственно).[47] Продолжительность приема прогестерона увеличивается при внутримышечном введении из-за депо эффект, в котором он хранится локально в жировая ткань и можно вводить один раз в 1-3 дня.[17] Период полувыведения внутримышечного прогестерона значительно увеличивается, когда он вводится в организм. ягодичные мышцы из ягодицы а не дельтовидная мышца из плечо.[17] Внутримышечный прогестерон традиционно был самой популярной формой прогестерона, используемой для лютеиновая поддержка в вспомогательная репродукция в Соединенные Штаты, хотя прогестерон вагинальный также используется и эффективен.[47][17]
При внутримышечном введении 10 мг прогестерона в растительном масле максимальные концентрации в плазме (CМаксимум ) достигаются примерно через 8 часов после приема, а уровни в сыворотке остаются выше исходного уровня в течение примерно 24 часов.[41] Было обнаружено, что дозы 10, 25 и 50 мг при внутримышечной инъекции дают средние максимальные концентрации 7, 28 и 50 нг / мл, соответственно.[41] При внутримышечной инъекции доза 25 мг обеспечивает нормальный уровень прогестерона в сыворотке лютеиновой фазы в течение 8 часов, а доза 100 мг обеспечивает максимальный уровень в середине беременности от 40 до 80 нг / мл.[21] В этих дозах уровни прогестерона остаются повышенными по сравнению с исходным уровнем в течение как минимум 48 часов (6 нг / мл на данном этапе для 100 мг),[21] с периодом полувыведения около 22 часов.[12]
Вследствие достижения высоких концентраций прогестерон при внутримышечной инъекции в обычном клиническом диапазоне доз способен подавлять гонадотропин секреция из гипофиз, демонстрируя антигонадотропный эффективность (и, следовательно, подавление выработки половых стероидов гонадными железами).[41]
Внутримышечный прогестерон часто вызывает боль при введении.[17] Это раздражает ткани и связан с реакции в месте инъекции например, изменение цвета кожи, боль, покраснение, временный уплотнения (из-за воспаление ), экхимоз (синяки / обесцвечивание) и другие.[180][17] Редко, стерильные абсцессы может случиться.[17] Большие дозы прогестерона для внутримышечной инъекции, например 100 мг, вызывают реакции в месте инъекции от умеренной до тяжелой.[181]
Водные суспензии
Было обнаружено, что прогестерон действует значительно дольше. продолжительность действия от внутримышечная инъекция при введении в виде микрокристаллический водная суспензия (размер кристаллов 0,02–0,1 мм), чем как масляный раствор.[182][183][184][185][186] В то время как однократная внутримышечная инъекция от 25 до 350 мг прогестерона в масляном растворе имеет продолжительность от 2 до 6 дней с точки зрения клинических проявлений. биологический эффект в матка У женщин однократная внутримышечная инъекция от 50 до 300 мг микрокристаллического прогестерона в водной суспензии имеет продолжительность от 7 до 14 дней.[166][163][160] В результате внутримышечный прогестерон в масляном растворе вводится один раз каждые 1-3 дня в типичных клинических дозах.[17] тогда как внутримышечный микрокристаллический прогестерон в водной суспензии можно вводить один раз в неделю или даже с более длительными интервалами.[166][160][187] Продолжительность микрокристаллических водных суспензий зависит как от концентрации лекарственного средства, так и от размер кристалла.[188][189][190][191] Более крупный размер иглы необходим для водных суспензий стероидов, чтобы позволить кристаллам проходить через просвет иглы.[192] Сообщалось, что игла калибра 20 или 21 подходит для инъекции водных суспензий микрокристаллического прогестерона.[193]
Композиции микрокристаллического прогестерона в водной суспензии для длительного использования депо путем внутримышечной инъекции были на рынке в 1950-х годах под различными торговыми марками, включая флаволутан, лютеозан, лютоциклин М и лутрен.[194] Другой препарат - Agolutin Depot, который был представлен к 1960 году и, по всей видимости, продолжает продаваться в Чехия и Словакия сегодня.[195][196][197][185][198] Систоциклин было торговым наименованием продукта, содержащего 10 мг микрокристаллического эстрадиола бензоат и 200 мг микрокристаллического прогестерона в водной суспензии, которая продавалась в 1950-х годах.[199][200][201][202] Сообщалось, что препарат имеет продолжительность действия от 10 до 12 дней с точки зрения прогестагенного компонента по сравнению с продолжительностью действия всего 2 дня для эстрадиолбензоата и прогестерона в масляном растворе.[203][204] К сожалению, внутримышечные инъекции водных суспензий прогестерона и других стероидов болезненны, часто очень болезненны.[205][206][207] В результате они были в значительной степени прекращены в пользу других препаратов, таких как прогестерон в масляном растворе и прогестины длительного действия.[205][168][207]
Прогестерон в водных суспензиях при внутримышечном введении оказывается более сильным с точки зрения прогестагенного действия, чем прогестерон в масляных растворах при внутримышечном введении.[208] В то время как дозы прогестерона 25 мг в виде микрокристаллов были необходимы, чтобы вызвать децидуализация женщинам потребовались дозы от 35 до 50 мг прогестерона в масле.[208] Это было связано с более стабильным и продолжительным уровнем прогестерона в водных суспензиях по сравнению с масляными растворами.[208]
Медроксипрогестерона ацетат (торговые марки Depo-Provera, Depo-SubQ Provera 104), а прогестин и структурная модификация прогестерона с метильная группа в позиции C6α и ацетоксигруппа в положении C17α формулируется в виде микрокристаллической водной суспензии для внутримышечной или подкожной инъекции.[209][210] Как и в случае с прогестероном, прием ацетата медроксипрогестерона таким образом значительно увеличивает его продолжительность.[209][172] Он имеет продолжительность от 16 до 50 дней в дозе 50 мг,[166] в то время как его продолжительность при дозе 150 мг составляет не менее 3 месяцев и от 6 до 9 месяцев.[209][172]
Эмульсии
Вода в масле эмульсии из стероиды изучались в конце 1940-х - 1950-х гг.[190][211][212][213][214][215][216][217] Эмульсии прогестерона пролонгированного действия были введены для внутримышечной инъекции только под торговой маркой Progestin и с эстрадиола бензоат под торговой маркой Di-Pro-Emulsion к 1950-м годам.[194][218][219][220][221] Сообщается, что стероидные эмульсии для внутримышечной инъекции имеют аналогичные свойства, такие как продолжительность действия, как водные суспензии.[190][211][212]
Микросферы
An водная суспензия прогестерона инкапсулированный в микросферы продается для использования внутримышечная инъекция под торговой маркой ProSphere в Мексика.[180][222][223] Его вводят один раз в неделю или один раз в месяц, в зависимости от показаний.[180] Например, лекарство вводят в дозе от 100 до 300 мг внутримышечно один раз в 7 дней для лечения угроза выкидыша.[35] Микросферы имеют размер от 33 до 75 мкг и доставляются с использованием предварительно заполненные шприцы иглой 20 калибра 38 мм.[180] Пик Уровни прогестерона после однократной внутримышечной инъекции 100 или 200 мг ProSphere достигаются примерно через 1,5 дня.[35] В период полувыведения прогестерона с этим составом составляет около 8 дней.[35] Однократная внутримышечная инъекция 200 мг поддерживает уровень прогестерона более 10 нг / мл в течение 5-7 дней.[35] ProSphere хорошо переносится с точки зрения реакции в месте инъекции.[180]
Сочетание обоих эстрадиол и прогестерон, инкапсулированный в микросферы в виде водной суспензии для внутримышечной инъекции, продается под торговой маркой. Ювенум в Мексике.[224][225][226] Опубликованы исследования этой формулировки.[227][228]
Эстрадиол и прогестерон, инкапсулированные в микросферы, были изучены для использования один раз в месяц. комбинированный инъекционный контрацептив но не получил дальнейшего развития и не внедрен для медицинского использования.[229][230][231][232][233][234]
- Уровни гормонов с прогестерон внутримышечно
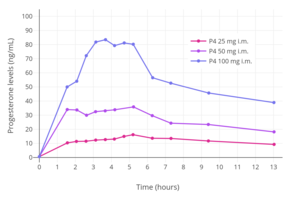
Уровни прогестерона при однократной внутримышечной инъекции 25, 50 или 100 мг прогестерона (P4) в масляном растворе у женщин в постменопаузе.[75]

Уровни прогестерона при однократной внутримышечной инъекции 10, 25, 50 или 100 мг прогестерона в масляном растворе у женщин.[157]
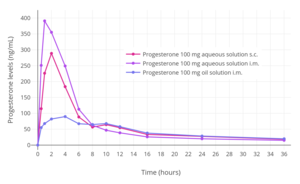
Уровни прогестерона после однократной внутримышечной или подкожной инъекции 100 мг прогестерона в водном растворе (Пролутекс) или масляном растворе (Пронтогест) женщинам в постменопаузе.[12]

Уровни прогестерона после однократной внутримышечной инъекции 25, 50 или 100 мг прогестерона в комплексе с β-циклодекстрин в водном растворе (Пролутекс) у женщин в постменопаузе.[12]
Подкожная инъекция
Прогестерон можно вводить подкожная инъекция вместе с Prolutex, водным раствором прогестерона, продаваемым в Европе, который предназначен для ежедневного введения этим путем.[12][235][236] Этот состав быстро абсорбируется, и было обнаружено, что он приводит к более высоким пиковым уровням прогестерона по сравнению с прогестероном в масляном растворе при внутримышечной инъекции.[236] Кроме того, подкожное введение прогестерона считается более простым, безопасным из-за меньшего риска реакций в месте инъекции и менее болезненным по сравнению с внутримышечным введением прогестерона.[236] Период полувыведения этого состава составляет от 13 до 18 часов.[12] по сравнению с 20–28 часами для внутримышечного введения прогестерона в масляном растворе.[11][9][12]
Подкожная имплантация
Прогестерон ранее продавался в 1950-х и 1960-х годах в форме 50 и 100 мг. подкожные гранулы имплантатов под торговыми марками Флаволутан, Лютеозид, Лутоциклин и Пролутон.[194][237] Однако в отличие от эстрадиол и тестостерон имплантаты, которые сегодня остаются доступными как фармацевтические продукты,[238] Продукты для имплантатов прогестерона были прекращены и, похоже, больше не доступны в фармацевтике.[94] Имплантаты с прогестероном могут быть доступны в некоторых рецептура аптек однако, хотя такие продукты не регулируются по качеству или эффективности.[239][240][241]
Ранние исследования имплантатов прогестерона у людей проводились в 1930-1950-х годах.[242][243][244][245][246][247][248][249] Подкожные имплантаты прогестерона плохо переносятся, с стерильные абсцессы и экструзия встречается от 15 до 20% имплантаций.[250] Имплантаты прогестерона также изучались как форма длительного гормонального контроля над рождаемостью у женщин в 1980-х годах, но в конечном итоге никогда не продавались.[251][252][253][254] Было обнаружено, что имплантация шести гранул, содержащих 100 мг прогестерона каждая (всего 600 мг), приводит к относительно низким средним уровням прогестерона около 3 нг / мл, при этом уровни прогестерона сохраняются в течение пяти месяцев.[252][253][254] Подкожная имплантация прогестерона также изучалась на животных.[255] Подкожные имплантаты гранул наиболее практичны, когда лекарство действует в очень малых дозах.[189]
Хотя имплантаты прогестерона не доступны в виде фармацевтических препаратов, подкожные имплантаты прогестинов, такие как этоногестрел (Импланон / Nexplanon ) и левоноргестрел (Жадель / Норплант ), доступны как фармацевтические продукты.[256][257] Они используются как формы длительного гормональные противозачаточные.[256][257]
Внутриматочное введение
Годовой прогестерон внутриматочная спираль (ВМС) для гормональные противозачаточные ранее был доступен в Соединенные Штаты и несколько других стран под торговой маркой Progestasert.[258][259] Он продавался с 1976 по 2001 год.[258] ВМС никогда не использовались широко из-за относительно высокого процента неудач противозачаточных средств (2,9%) и необходимости ежегодной замены.[258] Он содержал 38 мг прогестерона и высвобождал 65 мкг прогестерона в матка в день (всего около 35 мг через год).[258][259] Для сравнения: организм женщины вырабатывает в среднем около 25 мг прогестерона в день в течение лютеиновой фазы.[17][106] Хотя эффективен как форма контрацепции и для уменьшения менструальное кровотечение и дискомфорт, долгоживущие ВМС в принципе могут доставлять только небольшое количество прогестерона в день, и, следовательно, внутриутробный прогестерон не может достичь адекватных уровней циркулирующего прогестерона и не подходит в качестве формы системной терапии.[106] Помимо прогестерона, ВМС прогестинов, таких как левоноргестрел (Мирена / Левосерт / Скила ), также доступны.[260]
Внутривенная инъекция
Прогестерон имеет очень короткое период полувыведения от 3 до 90 минут, когда задается внутривенная инъекция.[13]
An водный раствор прогестерона для внутривенных инъекций когда-то продавались Schering AG под торговой маркой Primolut Intravenous.[37][38]
Общее
Абсорбция
В поглощение прогестерона варьируется в зависимости от пути введения.[16]
Распределение
Прогестерон проникает через гематоэнцефалический барьер.[261] С точки зрения связывание с белками плазмы, прогестерон на 98-99% связан с белками в кровотоке.[5][6] Он привязан на 80% к альбумин, От 18% до кортикостероид-связывающий глобулин, и менее 1% до глобулин, связывающий половые гормоны, при этом оставшаяся часть от 1 до 2% циркулирует свободно или несвязанно.[5][6]
Метаболизм
При пероральном приеме прогестерон быстро метаболизируется в желудочно-кишечный тракт и печень.[118] Целых 30 разных метаболиты было обнаружено, что они образуются из прогестерона при пероральном приеме.[118] Независимо от способа введения, 5α-редуктаза главный фермент участвует в метаболизме прогестерона и отвечает примерно за 60-65% его метаболизма.[69] 5β-редуктаза также является основным ферментом метаболизма прогестерона.[69] 5α-Снижение прогестерона происходит преимущественно в кишечник (в частности двенадцатиперстная кишка ), тогда как 5β-восстановление происходит почти исключительно в печени.[69] Метаболиты прогестерона продуцируются 5α-редуктазой и 5β-редуктазой (после дальнейшего трансформация от 3α-гидроксистероид дегидрогеназа ) находятся аллопрегнанолон и прегнанолон соответственно.[118] При пероральном приеме прогестерона они возникают в кровотоке при очень высоких и фактически супрафизиологических концентрациях, которые намного превышают концентрации самого прогестерона (пиковые концентрации 30 нг / мл для аллопрегнанолона и 60 нг / мл для прегнанолона по сравнению с 12 нг / мл. для прогестерона через 4 часа после однократного перорального приема 200 мг прогестерона).[118] В одном исследовании однократная пероральная доза прогестерона 200 мг привела к пиковым уровням 20α-дигидропрогестерон около 1 нг / мл через 2 часа.[262]
Процентный состав прогестерона и его метаболитов, отраженный в сывороточных уровнях, был определен для однократной дозы 100 мг прогестерона перорально или вагинально.[71] При пероральном приеме прогестерон составляет менее 20% циркулирующей дозы, в то время как продукты с пониженным содержанием 5α и 5β, такие как аллопрегнанолон и прегнанолон, составляют около 80%.[71] При вагинальном введении прогестерон составляет около 50% дозы, а метаболиты с пониженным содержанием 5α и 5β - около 40%.[71]
Небольшое количество прогестерона преобразуется 21-гидроксилаза в 11-дезоксикортикостерон.[263][69] Повышение уровня 11-дезоксикортикостерона заметно выше, когда прогестерон вводится перорально, а не через парентеральный маршруты вроде вагинальный или внутримышечная инъекция.[69] Превращение прогестерона в 11-дезоксикортикостерон происходит в кишечнике (особенно в двенадцатиперстной кишке) и в кишечнике. почки.[263][69] 21-гидроксилаза, по-видимому, отсутствует в печени, поэтому считается, что превращение прогестерона в 11-дезоксикортикостерон в этой части тела не происходит.[69]
Эндогенный прогестерон метаболизируется примерно на 50% в 5α-дигидропрогестерон в желтое тело, 35% в 3β-дигидропрогестерон в печени и 10% в 20α-дигидропрогестерон.[60]
Метаболиты прогестерона с одним или несколькими доступными гидроксильные группы находятся сопряженный через глюкуронизация и / или сульфатирование и выводится.[264][32]
В биологический период полураспада прогестерона в обращение очень короткий; с участием внутривенная инъекция, его период полураспада варьировал от 3 до 90 минут в различных исследованиях.[13] В скорость метаболического клиренса прогестерона колеблется от 2100 до 2800 л / день и остается постоянным в течение менструальный цикл.[13][207]
Устранение
Прогестерон устранен в желчь и моча.[14][15]
Смотрите также
- Фармакодинамика прогестерона
- Фармакокинетика эстрадиола
- Фармакодинамика эстрадиола
- Фармакокинетика тестостерона
использованная литература
- ^ а б c d е ж г час я Левин Х., Уотсон Н. (март 2000 г.). «Сравнение фармакокинетики Кринона 8%, вводимого вагинально, и Прометрия, вводимого перорально женщинам в постменопаузе (3)». Fertil. Стерил. 73 (3): 516–21. Дои:10.1016 / S0015-0282 (99) 00553-1. PMID 10689005.
- ^ а б Griesinger G, Tournaye H, Macklon N, Petraglia F, Arck P, Blockeel C, van Amsterdam P, Pexman-Fieth C, Fauser BC (февраль 2019 г.). «Дидрогестерон: фармакологический профиль и механизм действия в качестве поддержки лютеиновой фазы при вспомогательной репродукции». Репродукция. Биомед. онлайн. 38 (2): 249–259. Дои:10.1016 / j.rbmo.2018.11.017. PMID 30595525.
- ^ а б Пандья М.Р., Гопинатан П., Гопинатх П.М., Дас С.К., Саута М., Шинде В. (2016). «Оценка клинической эффективности и безопасности прогестагенов при ведении угрожающего и повторяющегося выкидыша на ранних сроках беременности - обзор литературы». Индийский журнал исследований акушерства и гинекологии. 3 (2): 157. Дои:10.5958/2394-2754.2016.00043.6. ISSN 2394-2746.
- ^ а б c Полсон Р.Дж., Коллинз М.Г., Янков В.И. (ноябрь 2014 г.). «Фармакокинетика и фармакодинамика прогестерона с 3 дозировками и 2 режимами шипучей микронизированной вагинальной вставки с прогестероном». J. Clin. Эндокринол. Метаб. 99 (11): 4241–9. Дои:10.1210 / jc.2013-3937. PMID 24606090.
- ^ а б c Фриц М.А., Сперофф Л. (28 марта 2012 г.). Клиническая гинекологическая эндокринология и бесплодие. Липпинкотт Уильямс и Уилкинс. С. 44–. ISBN 978-1-4511-4847-3.
- ^ а б c Маршалл В.Дж., Маршалл В.Дж., Бангерт СК (2008). Клиническая химия. Elsevier Health Sciences. С. 192–. ISBN 978-0-7234-3455-9.
- ^ а б c Пикар Дж. Х., Бон С., Амадио Дж. М., Миркин С., Берник Б. (декабрь 2015 г.). «Фармакокинетика первой комбинации 17β-эстрадиола / капсулы прогестерона в клинической разработке для гормональной терапии менопаузы». Менопауза. 22 (12): 1308–16. Дои:10.1097 / GME.0000000000000467. ЧВК 4666011. PMID 25944519.
- ^ а б c d е Хомяк, Н. В., Мамчур, В. И., & Хомяк, Е. В. (2014). Клинико-фармакологические особенности современных лекарственных форм микронизированного прогестерона, применяемых во время беременности. Здоровье, (4), 90. https://web.archive.org/web/20180808140010/http://health-ua.com/wp-content/uploads/2015/09/MAZG2-2015_28-35.pdf
- ^ а б c http://www.accessdata.fda.gov/drugsatfda_docs/label/2013/020701s026lbl.pdf
- ^ а б c Мирчиу Ч., Перджу А., Гриу Э., Калин Дж., Нягу А., Эначеску Д., Мирон Д.С. (1998). «Фармакокинетика прогестерона у женщин в постменопаузе: 2. Фармакокинетика после чрескожного введения». Европейский журнал метаболизма и фармакокинетики лекарственных средств. 23 (3): 397–402. Дои:10.1007 / bf03192300. PMID 9842983. S2CID 32772029.
- ^ а б c d е ж г час я j Саймон Дж. А., Робинсон Д. Э., Эндрюс М. С., Хильдебранд Дж. Р., Роччи М. Л., Блейк Р. Е., Ходген Г. Д. (июль 1993 г.). «Абсорбция микронизированного прогестерона перорально: влияние еды, пропорциональность дозы и сравнение с внутримышечным прогестероном». Фертильность и бесплодие. 60 (1): 26–33. Дои:10.1016 / S0015-0282 (16) 56031-2. PMID 8513955.
- ^ а б c d е ж г час я j k л м п о п q р Cometti B (ноябрь 2015 г.). «Фармацевтическая и клиническая разработка нового препарата прогестерона». Acta Obstetricia et Gynecologica Scandinavica. 94 (Дополнение 161): 28–37. Дои:10.1111 / aogs.12765. PMID 26342177.
- ^ а б c d е ж Aufrère MB, Benson H (июнь 1976 г.). «Прогестерон: обзор и последние достижения». Журнал фармацевтических наук. 65 (6): 783–800. Дои:10.1002 / jps.2600650602. PMID 945344.
- ^ а б http://www.accessdata.fda.gov/drugsatfda_docs/label/1998/20843lbl.pdf
- ^ а б http://www.accessdata.fda.gov/drugsatfda_docs/label/2007/017362s104lbl.pdf
- ^ а б c d е ж г час я j k л м п о п q р s т ты v Kuhl H (август 2005 г.). «Фармакология эстрогенов и прогестагенов: влияние разных путей введения» (PDF). Климактерический. 8 Дополнение 1: 3–63. Дои:10.1080/13697130500148875. PMID 16112947. S2CID 24616324.
- ^ а б c d е ж г час я j k л м п о п q р s Унфер V, ди Ренцо GC, Герли S, Casini ML (2006). «Использование прогестерона в клинической практике: оценка его эффективности при различных показаниях с использованием различных способов введения». Современная лекарственная терапия. 1 (2): 211–219. Дои:10.2174/157488506776930923.
- ^ Уитакер А, Гиллиам М (2014). Контрацепция для подростков и молодых взрослых женщин. Springer. п. 98. ISBN 9781461465799.
- ^ Чаудхури СК (2007). Практика контроля рождаемости: подробное руководство (7-е изд.). Эльзевир Индия. п. 153. ISBN 978-81-312-1150-2.
- ^ а б Йосимович Дж (11 ноября 2013 г.). Гинекологическая эндокринология. Springer Science & Business Media. С. 9, 25–29, 139. ISBN 978-1-4613-2157-6.
- ^ а б c d Сэмпсон Г.А. (1981). «Оценка роли прогестерона в терапии предменструального синдрома». In van Keep PA, Utian WH (ред.). Предменструальный синдром: материалы семинара, проведенного во время Шестого Международного конгресса по психосоматическому акушерству и гинекологии, Берлин, сентябрь 1980 г.. С. 51–69. Дои:10.1007/978-94-011-6255-5_4. ISBN 978-94-011-6257-9.
- ^ Штраус Дж. Ф., Барбьери Р. Л. (2009). Репродуктивная эндокринология Йена и Яффе: физиология, патофизиология и клиническое управление. Elsevier Health Sciences. С. 807–. ISBN 978-1-4160-4907-4.
- ^ Блэкберн S (14 апреля 2014 г.). Физиология матери, плода и новорожденного. Elsevier Health Sciences. С. 92–. ISBN 978-0-323-29296-2.
- ^ Стрикер Р., Эберхарт Р., Чевайллер М.С., Куинн Ф.А., Бишоф П., Стрикер Р. (2006). «Установление подробных эталонных значений лютеинизирующего гормона, фолликулостимулирующего гормона, эстрадиола и прогестерона во время различных фаз менструального цикла на анализаторе Abbott ARCHITECT». Clin. Chem. Лаборатория. Med. 44 (7): 883–7. Дои:10.1515 / CCLM.2006.160. PMID 16776638. S2CID 524952.
- ^ Сизоненко, Пьер К. (июль 1978 г.). «Эндокринология у подростков и подростков». Американский журнал болезней детей. 132 (7): 704–12. Дои:10.1001 / архпеди.1978.02120320064015. ISSN 0002-922X. PMID 149498.
- ^ Сизоненко, П. С. (1984). «Эндокринные аспекты нормального полового созревания». Детская эндокринология в клинической практике. С. 175–182. Дои:10.1007/978-94-009-5610-0_11. ISBN 978-94-010-8974-6.
- ^ Герхард, I .; Генрих, У. (1994). "Die Pubertät und ihre Störungen" [Половое созревание и его расстройства]. Gynäkologische Endokrinologie und Fortpflanzungsmedizin [Гинекологическая эндокринология и репродуктивная медицина]. С. 263–303. Дои:10.1007/978-3-662-07635-4_6. ISBN 978-3-662-07636-1.
- ^ Тульчинский Д., Хобель С.Дж., Йегер Э., Маршалл-младший (апрель 1972 г.). «Плазма эстрон, эстрадиол, эстриол, прогестерон и 17-гидроксипрогестерон при беременности человека. I. Нормальная беременность». Am. J. Obstet. Гинеколь. 112 (8): 1095–100. Дои:10.1016/0002-9378(72)90185-8. PMID 5025870.
- ^ "Drugs @ FDA: одобренные FDA лекарственные препараты". Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Получено 26 июля 2018.
- ^ Энгель Дж., Климанн А., Кучер Б., Райхерт Д. (14 мая 2014 г.). Фармацевтические субстанции, 5-е издание, 2009 г .: синтез, патенты и применение наиболее актуальных API. Тиме. С. 1145–. ISBN 978-3-13-179275-4.
- ^ Беккер К.Л. (2001). Принципы и практика эндокринологии и метаболизма. Липпинкотт Уильямс и Уилкинс. С. 2168–. ISBN 978-0-7817-1750-2.
- ^ а б c d е Анита М.В., Джайн С., Гоэль Н. (31 июля 2018 г.). Использование прогестагенов в клинической практике акушерства и гинекологии. JP Medical Ltd., стр. 4–. ISBN 978-93-5270-218-3.
- ^ Зауэр М.В. (1 марта 2013 г.). Принципы донорства ооцитов и эмбрионов. Springer Science & Business Media. С. 7, 117–118. ISBN 978-1-4471-2392-7.
- ^ Старейшина К., Дейл Б. (2 декабря 2010 г.). Экстракорпоральное оплодотворение. Издательство Кембриджского университета. С. 26–. ISBN 978-1-139-49285-0.
- ^ а б c d е https://web.archive.org/web/20191230051017/https://mx.prvademecum.com/medicamento/prosphere-11003/
- ^ Генрих Кар (8 марта 2013 г.). Консервативная терапия Frauenkrankheiten: Anzeigen, Grenzen und Methoden Einschliesslich der Rezeptur. Springer-Verlag. С. 21–. ISBN 978-3-7091-5694-0.
- ^ а б Базовая гормональная терапия. Шеринг А.Г. 1962. стр. 96.
- ^ а б Современные лекарства и лекарственные препараты. 1962. с. 40.
Primolut Intravenous (Шеринг А.Г. Берлин)
- ^ Халим С., Хан М.И. (март 2015 г.). «Изменение тенденций индийского рынка NMP: обзор» (PDF). Международный журнал фармацевтических исследований и обзоров. 4 (3): 28–30. ISSN 2278-6074.
- ^ а б c d е ж Зутши В., Ратор А.М., Шарма К. (2005). Гормоны в акушерстве и гинекологии. Jaypee Brothers, медицинские издательства. С. 74–75. ISBN 978-81-8061-427-9.
Было замечено, что микронизированный прогестерон не оказывает подавляющего действия на холестерин липопротеинов высокой плотности (ХС-ЛПВП). Jensen et al. Доказали, что микронизированный прогестерон при пероральном приеме не оказывает вредного воздействия на липиды сыворотки. Эти препараты обладают одинаковым антиэстрогенным и антиминералокортикоидным действием, но не обладают андрогенным действием. Он не влияет на синтез альдостерона, артериальное давление, углеводный обмен или изменения настроения. Не сообщалось о побочных эффектах в отношении липидного профиля, факторов свертывания и артериального давления.
- ^ а б c d Прогестерон - Drugs.com, получено 2015-08-23
- ^ а б c d е ж г час я j k л м Kuhl H (2011). «Фармакология прогестагенов» (PDF). Journal für Reproduktionsmedizin und Endokrinologie - Журнал репродуктивной медицины и эндокринологии. 8 (1): 157–177.
- ^ а б c d е ж г час я j k л м п о п q Kuhl H, Schneider HP (август 2013 г.). «Прогестерон - промотор или ингибитор рака груди». Климактерический. 16 Дополнение 1: 54–68. Дои:10.3109/13697137.2013.768806. PMID 23336704. S2CID 20808536.
- ^ а б c d е ж г час я j k л м п о п q р s т Дэйви Д.А. (март 2018 г.). «Гормональная терапия в период менопаузы: лучшее и безопасное будущее». Климактерический. 21 (5): 454–461. Дои:10.1080/13697137.2018.1439915. PMID 29526116. S2CID 3850275.
- ^ а б c d е ж г час я j Фотерби К. (август 1996 г.). «Биодоступность пероральных половых стероидов, используемых в оральной контрацепции и заместительной гормональной терапии». Контрацепция. 54 (2): 59–69. Дои:10.1016/0010-7824(96)00136-9. PMID 8842581.
Прогестерон быстро метаболизируется, что приводит к низкой биодоступности и необходимости приема высоких доз (200 мг); его фармакологические действия, за исключением репродуктивных процессов, слабы. [...] В течение многих лет после его выделения и синтеза прогестерон можно было использовать в терапевтических целях только путем внутримышечной инъекции больших доз, так как было быстро установлено, что после перорального приема прогестерон плохо всасывается и быстро метаболизируется в желудочно-кишечном тракте, печени. и большинство тканей, а затем удаляются. Однако, как и эстрадиол, абсорбция прогестерона может быть улучшена микронизацией16. Это привело к разработке препаратов прогестерона, в основном с размером частиц <10 мкг, растворенных в масле в желатиновой капсуле. [...] сравнивали пять составов, различающихся размером частиц и носителем; все они привели к значительной абсорбции прогестерона и с аналогичными концентрациями прогестерона в плазме через 6 часов после приема, но только микронизированные или масляные препараты-носители улучшили абсорбцию (вероятно, за счет увеличения лимфатической абсорбции и, таким образом, избежания некоторого эффекта первого прохождения). [...] Концентрация прогестерона в плазме может быть выше, когда состав вводится с пищей, но даже в лучших условиях биодоступность оказывается очень низкой, поскольку AUC после внутримышечной инъекции прогестерона как минимум в десять раз выше, чем после перорального приема. .21
- ^ а б c де Линьер Б (1999). «Пероральный микронизированный прогестерон». Clin Ther. 21 (1): 41–60, обсуждение 1-2. Дои:10.1016 / S0149-2918 (00) 88267-3. PMID 10090424.
- ^ а б c d е ж г час я j k л м п Руан Х, Муек А.О. (ноябрь 2014 г.). «Системная терапия прогестероном - пероральная, вагинальная, инъекционная и даже трансдермальная?». Maturitas. 79 (3): 248–55. Дои:10.1016 / j.maturitas.2014.07.009. PMID 25113944.
- ^ Wecker L (31 мая 2018 г.). Электронная книга по фармакологии человека Броди. Elsevier Health Sciences. С. 419–. ISBN 978-0-323-59662-6.
- ^ Анита М.В., Джайн С., Гоэль Н. (31 июля 2018 г.). Использование прогестагенов в клинической практике акушерства и гинекологии. JP Medical Ltd., стр. 4, 15–20. ISBN 978-93-5270-218-3.
Прогестерон также доступен в форме вагинальных или ректальных суппозиториев или пессариев (Cyclogest), [...]
- ^ Hauss DJ (8 июня 2007 г.). Пероральные составы на основе липидов: повышение биодоступности плохо растворимых в воде лекарственных средств. CRC Press. С. 17–. ISBN 978-1-4200-1726-7.
- ^ Микоцци MS, Dog TL (19 августа 2004 г.). Электронная книга по женскому здоровью в дополнительной и интегративной медицине: клиническое руководство. Elsevier Health Sciences. С. 69–. ISBN 0-7020-3598-X.
- ^ Портер С.Дж., Путон С.В., Куин Дж.Ф., Чарман В.Н. (март 2008 г.). «Повышение солюбилизации кишечных лекарств с использованием систем доставки на основе липидов». Adv. Препарат Делив. Rev. 60 (6): 673–91. Дои:10.1016 / j.addr.2007.10.014. PMID 18155801.
- ^ а б Хамберстон AJ, Чарман WN (1997). «Носители на липидной основе для пероральной доставки плохо растворимых в воде лекарственных средств». Расширенные обзоры доставки лекарств. 25 (1): 103–128. Дои:10.1016 / S0169-409X (96) 00494-2. ISSN 0169-409X.
- ^ а б Kincl FA, Ciaccio LA, Benagiano G (январь 1978 г.). «Повышение пероральной биодоступности прогестерона за счет рецептуры». J. Стероид Биохим. 9 (1): 83–4. Дои:10.1016/0022-4731(78)90106-1. PMID 628211.
- ^ а б Харгроув Дж. Т., Максон В. С., Венц А. С. (октябрь 1989 г.). «Абсорбция прогестерона при пероральном приеме зависит от носителя и размера частиц». Am. J. Obstet. Гинеколь. 161 (4): 948–51. Дои:10.1016 / 0002-9378 (89) 90759-X. PMID 2801843.
- ^ Шиндлер А.Е., Кампаньоли С., Друкманн Р., Хубер Дж., Паскуалини Дж. Р., Швеппе К. В., Тийссен Дж. Х. (2008). «Классификация и фармакология прогестинов» (PDF). Maturitas. 61 (1–2): 171–80. Дои:10.1016 / j.maturitas.2008.11.013. PMID 19434889.[постоянная мертвая ссылка ]
- ^ а б c d е ж Герман А.С., Нафцигер А.Н., Победа Дж., Кулавы Р., Роччи М.Л., Бертино Дж.С. (2005). «Безрецептурный крем с прогестероном оказывает значительное воздействие на лекарства по сравнению с одобренными администрацией пищевых продуктов и медикаментов пероральными продуктами прогестерона». J Clin Pharmacol. 45 (6): 614–9. Дои:10.1177/0091270005276621. PMID 15901742. S2CID 28399314.
- ^ Джеймсон Дж. Л., Де Гроот Л. Дж. (25 февраля 2015 г.). Эндокринология: электронная книга для взрослых и детей. Elsevier Health Sciences. С. 2660–. ISBN 978-0-323-32195-2.
- ^ Маколи Дж. В., Кробот Ф. Дж., Кробот П. Д. (1996). «Пероральное введение микронизированного прогестерона: обзор и дополнительный опыт». Фармакотерапия. 16 (3): 453–7. Дои:10.1002 / j.1875-9114.1996.tb02977.x (неактивно 29.09.2020). PMID 8726605.CS1 maint: DOI неактивен по состоянию на сентябрь 2020 г. (ссылка на сайт)
- ^ а б Андерсон Г.Д., Одегард П.С. (октябрь 2004 г.). «Фармакокинетика эстрогенов и прогестерона при хронической болезни почек». Adv Хроническая болезнь почек. 11 (4): 357–60. Дои:10.1053 / j.ackd.2004.07.001. PMID 15492972.
- ^ а б https://www.accessdata.fda.gov/drugsatfda_docs/label/2018/210132s000lbl.pdf
- ^ Интегративная медицина. Elsevier Health Sciences. 2012. с. 343. ISBN 978-1-4377-1793-8.
- ^ Шохам З., Коперник Г. (июнь 2004 г.). «Инструменты для принятия правильных решений относительно гормональной терапии. Часть I: Предпосылки и препараты». Fertil. Стерил. 81 (6): 1447–57. Дои:10.1016 / j.fertnstert.2003.10.052. PMID 15193460.
- ^ а б c d е де Линьер Б., Деннерштейн Л., Бэкстрем Т. (апрель 1995 г.). «Влияние способа введения на метаболизм прогестерона». Maturitas. 21 (3): 251–7. Дои:10.1016/0378-5122(94)00882-8. PMID 7616875.
- ^ а б Ван-Ченг Р., Нойнер Дж. М., Барнабей В. М. (2007). Менопауза. ACP Press. п. 97. ISBN 978-1-930513-83-9.
- ^ а б Бергеманн Н., Арихер-Рёсслер А. (27 декабря 2005 г.). Эффекты эстрогенов при психических расстройствах. Springer Science & Business Media. п. 179. ISBN 978-3-211-27063-9.
- ^ Редди Д.С. (2010). «Нейростероиды: эндогенная роль в мозге человека и терапевтические возможности». Прогресс в исследованиях мозга. 186: 113–37. Дои:10.1016 / B978-0-444-53630-3.00008-7. ЧВК 3139029. PMID 21094889.
- ^ а б c Алам В., Вега М, Рискес Ф (2001). «Поддержка лютеиновой фазы». Репродукция. Биомед. онлайн. 3 (3): 250–262. Дои:10.1016 / S1472-6483 (10) 62044-5. PMID 12513863.
- ^ а б c d е ж г час я j k Наул К., Дехеннин Л., Жондет М., Роджер М. (май 1993 г.). «Профили эстрогенов плазмы, прогестерона и их метаболитов после перорального или вагинального введения эстрадиола или прогестерона». Maturitas. 16 (3): 185–202. Дои:10.1016 / 0378-5122 (93) 90064-О. PMID 8515718.
- ^ а б Уоррен М.П., Шанта С. (1999). «Использование прогестерона в клинической практике». Женщины Int J Fertil Med. 44 (2): 96–103. PMID 10338267.
- ^ а б c d е ж г час я j k де Зиглер Д., Фанчин Р. (2000). «Прогестерон и прогестины: применение в гинекологии». Стероиды. 65 (10–11): 671–9. Дои:10.1016 / s0039-128x (00) 00123-9. PMID 11108875. S2CID 5867301.
- ^ Söderpalm AH, Lindsey S, Purdy RH, Hauger R, Wit de H (2004). «Введение прогестерона вызывает у мужчин и женщин легкое седативное действие». Психонейроэндокринология. 29 (3): 339–54. Дои:10.1016 / s0306-4530 (03) 00033-7. PMID 14644065. S2CID 21796848.
- ^ де Вит Х, Шмитт Л., Парди Р., Хаугер Р. (2001). «Эффекты острого введения прогестерона у здоровых женщин в постменопаузе и женщин с нормальным циклом». Психонейроэндокринология. 26 (7): 697–710. Дои:10.1016 / s0306-4530 (01) 00024-5. PMID 11500251. S2CID 20611661.
- ^ ван Брукховен Ф, Бэкстрём Т., Веркес Р. Дж. (2006). «Пероральный прогестерон снижает скорость саккадических движений глаз и увеличивает седативный эффект у женщин». Психонейроэндокринология. 31 (10): 1190–9. Дои:10.1016 / j.psyneuen.2006.08.007. PMID 17034954. S2CID 40466952.
- ^ а б де Вит Х, Шмитт Л., Парди Р., Хаугер Р. (октябрь 2001 г.). «Эффекты острого введения прогестерона у здоровых женщин в постменопаузе и женщин с нормальным циклом». Психонейроэндокринология. 26 (7): 697–710. Дои:10.1016 / s0306-4530 (01) 00024-5. PMID 11500251. S2CID 20611661.
- ^ Туркмен С., Бэкстрем Т., Вальстрем Г., Андрин Л., Йоханссон И.М. (2011). «Толерантность к аллопрегнанолону с акцентом на рецептор ГАМК-А». Br. J. Pharmacol. 162 (2): 311–27. Дои:10.1111 / j.1476-5381.2010.01059.x. ЧВК 3031054. PMID 20883478.
- ^ Тимби Э., Балгард М., Нюберг С., Спигсет О, Андерссон А., Поранкевич-Асплунд Дж., Пурди Р. Х., Жу Д., Бэкстрём Т., Поромаа И.С. (2006). «Фармакокинетические и поведенческие эффекты аллопрегнанолона у здоровых женщин». Психофармакология. 186 (3): 414–24. Дои:10.1007 / s00213-005-0148-7. PMID 16177884. S2CID 16928783.
- ^ Перлштейн Т (2016). «Лечение предменструального дисфорического расстройства: терапевтические проблемы». Эксперт Рев Клин Фармакол. 9 (4): 1–4. Дои:10.1586/17512433.2016.1142371. PMID 26766596. S2CID 12172042.
Недавнее исследование с ингибитором 5α-редуктазы дутастеридом, который блокирует превращение прогестерона в ALLO, показало, что дутастерид в дозе 2,5 мг в день уменьшал некоторые предменструальные симптомы [7].
- ^ Шрипада Р.К., Маркс CE, Кинг А.П., Рэмптон Дж. К., Хо СС, Либерзон I (2013). «Повышение уровня аллопрегнанолона после введения прегненолона связано с усиленной активацией нейросетей регуляции эмоций». Биол. Психиатрия. 73 (11): 1045–53. Дои:10.1016 / j.biopsych.2012.12.008. ЧВК 3648625. PMID 23348009.
- ^ Дюшарм Н., Бэнкс В.А., Морли Дж. Э., Робинсон С. М., Нихофф М. Л., Маттерн С., Фарр С. А. (2010). «Распределение мозга и поведенческие эффекты прогестерона и прегненолона после интраназального или внутривенного введения». Евро. J. Pharmacol. 641 (2–3): 128–34. Дои:10.1016 / j.ejphar.2010.05.033. ЧВК 3008321. PMID 20570588.
- ^ Саудан К., Десмаршелье А., Соттас П.Е., Мангин П., Соги М. (2005). «Мочевой маркер перорального приема прегненолона». Стероиды. 70 (3): 179–83. Дои:10.1016 / j.steroids.2004.12.007. PMID 15763596. S2CID 25490229.
- ^ а б Пайпер Т., Шлуг С., Марек Ю., Шенцер В. (2011). «Исследования изменения соотношения ³C / ²C эндогенных стероидов в моче после введения прегненолона». Анальный тест на наркотики. 3 (5): 283–90. Дои:10.1002 / dta.281. PMID 21538944.
- ^ Зауэр М.В. (1 марта 2013 г.). Принципы донорства ооцитов и эмбрионов. Springer Science & Business Media. С. 117–. ISBN 978-1-4471-2392-7.
- ^ Франк Р., Гутерман Х.С. (1954). «Сравнение препаратов прогестерона при вторичной аменорее». Fertil. Стерил. 5 (4): 374–81. Дои:10.1016 / S0015-0282 (16) 31687-9. PMID 13183192.
- ^ Траберт Б., Шерман М.Э., Каннан Н., Станчик Ф.З. (сентябрь 2019 г.). «Прогестерон и рак груди». Endocr. Rev. 41 (2): 320–344. Дои:10.1210 / endrev / bnz001. ЧВК 7156851. PMID 31512725.
- ^ а б c Малик С., Кришнапрасад К. (февраль 2016 г.). «Натуральный микронизированный прогестерон с замедленным высвобождением (SR) и лютеиновая фаза: новое определение роли !!». Журнал клинико-диагностических исследований. 10 (2): QE01-4. Дои:10.7860 / JCDR / 2016 / 17278.7212. ЧВК 4800604. PMID 27042538.
- ^ Пурандаре А.Ч., Хаджаре А., Кришнапрасад К., Бхаргава А. (2014). «Исследование по мониторингу рецептурных событий для оценки профиля безопасности перорального натурального микронизированного прогестерона с замедленным высвобождением в Индии». Международный журнал медицинских исследований и наук о здоровье. 3 (4): 975. Дои:10.5958/2319-5886.2014.00034.4. ISSN 2319-5886.
- ^ Халим С., Хан М.И. (март 2015 г.). «Изменение тенденций индийского рынка NMP: обзор» (PDF). Международный журнал фармацевтических исследований и обзоров. 4 (3): 28–30. ISSN 2278-6074. S2CID 74224514. Архивировано из оригинал (PDF) на 2020-08-19.
- ^ Нигам А (2018). «Поддержка лютеиновой фазы: почему, когда и как» (PDF). Паназиатский журнал акушерства и гинекологии. 1 (2): 79–83. Архивировано из оригинал (PDF) на 2020-08-19.
- ^ Малхотра Дж., Кришнапрасад К. (январь 2016 г.). «Открытое проспективное исследование по инициативе исследователя для оценки клинической роли перорального природного или синтетического прогестерона во время циклов стимулированного ВМИ при необъяснимом бесплодии». Журнал клинико-диагностических исследований. 10 (1): QC08-10. Дои:10.7860 / JCDR / 2016 / 17058.7106. ЧВК 4740654. PMID 26894126.
- ^ Прабхат П., Коруконда К. (2018). «Исследование по надзору за использованием лекарств для оценки клинической пользы и безопасности перорального натурального микронизированного прогестерона SR при беременностях с высоким риском: исследование NAP-DELAY». Журнал клинико-диагностических исследований. Дои:10.7860 / JCDR / 2018 / 34886.12118. ISSN 2249-782X.
- ^ Сингх Н., Редди А. (апрель – июнь 2015 г.). «Современные концепции ведения преждевременных родов - обзорная статья». Индийское акушерство и гинекология. 5 (2).
- ^ а б c Кирк Е.П., Серат С., Берроуз Л.Дж., Мотт Л.А., Йео К.Дж., Фицморис Т., Льюис Л.Д. (1997). «Фармакокинетическое исследование микронизированных таблеток с пролонгированным высвобождением природного прогестерона». Восстановить здоровье. Архивировано из оригинал на 2019-03-04.
- ^ а б https://www.drugs.com/international/progesterone.html
- ^ Рен Б.Г., Дэй Р.О., Маклахлан А.Дж., Уильямс К.М. (июнь 2003 г.). «Фармакокинетика эстрадиола, прогестерона, тестостерона и дегидроэпиандростерона после трансбуккального введения женщинам в постменопаузе». Климактерический. 6 (2): 104–11. Дои:10.1080 / cmt.6.2.104.111. PMID 12841880. S2CID 26455195.
- ^ Джайн С.К., Джайн А., Гупта Й, Харья А. (февраль 2008 г.). «Дизайн и разработка мукоадгезивной буккальной пленки, содержащей прогестерон». Pharmazie. 63 (2): 129–35. Дои:10.1691 / тел.2008.7114. PMID 18380399.
- ^ Whitelaw MJ (январь 1955). «Влияние парентерального, перорального, буккального и вагинального прогестерона на эндометрий». Журнал клинической эндокринологии и метаболизма. 15 (7): 881–882. ISSN 0021-972X.
- ^ Соул С.Д., Янов М. (июль 1953 г.). «Извлечение прегнандиола из мочи после перорального приема ангидрогидроксипрогестерона, буккального прогестерона и внутримышечного прогестерона». Акушер Гинеколь. 2 (1): 68–72. PMID 13073082.
- ^ Мэддокс Д.Х., Бернсайд Б.А., Кейт А.Д. (1990). «Буккальное введение прогестерона». Материалы Международного симпозиума по контролируемому выбросу биоактивных материалов. 17. С. 291–292.
- ^ Voorspoels J, Comhaire F, De Sy W., Remon JP (1997). «Буккальное всасывание прогестерона у собак». Материалы Международного симпозиума по контролируемому выбросу биоактивных материалов. 24. С. 185–186.
- ^ а б Ганс Герман Юлиус Хагер; Вальтер Керн; Список Пола Хайнца; Герман Йозеф Рот (1969). Hagers Handbuch der Pharmazeutischen Praxis: Für Apotheker, Arzneimittelhersteller, Ärzte und Medizinalbeamte: Wirkstoffgruppen II Chemikalien und Drogen (A-AL). Springer-Verlag. С. 178–. ISBN 978-3-662-25655-8.
- ^ Эштон Лерой Уэлш (1951). Дерматологический формуляр: руководство для студентов-медиков и врачей-дерматологов. Образовательные издательства. п. 155.
- ^ а б Чакмакджян Ж. Захария, Нью-Йорк (июнь 1987 г.). «Биодоступность прогестерона при разных способах введения». Журнал репродуктивной медицины. 32 (6): 443–8. PMID 3612635.
- ^ а б Вильянуэва Б., Каспер РФ, Йен СС (апрель 1981 г.). «Интравагинальное введение прогестерона: усиление абсорбции после лечения эстрогенами». Fertil. Стерил. 35 (4): 433–7. Дои:10.1016 / S0015-0282 (16) 45439-7. PMID 7215569.
- ^ а б c Зигмунт М., Сапа Ю. (2017). «Прогестерон - новый взгляд на старый препарат». Репродуктивная эндокринология. 0 (33): 17–25. Дои:10.18370/2309-4117.2017.33.17-25. ISSN 2411-1295.
[В других фармакокинетических исследованиях было доказано, что после приема 100 мг прогестерона гормон достиг максимальной концентрации в плазме через 1-4 часа, которая составляла в среднем 13,5 нг / мл.]
- ^ а б c d е ж г час я j Unfer V, Casini ML, Marelli G, Costabile L, Gerli S, Di Renzo GC (2005). «Различные способы введения прогестерона и синдром поликистозных яичников: обзор литературы». Гинеколь. Эндокринол. 21 (2): 119–27. Дои:10.1080/09513590500170049. PMID 16109599. S2CID 24890723.
- ^ а б c d Стовалл Д.В., Ван Вурхис Б.Дж., Маттингли К.Л., Спаркс А.Е., Чаплер Ф.К., Сироп С.Х. (май 1996 г.). «Эффективность сублингвального введения прогестерона во время циклов переноса криоконсервированных эмбрионов: результаты согласованного последующего исследования». Fertil. Стерил. 65 (5): 986–91. Дои:10.1016 / S0015-0282 (16) 58274-0. PMID 8612862.
- ^ Чакмакджян Ж. Захария, Нью-Йорк (июнь 1987 г.). «Биодоступность прогестерона при разных способах введения». J Reprod Med. 32 (6): 443–8. ISSN 0024-7758. PMID 3612635.
- ^ Бикерс В. (август 1949 г.). «Прогестерон; сравнение внутримышечного, перорального и сублингвального способов введения». J. Clin. Эндокринол. Метаб. 9 (8): 736–42. Дои:10.1210 / jcem-9-8-736. PMID 18133494.
- ^ Угловой GW (1944). «Поглощение стероидных гормонов слизистыми оболочками рта, с особым упором на сублингвальное введение прогестерона». Американский журнал акушерства и гинекологии. 47 (5): 670–677. Дои:10.1016 / S0002-9378 (16) 40321-2.
- ^ Гринблатт РБ (1944). «Сублингвальная абсорбция прогестерона и ангидрогидроксипрогестерона». Журнал клинической эндокринологии и метаболизма. 4 (4): 156–158. Дои:10.1210 / jcem-4-4-156. ISSN 0021-972X.
- ^ Гринблатт РБ (1944). «Перлингвальная абсорбция прогестерона и ангидрогидроксипрогестерона». Журнал клинической эндокринологии и метаболизма. 4 (7): 321–325. Дои:10.1210 / jcem-4-7-321. ISSN 0021-972X.
- ^ а б Стидж Дж. Ф., Рупп С. Л., Стаут А. Л., Бернхизель М. (октябрь 1986 г.). «Биодоступность прогестерона, вводимого через нос». Fertil. Стерил. 46 (4): 727–9. Дои:10.1016 / S0015-0282 (16) 49661-5. PMID 3758397.
- ^ Посачи К., Смитц Дж., Камю М., Османагаоглу К., Деврой П. (июнь 2000 г.). «Прогестерон для лютеиновой поддержки вспомогательных репродуктивных технологий: клинические варианты». Гм. Репрод. 15 Дополнение 1: 129–48. Дои:10.1093 / humrep / 15.suppl_1.129. PMID 10928425.
- ^ а б c d е ж г час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае Станчик ФЗ (2014). «Лечение женщин в постменопаузе местными кремами и гелями с прогестероном: эффективны ли они?». Климактерический. 17 Дополнение 2: 8–11. Дои:10.3109/13697137.2014.944496. PMID 25196424. S2CID 20019151.
- ^ а б c d е ж г час я j k л м п о п q р s т ты v ш Икс у z аа ab ac объявление ае аф аг ах ай эй ак аль я ан ао ap водный ар так как в au Станчик Ф.З., Полсон Р.Дж., Рой С. (2005). «Чрескожное введение прогестерона: уровни в крови и защита эндометрия». Менопауза. 12 (2): 232–7. Дои:10.1097/00042192-200512020-00019. PMID 15772572. S2CID 10982395.
- ^ а б c d е ж г час я Sitruk-Ware R (январь 1989 г.). «Трансдермальная доставка стероидов». Контрацепция. 39 (1): 1–20. Дои:10.1016/0010-7824(89)90012-7. PMID 2642780.
- ^ а б c d е ж Биньковская М., Воронь Ю. (июнь 2015 г.). «Прогестагены в гормональной терапии менопаузы». Przeglad Menopauzalny = Обзор менопаузы. 14 (2): 134–43. Дои:10.5114 / pm.2015.52154. ЧВК 4498031. PMID 26327902.
- ^ https://www.drugs.com/international/progestogel.html
- ^ Маркер RE, Krueger J (1940). «Стерины. CXII. Сапогенины. XLI. Приготовление триллина и его превращение в прогестерон». Варенье. Chem. Soc. 62 (12): 3349–3350. Дои:10.1021 / ja01869a023.
- ^ Зава Д.Т., Доллбаум К.М., Блен М. (март 1998 г.). «Биоактивность эстрогена и прогестина в пищевых продуктах, травах и специях». Труды Общества экспериментальной биологии и медицины. 217 (3): 369–78. Дои:10.3181/00379727-217-44247. PMID 9492350. S2CID 20673587.
- ^ Комесаров П.А., Черный CV, Кабель V, Судхир К. (июнь 2001 г.). «Влияние экстракта дикого ямса на симптомы менопаузы, липиды и половые гормоны у здоровых женщин в период менопаузы». Климактерический. 4 (2): 144–50. Дои:10.1080/713605087. PMID 11428178.
- ^ а б Sitruk-Ware R (февраль 1993 г.). «Чрескожная и трансдермальная заместительная терапия эстрогенами». Анналы медицины. 25 (1): 77–82. Дои:10.3109/07853899309147862. PMID 8435193.
- ^ а б c d е Мове-Джарвис П., Ситрук-Варе Р., Куттенн Ф. (1981). «Доброкачественное заболевание груди». Рак груди 4. С. 51–94. Дои:10.1007/978-1-4615-6571-0_3. ISBN 978-1-4615-6573-4.
- ^ Де Боевер Дж, Ферхойген С., Ван Маэле Дж., Вандекеркхове Д. (1983). «Концентрации стероидов в сыворотке, железистой ткани молочной железы и жидкости кисты молочной железы у контрольных пациентов и пациентов, получавших прогестерон» (PDF). В Альберто Анджели (ред.). Эндокринология кистозной болезни груди. Raven Press. С. 93–99.
- ^ а б c Тауберт HD (1989). "Lokaltherapie mit Sexualsteroiden". Gießener Gynäkologische Fortbildung 1989. С. 214–224. Дои:10.1007/978-3-642-50217-0_25. ISBN 978-3-540-51234-9.
- ^ Видерсберг С., Гай Р.Х. (сентябрь 2014 г.). «Трансдермальная доставка лекарств: 30+ лет войны, а борьба продолжается!» (PDF). Журнал контролируемого выпуска. 190: 150–6. Дои:10.1016 / j.jconrel.2014.05.022. PMID 24852092.
- ^ Джонс Х (25 сентября 2008 г.). Дефицит тестостерона у мужчин. ОУП Оксфорд. С. 89–. ISBN 978-0-19-954513-1.
- ^ Растрелли Г., Райзман Ю., Ферри С., Пронтера О, Сфорца А., Магги М., Корона Г. (2019). «Заместительная терапия тестостероном». Сексуальная медицина. С. 79–93. Дои:10.1007/978-981-13-1226-7_8. ISBN 978-981-13-1225-0.
- ^ а б Поттс Р.О., Лобо Р.А. (май 2005 г.). «Трансдермальная доставка лекарств: клинические соображения для акушера-гинеколога». Акушер Гинеколь. 105 (5, Pt 1): 953–61. Дои:10.1097 / 01.AOG.0000161958.70059.db. PMID 15863530. S2CID 23411589.
- ^ а б c d е ж г час Du JY, Санчес П., Ким Л., Азен К.Г., Зава Д.Т., Станчик Ф.З. (2013). «Чрескожная доставка прогестерона посредством нанесения крема или геля у женщин в постменопаузе: рандомизированное перекрестное исследование уровней прогестерона в сыворотке, цельной крови, слюне и капиллярной крови». Менопауза. 20 (11): 1169–75. Дои:10.1097 / GME.0b013e31828d39a2. PMID 23652031. S2CID 33857615.
- ^ а б c Heustess A, Asbill S, Eagerton D, Arnold J (2014). «Проникновение в кожу in vitro и содержание в коже прогестерона из различных составов для местного применения». Int J Pharm Compd. 18 (6): 512–5. PMID 25906629.
- ^ а б c Райт Ф., Мове-Джарвис П. (1989). «Метаболизм половых стероидов в справочнике экспериментальной фармакологии». Справочник по экспериментальной фармакологии, продолжение Handbuch der Experimentellen Pharmakologie. 87 / 1: 247–255. Дои:10.1007/978-3-642-73797-8_15. ISSN 0171-2004.
- ^ а б Mauvais-Jarvis P, Kuttenn F, Ohlgiesser C (апрель 1974 г.). "Résultats du traitement de mastodynies et de mastopathies par la progestérone percutanée" [Результаты лечения мастодинии и мастопатии чрескожным прогестероном]. Nouv Presse Med (На французском). 3 (16): 1027–8. PMID 4836479.
- ^ Mauvais-Jarvis P, Kuttenn F, Baudot N (январь 1974 г.). «Подавление превращения тестостерона в дигидротестостерон у мужчин, получавших чрескожно прогестерон». J. Clin. Эндокринол. Метаб. 38 (1): 142–7. Дои:10.1210 / jcem-38-1-142. PMID 4809637.
- ^ Mauvais-Jarvis P, Baudot N, Bercovici JP (декабрь 1969 г.). «Исследования in vivo метаболизма прогестерона в коже человека». J. Clin. Эндокринол. Метаб. 29 (12): 1580–5. Дои:10.1210 / jcem-29-12-1580. PMID 5347688.
- ^ Заргар-Шоштари С., Ваххабагей Х., Мехрсаи А., Вен Дж., Алани Р. (2010). «Трансдермальная доставка биоидентичного прогестерона с использованием дутастерида (ингибитор 5α-редуктазы): пилотное исследование». J Pharm Pharm Sci. 13 (4): 626–36. Дои:10.18433 / j3rw2h. PMID 21486536.
- ^ Заргар-Шоштари С., Ваххабагей Х., Мехрсаи А., Вен Дж., Алани Р. (2011). «Трансдермальная доставка биоидентичного прогестерона со стероидным ингибитором 5α-редуктазы (дутастерид): пилотное исследование». Журнал фармации и фармацевтических наук. 13 (4): 626–36. Дои:10.18433 / J3RW2H. ISSN 1482-1826. PMID 21486536.
- ^ Заргар-Шоштари, С. (2011). Трансдермальная доставка прогестерона (докторская диссертация). http://hdl.handle.net/2292/8199
- ^ Ракель Д. (2012). Интегративная медицина. Elsevier Health Sciences. С. 330–. ISBN 978-1-4377-1793-8.
- ^ а б De Boever, J .; Desmet, B .; Вандекеркхове, Д. (1980). «Изменение концентраций прогестерона, 20α-дигидропрогестерона и эстрадиола в ткани молочной железы человека и крови после местного применения прогестерона». В P. Mauvais-Jarvis (ed.). Чрескожная абсорбция стероидов. Академическая пресса. С. 259–265. ISBN 9780124806801.
- ^ а б Chang KJ, Lee TT, Linares-Cruz G, Fournier S, de Ligniéres B (апрель 1995 г.). «Влияние чрескожного введения эстрадиола и прогестерона на цикл эпителиальных клеток молочной железы человека in vivo». Fertil. Стерил. 63 (4): 785–91. Дои:10.1016 / S0015-0282 (16) 57482-2. PMID 7890063.
- ^ Спайсер Д.В., Урсин Г., Пайк М.С. (май 1996 г.). «Концентрации прогестерона - физиологические или фармакологические?». Fertil. Стерил. 65 (5): 1077–8. Дои:10.1016 / s0015-0282 (16) 58295-8. PMID 8612843.
- ^ а б c d е ж г час фон Ай Корлета Н, Капп Э, Феррейра МБ (2004). «Фармакокинетика натуральных вагинальных суппозиториев прогестерона». Гинеколь. Акушерство. Вкладывать деньги. 58 (2): 105–8. Дои:10.1159/000078842. PMID 15192285. S2CID 46611378.
- ^ Рао К., Карп Х. Дж., Фишер Р. (30 сентября 2013 г.). Принципы и практика вспомогательных репродуктивных технологий (3 тома). JP Medical Ltd. стр. 1025–. ISBN 978-93-5090-736-8.
Вагинальное введение прогестерона может осуществляться разными путями, такими как микронизированные вагинальные суппозитории (например, Утрожестан или Циклогест 600 мг в день), пенные вагинальные вставки (эндометрин) или вагинальные гели (8% гель Crinone, содержащий 90 мг микронизированного прогестерона, одно или два применения в день).
- ^ Раковски С., Шлегель П.Н., Фаузер Б.К., Барнард Л. (7 июня 2011 г.). Двухгодичный обзор бесплодия. Springer Science & Business Media. С. 84–85. ISBN 978-1-4419-8456-2.
В настоящее время коммерчески доступны три стандартизированных вагинальных препарата прогестерона для использования при ЭКО. Микронизированные капсулы с прогестероном (Утрожестан / Прометриум) доступны и широко используются в Европе и Южной Америке, но не одобрены FDA для использования при ЭКО / АРТ в Соединенных Штатах. Двумя препаратами прогестерона, одобренными FDA для использования при ЭКО, являются вагинальный гель Crinone 8%, а с недавнего времени - эндометрин 100 мг (натуральный прогестерон в капсулах).
- ^ Друг DR (октябрь 2016 г.). «Разработка систем с контролируемым высвобождением за последние 50 лет в области контрацепции». J Control Release. 240: 235–241. Дои:10.1016 / j.jconrel.2015.12.043. PMID 26732558.
- ^ Майлз Р.А., Полсон Р.Дж., Лобо Р.А., Пресс М.Ф., Дамуш Л., Зауэр М.В. (сентябрь 1994 г.). «Фармакокинетика и уровни прогестерона в тканях эндометрия после введения внутримышечно и вагинально: сравнительное исследование». Fertil. Стерил. 62 (3): 485–90. Дои:10.1016 / s0015-0282 (16) 56935-0. PMID 8062942.
- ^ Шмидт Дж. У., Воллнер Д., Курцио Дж., Ридлингер Дж., Ким Л. С. (октябрь 2006 г.). «Заместительная гормональная терапия у женщин в менопаузе: прошлые проблемы и будущие возможности». Гинеколь. Эндокринол. 22 (10): 564–77. Дои:10.1080/09513590600927017. PMID 17135036. S2CID 11567574.
- ^ а б c d е Голетиани Н.В., Кейт Д.Р., Горски С.Дж. (октябрь 2007 г.). «Прогестерон: обзор безопасности для клинических исследований». Exp Clin Psychopharmacol. 15 (5): 427–44. Дои:10.1037/1064-1297.15.5.427. PMID 17924777.
- ^ Пороги ES (7 сентября 2015 г.). Скрининг одиночного эуплоидного эмбриона: молекулярная генетика в репродуктивной медицине. Springer. С. 276–277. ISBN 978-3-319-16892-0.
- ^ Tatford EP (6 декабря 2012 г.). Проблемы в гинекологии. Springer Science & Business Media. С. 85–. ISBN 978-94-009-4125-0.
Прогестерон также можно вводить в виде ректальных или вагинальных суппозиториев (Циклогест) в дозе 400 мг в день.
- ^ Агса М.М., Рахманпур Х., Багери М., Давари-Танха Ф., Наср Р. (октябрь 2012 г.). «Рандомизированное сравнение эффективности, побочных эффектов и удобства для пациентов вагинального и ректального введения Циклогеста (®) при использовании для поддержки лютеиновой фазы при лечении ИКСИ». Архив гинекологии и акушерства. 286 (4): 1049–54. Дои:10.1007 / s00404-012-2410-7. PMID 22714063. S2CID 12892111.
- ^ Khrouf M, Slimani S, Khrouf MR, Braham M, Bouyahia M, Berjeb KK и др. (2016). «Прогестерон для поддержки лютеиновой фазы при экстракорпоральном оплодотворении: сравнение вагинальных и ректальных пессариев с вагинальными капсулами: рандомизированное контролируемое исследование». Insights Clinical Medicine. Женское здоровье. 9: 43–47. Дои:10.4137 / CMWH.S32156. ЧВК 5217976. PMID 28096703.
- ^ а б Тай П.Й., Лентон Е.А. (июнь 2005 г.). «Влияние лютеиновой добавки на исход беременности после стимулированных циклов ЭКО» (PDF). Медицинский журнал Малайзии. 60 (2): 151–7. PMID 16114155.
- ^ ван дер Меер Ю.Г., ван Лоенен А.С., Лендерслот Е.В., Ясманн Л.Дж. (октябрь 1982 г.). «Уровни прогестерона в плазме после использования суппозиториев с высокой дозой. Предварительный отчет». Pharmaceutisch Weekblad. Научное издание. 4 (5): 135–6. Дои:10.1007 / BF01959031. PMID 7145597. S2CID 19671703.
- ^ а б Ниллиус SJ, Йоханссон ED (июнь 1971 г.). «Уровни прогестерона в плазме после вагинального, ректального или внутримышечного введения прогестерона». Американский журнал акушерства и гинекологии. 110 (4): 470–7. Дои:10.1016/0002-9378(71)90686-7. PMID 5582003.
- ^ Гамбургер C (1965). «Прием прогестерона в виде суппозиториев». Acta Endocrinologica. 49 (3_Suppl): S101. Дои:10.1530 / acta.0.049S101. ISSN 0804-4643.
- ^ Ван дер Меер Ю.Г., Бенедек-Ясманн Л.Дж., Ван Лоенен А.С. (2009). «Влияние высоких доз прогестерона на предменструальный синдром; двойное слепое перекрестное исследование». Журнал психосоматического акушерства и гинекологии. 2 (4): 220–222. Дои:10.3109/01674828309088321. ISSN 0167-482X.
- ^ а б c Knörr K, Beller FK, Lauritzen C (17 апреля 2013 г.). Lehrbuch der Gynäkologie. Springer-Verlag. С. 214–. ISBN 978-3-662-00942-0.
- ^ Knörr K, Knörr-Gärtner H, Beller FK, Lauritzen C (8 марта 2013 г.). Geburtshilfe und Gynäkologie: Physiologie und Pathologie der Reproduktion. Springer-Verlag. С. 583–. ISBN 978-3-642-95583-9.
- ^ А. Лабхарт (6 декабря 2012 г.). Клиническая эндокринология: теория и практика. Springer Science & Business Media. С. 554–. ISBN 978-3-642-96158-8.
- ^ а б Horský J, Presl J (1981). «Гормональное лечение нарушений менструального цикла». В Horsky J, Presl K (ред.). Функция яичников и ее нарушения: диагностика и лечение. Springer Science & Business Media. С. 309–332. Дои:10.1007/978-94-009-8195-9_11. ISBN 978-94-009-8195-9.
- ^ Иоахим Уфер (1969). Принципы и практика гормональной терапии в гинекологии и акушерстве. де Грюйтер. п. 49.
17α-гидроксипрогестерона капроат является депо-гестагеном, не имеющим побочных действий. Доза, необходимая для индукции секреторных изменений в примированном эндометрии, составляет около 250 мг. за менструальный цикл.
- ^ Виллибальд Пшайрембель (1968). Praktische Gynäkologie: für Studierende und Ärzte. Вальтер де Грюйтер. С. 598, 601. ISBN 978-3-11-150424-7.
- ^ а б c d Ферин Дж (сентябрь 1972 г.). «Эффекты, продолжительность действия и метаболизм у человека». В Тауск М (ред.). Фармакология эндокринной системы и родственные препараты: прогестерон, препараты для прогестации и противозачаточные средства. II. Pergamon Press. С. 13–24. ISBN 978-0080168128. OCLC 278011135.
- ^ Хенцл М.Р., Эдвардс Дж. А. (10 ноября 1999 г.). «Фармакология прогестинов: производные 17α-гидроксипрогестерона и прогестины первого и второго поколения». В Sitruk-Ware R, Mishell DR (ред.). Прогестины и антипрогестины в клинической практике. Тейлор и Фрэнсис. С. 101–132. ISBN 978-0-8247-8291-7.
- ^ а б Джанет Браттон (1976). Фармакология половых гормонов. Академическая пресса. п. 114. ISBN 978-0-12-137250-7.
- ^ Пел GW (апрель 1994). «Фармакодинамические эффекты вводимых один раз в месяц комбинированных инъекционных контрацептивов». Контрацепция. 49 (4): 361–85. Дои:10.1016/0010-7824(94)90033-7. PMID 8013220.
- ^ Toppozada MK (апрель 1994). «Существующие раз в месяц комбинированные инъекционные контрацептивы». Контрацепция. 49 (4): 293–301. Дои:10.1016/0010-7824(94)90029-9. PMID 8013216.
- ^ Багаде О, Павар В., Пател Р., Пател Б., Авасаркар В., Дивейт С. (2014). «Увеличение использования обратимых контрацептивов длительного действия: безопасный, надежный и экономичный контроль над рождаемостью» (PDF). World J Pharm Pharm Sci. 3 (10): 364–392. ISSN 2278-4357. Архивировано из оригинал (PDF) на 2017-08-10. Получено 2016-08-24.
- ^ а б c Goebelsmann U (1986). «Фармакокинетика противозачаточных стероидов у людей». В Gregoire AT, Blye RP (ред.). Противозачаточные стероиды: фармакология и безопасность. Springer Science & Business Media. С. 67–111. Дои:10.1007/978-1-4613-2241-2_4. ISBN 978-1-4613-2241-2.
- ^ Беккер H, Дюстерберг B, Клостерхалфен H (1980). «[Биодоступность ацетата ципротерона после перорального и внутримышечного применения у мужчин (авторский перевод)]» [Биодоступность ацетата ципротерона после перорального и внутримышечного применения у мужчин]. Urologia Internationalis. 35 (6): 381–5. Дои:10.1159/000280353. PMID 6452729.
- ^ Мольц Л., Хаазе Ф., Шварц Ю., Хаммерштейн Дж. (Май 1983 г.). «[Лечение вирилизованных женщин с внутримышечным введением ципротерона ацетата]» [Эффективность внутримышечно применяемого ципротерона ацетата при гиперандрогении]. Geburtshilfe Und Frauenheilkunde. 43 (5): 281–7. Дои:10.1055 / с-2008-1036893. PMID 6223851.
- ^ Райт Дж. К., Берджесс диджей (29 января 2012 г.). Инъекции и имплантаты длительного действия. Springer Science & Business Media. С. 114–. ISBN 978-1-4614-0554-2.
- ^ Чу Й.Х., Ли Ц., Чжао Ц.Ф. (апрель 1986 г.). «Фармакокинетика мегестрола ацетата у женщин, получающих внутримышечно инъекционный контрацептив эстрадиол-мегестрола длительного действия». Китайский журнал клинической фармакологии.
Результаты показали, что после инъекции концентрация МА в плазме быстро увеличивалась. Среднее время пикового уровня MA в плазме составляло 3-й день, наблюдалась линейная зависимость между логарифмом концентрации MA в плазме и временем (днем) после введения у всех субъектов, период полувыведения фазы элиминации t1 / 2β = 14,35 ± 9,1 дня.
- ^ Раннебаум BC, Рабе Т., Кизель Л. (6 декабря 2012 г.). Женская контрацепция: новости и тенденции. Springer Science & Business Media. С. 429–. ISBN 978-3-642-73790-9.
- ^ Артини П.Г., Генаццани А.Р., Петралья Ф. (11 декабря 2001 г.). Достижения в гинекологической эндокринологии. CRC Press. С. 105–. ISBN 978-1-84214-071-0.
- ^ Кинг Т.Л., Брукер М.С., Крибс Дж. М., Фейи Дж. О. (21 октября 2013 г.). Акушерство Варни. Издательство "Джонс и Бартлетт". С. 495–. ISBN 978-1-284-02542-2.
- ^ а б c d е Бернардо-Эскудеро Р., Кортес-Бонилья М., Алонсо-Камперо Р., Франсиско-Доче М. Т., Чаварин-Гонсалес Дж., Пиментель-Мартинес С., Замбрано-Тапиа Л. (2012). «Наблюдательное исследование местной переносимости инъекционных микросфер прогестерона». Гинеколь. Акушерство. Вкладывать деньги. 73 (2): 124–9. Дои:10.1159/000330711. PMID 21997608. S2CID 5163167.
- ^ Тайлер ET, Олсон HJ (апрель 1959 г.). «Стимулирующие фертильность и ингибирующие эффекты новых стероидных гормональных веществ». J Am Med Assoc. 169 (16): 1843–54. Дои:10.1001 / jama.1959.03000330015003. PMID 13640942.
- ^ Ферин Дж (сентябрь 1972 г.). «Эффекты, продолжительность действия и метаболизм в человеке». В Тауск М (ред.). Фармакология эндокринной системы и родственные препараты: прогестерон, препараты для прогестации и противозачаточные средства. II. Pergamon Press. С. 13–24. ISBN 978-0080168128. OCLC 278011135.
- ^ Horský J, Presl J (1981). «Гормональное лечение нарушений менструального цикла». В J. Horsky, J. Presl (ред.). Функция яичников и ее нарушения: диагностика и лечение. Springer Science & Business Media. С. 309–332. Дои:10.1007/978-94-009-8195-9_11. ISBN 978-94-009-8195-9.
- ^ Knörr K, Beller FK, Lauritzen C (17 апреля 2013 г.). Lehrbuch der Gynäkologie. Springer-Verlag. С. 214–. ISBN 978-3-662-00942-0.
- ^ а б Henzl M, Horský J, Presl J (1965), "Racionální Léčba Gestageny v Gynekologii" [Рациональное лечение гестагенами в гинекологии], Československá Gynekologie (на чешском языке), 30/44 (1/2): 10–16, ISSN 0374-6852,
Рациональные показания к применению чистого прогестерона и некоторых гестагенов. Это депо-микрокристаллические препараты (аголютин-депо), неолютин и новые эффективные пероральные гестагены (нор-стероиды, суперлютин). [...]
- ^ Обер KG, Klein I, Weber M (1954). «[Проблема прогестероновой терапии; экспериментальные исследования теста Хукера-Форбса и клинические наблюдения за кристаллическими суспензиями]» [К вопросу о лечении прогестероном: экспериментальные исследования с тестом Хукера-Форбса и клинические наблюдения с кристаллическими суспензиями]. Archiv für Gynakologie. 184 (5): 543–616. Дои:10.1007 / BF00976991. PMID 13198154. S2CID 42832785.
- ^ Энгелькинг Э (13 марта 2013 г.). Der Deutschen Ophthalmologischen Gesellschaft: В Мюнхене 1950 г. [Немецкое офтальмологическое общество: в Мюнхене, 1950 г.]. Springer-Verlag. С. 145–146. ISBN 978-3-642-47081-3.
Intramuskulare Injektionen öliger Progesteronlösungen erzielen wohl eine hohe Stoßwirkung, der Dauereffekt ist jedoch nur gering. So kann die Wirkung einer Injektion von 10 mg [intramuskulär] in schweren Glaukomfällen schon nach etwa 6 Stunden vergehen. Das Ergebnis ist dann ein Wiederhochschnellen des Augendruckes. Um den Hormonspiegel nicht zu rasch wieder abfallen zu lassen und gleichzeitig eine Stoßwirkung zu erzielen, mischen wir aus diesem Grunde gerne die ölige Lösung mit einer Kristallsuspension. Wir injizierten meist в den Deltoideus. Bei Hormonkristallsuspensionen braucht man ziemlich dicke Nadeln und benützt am besten eine 1 ccm Spritze. Für die augenärztliche Praxis ist letztere Art der Depotbehandlung am zweckmäßigsten. In schwereren Fällen mit chronischer hoher Drucksteigerung wirken [zum Beispiel] bei Verwendung von [Ampulle] mit je 30 mg [Kristallsuspension] die ersten Injektionen nur wenige Tage; mit zunehmender Dauer der Behandlung kann man dann jedoch die Zeitabstände zswischen den einzelnen Spritzen bis auf mehrere Wochen erhöhen. Die meisten Patienten spuren selbst deutlich, wenn die Depotwirkung nachläßt und kommen spontan, sich eine neue Injektion zu holen. [...] Депо: флаволутан (Boehringer & Söhne) Кристаллсуспензия в ампуле 30 мг.
- ^ Ширман Р.П. (июнь 1975 г.). «Разработка депо контрацептивов». Журнал стероидной биохимии. 6 (6): 899–902. Дои:10.1016/0022-4731(75)90323-4. PMID 1177432.
- ^ а б Эдкинс Р.П. (1959). «Модификация продолжительности действия лекарств». Журнал фармации и фармакологии. 11 (S1): 54–66 зуб. Дои:10.1111 / j.2042-7158.1959.tb10412.x. ISSN 0022-3573. S2CID 78850713.
- ^ а б c Линза Дж., Овербек Г.А., Полдерман Дж. (1949). «Влияние половых гормонов в некоторых органических растворителях; эмульгированные в воде». Acta Endocrinologica. 2 (4): 396–404. Дои:10.1530 / acta.0.0020396. PMID 18140399.
- ^ Herrmann U (1958). "Abhängigkeit der durch Oestrogen- und Progesteron-Kristalle Indzierten Abbruchblutung von der Korngröße". Гинекологическое и акушерское обследование. 146 (4): 318–323. Дои:10.1159/000306607. ISSN 1423-002X.
- ^ Раппапорт Ф., Девушка Н. (август 1947 г.). «Инъекционные кристаллические гормоны». Ланцет. 2 (6469): 296–297. Дои:10.1016 / с0140-6736 (47) 92066-7. PMID 20344499.
- ^ Мастерс WH, Grody MH, Magallon DT (ноябрь 1952 г.). «Прогестерон в водной кристаллической суспензии по сравнению с прогестероном в масле; сравнение с помощью тестов на кровотечение отмены у женщины-человека». Журнал клинической эндокринологии и метаболизма. 12 (11): 1445–53. Дои:10.1210 / jcem-12-11-1445. PMID 12999984.
- ^ а б c Кар Х (8 марта 2013 г.). Консервативная терапия Frauenkrankheiten: Anzeigen, Grenzen und Methoden Einschliesslich der Rezeptur. Springer-Verlag. С. 20–21. ISBN 978-3-7091-5694-0.
- ^ https://web.archive.org/web/20190519061250/http://www.sukl.cz/download/spc/SPC14550.pdf
- ^ Články v českých časopisech. Статные книжные ЧССР. 1960. С. 1601, 1642.
- ^ Пльзенский лекарственный сборник. Дополнение. 1961. с. 169.
- ^ Обзор чехословацкой медицины. Avicenum - Чехословацкая медицинская пресса. 1973. с. 5.
Прогестерон, водная микрокристаллическая суспензия (Agolutin Depot SPOFA)
- ^ Уфер Дж. (1968). "Die therapeutische Anwendung der Gestagene beim Menschen" [Терапевтическое использование прогестагенов у людей]. Die Gestagene [Гестагены]. Springer-Verlag. С. 1026–1124. Дои:10.1007/978-3-642-99941-3_7. ISBN 978-3-642-99941-3.
C. Dysfunktionelle Uterusblutungen. [...] 1. Depotinjektionen. 1. Оригинальный метод KAUFMANN und OBER. Es wird 1 ампер. с 200 мг прогестерона и 10 мг эстрадиол-монобензоатов и кристаллической суспензии (систоциклин) [676, 678, 679, 295, 482, 365, 434, 563, 400]. [...] Beispiele. KAUFMANN et al. [485]: 400 мг прогестерона + 20 мг эстрадиолмонобензоата кристалла суспензии. ЭЛЕРТ [224] У. ХЕРРМАНН [363]: 200 мг прогестерона + 10 мг эстрадиолмонобензоат кристаллической суспензии.
- ^ Симпозиум Ciba. Ciba. 1957 г.
Ассортимент гормональных препаратов CIBA был увеличен с появлением «Систоциклина», одна ампула которого содержит 200 мг прогестерона и 10 мг монобензоата эстрадиола в кристаллической суспензии; таким образом, он отвечает требованиям - в соответствии с последними данными клиники KAUFMANN - случаев, отмеченных дефицитом гормона желтого тела, например. г. при функциональном кровотечении, таком как геморрагическая метропатия.
- ^ Ciba Zeitschrift. 1957. с. 3001.
Систоциклин - микрокристаллическая суспензия, содержащая 200 мг прогестерона и 10 мг монобензоата эстрадиола на ампулу - стал особенно полезным при лечении так называемых функциональных [...]
- ^ Виллибальд Пшайрембель (1968). Praktische Gynäkologie: für Studierende und Ärzte. Вальтер де Грюйтер. стр. 601–. ISBN 978-3-11-150424-7.
- ^ Иоахим Уфер (1960). Гормональная терапия в фрауэнхейлькунде: Grundlagen und Praxis. Грюйтер. п. 153. ISBN 9783111138770.
- ^ Виллибальд Пшайрембель (15 июня 2011 г.). Praktische Gynäkologie: für Studierende und Ärzte. Вальтер де Грюйтер. стр. 601–. ISBN 978-3-11-150424-7.
- ^ а б Свайер Г.И. (январь 1960 г.). «Прогестагены и их клиническое применение: Часть I». Br Med J. 1 (5165): 48–9. Дои:10.1136 / bmj.1.5165.48. ЧВК 1966392. PMID 13836156.
- ^ Джанет Браттон (1976). Фармакология половых гормонов. Академическая пресса. п. 38. ISBN 978-0-12-137250-7.
- ^ а б c Ян С. Фрейзер (1998). Эстрогены и прогестагены в клинической практике. Черчилль Ливингстон. С. 13, 92. ISBN 978-0-443-04706-0.
- ^ а б c Bradbury JT, Long RC, Durham WC (1953). «Требования к прогестерону и эстрогену для индукции и поддержания децидуальной оболочки». Fertil. Стерил. 4 (1): 63–75. Дои:10.1016 / s0015-0282 (16) 31145-1. PMID 13021207.
- ^ а б c Мишель Д.Р. (май 1996 г.). «Фармакокинетика противозачаточного средства депо медроксипрогестерона ацетата». Журнал репродуктивной медицины. 41 (5 Дополнение): 381–90. PMID 8725700.
- ^ Goebelsmann U (1986). «Фармакокинетика противозачаточных стероидов у людей». В Gregoire AT, Blye RP (ред.). Противозачаточные стероиды: фармакология и безопасность. Springer Science & Business Media. С. 67–111. Дои:10.1007/978-1-4613-2241-2_4. ISBN 978-1-4613-2241-2.
- ^ а б Ферин Дж (январь 1952 г.). «Относительная продолжительность действия природных и синтетических эстрогенов, вводимых парентерально у женщин с дефицитом эстрогенов». Журнал клинической эндокринологии и метаболизма. 12 (1): 28–35. Дои:10.1210 / jcem-12-1-28. PMID 14907837.
- ^ а б Овербек CA (1952). «Некоторые данные об эмульсиях стероидных гормонов». Симпозиум Фонда Ciba - Введение стероидных гормонов (Книга II коллоквиумов по эндокринологии, том 3). Симпозиумы Фонда Новартис. С. 254–262. Дои:10.1002 / 9780470715154.ch2. ISBN 9780470715154. ISSN 1935-4657.
- ^ Гамбургер C (1952). «Экскреция 17-кетостероидов и способы введения препаратов тестостерона». Симпозиум Фонда Ciba - Введение стероидных гормонов (Книга II коллоквиумов по эндокринологии, том 3). Симпозиумы Фонда Новартис. С. 304–322. Дои:10.1002 / 9780470715154.ch7. ISBN 9780470715154. ISSN 1935-4657.
- ^ Гамбургер C (1949). «Лечение тестостероном и выведение 17-кетостероидов; введение тестостерона пропионата, эмульгированного в воде». Acta Endocrinologica. 3 (2): 119–28, ил. Дои:10.1530 / acta.0.0030119. PMID 15397391.
- ^ Eversole WJ, Leathem JH, Schraer H (декабрь 1950 г.). «Препараты тестостерона пролонгированного действия». Эндокринология. 47 (6): 448–53. Дои:10.1210 / эндо-47-6-448. PMID 14802345.
- ^ Гамбург С, Биркет-Смит Э, Каи С (январь 1952 г.). «Лечение тестостероном и выведение 17-кетостероидов. III. Сравнение времени всасывания и выведения пропионата тестостерона, изобутирата тестостерона и н-валерата тестостерона». Acta Endocrinologica. 9 (1): 79–98. Дои:10.1530 / acta.0.0090079. PMID 14932696.
- ^ Гамбургер C (август 1956 г.). «Лечение тестостероном и выведение 17-кетостероидов. IV. Введение тестостерона бета-циклопентилпропионата, тестостерона фураната и тестостерона энантата». Acta Endocrinologica. 22 (4): 379–89. Дои:10.1530 / acta.0.0220379. PMID 13354228.
- ^ Йозеф Киммиг (14 марта 2013 г.). Therapie der Haut- und Geschlechtskrankheiten. Springer-Verlag. С. 508–. ISBN 978-3-642-94850-3.
- ^ Артур Джорес; Хенрик Новаковский (1960). Praktische Endokrinologie. Г. Тиме. п. 295.
- ^ Фон Нумерс С. (1951). «Одновременное лечение вторичной аменореи эстрогеном и прогестероном». Acta Endocrinologica. 6 (1): 67–89. Дои:10.1530 / acta.0.0060067. PMID 14810456.
- ^ "Neue Spezialitäten". Klinische Wochenschrift. 36 (17): 833. 1958. Дои:10.1007 / BF01481957. ISSN 0023-2173. S2CID 42166026.
- ^ Tobías GM, Usabiaga RA, Riaño JD, Espinoza AB, Tovar SR, Martínez ER (2008). "Progesterona en Microesferas para el Tratamiento en Infertilidad" (PDF). Acta Médica Grupo Ángeles. 6 (1): 8.
- ^ Тобиас GM, Мартинес ER (2009). "Técnica para Aplicación de Fármacos con Microesferas en Suspensión" (PDF). Acta Médica Grupo Ángeles. 7 (1): 13.
- ^ «Ювенум (эстрадиол / прогестерон) - Медикаментос ПЛМ». Медикаментоз PLM. Архивировано из оригинал на 2018-09-18. Получено 2018-09-17.
- ^ http://adisinsight.springer.com/drugs/800044558
- ^ https://www.drugs.com/international/juvenum.html
- ^ Кортес-Бонилья М., Алонсо-Камперо Р., Бернардо-Эскудеро Р., Франсиско-Доче М. Т., Чаварин-Гонсалес Дж., Перес-Куэвас Р., Чедрауи П. (октябрь 2016 г.). «Улучшение качества жизни и улучшение симптомов менопаузы у женщин в климактерическом периоде, получавших ежемесячные парентеральные препараты низких доз неполимерных микросфер 17β-эстрадиола / прогестерона». Гинеколь. Эндокринол. 32 (10): 831–834. Дои:10.1080/09513590.2016.1183628. PMID 27187320. S2CID 22688585.
- ^ Кортес-Бонилья М., Бернардо-Эскудеро Р., Алонсо-Камперо Р., Франсиско-Доче М. Т., Эрнандес-Валенсия М., Селис-Гонсалес С., Маркес-Оньяте Р., Чедрауи П., Урибе Х.А. (июль 2015 г.). «Лечение симптомов менопаузы тремя низкими дозами непрерывного последовательного парентерального введения 17β-эстрадиола / прогестерона ежемесячно с использованием новой технологии неполимерных микросфер». Гинеколь. Эндокринол. 31 (7): 552–9. Дои:10.3109/09513590.2015.1019853. ЧВК 4776687. PMID 26062108.
- ^ Toppozada MK (апрель 1994). «Существующие раз в месяц комбинированные инъекционные контрацептивы». Контрацепция. 49 (4): 293–301. Дои:10.1016/0010-7824(94)90029-9. PMID 8013216.
- ^ Гарза-Флорес Дж (апрель 1994 г.). «Фармакокинетика инъекционных контрацептивов, вводимых один раз в месяц». Контрацепция. 49 (4): 347–59. Дои:10.1016/0010-7824(94)90032-9. PMID 8013219.
- ^ Багаде О, Павар В., Пател Р., Пател Б., Авасаркар В., Дивейт С. (2014). «Увеличение использования обратимых контрацептивов длительного действия: безопасный, надежный и экономичный контроль над рождаемостью» (PDF). World J Pharm Pharm Sci. 3 (10): 364–392. ISSN 2278-4357. Архивировано из оригинал (PDF) на 2017-08-10. Получено 2019-05-19.
- ^ Ньютон JR, D'arcangues C, Hall PE (1994). «Обзор комбинированных инъекционных контрацептивов« раз в месяц ». J Obstet Gynaecol (Лахор). 4 Дополнение 1: S1–34. Дои:10.3109/01443619409027641. PMID 12290848.
- ^ Гарза-Флорес Дж., Фатиникун Т., Эрнандес Л., Рамос И., Карденас М., Мендживар М. (июль 1991 г.). «Пилотное исследование по оценке пролонгированного действия прогестерона / эстрадиола в качестве контрацептива, вводимого один раз в месяц». Контрацепция. 44 (1): 45–59. Дои:10.1016 / 0010-7824 (91) 90105-О. PMID 1893701.
- ^ Гарза-Флорес Дж, Холл ЧП, Перес-Паласиос Дж. (1991). «Гормональные противозачаточные средства длительного действия для женщин». J. Steroid Biochem. Мол. Биол. 40 (4–6): 697–704. Дои:10.1016 / 0960-0760 (91) 90293-Е. PMID 1958567. S2CID 26021562.
- ^ Локвуд Дж, Гризинджер Дж, Кометти Б. (2014). «Подкожный прогестерон по сравнению с вагинальным гелем прогестерона для поддержки лютеиновой фазы при экстракорпоральном оплодотворении: рандомизированное контролируемое исследование не меньшей эффективности». Fertil. Стерил. 101 (1): 112–119.e3. Дои:10.1016 / j.fertnstert.2013.09.010. PMID 24140033.
- ^ а б c Бейкер В.Л., Джонс КА, Дуди К., Фоулк Р., Йи Б., Адамсон Г.Д., Кометти Б., Девейн Г., Хьюберт Г., Тревизан С., Хелер Ф., Джонс С., Соулз М. (2014). «Рандомизированное контролируемое исследование, сравнивающее эффективность и безопасность водного подкожного прогестерона с вагинальным прогестероном для поддержки лютеиновой фазы оплодотворения in vitro». Гм. Репрод. 29 (10): 2212–20. Дои:10.1093 / humrep / deu194. ЧВК 4164149. PMID 25100106.
- ^ Киммиг Дж (1962). Therapie der Haut- und Geschlechtskrankheiten. Springer-Verlag. С. 507–. ISBN 978-3-642-94850-3.
- ^ Лобо Р.А., Келси Дж., Маркус Р. (22 мая 2000 г.). Менопауза: биология и патобиология. Академическая пресса. стр. 619–. ISBN 978-0-08-053620-0.
- ^ СП Пинкертона, Пикар Дж. Х. (февраль 2016 г.). «Обновленная информация о медицинских и нормативных вопросах, касающихся комбинированных и одобренных FDA лекарств, включая гормональную терапию». Менопауза. 23 (2): 215–23. Дои:10.1097 / GME.0000000000000523. ЧВК 4927324. PMID 26418479.
- ^ Санторо Н., Браунштейн Г.Д., Баттс К.Л., Мартин К.А., МакДермотт М., Пинкертон СП (апрель 2016 г.). «Составные биоидентичные гормоны в эндокринологической практике: научное заявление эндокринного общества». J. Clin. Эндокринол. Метаб. 101 (4): 1318–43. Дои:10.1210 / jc.2016-1271. PMID 27032319.
- ^ СП Пинкертон (декабрь 2014 г.). «Что вызывает беспокойство по поводу индивидуализированной« биоидентичной »гормональной терапии?». Менопауза. 21 (12): 1298–300. Дои:10.1097 / GME.0000000000000376. PMID 25387347.
- ^ Мишель Д.Р. (1941). «Клиническое исследование прогестероновой терапии путем имплантации гранул». Американский журнал акушерства и гинекологии. 41 (4): 687–693. Дои:10.1016 / S0002-9378 (41) 90665-8. ISSN 0002-9378.
- ^ Епископ П.М. (1944). «Эндокринная терапия в гинекологии и акушерстве». BJOG: Международный журнал акушерства и гинекологии. 51 (1): 51–63. Дои:10.1111 / j.1471-0528.1944.tb07317.x. ISSN 1470-0328. S2CID 71319436.
- ^ Foss GL (1943). «Имплантация таблеток полового гормона человеку». Британский медицинский бюллетень. 1 (2): 21–22. Дои:10.1093 / oxfordjournals.bmb.a070135. ISSN 1471-8391.
- ^ Гринблатт РБ, Волосы LQ (1945). «Поглощение гранул прогестерона». Журнал клинической эндокринологии и метаболизма. 5 (1): 38–39. Дои:10.1210 / jcem-5-1-38.
- ^ Гринблатт РБ, Суран РР (февраль 1949 г.). «Показания к применению гормональных гранул в терапии эндокринных и гинекологических заболеваний». Am. J. Obstet. Гинеколь. 57 (2): 294–301. Дои:10.1016/0002-9378(49)90429-9. PMID 18123090.
- ^ Епископ П.М., Ричардс Н.А., Долл Р. (июль 1950 г.). «Привычный аборт; профилактическое значение имплантации гранул прогестерона». Br Med J. 2 (4671): 130–3. Дои:10.1136 / bmj.2.4671.130. ЧВК 2038208. PMID 15434335.
- ^ Епископ PM, Фолли SJ (август 1951 г.). «Абсорбция гормонов имплантатами у человека». Ланцет. 2 (6676): 229–32. Дои:10.1016 / S0140-6736 (51) 93237-0. PMID 14862159.
- ^ Епископ П.М., Ричардс Н.А. (февраль 1952 г.). «Привычный аборт; дальнейшие наблюдения о профилактической ценности имплантации гранул прогестерона». Br Med J. 1 (4752): 244–6. Дои:10.1136 / bmj.1.4752.244. ЧВК 2022587. PMID 14896102.
- ^ Скоу Р.О., Эблинг Ф.Дж., Хендерсон И.В. (1973). Эндокринология: материалы Четвертого Международного конгресса эндокринологов, Вашингтон, округ Колумбия, 18-24 июня 1972 г.. Excerpta Medica. п. 978. ISBN 978-90-219-0166-4.
Подкожные имплантаты. Еще один способ получить длительную активность - использовать подкожные имплантаты, изготовленные путем сжатия кристаллических гормонов. Однако гранулы прогестерона плохо переносятся, и стерильные абсцессы или экструзия могут возникать примерно в 15-20% случаев (Greenblatt, личное сообщение, 1969). По этой причине кажется, что имплантаты, изготовленные из чистых гестагенных стероидов, имеют мало шансов найти место в противозачаточной терапии. [...]
- ^ Croxatto HB, Díaz S (1987). «Место прогестерона в контрацепции человека». J. Стероид Биохим. 27 (4–6): 991–4. Дои:10.1016/0022-4731(87)90179-8. PMID 3320572.
- ^ а б Шаабан М.М. (1991). «Контрацепция с прогестагенами и прогестероном при кормлении грудью». J. Steroid Biochem. Мол. Биол. 40 (4–6): 705–10. Дои:10.1016 / 0960-0760 (91) 90294-Ф. PMID 1835650. S2CID 25152238.
- ^ а б Croxatto HB, Díaz S, Peralta O, Juez G, Casado ME, Salvatierra AM, Durán E (сентябрь 1982 г.). «Регулирование фертильности у кормящих женщин. II. Сравнительная эффективность имплантатов прогестерона по сравнению с плацебо и медью Т». Am. J. Obstet. Гинеколь. 144 (2): 201–8. Дои:10.1016/0002-9378(82)90628-7. PMID 7114130.
- ^ а б Диас С., Перальта О., Хуэс Дж., Эррерос С., Касадо М.Э., Сальватьерра А.М., Миранда П., Кроксатто HB (октябрь 1984 г.). «Регулирование фертильности у кормящих женщин. VI. Противозачаточная эффективность подкожного имплантата прогестерона». Контрацепция. 30 (4): 311–25. Дои:10.1016 / S0010-7824 (84) 80023-2. PMID 6509984.
- ^ Mannino CA, South SM, Inturrisi CE, Quinones-Jenab V (декабрь 2005 г.). «Фармакокинетика и эффекты имплантатов 17бета-эстрадиола и прогестерона у овариэктомированных крыс». J Pain. 6 (12): 809–16. Дои:10.1016 / j.jpain.2005.07.007. PMID 16326369.
- ^ а б Benagiano G, Gabelnick H, Farris M (сентябрь 2008 г.). «Противозачаточные средства: системы подкожной доставки». Устройства Expert Rev Med. 5 (5): 623–37. Дои:10.1586/17434440.5.5.623. PMID 18803473. S2CID 207201811.
- ^ а б Фримен С., Шульман LP (февраль 2010 г.). «Рекомендации по использованию противозачаточных средств, содержащих только прогестин». J Am Acad Медсестра Практика. 22 (2): 81–91. Дои:10.1111 / j.1745-7599.2009.00473.x. PMID 20132366. S2CID 36724865.
- ^ а б c d Фальконе Т., Херд WW (1 января 2007 г.). Клиническая репродуктивная медицина и хирургия. Elsevier Health Sciences. С. 406–. ISBN 978-0-323-03309-1.
- ^ а б Слоан Э (2002). Биология женщины. Cengage Learning. С. 445–. ISBN 0-7668-1142-5.
- ^ Айкен А.Р., Трассел Дж. (2014). «Последние достижения в области контрацепции». F1000Prime Rep. 6: 113. Дои:10.12703 / P6-113. ЧВК 4251416. PMID 25580267.
- ^ Лобо РА (5 июня 2007 г.). Лечение женщины в постменопаузе: основные и клинические аспекты. Эльзевир. С. 210–. ISBN 978-0-08-055309-2.
- ^ Sitruk-Ware R, Bricaire C, De Lignieres B, Yaneva H, Mauvais-Jarvis P (октябрь 1987 г.). «Пероральный микронизированный прогестерон. Фармакокинетика биодоступности, фармакологические и терапевтические последствия - обзор». Контрацепция. 36 (4): 373–402. Дои:10.1016/0010-7824(87)90088-6. PMID 3327648.
- ^ а б Саймон Дж. А. (декабрь 1995 г.). «Микронизированный прогестерон: вагинальное и оральное применение». Клиническое акушерство и гинекология. 38 (4): 902–14. Дои:10.1097/00003081-199538040-00024. PMID 8616985.
- ^ Станчик Ф.З., Хэпгуд Дж. П., Винер С., Мишелл Д. Р. (апрель 2013 г.). «Прогестагены, используемые в постменопаузальной гормональной терапии: различия в их фармакологических свойствах, внутриклеточном действии и клинических эффектах». Endocr. Rev. 34 (2): 171–208. Дои:10.1210 / er.2012-1008. ЧВК 3610676. PMID 23238854.
- ^ Aufrère MB, Benson H (июнь 1976 г.). «Прогестерон: обзор и последние достижения». Журнал фармацевтических наук. 65 (6): 783–800. Дои:10.1002 / jps.2600650602. PMID 945344.
дальнейшее чтение
- Лангекер Х (1968). «Резорбция, Verteilung und Ausscheidung der Gestagene» [Поглощение, распределение и выведение прогестагенов]. Die Gestagene [Прогестагены]. Springer-Verlag. С. 264–351. Дои:10.1007/978-3-642-99941-3_3. ISBN 978-3-642-99941-3.
- Sitruk-Ware R, Bricaire C, De Lignieres B, Yaneva H, Mauvais-Jarvis P (октябрь 1987 г.). «Пероральный микронизированный прогестерон. Фармакокинетика биодоступности, фармакологические и терапевтические последствия - обзор». Контрацепция. 36 (4): 373–402. Дои:10.1016/0010-7824(87)90088-6. PMID 3327648.
- Саймон Дж. А. (декабрь 1995 г.). «Микронизированный прогестерон: вагинальное и оральное применение». Клиническое акушерство и гинекология. 38 (4): 902–14. Дои:10.1097/00003081-199538040-00024. PMID 8616985.
- Руан Х, Муек А.О. (ноябрь 2014 г.). «Системная терапия прогестероном - пероральная, вагинальная, инъекционная и даже трансдермальная?». Maturitas. 79 (3): 248–55. Дои:10.1016 / j.maturitas.2014.07.009. PMID 25113944.










